1.1.1.
![]()
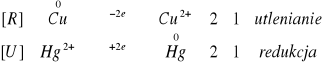
W miejscu gdzie umieściliśmy krople roztworu CuCl2 blaszka zczerniała.
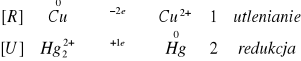
Zaobserwowaliśmy na powierzchni blaszki szare odbarwienie.
![]()
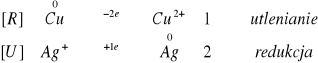
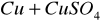
nie zajdzie reakcja
![]()
nie zajdzie reakcja
Nic się nie dziaje na powierzchni blaszki i reakcja nie zachodzi.
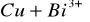
nie zajdzie reakcja
Nic się nie dzieje. Powstałe czarne zabrudzenie można zakwalifikować do zabrudzenia blaszki, a nie do reakcji. Z teoretycznego punktu widzenia, mając przed oczyma szereg napięciowy metali ta reakcja nie zachodzi.
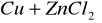
nie zajdzie reakcja
![]()
nie zajdzie reakcja
W tej reakcji po umieszczeniu kropli roztworu ZnCl2 na blaszce miedzianej nic się nie dziaje, nawet po upływie kilku minut.
1.1.2.
![]()
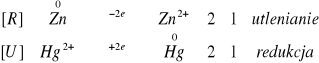
Z teoretycznego punktu widzenia reakcja powinna zajść, niestety w naszym przypadku nie zaobserwowaliśmy nic, zupełnie jakby reakcja wogóle nie zachodziła.
![]()
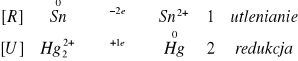
Reakcja powinna zajść, niestety na powierzchni blaszki nic nie zaobserwowaliśmy.
![]()
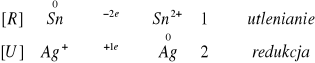
Na powierzchni blaszki zaobserwowaliśmy blado popielaty osad.
![]()
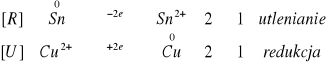
Na blaszce zaobserwowaliśmy lekko szrawy osad.
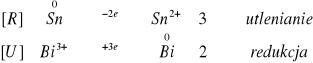
Na blaszce zaobserwowaliśmy ślady, świadczące o tym, że reakcja zaszła.
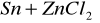
nie zajdzie reakcja
![]()
nie zajdzie reakcja
Reakcja nie zajdzie, bowiem cyna leży za cynkiem w szeregu napięciowym metali i nie jest w stanie go wyprzeć z roztworu.
1.1.3.
![]()
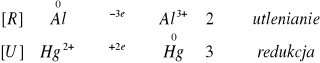
Na powierzchni blaszki aluminiowej zuważyliśmy szaro-czarne przebarwienia, świadczące o zajściu reakcji. Reakcja teoretyczna dała identyczny rezultat jak praktyczna.
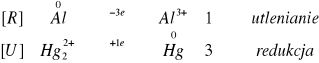
Podobnie jak na powierzchni poprzedniej blaszki po dodaniu kropli roztworu ![]()
zauważyliśmy szaro-czarne przebarwienia aluminiowej podkładki.
![]()
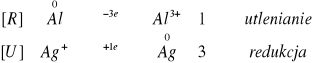
Aluminiowa blaszka po dodaniu kropli roztworu ![]()
przebarwiła się na ciemno-szary, wpadający w czarny kolor. Również i tu teoria potwierdza się z praktyką.
![]()
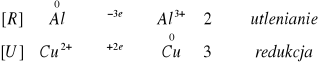
Nie zaobserwowaliśmy żadnych zmian na powierzchni blaszki, choć teoretycznie reakcja powinna zajść, bowiem glin wyprzez z roztworu miedź.
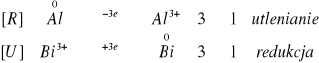
Po dodaniu kropli roztworu jonów ![]()
blaszka aluminiowa uzyskała czarne plamki przebarwieniowe, świadczące o zajściu reakcji.
![]()
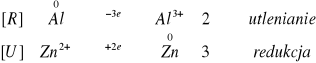
Niestety po dodaniu kropli roztworu ![]()
na powierzchni blaszki glinowej nie zaszły żadne zmiany, świadczące o zajściu reakcji.
1.2.1.
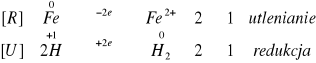
Zaszła energiczna reakcja, ale słabsza niż w przypadku cynku. Wydzielił się gazowy wodór. Reakcja nie wymagała podgrzewania.
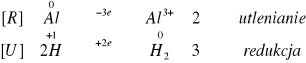
Na poczatku, gdy dodaliśmy do opiłków glinu HCl reakcja zachodziła bardzo powoli, jednak z biegiem czasu reakcja nabrała tempa i zaczęła znacznie gwałtowniej przebiegać. Reakcja nie wymagała podgrzewania. Wydzielił się również jak w przypadku żelaza gazowy wodór.
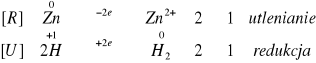
Reakcja przebiegła szybko i sprawnie. Wydzielił się przy okazji wodór.
![]()
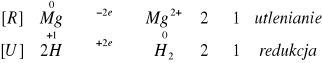
Bardzo gwałtowna reakcja, która nie wymagała podgrzewania. Wydzieliło się przy tym bardzo dużo ciepła. Jak w poprzednich reakcjach wydzielił się również wodór.
Najbardziej efektownie reagował magnez. Poczatkowo po wlaniu kwasu solnego nie działo się nic, z czasem zaczęła przebiaegać gwałtowna reakcja i zaczęła tworzyć się „piana” świadcząca o rozpuszczaniu magnezu. We wszystkich tych reakcjach metale użyte w doświadczeniu wypierały wodór z kwasu beztlenowego, bowiem zgodnie z szeregiem napięciowym metali, metale leżące przed wodorem (te o niższym potencjale) wypierają wodór z kwasów. Tak też było tym razem.
1.2.2.
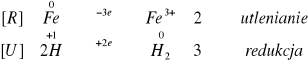
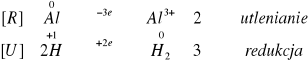
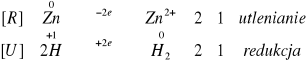
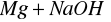
reakcja nie zajdzie
Reakcje zachodzą tylko w probówkach w których do reakcji z NaOH wzięto metale wykazujące właściwości amfoteryczne.
1.3.1.
![]()
Roztwór ![]()
po sporządzeniu był bezbarwny. Po dodaniu kilku kropel 0,01M jodku potasu nic się nie wydarzyło.
1.3.2.
![]()
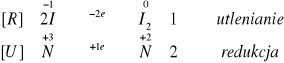
Po dodaniu do reakcji skrobi stwierdzono charakterystyczną dla jodu zmianę zabarwienia roztworu na fioletowy kolor, co świadczy o utlenieniu się jodu (2I-==>I2). Początkowo roztwór miał żółte zabarwienie.
1.3.3.
Z braku odczynników nie przeprowadziliśmy tej reakcji (nie było Na2S). Teoretycznie reakcja powinna mieć przebieg:
![]()
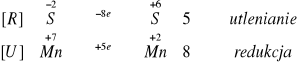
Teoretycznie powinniśmy w tej reakcji zaobserwować odbarwienie manganu występującego na +7 stopniu utlenienia do manganu na +2 stopniu utlenienia. (Reakcje charakterystyczne dla manganu).
1.3.4.
![]()
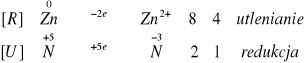
Papierek wskaźnikowy przyłożony podczas ogrzewania odbarwił się na niebiesko, co świadczy o zasadowym środowisku. Z probówki wydzielał się amoniak.
1.4.1.
![]()
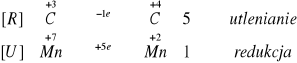
Do roztworu szczawianu amonowego dodaliśmy kwas siarkowy VI a następnie kilka kropel KMnO4. Roztwór się odbarwia co świadczy o obniżeniu swojego stopnia utlenienia przez manganu z +7 na +2.
1.4.2.
![]()
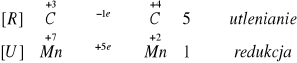
1.4.4.
![]()
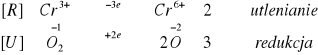
![]()
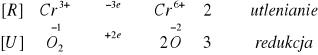
W pierwszym etapie reakcji widzimy zielony kolor roztworu, świadczący o obecności jonów chromu na +3 stopniu utlenienia, następnie podgrzewamy wszystko. Do wcześniej ogrzewanej probówki po dodaniu jonów ołowiu II wytrącił się żółty osad. Natomiast w nieogrzewanej probówce po dodaniu jonów ołowiu II wytrącił się żółto-zielony osad. Świadczy to o tym, że chrom podwyższył swój stopień utlenienia z +3 na +6 stopień utlenienia.
Wyszukiwarka
Podobne podstrony:
teoria do redoksów 2a, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, chemia ogolna nie or
teoria do redoksów 1a, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, chemia ogolna nie or
Redoksy, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, chemia ogolna nie organiczna
teoria do redoksów 2, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, chemia ogolna nie org
kationy, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, chemia ogolna nie organiczna
Chemia mat. bud, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, 1sem.chemia.laborki, Chemi
sciaga na egzmin, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, 1sem.chemia.laborki
sprawko z osadów, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, chemia ogolna nie organic
6!!!!!!!!!, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki
hydroliza, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, 1sem.chemia.laborki, Chemia - I
sprawko cw1, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, chemia ogolna nie organiczna
sprawozdanie z cw 4, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, chemia ogolna nie orga
Odczyn roztworów wodnych soli, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, chemia ogoln
Badanie substancji błonotwórczych, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, 1sem.che
Cw12 Rozdzial przez stracanie, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, chemia ogoln
ćw.5 Ania, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki
Cw10 Reakcje utleniania i redukcji, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, chemia
więcej podobnych podstron