
LANTANOWCE
1

PLAN PREZENTACJI
1.
Lantanowce
2.
Występowanie lantanowców w przyrodzie
3.
Rozdzielanie i otrzymywanie lantanowców
4.
Metody rozdzielania lantanowców
5.
Widma elektronowe lantanowców,
właściwości optyczne
6.
Przejścia f - f
7.
Luminescencja lantanowców
8.
Właściwości magnetyczne
2

LANTANOWCE
Nazwa lantanowce obejmuje 14 pierwiastków
położonych w układzie okresowym za lantanem.
Lantanowce zwane czasami metalami ziem
rzadkich i występują w przyrodzie razem; są one
metalami o charakterze elektrododatnim. W ich
chemii dominuje stopień utlenienia +3 i jony o
konfiguracji (4f)
n
. Pod względem właściwości
chemicznych wszystkie lantanowce są do siebie
podobne.
3
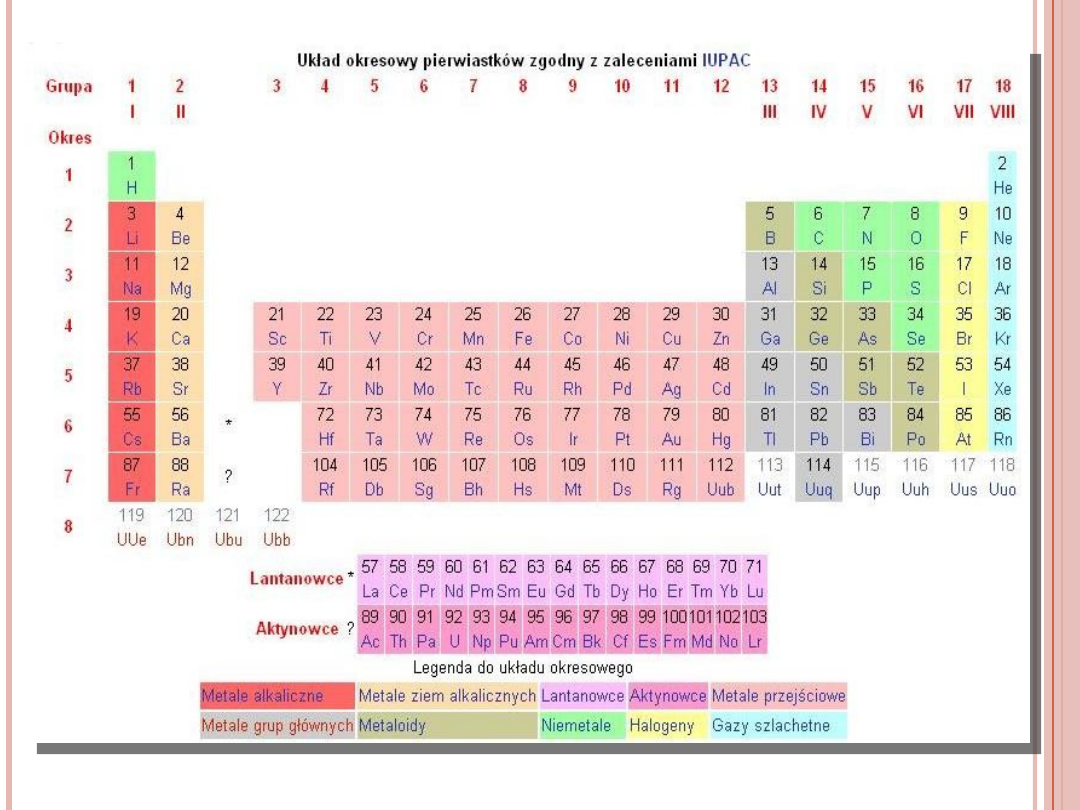
4

WYSTĘPOWANIE
LANTANOWCÓW W
PRZYRODZIE
Lantanowce zarówno jak skandowce występują w
przyrodzie głównie w postaci fosforanów i
krzemianów. Zbliżony promień jonowy i duże
podobieństwo chemiczne tych pierwiastków
powoduje, że spotykamy je niemal wszystkie
obok siebie w tych samych minerałach.
5

Do najważniejszych minerałów zawierających
lantanowce należy monacyt, CePO
4
występujący w złożach pierwotnych w
pegmatytach, granitach i gnejsach, a także
często w postaci lepiej nadającego się do
eksploatacji piasku monacytowego.
6
6

Innym minerałem zawierającym lantanowce
jest bastnazyt o wzorze sumarycznym
LnFCO
3
, który występuje w Kalifornii.
7
7

Cięższe lantanowce o
liczbach atomowych od
64 do 71 (od gadolinu
do lutetu) występują
natomiast w minerałach
zawierających itr. Do
najważniejszych
minerałów tego rodzaju
należy gadolinit, o
wzorze sumarycznym
Y
2
Fe
II
Be
2
Si
2
O
10
8
8

ROZDZIELANIE I
OTRZYMYWANIE
LANTANOWCÓW
Przeróbka rud lantanowców uzależniona jest od
chemicznego składu rudy i może mieć różny
przebieg. W poniższych tabelach przedstawione
są dwa schematy wstępnej przeróbki piasku
monacytowego, mającego na celu oddzielenie
zanieczyszczeń: krzemionki, związków tytanu i
cyrkonu.
9
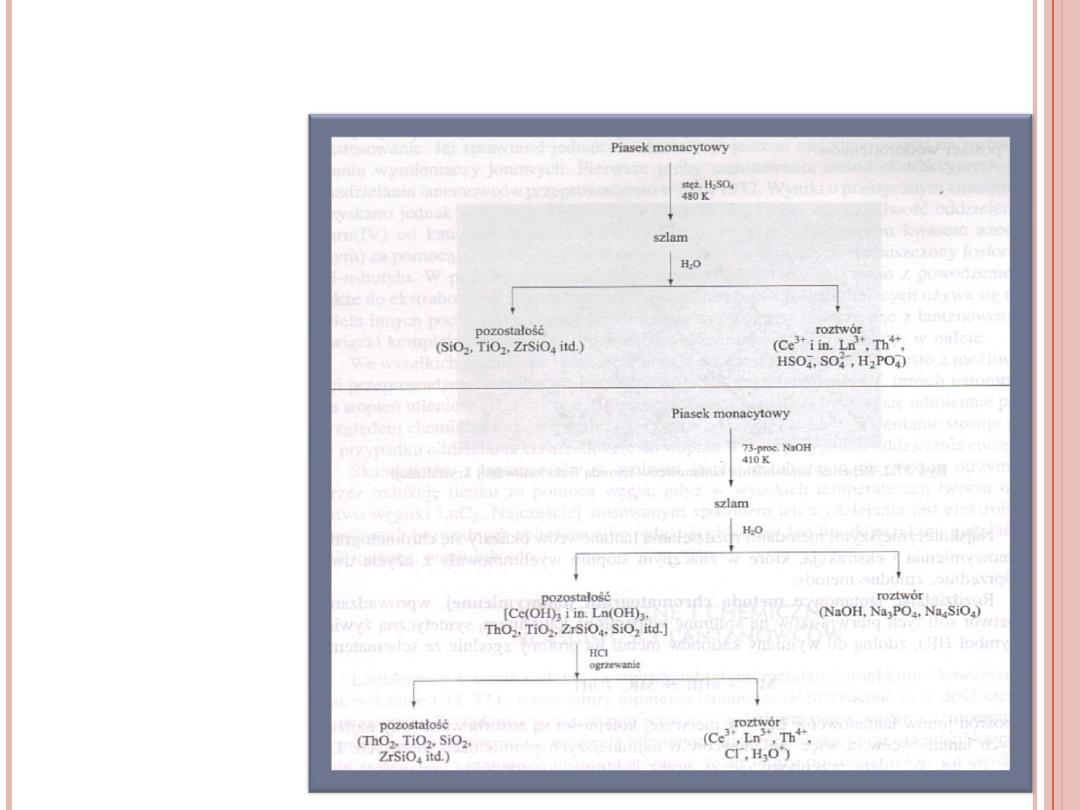
SCHEMATY PRZERÓBKI
PIASKU
MONACYTOWEGO
10

METODY ROZDZIELANIA
LANTANOWCÓW
Rozdzielanie lantanowców stanowi jedno z
najtrudniejszych zadań nieorganicznej preparatyki
chemicznej. Do najważniejszych metod
stosowanych w celu rozdziału tych związków należą:
1. Krystalizacja frakcjonowana
2. Frakcjonowane strącanie z roztworu
3. Chromatografia jonowymienna
4. Ekstrakcja
11

KRYSTALIZACJA
FRAKCJONOWANA
Rozdzielanie lantanowców metodą
frakcjonowanej krystalizacji polega na
wykorzystaniu niewielkich różnic w
rozpuszczalności niektórych soli lantanowców.
Krystalizację przeprowadza się zawsze z
roztworów wodnych.
12
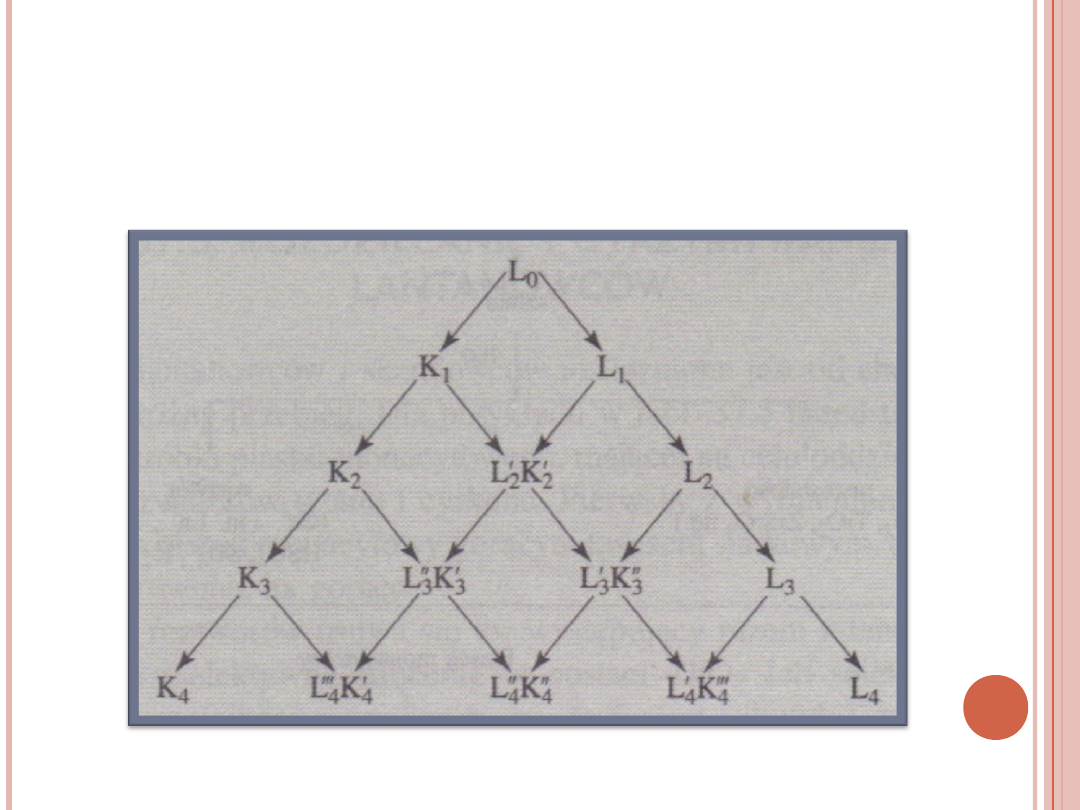
SCHEMAT ROZDZIELANIA
LANTANOWCÓW METODĄ
KRYSTALIZACJI
FRAKCJONOWANEJ
13

W krystalizacji frakcjonowanej do rozdzielania lantanowców
jako związki dające najefektywniejsze rozdzielania stosuje się:
bromiany Ln(BrO
3
)
3
*9H
2
O i etylosiarczany Ln
2
(C
2
H
5
SO
4
)
3
*9H
2
O
do rozdzielania grupy itrowej i oddzielenia itru
siarczany Ln(SO
4
)
3
*8H
2
O do oddzielenia lantanu, ceru, a
przede wszystkim rozdzielania lantanowców zawierających
grupę cerową i itrową
azotany Ln(SO
4
)
3
*5H
2
O do oddzielenia gadolinu
podwójne azotany Ln(NO
3
)
3
*2NH
4
NO
3
*4H
2
O do wydzielania
lantanu i rozdzielenia pary prazeodym – neodym
podwójne azotany 2Ln(NO
3
)
3
*3Mg(NO
3
)
2
*24H
2
O do
rozdzielania grupy cerowej (lecz nie grupy itrowej)
Frakcjonowana krystalizacja jest bardzo efektywna dla
lantanu i lekkich lantanowców, których sole znacznie bardziej
różnią się rozpuszczalnością.
14

FRAKCJONOWANE
STRĄCANIE
Różnica między krystalizacją a procesem strącania
dotyczy sposobu powstawania osadu soli i jej
rozpuszczalności. W metodzie strącania stosuje się
reakcje dwu lub więcej soli, której produkt jest trudniej
rozpuszczalny w danym środowisku niż substraty.
Można wyróżnić trzy główne rodzaje strącania
frakcjonowanego:
strącanie różnych soli bez wytworzenia
kompleksów
strącanie wodorotlenków, czyli tzw. strącanie
zasadowe
strącanie w obecności czynnika
kompleksującego
15

STRĄCANIE RÓŻNYCH SOLI
Do rozdzielania lantanowców ta metodą stosowane są
następujące związki:
podwójne siarczany Ln
2
(SO
4
)
3
*K
2
SO
4
*2H
2
O do rozdzielania
lantanowców na grupę cerową, irytową oraz do
wydzielania irytu
szczawiany Ln
2
(C
2
O
4
)3*nH
2
O do rozdzielania lantanu od
grupy cerowej i irytu od grupy irytowej
podwójne węglany lantanowo – potasowe do rozdzielania
mieszaniny lantanowców na grupę cerową i irytową, a
także do oddzielania toru od lantanowców
chromiany Ln
2
(CrO
4
)*nH
2
O do oddzielania irytu od
lantanowców i holmu od erbu
tereftalany do rozdzielania lantanowców na lekkie i ciężkie
oraz do oddzielania irytu od lantanowców
16

STRĄCANIE ZASADOWE
Dotyczy wszystkich reakcji powstawania osadów tlenków
lub wodorotlenków pod wpływem dodawania lub tworzenia
się w roztworze zasad.
każdy osad zaczyna wytrącać się przy odpowiednim pH,
które zależy od stężenia pierwiastka strącanego
na efektywność rozdziału wpływa zarówno różnica
zasadowości strącanych wodorotlenków jak i zasadowość
odczynnika strącającego
najczęściej stosowane są odczynniki strącające w postaci
gazowej, co prowadzi do powolnej zmiany pH, jednakowej w
całej objetości roztworu
stosowane odczynniki to roztwór wody amoniakalnej,
gazowy amoniak, gazowy amoniak rozcieńczony
powietrzem, roztwory wodorotlenków litowców (np. NaOH),
zasady organiczne (anilina) i mocznik
17

STRĄCANIE W OBECNOŚCI
ODCZYNNIKA KOMPLEKSUJĄCEGO
W metodzie tej kolejność przechodzenia lantanowców do fazy stałej
zależy od dwóch czynników:
od trwałości powstających kompleksów
od rozpuszczalności soli lantanowców
Jeżeli proces kompleksowania przedstawimy równaniem:
Ln
3+
+ H
x
C
x-4
LnC
-
+ xH
+
a z drugiej strony reakcję dtrącania kwasem HA jako:
αLn
3+
+ 3A
α-
Ln
α
A
3
To stałą trwałości kompleksu możemy zapisać wzorem:
K
c
= [LnC
-
] [H
+
]
x
/ [Ln
3+]
[C
x-4
]
a iloczyn rozpuszczalności jako:
K
s
= [Ln
3+
]
α
[A
α-
]
3
18

CHROMATOGRAFIA
JONOWYMIENNA
Metoda ta jest najlepsza w otrzymywaniu lantanowców o
największej czystości
W procesie wymiany jonowej jony Ln
3+
w roztworze
wymieniają się z protonem, jonem amonowym lub innym
kationem z fazy jonitu – żywicy jonowymiennej.
Powinowactwo kationitu do jonitu zależy od wymiarów
jonu i jego ładunku. Jednak przy sorpcji Ln (III) na jonicie
nastepuje praktycznie ich rozdzielenie, ponieważ jonit jest
zbyt mało selektywny
19

Gdy na kolumnę wprowadzi się czynnik kompleksujacy L,
to rozdzielenie nastąpi, jeżeli stałe trwałości reakcji
kompleksowania kolejnych lantanowcw Ln dla reakcji:
Ln + L LnL
różnią się wystarczająco między sobą. Możliwe jest to gdy
w układzie Ln – L tworzy się tylko jeden kompleks. Jeżeli
tworzą się różne kompleksy, które konkurują między sobą,
to krzywe elucji poszczególnych lantanowców zachodzą na
siebie, a co za tym idzie rozdzielenie nie jest efektywne.
Współczynnik rozdzielnia dla pary Ln i Ln’ opisujemy
równaniem
β = λ
Ln
K
Ln’
/ λ
Ln’
K
Ln
gdzie:
λ
Ln
, λ
Ln’
- współczynniki podziału Ln między wodny roztwór
i żywicę jonowymienną w obecności czynnika
kompleksującego
K
Ln
, K
Ln’
– stałe trwałości kompleksów
20

Jeżeli wartości współczynników podziału są do siebie zbliżone, a
stałe trwałości jonów Ln są znane to w wyrażeniu na
współczynnik rozdzielenia można pominąć stężenie czynnika
kompleksującego. Otrzymujemy wówczas wyrażenie:
β = K
Ln’
/ K
Ln
Do rozdzielania lantanowców tą metodą stosuje się kationity
takie jak Dowex – 50, Amberlit IR – iGO, Zerolit 225, Wofatit
KPS, a jako czynniki kompleksujące hydroksykwasy, np. kwas α
– hydroksyizomasłowy, mlekowy, cytrynowy oraz kwasy
aminopolioctanowe, jak np. kwas nitrylotrioctowy (NTA), EDTA,
kwas N – hydroksyetyloetylenodiaminotrioctowy (HEDTA)
21

EKSTRAKCJA
Metoda ta polega na rozdzielaniu lantanowców za
pomocą cieczy nie mieszających się z wodą, zdolnych
jednak do rozpuszczania soli Ln
3+
.
W procesie ekstrakcji kompleksy lantanowców ulegają
podziałowi między fazę organiczną a fazę wodną,
zgodnie z prawem Nernsta:
α = C
org
/ C
aq
Gdzie:
α – współczynnik podziału
C
org
– całkowite stężenie substancji w fazie organicznej
C
aq
– stężenie substancji w fazie wodnej
22

W zależności od rodzaju kompleksów tworzących
się w fazie organicznej, ekstrahenty można
podzielić na trzy grupy:
ekstrahenty solwatujące z obojętną donorową
parą elektronów (alkohole, estry, np. fosforan tri-
n-butylowy(TBP), etery, ketony)
ekstrahenty o charakterze kwasowym tworzące
kompleksy, tj. kwasy organofosforowe, kwasy
tłuszczowe (C
5
– C
9
)
ekstrahenty tworzące pary jonowe metal – zasada
organiczna, np. aminy wielkocząsteczkowe
23
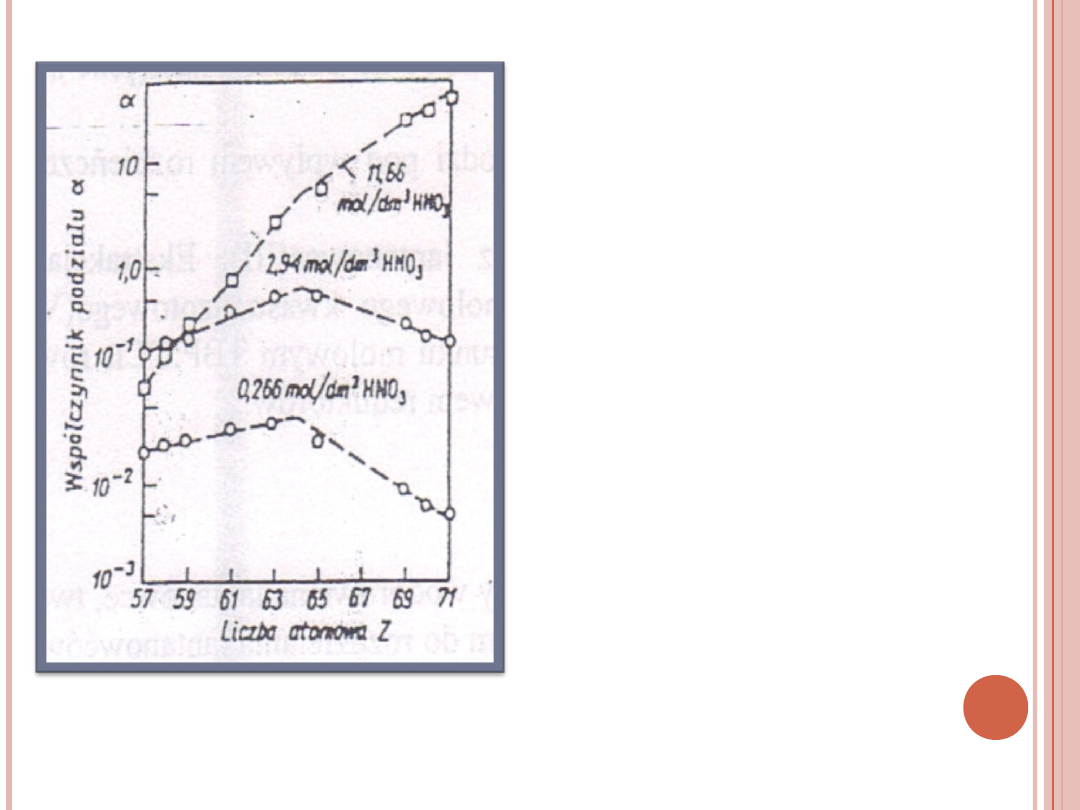
lantanowce
ekstrahują się TBP z
wodnego roztworu
czystego kwasu
azotowego (V)
wydajność ekstrakcji
lantanowców (III) za
pomocą TBP z
kwaśnych roztworów
rośnie wraz ze
wzrostem stężenia
kwasu
Rys. Zależność współczynnika podziału α od liczby
atomowej lantanowca Z przy ekstrakcji TBA
24

WIDMA ELEKTRONOWE
LANTANOWCÓW,
WŁAŚCIWOŚCI OPTYCZNE
Związki większości lantanowców wykazują
intensywne zabarwienie, które nie ulega zmianie w
roztworach wodnych i niewodnych ani też wskutek
wytworzenia się połączenia kompleksowego.
25
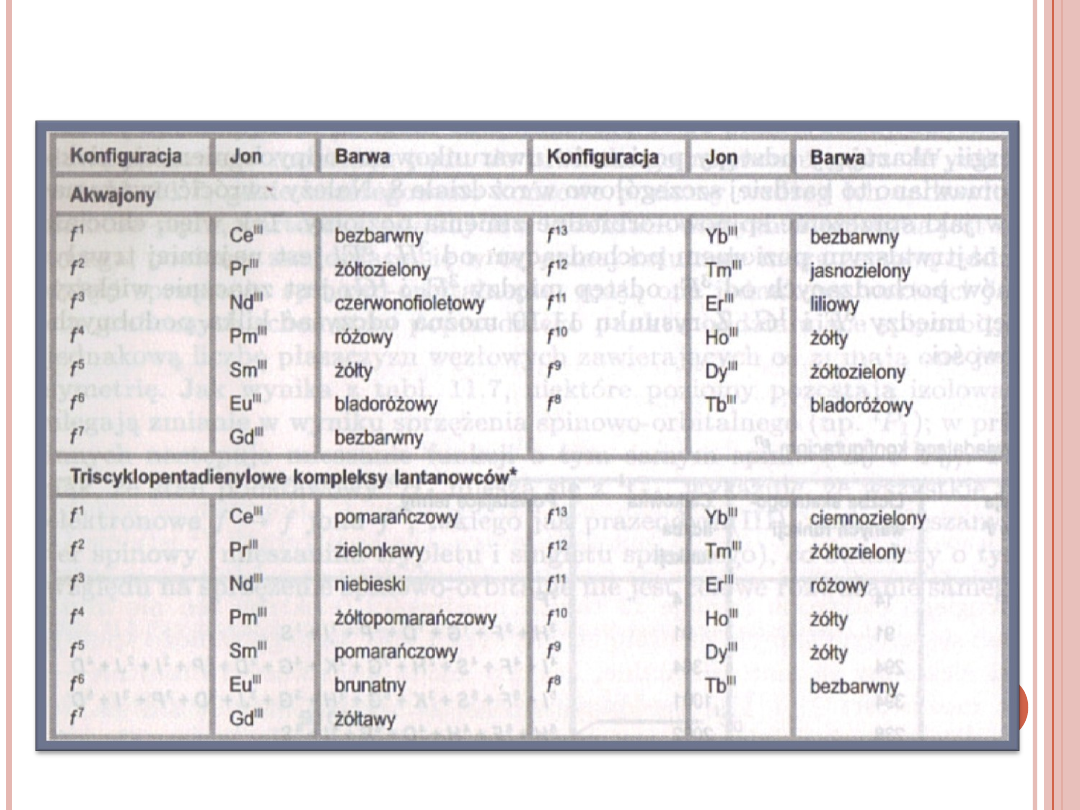
BARWA ZWIĄZKÓW ZAWIERAJĄCYCH
JONY LN
3+
26
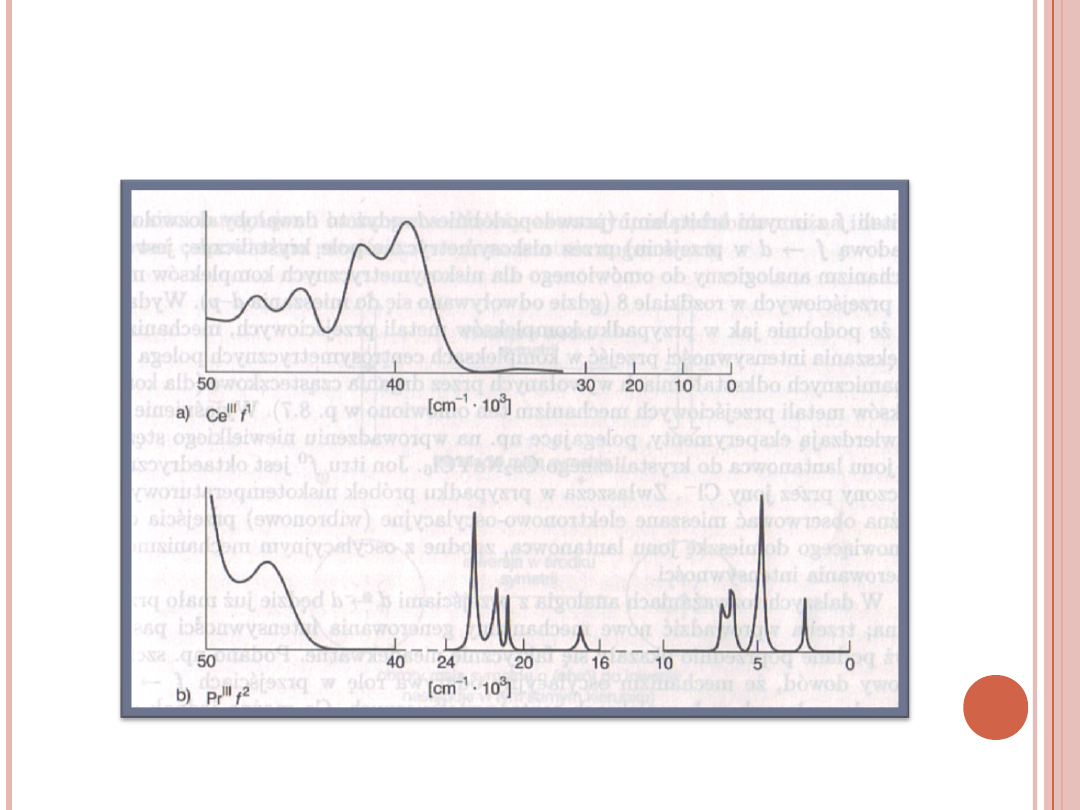
Cechą charakterystyczną widma absorpcyjnego
lantanowców jest pojawienie się ostro
zaznaczonych pasm pochłaniania.
Rys. a) widmo elektronowe Ce
III
(jon f
1
), b) widmo elektronowe Pr
III
(jon f
2
)
27

PRZEJŚCIA F - F
Przejścia te są całkowicie zlokalizowane na
powłoce f i formalnie są wzbronione.
Podobnie jak w przypadku przejść d – d,
zachodzą i powodują powstawanie wielkiej
ilości słabych, ostrych pasm, występujących
w zakresie od podczerwieni do obszaru
widzialnego.
28

Pochłanianie światła przez jony lantanowców wiąże
się z przejściami energetycznymi elektronów f.
Elektrony te położone są tak głęboko w atomie, że
jego otoczenie praktycznie nie wywiera wpływu na
ich energię i tym tłumaczy się znikomy wpływ
ligandów na barwę związków lantanowców. Pod tym
względem różnią się one bardzo od barwnych
połączeń metali przejściowych w których absorpcja
światła związana jest z przejściami elektronów d, a
więc elektronów położonych w bardziej
zewnętrznych częściach atomu i z tego powodu
zmieniających swą energię w polu ligandów.
29

LUMINESCENCJA LANTANOWCÓW
Jony wielu lantanowców fluoryzują pod wpływem
promieniowania nadfioletowego, a źródłem fluorescencji
są omówione wcześniej przejścia f – f.
Wszystkie jony Ln
3+
za wyjątkiem f
0
La
3+
i f
14
Lu
3+
wykazują luminescencję: Eu
3+
i Tb
3+
wyjątkowo silną
Bezpośrednie wzbudzenie jonów Ln
3+
wymaga
intensywnych źródeł promieniowania (lasery) ze względu
na niską intensywność i ostrość pasm f-f
Pośrednie wzbudzenie jonów Ln
3+
następuje poprzez
przeniesienie energii ze stanu wzbudzonego liganda,
który posiada szerokie i intensywne wewnątrzligandowe
pasmo absorpcji, jest to tzw. efekt antenowy
30
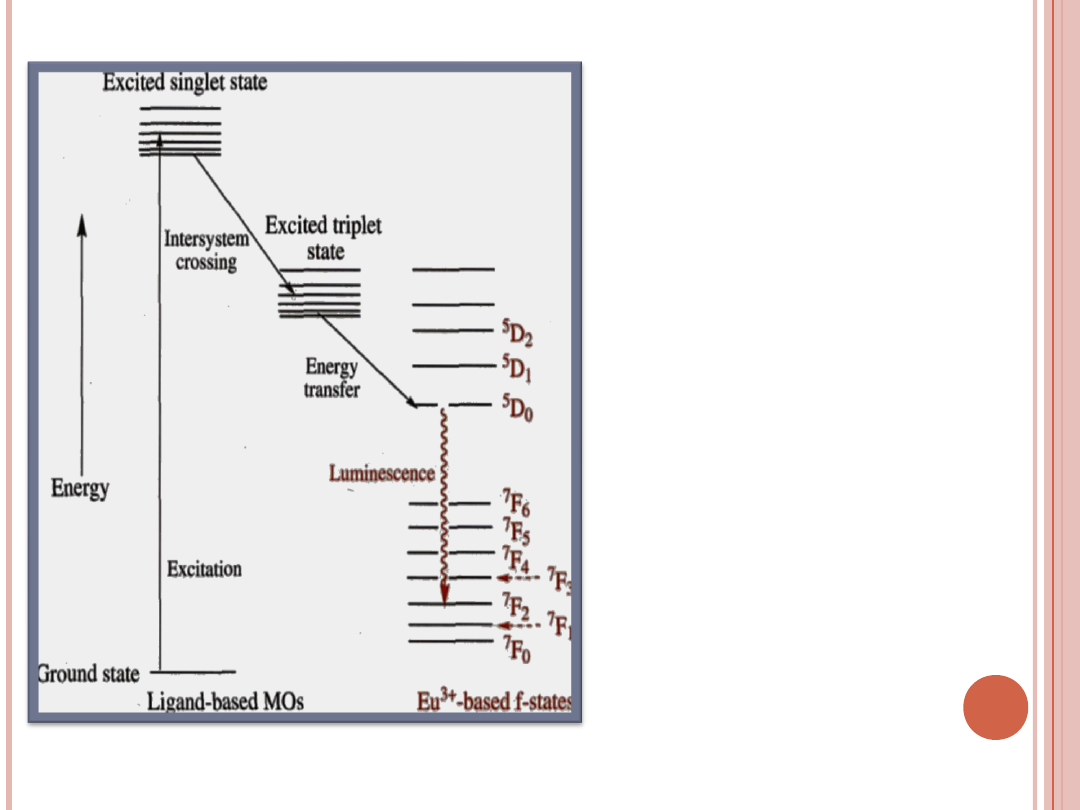
Schematyczny diagram poziomów
energii pokazujący źródło
luminescencji Eu
3+
w efekcie
antenowym
31

Jedne z najbardziej wydajnych, stosowanych obecnie
luminoforów zawierają europ (III) (emisja światła
czerwonego i niebieskiego) i terb (III) (emisja światła
zielonego).
Matrycą , w którą wbudowywane są jony lantanowców w
luminoforze, są szkłotwórcze oksoaniony – borany,
krzemiany, gliniany i wolframiany.
Ist0otny jest także wybór substancji, ponieważ jeden z
etapów z etapów procesu emisji stanowi przeniesienie
pochłoniętego promieniowania nadfioletowego przez sieć
krystaliczną emitera.
32

WŁAŚCIWOŚCI MAGNETYCZNE
Jony lantanowców, z wyjątkiem jonów o
konfiguracji f
0
(La
3+
, Ce
4+
) oraz o konfiguracji
f
14
(Yb
2+
, Lu
3+
), wykazują silny
paramagnetyzm.
W swych właściwościach magnetycznych
różnią się jednak od paramagnetycznych
jonów metali zewnętrznoprzejściowych.
33

W jonach metali zewnętrznoprzejściowych na
skutek oddziaływania elektronów d z polem
krystalicznym następuje zerwanie sprzężenia LS i
„zamrożenie” momentu orbitalnego, a
obserwowany moment magnetycznym jest
momentem spinowym.
μ
ef
= μ
B
[4S(S+1)]
1/2
gdzie S jest wypadkową spinową liczbą kwantową
34
W jonach lantanowców elektrony f są osłaniane przez
elektrony w bardziej zewnętrznych powłokach i ich
oddziaływanie z polem krystalicznym jest znacznie
słabsze. W rezultacie sprzężenie LS zostaje
zachowane, a całkowity moment magnetyczny jonów
lantanowców jest sumą momentu spinowego i
orbitalnego.
35
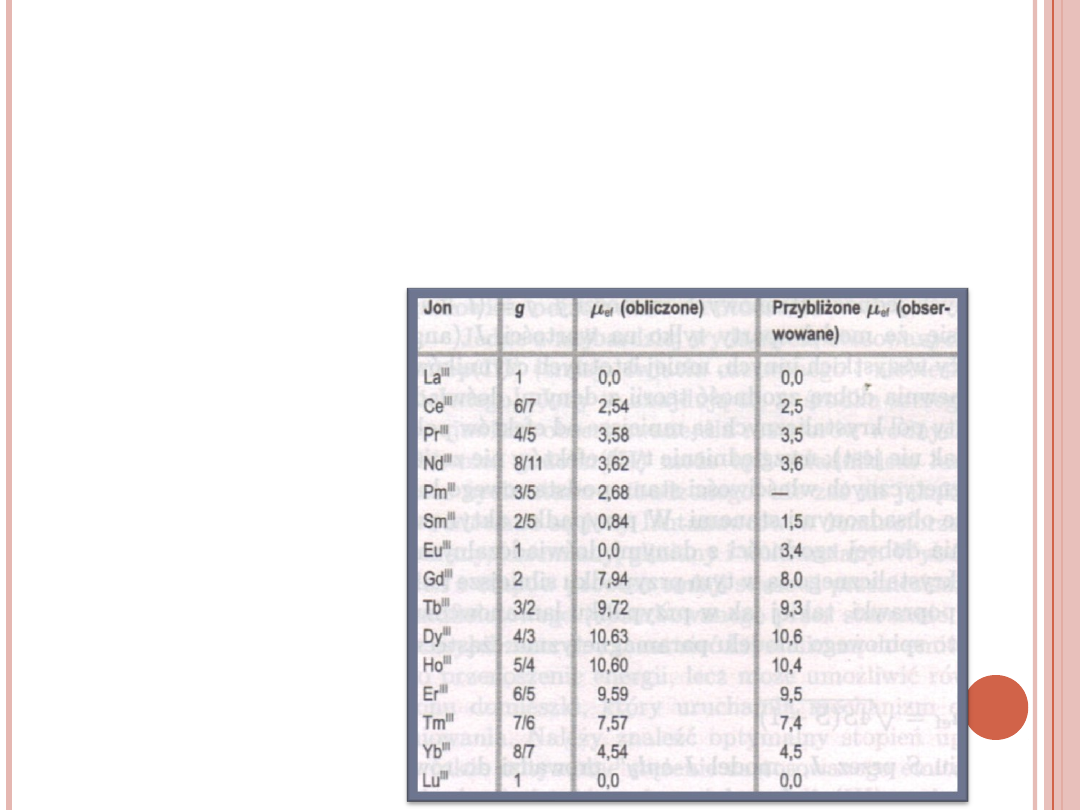
Wartości μ
ef
dla
jonów lantanowców
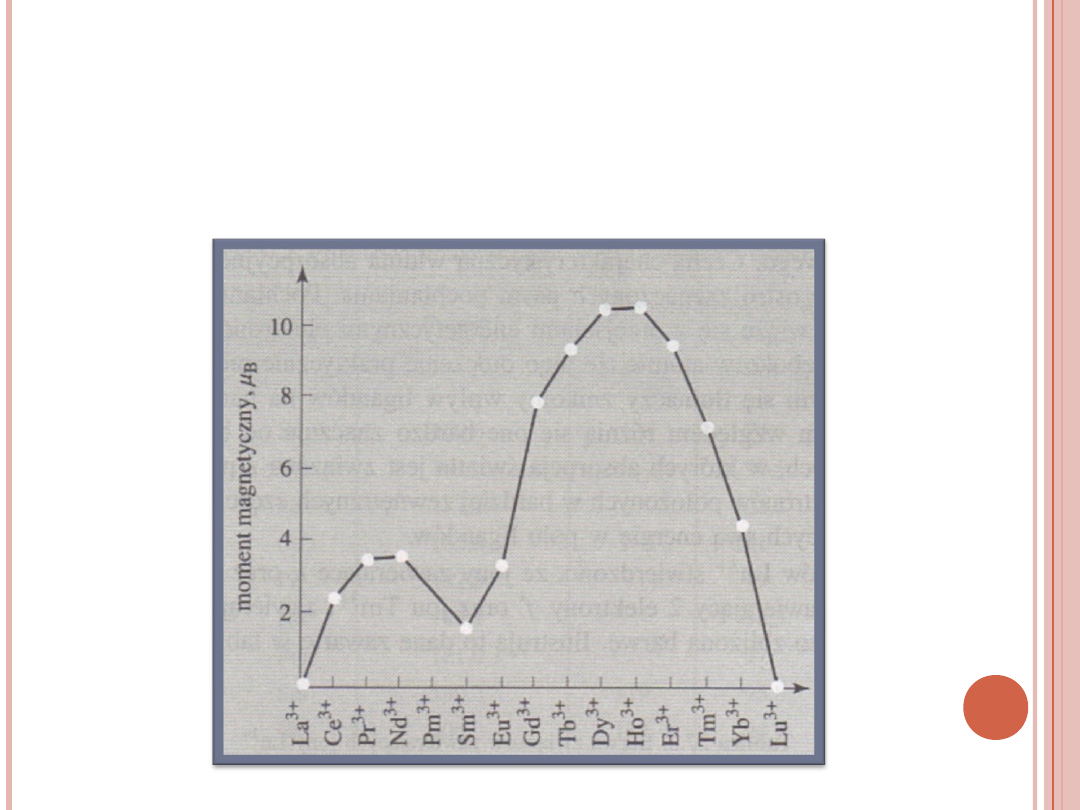
WYKRES MOMENTÓW
MAGNETYCZNYCH
JONÓW
LN
3+
W
ZALEŻNOŚCI OD LICZBY
ATOMOWEJ
36

BIBLIOGRAFIA
1.
A. F. Williams, „Chemia nieorganiczna.
Podstawy teoretyczne”, Państwowe
Wydawnictwo Naukowe, Warszawa 1986
2.
S. F. A. Kettle, „Fizyczna chemia
nieorganiczna na przykładzie chemii
koordynacyjnej”, Wydawnictwo Naukowe
PWN, Warszawa 1999
3.
A. Bielański, „Podstawy chemii
nieorganicznej” część 2, Wydawnictwo
Naukowe PWN, Warszawa 2005
37

DZIĘKUJEMY ZA
UWAGĘ
38
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
Wyszukiwarka
Podobne podstrony:
Lantanowcex
lantanowce
Lantanowce(2)
lantanowce spr2012
lantanowce
lantanowce, chemia nieorganiczna, laboratorium, Chemia nieorganiczna
Lantanowce, chemia
11 lantanowce
11 Lantanowce
11 lantanowce, uran, reaktor
Lantanu (III) tlenek
Pytania na kolokwium lantanowce
Charakterystyka lantanowców i aktynowców
Lantanu (III) azotan 6 hydrat
REAKCJE ZWI¥ZKÓW LANTANUPOPRAWIONE
Związki chemiczne lantanowców i aktynowców
11 lantanowce, uran, reaktor
więcej podobnych podstron