
1
Analiza miareczkowa
alkalimetryczne oznaczenie kwasu siarkowego(VI) H
2
SO
4
mianowanym
roztworem wodorotlenku sodowego NaOH
! "$#%&'(')
†
*+'*+,.-0/
1
2
3547698;:'<
<9=7<>?:A@'BCD=7<FE6HG%@JIDH:?<9KL6M8
CM47698N:?:ODH<PE08RQSE
TUMVW
X0Y
Z
[9\7[]'^?_H`
acb9d7e
f
gh?i$jlk
monpqr's
stwier
tuHv9w7x'vMy{zc|9}7x'v"~}|t$w7x}7x zc$w7|M$y7uH
L7597MN'977$Sc ¡0'¢
£¥¤7¦§¦M¨©$ª
«N¬ML®9¯°?¬±'®³²P¬9´7¬±'°Aµ·¶$¯¬¸¹¬9´7¬±'°¸Hº³°?±'¶7»0¼°'¶$½¾ºH¿À¼¸Á±'°Â'½l°?®9¯Ã¸H®M´7°'®9«Ä¿½OŬMÆ7°'®ÅÇ°'±?¶7»0¼°È¶$´7®É½Ê´7°«
½ÀÁÂË
ÌÍSÎÏ
ÐÒÑ
Ó9Ô7Õ9Ö;×'×ÊØ9Ù7ØÚ'×AÛ?ÜÓ9ÝÙ7ÕÞ
ßÛLà7ß0à$álØMÙ7Õ
ß0â
Ö;ÕMÛàãÜ
Ó9Ô7Õ9Ö;×'ÓÝÙ7Õ
à$ä%ØÝ
ÖNÕSÛàãÜ
instrumentalne.
Metody chemiczne
åçæè?éêëìcíïî7ë
wzroskowym
ð0è?éñòHé9î7óôõåö%òHé9÷7ó?éêôõöéëMø7ùìó
ú9û7ü9ýNþ?úÿú9ûÿHü9ýNþþÿúÿú9ûü
ü'ü7þ'ü lúMû"!#ÿ%$&'(#7þ7þ)"#7ü*!
ý+,Lüþ'-.ÿ/
012354768:9;6<=3->8?"3>@6BA"CD%EF12G?">@6B<1H9;6"EID0%>?"3DJC-D,K"6LFD,M6LN1POI?">@6RQSETGAU(6
laboratoryjne, wagi, zestawy do destylacji, kolumny chromatograficzne itp.)
Metody
VWYXZ\[-V^]H_YXa`_Y`b-[c]de[-b(f
gPhi(jlknmPo
p
q%r%sIrtq%uvwtq%u-vxyzsIu{}|"r}~+v^t:pr pvwSrqw~+v^t:
+-,F"=,:==;Pn "¡ "%, "¢£%=N"¤I¦¥&§ "5"¨ "©;"¥F=-
masy nierozpuszczaln
ª"¥I¢«¬¥&§( ""¥F-F "«/F(=¢ª:;=- "
¥&¢¥T% "
¢®
:S¯% "°7±
¡,,²
+-,F"²
%=N"¤
³
´&µ¶
adnika
·¸¹"º»¸%º¹"¼½·¾·¿"ÀÁ-»¸%º´TÁ-ÂÄÃ
·:Å;º,ÆF»Á5ÇJ·aÀÁ-»¸¿"Â
cm
3
tzw. titranta (roztworu mianowanego)
dodawanego z biurety do roztworu ozna
»¸%º¹"¼½·È´Fµ¶ºÉ¹"Á5µ"ººÊnÉ·ËÅǹµÌ-ÇÍÆSÎÃϹ"·Ã=ºÊ¹"Á5µ"·Ã¼½·
ÆF¼ºµ"»NÐÑÁÒ´&µ¶(ºÉ¹"Áµ"º©·¸¹"º»¸%º,¹"¼½·Ó¸ËɷɺÃ=º¹Ô:ÕÖÌÁcÌ(ÆFº,¹Ì¼Õ×
Metody instrumentalne
Å;·À¼½ºÐPØ)¹"º
Ù
À-¼É¸%¼,¹"ÁÇ.¸FÐPºÃÁ(´&µ£ÚNÁ¸Ô»¸¹Ô»,Û£ÀÇ¿£ÚNÁ¸Ô:µ"·»Û"¼Õ¡Á-»¸¹Ô»Û.¸ËÇ"ɸ%Áº¶¼,ÕB¿"ºÉº,¹Ô»ÛÜ´&µ¶ºÉ¹"Á5µ"ÎéݰÅÆS¸Ô
pomocy aparatury elektronicznej o
ÆFÎʹÔ:ÕB´FÌ·:Ź"ÁÇ͸¶·Ê%·¹"·
Ù
»ÁßÞN·ÉËÅÆS·"´FÌ-Ô»ÛÓÕ+Á¼Æ¹"Á5µ"ÎÃ}ÅÆFØÉÇ
elektrycznego do wysoko wyspecjalizowanych spektrometrów).
1.2. Analiza miareczkowa
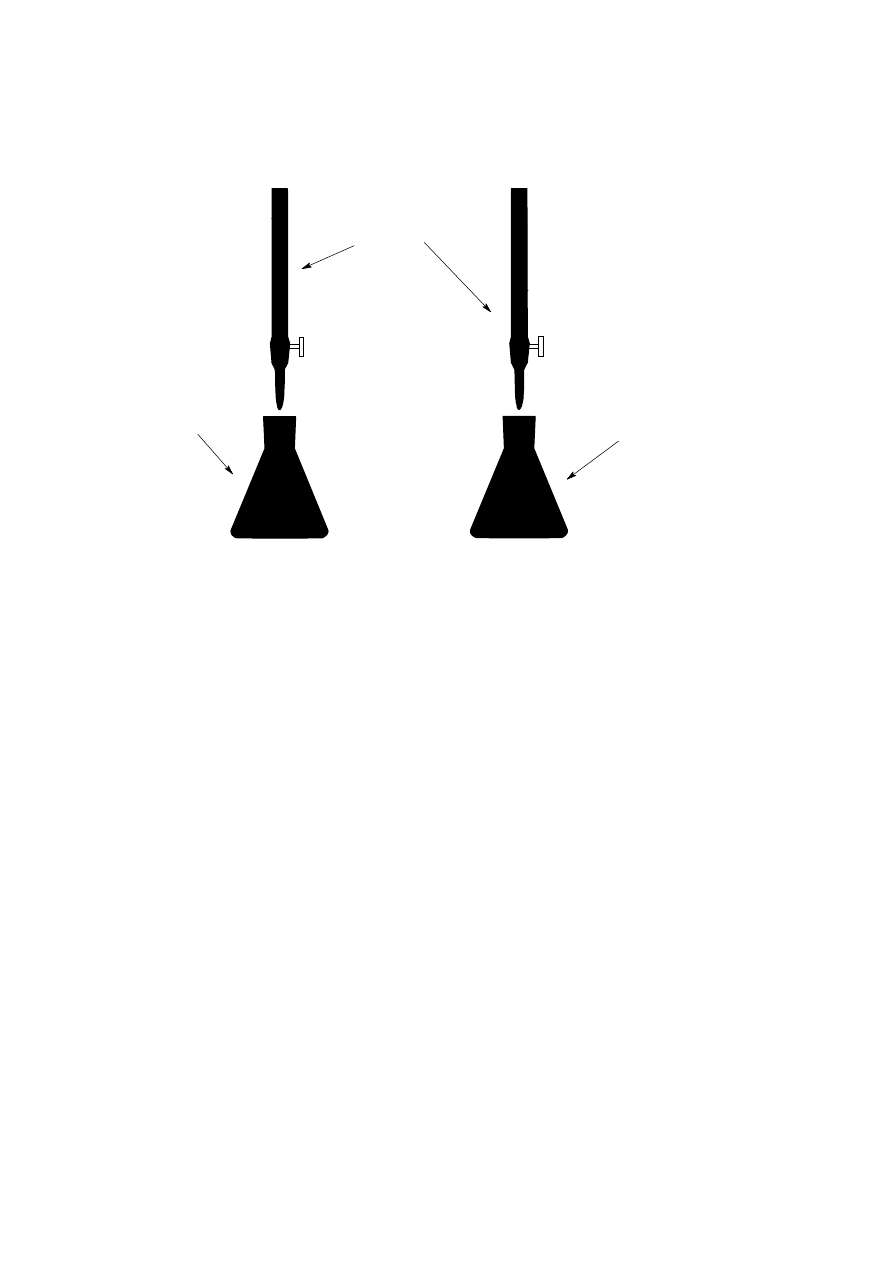
Rys. 1 w uproszczony sposób przedstawia typowy zestaw do analizy miareczkowej. W
biurecie (1
à
¸\Õ¡Á-ÀÁ-À-ÁcÌ(ÆS·ÃØ¡Å;·É¸%Á-º
¶µ"ØÓÉ·á·É»¸ÔHÌ(Çâ·¿^ÐÑÂ^Ì·
Ù
»Á¦¸¹"ºNÐÑÉÇ^ÐѼ\´IÁÂË̸Ãn×
titrant (roztwór
Õ+Á-º,¹"·Ãº¹Ô
à
·É·µ¶(ºÉ¹"Á-¼·¸¹"º»¸%·¹Ô:ÕR´FÌÂÊ%¼,¹"ÁÇÝÃÔ:ÆFºÊ
ãäå:æèçwæ¡ãé5êëæ
3
ì;í
î
ãé5ï"ð-ñnòFóãô
î
ãç=ñõ
(2
öÈ÷
ä"øõPëù^õÑñúòIðû
analit
ü
ãë:ý;ãçðñëä"ð-ãòSý;ãþ
÷%ÿ
ë
÷
ãäåý;ø,ó-þ
÷÷
û
ñ
î
òFý;ñ,þNå:æ+ñäóøéä"ø
ö
þFã
÷
ó-çþ
ï"øëøä"ñã¡ò
î
øëä"ð
î
øãä"ð-ñ
÷
ä"øäåæÖòFóûô%ñä"ð5ùæ¡ãô%ñ
óãþçÏä"ðñôÏïå
÷
ø,çðñ%òIðä"ø=ò&ùïòFóøä
õPðYòFóø
ñõ¦ç
ä"ð-ñ
÷
ä"øä"ñNõ
ð-éã
ð
ö
ì
ð-øþSñ
÷
î
ãç=øä"ð-ñ
çúóø
î
ð5æwù
î
øë
÷
ð-ñ
ý;ãé-ñø
ä"ø
ý;ãçãé5äåæä"øõPé-ñ,ý;ðñõ
ý
o kropli)
dodawaniu titranta do analitu
ü
ý;ã
ÿ÷
ãäå:æ
÷
ùçøôä
ÿ
ãïòIñ,þç=ø
õ
ÿ
þSñø
î
õPð
ñæ+ð
÷
ä"ñõ
÷
ø
ãë
÷%ÿ
ñNõ.ý;ãæ¡ð-û
! #"%$&'($*),+.-0/12*&435)617/98:(;&9<=+.&?>@=$A8@-$A2*&'B$$<9CD3B&
-1EF+GH2I1.J
K+.CL$K(91MNCOPCD2$CO1QR(+SGI&9$(
o przebiegu reakcji. Miareczkowanie
ET2I+.&?$U/98
VWYXZW.X[\]=^0_a`VcbedFWfVWVg\h^jik[V.\[*i4lmIWcdFn=hpoqW.lsrut0rvtTwexX
3
)
]Lh]=mIg\]LgydFW6i6gz?h=gqi6{xg
|h=}~\W.z?g~gm*z?g~\
h=[\hlg_xWz|Ilg^5i6[~\g@xgA =lW.z?h]O[dTm*[mI[g`W.z?g\h=[gVg\[`WB|Hl DgV.\hJlg
g\gn=hP]D^h]DmqzgA L{?W.[x\W|I^0|I]Og\xqi6h]Oh]=m*^5ik{
*U99..5uLD
uss %¢¡
£
¤¥¦¨§e©Oª¬«y
®¯=°A±I²³´µ¶.·?°¸¯9°.¹
º »¸µ¼
µ¶
½¾¿.À'Á
À'ÁÂÃľÂÄ
Â
ÅFÆÀ4ÃÇ
È¿.ÉÊLÄÈ.ÿ˾Ì=Ç
ÍDÂÀÎ
punkt
ÏÐÑjÒuÓÑÔ
Õ
Öu×9ØuÙÚ?ÛSÜ!ݬÞ'ß
miareczkowania, który w
à.áâãâ
ä'àå9æçâè9å9éê.ä?âëì
íIàïîDðâñqò6óôõæcàNä
kolbie (2
ö÷éâáIø.ä4ëêRêéëâñéâëàeíHùúDâæ.ëåJùeâëâè9åî=ð0ôòkâùûå%íIðü0íIîOâëñqò6â?îOåPîDá*ð5òkìñâyíì?ëå9çê.üçñëçcýþ5çãçè=å
éâáIø.ä4ëê
êéëâñéâëà
íHùúDâæ.ëåJù
âëâè9åî=ð0ôÿòkâù
áø.ä¨ëå9çã
îOåî=áIâëî
íì
üçéüâá*ä4ëçô
ä
ñçèð
†
Opracowa
"!#
: J. Minczewski, Z. Marczenko, „Chemia analityczna” tom 2, „Analiza
$&%&'
(
)+*,.-0/2143-56/7*&89;:=<>*8=7*,.78+3.?A@CBD@E/FHGI:4/-/KJLMNO
2
PRQSUTWV+XY[Z\SUZ]Q^`_Qbadce^efhgicjf`SUk`lS
Z]XmhSnV=gIS`VcpoXDV+_qDV=arXlso4Qtu^`X
vxw4y{z
|~}{
h UU```2
`s+`srU`sURsAE`Uhhx ¡eW =I`s4``[\¢ER 2R``£`Ue=+¤Uh¥`e¤U4¦
§
¨
©dª
«¬¯®°«
±d²³.´2µ¶·p¸H¹"¶
º.»¼.½¾2».½¼.½
¿
ÀÂÁÃÄpÅpÆÇ
Ã
ÈdÉÊ
ÁËÄÆ.Ì[Í"ÄÎ.ÅÆ.ÄÌ2Å.ÄÆ.Ä
Ï
ÐÑÒÐ+ÓÕÔ
ÖÑ×Ô
ØÙÔ
Ú
ÐÛ+ÜÂݯÔ
ݯޯØ×4Ý&Ø
ß
Ó{Ûà2Ø.á×Ô
à
(a)
(b)
Rys. 1. Typowy zestaw do analizy miare
âãäåæçuè4éeêë2ìÂíî"ïpðIç=ñë>æ{òóç=ôõî&åõë>ñîöñ&ðIë=õpñç÷ùøåúóåã+î&å÷ï\û]ê÷>îçè=üâ2ç>ýì
ïüñëæîå.õëEõë2øþäåÿ"í
!#"$&%' ()*,+-* !/. 1023%
4!5687:9;=<>9@? AB5B7 CD7E
FGH$IKJ
miareczkowania –
H$LMNOH:P
Q1R/S:T
U VW/X:Y2VZV[]\^BV\_Y:` abcU V\^\_bedfY ` b-Z\!gihZ@jlkmZWon!p]a!qsrutvVi[j#\/gw\1b!kmZi\
na barwy
mieszaniny w kolbie.
x
y{z|y{} ~},z! 'c}
e
~~ 'z|z|}z
,
y:}z|:~}~},c}:c3z ]
z|B z -
¡¢]£¤¥e¢¦¢'§¨:©¢]¨«ªu¬¥®¥|¯°¦²±³£:©¦²¨³¨:´¨:§µ¢]¥¶-±¦D·/¸¹'¨º|©¦o¸¨{¯¨º¨:©£¤¥1´¨:©¨°¦±¦£»©¨°²£¼¡
½
¼¡¾=¿£¤¥À¥|¯B¿ÂÁ ¢]¥¶¾Ã¥±³Ä ¢'¸¥|´ÄÅçc³£º§!¥³±¦²£:Ʊ³£
©¦²£:ÇÈ!ÉÊ¥|¯B¿Á ¢¥¶-¾Ë³
½
¼¡«¢£¤¥¢]¦)¢'§¨:©¢]¨Å´@¡«§!¨¼¥|©£
w cm
3
È=¥|§!¨:³Ì·!¢]Á¼£ ©¦£@¢¦¢'§¨:©¢]¨ËÅ]´Í¡|§¨¼¥|©£´ÎÇ{¥°Ïº|Ç
3
È-ª¬¥{º¥|¸¹'¨º|©£¤¥{¥³©¨±³£:©¦¨Ð·/¸¹¨º|©¦¸¨´
¨:©¨°¦²±¦£@´@¡«Ç{¨¤|¨:©£Ñ¿£f·!¢±¥©¨Ò¿-Ç©¦²£c¿Ó¢§!Ô¿¸§!¥«¢'©£@´@¡«¸¥|©¨:©¦£@Ç{¦¨ §!£±³¸¥|´¨:©¦²¨|ªÕB£¤¥Ì³¨:´Ë¨ §Ò¢]¥¶¾
w
¯¨º¨:©£c¿ÖçÔ|¯±£×´Í¡³©¨±:³¨Ø·-¦Ál¿Â¨:¸¥
¶
§£º|©¦ÄÙ¨ §Ò¡¢'Ç{£B¢¡±³©Ä׳ٴ͡|©¦¸Ô|´
½
³¡·/¸¨:©¡±:ÚÛ´
poszczególnych eksperymentach.
ÕB¨:¸´@¡«©¦o¸¨Ì³,º¥«¢¡±:Ú±³¨·-¥|´Í¡±:Ú§!¥³´¨¼¨:ÆÜÉKÃ¥º·!¢¨:´ÄÌÇ{¦²¨:§!£±:³¸¥|´Ë¨:©¦²¨Ý¿£f·!¢Þ§£¨:¸±c¿Â¨±:Ú£:Ǧ±³©¨
³¨±:Ú¥º³Ä±¨{´ß¸¥°o¯¦²£·¢]¥¼¸¥|´£c¿ÌÅ
2
ÈvÃ¥|Ç{¦²Á
àáâã]ä)ã'å!æ çã]è:é»æ{êæàæ:çâ«éìë!íîæà|çäíäè:é»æ:çæï²äãðKñóòÞâ
oznaczeni
ô
õ{ö÷«ø'ö
ùúû
öü«ýö|þËÿ²ôüÿö
üö
øüô
þ
õ{ôöü
õ{ÿ!ô
ö|þ@ú
²ô
! #"$&%'(#)%*,+-).*/)021*3)4
a)
56879#:<;!9=:>?:@A,B
C
DFEGD
H$IKJL8IMNOPQ2IL$RTSMUVO$IXWTO$HPY
Z[\]^\_#`
b)
ab8cd#e<f!dgeh[eij,kmlXn\o#b8jpb8eZgq[eKorgsha\`
c)
]tabucdTsZv^f!wqabxdc]yq\]&jzq[{a\]Ksy|2\zqj(]KsgqjZgs}(gKn\o#b8jbueZgqlXn
\a~jnq\FZ[l`
d)
]abucdTsZvh[$\dlwng[$j~g]^[lga[Zve|2[Zgqenj,kmlZe d#\gb]&\dTsn\o#bujb8eZgq[$ebd,]&j~e]
warunkach miareczkowania.
&$X,-{ #¡u$#¡8¢$(¡u£¡¤¡8.¥¦&F$.§#¡8&$$©¨u #¡8$ª
«2¬$®¯#°±²$³^°¯T´¶µ ·¸#²8¹2¸F¬º(»m¼2¸#²u°¸½´p»-¾¿¸½´À ¸#²u®¿,»-¼Á°Â¸#²8³^°³&¼¹£´Àì{®®Äů#°±²$³^Ư<«¬$®°³&®Ä µ
ÇÉÈ$ÊËÌÍ Î#ÏuÊÐ&È$ÌËÑ&ËÊνÍÒ Î#ÏuÊËÓ,ÔmÕyÖÌ×Î#Ï8ÊÐ&ÌÐ&Ø&ËÊÙÚÐ&ÊÎFÈÕyÛ2ÈÊËÑÛÜÒÑÙÐ&ÙÝÞÕ×ËÚÛàß
Substancje
podstawowe
ÖÑá$ËÈØÓÑÐÜÛÑÏ8Ì×ÊÓâÛ2ÈÊã#ÑÓÙäÌÐÚÓâã#ÌÞÕÐyÙÌã#ÓåÐæçÛÍ ÎrÙØ2Î#ÖÑá$ËÈÊèÌäãÑéFÞ$ÌËÑ
ÐÚÛ2ÊÝÊËÈ$ÊßêçÌÐ&È{ËËÚÏ8ÌÒÚèÎ#ÍÒ Î#Ï8ÊËÓTÔ-ÑÎÏ8ÊáÑæÌ×Í!ëÚÛìÎÏ8ÌÖ!ËÈ{Í2ÓÙÚÎÏ8ÌéFÓÈíáuÊpÏÐ&Ñ&×ÌÐKÚÎ#Í ÎrÙÑËÈ$Ê
È&ËÈ$ÑâÈÝã#ÌνäÌÖÈ
ÔFËÑßîêíãÙÑÒÈÑÝïã#ÑÊäÓ,Ô-È&ÛÈ$Õ×ÙÚðÎ#ÍÒ Î#Ï8ÊËÓTÔ-ØñÖÌ×Î#Ï8ÊÐ^ÌÐ&ØòÊÉãÌÙÏ
worem, którego
Û2È$ÊËÌÎFÈ$Õ(Í ÎÏ8ÊÞÊ(ÛÍ ÎFÈ!ÒÚè.ÌÓÙÚÐ&ÈuérÓÈ$ÑKérÓÈuéFÞÑKÎ#ÏuÑÓâÈ$ÌÛÑÏãóÚÓÙËÚxß
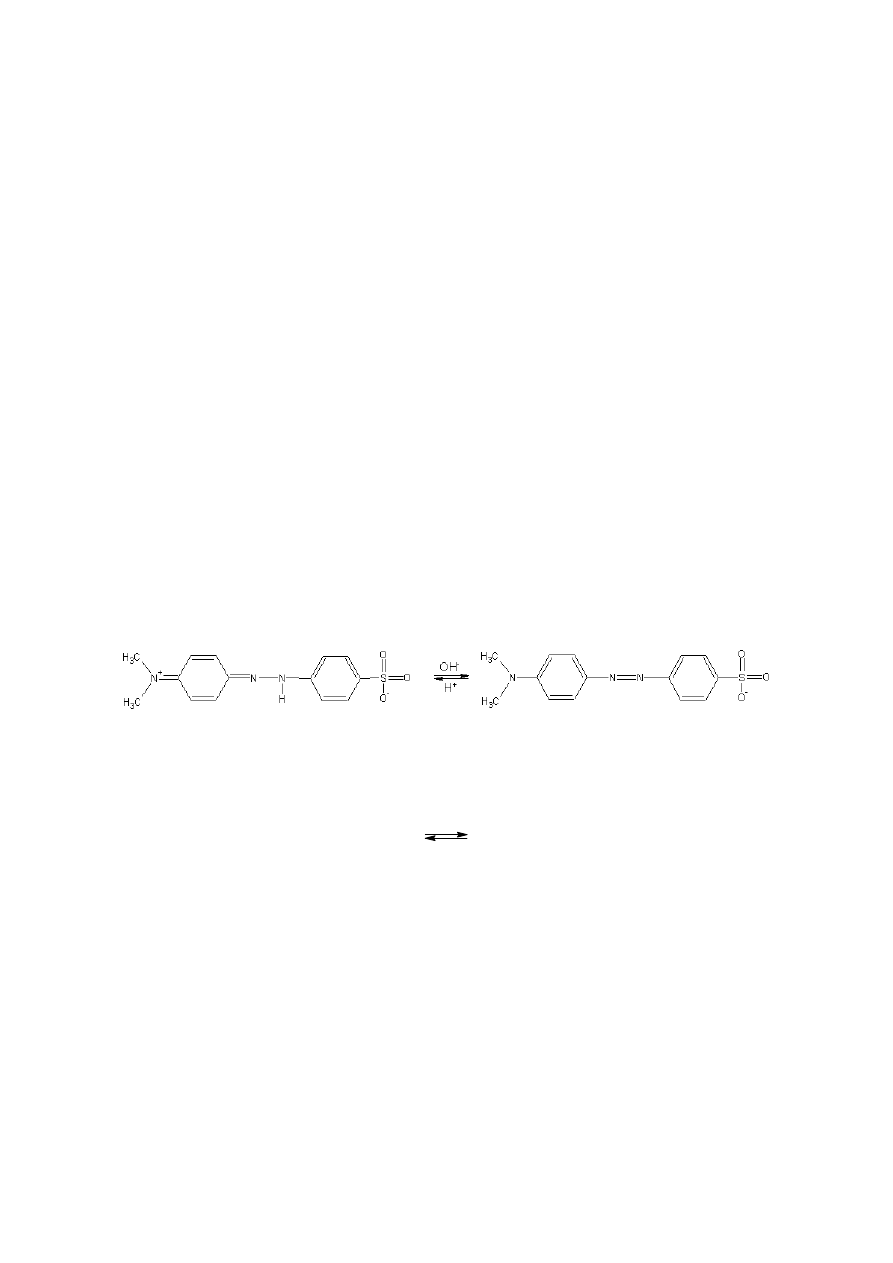
3
1.3. Miareczkowanie alkacymetryczne
ôpõö÷øùûúöúüýþuÿ
ý÷ýüúøù2üý#õú^õ-õ
alkacymetria
ý8ýy÷ý#õý-ý
ú÷üõ÷ü$ý
ù2üöúø&ýFýùü üúýFýöýùü÷ "!
HCl + NaOH
→ NaCl + H
2
O,
#
%$&uõ(')÷
H
+
+ Cl
-
+ Na
+
+ OH
-
→ Na
+
+ Cl
-
+ H
2
O
H
+
+ OH
-
→ H
2
O)
Alkacymetria obejmuje ona
* +-,"* +./1023(.
4
576
8(9;: <=>(?(<>=@ACBEDF: <(6GB:D<AH<>B>D6I:JK?@)LB&>MONBP<>
Q
:RS:?TURS@->DFA(?(<L:B&>=@>URS@->=:B&>= VRWD: <(6GB:DFARX<>MO>YV5):DF><
Z[\;]^\`_1abFcdGe
, tj. oznaczanie
za
f&ghij klmfongpgq jrshFt u(if&thuvwugxKgpSugzytrStk({rS|ghFvk(u}tfgq|-grS|gqtf&gq jr~ht u(iGfthFvr
kwasu. Metody alkacymetryczne w stosunku do kwasów i zasad, zarówno nieorganicznych,
g}|"thFgq|k(uq j klk(vkl
v&xOu(jn}t
`^FFI 7FI& G
analitycznej produkcji kwasu siarkowego, kwasu azotowego, kwasu fosforowego, sody czy
oznaczenie tzw. liczby kwasowej olejów w celu ich kwalifikacji np. jako smarów.
-( ¡^¢& £¤(E ¥¢¦K§^¨- ¤©ª&O«
¬¢Ks K -o®s
roztworze,
¯¤¨°¢(®K 1^¨ ¨±
²³(´µ&¶·´¸µX¹¥º»G¼½¾¼¿¼À-ÁÂìĴµ&Á¿Á¶¿¾µ³Å´½ ÆÁÇ
´ºÈF¶ÉKÀ-´¿ ÊmµC¹¥º¼
Ë
ÌÍ%ÎÐÏÑHÒ`Ó;ÔÕ(Ö1Õ×SÍ-ØÌÍÙÛÚ¥ÔÜÝÜÞ&ÍGߥÎØHÕHÎÞ&ØàÚ¥ÌÙá ÜÌØHÕØßOØÝÜÞ&Ùàâ"ÝØÌ ÖÞwߥÎØ(ãÌÍÎâ
ÞåäæØÔFØÎ çIÙÔÖÕèêéë(äÖ×
á ÜìÕØÎÔFÙßKÍ-ÙíÏÑîÕ×SÍ-ÙÌÍØíïØÔÞð
ñóò)ôõö÷øùú1ûúüFýCýþ
ÿþ
õ%ùøûö±ÿô
!
"#$&%'()*,+.-/10234"5,67+,89-:5-<;$&= >?<'
@%AB,$BCDE<?AGF-<;IHJ%*
-<4"#%8'#HJK%H
-:4AGLMNO?-<?5A7P%HQ-:B'
RSNTUWVYX[Z]\G^_`MaP_
bc#def8ghijkge?icElMgem1n8c#o,dp<e4g5qGghgf8ihdrsptvuxw3yzwN{G|ieMfPi~}#BqGij
barwa czerwona
&
c
8@7L#:[)~,?, &k¡J£¢
(gdzie skrót In znaczy indykator,
¤,¥BO?¦
§¨ ©<ª)«¬7§,§®°¯:±5¯<²³&´µM§®°¶·?©´¸§¨ ©¨¹¯º
»G±£¼
½
®§±,³B±
½
»G´³&®¨¾§´#¿,À,Á[©¨¾»£À,µ4±Ã@±5»&Ä5Ã@±,³B±¶CÄ<¿,ÅÆ#®µ¶8¨&®Ç1©,µ4®Æ#±,³&±¶8´#¿,È,¨ §¨¾»&µ?±
½
®§±,³7¿É#ÊÁ7ŨB®ÇQ´³&¨ Æ#´µMÄ5§±¶P´Ë¿
ÅÆ#®µ¶8¨&®ÇÌÃ@®»BÄ,³B±¶P´Í¨:¨ §,§®«
ÎÐÏ
Ñ
Ò
Ó
ÔÕ#Ö
×
ØÚÙ
4
Û:Ü5ÝßÞáàãâäæåä£ç[èêé
wiczenia.
ë:ì&íîì<ï3ðæñ,òIó
ô
õYöî÷øæù&úêùYûüù[÷øæýËþ1÷øæù&úÍÿýîö[þQý,ÿP÷
!"$#&%'(*)+! %-,)/.012-!3)456.71%89-%;:9%%<!".0%!%1=
.0/91=>?)$5@
ABC-DAFEGHIKJML/ANOPAL1QSRUT-VXW
PAYZ[YC]\/O^_APTBZ`bacP d&CeAfP8^DA"O$APTBZ`gBdC
NTP d&CL/TihjZ-k-Z
lnm
2
oqp
rs"tvuw-xzy|{}-x&w~s
0/}- r/~-{&w00wr$out
3
txz r$~{w-
/r1y}]</u-&wus3 w /r&sx& }{j;r ¡
¢-£¥¤0¦§U¢¨
3
w kolbie miarowej na
250 cm
3
©-ª3«¬7c®¯°±
¨£²
+«¯;°
£
°³n°¯-´
²µ
¬ ¶·¸¹«
²nº
¬
¨£²
c«¯-»©
¼7½
³
µ²
°
£&²
·
½
¹1«¬
¨
¯°
²-¾
·
º
½
²
°b/¿0·+À¸g¹/·«
½
º
À¹iÁï]Ä<ÅÆ°
£²º
¬"°·
£
¶·®Ç ¯
dnie 0,1 mol/dm
3
, w
«
º £
±«-®Á«
½
¬
¨
¯¸¬È°¯-´
²µ
¬
º
¬«-°¯
¢
«¬»É
²-¾
·
¨£
¯°·Ê©ÌË
½
¬
¨F¢-²
´zÁ°¯´
²µ
¬¶·g®·´z¸¬Í
½
·
µ
®·
º²
É
·¶
¨£²
¹«¬» ¿
£
¿
²
½
±
¤0¦¢¨
3
®
º
¯cÁÃ4·´z°
²¾
·Î·*«-°¯°¬
¨
½
³
µ²
°
£
ÁÐÏ
½
³
µ²
°
£&²
·¶
¢
«¬
½
¯-» «
²
½
¨
£&²
½
®
£
°¯
¸Á
½
²
´
¢-²ÑcÒ
¶·¶¯-»
¤
-
Ó
®¹/·"¿0´
²Ôº
c®¯Õ
Ö×zØÙÆÚÜÛ0ÝÞ;ßÆ×bàáØâ Ù-àÖ×&ãåäXæç×ãè+é
ÙêÝÃëì×zíî/ãï$ðåÖÙ;ñ0ã;âÖ×ê
î/áéïäáî/ã;çfíñ7îéã-àÖ×&áÃñ7î1éæòá"ï áä Ù;Öã-òáÃä áàáîá"ï$óã;ÖØíÍè4áàíÝô×&Ùî/ãõé-Øáä Ùêàáöé-ç×ÙÖæÐ÷Ùî1äXæ
î/áéïäáî1íøéXõéãî1äáÖã1ùúÖÙné×ã-ó&áÖûÝÜüXé-ÖÙõéãÖ×ã6á"ñ0Ùîiï ãýùjãèïÊÖÙnîã-ÙØõ1ù>×þ
NaOH + HCl = NaCl + H
2
O
ô×Ùîã-õé-ØáäÙÖ×ãbñ7î1éã;ñ7î/áäÙ-àé×&ê
ÿ
îÙéæ
ØÙàáî/Ùéáäá?Öá"ïíù>û-õ
á
÷ùjðï$á4ê
é-íæÜï$ãòá?î/áéïä áîií
Ù]üÝ
ü
÷ó×&õéæê
cîã-àÖ×û
á÷ù>ð;ï$á4êvÙ
ÖÙ]è/ï$ð;ñ7Ö×&ã
ÖÙSùjã1ù
ñ0áàè/ï$Ùä×ã
èï$ðãÖ×&ã
î/áéïä áîií
ä áàáîá"ï$óã;ÖØí
è4áàíøéXàáØâ Ù-àÖá+õ-×û
3
.
v
1
=
v
2
= v
=
v
3
=
c
NaOH
= c
HCl
c
NaOH
= .................... mol/dm
3
!#"%$&(')*$+&
,
-/.
021
o 0,0001 mol/dm
3
)
2.2. Oznaczanie kwasu siarkowego H
2
SO
4
354 6879;:=<>(9?6A@(74 BDC6FEBG<IHKJLHNMO<6PE@BGQSR(@TUGVXWZY@<><S[OMO79\687IQ]>M QI^N_`M [O@^NaSM @BG@Y@E@[cb(9:=MO<6A@BGQPd
@e\f@gdhQ:i>@^jaSMlkmmea:
3
MnY@;\fQ]o >M _pBD@YqrYQ/HA4 9([ @BG<>q
stvuw8xIyKuz|{~}%t(Gwstu Ssz x
;=zOxIyjIS{zfx]XLts=zOxw8(f
cm
3
Xx(tw8t(GtwPwPIxz x/NLstutc(yAt(SutDx| z¡stsS
yKu¢Szcu£¤f{¥]¦{¨§~zOwAxS©SutDSstªSz («wP¬2yKu¢Szu®¯©IxwPGtxPn°IzOxS t;{
ts©IIy±=zOwAx©SutD]z ²IS©]³ts(IzIyA´]µg©S%wAxu©Pg(¶
H
2
SO
4
+ 2NaOH = Na
2
SO
4
+ 2H
2
O
§~z w8xS©SutGz x¡w8Ix]w8tDSs(IzO·`wA
tOz ©(¬Kw8xSsz 5tµh´]Xtj²S;xS(t`zw8(X;{
v
1
=
v
2
= v
NaOH
= v
¸c¹ º
=
v
3
=
m
H2SO4
’
=
(w 25 cm
3
roztworu)
v
HCl
v
NaOH
1 v
NaOH
c
NaOH
M
H2SO4
2 1000

5
m
H2SO4
= 4 m
H2SO4
’
(w 100 cm
3
roztworu)
M
H2SO4
= 98,072 g/mol
m
H2SO4
= ...................... g
»#¼²½¾(¿]ÀÁ½Â¾;Ã]ÄIÅÆ
ÇÈiÉ]ÊPÉÉÉËÍÌÏÎ
Wyszukiwarka
Podobne podstrony:
Cw1 Analiza miareczkowa
ANALIZA MIARECZKOWA
ANALIZA MIARECZKOWA, Farmacja studium 2 letnie, I II semestr, analiza
CHEMIA ANALIZA MIARECZKOWA, PWR, chemia
Analiza Miareczkowa 1
Ćwiczenia z analizy miareczkowej 1
ANALIZA MIARECZKOWA. ALKACYMERIA, Biochemia, Biochemia
Ćwiczenia z analizy miareczkowej
podstawy analizy miareczkowej
ANALIZA MIARECZKOWA
Analiza miareczkowa
analiza miareczkowa2012
Analiza miareczkowa jest metodą ilościowego oznaczania substancji, Studia, Ogólne, Fiyzka, od romka,
Analiza miareczkowa, kompleksom Nieznany
ANALIZA MIARECZKOWA
sprawozdanie analiza miareczkowa 3
sprawozdanie analiza miareczkowa 2
więcej podobnych podstron