
1
POLITECHNIKA WROCŁAWSKA
INSTYTUT INŻYNIERI BIOMEDCZNEJ I POMIAROWEJ
PL. GRUNWALDZKI 13, BUD. D1, POK. 026B
Laboratorium z Biofizyki
Typ dokumentu:
Sprawozdanie #1
Data
wykonania
ćwiczenia:
08.10.2012
Tytuł:
Ćwiczenie 2.
Zależność od optycznych właściwości
ośrodka w pomiarach
spektrofotometrycznych.
Autorzy:
CZĘŚĆ B.
Cel ćwiczenia:
Określenie charakterystyki spektralnej kuwet pomiarowych wykonanych z różnych
materiałów, zbadanie stabilności absorpcji dla wybranych roztworów, zbadanie efektu rodzaju
materiału kuwety na zebrane widma związków.
Wstęp:
Absorbancja- współczynnik absorpcji (pochłaniania) światła, stosowany w spektrofotometrii
do oznaczania stężenia substancji w roztworze; absorbancja jest funkcją liczby cząsteczek
absorbujących promieniowanie, znajdujących się na drodze promienia świetlnego, jest więc
wprost proporcjonalna do stężenia roztworu. Absorbancja jest równa logarytmowi
dziesiętnemu ilorazu natężenia monochromatycznej wiązki wchodzącej do ośrodka
absorbującego i natężenia wiązki przepuszczonej przez ten ośrodek.
Absorpcja- proces pochłaniania energii fali elektromagnetycznej przez substancję.
Kalibracja spektrofotometru- jest wiele metod kalibracji spektrofotometru, najczęściej
stosuje się metodę serii wzorców polegającą na przygotowaniu roztworów wzorcowych (o
znanym stężeniu) następnie poddaje się go pomiarom. Dzięki temu wartość sygnału
mierzonego dla danego stężenia analitu nie ulega zmianie.
Linia bazowa- zebrane widmo, do którego odnosi się kolejne pomiary.
Spektrofotometr UV-Vis- urządzenie służące do badania absorpcji promieniowania
elektromagnetycznego z zakresu nadfioletu oraz światła widzialnego przez ciecze, ciała stałe i
gazy. Głównymi częściami spektrofotometru są: źródło światła, monochromator, kuwety
pomiarowe, detektor, wzmacniacz, miernik urządzenia rejestrującego lub interfejs połączony
z komputerem.
Widmo absorpcyjne- zależność absorbancji od długości fali promieniowania
elektromagnetycznego.
2
Odczynniki, materiały i urządzenia.
- woda destylowana;
- bufor fosforanowy;
- metanol techniczny;
- błękit metylenowy;
- pipeta szklana o pojemności 5ml
- pompka do pipetowania o pojemności 25 ml
- spektrofotometr VIS-723G;
- kuwety pomiarowe: kwarcowa, szklana, plastikowa, o szerokości 1 cm
- wszystkie pomiary wykonane zostały w programie UVSoftware [Spectrum Scan] i zapisane
zostały w formacie Excel.
1. Charakterystyka spektralna kuwet pomiarowych.
a)Ustawienie spektrofotometru na zakres pomiarowy 340-500nm.
b) Kalibracja spektrofotometru dla powietrza, a następnie pomiar widma spektralnego dla
pustej kuwet plastikowej.
c) Kalibracja spektrofotometru dla powietrza, a następnie pomiar widma spektralnego dla
pustej kuwety kwarcowej.
d) Kalibracja spektrofotometru dla powietrza, a następnie pomiar widma spektralnego dla
pustej kuwety szklanej.
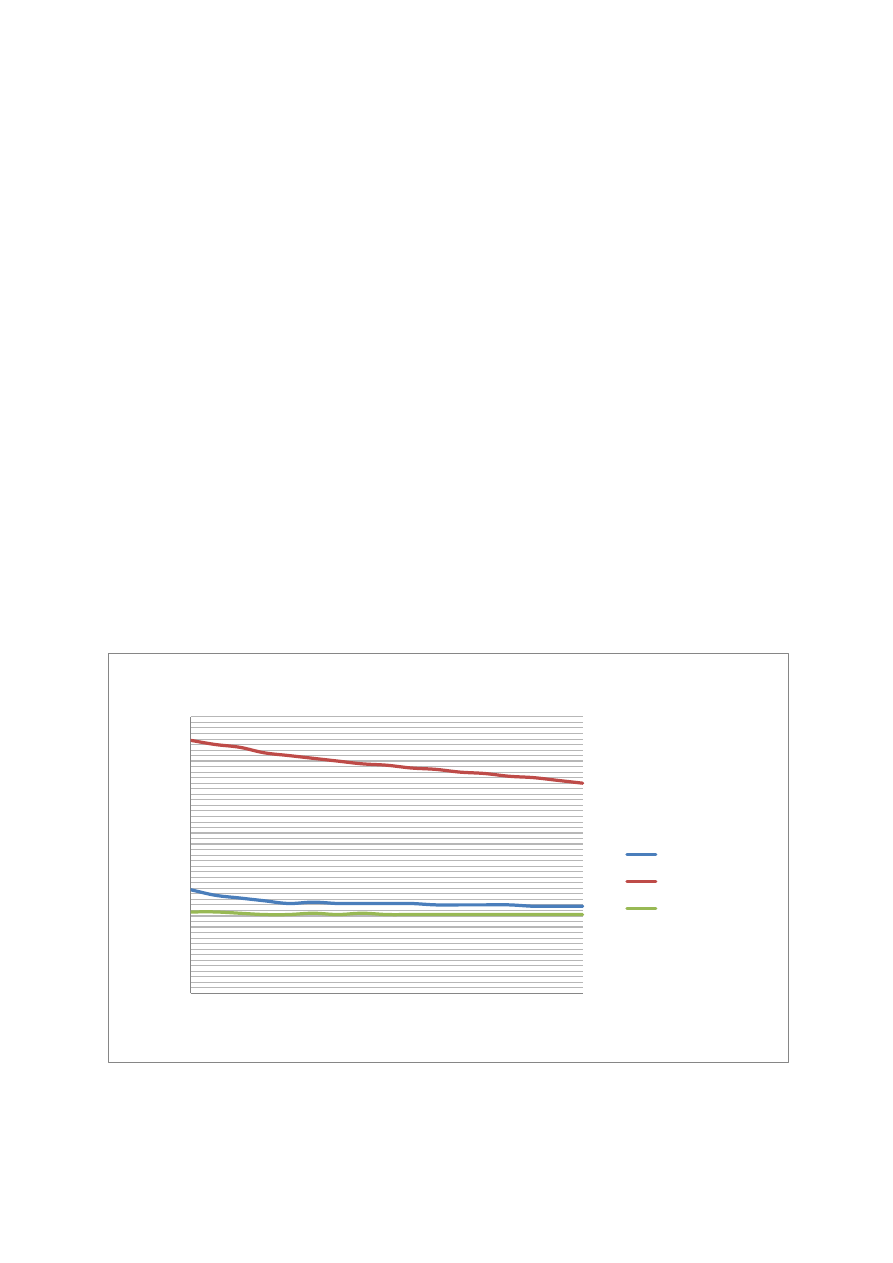
Rysunek 1. Wykres absorbancji w funkcji długości fali dla trzech analizowanych kuwet.
2. Pomiar linii bazowej dla wybranych roztworów.
0
0,02
0,04
0,06
0,08
0,1
0,12
0,14
0,16
0,18
0,2
340,00
390,00
440,00
490,00
A
b
sor
b
an
cja
Długość fali [nm]
A(λ)
Kuweta plastikowa
Kuweta szklana
Kuweta kwarcowa
3
a) Zebrano linię bazową dla pustej kuwety szklanej w zakresie 340-500nm, a następnie do
kuwety odmierzono 3ml buforu fosforanowego za pomocą szklanej pipety o pojemności 5 ml
i zmierzono widmo spektralne co 1nm.
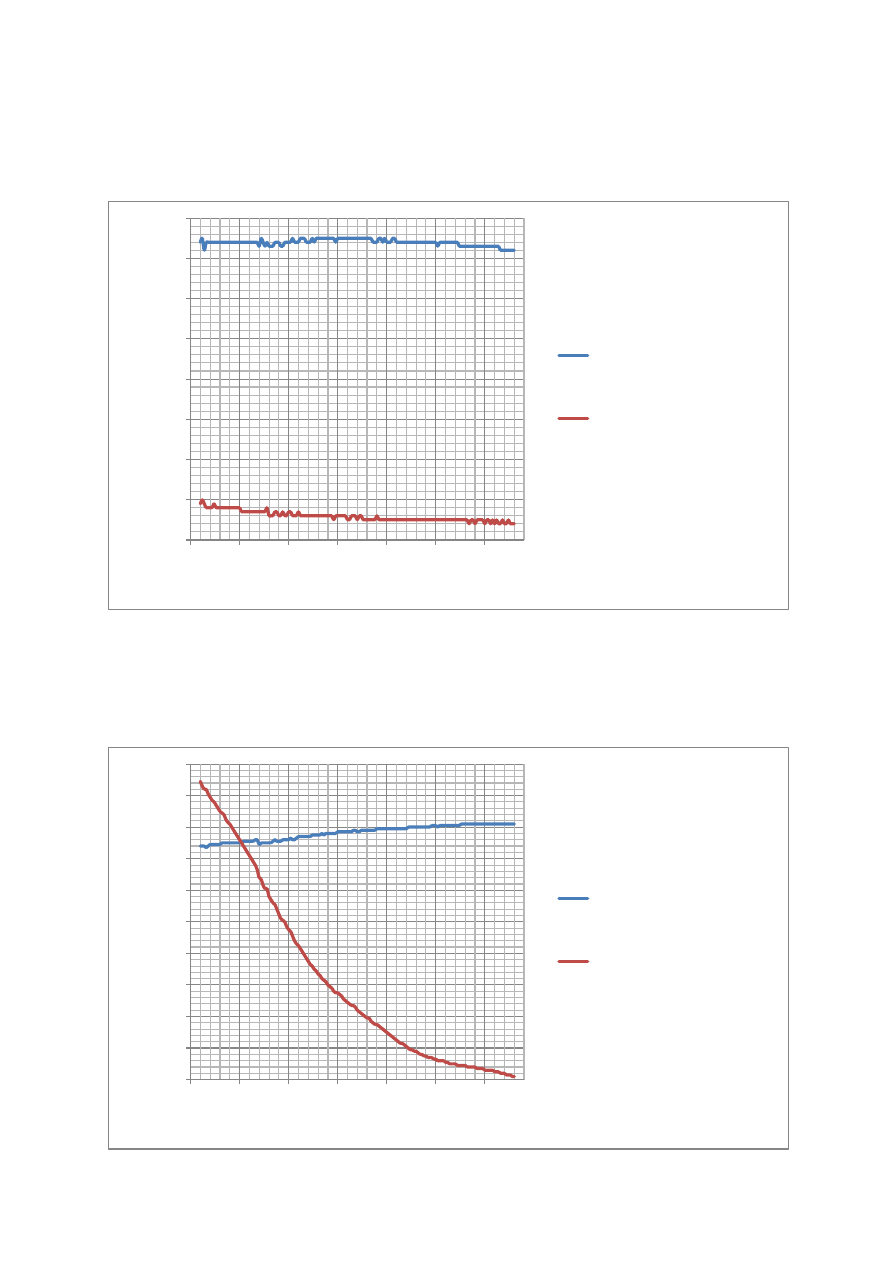
Rysunek 2. Wykres absorbancji w funkcji długości fali dla buforu fosforanowego w kuwecie szklanej.
b) Zebrano linię bazową dla pustej kuwety szklanej w zakresie 340-500nm, a następnie do
kuwety odmierzono 3ml metanolu technicznego za pomocą szklanej pipety o pojemności 5 ml
i zmierzono widmo spektralne co 1nm.
0,03
0,04
0,05
0,06
0,07
0,08
0,09
0,1
0,11
335
360
385
410
435
460
485
A
b
sor
b
an
cja
Długość fali [nm]
Krzywa kalibracyjna dla pustej
kuwety szklanej
Pomiary absorbancji dla
kuwety szklanej z buforem
fosforanowym
0,05
0,07
0,09
0,11
0,13
0,15
0,17
0,19
0,21
0,23
0,25
335
360
385
410
435
460
485
A
b
sor
b
an
cja
Długość fali [nm]
Krzywa kalibracyjna dla pustej
kuwety szklanej
Pomiary absorbancji dla
kuwety szklanej z metanolem
technicznym
4
Rysunek 3. Wykres absorbancji w funkcji długości fali dla metanolu technicznego w kuwecie szklanej.
3. Efekt rodzaju materiału kuwety na zebrane widma związków.
a) Zebrano linię bazową dla pustej kuwety szklanej w zakresie 500-600 nm. Następnie
odmierzono za pomocą pipety szklanej o pojemności 5 ml 3 ml roztworu błękitu
metylenowego do szklanej kuwety i zebrano jego widmo spektralne.
b) Zebrano linię bazową dla pustej kuwety plastikowej w zakresie 500-650nm. Następnie
odmierzono za pomocą szklanej pipety o pojemności 5 ml 3ml roztworu błękitu metylowego
do kuwety plastikowej i zebrano jego widmo spektralne.
c) Zebrano linię bazową dla pustej kuwety kwarcowej w zakresie 500-650nm. Następnie
odmierzono za pomocą szklanej pipety o pojemności 5 ml 3ml roztworu błękitu metylowego
do kuwety kwarcowej i zebrano jego widmo spektralne.
d) Odmierzono za pomocą szklanej pipety o pojemności 5 ml 3 ml wody destylowanej i
wlano do kuwety kwarcowej. Zebrano linię bazową dla kuwety kwarcowej z wodą. Następnie
odmierzono 3 ml roztworu błękitu metylenowego za pomocą szklanej pipety o pojemności 5
ml i zmierzono widmo błękitu metylowego w kuwecie kwarcowej.
e) Odmierzono za pomocą szklanej pipety o pojemności 5 ml 3 ml wody destylowanej i wlano
do kuwety szklanej. Zebrano linię bazową dla kuwety szklanej z wodą. Następnie odmierzono
3 ml roztworu błękitu metylenowego za pomocą pipety szklanej o pojemności 5 ml i
zmierzono widmo błękitu metylowego w kuwecie szklanej.
f) Odmierzono za pomocą pipety szklanej o pojemności 5 ml 3 ml wody destylowanej i wlano
do plastikowej kuwety. Zebrano linię bazową dla kuwety plastikowej z wodą. Następnie
odmierzono 3 ml roztworu błękitu metylenowego za pomocą pipety szklanej o pojemności 5
ml i zmierzono widmo błękitu metylowego w kuwecie plastikowej.
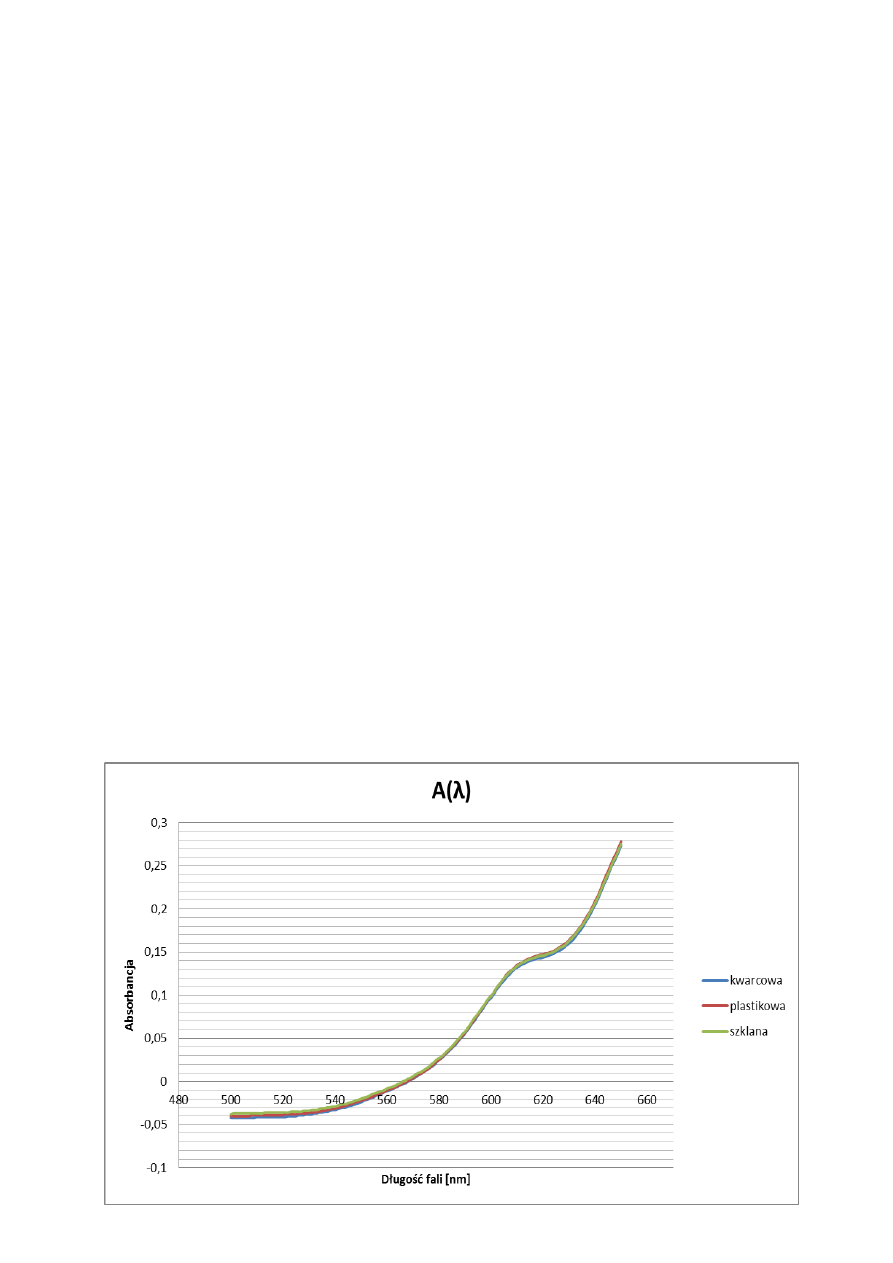
Rysunek 4. Wykres zależności absorbancji roztworu błękitu metylenowego od długości fali dla różnych kuwet (po
wyzerowaniu na pustą kuwetę)
5
Wnioski:
Wnioski do części 1:
Na podstawie wykresu rys.1
widać, że największą absorbancję ma kuweta wykonana ze szkła.
Najmniejszą z kolei kuweta kwarcowa, właśnie dlatego to kuwetę z tego tworzywa najlepiej
jest używać w pomiarach. Szczególnie tych, gdzie zakres pomiarowy jest poniżej 380 nm
(zakres UV) powyżej tego zakresu można też używać kuwet wykonanych ze szkła.
Postępując zgodnie z tą zasadą można uniknąć wielu przekłamań podczas pomiarów. Kuweta
kwarcowa ma najmniejszą absorbancję dlatego najmniej wpływa na wyniki badań substancji
znajdujących się w ich wnętrzu.
Dzięki wykresowi porównawczemu przedstawionemu na rys.1
możemy zauważyć kilka
zasadniczych różnic między kuwetami w kontekście mierzonej długości fali:
Wartość absorbancji dla wszystkich kuwet spada wraz ze wzrostem długości fali.
Można zauważyć, że dla kuwety szklanej jest on dużo bardziej dynamiczny niż dla
pozostałych dwóch kuwet.
Różnica między wartością absorbancji na początku i końcu pomiaru dla kuwety
kwarcowej jest najmniejsza.
Dla kuwety plastikowej można zaobserwować, że wartość absorbancji szybciej spada
dla długości fali w przedziale 340,00-380,00 nm, czyli dla pomiarów w zakresie UV,
niż dla pomiarów w zakresie światła widzialnego 380,00-500,00 nm. Podobną
zależność można zauważyć dla pozostałych dwóch kuwet, nie jest jednak ona, aż tak
znacząca.
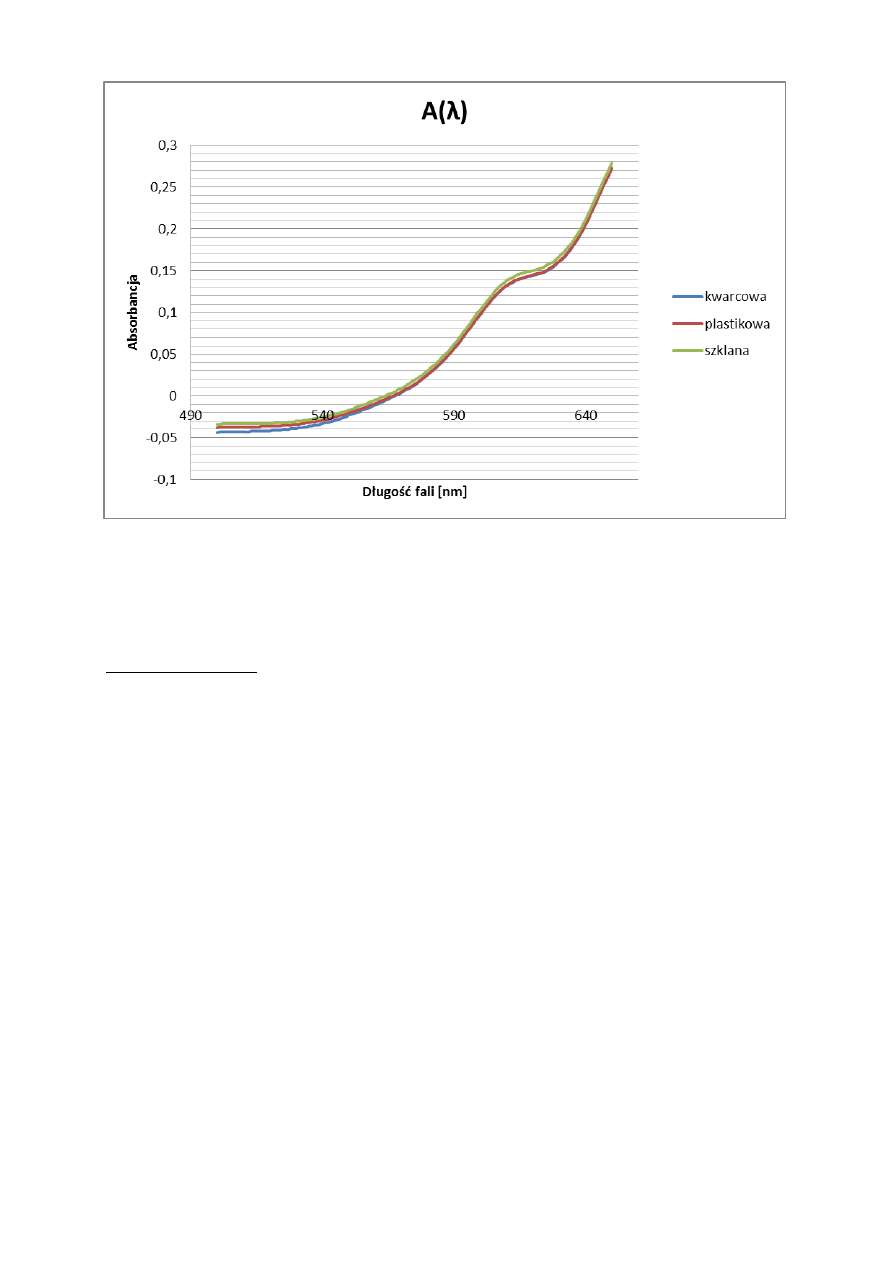
Rysunek 5. Wykres zależności absorbancji roztworu bółękitu metylenowego od długości fali dla różnych kuwet (po
wyzerowaniu na kuwetę z wodą)

6
Wnioski do części 2.
Na podstawie wykresów: rys. 2 i rys. 3
można stwierdzić, że bufor fosforanowy wykazuje
większą stabilność niż metanol techniczny, ponieważ absorbancja buforu nie ma znacznych
odchyleń wraz ze zmianą długości fali. Niewielkie odchylenia mogły być spowodowane
obecnością pęcherzyków powietrza w kuwecie, zarysowaniami bądź zabrudzeniami.
Jednakże nie można porównać stabilności tych dwóch roztworów ze stabilnością wody,
ponieważ dane zostały niezapisane bądź nieskopiowane na nośnik.
Wnioski do części 3:
Wykresy zależności absorbancji od długości fali dla kuwet wykonanych z różnych materiałów
są zbliżone do siebie. Największe różnice występują dla krótszych fal (500-580 nm). Dla
kuwety szklanej absorbancja jest największa, a dla kwarcowej najmniejsza. Przy dłuższych
falach wykresy absorbancji dla kuwety plastikowej i kwarcowej pokrywają się, natomiast
absorbancja dla roztworu w kuwecie szklanej jest większa.
Mierzyłyśmy widmo tej samej substancji: roztworu błękitu metylenowego, jednak dla
różnych kuwet otrzymałyśmy nieco różniące się między sobą wykresy. Świadczy to o tym, że
materiał, z którego jest wykonana kuweta ma wpływ na pomiar absorbancji. Absorbancja jest
addytywna, więc widmo zebrane dla błękitu metylenowego jest sumą absorbancji samego
roztworu, jak i kuwety, w której się on znajdował. Różnice między wykresami dla różnych
kuwet są niewielkie: największa różnica wynosi ok. 0,01 jednostek absorbancji i występuje
między pomiarem dla kuwety szklanej, a pomiarem dla kuwety kwarcowej przy długości fali
500 nm (Przy kalibrowaniu urządzenia na kuwety z wodą). Materiałem najbardziej
absorbującym jest szkło, a najmniej: kwarc. Największy wpływ materiału kuwety na pomiar
jest dla fal w zakresie 500-580 nm. Kuweta kwarcowa wykazuje najmniejszą absorbancję, a
więc jest ona najlepsza do wykonywania pomiarów spektrofotometrycznych. Na błędy
pomiarowe mogą mieć wpływ bąble powietrza w roztworze oraz ewentualne
zanieczyszczenia na danej kuwecie.
Ćwiczenie przewidywało również badanie efektu długości drogi optycznej na wartość
absorbancji, jednak ze względu na brak odpowiednich kuwet pomiarowych (o różnych
drogach optycznych), nie mogłyśmy wykonać tej części ćwiczenia.
Bibliografia:
http://aneksy.pwn.pl/biologia/1.php?id=1467628
http://portalwiedzy.onet.pl/73596,,,,absorbancja,haslo.html
http://pl.wikipedia.org/wiki/Absorpcja_%28optyka%29
http://www.chemia.uj.edu.pl/chemanal/dydaktyka/analitycznaI_pliki/spektrometria.pdf
Z. Jóźwiak „Biofizyka. Wybrane zagadnienia wraz z ćwiczeniami” s.114
W. Zieliński „Metody spektroskopowe i ich zastosowanie do identyfikacji związków
organicznych”
Wyszukiwarka
Podobne podstrony:
19 Dobór ćwiczeń w zależności od siłyid 18263 ppt
FIZYK~32, AGH, agh, programinski, Laborki, Laborki, Lab, FIZYKA - Laboratorium, lab-fizyka, Zależnoś
Fizyka 2, AGH, i, Laborki, Laborki, Lab, FIZYKA - Laboratorium, lab-fizyka, Zależność okresu drgań w
Ćwiczenie 72 - Drgania relaksacyjne, Weterynaria Lublin, Biofizyka , fizyka - od Bejcy
Pomiar strat ciepła w zależności od różnicy temperatur, LAB17A, Ćwiczenie 17
5 - Miar. pH - metryczne, Sprawozdanie - 5 - xx, Celem ćwiczenia jest wyznaczenie zależności potencj
20 DOBÓR ĆWICZEŃ W ZALEŻNOSCI OD SIŁY MIĘSNIid 21301 ppt
biofizyka1 ZALEŻNOŚĆ POMIARU OBJĘTOŚCI IMASY W ZALEŻNOŚCI OD LEPKOŚCI WPŁYW ADHEZJI CIECZY DO MATERI
19 Dobór ćwiczeń w zależności od siłyid 18263 ppt
właściwości reologiczne jogurtów w zależności od czasu ich dojrzewania
Organizacja działu handlu zagranicznego w zależności od grup
Pielęgniarstwo w intensywnej terapii w zależności od rodzaju zabiegu 2009
DYNAMIKA PLONOWANIA ŁĄK W ZALEŻNOŚCI OD SUMY OPADÓW I NAWOŻENIA
Mostek Wheatstonea slizgowo, Fizyka, FIZYKA, Fizyka ćwiczenia Miszta, Fizykaa, LabFiz1 od izki, LabF
Ćwiczenie 71, Studia, 1 rok, od Magdy, FIZYKA, Fizyka, Labolatorium
Spraw 22b, Weterynaria Lublin, Biofizyka , fizyka - od Bejcy
Drgania tlumione wahadlo, Fizyka, FIZYKA, Fizyka ćwiczenia Miszta, Fizykaa, LabFiz1 od izki, LabFiz1
cwiczenie lab nr 5i6 SPC
więcej podobnych podstron