
1
Wpływ leków, suplementów
diety i używek na wyniki
badań laboratoryjnych.
mgr Kamil Górski
Pracownia Analityczna Zespołu Pracowni Laboratoryjnych Szpitala
Powiatowego im. Miłosierdzia Bożego w Limanowej
Streszczenie
Wiele substancji aktywnych zawartych w lekach, suplementach diety oraz
używkach wpływa na przemiany biochemiczne białek, lipidów,
węglowodanów, oraz na gospodarkę wodnoelektrolitową, układ równowagi
krwi, układy enzymatyczne, układ krwiotwórczy, mogą zmieniać
wartość diagnostyczną niektórych testów laboratoryjnych opartych na badaniu
aktywności enzymów, stężenia lub ilości różnych substancji w organizmie.
Wiele z nich przyjmowanych jest przez pacjentów mechanicznie i bez
jakiejkolwiek kontroli lekarskiej. Mogą one w różny sposób wpływać na wyniki
badań laboratoryjnych powodując rozmaite interferencje w badania
laboratoryjne, a co za tym idzie uzyskanie błędnych wyników i błędne decyzje
terapeutyczne. Błąd taki jest błędem przedlaboratoryjnym, przedanalitycznym,
czasem trudny do wyeliminowania na etapie laboratorium. Szczególne ryzyko
wiąże się z pacjentem badanym po raz pierwszy, gdzie nie posiada się w
systemie informatycznym wcześniejszych wyników badań i nie ma możliwości
odniesienia się do ewentualnych, często dziwnych zmian w wynikach badań.
Wobec stale rosnącej liczby leków oraz rosnącej liczby metod i badań
laboratoryjnych liczba krzyżowych możliwości wpływu różnych substancji na
wyniki badań laboratoryjnych jest ogromna, a problem tego rodzaju interakcji

2
pozostaje otwarty. Nie uwzględnianie tego zjawiska w praktyce lekarskiej jest
często przyczyną błędnej interpretacji wyników badań, a w następstwie
niewłaściwego rozpoznania choroby i niewłaściwej oceny skuteczności jej
leczenia.
Słowa kluczowe
Leki, suplementy, interferencja, używki, błędy przedlaboratoryjne.

3
1. Interferencja i mechanizmy interferencji
Interferencja jest opisywana jako wpływ substancji obecnej w systemie
analitycznym, która powoduje zmianę zmierzonego poziomu analitu w stosunku
do wartości prawdziwej, wyrażanej jako stężenie lub aktywność.
Międzynarodowa Federacja Chemii Klinicznej (IFCC) proponuje następującą
definicję: interferencja analityczna jest systematycznym błędem pomiaru
spowodowanym przez składnik próbki, który sam może nie wytwarzać sygnału
w procesie analitycznym.
Interferencje mogą być zależne lub niezależne od oznaczanego analitu;
pozytywne jeśli powodują podwyższenie wyniku lub negatywne, jeśli
przyczyniają się do obniżenia wyniku.
Interferencje w badania laboratoryjne są często spotykane z powodu ich
liczebności i powszechnego użycia różnych preparatów. Wpływ tych substancji
można podzielić na:
Mechanizmy wynikające z farmakologicznych właściwości substancji.
Mechanizmy wynikające z fizykochemicznych właściwości substancji.
toksyczny (prowadzący do interferencji)
Mechanizmy wynikające z fizykochemicznych właściwości substancji:
Substancja interferująca lub jej metabolit ma podobną budowę lub działanie
biochemiczne lub antygenowe do analitów oznaczanych w testach
biochemicznych/immunochemicznych np. metabolit propranololu (4-
hydroksypropranolol) interferuje w 2 metodach oznaczania bilirubiny (met.
Jendrassika – Graf i Evelyna – Malloy`a) Powoduje to wystąpienie fałszywie
dodatniej lub fałszywie ujemnej reakcji służącej do oznaczania określonego
wskaźnika laboratoryjnego. Interakcje te występują jednak zwykle tylko przy
zastosowaniu jednej z metod używanych do oceny danego wskaźnika.
Mechanizmy wynikające z farmakologicznych właściwości substancji:

4
Są one związane z wywoływanymi przez leki pożądanymi lub niepożądanymi
objawami ich działania w organizmie np. zwiększenie stężenia glukozy we krwi
po zastosowaniu adrenaliny lub hipokalemia po zastosowaniu furosemidu nie
ma żadnego związku z chorobą lecz jest wynikiem działania leków.
Interferencje toksyczne
Polegają na uszkodzeniu, indukowaniu apoptozy lub nekrozy komórek
organizmu przez substancje lub ich metabolity – prowadząc do podniesienia
poziomu analitów mierzonych np. hepatotoksyczność prowadząca do
podniesienia aktywności ALAT i ASAT. Ponadto wiązanie się metabolitów z
białkami może prowadzić do powstania nieswoistych, heterofilnych przeciwciał
i w konsekwencji chorób z autoagresji.
2. Wpływ leków na badania biochemiczne
2.1 Glukoza w surowicy i moczu
Wpływ leków na stężenie glukozy we krwi może być spowodowane wpływem
na metodę oznaczenia lub zmianami metabolizmu i wydalania glukozy
spowodowanymi fizjologicznym lub farmakologicznym działaniem leków. Na
heksokinazową (najbardziej czułą) metodę oznaczania stężenia glukozy we krwi
leki na ogół nie wywierają wpływu, natomiast na metodę z oksydazą i
peroksydazą może mieć wpływ wysokie stężenie wysokie stężenie kwasu
askorbinowego (powodując obniżenie stężenia)
Tabela 1 - Leki i substancje mające wpływ na stężenie glukozy we krwi i moczu
Leki zwiększające stężenie (odsetek
zmiany)
Leki zmniejszające stężenie (odsetek
zmiany)
adrenalina (30-94%)
akarboza (70%),
chlorpromazyna (48%)
salicylany (11-14%)
doustne śr. antykoncepcyjne (6%)
furosemid (15%)
deksametazon (52%)
metformina ( kobiety w ciąży – 29%)
tiazydowe śr. moczopędne (10-45%)
steroidy anaboliczne (9%)
indometacyna (29%)
paracetamol (24 – 72%)

5
izofluran (14%)
izoprenalina (10%)
loperamid (20%)
metoprolol (13%)
fenytoina, kortykosteroidy, salbutamol
(2 - 38%)
Oznaczanie glukozy w moczu -
metoda enzymatyczna oraz testy paskowe
Leki zwiększające stężenie
Leki zmniejszające stężenie
Cafelosporyny, chloramfenikol, kwas
nikotynowy, penicylina
Diazepam, lewodopa, fenobarbital,
tetracykliny, glutation
2.2 Elektrolity
Wpływ na metodę oznaczania elektrolitów w organizmie wywiera niewiele
substancji leczniczych. Natomiast poważne zaburzenia równowagi wodno-
elektrolitowej wywołują leki poprzez farmakologiczne działanie, zwłaszcza na
czynność nerek.
Do substancji tych należą przede wszystkim różne grupy leków moczopędnych
powodujących utratę wody, sodu, potasu i chlorków z organizmu. Niektóre
hormony zmieniają zawartość elektrolitów i wody poprzez ich wpływ na
czynność nerek, są to przede wszystkim hormon entydiuretyczny (ADH) i
aldosteron (regulatory równowagi wodno-elektrolitowej). Stany patologiczne
związane z nadmiarem lub niedoborem niektórych hormonów jak kortyzol,
estrogen, progesteron, hormon wzrostu, androgeny mogą powodować
zaburzenia równowagi wodno-elektrolitowej jak zatrzymanie wody, sodu, utratę
potasu i jonów amonowych.

6
Tabela 2 Leki wpływające na zawartość sodu we krwi
Zwiększające stężenie sodu
Zmniejszające stężenie sodu
Zatrzymane sodu i wody w
organizmie: steroidy anaboliczne,
kortykosteroidy,
metyldopa, estrogeny, doustne środki
antykoncepcyjne
Działanie moczopędne: furosemid,
tiazydy, triamteren, mannitol,
mocznik, spironolaktoon
Wpływ na nerki: klonidyna ,
tetracykliny
Tabela 3 - Leki wpływające na zawartość potasu we krwi
Zwiększające stężenie potasu
Zmniejszające stężenie potasu
Leki uszkadzające nerki:
amfoterycyna B, niektóre
cefalosporyny, tetracykliny
Leki działające moczopędnie: tiazydy,
furosemid, acetozalamid
Leki zwiększające retencję potasu:
spironolakton, triamteren, amylorid
Zwiększenie wydalania nerkowego,
uszkodzenie nerek: kwas
aminosalicylowy, kortykosteroidy
Leki wpływające na zmniejszenia
aldosteronu: beta-blokery, inhibitory
konwertazy angiotensynowej, NLPZ
Inne mechanizmy: aldosteron,
testosteron, mocznik, glikozydy
nasercowe, chlorek amonu,
długotrwałe stosowanie śr.
przeczyszczających
Inne mechanizmy: izoniazyd
Tabela 4 - Leki mające wpływ na zawartość jonu chlorkowego we krwi
Zatrzymanie sodu i wody w
organizmie: androgeny,
kortykosteroidy, estrogeny,
metyldopa
Zmniejszające stężenie jonu
chlorkowego
Wpływ na powstawanie zasadowicy
metabolicznej: po długotrwałym
stosowaniu – tiazydy
Leki działające moczopędnie: tiazydy,
furosemid, triamteren
Leki zwiększające retencję potasu:
spironolakton, triamteren, amylorid
Przez zasadowicę: aldosteron,
kortykosteroidy, kortykotropina

7
2.3 Azot mocznika
Azot mocznika stanowi 45% niebiałkowych związków azotu w organizmie.
Mocznik jako produkt końcowy metabolizmu białek jest syntetyzowany w
wątrobie i wydalany przez nerki drogą filtracji kłębuszkowej: około 40%
mocznika wchłania się zwrotnie przez kanaliki poprzez dyfuzję bierną.
Oznaczanie stężenia azotu mocznika, nie jest swoistym, ani czułym testem
wydolności nerek i zmienia się w zależności od stanu nawodnienia organizmu
chorego i sposobu odżywiania się. Wzrost stężenia azotu mocznika ponad
normę poprzedzony jest zwykle znacznym zmniejszeniem klirensu kreatyniny.
Najistotniejszą przyczyną wpływu na wzrost stężenia azotu mocznika jest
nefrotoksyczność leków, a ponadto wpływ leków na metabolizm białek, poprzez
ten ostatni mechanizm działania zwiększają stężenie azotu mocznika steroidy
anaboliczne.
Tabela 5 - Leki zwiększające stężenie azotu mocznika i kreatyniny we krwi
Leki zwiększające stężenie azotu
mocznika (odsetek zmiany)
Leki zwiększające stężenie kreatyniny
(odsetek zmiany)
tiazydy (7-21%)
allopurinol (29%)
kotrymoksazol (60%)
kwas acetylosalicylowy (38%)
furosemid (27%)
kotrymoksazol (4027%)
propranolol (5-10%)
glukoza
acyklowir
tiazydy
kwas acetylosalicylowy
aminoglikozydy
amfeterycyna B
barbiturany (fenobarbital)
karbamazepina
androgeny
tetracykliny
aminoglikozydy
paracetamol
metamizol
2.4 Wapń
Prawidłowe stężenie wapnia całkowitego w organizmie wynosi 2.5 mmol/1,
46% wapnia występuje w postaci związanej z białkiem, pozostałe 54% w formie
wapna zjonizowanego.

8
Za pomocą metod analitycznych dokonuje się pomiaru stężenia wapnia
całkowitego. Następstwem zmian zawartości białka całkowitego w organizmie,
zwłaszcza albumin, jest zmiana stężenia wapnia całkowitego lecz nie jego
postaci zjonizowanej. Leki na ogół nie wpływają na obecnie najczęściej
używane czułe metody oznaczania stężenia wapnia w organizmie (np. atomowa
spektroskopia absorpcyjna).
Oprócz wpływu na metody oznaczania wapnia leki mogą zmieniać jego stężenie
w surowicy wpływając na równowagę wapniową poprzez zmianę:
a) wchłaniania wapnia w przewodzie pokarmowym,
b) resorpcji wapnia z kości,
c) wchłaniania zwrotnego w kanalikach nerkowych,
d) kontroli hormonalnej.
Tabela 6 - Leki wpływające na zawartość wapnia we krwi
Zwiększające stężenie wapnia
Zmniejszające stężenie wapnia
Wpływ na wchłanianie z przewodu
pokarmowego: witamina D, sole
wapnia,
laktoza
Wpływ na wchłanianie z przewodu
pokarmowego: leki przeczyszczające,
fosforany, sole magnezu, siarczan
sodu, kortykosteroidy, związki
alkalizujące
Wpływ na resorpcję z kości: witamina
D, hormony tarczycy, tamoksyfen
Wpływ na resorpcję z kości:
kortykosteroidy, kalcytonina
Wpływ na resorpcję zwrotną w
kanalikach
nerkowych: furosemid, tiazydy,
hormony
przytarczyc
Wpływ na wchłanianie w kanalikach
nerkowych: kortykosteroidy, hormony
przytarczyc, acetozalamid, furosemid ,
glukoza
Antagonizm hormonalny:
kortykosteroidy, glukagon
Zahamowanie syntezy albumin:
estrogeny, doustne środki
antykoncepcyjne
Inne mechanizmy: leki
przeciwpadaczkowe
(fenytoina)

9
2.5 Żelazo w surowicy
Niewiele leków wpływa na metody oznaczania żelaza w surowicy krwi.
Wyjątek stanowi deferoksamina, lek chelatujący, stosowany w stanach
związanych z nadmiarem żelaza w organizmie. Zwiększona zawartość żelaza w
surowicy może być następstwem polekowej niedokrwistości hemolitycznej
spowodowanej stosowaniem metylodopy czy penicylin.
Zmniejszona zawartość żelaza w surowicy może być spowodowana
upośledzeniem jego wchłaniania z przewodu pokarmowego podczas stosowania
neomycyny czy cholestyraminy.
2.6 Czas protrombinowy
Wpływ leków na czas protrombinowy, poprzez ich farmakologiczne działanie,
może być spowodowany, (u osób, które nie zażywają leków hamujących
krzepnięcie krwi):
a) interakcją z witaminą K,
b) zakłóceniem syntezy białek i czynników krzepnięcia,
c) uszkodzeniem czynności wątroby,
d) zmniejszeniem zawartości i aktywności protrombiny w organizmie.
Natomiast u osób zażywających leki hamujące krzepnięcie - interakcjami z
pochodnymi kumaryny (np. acenokumarol).
2.7 Fosfataza zasadowa
Fostataza zasadowa (ALP) jest użytecznym wskaźnikiem cholestazy, podczas
której aktywność tego enzymu w surowicy wzrasta jako skutek przedostania się
go do krwi. Fosfataza alkaliczna jest również wskaźnikiem chorób kości
związanych ze zwiększoną aktywnością osteoblastów (choroba Pageta,
krzywica, osteomalacja, mięsak kościopochodny, przerzuty nowotworów do
kości). Niewiele leków wpływa na metodę oznaczenia fosfatazy zasadowej, ich
wpływ na metodę oznaczania polega na hamowaniu aktywności enzymu.
Jedyną i najważniejszą przyczyną zwiększenia aktywności fosfatazy zasadowej
jest farmakologiczne działanie leków, które mogą wywołać uszkodzenie
wątroby poprzez takie mechanizmy jak: hepatotoksyczność, martwica
hapatocytów, reakcje nadwrażliwości.

10
Tabela 7 – Leki zwiększające aktywność ALP
Amiodaron, steroidy anaboliczne, barbiturany, kwas acetylosalicylowy,
furosemid, klozapina, propranolol i inne beta-blokery, insuliny, izoniazyd,
ketokonazol, metyldopa, paracetamol, chinidyna, rifampicyna, tetracykliny,
androgeny, opioidy
2.8 Aminotransferazy
Lekami, które poprzez chemiczne interakcje mogą zmieniać aktywność
aminotranferaz (AST, ALT) wpływając na metodę oznaczania są: kwas
askorbowy, erytromycyna, hydralazyna, izoniazyd, izoprenalina, lewodopa,
metylodopa, paracetamol. Zwiększenie aktywności aminotransferaz może
wystąpić podczas stosowania leków wywołujących skurcz zwieracza Oddiego
(leki cholinergiczne i opioidy), oraz uszkodzenia tkanki mięśniowej
spowodowanego domięśniowymi wstrzyknięciami niektórych antybiotyków
(ampicylina, gentamycyna). W przypadku braku znalezienia innej przyczyny
najbardziej prawdopodobną przyczyną zwiększenia aktywności aminotransferaz
pod wpływem leków jest polekowe uszkodzenie wątroby, to znaczy, że
wszystkie leki, które mogą wywierać działanie hepatotoksyczne lub wywoływać
cholestazę mogą spowodować zwiększenie aktywności aminotransferaz.
Tabela 8 – Leki zmieniające aktywność aminotransferaz
Leki i substancje zwiększające aktywność AST we krwi (odsetek zmiany)
Allopurynol (20%), amiodaron (200-400%), steroidy anaboliczne, leki
przeciwpadaczkowe,
kwas acetuylosalicylowy, barbiturany (stosowane długotrwale), kaptopryl,
chlorpromazyna, cymetydyna, cisplatyna, klindamycyna, cyklosporyna,
wziewne środki
znieczulenia ogólnego, erytromycyna, fluorouracyl, sole złota (w zależności od
dawki),
heparyna, izoniazyd, ketamina, ketokonazol, merkaptopuryna, metyldopa,
narkotyczne leki
przeciwbólowe, nitrofurantoina, estrogeny, paracetamol, chinidyna, ranitydyna,
ryfampicyna, streptokinaza, salazosulfapirydyna, tamoksyfen,

11
Leki i substancje zwiększające aktywność ALT we krwi (odsetek zmiany)
Amiodaron (20%), leki przeciwpadaczkowe, salicylany, azatiopryna,
barbiturany, busulfan,
chloropromazyna, klindamycyna, wziewne środki znieczulenia ogólnego,
erytromycyna,
heparyna, ibuprofen, insulina, izofosfamid, izoniazyd, ketokonazol,
merkaptopuryna,
metotreksat, metyldopa, narkotyczne leki przeciwbólowe, estrogeny,
paracetamol
Leki zmniejszające aktywność ALT (odsetek zmiany)
Fenytoina, ranitydyna, ryfampicyna, streptokinaza, tamoksyfen, kwas
walproinowy,
warfaryna
2.9 Amylaza i lipaza
Amylaza i lipaza są enzymami układu pokarmowego wydzielanymi przez
trzustkę. Amylaza jest ponadto wydzielana przez gruczoły ślinowe. Aktywność
tych enzymów wzrasta w stanach chorobowych związanych z uszkodzeniem
anatomicznego obszaru trzustki.
Ich wartość diagnostyczna ma ogromne znaczenie w zapaleniu trzustki.
Cholecystokinina zawierająca amylazę i lipazę może wywołać fałszywy wzrost
aktywności obu enzymów w płynach biologicznych. Cytryniany i szczawiany
wiążą jony wapnia, co powoduje zmniejszenie aktywności amylazy. Leki
powodujące poprzez działanie farmakologiczne zwiększenie aktywności
amylazy i lipazy zazwyczaj uszkadzają trzustkę lub przewody trzustkowe i
żółciowe. Farmakologicznie indukowane zmniejszenie aktywności amylazy w
surowicy stwierdzono po podaniu glukozy, insuliny i kortyzonu .
Tabela 9 - Leki i substancje mające wpływ na aktywność amylazy i lipazy we
krwi
Leki i substancje zwiększające aktywność amylazy we krwi
Wywołanie ostrego zapalenia trzustki: azatiopryna, chlortalidon,
kortykosteroidy,
furosemid, hydrochlorotiazyd, merkaptopuryna,

12
Wywołanie skurczu zwieracza Oddiego: morfina, kodeina, fentanyl,
pentazocyna,
petydyna, leki cholinergiczne
Uszkodzenie wątroby: doustne środki antykoncepcyjne
Leki zwiększające aktywność liupazy we krwi
Wywołanie skurczu zwieracza Oddiego: morfina, kodeina, pentazocyna,
petydyna,
leki cholinergiczne
Uszkodzenie wątroby: indometacyna
2.10
Bilirubina
Większość leków lub innych substancji, wywierających wpływ na metody
oznaczania powoduje fałszywe zwiększenie stężenia bilirubiny w surowicy
poprzez udział w reakcjach diazowych. Często przeoczoną przyczyną
fałszywego zmniejszenia stężenia bilirubiny w surowicy bywa ekspozycja
próbek na światło, które rozkłada bilirubinę (odpowiednie przechowywanie
próbek). Tworzenie, transport i wydalanie bilirubiny może być zakłócone przez
wiele leków, zwłaszcza tych, które uszkadzają czynność wątroby. Leki mogą
wpływać na przemianę bilirubiny na różnych etapach, od hemoglobiny poprzez
jej wydalanie.
Niektóre leki zwiększają stężenie bilirubiny jako wynik ich działania
hepatotoksycznego i uniemożliwienia prawidłowego metabolizmu bilirubiny
przez hepatocyty. Leki wywołujące cholestazę uniemożliwiają wydalenie
bilirubiny. Salicylany i sulfonamidy wypierają bilirubinę z połączeń z
albuminami krwi. Nadmierny rozpad krwinek czerwonych, zwłaszcza w
przypadku hemolizy połączonej z odczynem nadwrażliwości, powoduje znaczne
przeciążenie, upośledzenie czynności hepatocytów, a w związku z tym
zwiększone stężenie bilirubiny w surowicy. Zmniejszenie stężenia bilirubiny w
surowicy powodują pochodne
kwasu barbiturowego, zwłaszcza fenobarbital, który indukuje aktywność
enzymów odpowiedzialnych za metabolizm bilirubiny.

13
Tabela 10 Leki i substancje mające wpływ na zmianę stężenia bilirubiny we
krwi.
Leki i substancje zwiększające stężenie bilirubiny we krwi (odsetek zmiany)
Leki działające
hepatotoksycznie
cytostatyki – metotreksat, merkaptopuryna, asparaginaza –
(do
100%), kwas aminobenzoesowy, amfoterycyna B, leki
przeciwpadaczkowe, barbiturany (40%), metyldopa,
nitrofurantoina, paracetamol (u dzieci), antybiotyki
aminoglikozydowe, kwas acetylosalicylowy, kaptopryl,
wziewne
środki znieczulenia ogólnego, kwas nikotynowy (200-300%),
ryfampicyna, spironolakton(121%), tetracykliny,
Leki wywołujące
cholestazę
steroidy anaboliczne, androgeny, karbamazepina,
chloramfenikol, chlorpropamid, chlorprotiksen, dienestrol,
erytromycyna, tiazydy, indometacyna, izoniazyd (u 1%
chorych – 300%), linkosamidy, metamizol, testosteron,
metyltestosteron, tiouracyl, metyltiouracyl,
nitrofurantoina, estrogeny, doustne środki antykoncepcyjne,
pochodne fenotiazyny, propoksyfen, sulfonamidy,
tetracykliny,
Leki wywołujące
hemolizę i
niedokrwistość
hemolityczną
busulfan, melfalan, mefenytoina, cefalotyna, nitrofurany,
chinidyna, streptomycyna,
Leki wywołujące
hemolizę
spowodowaną
niedoborem
dehydrogenazy
glikozo-6-
fosforanu
furazolidon, błękit metylenowy, nitrofurazon, sulfacetamid,
sulfasalazyna, witamina K
2.11
Kwas moczowy
Wiele leków lub ich metabolitów wpływając na metodę oznaczania kwasu
moczowego może fałszywie zawyżać zawartość tego parametru w organizmie.

14
Zmiany te są na ogół niewielkie, jednakże znacznie bardziej istotne fałszywe
zwiększenie stężenia kwasu moczowego mogą wywołać lewodopa, metylodopa,
kwas askorbowy. Niektóre leki zmieniają zawartość kwasu moczowego w
organizmie poprzez działanie farmakologiczne na jego metabolizm i wydalanie.
Zwiększenie stężenia kwasu moczowego może wystąpić na skutek:
a) zmniejszenia jego wydalania przez nerki,
b) rozpadu komórek i zwiększania metabolitów kwasów
nukleinowych.
Wiele leków upośledza nerkowe wydalanie kwasu moczowego poprzez
zmniejszenie jego klirensu nerkowego, zmniejszenie wydalania kanalikowego,
upośledzenie czynności nerek.
Niektóre leki mogą wywoływać napady dny moczanowej (fenytoina, lewodopa).
Leki cytostatyczne działające toksycznie na komórki zwiększają stężenie kwasu
moczowego w organizmie poprzez zwiększenie metabolizmu kwasów
nukleinowych. Stężenie kwasu moczowego, poprzez zahamowanie syntezy
moczanów i działanie urykozuryczne, zmniejszają leki stosowane w leczeniu
dny moczanowej, zwłaszcza allopurynol.
Tabela 11 Leki mające wpływ na zmiany stężenia kwasu moczowego we krwi
Leki zwiększające stężenie kwasu moczowego we krwi (odsetek zmiany)
Acetazolamid (5%), leki beta-adrenolityczne (6-13%), kwas acetylosalicylowy
(17%),
diuretyki tiazydowe (20-50%), chlortalidon, cyklosporyna (10%), etambutol
(15-74%),
furosemid (9%), lewodopa, metyldopa (47%), kwas nikotynowy (20-28%),
Leki zmniejszające stężenie kwasu moczowego we krwi (odsetek zmiany)
Allopurynol (22%), kwas askorbinowy (31%), leki beta-adrenolityczne (6-
23%),
karbamazepina (22%), kortyzon (41%), ibuprofen (28%), insulina (61%),
fenytoina
(17%), piroksykam (16%),

15
2.12
Cholesterol i trój glicerydy
Wiele dróg metabolicznych lipidów i lipoprotein dotąd jeszcze nie jest znanych.
Ponieważ wątroba jest najważniejszym narządem odpowiedzialnym za syntezę,
magazynowanie i metabolizm cholesterolu, jest zrozumiałe, że leki które
działają hepatotoksycznie lub wywołują żółtaczkę cholestatyczną mogą
zmieniać zawartość lipidów w organizmie.
Tabela 12 - Leki i substancje mające wpływ na zmiany stężenia cholesterolu we
krwi
Leki i substancje zwiększające stężenie cholesterolu we krwi (odsetek zmiany)
Cholesterol całkowity:
kwas acetylosalicylowy (38%), beklometazon (11%), karbamazepina (11%),
chlortalidon
(5%), cyklosporyna (23%), diazepam (12%), tiazydy (7%), lewodopa (10%),
estrogeny
(20%), doustne środki antykoncepcyjne (13-14%), fenytoina (10-17%),
kortykosteroidy
(17-51%), werapamil (10%)
Leki zmniejszające stężenie cholesterolu we krwi (odsetek zmiany)
Cholesterol całkowity:
kwas askorbinowy (8-14%), heparyna (22%), izoniazyd (duże dawki – 28%),
metronidazol (14%), estrogeny (kobiety po menopauzie – 9%), beta-
adrenolityki,
chlorpromazyna

16
Tabela 13 - Leki i substancje mające wpływ na zmiany stężenia triglicerydów
we krwi
Leki i substancje zwiększające stężenie triglicerydów we krwi
(odsetek zmiany)
Salicylany (19%), chlortalidon (10%), doustne środki antykoncepcyjne (12-
48%),
cyklosporyna A (64%), tiazydy (26%), metyldopa (27%), metoprolol (10%),
estrogeny
(14%), fenytoina (26-43%), kortykosteroidy (19-100%)
Leki zmniejszające stężenie triglicerydów we krwi
(odsetek zmiany)
Azatiopryna (39%), heparyna (34-38%), fenobarbital (34%), kwas walproinowy
(36%)
2.13
Białko całkowite, Elektroforeza białek, białka specyficzne w
surowicy
Tabela 14 – Leki mające wpływ na frakcje białkowe
Leki i substancje zwiększające stężenie frakcji białkowych we krwi
(odsetek zmiany)
Albumina:galamina, alkuronium, felodypina (5%), tiazydy (7%)
alfa1-globulina: doustne środki antykoncepcyjne
alfa2-globulina: steroidy anaboliczne, doustne środki antykoncepcyjnew,
fenytoina
grammaglobulina: leki przeciwpadaczkowe, asparaginaza, hydralazyna,
progesteron
Leki i substancje zmniejszające stężenie frakcji białkowych we krwi
(odsetek zmiany)
Albumina: ibuprofen (20%0, metyldopa (37%), nitrofurantoina, estrogeny (7-
16%),
doustne środki antykoncepcyjne (9-22%), fenytoina (9-30%), spironolakton
(11%), kwas
walproinowy, asparaginaza, azatiopryna, cyklofosfamid, halotan, niacyna,
paracetamol,
pirazynamid
17
alfa2-globulina: asparaginaza
grammagflobulina: metotreksat
Tabela 15 – Leki mające wpływ na białka specyficzne
Białko
Wzrost zawartości
Spadek Zawartości
α1 - antytrypsyna
Estrogeny, doustne
środki antykoncepcyjne,
oksymetolon
Orozomukoid
Oksymetolon
Etynyloestradiol,
norestriogen, estrogeny,
doustne środki
antykoncepcyjne
α2 - makroglobulina
Mestranol, estrogeny,
doustne środki
antykoncepcyjne,
Dekstran, streptokinaza
Haptoglobulina
Steroidy anaboliczne,
testosteron,
metylotestosteron,
oksymetolon
Kwas acetylosalicylowy,
chloropromazyna,
difenylohydramina,
indometacyna,
nitrofurantoina,
streptomycyna,
sulfonamidy.
IgG
Asparaginaza, opioidy
Dekstran, fenytoina
IgA
Asparaginaza
Etanol,
metyloprednizolon,
doustne środki
antykoncepcyjne,
fenytoina
IgM
Asparaginaza, opioidy
Azatriopryna, dekstran,
metyloprednizolon.
3. Wpływ leków na terapię monitorowaną leków.
Terapeutyczne monitorowanie leków (TDM) można zdefiniować jako
monitorowanie stężenia leków we krwi i innych płynach ustrojowych w celu
stworzenia i realizacji skutecznych oraz bezpiecznych schematów
farmakoterapii u poszczególnych chorych.

18
W trakcie prowadzenia terapii należy pamiętać, że inne leki mogą dawać
interakcje w fazie farmakokinetycznej (jeden lek wpływa na wchłanianie,
dystrybucję lub eliminację drugiego). Powoduje to konieczność modyfikacji
dawkowania oraz prowadzenie terapii monitorowanej. Do najważniejszych
interakcji zachodzi w trakcie dystrybucji – niektóre substancje mają zdolność
zwiększania stężenia we krwi białek wiążących leki, co może prowadzić do
wzrostu stężenia poziomu analitów związany z tymi białkami. Np. doustne
środki antykoncepcyjne zwiększają stężenie globuliny wiążącej tyroksynę
(wzrost stężenia tyroksyny), ceruloplazminy (wzrost stężenia miedzi),
transferyny (wzrost stężenia żelaza), transkortyny (wzrost stężenia kortyzolu).
Na wiązanie leków z białkami może wpływać również obecność innego leku
konkurującego o to samo miejsce wiązania na białku lub zwiększony poziom
kwasów tłuszczowych (leki, które wiążą się słabo są wypierane z połączenia
przez inne leki i kwasy tłuszczowe). W tych warunkach może wystąpić
podwyższenie stężenia wolnego leku w surowicy krwi. Ponadto, jeśli uwolniony
z połączenia lek nie jest szybko metabolizowany przez organizm, jego poziom
może osiągnąć stężenie toksyczne przy normalnej dawce terapeutycznej.
Niski poziom albumin spotykany u pacjentów z chorobami wątroby i nerek
również wpływa na wiązanie leków. W takich przypadkach, gdy pacjentowi
podaje się wiele preparatów, konkurencja o miejsce wiązania się z albuminami
jest znacząca. Na przykład kwas walproinowy stosowany razem z fenytoiną
wypiera ją z połączeń z albuminą i doprowadza do obniżonego stężenia
całkowitego fenytoiny we krwi (z powodu jej szybkiego metabolizmu do postaci
nieaktywnej). Stopień wiązania leku przez białka może być dramatycznie
zmieniony w stanach patologicznych jak np. mocznica (kiedy wiązanie
fenytoiny może zmieniać się w zakresie od 70% do blisko 0%).
Tabela 16 – Interakcje pomiędzy lekami w TMD
Digoksyna – glikozyd nasercowy stosowany u chorych z niewydolnością serca
oraz w niektórych postaciach zaburzeń rytmu.
↑ stężenia digoksyny we
krwi
Amiodaron, chinidyna, diklofenak, diltiazem,
ibuprofen, werapamil
↓ stężenia digoksyny we
krwi
Alkalia, cholestyramina, metoklopramid,
neomycyna, sulfasalazyna, węgiel aktywowany
Teofilina – stosowany jako lek rozkurczający oskrzela we wszystkich
postaciach astmy oskrzelowej, oraz ze względu na jej działanie pobudzające
19
ośrodek oddechowy (np. bezdech noworodków). Objawy zatrucia: nudności,
wymioty, biegunka, bezsenność, tachykardii, a w dużych dawkach drgawki,
zaburzenia rytmu serca i zatrzymanie krążenia
↑ stężenia teofiliny we
krwi
Alkalia, allopurinol, antybiotyki makrolidowe,
cymetydyna, doustne środki antykoncepcyjne,
kortykosteroidy.
↓ stężenia teofiliny we
krwi
Barbiturany, fenytoina, ryfampicyna,
karbamazepina
Karbamazepina – lek przeciwpadaczkowy stosowany w napadach częściowych,
głównie pochodzenia skroniowego, oraz napadach uogólnionych toniczno –
klonicznych. Ponadto używana w neuralgiach, w neuropatii cukrzycowej oraz
w psychiatryce. Objawy uboczne stosowania zależne SA od dawki i obejmują:
podwójne widzenie, nieostre widzenie, senność, oczopląs, ataksję, bóle i
zawroty głowy, nudności i wymioty
↑ stężenia karbamazepiny
we krwi
Cymetydyna, diltiazem, erytromycyna,
imipramina, izoniazyd, propoksyfenon, ranitydyna,
werapamil
↓ stężenia karbamazepiny
we krwi
Fenobarbital, fenytoina, prymidon
Fenytoina – lek przeciwpadaczkowy stosowany w leczeniu chorych z napadami
padaczki psychomotorycznej. Efekty uboczne zależne od dawki i mogą
manifestować się zmianami zachowania, zaburzeniami widzenia, sennością,
śpiączką i zwiększeniem liczby napadów padaczkowych
↑ stężenia fenytoiny we
krwi
Chloramfenikol, cymetydyna, disulfiram,
fenylobutazon, izoniazyd, pochodne kumaryny,
propoksyfen, sulfonamidy
↑ stężenia frakcji wolnej
fenytoiny we krwi
Fenylobutazon, kwas walproinowy, salicylany,
pochodne sulfonylomocznika
↓ stężenia fenytoiny we
krwi
Etanol, fenobarbital, karbamazepina
Kwas walproinowy (VPA) – lek przeciwpadaczkowy stosowany we wszystkich
postaciach tej choroby u dzieci i dorosłych. Objawy uboczne: wypadanie
włosów, nudności, wymioty, trombocytopenia, wzrost markerów uszkodzenia
wątroby, zapalenie wątroby.
↑ stężenia kwasu
walproinowego we krwi
Salicylany
20
↓ stężenia kwasu
walproinowego we krwi
Etosuksymid, fenobarbital, fenytoina,
karbamazepina, prymidon
Fenobarbital i prymidon – fenobarbital (luminal) jest najstarszym lekiem
przeciwpadaczkowym nadal stosowanym w monoterapii lub w połączeniu z
innymi lekami przeciwdrgawkowymi. Prymidon w organizmie rozpada się na
czynne metabolity – fenobarbital i amid kwasy fenylomalonowego (PEMA).
Jego skuteczność jest więc zbliżona do fenobarbital. Oba leki są stosowane w
napadach częściowych i uogólnionych kloniczno – tonicznych, fenobarbital
może ponadto przerwać stan padaczkowy, jest skuteczny w drgawkach
gorączkowych, a w zależności od dawki działa też uspokajająco i nasennie.
Objawy uboczne zalezą od dawki. Należą do nich: znużenie, senność, apatia,
pobudzenie, depresja, osłabienie, bezsenność, niedobór kwasu foliowego
(niedokrwistość megaloblastyczna), niedobór Wit. D (osteomalacja),
hipokaliemia.
↑ stężenia fenobarbitalu
we krwi
Chloramfenikol, cymetydyna, fenytoina,
klonazepam, kwas walproinowy
↓ stężenia fenobarbitalu
we krwi
Etanol (stosowany przewlekle)
↑ stężenia prymidonu we
krwi
Izoniazyd, klonazepam, kwas walproinowy
↓ stężenia prymidonu we
krwi
Fenytoina, karbamazepina
Antybiotyki aminoglikozydowe – AAm (gentamycyna, netylmycyna,
tobramycyna, amikacyna) – działają bakteriobójczo hamując syntezę białek
bakteryjnych i uszkadzając błony komórkowe bakterii. Wykazują niestety
działanie nefro i ototoksyczne.
↑ stężenia AAm we krwi Amfoteryczna, cefalosporyny, furosemid,
klindamycyna, kwas etakrynowy, wankomycyna
↓ stężenia AAm we krwi Heparyna, teofilina, penicyliny naturalne
Cyklosporyna A (CsA) – lek immunosupresyjny, stosowany w zapobieganiu
odrzuceniu narządu po przeszczepie, w leczeniu chorób
autoimmunologicznych. Objawy uboczne: nudności, wymioty, brak łaknienia,
pogorszenie czynności nerek, zaburzenia czynności wątroby, drżenie
mięśniowe.
↑ stężenia CsA we krwi
Danazol, diltiazem, doustne środki
antykoncepcyjne, erytromycyna, flukonazol,
21
werapamil, ketokonazol, metyloprednizolon.
↓ stężenia CsA we krwi
Fenobarbital, fenytoina, izoniazyd, karbamazepina,
ryfampicyna, sulfonamidy
Takrolimus (FK 506) – związek makrolidowy wywierający działanie
immunosupresyjne poprzez zmniejszanie syntezy IL-2 i innych cytokin w limf.
T, czego efektem jest zahamowanie ich aktywacji. Jest stosowany u biorców
przeszczepu. Efekty uboczne obejmują: działanie neurotoksyczne,
niedokrwistości. Objawy uboczne: wykazuje działanie neurotoksyczne (bóle
głowy, drgawki, parestezje), niedokrwistość, zaburzenia czynności przewodu
pokarmowego.
↑ stężenia takrolimusu we
krwi
Diltiazem, werapamil, ketokonazol, flukonazol,
erytromycyna, wankomycyna, metoklopramid,
omeprazol, metyloprednizolon, ritonawir,
indinawir.
↓ stężenia takrolimusu we
krwi
Karbamazepina, fenobarbital, fenytoina,
ryfampicyna.
Kwas mykofenolowy – mykofenolan mofetylu (MMF) jest pro lekiem
przekształcanym w wątrobie do kwasu mykofenolowego (MPA), który
zakłócając syntezę puryn i hamując proliferację limf. B i T działa
immunosupresyjnie. Jest stosowany u biorców przeszczepów oraz w leczeniu
niektórych chorób autoimmunologicznych. Do ubocznych działań należą:
nudności, wymioty, biegunka, leukopenia, zakażenia, niedokrwistości,
zapalenia przełyku, krwawienia z górnego odcinak przewodu pokarmowego.
↑ stężenia MPA we krwi
Acyklowir
↓ stężenia MPA we krwi
Leki alkalizujące, cyklosporyna A, ryfampicyna,
metoprednizol.
Lit – stosowany w leczeniu i profilaktyce schorzeń afektywnych (zwłaszcza
depresji), innym obszarem jego wykorzystywania jest hematologia, kiedy
podawany jest w celu pobudzenia leukopoezy. Zatrucia litem charakteryzują się
apatią, osłabieniem, drżeniem mięśniowym i drgawkami, zaburzeniami rytmu
sera, ostrą niewydolnością nerek. U niektórych powoduje objawy moczówki
prostej i zaburzenia czynności tarczycy.
↑ stężenia litu we krwi
Acetazolamid, spironolakton, teofilina,
wodorowęglan sodu.
↓ stężenia litu we krwi
Diklofenak, indometacyna, hydrochlorotiazyd.
Metotreksat (MTX) – jest antymetabolitem kwasu foliowego, zmniejsza
22
syntezę kwasów nukleinowych. Lek stosowany w leczeniu nowotworów –
ostrych białaczek, raka płuc, sutka, jajnika. Bywa także stosowany w leczeniu
RZS, kolagenoz, łuszczycy. Działania uboczne: nudności, wymioty, biegunka,
zapalenia, nadżerki, upośledzenie czynności krwiotwórczej szpiku,
niewydolność nerek, zapalenie/marskość wątroby.
↑ stężenia MTX we krwi Antybiotyki aminoglikozydowe, cefalotyna,
cisplatyna, penicylina, salicylany, sulfonamidy
↓ stężenia MTX we krwi Neomycyna, gryzeofulwina.
4. Narkotyki
Narkotyki i substancje psychoaktywne jako substancje o wysokim potencjale
farmakologicznym również mają wpływ na uzyskiwane wyniki badań
laboratoryjnych.
Tabela 17 – Wpływ narkotyków na wybrane parametry
Narkotyk
Wzrost w surowicy
Spadek w surowicy
Amfetamina
Wolne kwasy tłuszczowe
Morfina
α-amylaza, lipaza, AST,
ALT, bilirubina, ALP,
gastryna, TSH,
prolaktyna
Insulina, noradrenalina
neurotensyna, polipeptyd
trzustkowy
Heroina
pCO
2
, tyroksyna,
cholesterol, potas (na
skutek rabdomiolizy)
pO
2
, albumina
Marihuana
Sód, potas, mocznik,
chlorki, insulina
Kreatynina, glukoza,
kwas moczowy
4.1 Wykrywanie narkotyków za pomocą szybkich testów
Zwiększone zapotrzebowanie na oznaczanie narkotyków w laboratoriach
medycznych jest spowodowane rosnącą liczbą ostrych zatruć tymi substancjami,
a także aktywną działalnością jednostek prowadzących programy substytucyjne
dla osób uzależnionych od narkotyków. Jednym z warunków uczestnictwa w
terapii substytucyjnej jest okresowa kontrola moczu pacjentów pod kątem
obecności substancji psychoaktywnych. Ponadto w ostatnich latach, wzorem

23
krajów zachodnich, pojawiło się zainteresowanie oznaczaniem narkotyków
wśród pracowników, sportowców czy uczniów. Przez szereg lat oznaczenia
substancji psychoaktywnych były domeną specjalistycznych laboratoriów
toksykologicznych. W chwili obecnej badania narkotyków wykonywane są w
wielu laboratoriach medycznych o profilu ogólnym. Niewątpliwie zachętą dla
tych placówek jest szeroka oferta dostępnych na rynku narkotestów – szybkich,
tanich i prostych w wykonaniu. Współczesne kasetowe testy immunochemiczne
są znacznie doskonalsze niż ich poprzednicy, jednak producentom wciąż nie
udało się wyeliminować ich niskiej specyficzności. Dlatego oznaczenia
wykonywane przy ich pomocy mają charakter badań przesiewowych,
a wyniki wątpliwe powinny być weryfikowane w laboratoriach
toksykologicznych dysponujących metodami referencyjnymi. Diagnosta
laboratoryjny podejmujący się oznaczeń narkotyków za pomocą szybkich testów
powinien posiadać specjalistyczną wiedzę z zakresu toksykologii i zdawać sobie
sprawę z wagi wyniku. Oznaczane szybkimi testami narkotyki i leki to silnie
działające substancje, które mogą być przyczyną ciężkich zatruć i uzależnień.
Niektóre z nich wykorzystywane są w celu ułatwiania przestępstw na tle
seksualnym i rabunkowym, co pociąga za sobą zaangażowanie policji i sądu.
Analityk powinien wiedzieć, że grupowy charakter oznaczeń nie pozwala na
odróżnienie badanego analitu od substancji pochodnych, posiadających zbliżoną
budowę, które mogą wchodzić w skład popularnych leków czy suplementów.
Wszystko to sprawia, że interpretacja wyniku może przysparzać wielu
problemów, a raportowanie wyników pozytywnych, bez uwzględnienia
wywiadu lekarskiego, stanu pacjenta, a w uzasadnionych przypadkach
wykonania badań potwierdzających może prowadzić do błędów
terapeutycznych i mieć konsekwencje medyczno prawne. Należy zwrócić na te
aspekty szczególną uwagę i do wyniku dołączać stosowny komentarz
informujący, że wynik służy jedynie dla celów diagnostyki medycznej.
Dostępne na rynku narkotesty obejmują swoim zakresem podstawowe,
klasyczne narkotyki oraz niektóre leki. Należą do nich: amfetamina, kokaina,
metamfetamina, ekstazy (MDMA), morfina, opiaty, tetrahydrokanabinole
(THC), metadon, fencyklidyna (mało popularna na polskim rynku
narkotykowym), barbiturany, benzodiazepiny i trójcykliczne leki
przeciwdepresyjne. Oczywiście nie są to wszystkie możliwe substancje
psychoaktywne, jakie znajdują się na rynku narkotykowym. W nielegalnych
laboratoriach ciągle powstają nowe specyfiki, wiele z nich pojawia się lokalnie
bądź sezonowo i znika wraz ze zmieniającymi się modami. Ostatnio dużą

24
popularność wśród młodzieży zyskały tzw. dopalacze (mefedron, pochodne
benzylopiperazyny, syntetyczne kanabinoidy i inne). Wciąż aktualny i żywo
dyskutowany jest temat tzw. pigułek gwałtu (GHB, flunitrazepam i inne).
Oznacza to, że dostępny panel oznaczeń narkotestów obejmuje jedynie część
stosowanych substancji psychoaktywnych, a ujemny wynik nie oznacza, że
pacjent nie jest pod wpływem innego środka (syntetycznego lub naturalnego).
W takich wypadkach należy liczyć się z rozbieżnością pomiędzy stanem
klinicznym pacjenta, u którego obserwuje się objawy działania narkotyku, a
ujemnymi wynikami oznaczeń.
4.2 Wpływ fazy przedanalitycznej (pobieranie, przygotowanie,
przechowywanie i transport materiału) na wyniki oznaczeń narkotyków
Mocz w ilości ok. 30 ml powinien być pobrany do szczelnego, nietłukącego się i
dokładnie opisanego pojemnika i wraz ze skierowaniem przesłany do
laboratorium. W razie potrzeby materiał może być przechowywany w
temperaturze 4-8°C przez 48 h, lub zamrożony w temp. -20°C przez 3 miesiące.
Rycina 1 – okna detekcji substancji psychoaktywnych

25
4.3 Fałszowanie materiału badanego
Osoby uzależnione od narkotyków oraz kontrolowane w kierunku abstynencji
narkotykowej mogą stosować różne sposoby, mające na celu zafałszowanie
wyniku analizy toksykologicznej. Stosowane są różne praktyki: rozcieńczenie
moczu, dodatek obcych substancji czy podmiana próbki. Najpopularniejszą z
nich jest rozcieńczenie przez dodatek wody lub innych płynów do próbki
moczu. Rozcieńczenie może być też wynikiem zwiększonej podaży
płynów lub zażyciem diuretyków na kilka godzin przed planowanym badaniem.
Wywołanie zwiększonej diurezy ma na celu przyśpieszenie eliminacji narkotyku
i zmianę ostatecznego wyniku analizy. Ten wpływ nie jest jednak jednakowy
dla wszystkich substancji. Związki lipofilne o dużych objętościach dystrybucji
nie reagują na rosnącą diurezę tak „chętnie” jak substancje hydrofilne. Dlatego
w przypadku wysoce lipofilnych tetrahydrokanabinoli spadek ich stężenia
w moczu w momencie badania może być niewystarczający dla uzyskania
wyniku negatywnego. Rozcieńczenie moczu można rozpoznać wizualnie
(wodojasne zabarwienie próbki) i może być ocenione przez oznaczenie ciężaru
właściwego lub stężenia kreatyniny. Czasami ten sposób fałszowania próby
może być maskowany dostępnymi w internecie specyfikami zawierającymi m.
in. witaminy z grupy B i kreatynę – prekursor kreatyniny, które mają imitować
prawidłową barwę i normować zawartość fizjologicznych składników moczu.
Innym sposobem fałszowania wyniku oznaczenia jest dodatek do próbki moczu
obcych substancji niszczących strukturę badanych związków. W tym celu często
wykorzystywane są azotany, które utleniają tetrahydrokanabinole oraz opiaty.
Azotany pozostają natomiast bez wpływu na stężenia kokainy, pochodnych
amfetaminy czy fencyklidyny. Z kolei dodatek preparatów „łazienkowych” –
specyfików do czyszczenia urządzeń sanitarnych, mydeł w płynie itp. sprawia,
że mocz podejrzanie się pieni, ma odmienny zapach i odczyn pH. Wymienione
praktyki mogą doprowadzić do spadku stężeń badanych substancji poniżej
czułości testu, zwłaszcza, gdy wyjściowe stężenie analitu było niskie.

26
Rycina 2 – Sposoby manipulacji i rozpoznanie fałszowania moczu
4.4 Zasada działania i wykonanie szybkich testów
Szybkie testy narkotykowe to jednostopniowe testy immunochromatograficzne,
jedno- lub wieloskładnikowe, bazujące na wysoko specyficznych reakcjach
zachodzących pomiędzy antygenami i przeciwciałami. Ich istotą jest
współzawodnictwo narkotyku oraz jego postaci skoniugowanej o miejsca
wiązania na ograniczonej liczbie przeciwciał, osadzonych na membranie.
Oznaczenie polega na naniesieniu próbki moczu do specjalnego portu w kasetce
i obserwacji barwnych linii w okienku wyniku. Jeśli w badanej próbce znajduje
się narkotyk w stężeniu większym od wartości odcięcia (cut-off), dochodzi do
wysycenia przeciwciał oraz zahamowania reakcji z testowym koniugatem
narkotyk-barwnik. W efekcie na membranie w odpowiedniej dla danego
związku pozycji nie pojawia się barwna linia. Jeśli próbka nie zawiera
narkotyku, z przeciwciałami wiąże się testowy koniugat, o czym świadczy
barwna linia powstająca obok linii kontrolnej. Linia kontrolna musi być
wyraźnie widoczna w okienku każdej kasetki, spełnia ona bowiem rolę kontroli
wewnętrznej, sprawdzającej prawidłowe przeprowadzenie procedury. Szybkie
testy mają charakter przesiewowy i z pewnymi zastrzeżeniami, pozwalają na
odróżnienie próbek pozytywnych, zawierających narkotyk od negatywnych.
Wartość odcięcia to stężenie ksenobiotyku, powyżej którego wynik oznaczenia
interpretowany jest jako pozytywny. Wartość odcięcia jest zawsze wyższa od
granicy wykrywalności

27
metody. Producenci mogą oferować testy o różnych poziomach odcięcia dla tej
samej substancji. Od naszych potrzeb zależy, na których zdecydujemy się
pracować.
4.5 Interpretacja wyniku
Prosty sposób wykonania narkotestów nie przekłada się na prostą interpretację
uzyskanych dzięki nim rezultatów. Przyczyną jest ograniczona swoistość metod
immunologicznych, na których opierają się testy. Może to prowadzić do
generowania wyników fałszywych (zarówno dodatnich jak i ujemnych), co
rzutuje nie tylko na postępowanie lecznicze wobec pacjenta, ale też, zwłaszcza
w przypadku wyników fałszywie dodatnich, może mieć dla niego konsekwencje
prawne. Dlatego we wszystkich próbach zakwalifikowanych przez szybkie testy
jako pozytywne, zaleca się wykonanie badań potwierdzających technikami o
wyższej swoistości (GC-MS, LC-MS). Wiarygodność wychodzącej
z laboratorium informacji zależy od rzetelności producenta testów, który w
dołączonej ulotce umieszcza szereg istotnych informacji, w tym listę substancji
przebadanych pod kątem reakcji krzyżowych. Oprócz związków, które służą
do wyznaczenia wartości odcięcia, znajdują się na niej niektóre produkty
biotransformacji ksenobiotyku, jego analogi, związki o zbliżonej do analitu
strukturze chemicznej oraz te o odmiennej budowie cząsteczki (mające
zastosowanie medyczne i niemedyczne). Analizując informacje producentów
nietrudno zauważyć, że wynik pozytywny generują nie tylko związki, którym
dedykowany jest test, ale też inne, nie należące do badanej grupy substancje
Kolejnym aspektem jest trafność doboru substancji „kalibrującej”. W przypadku
oznaczeń benzodiazepin najczęściejmjest nią oksazepam - metabolit wielu z
nich. Jednak biotransformacja niektórych pochodnych benzodiazepin (np.
bromazepam, lorazepam i in.) nie biegnie szlakiem oksazepamu. Ponadto
benzodiazepiny występują w moczu zazwyczaj w postaci sprzężonej z kwasem
glukuronowym, a takie połączenie jest słabo wykrywane przez testy.

28
Tabela 20 – substancje psychoaktywne wykrywane przez narkotesty
Narkotyk
Substancja/składnik powiązany
Amfetamina
D – amfetamina; 3,4 – Metylenodioksyamfetamina; D,L –
amfetamina; Fentermina, L - amfetamina
Barbiturany
Butabarbital, butethal, fenobarbital, alfenal, aprobarbital,
amobarbital, sekobarbital, pentobarbital, cyklopentanobarbital,
butalbital.
Benzodiazepiny Nitrezapam, klonazepam, temazepam, alprazolam, diazepam,
klorazepam, oksazepam, dezalkilflurazepam, flunitrazepam,
nordiazepam, klonazepam, bromazepam, lorazepam,
estazolam, tridazolam, midazolam.
Kokaina
Benzoiloekgonina, kokaina, kokainoetylen, ekgonina
Ectasy
3,4-Metylenodioksyetylenoamfetamina;
3,4-Metylenodioksymetamfetamina;
3,4-Metylenodioksyamfetamina
Metamfetamina D-Metamfetamina; 3,4-Metylenodioksymetamfetamina; L-
Metamfetamina; p-Hydroksymetamfetamina, Mefentermina
Morfina
Morfina, kodeina, morfino 3-β-D-glukuronid, leworfanol,
hydromorfon, etylenomorfina, nor kodeina, tebaina,
oksykodon, hydrokodon
Metadon
Metadon, doksylamina
Trójcykliczne
antydepresanty
Dezypramina, imipramina, nordoksepina, nortryptylina,
amitryptylina, promazyna, doksepina, maprotylina,
trimipralina, klomipramina, prometazyna.
Marihuana
Kanabinol, Δ
9
-THC, Δ
8
-THC, 11-nor- Δ
8
-THC-COOH,
11-nor- Δ
9
-THC-COOH
Należy zwrócić uwagę, że pola testowe narkotestów oprócz wyżej
wymienionych leków mogą dawać wynik dodatni z różnych środków
spożywczych, innych leków i suplementów diety:
Amfetamina, metamfetamina i ecstasy: Reagują tu związki o podobnej
budowie zarówno narkotyki (pochodne amfetaminy takie jak metamfetamina, p-
metoksyamfetamina, p-metoksymetamfetamina, MDMA czyli
metylenodioksymetamfetamina, itd jak i np. niektóre leki podobne budową do
amfetaminy np. pseudoefedryna, a także aminy gnilne np. beta-
fenyloetyloamina). Istnieje możliwość wykrycia w organizmie pochodnych
amfetaminy, pochodzących z różnorodnych legalnych źródeł. Do najczęstszych

29
należą środki zmniejszające przekrwienie śluzówek (pseudoefedryna,
fenylopropanoloamina), efedryna oraz tabletki odchudzające (fentermina), w
tym również niektóre preparaty pochodzące z Meksyku (Asenlix, Fenproporex).
Testy wykrywające narkotyki przeważnie umożliwiają różnicowanie pomiędzy
metamfetaminą i pochodnymi amfetaminy na podstawie orientacji cząsteczki
oraz stosunku metamfetaminy do amfetaminy. Dawka ecstasy, przyjęta ostatniej
nocy, nie zostanie mylnie uznana za lekarstwo przeciwko przeziębieniu. Jednak
meksykańskie tabletki odchudzające, zawierające metamfetaminę, mogą
spowodować dodatni wynik testu w kierunku ecstasy. Aerozol do nosa Vicks
również może być przyczyną dodatnich wyników testu wykrywającego ecstasy.
Vicks zawiera L-metamfetaminę, zaś ecstasy – D-metamfetaminę, substancję
nieomal identyczną, lecz dziesięciokrotnie silniejszą w działaniu.
Barbiturany: Grupa leków o małym zastosowaniu, w Polsce używa się
tiopentalu, fenobarbitalu, cyklobarbitalu i allobarbitalu. Wszystkie wykazują
reaktywność krzyżową w testach immunologicznych. Działają nasennie i
przeciwdrgawkowo. Tiopental stosuje się w lecznictwie zamkniętym -
premedykacja oraz w weterynarii.
Opioidy: W teście reaguje morfina i jej metabolity jakimi są glukuroniany
morfiny oraz kodeina i w różnym stopniu inne związki o podobnej budowie.
Sztandarowym przykładem wyniku fałszywie dodatniego jest spożycie porcji
maku (np. makowca) . Innym powodem jest przyjęcie leków
przeciwkaszlowych zawierających bromowodorek dekstrometorfanu, fosforan
kodeiny. Maksymalna dawka dobowa dekstrometorfanu wynosi 120 mg, a
kodeiny 300 mg. Spożycie większej ilości może wywołać objawy podobne do
objawów przedawkowania popularnych narkotyków oraz dawać fałszywie
dodatni wynik.
Kokaina
W testach stosuje sie przeciwciała przeciw głównemu metabolitowi kokainy
występującemu w moczu jakim jest benzoiloekgonina, inne metabolity kokainy i
sama kokaina też reagują z tym przeciwciałem. W laryngologii i okulistyce
stosuje się 1–20% roztwór chlorowodorku kokainy w celu znieczulenia
miejscowego ze względu na efekt sympatykomimetyczny, dzięki któremu
dochodzi do obkurczenia naczyń błony śluzowej zmniejszając przy tym

30
krwawienie, lub rozszerzenia źrenicy ułatwiającego prowadzenie wielu
zabiegów na oku. Mechanizm tego działania związany jest ze zmniejszeniem
przepuszczalności błony komórkowej w stosunku do jonów sodu, co hamuje
proces depolaryzacji, w efekcie czego tworzy się lokalny blok przewodzenia
impulsów nerwowych. Dawka jednorazowa nie może przekraczać 30 mg, a
dobowa – 60 mg. W Polsce nie znajduje się w urzędowym wykazie leków
dopuszczonych do obrotu.
THC – Tetrahydrocannabinol, marihuana
Związek psychoaktywny zwarty w konopiach i ich przrtworach czyli
marihuanie, haszyszu, oleju haszyszowym. testy zawierają przeciwciała nie dla
THC tylko dla jego głównego nieczynnego farmakologicznie metabolitu
występujacego w moczu , jakim jest kwas tetrahydrokannabinolowy (THC-
COOH). Z tego względu możliwe są fałszywie dodatnie wyniki u osób
spożywających olej konopny zawierający kannabidiol – główny składnik oleju
CBD, któremu przypisuje się: hamowanie rozrostu komórek rakowych,
łagodzenie stanów zapalnych, spowalnianie rozwoju bakterii. Innym
potencjalnym źródłem jest białko konopne i siemię konopne spożywane w
dużych ilościach jako suplementy diety.
Poniżej podano substancje, które wg producentów narkotestów nie mają wpływu
na wyniki badań (reakcje krzyżowe) do stężenia 100 µg/ml. Pozostawiają sobie
jednak furkę zabezpieczającą, że jeśli pacjent przyjął koktajl kilku leków lub
narkotyków, nie można wykluczyć, że wyniki zostaną zafałszowane na skutek
nieodtwarzanej reakcji krzyżowej i zalecają wykonanie testu potwierdzającego
metodą chromatografii.
Tabela 21 – Składniki nie reagujące krzyżowo
Acetofenon
Deoksykortykostero
n
Meprobamat
Tetracyklina
N-
acetyloprocainami
d
Dekstrometorfan
Metoksyframin
a
Tetrahydrokortyzo
n
Kwas
acetylosalicylowy
Diklofenak
Kwas
nalidyksowy
Tiamina
31
Aminopiryna
Diflunisal
Naproksen
Tyrozyna
Amoksycylina
Digoksyna
Amid niacyny
Tolbutamid
Ampicylina
Difenylohydramina
Nifedypina
Trimetoprin
Kwas L-
askorbinowy
Etylo – p -
aminobenzoesan
Norethindron
Tryptofan
Apomorfina
Estradiol
Noskapina
Kwas moczowy
Aspartam
Tiosiarczan estronu
Oktopamina
Werapamil
Atropina
Erytromycyna
Kwas
szczawiowy
Zomepirak
Kwas benzylowy
Fenoprofen
Kwas
oksolinowy
Kwas benzoesowy Furosemid
Oksymetazolin
a
Bilirubina
Kwas gentyzynowy
Papaweryna
D,L –
Bromfeniramina
Hemoglobina
Penicylina G
Kofeina
Hydralazyna
Perfenazyna
Wodzian chloralu
Hydrochlorotiazyd
Fenelazyna
Chloramfenikol
Hydrokortykosteron Prednizolon
Chlorotiazyd
Kwas hipurowy
Propranolol
D, L –
Chlorfeniramina
Dopamina
Chinidyna
Choloesterol
Isoxupryna
Chinina
Klonidyna
Ketamina
Kwas
salicylowy
Kortyzon
Ketoprofen
Serotonina
Kotynina
Labetolol
Sulfametazyna
Kreatynina
Loperamid
Sulindak
4.6 Interpretacja prawna
Substancje oznaczane narkotestami wymienione są w Ustawie o
przeciwdziałaniu narkomanii oraz Ustawie o ruchu drogowym. Diagnosta musi
zdawać sobie sprawę, że wynik potwierdzający obecność którejś z objętych
kontrolą prawną substancji może mieć dla pacjenta konsekwencje prawne (na
przykład w sytuacji, gdy pacjent brał udział w wypadku drogowym lub innym

32
zdarzeniu). Pomimo tego, że oznaczenie zostało wykonane jedynie dla celów
medycznych, należy się liczyć z możliwością powołania diagnosty do sądu, w
celu określenia wiarygodności wyniku. Dlatego ważną sprawą jest określenie
procedur prowadzenia kontroli oraz sposób raportowania wyników oznaczeń
narkotestów.
4.7 Sposób raportowania wyniku
Oznaczenie substancji w moczu szybkim testem kasetowym daje dwie
możliwości wyniku: pozytywny lub negatywny. Może się jednak zdarzyć, że
obiektywna ocena testu jest trudna. W takim wypadku najczęściej wykonywane
jest ponowne oznaczenie z użyciem kolejnej kasetki, co zwykle daje taki sam
trudny do interpretacji wynik. Diagnosta powinien wówczas zinterpretować
wynik oznaczenia jako wątpliwy lub niejednoznaczny, to znaczy do
potwierdzenia metodą referencyjną. W uzasadnionych przypadkach wykonanie
badań potwierdzających zalecane jest też dla wyników pozytywnych
i negatywnych. Praktycznie nie zawsze badania potwierdzające są wykonywane,
gdyż wiąże się to z dodatkowymi kosztami, koniecznością wysłania materiału
do laboratorium toksykologicznego i wydłużeniem czasu oczekiwania
na wynik. Należy wówczas zadbać o to, żeby wynik został odpowiednio
skomentowany. Biorąc pod uwagę ograniczenia szybkich testów
immunologicznych wskazane jest podanie pod wynikiem informacji o rodzaju
zastosowanego testu (nazwa handlowa, producent), czułości testu (cut-off)
i możliwych interferencjach. Dodatkowy komentarz powinien dotyczyć okna
czasowego charakterystycznego dla oznaczanej substancji. Na wynik oznaczenia
ma również wpływ toksykokinetyka badanego związku oraz czynniki
indywidualne (np. wiek, dieta, wydolność narządów, zażywane leki i używki,
czas trwania uzależnienia, tolerancja i inne), które powinny być uwzględnione
przez lekarza.
4.8 Dopalacze – nowe narkotyk
Omawiając temat narkotyków nie sposób chociaż wspomnieć o problemie
ostatnich lat, jaki stanowią dopalacze. Dopalacze to substancje
psychoaktywne - działając na ośrodkowy układ nerwowy wywierają wpływ na
procesy myślowe, nastrój i zachowanie człowieka.

33
DOPALACZE – PROBLEM GLOBALNY XXI WIEKU!
RÓŻNORODNE SUBSTANCJE NATURALNE LUB SYNTETYCZNE
OFEROWANE W POSTACI TABLETEK, SUSZU, PROSZKU, PŁYNU.
Sprzedawane jako produkty kolekcjonerskie, sól do kąpieli, kadzidełka,
nawóz do kwiatów, ozdoby choinkowe
Reklamowane jako bezpieczne i legalne
W założeniu mają być alternatywą dla zakazanych substancji
narkotycznych
Na opakowaniach informacja: „nie do spożycia” - brak możliwości
udowodnienia ich rzeczywistego przeznaczenia i wdrożenia procedur karnych.
Lista zakazanych substancji nie nadąża za nowo wprowadzanymi na rynek
dopalaczy substancjami psychoaktywnymi . Nieznaczna modyfikacja struktury
chemicznej daje nową jakość – legalny, ale szkodliwy zamiennik substancji
zakazanej, nielegalnej.
Działanie dopalaczy:
pobudzające ośrodkowy układ nerwowy
poprawiające nastrój
empatogenne (indukują uczucie empatii, miłości do świata i ludzi,
otwartości emocjonalnej)
relaksujące
halucynogenne
psychodeliczne - elementami doświadczenia psychodelicznego zwykle są
efekty wizualne, zaburzenia percepcji za pomocą zmysłów, synestezja
(wzajemne przenikanie się wrażeń zmysłowych, np. barwne słyszenie),
intensyfikacja bodźców zewnętrznych, doznania mistyczne,
a czasem psychotyczne.
Poszczególne dopalacze różnią się pod względem farmakokinetyki
i metabolizmu w ustroju.
Przyjmowane doustnie lub palone jak tytoń wchłaniają się szybko, niektóre już
przez błonę śluzową jamy ustnej i równie szybko zaczynają działać w
organizmie (zwykle w ciągu kilku minut)
Działanie amfetaminowe (podobne do amfetaminy) – BZP, katynony
Działanie kanabinoidowe (podobne do marihuany) – JWH-018
Działanie psychodeliczne (podobne do LSD) – szałwia wieszcza
Działanie narkotyczne (podobne do opium) – kratom; dekstrometorfan
OBRAZ KLINICZNY ZATRUCIA DOPALACZAMI

34
Obraz kliniczny zatruć dopalaczami syntetycznymi jest podobny do
zatruć, odpowiednio amfetaminą lub marihuaną
Dopalacze ziołowe powodują rozmaite zaburzenia psychiczne, od
pobudzenia (muchomor czerwony) do senności (duże dawki kratomu);
szałwia wieszcza działa psychodelicznie
Zwykle zaburzenia żołądkowo-jelitowe (wymioty, bieguna), możliwe
głębokie zaburzenia świadomości, rytmu serca, oddychania, wzrost lub
spadek ciśnienia tętniczego, hipoglikemia, drgawki
Opisy przypadków zatruć jako źródło wiedzy – niewystarczające (różne
substancje zażywane łącznie; oznaczenie dopalaczy w płynach
ustrojowych – niewykonalne lub trudne i kosztowne)
Brak zgodności deklarowanego na opakowaniu składu i ilości składników
dopalaczy w stosunku do rzeczywistej ich zwartości
Dopalacze zażyte w dużych dawkach mogą być groźne dla życia!
Odnotowane przypadki śmiertelne – niejasne (być może ofiary
przyjmowały inne zakazane substancje psychoaktywne)
Toksyczność wzrasta przy równoczesnym spożyciu alkoholu lub innych
związków psychoaktywnych (leki, narkotyki)
ROZPOZNANIE ZATRUCIA DOPALACZAMI
Rozpoznanie orientacyjne opiera się przede wszystkim na wywiadzie.
Ustalenie rozpoznania na podstawie objawów klinicznych jest
nieprawdopodobne - dopalacze są często przyjmowane w różnych
kombinacjach
Wywiady mogą być mylące – pacjent lub jego otoczenie ukrywają przed
lekarzem, że przyjął oprócz dopalaczy także inne, zakazane substancje
Nie istnieje jeden wzorzec reakcji organizmu na substancje zawarte w
dopalaczu!
Możliwe użycie metod chromatograficznych (chromatografia
cienkowarstwowa, cieczowa i gazowa z detekcją mas) ALE: DUŻY
KOSZT I NIEWIELKA DOSTĘPNOŚĆ WW. METOD W
WIĘKSZOŚCI OŚRODKÓW!!!
Metody immunologiczne, rutynowo stosowane do oznaczania
narkotyków NIE WYKRYWAJĄ substancji zawartych w dopalaczach
syntetycznych i naturalnych

35
Podstawą rozpoznania lekarskiego - wywiad toksykologiczny i badanie
przedmiotowe!
5. Wpływ spożywania alkoholu etylowego na wyniki badań
laboratoryjnych
Alkohol etylowy jest silnym środkiem odurzającym, który spożywany w
nadmiernych ilościach doprowadza do uszkodzenia wielu narządów
wewnętrznych. Alkoholizm powoduje, między innymi, spichrzanie tłuszczów w
wątrobie, hiperlipemię oraz marskość wątroby. Mimo działania silnie
uzależniająco, alkohol etylowy jest powszechnie stosowaną używką. Skutki
oddziaływania alkoholu etylowego na organizm zależą od ilości wypijanego
alkoholu, osobniczej podatności oraz czasu systematycznego spożywania.
Nadużywanie alkoholu prowadzi u chorego nie tylko do uszkodzenia wątroby,
ale też trzustki, mózgu, układu krwiotwórczego i układu krążenia. Zmiany
narządowe spowodowane przewlekłym spożywaniem etanolu uwidaczniają się
również w wynikach badan laboratoryjnych.
5.1 Zmiany obserwowane w badaniach laboratoryjnych spowodowane
spożyciem alkoholu etylowego
W krótkim czasie po spożyciu etanolu przejściowo występuje kwasica
mleczanowa, ketonemia, hiperlipidemia, porfirynuria. Spożyte jednorazowo
duże dawki etanolu hamują syntezę albumin w wątrobie. Natomiast długotrwałe
przyjmowanie alkoholu etylowego nie wpływa na stężenie albumin, ale
prowadzi do ograniczenia całkowitej syntezy białek i glikoprotein. Etanol
hamuje absorpcje i transport aminokwasów w jelicie. Skutkiem picia alkoholu
etylowego jest zmniejszone wchłanianie substancji odżywczych, co prowadzi do
niedoboru retinolu, tiaminy, witaminy B12 i kwasu foliowego. U alkoholików
nie dochodzi również do konwersji tiaminy w jej postać aktywną - pirofosforan
tiaminy. Zaburzenia wchłaniania i przemian witaminy B12 oraz folianów
powoduje niedokrwistość oraz prowadzi do zmian syderoblastycznych w szpiku
kostnym. W obrazie morfologii u osób przewlekle spożywających alkohol
etylowy obserwuje się makrocytozę z hiperchromią. Znacznie podwyższone są
wskaźniki czerwonokrwinkowe (MCH, MCV). Zaburzenia przemiany witaminy
A skutkuje utratą zdolności adaptacji do ciemności, potocznie nazywaną kurzą
ślepotą, często spotykaną u alkoholików. U osób przewlekle spożywających

36
alkohol etylowy zaburzeniu ulega również tor przemian witaminy D. Obniżone
stężenie aktywnej formy witaminy D3 prowadzi do zaburzenia przemian
metabolicznych tkanki kostnej oraz zmniejszenia masy kości, któremu
towarzyszy niskie stężenie osteokalcyny w surowicy.
Przewlekły alkoholizm wiąże się często z niedożywieniem, co pociąga za sobą
zwykle obniżone stężenie wapnia, potasu, magnezu oraz fosforanów w
surowicy. Zwiększa się również wydalanie cynku i magnezu z moczem.
Spożycie etanolu może spowodować zarówno hipoglikemię, jak i hiperglikemię,
co uzależnione jest od zapasów glikogenu w wątrobie. U osób sytych po
spożyciu większych ilości alkoholu etylowego obserwuje się zwiększenie
stężenia glukozy w surowicy. Jest to spowodowane ograniczeniem obwodowego
zużycia glukozy, przyspieszeniem procesu glikogenolizy oraz zahamowaniem
procesu glikolizy. Częste po spożyciu etanolu obniżenie stężenia glukozy w
surowicy obserwuje się z kolei u osób głodnych oraz alkoholików, u których
zapasy glikogenu w wątrobie są znacznie ograniczone.
Izolowany wzrost aktywności gamma-glutamylotransferazy (GGT) wskazuje
na spożycie alkoholu w ciągu 7 dni przed badaniem, choć może on być również
wywołany ekspozycją na inne ksenobiotyki lub przyjmowaniem leków
przeciwzakrzepowych.
Przyczyną podwyższonej aktywności GGT mogą być także różne choroby
wątroby (np. cholestaza, HCV) niezwiązane ze spożyciem etanolu. Poziom
GGT w surowicy powraca do normy zwykle w ciągu 1 - 1,5 tygodnia od
zaprzestania spożywania alkoholu etylowego.
Przy okazjonalnym spożywaniu etanolu nie obserwuje się zwykle wzrostu
aktywności fosfatazy zasadowej (ALP) i bilirubiny. Parametry te są
podwyższone w zaawansowanym uszkodzeniu wątroby i dróg źółciowych, które
może być spowodowane alkoholizmem. Nieznacznie podwyższona jest zwykle
aktywność aminotransferazy asparaginianowej (AST) i aminotransferazy
alanianowej (ALT). Aktywność AST jest wyższa niż ALT z powodu
uszkodzenia mitochondriów hepatocytów i uwolnienia do krwi zawartej tam
aminotransferazy asparaginianowej. Stosunek AST do ALT zwykle przewyższa
2:1. Wzrost aktywności amylazy i lipazy, zarówno w surowicy, jak i w moczu
jest najczęściej objawem poalkoholowego uszkodzenia trzustki. U osób
spożywających duże ilości alkoholu etylowego obserwuje się wzrost
aktywności kinazy kreatyninowej (CPK), głównie izoformy mięśniowej (CK-
MM), na skutek toksycznego wpływu alkoholu na tkankę mięniową. Miopatia
poalkoholowa prowadzi również do wzrostu aktywności AST. Gwałtowna
37
rabdomioliza może być także przyczyną niewydolności nerek. Spożywanie
alkoholu etylowego prowadzi do wzrostu stężenia kwasu moczowego
we krwi, co jest spowodowane nasiloną syntezą kwasu moczowego w wyniku
przyspieszenia obrotu nukleotydów oraz zmniejszeniem jego wydalania przez
nerki. Za ograniczone wydalanie kwasu moczowego przez nerki odpowiedzialne
jest zwiększone stężenie mleczanów, które utrudniają wydzielanie kwasu
moczowego w dystalnych częściach nefronu.
Ze względu na stosunkowo niską czułość i swoistość wskaźników
biochemicznych nadużywania alkoholu, poszukuje się specyficznych markerów
choroby alkoholowej. Za nowe wskaźniki biochemiczne nadużywania alkoholu
uważa się transferynę desjalowaną (transferynę ubogoglikozylowaną - CDT),
aldehyd octowy związany z hemoglobiną (HAA), beta-heksoaminidazę
(β-HEX), des-g-karboksyprotrombinę (DCP) oraz mitochondrialną frakcję AST.
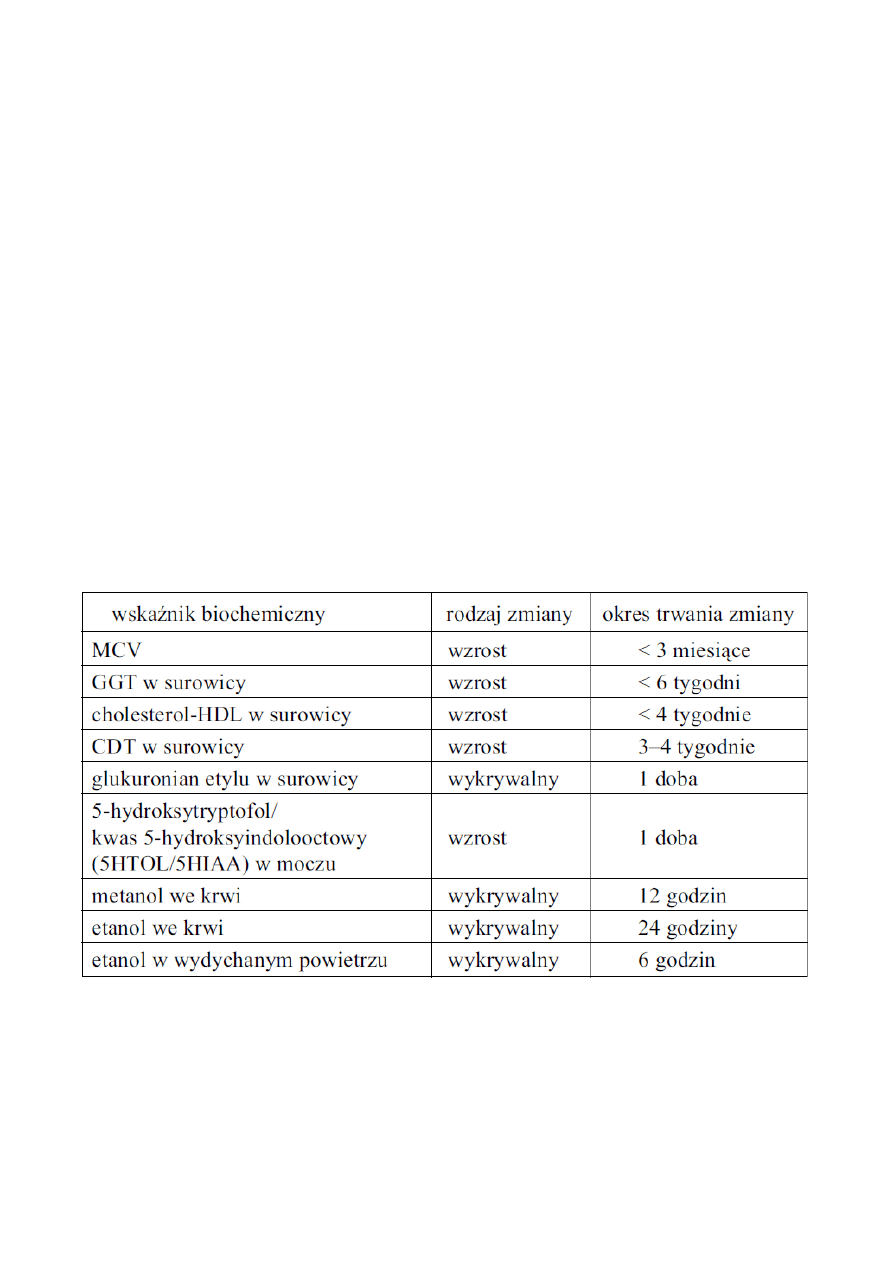
Tabela 22 – Okres trwania wskaźników biochemicznych związanych ze
spożywaniem alkoholu

38
5.2 Ostry i przewlekły efekt spożywania alkoholu etylowego
Spożywanie alkoholu etylowego wywołuje w organizmie zmiany metaboliczne
określane jako efekt ostry lub jako efekt przewlekły.
Do efektu ostrego dochodzi zwykle po upływie 2 - 4 godzin od spożycia
etanolu. Sporadyczne spożycie większych ilości alkoholu etylowego prowadzi
do zahamowania glukoneogenezy w wątrobie, w związku z czym w surowicy
obniża się stężenie glukozy, zaś podwyższa stężenie mleczanów. Powstające
metabolity, takie jak aldehyd octowy i octan, powodują wzrost tworzenia kwasu
moczowego przez wątrobę. Z kolei mleczany i octany obniżają stężenie
wodorowęglanów. Obserwuj się również zmiany stężeń wielu innych
parametrów biochemicznych.
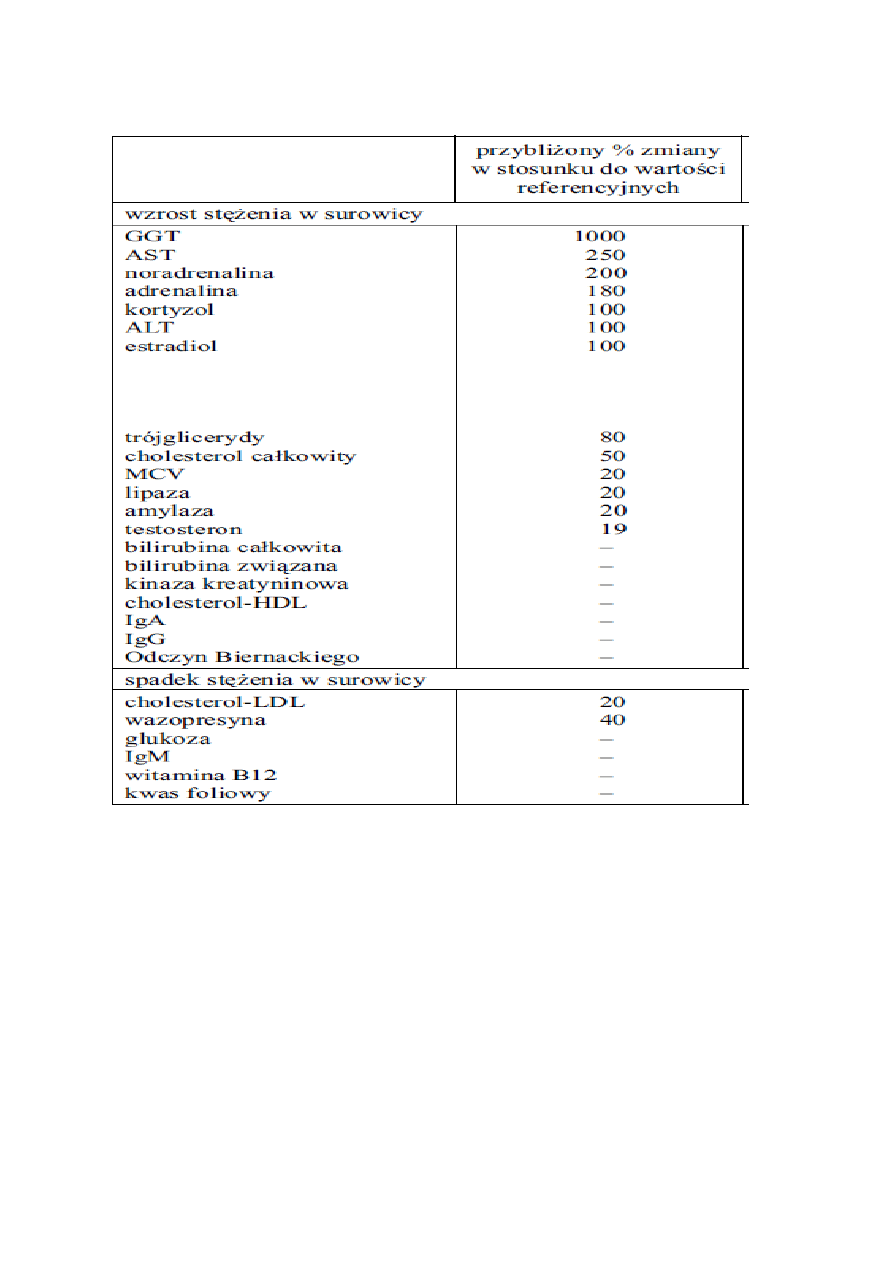
Tabela 23 – Efekt ostry spożywania alkoholu etylowego

39
Większość zmian biochemicznych spowodowanych okazjonalnym
spożyciem większej ilości etanolu ustępuje zwykle po upływie 48 godzin.
Zaleca się zatem, aby krew do badań była pobierana przynajmniej po 2 dobach
od spożycia alkoholu etylowego.
5.3 Przewlekły efekt działania alkoholu etylowego obserwuje się u osób
dotkniętych alkoholizmem.
Skutkiem długoterminowego spożywania etanolu jest między innymi wzrost
aktywności gamma-glutamylotransferazy wywołany indukcją
enzymów. Bezpośrednim efektem intoksykacji wątroby jest zwiększenie
aktywności dehydrogenazy glutaminianowej oraz aminotransferaz (AST, ALT).
Inhibicja enzymatycznej glikozylacji podczas potranslacyjnych przemian białek
w wątrobie skutkuje wzrostem stężenia białek desjalowanych (carbohydrate
deficient transferrins). Obserwowany wzrost stężenia trójglicerydów
spowodowany jest z kolei ograniczonym ich rozpadem w osoczu. Działanie
alkoholu na komórki szpiku w trakcie erytropoezy prowadzi do zwiększenia
MCV. Przyczyną zaburzeń morfologii krwinki czerwonej mogą być również
niedobory kwasu foliowego lub witaminy B12. U alkoholików obserwuje się
zwykle zwiększoną diurezę w następstwie obniżenia wydzielania wazopresyny
przez zwiększoną sekrecję reniny i aldosteronu. Wydalanie dużych ilości
rozcieńczonego moczu powoduje również zmianę parametrów
fizykochemicznych wydalanego moczu, np. zmniejszenie jego ciężaru
właściwego.
40
Tabela 24 – Efekt przewlekłego spożywania alkoholu etylowego
6. Wpływ preparatów ziołowych na wyniki badań laboratoryjnych
Stosowanie preparatów ziołowych nie jest zabronione, uważa się , że nie można
przedawkować ziół, gdyż są one produktem naturalnym i tym samym powinny
być bezpieczne. Ziołolecznictwo było podstawą leczenia od początków
cywilizacji i wiele współczesnych leków jest opartych na substancjach
aktywnych zawartych w roślinach.
Mechanizm działania ziół jest różnorodny. Pojedynczy składnik lub mieszanka
ziołowa może hamować lub indukować rodzinę enzymów cytochromu P-450, P-
glikoproteinę. ATP – zależne białka transportowe w ścianie jelita cienkiego.

41
Mogą one interferować z zażywanymi lekami (poprzez działanie na jelitowy
polipeptyd A transportujący aniony organiczne). Takie efekty stają się
szczególnie istotne , kiedy interakcje preparat ziołowy – lek może zmieniać
wyniki badań laboratoryjnych.
6.1 Korzystne i toksyczne efekty stosowania ziół
Preparaty ziołowe mogą być skuteczne ale mogą także (czasem równocześnie)
wywierać działanie szkodliwe. Przykłady roślin o korzystnym działaniu:
Ostropest plamisty (łac. Silybum marianum, potocznie zwany ostem Maryi),
którego nasiona zawierają substancję o działaniu hepoatoprotekcyjnym –
silimarynę. Wyciąg z ostropestu zapobiega wnikaniu związków toksycznych do
hepatocytów (poprzez modyfikację ich błony komórkowej). Silimaryna jest
używana jako preparat ochronny na wątrobę oraz w leczeniu poalkoholowego
uszkodzenia tego narządu. Podwyższona aktywność transaminaz po 4
tygodniach leczenia zmniejsza się z równoczesną poprawą funkcji wątroby.
Gurmar (łac. Gymnema sylvestre) stymuluje wytwarzanie insuliny przez
komórki β wysp trzustkowych u pacjentów z cukrzycą typu 2. Liście tej rośliny
zawierają składnik aktywny zwany GS4. Gurmar stosowany łącznie z doustnymi
lekami przeciwcukrzycowymi istotnie obniża zarówno poziom glukozy na
czczo, jak i poziom hemoglobiny glikowanej.
Preparaty głogu dwuszyjkowego(łac. Crataegus laevigata) zawierając flawonoidy
i oligomeryczne proantocyjanamidy obniżają stężenie cholesterolu całkowitego,
cholesterolu we frakcji LDL oraz trój glicerydów już po 4 – tygodniowej terapii.
Japońska mieszanka 8 ziół o nazwie Hachimi-jio-gan wykazuje działanie
podwyższające stężenie cholesterolu we frakcji HDL po 7 miesięcznej terapii.
Jest ona powszechnie stosowana w Japonii i Chinach (na rynkach europejskich
dostępna głównie w sprzedaży internetowej) jako środek wzmacniający, do
leczenia cukrzycy, zaburzeń erekcji i schorzeń gruczołu krokowego.
Ekstrakt z owoców palmy sabalowej (łac. Serenoa repens) ma znaczenie w
leczeniu objawów urologicznych łagodnego rozrostu gruczołu krokowego oraz
zapalenia pęcherza moczowego.

42
Ajurwedyjskie zioło Salacia reticulata wywołuje efekt hipoglikemizujący,
ponieważ zawiera kotalanol (inhibitor α – glukozydazy) i jest stosowany w
leczeniu cukrzycy. Po 3 miesiącach stosowania jego preparatów dochodzi do
znacznego obniżenia poziomu hemoglobiny glikowanej.
Preparaty czystka (łac. Cistus) – ze względu na wysoką zawartość polifenoli o
silnych właściwościach antyoksydacyjnych przyczynia się do obniżenia
apoliproteiny A, LpX, wolnych rodników tlenowych. Obniża poziom
cholesterolu we frakcji LDL oraz zapobiega oksydacji lipoproteiny LDL i HDL.
Przykłady roślin o działaniu toksycznym dla organizmu:
Napój uzyskiwany z nasion pieprzu metystynowego (łac. Piper methysticum)
znanego jako Kava Kava. Wywołuje on uczucie odprężenia i jest zażywany przy
leczeniu stresu i stanów lękowych (za działanie odpowiadają kawalaktony
wiążące się z receptorami kwasy gamma aminomasłowego). Jednocześnie
odpowiedzialne są za efekt hepatotoksyczny powodując wzrost transaminaz i
bilirubiny całkowitej.
Przykładem rośliny neurotoksycznej jest chińskie zioło Aristolchia Fang Chi
(nazywane także Mu tong) obecne w wielu chińskich mieszankach
odchudzających. W jego składzie obecne są nefrotosyny – kwasy aristocholowe
I i II, które mogą wywoływać ciężką niewydolność nerek, prowadzącą do
znacznego podwyższenia kreatyniny (ze spadkiem eGFR) i mocznika w
surowicy krwi.
Glistnik jaskółcze ziele (łac. Chelidonium majus) ma silne działanie
hepatotoksyczne, jego używanie prowadzi do wzrostu aktywności transaminaz,
GGTP i poziomu bilirubiny (całkowitej i sprzężonej).
Ożanka właściwa (łac. Teucrium chamaedrys) – jej używanie prowadzi do
ostrego zapalenia wątroby ze znaczącym wzrostem aktywności transaminaz,
GGTP, ALP i bilirubiny po 3-18 tygodniach po spożyciu.
43
6.2 Wpływ stosowanych doustnie ziół na działanie leków.
Osobnym problemem działania leków roślinnych są liczne interakcje ze
stosowanymi lekami. Jeśli znane są mechanizmy interakcji można przewidzieć
skutek działania i odpowiednio zapobiec wystąpieniu niekorzystnego działania.
Gorsza sytuacja występuje wówczas, gdy nie można przewidzieć efektu
działania leku w interakcji z preparatem ziołowym, szczególnie kiedy występuje
genetyczna zmienność np. w przypadku izoformy CYP (rodzina enzymów
odgrywających role w metabolizmie leków), czego przykładem jest miłorząb
japoński, który indukuje CYP2C19 w sposób zależny genetycznie – wpływając
na stężenie maksymalne omeprazolu w surowicy krwi – dochodzi do obniżenia
stężenia maksymalnego (u homozygot intensywnie metabolizujących o 30,4%, u
homozygot intensywnie metabolizujących o 45,8%, a u heterozygot o 38,8%).
Tabela 25 – wpływ preparatów ziołowych na INR u leczonych acenokumarolem
Preparat
Wpływ na INR
Dziurawiec zwyczajny (łac. Hypericum perforatum)
Obniżenie
Żeń – szeń (łac. Panax ginseng)
Białka soi
Imbir
Podwyższenie
Szałwia czeronokorzeniowa (łac. Salvia miltiorrhiza)
Dzięgiel chiński (łac. Angelica sinensis)
Kolcowój zwyczajny (łac. Lycium barbarum)
Rumianek pospolity (łac. Chamomilla recutita)
Mleczko pszczele
44
Tabela 26 – Wpływ ziół na stężenie leków poprzez zmiany ich metabolizmu
Preparat
Wpływ na metabolizm
Efekt zmiany
Dziurawiec zwyczajny
(łac. Hypericum
perforatum)
Indukcja CYP3A4
Obniżenie stężenia
cyklosporyny,
indinawiru i digoksyny
Indukcja CYP2C9
Zmniejszenie efektu
warfaryny (↓ INR)
Miłorząb japoński (łac.
Gingko biloba)
Indukcja CYP2C19
Obniżenie stężenia
omeprazolu
Indukcja CYP2C9
Obniżenie stężenia
tolbutamidu
Żeń – szeń (łac. Panax
ginseng)
Hamowanie CYP3A4
Wzrost stężenia
nifedypiny
Sok grejpfrutowy
Hamowanie CYP3A4
Wzrost stężenia
metadonu, felodypiny,
simwastany i
amiodaronu
Czosnek (łac. Galium
sativum)
Indukcja grupy CYP 450
Obniżenie stężenia
inhibitora proteazy HIV -
sakwinaviru
Przy okazji soku grejpfrutowego - Coraz dłuższa jest lista leków, których nie
należy zażywać wraz sokiem grejpfrutowym. Sok grejpfrutowy spowalnia
metabolizm wielu farmaceutyków, co może doprowadzić do groźnego wzrostu
ich poziom w organizmie chorego. Specjaliści Lawson Health Research Institute
twierdzą, że w ciągu zaledwie ostatnich pięciu lat, od 2008 r. do 2012 r., z 17 do
43 zwiększyła się liczba znanych leków, z którymi sok grejpfrutowy powoduje
groźne interakcje. Są to preparaty kardiologiczne, takie jak werapamil i
amiodaron, onkologiczne, statyny (leki obniżające poziom cholesterolu we krwi)
oraz leki immunosupresyjne (chroniące przed odrzuceniem przeszczepu przez
organizm biorcy). Sok grejpfrutowy do tego stopnia spowalnia metabolizm tych

45
leków, że gdy zażyjemy jedną tylko tabletkę, to efekt może być taki jak po
połknięciu od 5 do 10 pastylek. Skutkiem tego rodzaju niekorzystnych interakcji
mogą być krwawienia z żołądka, zaburzenia rytmu serca, zakłócenia
oddechowe, uszkodzenie nerek, a nawet nagły zgon. Sok grejpfrutowy zawiera
furanokumarynę, pochodną kumaryny, która hamuje rozkład niektórych leków
w przewodzie pokarmowym zanim jeszcze przedostanie się on do krwioobiegu.
Ten proces uwzględnia się podczas opracowywania dawek preparatów. Gdy
jednak ten mechanizm zostanie zakłócony lek przenika w zbyt dużym stężeniu.
Sok grejpfrutowy spowalnia również metabolizm leków przeciwhistaminowych,
czyli przeciwalergicznych. Skutkiem tego jest wzrost jego stężenia nawet o od
trzech do siedmiu razy i zaburzenia rytmu serca. Groźne interakcje z lekami
mogą powodować także inne owoce, takie jak gorzka pomarańcza i olbrzymia
pomarańcza pomelo.
7. Wpływ sterydów anaboliczno – androgennych (SAA) i prohormonów
na wyniki badań laboratoryjnych
Stosowanie niedozwolonych środków wspomagających budowę muskulatury
takich jak sterydy anaboliczno-androgenne (w skrócie – SAA) i ich pseudo-
legalne klony, czyli tzw. prohormony, może wydawać się niezwykle atrakcyjne
dla osób, które trenują po to by zwiększyć rozmiary. Niestety wypracowane
podczas cyklu sterydowego efekty w dużej mierze mają charakter ulotny i
pewna ich część czasem znika, pomimo kontynuowania intensywnych
treningów i trzymania dobrze zbilansowanej diety. Za ten fakt odpowiada
zmiana środowiska hormonalnego. W trakcie przyjmowania SAA poziom
anabolicznych hormonów w organizmie przekracza fizjologiczne granice co
umożliwia szybki rozwój masy mięśniowej i siły. Po zakończeniu cyklu pojawia
się androgenowa dziura, gdyż z jednej strony przestajemy aplikować testosteron
i jego analogi z zewnątrz, a z drugiej – endogenna synteza ciągle jest
zmniejszona, lub całkowicie zablokowana (stosowanie sterydów blokuje oś
przysadka- podwzgórze- jądra hamując syntezę testosteronu). Przy niskim
poziomie hormonów nie tylko rozbudowa muskulatury jest utrudniona, ale także
utrzymanie wypracowanych efektów. Środki farmaceutyczne stosowane w celu
przywróceniu hormonalnej równowagi nie zawsze działają szybko i precyzyjnie.

46
7.1 Czym są pro-hormony
Pro-hormony sprzedawane w sieci to w teorii substancje, które po dostaniu się
do organizmu konwertują do konkretnych hormonów mogących wywierać efekt
fizjologiczny. W praktyce jednak to po prostu sterydy anaboliczno-androgenne
„przebrane” za suplementy diety. Z tym, że klasyczne „sterydy” dostępne są w
aptekach i wydawane jedynie na podstawie recepty lekarskiej bądź też na
„czarnym rynku” u tzw. dilerów i nikt nie ma wątpliwości czym są w istocie.
Pro-hormony natomiast zakupić można „legalnie” na polskich serwisach
aukcyjnych. Pod nazwami takimi jak Trenadrol, Massdrol, Oxanvar, H-DROL,
S-DROL, Epithin-E, X-TREN, P-PLEX, MEDROID, SUPER-DMZ, QUAD
STAK, FINABOLIC, ANDRO XS, SUS500, MASSFIRE, EPIFIRE, Finabolic,
DECAPRO czy DECAFIRE kryją się niezwykle silne, ale przede wszystkim
wyjątkowo niebezpieczne substancje, które co prawda powodują gwałtowne
przyrosty masy i siły, ale przy okazji - sieją prawdziwe spustoszenie w
organizmie. Tymczasem w przekonaniu wielu młodych osób, które skuszone
kolorowymi obietnicami szybkich przyrostów klikają „kup teraz”, pro-hormony
to po prostu silne, ale bezpieczne suplementy diety!
Lista negatywnych konsekwencji stosowania tych środków jest bardzo długa i
obejmuje m.in. zaburzenia hormonalne z impotencją włącznie (często
wymagającą leczenia farmakologicznego), ginekomastię, trądzik, nadciśnienie
tętnicze, uszkodzenia nerek i wątroby. Pojawić się także mogą zaburzenia
zachowania takie jak napady agresji, co w wypadku osób podatnych, młodych
może prowadzić do konfliktów z prawem. Poza tym po zaprzestaniu stosowania
dość często występuje silna zniżka psychicznej (i fizycznej) formy, która
prowadzić może do depresji. Warto także wspomnieć, że o ile zdrowotne skutki
stosowania pro-hormonów mogą być nieodwracalne, o tyle uzyskane przyrosty
masy i siły są jedynie chwilowe.
7.2 Sterydy anaboliczno androgenne
Sterydy anaboliczne to grupa steroidów pochodzenia naturalnego lub
syntetycznego, która ma silne działanie anaboliczne tzn. powodujące
przyspieszenie dzielenia się komórek tworzących określone tkanki organizmu
zwierząt w tym ludzi. Są to pochodne testosteronu lub 19-nortestosteronu.

47
Działanie niektórych sterydów anabolicznych polega na stymulowaniu wzrostu
masy mięśni i czasami również kości poprzez pobudzanie syntezy białka lub
wapnia. Efekt ten jest szczególnie ważny w dopingu sportowym. Sterydy
anaboliczne mają jednak także wiele ubocznych efektów, gdyż wpływają silnie
na ogólną równowagę hormonalną organizmu. Jednym z najbardziej znanych
naturalnych sterydów anabolicznych jest testosteron, który pełni też rolę
męskiego hormonu płciowego.
Sterydy anaboliczne działają poprzez aktywowanie receptorów androgenowych
obecnych na powierzchni błon komórkowych komórek. Efekty tego pobudzania
dzieli się zwykle na ogólnie anaboliczne i związane z powstawaniem różnic
między płciami.
Przykłady efektów anabolicznych:
wzmożona synteza białek,
wzrost tempa przyrostu masy, siły i wytrzymałości mięśni,
wzrost apetytu,
wzrost tempa przyrostu kości,
zwiększona produkcja krwinek czerwonych.
Przykłady efektu różnicowania płciowego:
wzrost rozmiarów penisa i łechtaczki u dzieci (u osób dorosłych
podawanie jakichkolwiek sterydów nie ma już najmniejszego wpływu na
rozmiary organów płciowych)
wzrost rozmiarów klatki piersiowej u chłopców, piersi i bioder u
dziewcząt
wzmożony przyrost owłosienia całego ciała u mężczyzn i sfer erogennych
u kobiet
efekty mutacji głosu u chłopców.
Jakkolwiek chemicy dążą do uzyskania sterydów które powodowałyby
wyłącznie efekty anaboliczne i nie zaburzały efektów różnicowania płciowego,
współcześnie praktycznie wszystkie syntetyczne sterydy anaboliczne powodują
oba te efekty. Wynika to z faktu, że wszystkie one są metabolizowane przez
organizm człowieka, a produkty ich metabolizmu mają uboczne działanie

48
poprzez aktywowanie receptorów estrogenowych, co powoduje rozmaite
niepożądane efekty, takie jak:
przyspieszone starzenie się niektórych tkanek (zwłaszcza kości u
mężczyzn)
nienaturalny rozrost piersi zarówno u kobiet jak i u mężczyzn
(ginekomastia)
zachwianie równowagi hormonów płciowych powodujący nienaturalny
spadek popędu seksualnego u mężczyzn i jego sztuczny wzrost u kobiet.
Tabela 27 – Stosowane SAA
Najpopularniejsze wśród młodych
mężczyzn sterydy:
metanabol
(methandrostenolone),
winstrol (stanazolol),
oxymetholone (anapolon),
oxandrolon (anavar),
Najbardziej toksyczne i rzadko
spotykane (w kolejności od
najbardziej toksycznych):
methyltrienolone
(Metribolone/R1881; pochodna
trenbolonu),
mibolerone,
fluoxymesteron (halotestin),
methyltestosterone (metylowany
testosteron),
oral turinabol
(dehydrochloromethyltestostero
ne),
Stosowane najczęściej oralne SAA:
methandrostenolone
(metanabol),
stanozolol (winstrol),
oxymetholone (anapolon),
Stosowane najczęściej iniekcyjne
SAA:
nandrolone decanoate,
testosterone enanthate,
trenbolone enanthate

49
7.3 Wpływ SAA i prohormonów na wyniki badań laboratoryjnych
Badania naukowe przynoszą dziesiątki przykładów ćwiczących, których
należałoby nagrodzić za wyjątkowe poświęcenie w testowaniu najbardziej
toksycznych sterydów anabolicznych, w dawkach wielokrotnie
przekraczających zdrowy rozsądek. Niestety, doniesienia badaczy to tylko
czubek góry lodowej nieujawnionych przypadków uszkodzeń nerek, wątroby
oraz serca.
Do największych trucizn należy zaliczyć:
wszelkie prohormony, wykazują większą nefro i hepatoksyczność niż
sterydy anaboliczno-androgenne,
oralne SAA – wszelkiego rodzaju metylowane sterydy, z grupą 17-alfa,
toksyczne iniekcyjne SAA np. trenbolone,
Tabela 28 Wpływ SAA i prohormonów na wyniki badań.
Narząd/układ
Wpływ na badania
Oś podwzgórze – przysadka - gonady
W trakcie stosowania preparatów
wysoki poziom testosteronu (wolnego
i całkowitego), niskie stężenia FSH i
LH.
Po cyklu stosowania w przypadku
zablokowania osi wysokie stężenia
FSH i LH przy bardzo niskim stężeniu
testosteronu (wolnego i całkowitego)
Wątroba
-Aminotransferazy podniesione
niejednokrotnie ponad 100 x powyżej
górnej granice wartości referencyjnej
-Hiperbilirubinemia
-Wzrost stężenia amoniaku
-Spadek stężenia białka całkowitego i
albumin

50
-Wzrost aktywności LDH
Układ krzepnięcia
Wzrost czasów krzepnięcia, spadek
stężenia fibrynogenu, często wzrost d-
dimerów
Nerki
Wzrost stężenia kreatyniny
(niewydolne nerki oraz duże
uwalnianie z mięśni), spadek eGFR,
wzrost stężenia mocznika,
hiponatremia,
Serce
Wzrost aktywności CPK i CK-MB,
wzrost stężenia troponin i BNP
8. Wpływ suplementów diety na wyniki badań laboratoryjnych
Suplement diety - uzupełnienie diety, dodatek zawierający niezbędne dla
zdrowia składniki (zwłaszcza witaminy lub inne substancje egzogenne), których
może brakować w codziennej diecie. Suplement oferowany jest najczęściej w
postaci skoncentrowanej - jako tabletki, kapsułki, proszek lub płyn
Suplementy zazwyczaj są produkowane i wprowadzane do obrotu w formie
umożliwiającej ich precyzyjne i łatwe dawkowanie, co w połączeniu z często
spotykaną sprzedażą w aptekach może sugerować ich związek z lekami. Jednak
w Unii Europejskiej suplementy diety nie były i nie są traktowane jak leki. W
Polsce suplementy diety dopuszcza do obrotu Główny Inspektor Sanitarny i
podległe mu urzędy (a nie Główny Inspektor Farmaceutyczny lub Urząd
Rejestracji Leków i Produktów Biobójczych).
Istnieje bliski związek pomiędzy zdrowiem człowieka, długością i jakością jego
życia, a charakterystyką jego odżywiania się. Do normalnego funkcjonowania
komórek organizmu niezbędnych jest wiele mikroskładników, których część
może być dostarczana w postaci suplementów diety.
Przykłady działania suplementów diety na wyniki badań laboratoryjnych:
Witamina C (kwas askorbinowy) stosowana w dawkach ≥1g na dobę może
fałszować wyniki oznaczeń: glukozy, aminotransferaz, etyloestradiolu, LDH w
osoczu, bilirubiny, żelaza, ferrytyny, kwasu moczowego, obecność krwi utajonej
w kale, pH moczu.

51
Witamina E – Podczas długotrwałego przyjmowania w skojarzeniu z doustnymi
lekami przeciwzakrzepowymi może wydłużać czas protrombinowy
Witamina B2 – powoduje żółte zabarwienie moczu
Witamina PP – długotrwale stosowana może powodować uszkodzenie wątroby
z podniesieniem aktywności transaminaz i stężenia bilirubiny
Witamina D3 – poprzez swoją formę aktywną kalcytriol Wykazuje bezpośrednie
działanie hamujące na wydzielanie PTH przez przytarczyce oraz uwrażliwia je
na działanie hamujące wapnia. Kalcytriol w obecności PTH nasila osteolizę
kości. W jelitach, również w obecności PTH, zwiększa wchłanianie wapnia i
fosforu. Podobny wpływ na wchłanianie wapnia i fosforanów wywołuje w
nerkach.
Preparaty wapnia, magnezu, potasu – u pacjentów z niewydolnością nerek
mogą prowadzić do wzrostu stężenia tych parametrów powyżej wartości
referencyjne.
Kreatyna - W latach 90. XX wieku kreatyna zyskała szczególny rozgłos jako
naturalny sposób na zwiększenie wyników sportowych i budowanie
beztłuszczowej masy ciała. Stwierdzono, że ogólna zawartość kreatyny w
mięśniach szkieletowych jest zwiększona po doustnym podaniu suplementów
diety, a zawartość ta różni się i zależy od wielu czynników, m.in. od poziomu
spożycia węglowodanów, rodzaju aktywności fizycznej i typu włókien
mięśniowych. W skutek tego zaczęto stosować kreatynę w charakterze dodatku
do suplementów diety stosowanych przed treningiem. Na rynku dostępne są
różne formy kreatyny, m.in. cytrynian, jabłczan, ester etylowy, azotan,
chlorowodorek, glukonian, α-ketoglutaran i orotan. Jej przyjmowania podnosi
stężenie kreatyniny w moczu, co obniża wskaźniki wydalnicze. Ma również
wpływ na klirens kreatyniny.
Preparaty wapnia -
mogą ograniczyć lub nawet całkowicie uniemożliwić
wchłanianie niektórych leków, ponieważ tworzą z nimi sole wapnia, które są
nierozpuszczalne w wodzie. Interakcje te dotyczą takich leków, jak
fluorochinolony i tetracykliny, stosowanych często w leczeniu zakażeń dróg
oddechowych i moczowych – bak reakcji na leki.
Błonnik - może wpływać na wchłanianie preparatów naparstnicy, stosowanych
w leczeniu niewydolności krążenia i zaburzeń rytmu serca, a także
52
trójpierścieniowych leków przeciwdepresyjnych (np. amitryptyliny
i imipraminy). Interakcje tego typu prowadzą do ograniczenia skuteczności
terapii tymi lekami.
Witamina K – znosi działanie acenokumarolu wskutek czego nie dochodzi do
terapeutycznego wzrostu INR
9. Farmakoterapia a badanie ogólne moczu
Jednym z podstawowych i najczęściej zlecanych badań przesiewowych jest
badanie ogólne moczu. Jest ono wprawdzie pozornie łatwe w wykonaniu,
niewymagające dużego nakładu czasu, ale i z nim mogą się wiązać potencjalne
problemy. Leki mogą wpłynąć na zmianę barwy moczu oraz na parametry
mierzone przy pomocy testów paskowych.
9.1 Zmiana barwy moczu może wiązać się z dietą oraz niektórymi związkami
chemicznymi:
- W przypadku moczu o barwie czerwonej, pomarańczowej lub brązowej
możemy mieć do czynienia ze zwiększonym wydalaniem barwników
żółciowych, porfiryn, bilirubiny, z obecnością erytrocytów, mioglobiny.
Uzyskanie ww. koloru może wykazywać związek ze spożyciem buraków
ćwikłowych, rabarbaru, karotenem, bądź zażywaniem niektórych leków np.
lewodopy.
- Pojawienie się czerwonawej barwy moczu może świadczyć o stosowaniu
roślinnych leków przeczyszczających zawierających antrachinonowe glikozydy
na przykład Figura 1, Figura 2 (Herbapol Lublin), kora kruszyny (Kawon,
Herbapol Kraków, Lublin, Wrocław), Tabulettae laxantes (ICN Polfa Rzeszów),
Laxitab® (Biofarm).
- Infekcja bakteryjna Pseudomonas może prowadzić do implikacji w postaci
zielonkawego odcienia moczu. Podobny efekt dają leki takie jak amitryptylina,
indometacyna czy też błękit metylenowy, będący składnikiem niektórych
preparatów złożony takich jak Ginjal (Ikong).
- W moczu zasadowym pod wpływem soku z aloesu (Laboratoria Natury)
można obserwować barwę od żółtoróżowej do czerwonobrązowej. Podobny
rezultat obserwujemy w przypadku leku stymulujący odporność organizmu
Biostymina® (Phytopharm Klęka).
- Stosowanie nitrofurantoiny w leczeniu bakteryjnych zakażeń dróg moczowych
może zmieniać kolor moczu nadając mu barwę od rdzawożółtej do brązowej.

53
Analogiczne zmiany występują przy stosowaniu leku pierwotniakobójczego –
chlorochiny oraz leku na zakażenia bakteryjne jelit i zatrucia pokarmowe –
furazolidonu.
- Intensywnie żółtą barwę moczu możemy zawdzięczać dużym dawkom
ryboflawiny, będącej składnikiem preparatów witaminowych takich jak
Vitaminum B2(Pliva Kraków, Teva Pharmaceuticals Polska).
- Stosowanie soli żelaza w preparatach takich jak Ascofer ® (Gerda) może
prowadzić do zaczernienia moczu.
Niektóre środki farmakologiczne wywierają wpływ na procesy enzymatyczne
biosyntezy porfiryn i hemu. Mocz zmienia wtedy barwę na czerwoną,
czerwonobrunatną lub czarną. Ciemnieje on pod wpływem światła. Do takich
leków należą między innymi:
— środki znieczulające: lidokaina, barbiturany
— środki przeciwbólowe: diclofenak
— środki psychotropowe: hydroksyzyna
— leki przeciwbakteryjne: chloramfenikol, erytromycyna, klindamycyna,
nitrofurantoina, sulfonamidy
— hormony płciowe: progesteron i syntetyczne gestageny, luteina
— leki przeciwhistaminowe: klemastyna
Należy pamiętać, że zmiany barwy moczu mogą wynikać nie tylko ze
stosowanej farmakoterapii.
Żółtopomarańczowa barwa może wiązać się z obecnością wysokich stężeń
urobiliny i bilirubiny w moczu, czerwona lub brązowa z obecnością
erytrocytów, natomiast czerwonoróżowa z występowaniem moczanów.
9.2 Glukoza
Obecnie stosowane testy paskowe wykrywają glukozę w oparciu o metody
enzymatyczne. Ponieważ nie wykrywają one obecności innych cukrów
(galaktoza, ksyloza, fruktoza, laktoza), u dzieci z podejrzeniem zespołów
metabolicznych wykonuje się przyłóżkowo test tabletkowy na obecność w
moczu substancji redukujących.
Przyczyną fałszywie dodatnich wyników może być obecność związków
utleniających czy też peroksydaz bakteryjnych.
54
Na fałszywie ujemny wynik badania może mieć wpływ wysokie stężenie kwasu
askorbinowego i ciał ketonowych oraz niskie pH moczu (pH<5) [5].
9.3 Ciała ketonowe
Do ciał ketonowych należy acetooctan, betahydroksymaślan i aceton. Związki te
stanowią pośrednie metabolity przemian tłuszczów i białek. Pojawienie się ciał
ketonowych w moczu może wynikać z wystąpienia kwasicy ketonowej. Testy
paskowe pozwalają tylko na wykrycie acetooctanu.
Fałszywie pozytywne lub zawyżone wyniki uzyskuje się przy silnym
zabarwieniu moczu, spożywaniu przez pacjenta lewodopy lub kaptoprylu.
9.4 Ciężar właściwy
Badanie ciężaru właściwego moczu pozwala na określenie zdolności nerek do
zagęszczania moczu.
Fałszywie dodatnie wyniki można uzyskać przy podwyższonym poziomie białka
w moczu oraz obecności ciał ketonowych.
Przyczyną fałszywie ujemnych wyników może być silnie zalkalizowanie moczu,
wysokie stężenie glukozy, mocznika lub mannitolu.
9.5 Białko
Zasada działania testu paskowego opiera się na wykrywaniu albumin, stąd też w
badaniu można przeoczyć inne istotne białka takie jak mukoproteiny, globuliny i
białko Bence-Jones’a (szpiczak mnogi).
Fałszywie dodatnie wyniki można uzyskać w moczu silnie zagęszczonym lub o
znacznej zasadowości (pH≥9), a także przy współtowarzyszącej hematurii.
Wśród innych przyczyn należy wymienić przede wszystkim zanieczyszczenie
próbki pochodnymi amonowymi stosowanymi w środkach dezynfekcyjnych.
Fałszywie ujemne wyniki mogą występować przy silnym zakwaszeniu moczu
oraz przy intensywnym białkomoczu, związanym z wydalaniem białka Bence-
Jonesa.
9.6 Azotyny
Testy paskowe wykrywają obecność w moczu bakterii redukujących azotany do
azotynów. Bakterie Gram-ujemne przekształcają zawarte w moczu azotany (z
pokarmów) w azotyny. Wynik negatywny nie wyklucza infekcji bakteryjnej

55
(infekcje przez bakterie nie produkujące reduktazy lub dieta nie zawierająca
azotynów). Dodatni wynik powinien zostać potwierdzony poprzez wykonanie
mikroskopowego badania osadu moczu oraz posiewu badanego materiału.
Przyczyną fałszywie dodatnich wyników może być zbyt długie przechowywanie
moczu in vitro, prowadzące do namnożenia się bakterii. Leki zawierające
azotyny także mogą fałszować rezultat testu.
Na fałszywie ujemny wynik badania może mieć wpływ zbyt krótka inkubacja
moczu w pęcherzu, brak zdolności redukcyjnej bakterii (bakterie Gram-
dodatnie), wysokie stężenia kwasu askorbinowego.
9.7 Erytrocyty
Za pomocą testów paskowych można wykryć w moczu obecność barwników
hemowych lub hemoglobinę z wyługowanych erytrocytów. W zależności od
jednolitości lub punktowości zabarwienia pola testowego określamy rodzaj
erytrocytów (świeże, wyługowane). Erytrocyty świeże pojawiają się w moczu
przede wszystkim w przypadku zakażenia pęcherza i cewki moczowej, a
erytrocyty wyługowane w krwinkomoczach kłębuszkowych i krwawieniach z
górnego odcinka dróg moczowych. Ważnym uzupełnieniem wyniku testu
paskowego jest mikroskopowe badanie osadu moczu. Pozwala ono na
weryfikację uzyskanych rezultatów i jest pomocne w wykluczeniu mio- i
hemoglobinurii.
Przyczyną fałszywie dodatnich wyników może być obecność mioglobiny,
peroksydaz bakteryjnych (infekcje dróg moczowych), związków utleniających,
kwasu solnego oraz krwi menstruacyjnej.
Na fałszywie ujemny wynik badania może mieć wpływ podwyższony ciężar
właściwy moczu, wysokie stężenia białka, obecność kwasu askorbinowego,
kaptopril.
9.8 Leukocyty
Testy paskowe wykorzystują obecność esterazy indoksylowej w granulocytach i
makrofagach. Ze względu na fakt, iż wykrywany enzym nie występuje w
limfocytach, w przypadku limfoctyturii testy dają wynik fałszywie ujemny.
Testy wydają się mieć stosunkowo duże znaczenie, w porównaniu do
mikroskopowego badania osadu moczu, w przypadku zapalenia układu
moczowego u dzieci, gdzie z powodu małego ciężaru właściwego oraz częstego
odczynu zasadowego dochodzi czasami do lizy leukocytów.
56
Przyczyną fałszywie dodatnich wyników może być silna barwa moczu
(nitrofurantoina), substancje konserwujące (formaldehyd), związki utleniające,
kontaminacje z wydzieliną z pochwy.
Na fałszywie ujemny wynik badania może mieć wpływ spożycie kwasu
askorbinowego w ilości >1g/dzień, stężenie glukozy w moczu >20g/l, stężenie
białka w moczu >5g/l, wysoki ciężar właściwy, substancje konserwujące (kwas
borny), szczawiany, niektóre leki (tetracykliny, cefalosporyny, gentamycyna)
10. Wpływ na inne badania
Tabela 29 – Inne badania
Badania
hormonalne
Prolaktyna
Wzrost po Metoclopramidium (MCP)
Hormon
wzrostu
Spadek po podaniu 75 gramów glukozy po
2 godz. DTTG lub insuliny
TSH
Spadek po preparatach tyroksyny
Wazopresyna Adrenalina, kortyzol, steroidy płciowe
modulują jej wydzielanie
ACTH
i
kortyzol
Dekasmetazon obniża stężenie
fT3 i fT4
Wzrost
po
doustnych
środkach
antykoncepcyjnych
Morfologia
WBC, RBC,
PLT
Spadek po podaniu cytostatyków lub leków
immunosupresyjnych, metamizol sodowy
(Pyralgina)
może
wywoływać
osteomielofibrozę
OB
Spadek po stosowaniu azlocyliny
Serologia
BTA
Fałszywie
dodatni
przy
stosowaniu
amfoteryczny B, tadralazyny, butapirazolu,
cefalotyny,
ampicyliny,
chininy,
tolbutamidu
Chemia ogólna
Krew utajona
w kale
Fałszywie
dodatni
przy
stosowaniu
niesteroidowych leków przeciwzapalnych
(NLPZ)
–
kwas
acetylosalicylowy,
ibubrofen.

57
Podsumowanie
W niniejszym opracowaniu nie przedstawiono wszystkich możliwych interakcji
i interferencji. Zwrócono jedynie uwagę, na najczęściej spotykane w rutynowej
praktyce diagnosty w laboratorium.
Należy pamiętać, że wpływ leków na wyniki badań laboratoryjnych jest
indywidualny dla każdego pacjenta i zależy od rodzaju zastosowanego leku,
mechanizmu jego działania, dawki, drogi podania i czasu trwania terapii. W
przypadku niektórych leków wpływ na wyniki badań laboratoryjnych widoczny
jest wyłącznie podczas przyjmowania preparatu. W innych przypadkach
normalizacja parametrów laboratoryjnych może trwać nawet do kilu tygodni.
W celu uniknięcia błędnej interpretacji wyników badań laboratoryjnych
spowodowanej interferencją leków przyjmowanych przez Pacjenta, zaleca
się, aby informacja o rodzaju leku oraz jego dawce podana była na
skierowaniu do laboratorium.
Eliminacja błędnych wyników i/lub rozpoznanie interferencji zależy również od
prawidłowej współpracy Laboratorium z pozostałym personele
szpitala/przychodni (co jak uczy praktyka wygląda różnie, a nie zawsze dobrze).

58
Bibliografia
- Choroby wewnętrzne. Stan wiedzy na rok 2010, A. Szczeklik i wsp.
Medycyna Praktyczna Kraków 2010
-. Diagnostyka laboratoryjna z elementami biochemii klinicznej. Podręcznik dla
studentów medycyny. A. Dembińskiej – Kieć i J. W. Naskalskiego (red). Edra
Urban&Partner, Wrocław 2015
- Badania laboratoryjne w codziennej praktyce. Z. Jakubowski, J. Kabata, L.
Kalinowski. M. Szczepańska-Konkel, S. Angielski, Wyd. V, MakMed, Gdańsk
1998.
- Próbki: od pacjenta do laboratorium. W.G. Guder, S. Narayanan, H. Wissler,
B. Zawta. Wyd. I, MedPharm Polska 2009
- Farmakologia. Podstawy farmakoterapii, podręcznik dla studentów medycyny i
lekarzy. W. Kostowski i wsp. PZWL Warszawa 2001
- PHARMINDEX® BREVIER – podręczny indeks leków. Praca zbiorowa,
UBM Medica Polska, Warszawa 2011
- Wpływ leków na wyniki badań laboratoryjnych. Mrozikiewicz M., Ożarowski
M., Bogacz A., Karasiewicz M. Fundacja Wiener Lab, 2009
- Analiza środków psychoaktywnych w materiale biologicznym. Szykulski B.
Alkoholizm i Narkomania, Tom 14, Nr l, ss. 151-163
- Zalety i wady szybkich testów, czyli jak oznaczać narkotyki w laboratorium
medycznym? Gomółka E., Morawska A. diagnostyka laboratoryjna Journal of
Laboratory Diagnostics 2011 • Volume 47 • Number 2 • 197-203
- Wpływ spożywania alkoholu etylowego na wyniki badań laboratoryjnych. Lis
K. Alkoholizm i Narkomania 2009, Tom 22: nr 1, 65.73 © 2009 Instytut
Psychiatrii i Neurologii
- Biochemia Harpera. Murray RK, Grammer DK, Mayes PA, Rodwell VW,
PWZL Warszawa 2005
-Dziennik Ustaw nr 223 poz. 1794 z 2009. Rozporządzenie Ministra Zdrowia w
sprawie wymagań, jakim powinno odpowiadać medyczne laboratorium
diagnostyczne.

59
- Dziennik Ustaw nr 179 poz. 1485 z 2006. Ustawa o przeciwdziałaniu
narkomanii.
Wyszukiwarka
Podobne podstrony:
wpływ ksenobiotyków na wyniki badań laboratpryjnych
Co mowi Twoja krew Holistyczne spojrzenie na wyniki badan laboratoryjnych e 0iqt
Korzystny wp³yw suplementacji diety produktami na bazie soi na stężenie lipidów i czynniki ryzyka ch
Wpływ leków i innych związkow chemicznych na kwasy nukleinowe
Rumuński rynek suplementów diety Powrót na ścieżkę wzrostu w latach 2010 2012
Wyniki badań laboratoryjnych, Różne, Zdrowie, badania
Wpływ stosowania środków?rmakologicznych i suplementów diety na poprawienie wyniku sportowegox
04. Wpływ suplementów diety na urodę, Studium kosmetyczne, Chemia kosmetyczna
Wpływ suplementacji diety na masę urodzeniowa noworodka
Wpływ leków na wyniki oznaczeń markerów kardiologicznych(1)
wpływ leków na kwasy nukleinowe
(5) Wpływ leków na wchłanianie składników pokarmowyc h
Wpływ używek na organizm człowieka
wplyw leków na badania laboratoryjne, toksykologia
Wpływ leków Cytostatycznych na kwasy nukleinowe
Metody amortyzacji i ich wpływ na wyniki finansowe
10 Istota zjawiska refrakcji pionowej i jej wpływ na wyniki pomiarów niwelacji trygonometrycznej
więcej podobnych podstron