
Genetyka człowieka – choroby genetyczne
Genetyka człowieka zajmuje się badaniem biologicznej zmienności u
ludzi. Wiedza ta ma ogromne znaczenie kliniczne i umożliwia szybki
postęp w wykrywaniu i leczeniu chorób uwarunkowanych genetycznie.
Analizą chromosomów zajmuje się cytogenetyka, wykorzystując
właściwe techniki określa strukturę, kształt i liczbę chromosomów w
celu wykrycia anomalii chromosomowych*.
*Liczba chromosomów jest
stała i charakterystyczna dla danego gatunku, podobnie jak wielkość
chromosomów.W prawidłowej komórce somatycznej człowieka znajdują
się 23 pary chromosomów: 22 pary autosomów i jedna para
chromosomów płci.
Kariogram – zestaw chromosomów jednej komórki, sfotografowany i
uszeregowany według określonych zasad – chromosomy homologiczne
ułożone w pary od najmniejszego do największego**.
**Kariogram
typowy i reprezentatywny dla danego osobnika – to kariotyp..
Rozróżniamy pojęcia kariogram i kariotyp ze względu na mozaicyzm.
Mozaicyzm polega na tym, że badana osoba może mieć dwie lub więcej
linii komórkowych o różnym składzie chromosomowym, np.. Część
komórek prawidłowych i część z dodatkowym lub zmienionym
chromosomem (chromosomami).

Kariogram 46, XY – prawidłowy męski zestaw
chromosomów
Autosomy oznacza się liczbami arabskimi i dzieli się je w
zależności od wielkości i położenia centromeru na 7 grup
oznaczanych od A do G. Chromosomy płci oznacza się symbolami
X i Y.

Choroby genetyczne możemy podzielić na:
-jednogenowe – spowodowane mutacją w pojedynczym
genie, dziedziczą się zgodnie z prawem Mendla,gdy gen jest
umiejscowiony w jednym z autosomów, mówimy o
dziedziczeniu autosomalnym, gdy w chromosomie X – o
dziedziczeniu sprzężonym z płcią
- wieloczynnikowe – uwarunkowane są współdziałaniem
wielu genów (poligenów) oraz różnymi czynnikami
środowiska
Dziedziczenie jednogenowe (monogenowe)
Cechy uwarunkowane jednym genem dziedziczą się zgodnie z
prawem Mendla, mutacje takiego genu w znacznym stopniu
wpływają na zdrowie człowieka. Cecha ta może dziedziczyć się
w sposób dominujący lub recesywny. Sposób dziedziczenia
danej cechy można określić, przeprowadzając analizę
rodowodu na podstawie informacji uzyskanych z wywiadu
rodzinnego.
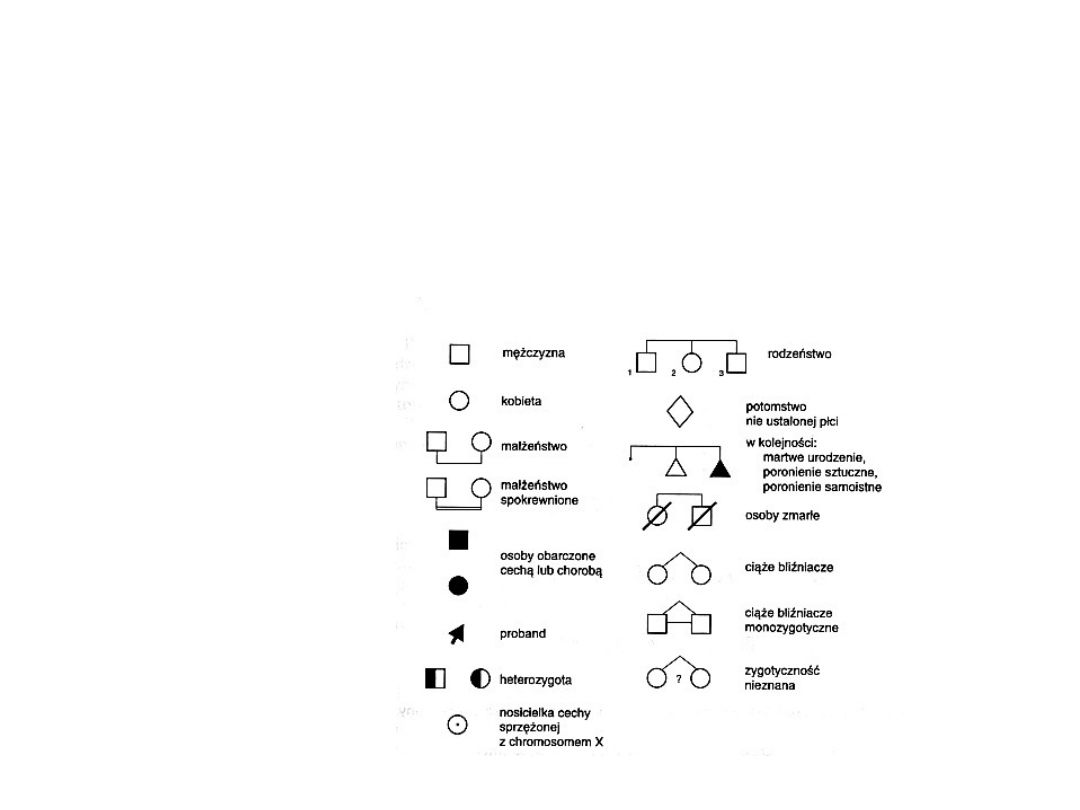
Symbole stosowane
w konstrukcji
rodowodów.
Pokolenia oznacza się
cyframi rzymskimi,
Osoby w danym
pokoleniu -
arabskimi
.
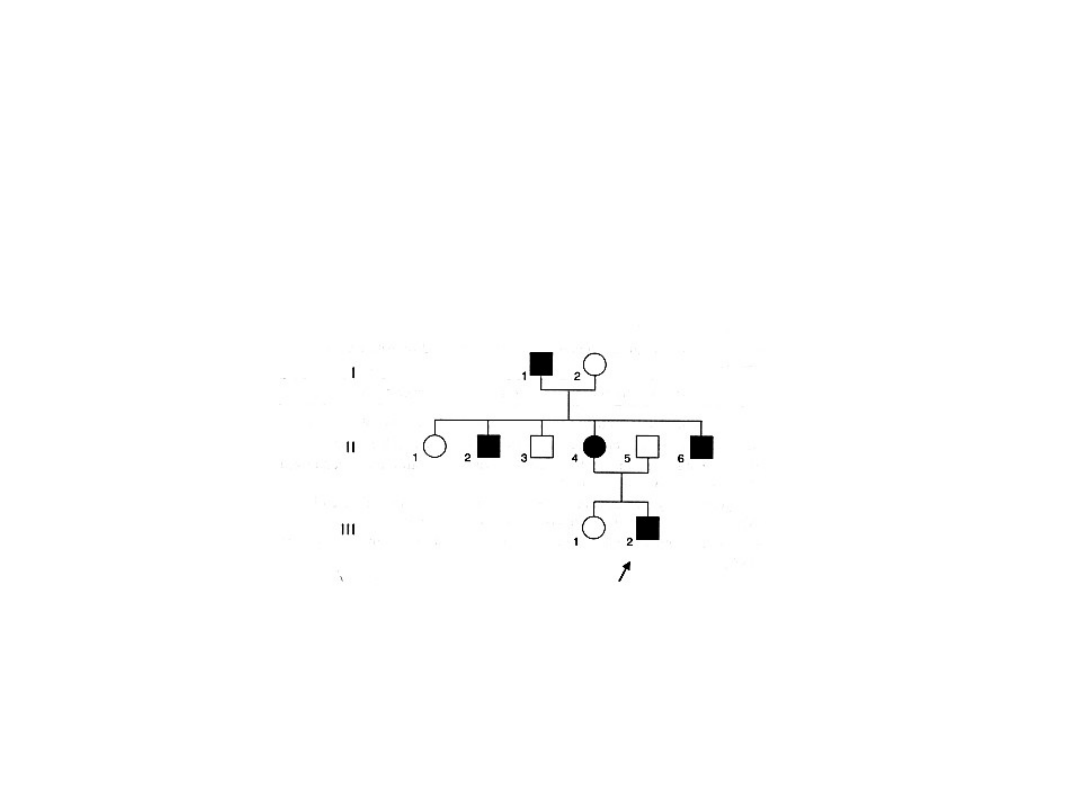
1/ Dziedziczenie chorób autosomalnych dominujących
Cechy dziedziczące się w sposób dominujący stanowią ponad
połowę opisanych dotychczas 4458 cech. Większość tych
chorób jest wynikiem świeżej mutacji i żadne z rodziców
chorego dziecka nie wykazuje objawów choroby. Jeśli
zmutowany gen jest odziedziczony od jednego z rodziców, to
rodzic ten jest zawsze (lub prawie zawsze) chory.
Rodowód ilustrujący autosomalny dominujący sposób
dziedziczenia

Cechy dziedziczenia autosomalnego dominującego:
-Ujawnianie się choroby u heterozygot. Stan
homozygotyczności dla genu dominującego występuje bardzo
rzadko; zazwyczaj jest to wtedy bardzo ciężka lub wręcz
śmiertelna postać choroby.
-Prawdopodobieństwo przekazania nieprawidłowego genu
potomstwu wynosi 50%.
-Duże ryzyko przekazania choroby jest stałe i nie zależy od
liczby posiadanych już zdrowych i / lub chorych dzieci

Do cech specyficznych występujących w chorobach
autosomalnych dominujących należą:
•Zmienna ekspresja* *
chorzy w tej samej rodzinie wykazują
różne nasilenie objawów choroby;
•Niepełna penetracja**
**cechy fenotypowe choroby mogą
być nieobecne, mimo że osoba jest nosicielem mutacji
genowej
;
•Mozaikowatość germinalna***
***obecność zmutowanych
genów tylko w części komórek gonad jednego z rodziców.
Efektem tego może być urodzenie się kolejnych chorych
dzieci z małżeństwa klinicznie zdrowych osób
.
Przykłady chorób autosomalnych dominujących:
1/rodzinna hipercholesterolemia
2/ choroba von Willebranda
3/wielotorbielowatość nerek u dorosłych,
4/ choroba Huntingtona
5/ dystrofia miotyczna
6/ polipowatość okrężnicy

2/ Dziedziczenie chorób autosomalnych recesywnych
Cechy dziedziczone w sposób recesywny stanowią 1/3 wszystkich
opisanych cech (obecnie 1730 cech).W dziedziczeniu
autosomalnym recesywnym choroba lub cecha ujawnia się tylko u
homozygot. Zmutowany allel recesywny nie ujawnia się w
obecności prawidłowego dominującego allela*.
*Szacuje się, że
każda zdrowa osoba jest nosicielem co najmniej kilku
zmutowanych alleli recesywnych, nie ujawniających się
fenotypowo. Wiele cech jest charakterystycznych dla chorób
dziedziczących się autosomalnie recesywnie.
Ponieważ choroby o tym typie dziedziczenia występują wśród
rodzeństwa, a bardzo rzadko u innych członków rodziny, mówimy
o „poziomym rozkładzie chorych” w rodowodach rodzin
obciążonych chorobami autosomalnymi recesywnymi.
W coraz liczniejszej grupie chorób heterozygoty mogą być
identyfikowane na podstawie specjalistycznych testów
diagnostycznych.
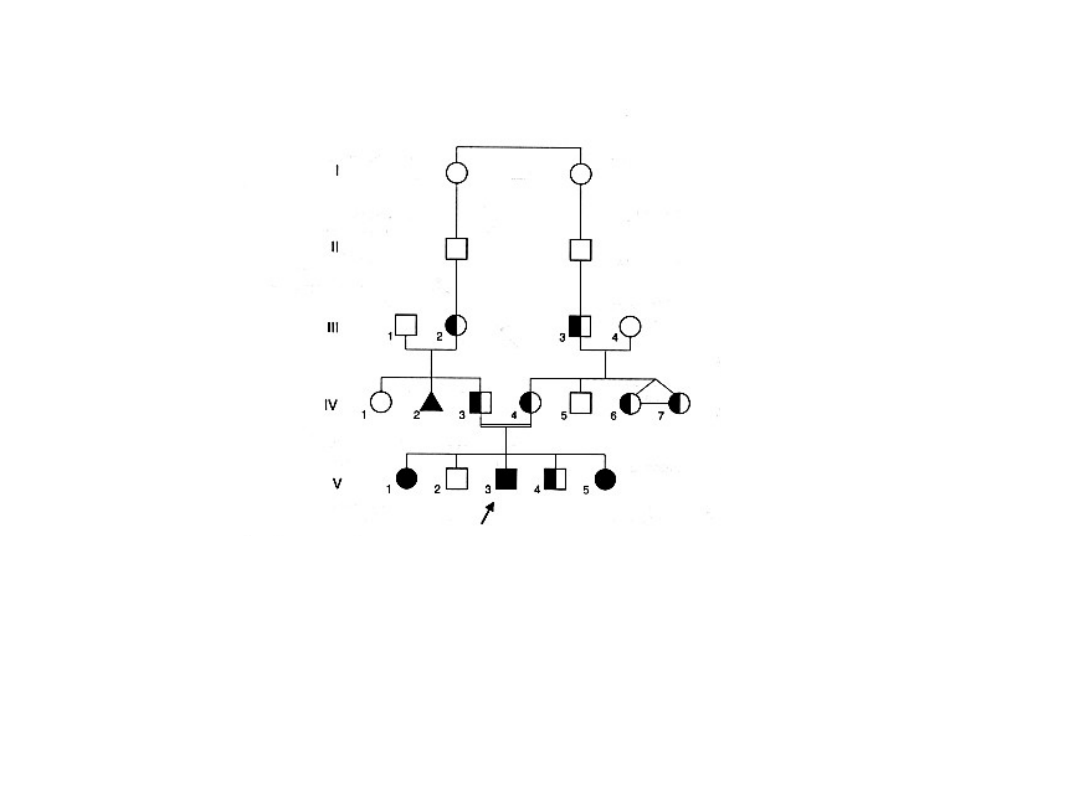
Rodowód ilustrujący sposób dziedziczenia autosomalny
recesywny

Cechy dziedziczenia autosomalnego recesywnego:
-Objawy choroby ujawniają się u osób obojga płci
-Oboje rodzice chorego dziecka są bezobjawowymi klinicznie
heterozygotami (nosicielami) pod względem zmutowanego genu
-Ryzyko ponownego urodzenia chorego dziecka jest zawsze duże i
wynosi 1 : 4 (25%).Jest ono stałe, niezależne od liczby posiadanych
już przez to małżeństwo zdrowych i / lub chorych dzieci
-Prawdopodobieństwo, że każde ze zdrowego rodzeństwa chorego
dziecka jest heterozygotą ( nosicielem mutacji) wynosi 2 :3.
-Jeśli choroba (lub cecha) występuje w populacji rzadko, istnieje
duże prawdopodobieństwo pokrewieństwa między rodzicami
chorego**.
-Osoba chora może być nosicielem dwóch różnych mutacji w danym
locus genowym
-Wszystkie dzieci osoby chorej będą nosicielami mutacji genowej
(heterozygotami)
**W niektórych lokalnych populacjach częstość alleli
recesywnych jest wyższa z uwagi na tzw. efekt założyciela.
Przykłady chorób recesywnych występujących częściej w
określonych grupach etnicznych:
Choroba
Grupa etniczna
Anemia sierpowata
Murzyni amerykańscy i afrykańscy; Hindusi
azjatyccy; mieszkańcy basenu Morza
Śródziemnego (szczególnie Grecy) populacje
Środkowego Wschodu
-talasemia
Mieszkańcy basenu Morza Śródziemnego
Tajowie; populacje Bliskiego Wschodu; Hindusi;
Chińczycy
Choroba Taya-Sachsa
Żydzi aszkenazyjscy; Kanadyjczycy pochodzenia
francuskiego
Choroba Gauchera
Żydzi aszkenazyjscy
Zespół Blooma
Żydzi aszkenazyjscy
Zespół nadnerczycowo-płciowy
Eskimosi
Ciężki złożony defekt odporności
Indianie Apacze
Mukowiscydoza
Europejczycy
Albinizm
Indianie Hopi
Fenyloketonuria
Europejczycy
Wrodzony przerost nadnerczy
Eskimosi
Nerczyca wrodzona
Finowie
Brak dehydrogenazy glukozo-6-
fosforanowej
Chińczycy; Afrykańczycy

3/ Dziedziczenie chorób recesywnych sprzężonych z chromosomem X
Do tej pory poznano 412 cech recesywnych sprzężonych z chromosomem X.
Cechy charakterystyczne dla dziedziczenia recesywnego sprzężonego
z chromosomem X :
-Tylko mężczyźni (nosiciele mutacji genowej) wykazują objawy choroby.
-Kobiety, nosicielki mutacji genowej, w zasadzie nie wykazują cech choroby.
-Heterozygotyczne kobiety maja 50% szansę przekazania zmutowanego
genu swemu potomstwu, zarówno synom, jak i córkom.
-Hemizygotyczny chory mężczyzna przekazuje zmutowany gen wszystkim
córkom, lecz nigdy synom. Wszystkie więc jego córki będą nosicielkami
mutacji.
-Częstość występowania mutacji genowej wśród kobiet jest dwukrotnie
większa niż wśród mężczyzn.
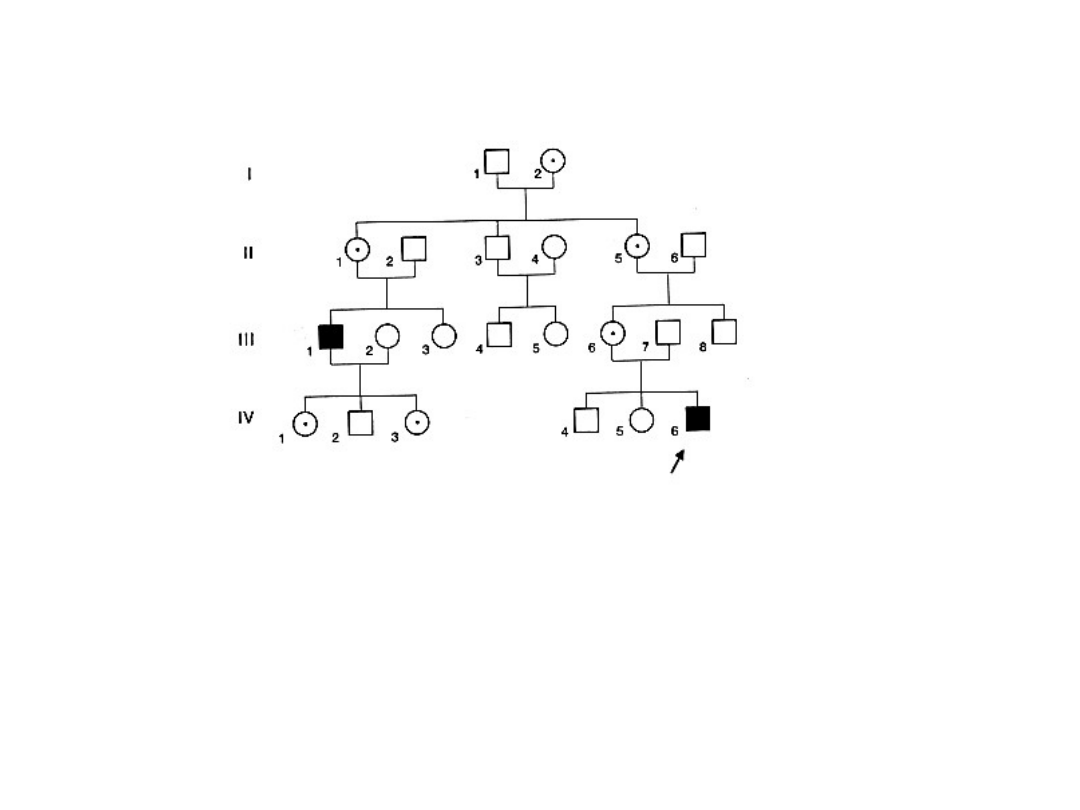
Rodowód ilustrujący sposób dziedziczenia recesywny sprzężony z
chromosomem X

Przykłady chorób recesywnych sprzężonych z chromosomem X:
1/ daltonizm – ślepota na barwę czerwoną i zieloną,
2/ dystrofia mięśniowa Duchenne’a (DMD)*,
3/dystrofia mięśniowa Beckera’,
4/ hemofilia A,
5/ hemofilia B,
6/ rybia łuska sprzężona z chromosomem X,
7/ zespół kruchego (łamliwego) chromosomu X

Dystrofia mięśniowa Duchenne’a jest przykładem choroby recesywnej
sprzężonej z płcią, objawia się zanikiem mięśni już w dzieciństwie,
ok.. 10 roku życia dziecko przestaje chodzić, z powodu niewydolności
sercowej i oddechowej następuje śmierć przed 20 rokiem życia.
Kobieta będąca nosicielką jest zwykle zdrowa, ponieważ w wyniku
inaktywacji jednego chromosomu X w części komórek dochodzi do
wyłączenia zmutowanego allelu. Objawy dystrofii mięśniowej
sprzężonej z X mogą wystąpić u kobiet w przypadku:
-nietypowej inaktywacji X, gdy w większości komórek mięśniowych
zinaktywowany jest prawidłowy chromosom X, jednak objawy są
łagodniejsze niż u chorych mężczyzn,
-Nowej mutacji na drugim chromosomie X u nosicielki, może zdarzyć
się nowa mutacja w tym locus na drugim „zdrowym” chromosomie X,
objawy są równie ciężkie, jak u chorych mężczyzn,
-Zespołu Turnera, nie może w tym przypadku dojść do inaktywacji
chromosomu ze zmutowanym allelem, choroba ujawnia się w takim
samym stopniu, jak u mężczyzn,
-Translokacji chromosomu X z mutacją na autosom, preferencyjnie
inaktywowany jest wówczas normalny chromosom X, ponieważ
inaktywacja chromosomu z translokacją (X-autosom) spowodowałaby
monosomię autosomu.

4/ Dziedziczenie chorób dominujących sprzężonych z chromosomem
X
W patologii człowieka choroby dominujące sprzężone z chromosomem X
występują rzadko.
Cechy charakterystyczne dla dziedziczenia dominującego
sprzężonego z chromosomem X:
-Zarówno mężczyźni, jak i kobiety , nosiciele zmutowanego genu
umiejscowionego w chromosomie X, wykazują objawy choroby.
-Chorzy mężczyźni są hemizygotami (maja jeden chromosom X), natomiast
chore kobiety mają prawidłowy allel na drugim chromosomie, więc choroba
u mężczyzn ma znacznie cięższy przebieg i często jest śmiertelna.
-Heterozygotyczne kobiety mają 50% szansę przekazania zmutowanego
genu zarówno córce, jak i synowi.
-Hemizygotyczni chorzy mężczyźni przekazują zmutowany gen wszystkim
córkom, nigdy synom.
-Częstość występowania mutacji genowej wśród kobiet jest dwukrotnie
większa niż wśród mężczyzn.
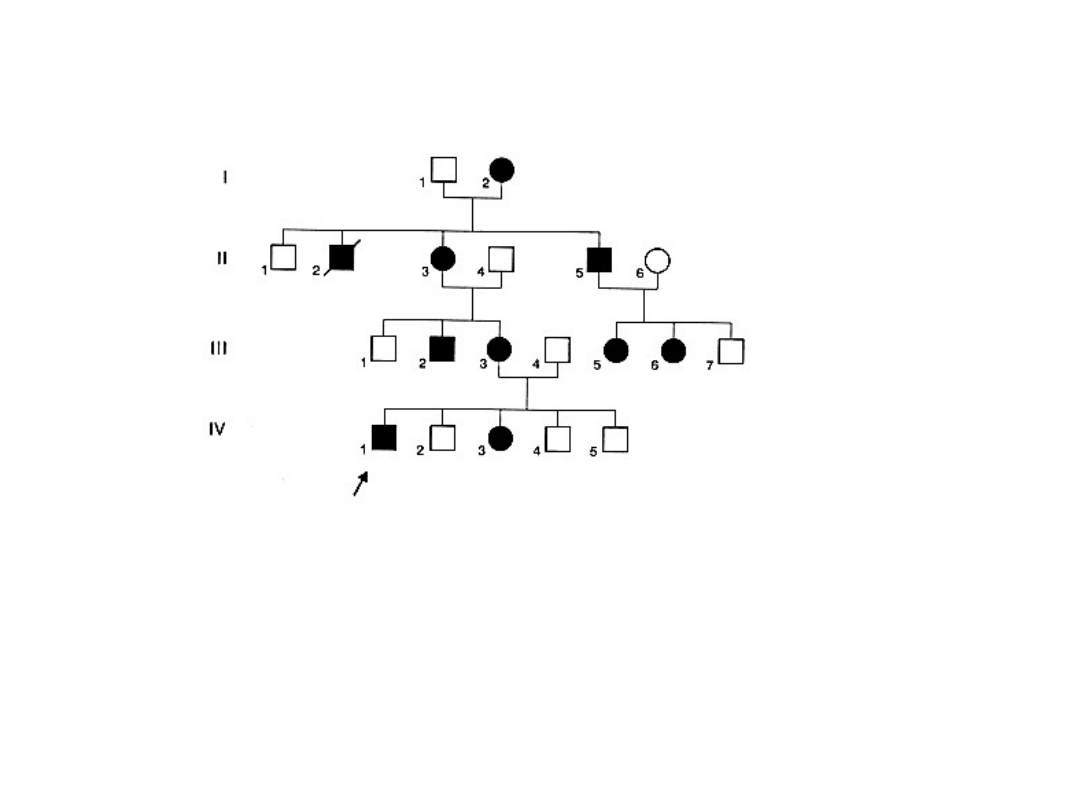
Rodowód ilustrujący sposób dziedziczenia dominujący sprzężony z
chromosomem X

Przykłady chorób dominujących sprzężonych z chromosomem X:
1/ krzywica oporna na witaminę D,
2/ grupa krwi X
g
,
3/ dziedziczna odmiana neuropatii ruchowej i czuciowej,
4/ zespół Retta,
5/ incontinentica pigmenti (nietrzymanie barwnika).
W przypadku zespołu Retta i nietrzymania barwnika uszkodzenia u
płci męskiej są tak poważne, że prowadzą do samoistnych poronień,
dlatego chorobę stwierdza się tylko u heterozygotycznych
dziewczynek.

Dziedziczenie wieloczynnikowe
Wśród chorób uwarunkowanych genetycznie, w których
etiologii istotną rolę odgrywają zarówno predyspozycja
genetyczna, jak i czynniki środowiskowe, najliczniejsze są
choroby dziedziczone wieloczynnikowo (poligenowe).
Predyspozycja genetyczna jest uwarunkowana istnieniem
zmienności genowej i zależy nie od jednego, ale od licznych
genów. Istnieje wiele cech, takich jak wzrost, masa ciała,
inteligencja czy ciśnienie krwi, determinowanych wielogenowo.
Wszystkie te cechy wykazują zarówno zmienność populacyjną,
jak i wewnątrzrodzinną. Istotne znaczenie dla kształtowania się
wymienionych cech mają też czynniki środowiskowe. Podobnie
jest ze skłonnością do ujawniania się pewnych chorób i wad
wrodzonych*.
*Wykazując zmienność populacyjną, skłonność
sama przez się nie decyduje o wystąpieniu choroby czy wady.
Dopiero współdziałanie określonych czynników środowiskowych
z dużą predyspozycją genetyczną może się przejawić
wystąpieniem objawów choroby lub wadą.
Dowodów na istnienie genetycznej predyspozycji dostarczają
wyniki badań rodzinnych oraz badań bliźniąt. Jeśli w badaniach
bliźniąt stwierdza się, że choroba w dużym stopniu jest
uwarunkowana genetycznie, a u jej podstaw nie leży zmiana
pojedynczego genu (lub aberracja chromosomowa), to z dużym
prawdopodobieństwem można przyjąć, że ujawnienie się
choroby lub wady zależy od wielu loci genowych, kształtujących
skłonność do niej.

cd.* Skłonność ta, jest z kolei „wyzwalana” przez działanie czynników
środowiskowych i ujawnia się w postaci choroby. Im czynnik
(czynniki) środowiskowy jest silniejszy, tym u większej liczby osób
(także tych z mniejszą skłonnością) ujawnią się objawy choroby.
Występowanie choroby uwarunkowanej wieloczynnikowo jest więc
biologicznym dowodem istnienia w rodzinie zwiększonej predyspozycji
do danego schorzenia.Zostało to udokumentowane empirycznie
wynikami badań rodzinnych dotyczących wielu chorób i wad, takich
jak: wrodzone zwichnięcie stawów biodrowych, rozszczep wargi i / lub
podniebienia, izolowane wady serca, wady cewy nerwowej, zwężenie
odźwiernika, atopia, wrzód trawienny żołądka, padaczka, nadciśnienie
samoistne,choroby alergiczne, reumatoidalne zapaleni stawów itp..
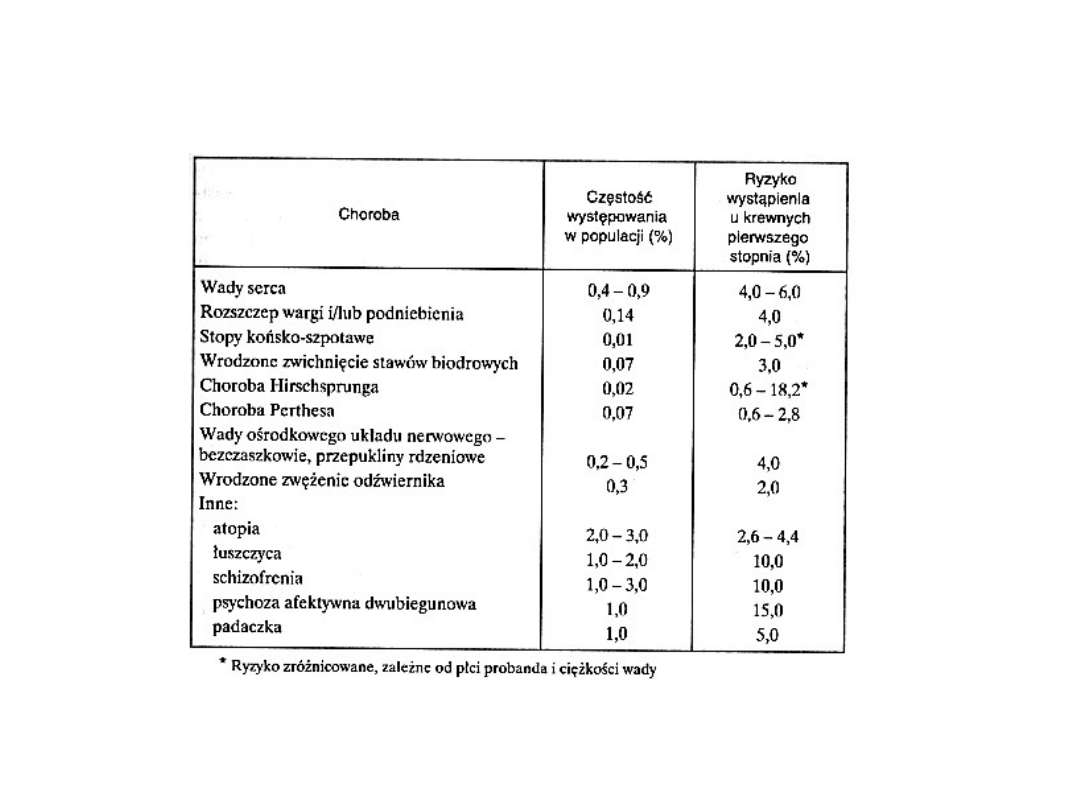
Szacunkowa częstość występowania niektórych chorób
wieloczynnikowych
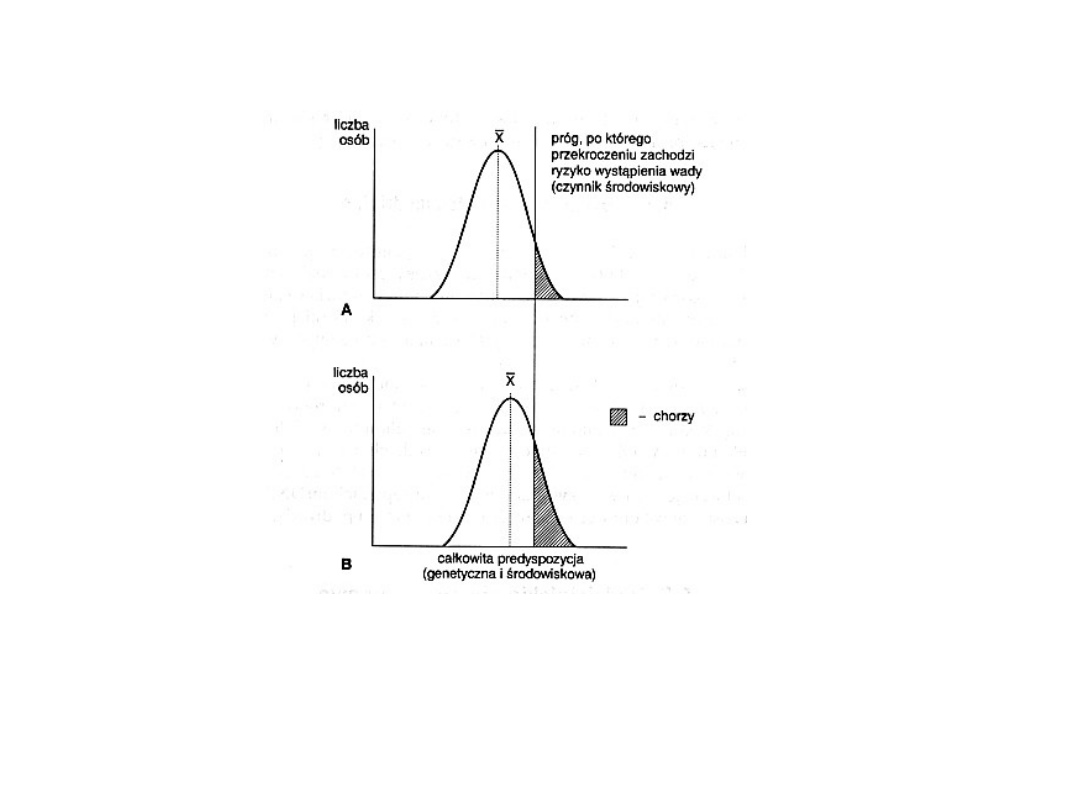
Model dziedziczenia
wieloczynnikowego. A – dla
populacji, B – dla krewnych
pierwszego stopnia osób chorych

Z punktu widzenia potrzeb poradnictwa genetycznego kierowanego
do rodzin obarczonych chorobami uwarunkowanymi wieloczynnikowo
należy pamiętać, że:
•Najważniejsze jest ustalenie prawidłowego rozpoznania choroby i
potwierdzenie jej wieloczynnikowego charakteru
•Wrodzone wady rozwojowe uwarunkowane wieloczynnikowo są
wadami izolowanymi.
•Ryzyko ponownego urodzenia dziecka z wadą wrodzoną lub chorobą
uwarunkowaną wieloczynnikowo, choć wielokrotnie większe od
populacyjnego, jest zazwyczaj małe (do 5%).
•Częstość występowania pewnych wad wieloczynnikowych wykazuje
zróżnicowanie populacyjne.
•Poznanie czynników środowiskowych mających wpływ na
występowanie określonych chorób lub wad umożliwia prowadzenie
programów profilaktyki pierwotnej (np. stosowanie kwasu foliowego
w okresie przedkoncepcyjnym jako profilaktyka wrodzonych wad
cewy nerwowej).

Dziedziczenie mitochondrialne
Przykładem dziedziczenia , w którym informacja genetyczna jest
przekazywana wyłącznie od matki (dziedziczenie matczyne) jest
dziedziczenie mitochondrialne. Rozwijający się zarodek
otrzymuje mitochondria wyłącznie od matki, ponieważ stanowią
one składnik cytoplazmy komórki jajowej. Do niej, po
zapłodnieniu, plemnik wnosi jedynie materiał genetyczny
zawarty w jego jądrze.
Do podstawowych cech dziedziczenia mitochondrialnego można
zaliczyć specyficzność tkankową i nasilanie się objawów
chorobowych wraz z wiekiem*.
*W komórce znajduje się
kilkaset mitochodriów i kilka tysięcy cząsteczek mtDNA. Objawy
kliniczne niektórych chorób mitochondrialnych ujawniają się
dopiero, gdy około 85% cząsteczek mtDNA zawiera zmutowaną
sekwencję. Jest więc kwestią czasu (rund replikacji mtDNA),
kiedy taki stan zostanie w komórce osiągnięty.

Rodzicielskie piętno genomowe
Równocenność informacji genetycznej otrzymywanej od matki i od
ojca poza różnicami dotyczącymi chromosomów płci, do niedawna nie
była kwestionowana. Uważano również, że w przypadku dowolnej
mutacji jej skutki fenotypowe są niezależne od tego, od którego z
rodziców została odziedziczona.
Okazało się jednak, że do prawidłowego rozwoju organizmu ważne
jest, aby określona informacja genetyczna była ojcowskiego, a inna
matczynego pochodzenia. Zjawisko różnej ekspresji genów,
zależnej od ich pochodzenia rodzicielskiego, zostało nazwane
piętnowaniem genomowym. Piętnowanie dotyczy określonych
genów lub fragmentów chromosomów*.
*Jak się wydaje, jest
mechanizmem genetycznym regulującym ekspresję genów
zaangażowanych w procesie różnicowania i rozwoju zarodka. Wzór
piętna genomowego może ulec zmianie w wyniku mutacji w
regionach regulatorowych piętnowanych genów. Mechanizmem
molekularnym ujawniającym, które geny, fragmenty chromosomów,
podlegają piętnowaniu, może być powstawanie delecji fragmentu
DNA na jednym z rodzicielskich chromosomów lub rodzicielskiej
disomii (dziedziczenie obu kopii genetycznego locus od jednego z
rodziców). Mechanizm piętnowania genomowego nie jest jeszcze w
pełni znany. Przyjmuje się, że inaktywacja genów jest związana z
metylacją ich fragmentów regulatorowych. Jedną z funkcji
piętnowania genomowego może być zapobieganie
homozygotyczności, np.partenogenezie. Udane próby klonowania
zwierząt dowodzą jednak, że bariery narzucane przez piętnowanie
mogą być eksperymentalnie przezwyciężane.

Priony
Choroby wywoływane przez priony charakteryzują się zmianami
degeneracyjnymi w obrębie ośrodkowego układu nerwowego. Ze
względu na widoczne ubytki w tkance mózgowej często są
określane jako encefalopatie gąbczaste. Przyczyną chorób jest
defekt w glikoproteinie błonowej występującej głównie w tkance
nerwowej, tzw. białku prionowym. Choroby wywołane przez
priony są równocześnie zakaźne i dziedziczne.
Dziedziczne postacie chorób prionowych stanowią około 10-15%
wszystkich zachorowań tego typu i wywołane są mutacjami w
genie PRNP*.
*Gen ten jest umiejscowiony w chromosomie 20 o
koduje białko o wysoce konserwatywnej strukturze, złożone z
około 250 aminokwasów. Funkcja białka nie jest znana. Sugeruje
się jedynie jego udział w stabilizacji komórek mózgowych oraz w
regulacji rytmu snu i czuwania. Wydaje się, że przejście białka
kodowanego w genie PRNP w formę prionu wiąże się głównie ze
zmianą jego konformacji. Zmiana ta nie musi być koniecznie
wynikiem mutacji.

cd.* Cechą białka prionowego jest przekształcenie, na swoje
podobieństwo, białek powstałych w wyniku ekspresji genu PRNP.
Mamy tu więc do czynienia ze swoistym efektem domina. Wystarczy
pojedyncza cząsteczka prionu, aby pozostałe białka PRNP przyjęły z
czasem konformację prionu. Nie wiadomo, w jaki sposób priony
powodują uszkodzenie mózgu. Obserwuje się jedynie ich
formowanie i odkładanie w postaci płytek, podobnie jak w chorobie
Alzheimera.
Opisano cztery choroby prionowe człowieka: kuru, chorobę
Creutzfeldta – Jakoba (CJD), zespół Gerstmanna – Stausslera –
Scheinkera i śmiertelną rodzinną bezsenność. Są to choroby
występujące niezwykle rzadko**.
**Kuru stwierdzono jedynie w
Nowej Gwinei. Jej „poziome” przekazywanie wśród członków
plemienia Fore kojarzone jest z rytualnym kanibalizmem. CJD
występuje z częstością 1 na milion. Większą częstość zachorowań
stwierdza się jedynie wśród Żydów libijskich. Znany jest natomiast
we Francji przypadek nieumyślnego przeniesienia tej choroby na
dzieci leczone hormonem wzrostu otrzymanym z przysadek
mózgowych osób zmarłych na CJD. Zespół Gerstmana – Stausslera –
Scheimkera zidentyfikowano w kilkudziesięciu rodzinach na
świecie, a śmiertelną dziedziczną bezsenność w kilku. Wszystkie
choroby prionowe dziedziczą się w sposób dominujący. Są
nieuleczalne.

Choroby prionowe występują również u zwierząt***.
***Najwcześniej opisaną chorobą (1732 r. ) jest scrapie
występujące u owiec i kóz. Zakażenia między gatunkowe są tym
łatwiejsze, im większe jest podobieństwo w sekwencji
aminokwasów białka prionowego.
Na przełomie lat 80/90 ubiegłego wieku w Wielkiej Brytanii
stwierdzono kilkanaście przypadków zachorowań na nowy,
nieznany do tej pory, wariant choroby CJD. Uważa się, że jest on
ludzką odmianą tzw. choroby wściekłych krów (BSE) i został
przeniesiony na człowieka w wyniku spożywania mięsa
(przetworów mięsnych) krów z BSE. Przypadki BSE wykryto w
wielu krajach europejskich. Choroba wściekłych krów jest
chorobą prionową. Źródła zachorowań poszukuje się w
skarmianiu bydła mączką mięsno-kostną wytwarzaną między
innymi z owiec chorych na scrapie. Zaskoczeniem było
pokonanie bariery międzygatunkowej przez niewielkie, jak się
sądzi dawki prionów.
Badanie i poznanie chorób prionowych oraz ewentualnych
czynników sprzyjających ich powstawaniu jest metodycznie
trudne i wyników nie można się spodziewać zbyt szybko.

Diagnostyka i leczenie chorób dziedzicznych
Cały czas trwają intensywne prace badawcze w celu wyjaśnienia
podłoża genetycznego wielu chorób dziedzicznych, szczególnie trudne
jest to w przypadku chorób uwarunkowanych zmianami w kilku
genach. Obecnie potrafimy rozpoznać już niektóre choroby, co
umożliwia postawienie prawidłowej diagnozy i udzielenie porady
genetycznej rodzinie obciążonej danym schorzeniem. W Polsce istnieje
sieć ośrodków naukowo-badawczych, które świadczą usługi w zakresie
diagnostyki chorób genetycznych i poradnictwa genetycznego.
Diagnostyka prenatalna pozwala na rozpoznanie chorób
genetycznych u płodu, co umożliwia właściwe postępowanie w czasie
ciąży i tuż po urodzeniu dziecka z wadami*.
*Badania prenatalne
wykonuje się we wczesnym okresie ciąży, biopsję kosmówki ok.. 9
tygodnia, a amniocentezę ok. 12-15 tygodnia. Badanie takie pozwala
na:
-ocenę płci płodu (test chromatyny płciowej),
-ocenę kariotypu (wykrywanie aberracji chromosomowych liczbowych i
strukturalnych),
-badanie stężenia enzymów w tkankach płodu ( wykrywanie chorób
metabolicznych),
-biochemiczne badanie płynu owodniowego (wykrywanie wady cewy
nerwowej),
-analizę DNA płodu (wykrywanie chorób monogenowych).

Diagnostyka preimplantacyjna pozwala na wprowadzenie
podczas zapłodnienia in vitro normalnego embrionu
nieobciążonego defektem genetycznym. Metodę tę
zastosowano po raz pierwszy w Belgii, w przypadku gdy
oboje rodzice byli nosicielami mukowiscydozy.
Leczenie chorób genetycznych polega na leczeniu objawowym,
ponieważ obecnie nie potrafimy jeszcze leczyć przyczyn tych
zaburzeń**.
**W celu poprawienia fenotypu możemy stosować:
a) podawanie leków, np.. Blokerów
-adrenergicznych,
zapobiegających powstawaniu tętniaka w zespole Marfana,
b) leczenie substytucyjne, np.. Podawanie hormonu wzrostu
osobom z niedoborem wzrostu, podawanie czynnika VIII w
hemofilii,
c) transplantację narządów,
d) rehabilikację, np.. W zespole Downa,
e) korekty chirurgiczne przy rozszczepie wargi i podniebienia,
f)
leczenie dietą, np.. Choroby metaboliczne – fenyloketonuria,
g) terapię genową komórek somatycznych i rozrodczych
Rozwój technologii umożliwia medycynie prowadzenie badań
genetycznych już w bardzo wczesnych etapach rozwoju
człowieka.

Zadanie1. Uzupełnij zdania:
1. Człowiek ma ..
pary autosomów i jedną parę
chromosomów
.... .....
.
2. Liczba chromosomów jest ..
.....
i charakterystyczna dla danego
gatunku, podobnie jak ich ..
.
3. Mężczyzna daltonista musiał otrzymać uszkodzony gen od .
...........
, ponieważ jest to cecha sprzężona z chromosomem ...
........
4. .
...........
spowodowana jest brakiem enzymu rozkładającego
fenuloalaninę.
5. Anemia sierpowata jest chorobą ....
......
...., a dystrofia
Duchenne’a ...
..................
.
Zadanie 2.
Choroba autosomalna recesywna ujawnia się tylko u:
a) homozygot z jednakową częstością u obu płci
b) tylko u jednej płci
c) Heterozygot z jednakową częstością u obu płci

Zadanie 3.
U ssaków choroby mitochondrialne dziedziczą się po linii .
.......
i
dotyczą głównie tkanek wykazujących duże zapotrzebowanie
na...
..........
Zadanie 4.
Choroby uwarunkowane jednym genem dziedziczą się:
a) zgodnie z prawem Mendla
b) czasem występują odstępstwa od prawa Mendla wynikające
ze zmniejszonej penetracji
c) niezgodnie z regułami genetyki mendlowskiej
Zadanie 5.
Choroby wieloczynnikowe to:
a) takie, w których etiologii istotną rolę odgrywają liczne geny
b) takie, w których etiologii istotną rolę odgrywają liczne geny i
czynniki środowiskowe
c) takie, w których etiologii istotną rolę odgrywa jeden gen

Zadanie 6.
W przypadku chorób uwarunkowanych wieloczynnikowo ryzyko urodzenia
dziecka z wadą wrodzoną dla krewnych pierwszego stopnia osób
chorych jest:
a) wielokrotnie większe od populacyjnego /prawidłowa /
b) równie duże jak dla populacji /nieprawidłowa /
c) trudne do określenia /nieprawidłowa /
Zadanie 7.
Zjawisko różnej ekspresji genów, zależnej od ich pochodzenia rodzicielskiego
(matczynego i /lub ojcowskiego) to:
a) dziedziczenie pozajądrowe /nieprawidłowa /
b) dziedziczenie mitochondrialne /nieprawidłowa /
c) rodzicielskie piętno genomowe /prawidłowa /
Zadanie 8.
Choroby wywołane przez priony mają charakter:
a)tylko dziedziczny/nieprawidłowa /
b)zakaźny /nieprawidłowa /
c)równocześnie zakaźny i dziedziczny /prawidłowa /

Zadanie 9.
Diagnostyka ..
prenatalna
.....pozwala na wykrycie niektórych zaburzeń
genetycznych już w czasie ciąży, natomiast
diagnostyka.....
preimplantacyjna
.......może towarzyszyć zapłodnieniu in
vitro u par obciążonych genetycznie.
Zadanie 10.
Objawy choroby dziedzicznej o charakterze autosomalnym dominującym
ujawniają się u:
a)homozygot pod względem zmutowanego genu / nieprawidłowa /
b)heterozygot /prawidłowa/
c)zarówno u homozygot, jak i heterozygot / nieprawidłowa /
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
Wyszukiwarka
Podobne podstrony:
CZLOWIEK I CHOROBA – PODSTAWOWE REAKCJE NA
Człowiek Choroby
CZLOWIEK I CHOROBA – PODSTAWOWE REAKCJE NA
4 Charakterystyka chorób genetycznych człowieka
Choroby genetyczne człowiekai ich diagnostyka Biologia
Choroby genetyczne czlowieka 2
Choroby genetyczne człowiekai ich diagnostyka Biologia
318 choroby genetyczne czlowiek Nieznany
Choroby genetyczne czlowieka
19101-choroby genetyczne człowieka(2), semestr IV, genetyka, Genetyka
Choroby Genetyczne człowieka
Choroby genetyczne u człowieka spowodowane są mutacjami
Choroby genetyczne człowieka, SZKOŁA, Biologia
BIOLOGIA Choroby genetyczne człowieka
Choroby genetyczne człowieka wynikajAce z mutacji chromosomowych strukturalnych
Choroby genetyczne u człowieka
więcej podobnych podstron