
REAKCJE ALIFATYCZNYCH
NASYCONYCH KWASÓW
KARBOKSYLOWYCH

REAKCJE ALIFATYCZNYCH
NASYCONYCH KWASÓW
KARBOKSYLOWYCH Z:
1)
metalami, tlenkami metali, wodorotlenkami
2)
solami kwasu węglowego
3)
nadtlenkiem wodoru
4)
alkoholami
5)
amoniakiem, aminami I-rzędowymi i II-
rzędowymi
6)
dekarboksylacja α- i β-ketokwasów, kwasów
1,1-dikarboksylowych, otrzymywanie metanu
7)
reakcja Hunsdieckera i anodowe utlenianie
kwasów karboksylowych.

REAKCJE Z METALAMI, TLANKAMI
METALI I WODOROTLENKAMI
W reakcjach kwasów karboksylowych z
metalami, tlenkami metali i
wodorotlenkami powstają SOLE
.

z metalami
z tlenkami metali
2 HCOOH+CaO →
(
HCOO
)
2Ca+ H2O
z wodorotlenkami
CH 3COOH +KOH→CH 3COOK+H 2O
octan sodu
mrówczan wapnia
octan potasu

SOLE WSZYSTKICH KWASÓW KARBOKSYLOWYCH W
ROZTWORACH WODNYCH ULEGAJĄ HYDROLIZIE
KWASY DIKARBOKSYLOWE TWORZĄ SOLE
OBOJĘTNE I WODOROSOLE
SOLE WYŻSZYCH KWASÓW KARBOKSYLOWYCH
(TŁUSZCZOWYCH) OKREŚLANE SĄ POTOCZNIE JAKO
MYDŁA, Z KTÓRYCH W WODZIE ROZPUSZCZAJĄ SIĘ
TYLKO MYDŁA SODOWE I POTASOWE
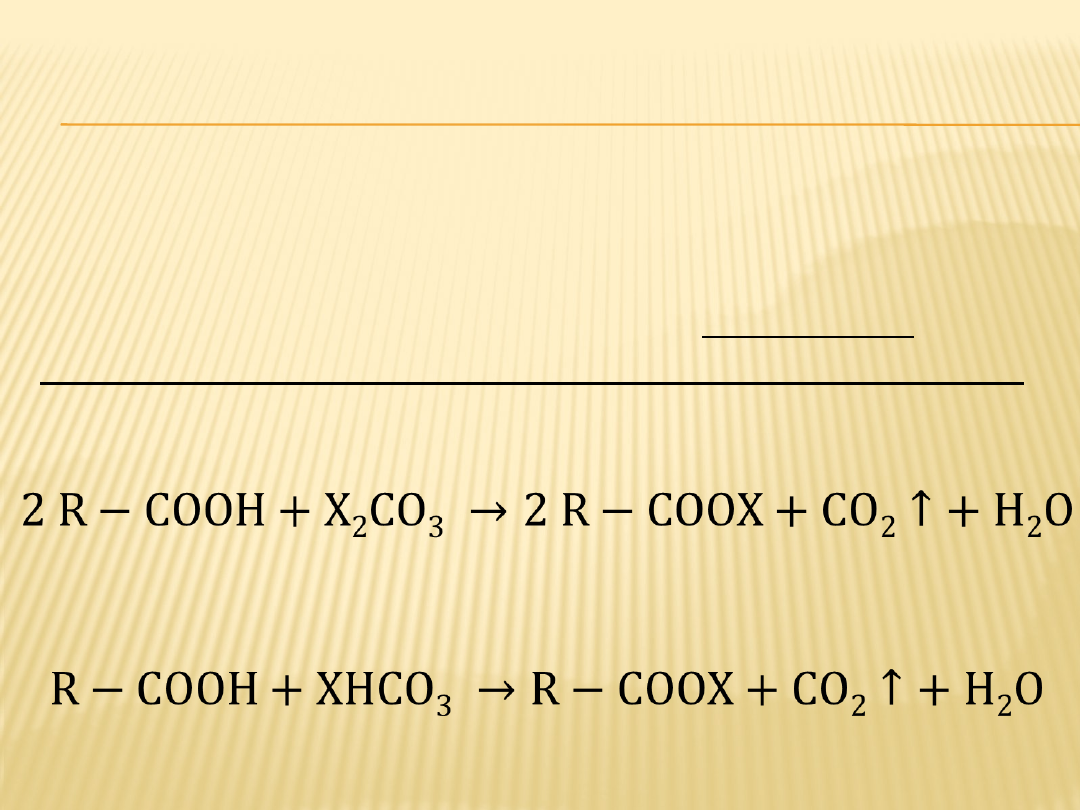
REAKCJE Z SOLAMI KWASU
WĘGLOWEGO
Reakcje kwasów karboksylowych z solami kwasu
węglowego zachodzą na zasadzie wypierania
kwasu słabszego przez kwas mocniejszy z jego soli
.
R−COOH + XHCO3→ R−COOX +CO 2↑+H 2O
2 R−COOH+X 2CO3→2 R−COOX+CO 2↑+H 2O

Kwas octowy jest mocniejszy od kwasu
węglowego, ponieważ wypiera CO
2
z jego
soli.
W reakcjach tego typu powstają SOLE.
CH 3COOH +NaHCO3→CH3 COONa+CO2↑+H 2O

REAKCJE Z NADTLENKIEM WODORU
Ze względu na odporność grupy –COOH na
działanie silnych utleniaczy reakcja utleniania
w przypadku kwasów karboksylowych nie
zachodzi.
Jednakże pod wpływem H
2
O
2
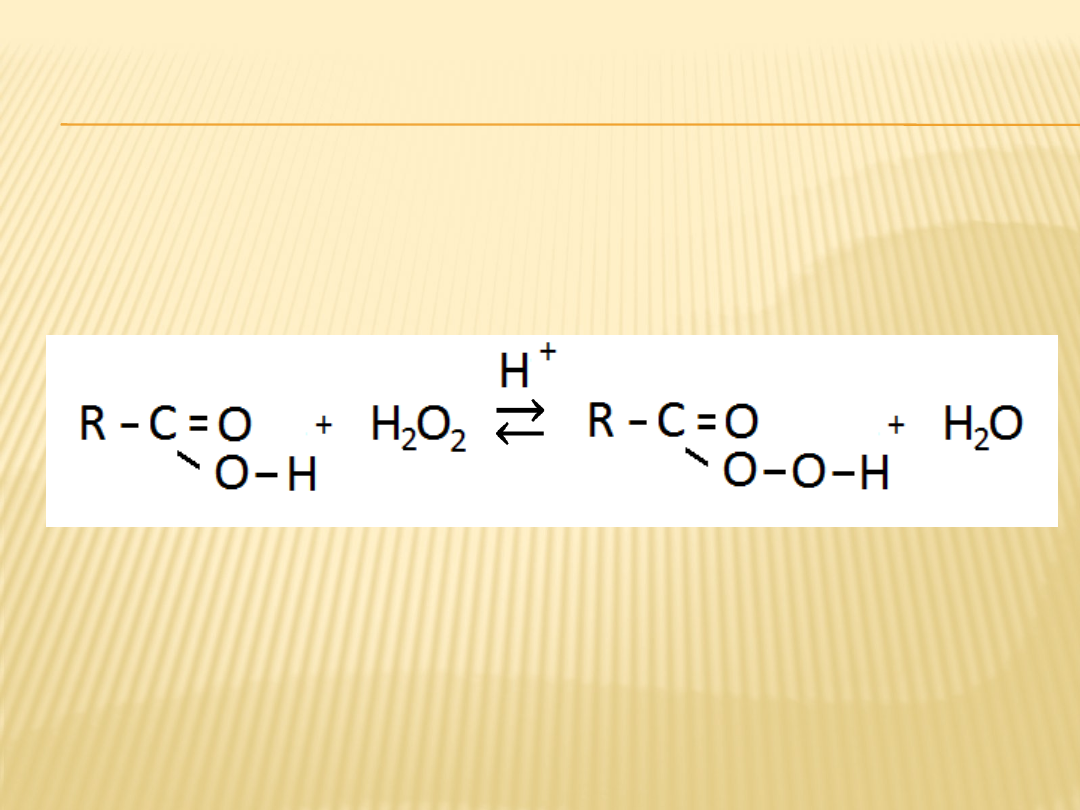
zachodzi
utlenianie grupy –OH wchodzącej w skład
grupy -COOH. W reakcji tej powstają
NADKWASY.
POWSTAWANIE NADKWASÓW
⇄

UTLENIANIE KWASÓW
KARBOKSYLOWYCH
Istnieją kwasy karboksylowe ulegające
utlenianiu (posiadające właściwości
redukujące):
kwas mrówkowy
kwas szczawiowy
kwas pirogronowy
REAKCJE Z ALKOHOLAMI
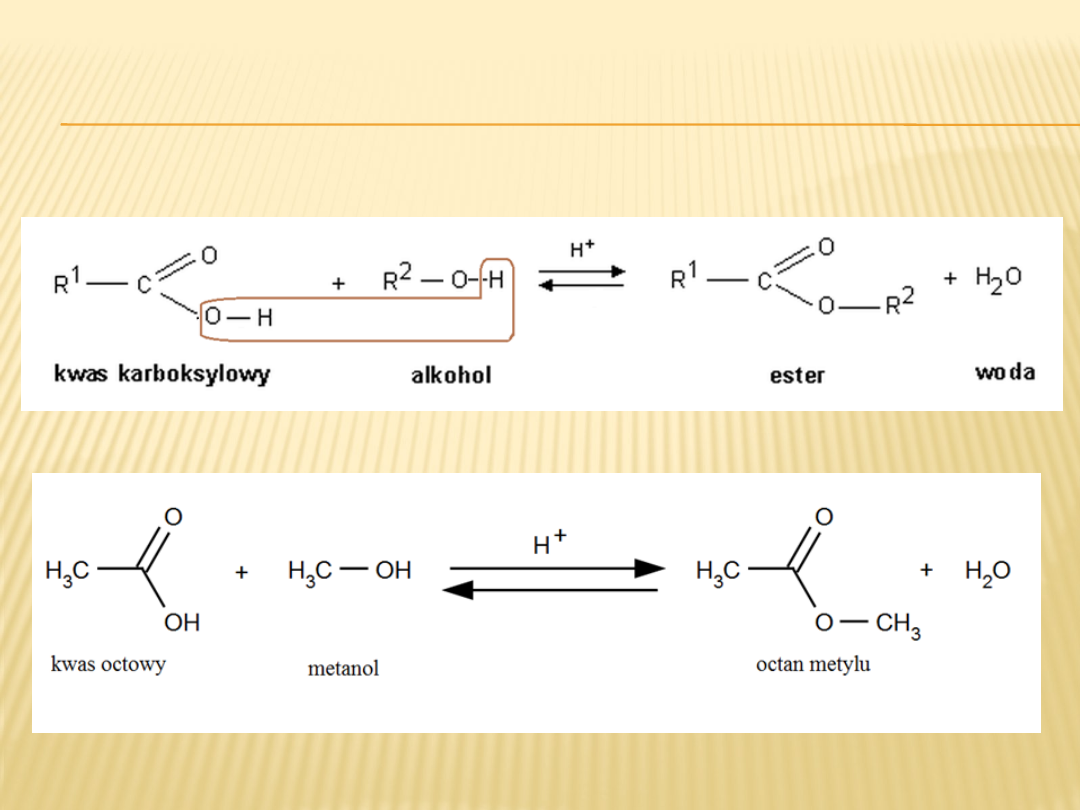
Reakcje alkoholi z kwasami karboksylowymi
nazywamy reakcjami ESTRYFIKACJI.
Produktami estryfikacji są ESTRY.
hydroliza
estryfikac
ja
kwa
s
alkoh
ol
est
er
wod
a
REAKCJA ESTRYFIKACJI

REAKCJA ESTRYFIKACJI
Właściwości:
niższe estry są cieczami, ale w miarę wzrostu łańcucha węglowego w
cząsteczce estru przechodzą one w ciecze oleiste, a następnie w
ciała stałe
są rozpuszczalnikami organicznymi do farb i lakierów np.
bezacetanowy zmywacz do paznokci to głownie octan etylu
substancje zapachowe roślin np. zapachy zwabiające owady
zapylające
estry kwasu salicylowego stosowane jako leki: salicylan fenylu –
środek przeciwreumatyczny, kwas acetylosalicylowy – środek
przeciwgorączkowy i przeciwbólowy (NLPZ)

REAKCJA Z AMONIAKIEM I
AMINAMI I- ORAZ II-RZĘDOWYMI
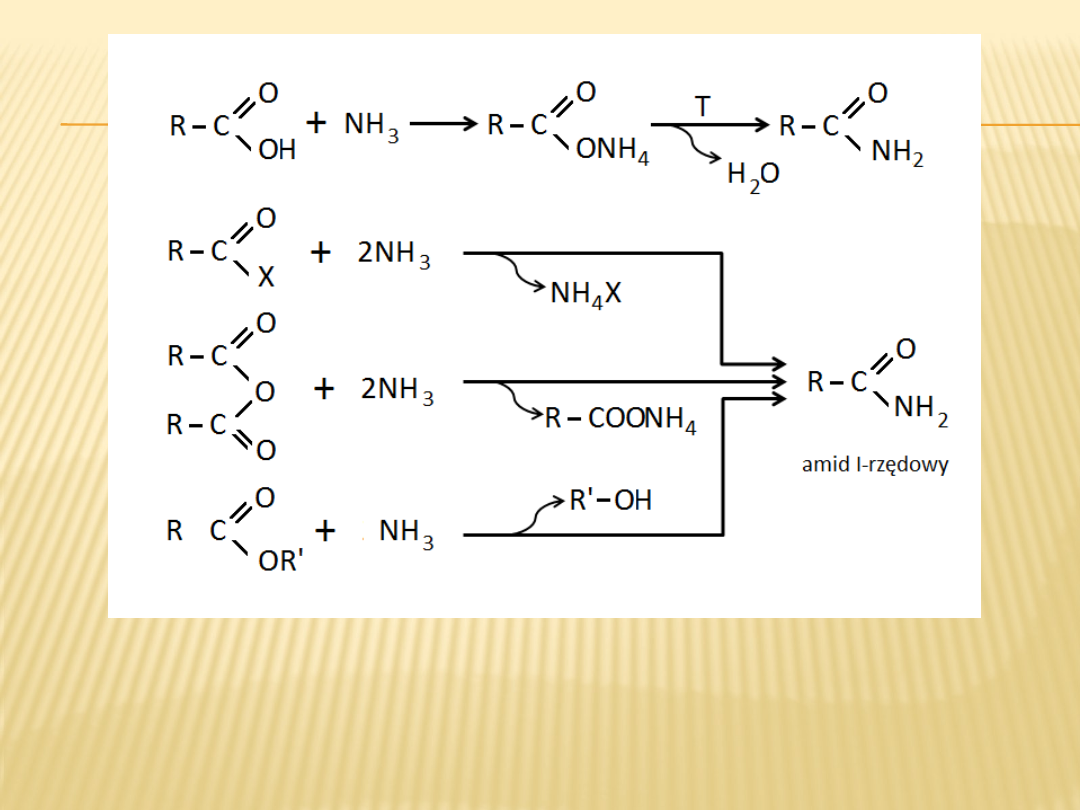
Kwasy karboksylowe w reakcjach z amoniakiem oraz aminami
I- i II-rzędowymi tworzą AMIDY KWASOWE.
Acylowanie amin to wprowadzenie grup acylowych do amin
przy pomocy różnych czynników acylujacych:
a)
kwasów karboksylowych
b)
ich bezwodników
c)
halogenów kwasowych
d)
estrów
W reakcji acylowania amin powstają:
1.
AMIDY KWASOWE II-RZĘDOWE (Z AMIN I-RZĘDOWYCH)
2.
AMIDY KWASOWE III-RZĘDOWE (Z AMIN II-RZĘDOWYCH)
UŻYWAJĄC AMINY I-RZĘDOWEJ ZAMIAST NH
3
OTRZYMAMY
AMID II-RZĘDOWY
UŻYWAJĄC AMINY II-RZĘDOWEJ ZAMIAST NH
3
OTRZYMAMY
AMID III-RZĘDOWY

DEKARBOKSYLACJA
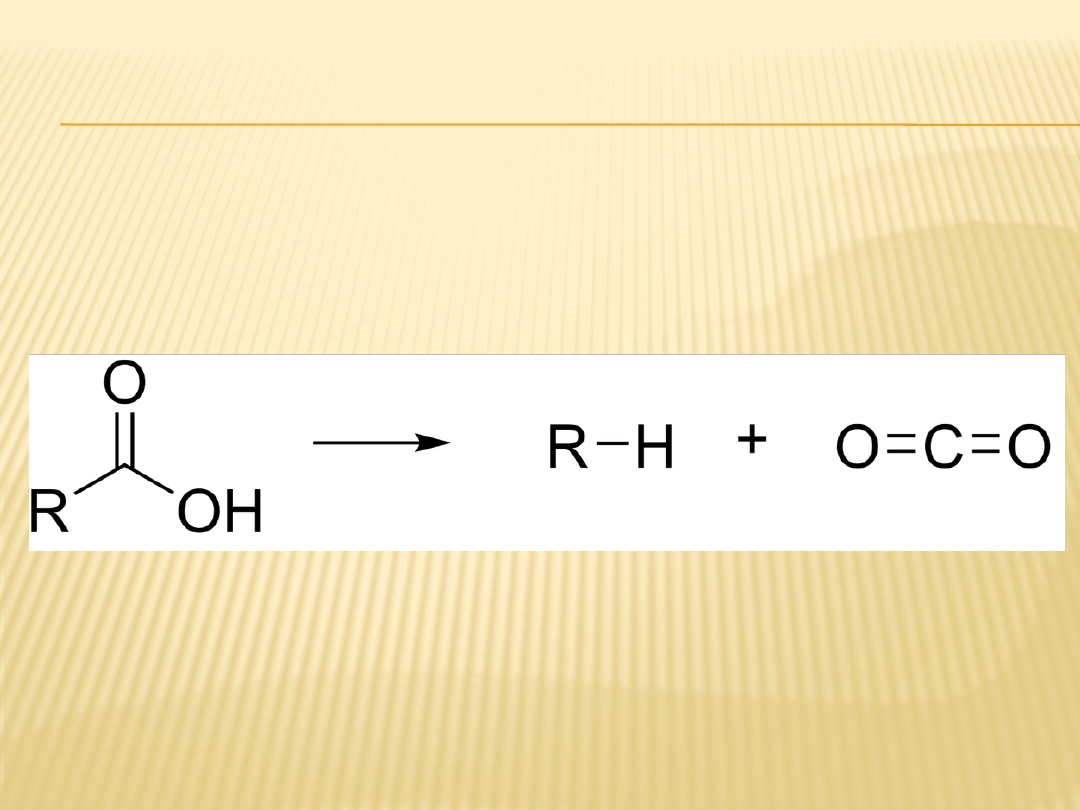
DEKARBOKSYLACJA to rozkład kwasów
karboksylowych z wydzieleniem CO
2
.
Najczęściej prowadzi do zastąpienia grupy –
COOH atomem wodoru.
Większość kwasów karboksylowych trudno ulega
reakcji dekarboksylacji.
Dekarboksylacji łatwo ulegają:
a)
β-ketokwasy
b)
kwasy 1,1-dikarboksylowe
c)
α-ketokwasy
DEKARBOKSYLACJA
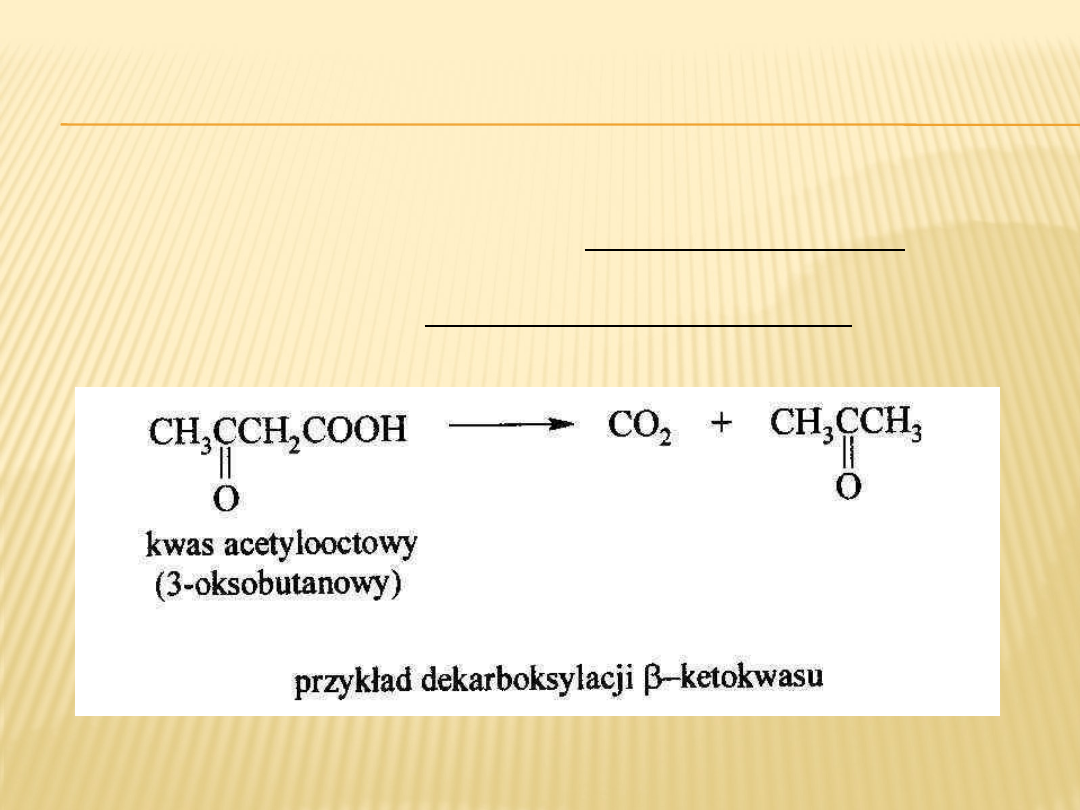
Najprostszym β-ketokwasem jest kwas acetylooctowy. Jego
dekarboksylacja następuje przy łagodnym ogrzewaniu i
prowadzi do powstania acetonu i dwutlenku węgla.
DEKARBOKSYLACJA β-
KETOKWASÓW
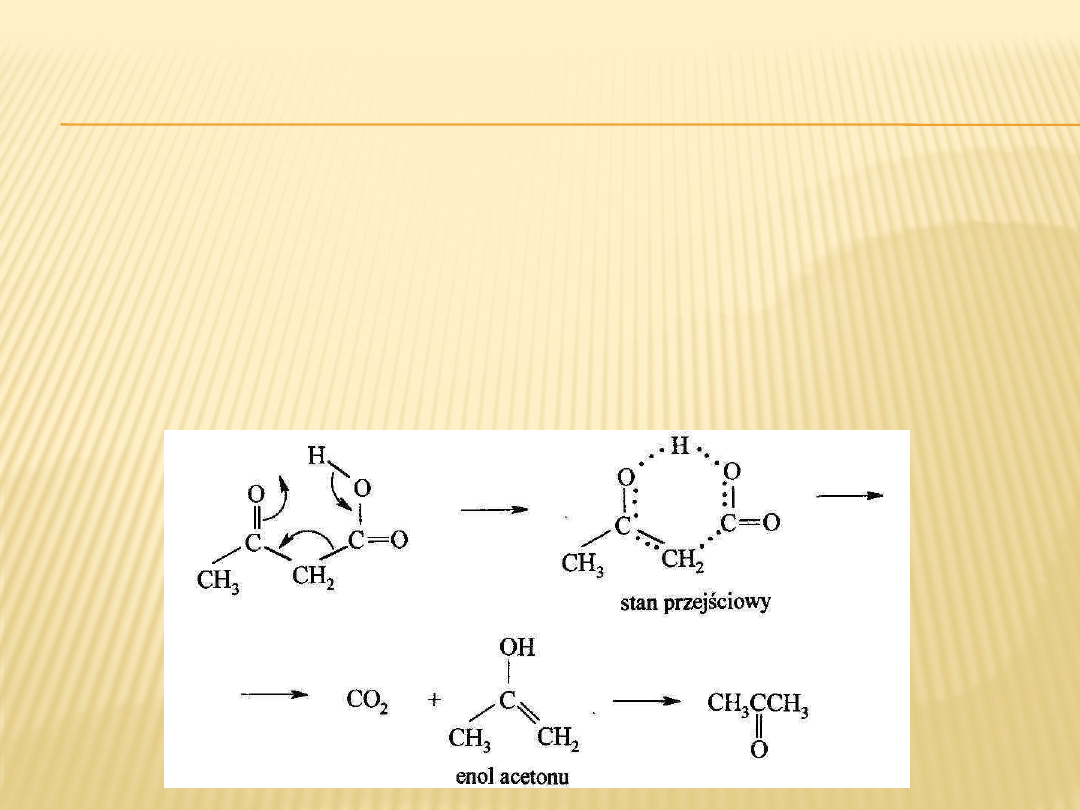
Łatwość dekarboksylacji polega na powstawaniu pierścieniowych
stanów przejściowych. Jest to proces jednoetapowy z
jednoczesnym rozpadem i powstawaniem wiązań na drodze
kołowych przesunięć elektronów co powoduje przesunięcie atomu
wodoru z grupy karboksylowej do karbonylowego atomu tlenu
oraz rozpad wiązania C-C i powstanie wiązania C=C w enolu.
MECHANIZM
DEKARBOKSYLACJI
β-KETOKWASÓW
DEKARBOKSYLACJA
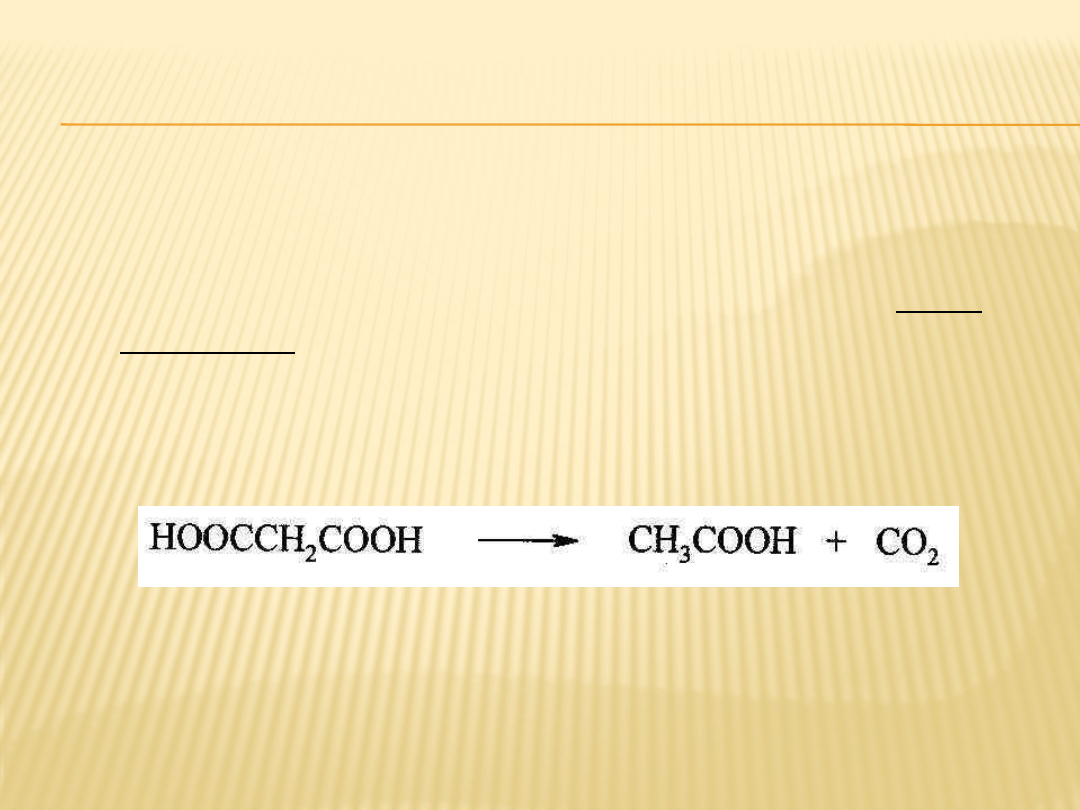
KWASÓW 1,1-DIKARBOKSYLOWYCH
Najprostszym kwasem dikarboksylowym jest kwas
malonowy.
Poddany ogrzewaniu ulega dekarboksylacji z
powstaniem kwasu octowego i wydzieleniem CO
2
.
Dekarboksylacji ulegają także pochodne kwasu malonowego,
w których jeden lub dwa atomy wodoru w grupie metylowej
zastąpione są grupami alkilowymi lub arylowymi.
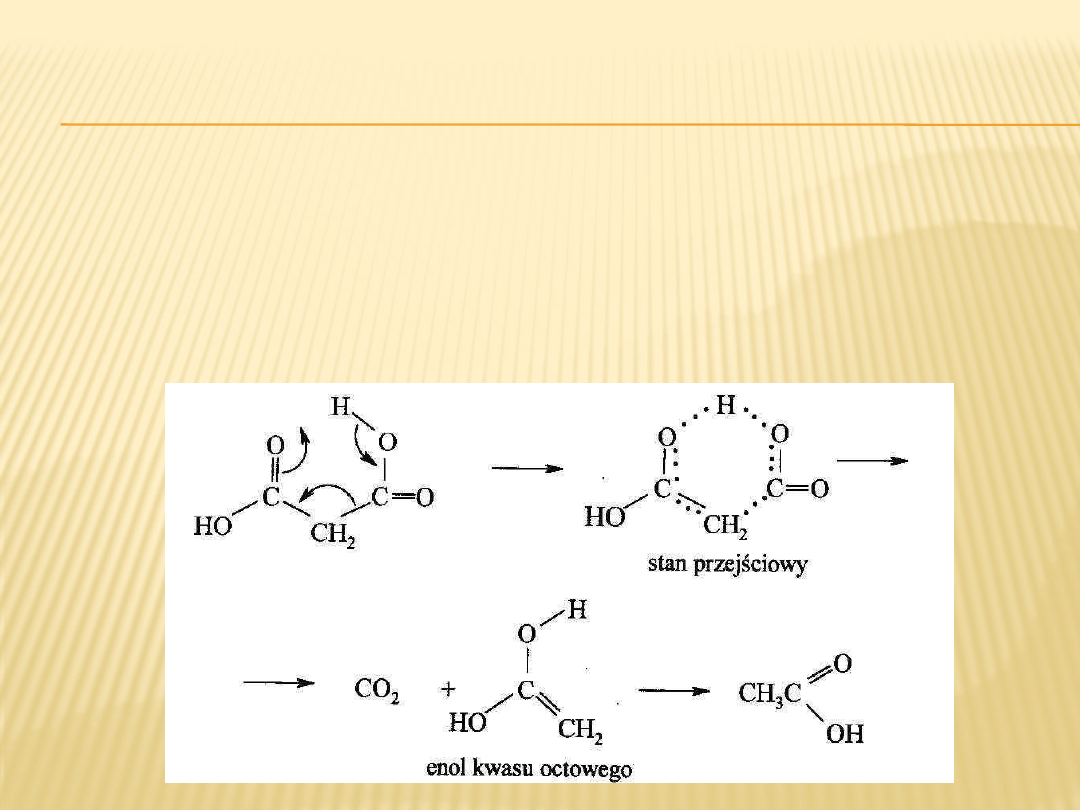
MECHANIZM DEKARBOKSYLACJI
KWASÓW 1,1-DIKARBOKSYLOWYCH
Mechanizm reakcji jest analogiczny do
mechanizmu dekarboksylacji β-
ketokwasów.

DEKARBOKSYLACJA α-KETOKWASÓW
α-ketokwasy są metabolitami w różnego rodzaju szlakach
metabolicznych ustroju człowieka
w organizmie ich dekarboksylacja wywoływana jest najczęściej
poprzez działanie enzymów
kwas pirogronowy (2-oksopropanowy) – produkt glikolizy, który w
zależności od rodzaju bioreakcji, w której bierze udział może
ulegać dekarboksylacji w warunkach tlenowych lub beztlenowych
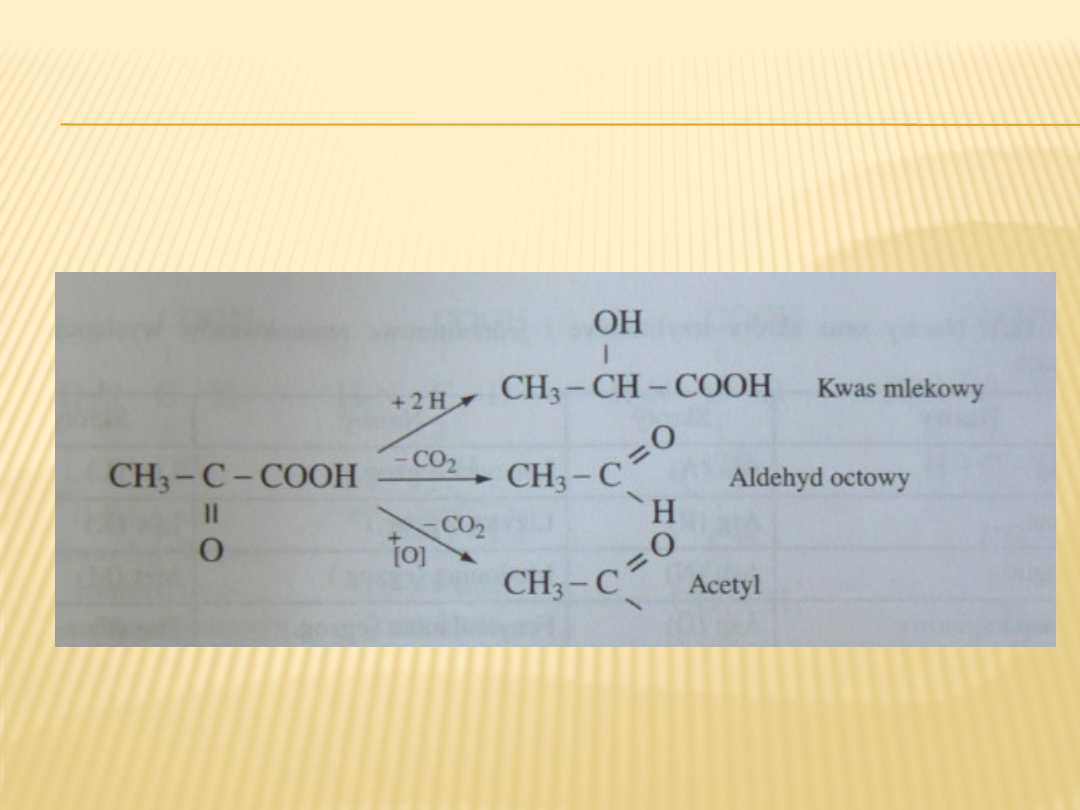
DEKARBOKSYLACJA α-KETOKWASÓW

OTRZYMYWANIE METANU
Metan można otrzymać w wyniku
prażenia octanu sodu z wodorotlenkiem
sodu
CH
3
COONa + NaOH → CH
4
+
Na
2
CO
3
T
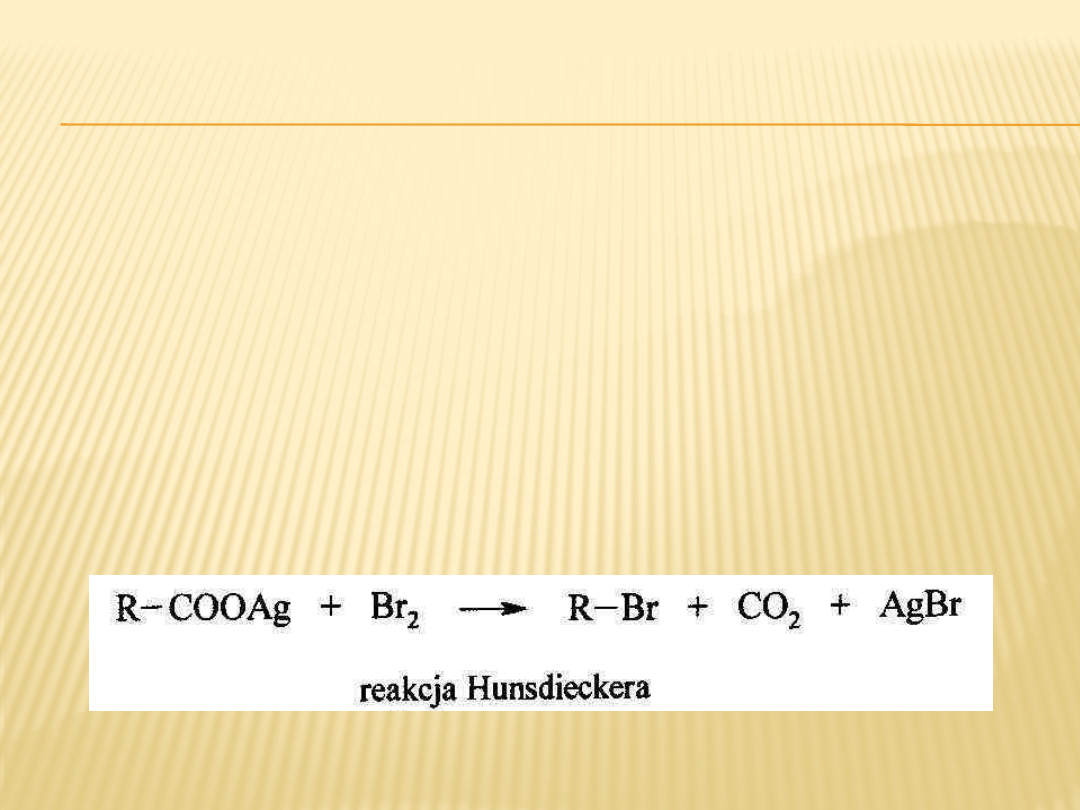
REAKCJA HUNSDIECKERA
Reakcja Hunsdieckera jest reakcją dekarboksylacji przy
jednoczesnym wprowadzeniu atomu bromu w miejsce
grupy karboksylowej.
Reakcji tej ulegają srebrowe lub rtęciowe sole kwasów
karboksylowych.
Reakcja jest wieloetapowa o mechanizmie rodnikowym
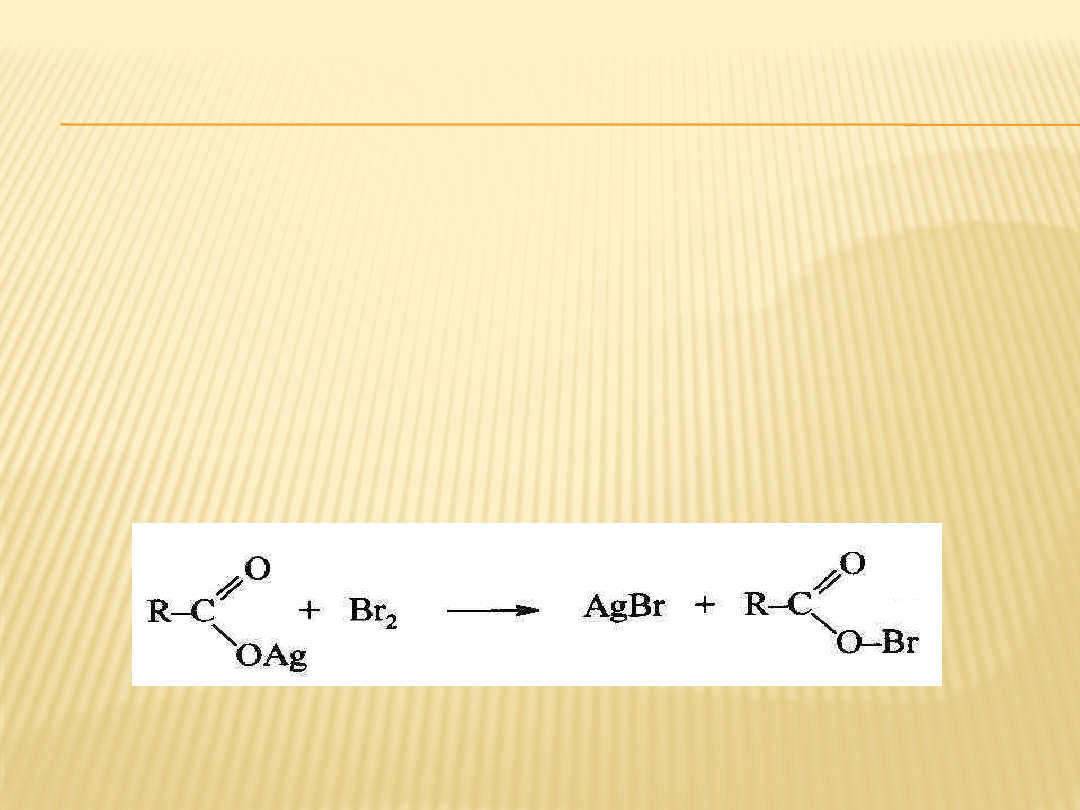
W pierwszym etapie powstaje nietrwała pochodna kwasu,
zawierająca wiązanie O-Br.
MECHANIZM REAKCJI
HUNSDIECKERA
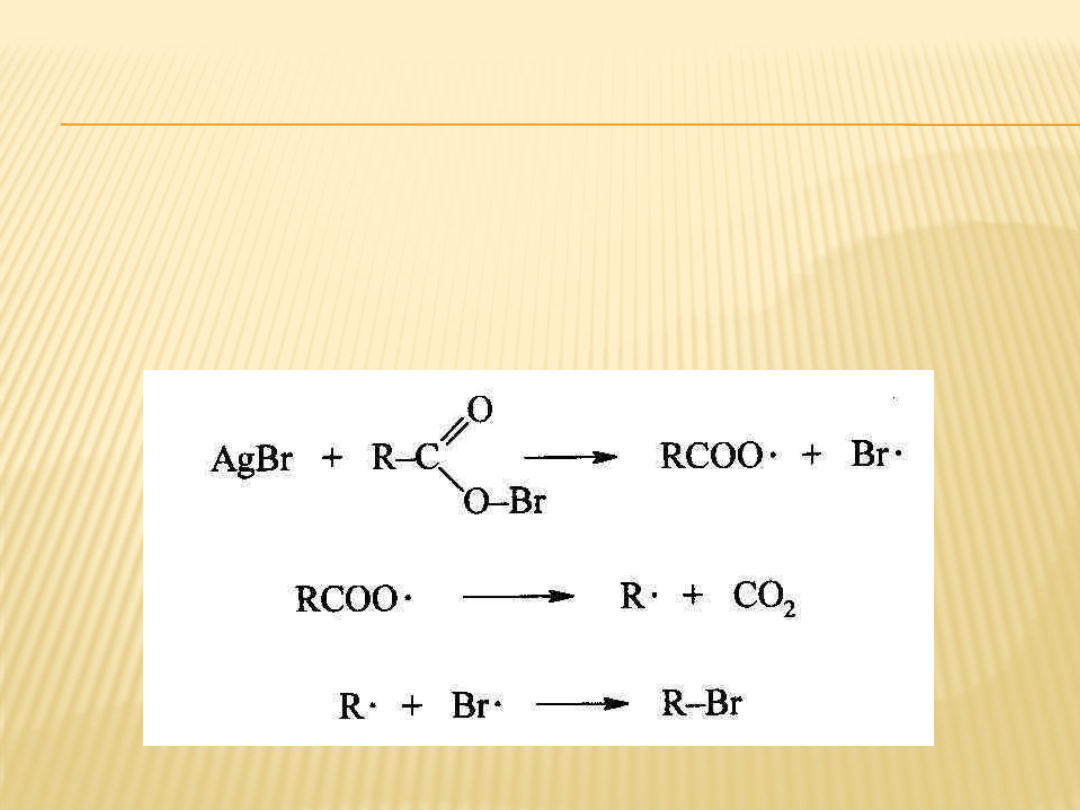
MECHANIZM REAKCJI
HUNSDIECKERA
Następnie rozpad wiązania 0-Br zapoczątkowuje reakcje
rodnikowe, które prowadzą do powstania dwutlenku węgla i
bromoalkanu.
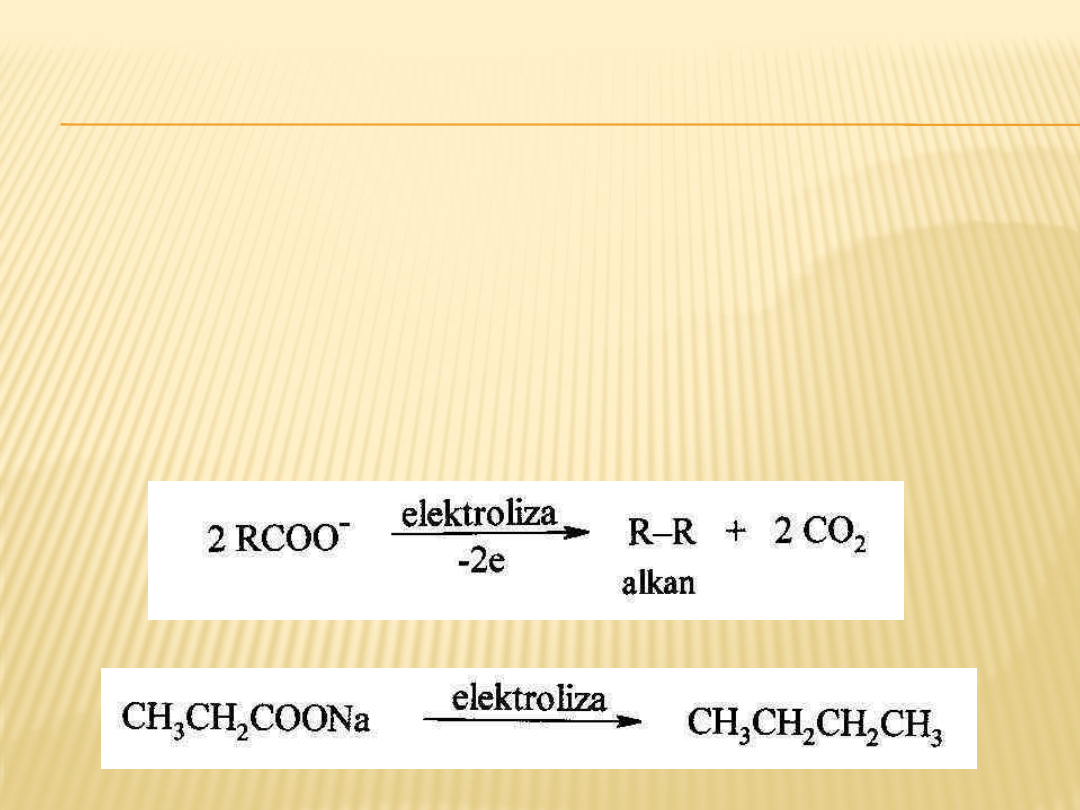
ANODOWE UTLENIANIE KWASÓW
KARBOKSYLOWYCH
Utlenianie odbywa się na anodzie, gdzie aniony kwasów
karboksylowych oddają elektrony – utleniając się do rodników.
Następnie zachodzi dekarboksylacja rodników karboksylowych
i dimeryzacja rodników alkilowych.
Jest to metoda przedłużania łańcucha węglowego, polegająca
na elektrolizie soli kwasów karboksylowych

PYTANIA KONTROLNE
1)
Co jest produktem utleniania kwasów karboksylowych
nadtlenkiem wodoru?
2)
Podaj reagenty reakcji estryfikacji.
3)
Czym jest dekarboksylacja?
4)
Jakie grupy funkcyjne zawierają ketokwasy?
5)
Jakie sole kwasów karboksylowych ulegają reakcji
Hunsdieckera?
Document Outline
- Slide 1
- REAKCJE ALIFATYCZNYCH NASYCONYCH KWASÓW KARBOKSYLOWYCH Z:
- REAKCJE Z METALAMI, TLANKAMI METALI I WODOROTLENKAMI
- Slide 4
- Slide 5
- REAKCJE Z solami kwasu węglowego
- Slide 7
- REAKCJE Z nadtlenkiem wodoru
- POWSTAWANIE NADKWASÓW
- UTLENIANIE KWASÓW KARBOKSYLOWYCH
- REAKCJE Z alkoholami
- REAKCJA ESTRYFIKACJI
- REAKCJA ESTRYFIKACJI
- REAKCJA z amoniakiem i aminami I- oraz Ii-rzędowymi
- Slide 15
- DEKARBOKSYLACJA
- DEKARBOKSYLACJA
- Slide 18
- Slide 19
- dekarboksylacja kwasów 1,1-dikarboksylowych
- MECHANIZM dekarboksylacjI kwasów 1,1-dikarboksylowych
- DEKARBOKSYLACJA α-KETOKWASÓW
- DEKARBOKSYLACJA α-KETOKWASÓW
- Otrzymywanie metanu
- REAKCJA Hunsdieckera
- MECHANIZM REAKCJI Hunsdieckera
- MECHANIZM REAKCJI Hunsdieckera
- ANODOWE UTLENIANIE KWASÓW KARBOKSYLOWYCH
- Pytania kontrolne
Wyszukiwarka
Podobne podstrony:
!!!Właściwości nasyconych kwasów karboksylowych
!!!Właściwości nasyconych kwasów karboksylowych
kawsy i mydła - chemia, Właściwości kwasów karboksylowych o rodniku alifatycznym
otrzymywanie i reakcje kwasow karboksylowych
otrzymywanie-i-reakcje-kwasow karboksylowych
15 Pochodne kwasów karboksylowych (08 11 2011)
Właściwości i zastosowanie kwasów karboksylowych
kwasy i pochodne Synteza pochodnych kwasów karboksylowych – estrów
Estry i tłuszcze, ESTRY KWASÓW KARBOKSYLOWYCH
wyk 10 pochodne kwasów karboksylowych
pochodne kwasów karboksylowych
16 Pochodne kwasów karboksylowych
16 Pochodne kwasow karboksylowych materiały dodatkowe
17 Estry kwasow karboksylowych
ściąga z kwasów karboksylowych
amidy kwasow karboksylowych
tabelka pochodne kwasow karboksylowych, farmacja cm umk, Farmacja III rok, chemia leków
OTRZYMYWANIE AMIDOW Z KWASOW KARBOKSYLOWYCH, Materiały, Chemiczne, Chemia organiczna
więcej podobnych podstron