
AMINOKWASY,
PEPTYDY,
BIAŁKA
Mgr Katarzyna Chojnacka

AMINOKWASY
organiczne związki chemiczne,
zawierające grupę aminową -NH
2
(zasadową) oraz grupę karboksylową
-COOH (kwasową)
Należą do wielofunkcyjnych
pochodnych węglowodorów (związki,
które zawierają co najmniej dwie różne
grupy funkcyjne połączone z grupą
węglowodorową)
Wzór ogólny aminokwasu
(NH
2
)
n
- R-(COOH)
m
R- fragment węglowodorowy
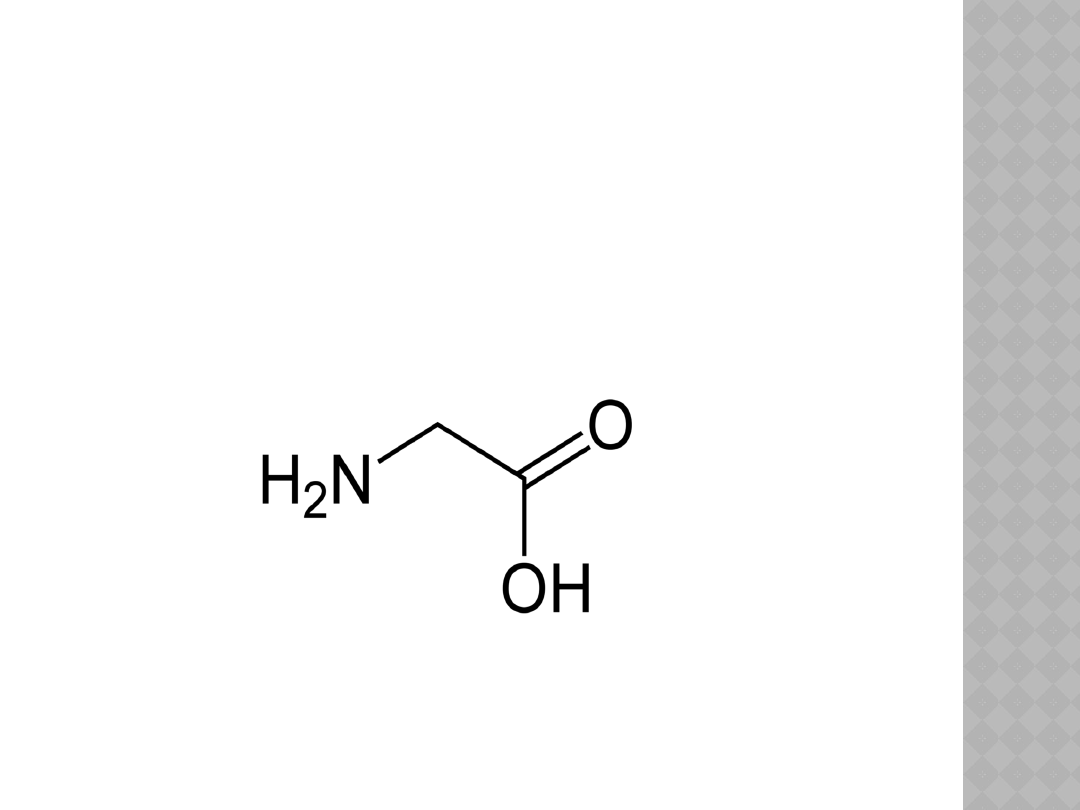
Najprostszym aminokwasem jest
glicyna – kwas aminooctowy:

WŁAŚCIWOŚCI OGÓLNE
AMINOKWASÓW
Aminokwasy z kilkoma wyjątkami są
dobrze rozpuszczalne w wodzie,
amoniaku i innych rozpuszczalnikach
polarnych, słabo rozpuszczalne w
rozpuszczalnikach niepolarnych i mniej
polarnych rozpuszczalnikach tj.
metanol, etanol, aceton. Spowodowane
jest to powstawaniem soli wewnętrznej.

WŁAŚCIWOŚCI OGÓLNE
AMINOKWASÓW
Aminokwasy tworzą tzw. sól
wewnętrzną (jon obojnaczy lub
dwubiegunowy) – w cząsteczce
aminokwasu grupy aminowa i
karboksylowa ulegają wzajemnemu
zobojętnieniu wskutek przeniesienia
kationu z grupy –COOH na grupę NH
2
NH
2
-R-COOH↔ NH
3
+
-R-COO
-
W punkcie izoelektrycznym aminokwas
występuje jako jon obojnaczy, wtedy
cząsteczka jest najsłabiej rozpuszczalna
– wykorzystuje się to do wytrącenia
aminokwasu z roztworu.

WŁAŚCIWOŚCI OGÓLNE
AMINOKWASÓW PUNKT
IZOELEKTRYCZNY
Punkt izoelektryczny (pI) –jest to
wartość pH, przy której aminokwas
występuje w postaci soli wewnętrznej,
czyli jest to takie pH środowiska przy
którym cząsteczka aminokwasu w
wdanych warunkach jest obojętna.
W punkcie izoelektrycznym cząsteczka
nie ma zdolności wędrowania w polu
elektrycznym
W roztworze o wyższym pH niż punkt
izoelektryczny cząsteczka występuje w
formie anionu a poniżej punktu
izoelektrycznego w formie kationu

WŁAŚCIWOŚCI OGÓLNE
AMINOKWASÓW
Aminokwasy są związkami
amfoterycznymi ponieważ reagują
zarówno z kwasami jak i zasadami. W
środowisku silnie kwasowym
równowaga przesuwa się w kierunku
tworzenia kationów, a w środowisku
silnie zasadowym w kierunku tworzenia
anionów.
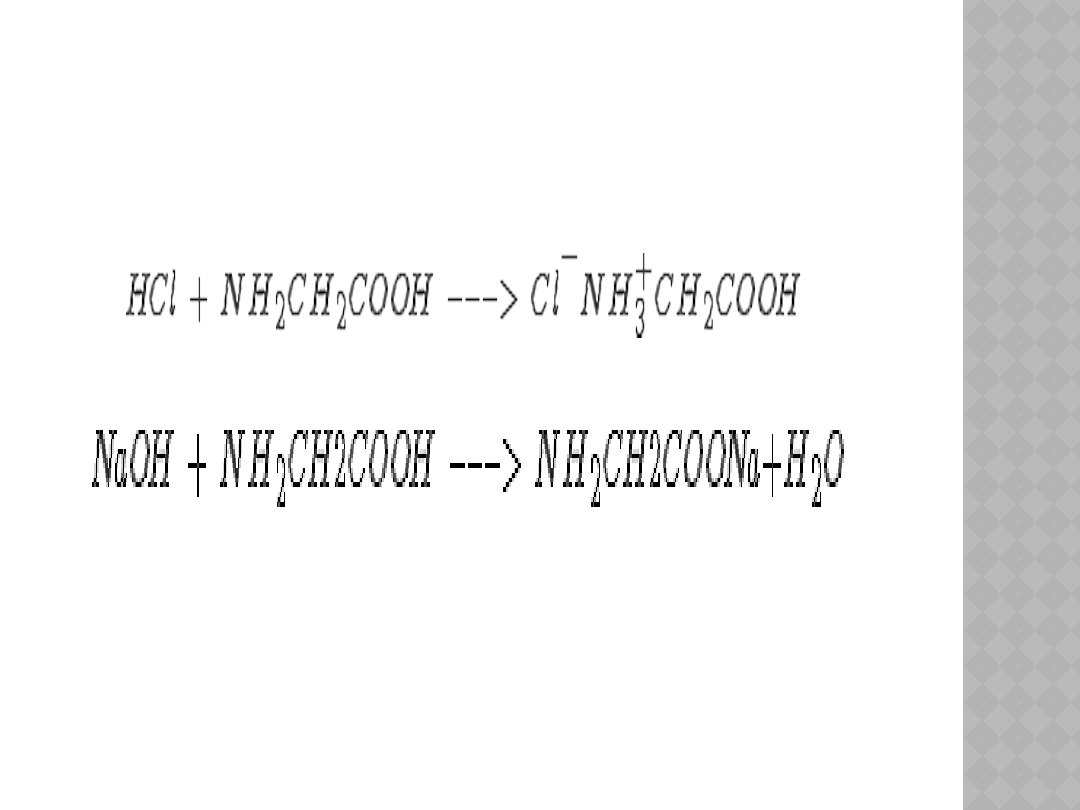
AMFOTERYCZNOŚĆ
AMINOKWASÓW
W tym przypadku czynnik atakujący (kwas) reaguje z
grupą aminową (gr. zasadowa) i powstaje chlorowodorek
glicyny.
A w tym przypadku czynnik atakujący (zasada) reaguje z
grupą karboksylową (gr. kwasowa) i powstaje glicynian
sodu.

PODZIAŁ
AMINOKWASÓW
Aminokwasy kwasowe – przewaga grup
karboksylowych w aminokwasie (np.
kwas asparginowy, kwas glutaminowy)
Aminokwasy zasadowe – aminokwasy z
przewagą grup aminowych (np. lizyna)
Aminokwasy obojętne – jednakowa
liczna grup zasadowych i kwasowych w
cząsteczce aminokwasu (np. alanina,
cysteina, seryna)

WIĄZANIE PEPTYDOWE
Cząsteczki aminokwasów mogą łączyć
się ze sobą w specyficzny sposób –
grupa karboksylowa jednego
aminokwasu reaguje z grupą aminową
drugiego. Produktami tej reakcji są
peptydy
Powstawanie peptydów jest przykładem
reakcji polikondensacji, ponieważ
równocześnie wydziela się
małocząsteczkowy produkt uboczny w
tym wypadku woda.
Wiązanie peptydowe jest
charakterystyczne dla wszystkich
peptydów i białek
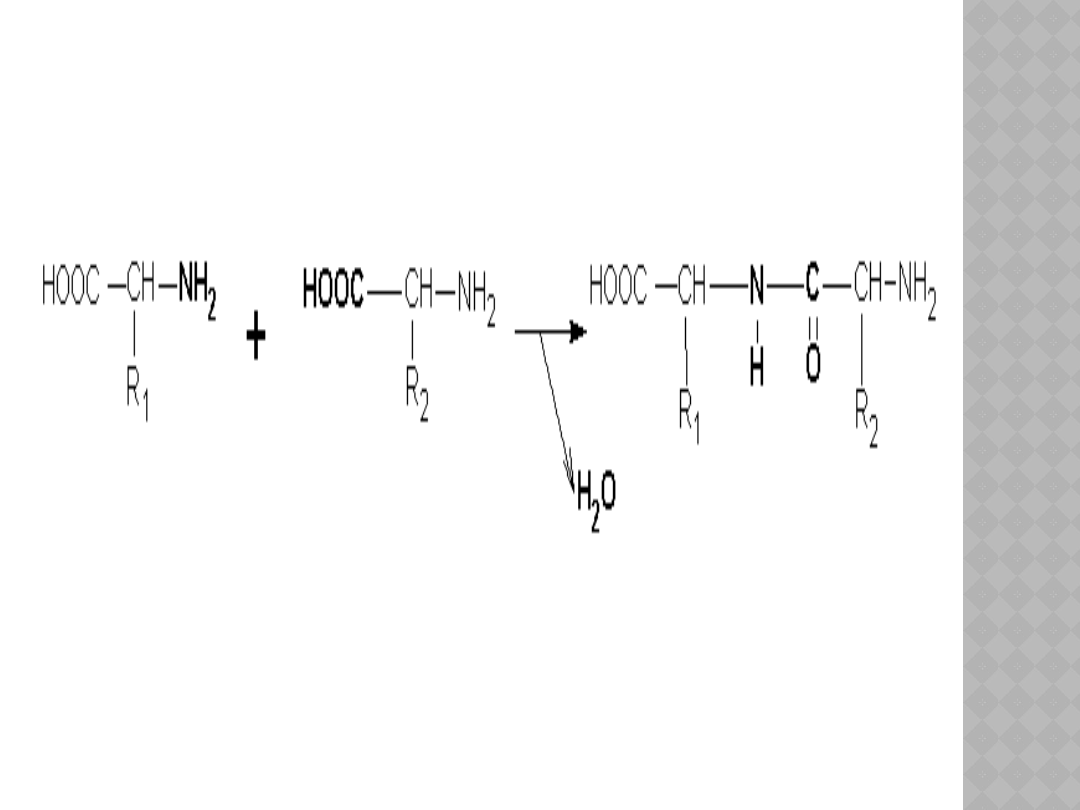
POWSTAWANIE WIĄZANIA
PEPTYDOWEGO

AMINOKWASY
BIAŁKOWE
Szczególne znaczenie mają aminokwasy, które
wchodzą w skład białek naturalnych.
Aminokwasów białkowych jest 20. W organizmie
człowieka może być syntetyzowane 12 z nich
(endogenne), zaś pozostałe tzw. aminokwasy
niezbędne – egzogenne są dostarczane
organizmowi w postaci pokarmów białkowych
Do rodziny aminokwasów białkowych zaliczamy
te aminokwasy, które są rozpoznawane przez kod
genetyczny.
Aminokwasy białkowe należą do α-aminokwasów,
ponieważ zawierają grupę aminową przy tym
atomie węgla, który w łańcuchu węglowym jest
najbliżej grupy karboksylowej.
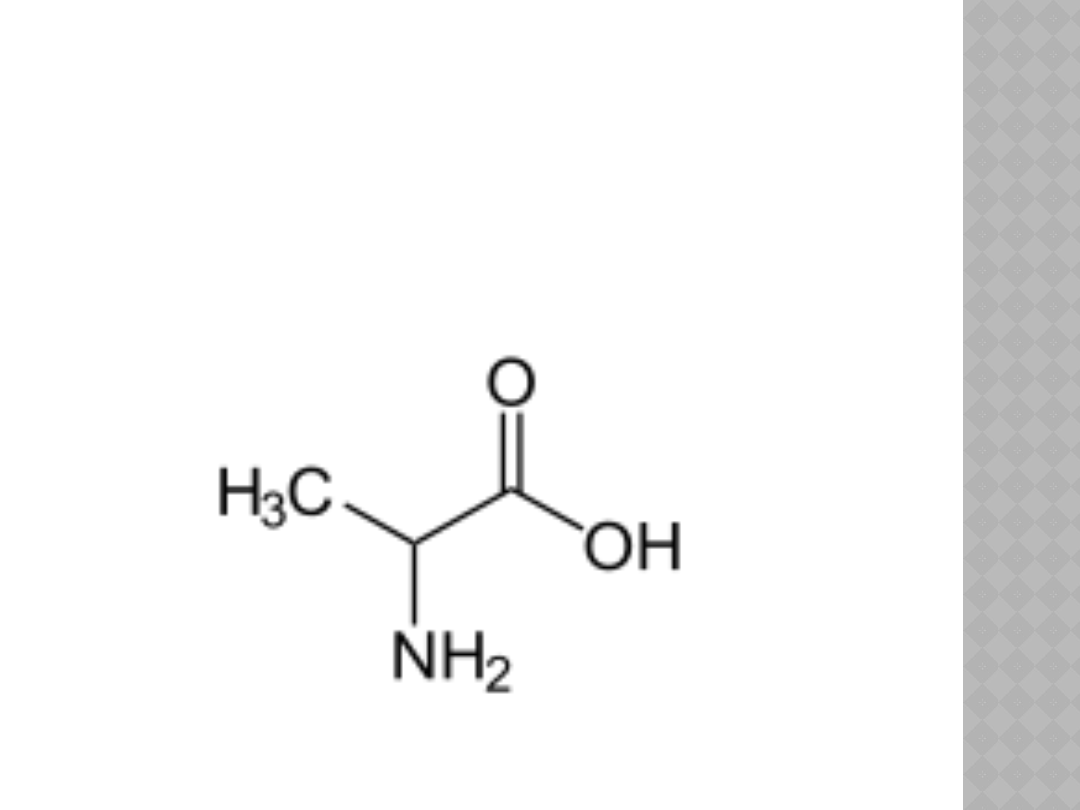
PRZYKŁADY AMINOKWASÓW
BIAŁKOWYCH
Alanina
Ala
PRZYKŁADY AMINOKWASÓW
BIAŁKOWYCH
Cysteina
Cys
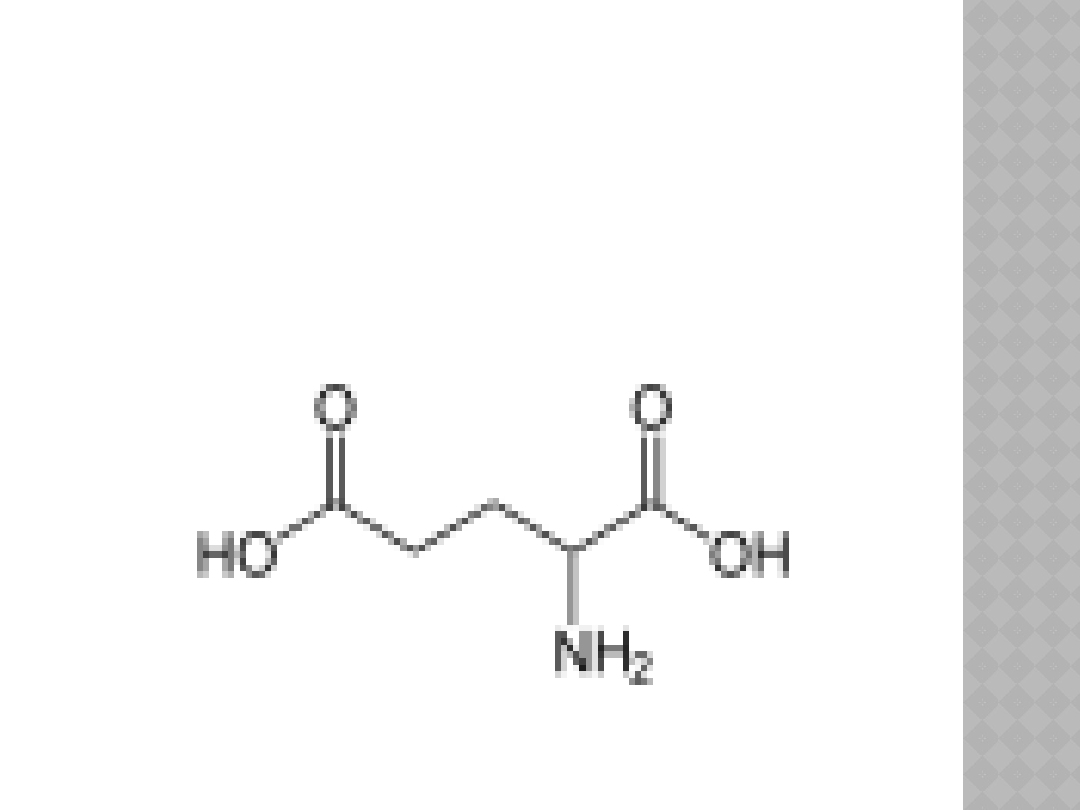
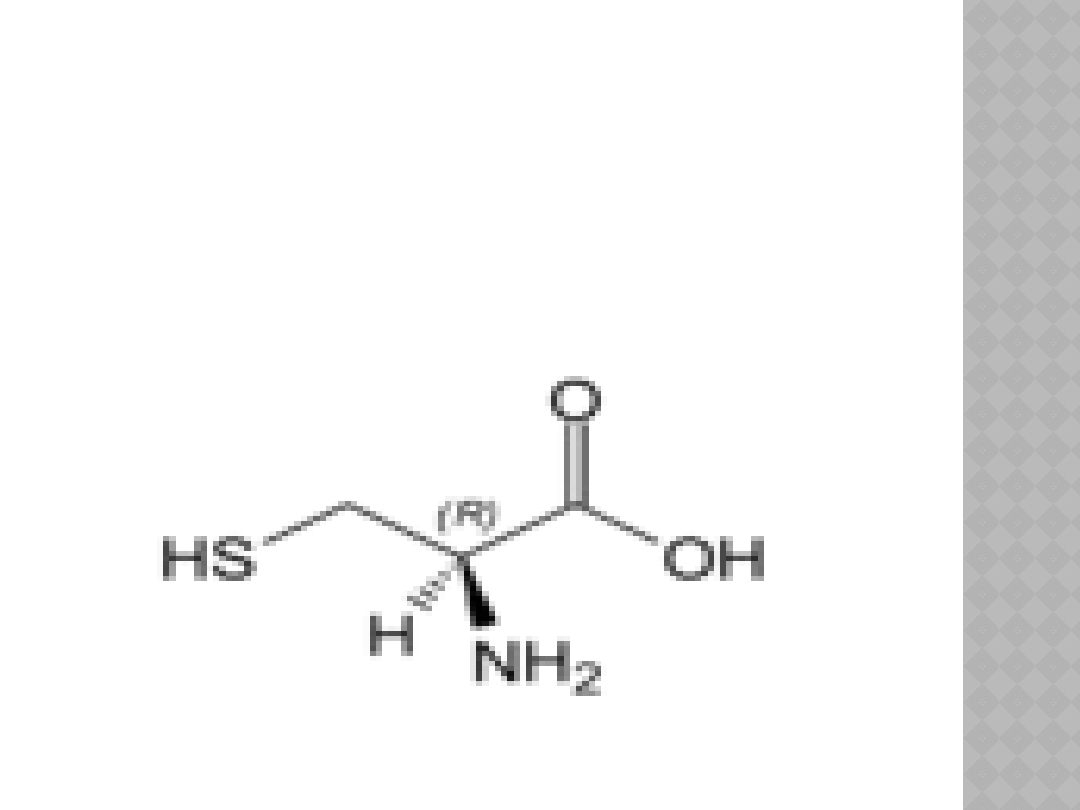
PRZYKŁADY AMINOKWASÓW
BIAŁKOWYCH
Kwas glutaminowy
Glu

KONFIGURACJA
AMINOKWASÓW
Konfiguracja – przestrzenna budowa
związku chemicznego.
Chiralność - cecha przedmiotu
polegająca na tym, że jest on
nieidentyczny ze swoim odbicie w
lustrze. Cząsteczka związku
chemicznego jest chiralna gdy nie jest
identyczna ze swoim odbiciem.
Aminokwasy są chiralne bo ich
cząsteczki zawierają asymetryczne
atomy węgla. Są to atomy połączone z
czterema różnymi podstawnikami.

KONFIGURACJA
AMINOKWASÓW
Wśród aminokwasów białkowych tylko
glicyna nie jest chiralna ponieważ nie
posiada czterech różnych podstawników.
Stereoizomery - izomery przestrzenne,
związki chemiczne, w których atomy
połączone są w tych samych sekwencjach, a
różnią się jedynie ułożeniem przestrzennym.
Enancjomery to izomery optyczne, które są
własnymi lustrzanymi odbiciami – mniej
więcej tak jak prawa i lewa rękawiczka.
Mogą istnieć tylko dwa enancjomery danego
związku chemicznego.

KONFIGURACJA
AMINOKWASÓW
Wszystkie pozostałe aminokwasy białkowe są
chiralne i wysterują w postaci dwóch
stereoizomerów, różniących się konfiguracją
podstawników przy asymetrycznych atomach
węgla. Są to atomy w położeniu α, czyli
sąsiadujące z grupą COOH.
Konfiguracja związków chiralnych może być
prawa (symbol D lub R) lub lewa (symbol L
lub S)
Izomery o przeciwnych konfiguracjach
nazywamy enancjomerami.
Wszystkie aminokwasy białkowe mają
jednakową konfigurację – konfigurację L

PEPTYDY
Związki utworzone z aminokwasów
połączonych wiązaniem peptydowym (-
CO-NH-)
Dzielimy je na :
- oligopeptydy – 2 do 10 reszt
aminokwasowych
- polipeptydy – 11 do 100 reszt
aminokwasowych
- białka – powyżej 100 reszt
aminokwasowych
W każdym peptydzie można wyróżnić
koniec zawierający grupę aminową
zwany końcem N-terminalnym
oraz koniec z wolną grupą
karboksylową nazywany końcem C-
terminalnym

PEPTYDY
Kolejność uszeregowania aminokwasów
w łańcuchu peptydowym nazywa się
sekwencją aminokwasów.
Peptydy zbudowane z takich samych
aminokwasów ale różniące się
sekwencją nazywamy izomerami.
Peptydy występują w komórkach
roślinnych i zwierzęcych oraz w
bakteriach, mogą być hormonami,
antybiotykami lub truciznami.

BIAŁKA
To naturalne polimery zbudowane z
aminokwasów połączonych wiązaniami
peptydowymi w długie łańcuchy
Łańcuchy polipeptydowe w białkach są
pozwijane w najprzeróżniejsze sposoby i
tworzą niezwykle skomplikowane
struktury przestrzenne. Struktury takie
nazywamy konformacjami.
Rozróżniamy cztery podstawowe
poziomy budowy białek: strukturę
pierwszo-, drugo-, trzecio- i
czwartorzędową.

BIAŁKA
Struktura pierwszorzędowa – określa
sekwencję aminokwasów w łańcuchu
peptydowym i informuje w jaki sposób
atomy są połączone wiązaniami
kowalencyjnymi w cząsteczce. Jest to
struktura stosunkowo trwała. Działanie
enzymów i kwasów powoduje hydrolizę
wiązań peptydowych i podział łańcucha
na aminokwasy, które go tworzą.

BIAŁKA
Struktura drugorzędowa – wskazuje
jaki układ przestrzenny stabilizowany
wiązaniami wodorowymi tworzą
łańcuchy polipeptydowe. Są to typy
regularnego ułożenia głównego
łańcucha polipeptydowego
stabilizowane wiązaniami wodorowymi.
Struktura drugorzędowa jest
uwarunkowana przede wszystkim
właściwościami wiązania peptydowego.
Wyróżniamy dwie podstawowe
struktury drugorzędowe: struktura
pofałdowanej kartki (struktura β) lub
struktura .helisy (struktura α)
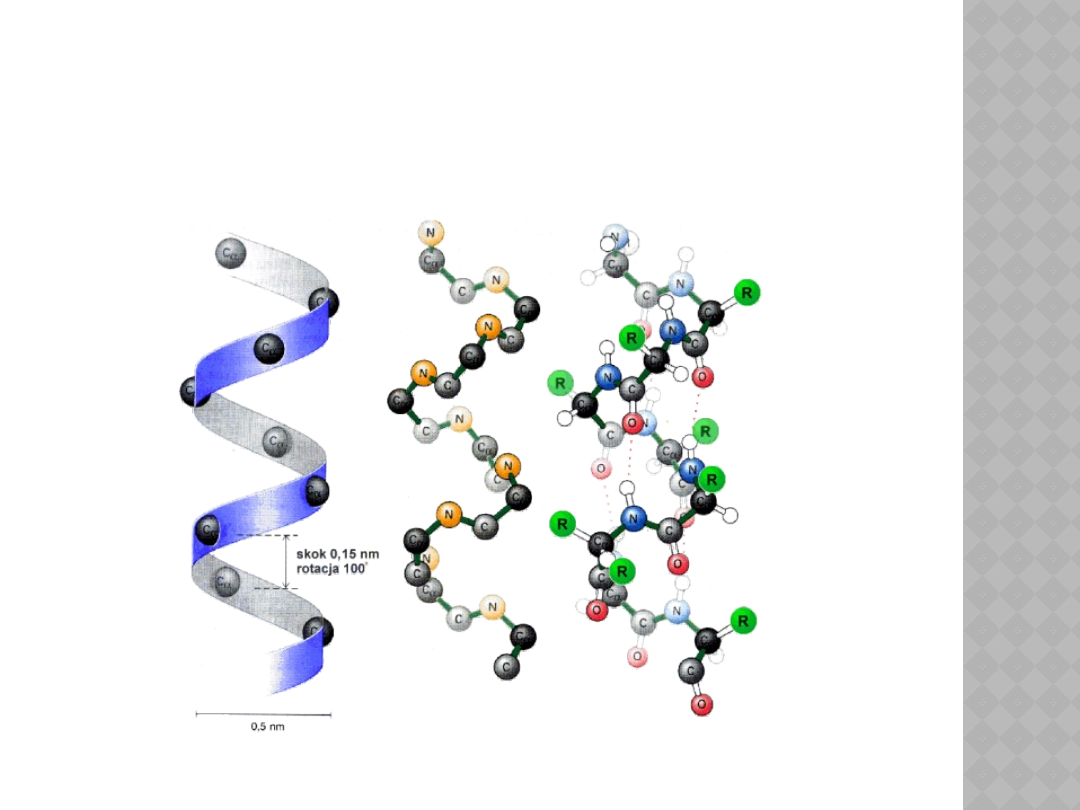
STRUKTURA HELISY
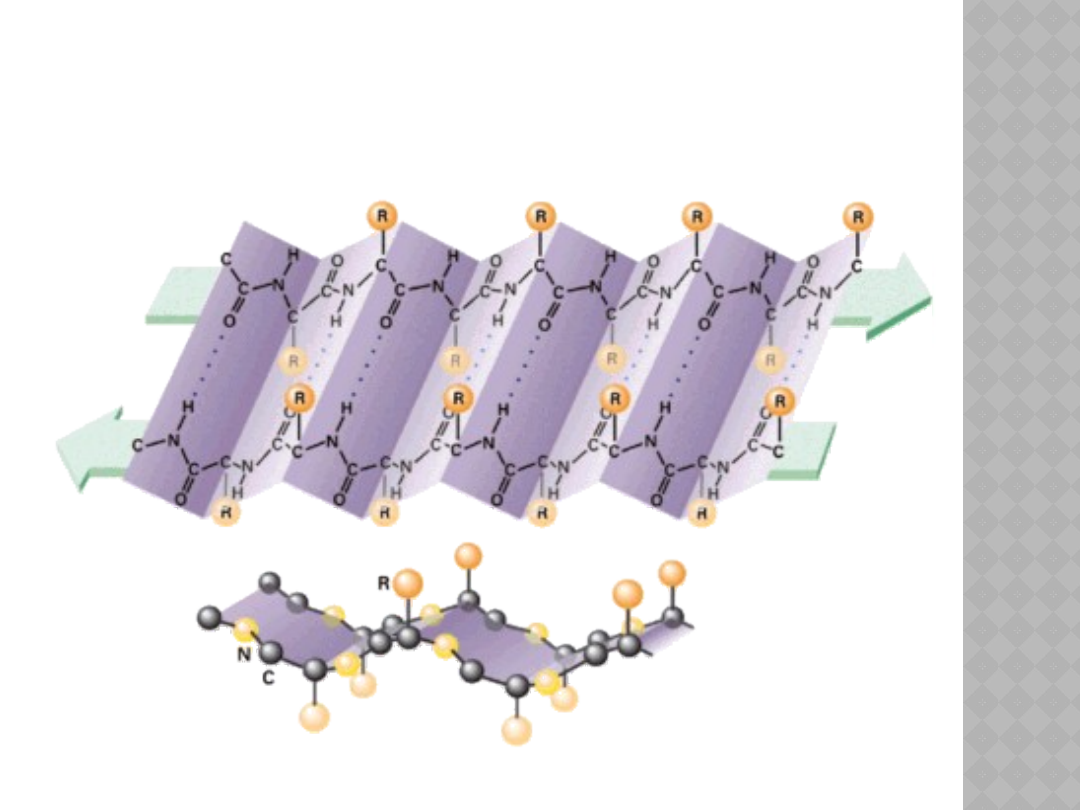
STRUKTURA
POFAŁDOWANEJ KARTKI
BIAŁKA
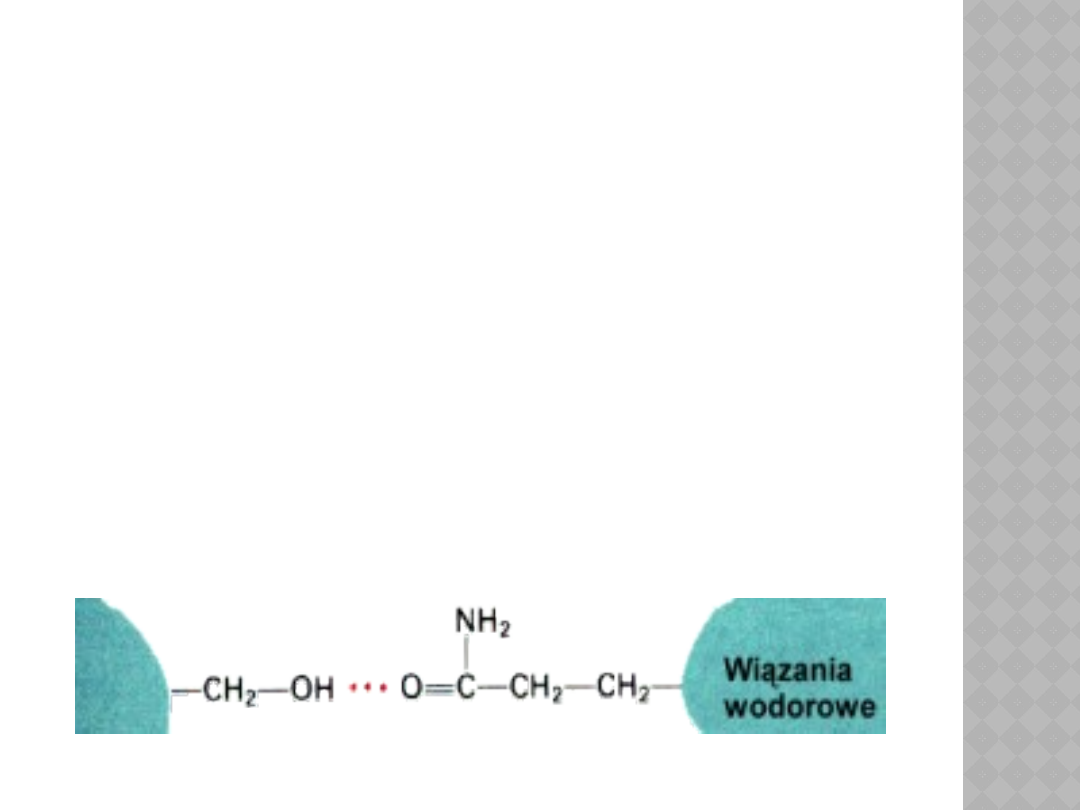
Struktura trzeciorzędowa –to
ułożenie poszczególnych odcinków
łańcucha polipeptydowego względem
siebie w przestrzeni, stabilizowane
m.in. Oddziaływaniami
elektrostatycznymi, wiązaniami
wodorowymi, albo tzw. mostkami
disulfidowymi –S-S-
powstaje w wyniku oddziaływania
poszczególnych reszt aminokwasowych
pomiędzy sobą.
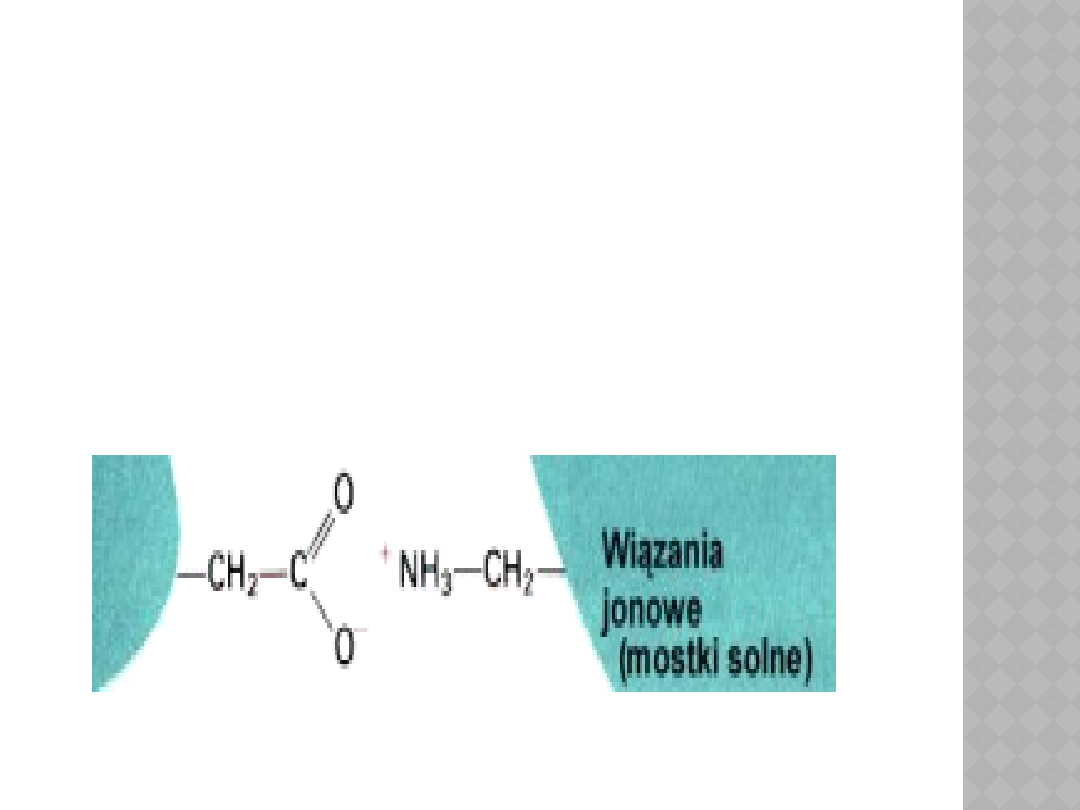
Oprócz wiązań wodorowych mogą
zostać utworzone tzw. "mostki solne" -
w reakcji pomiędzy grupami
funkcyjnymi pochodzącymi od
aminokwasów kwaśnych (Np.: kwas
glutaminowy) i zasadowych (Np.:
arginina).
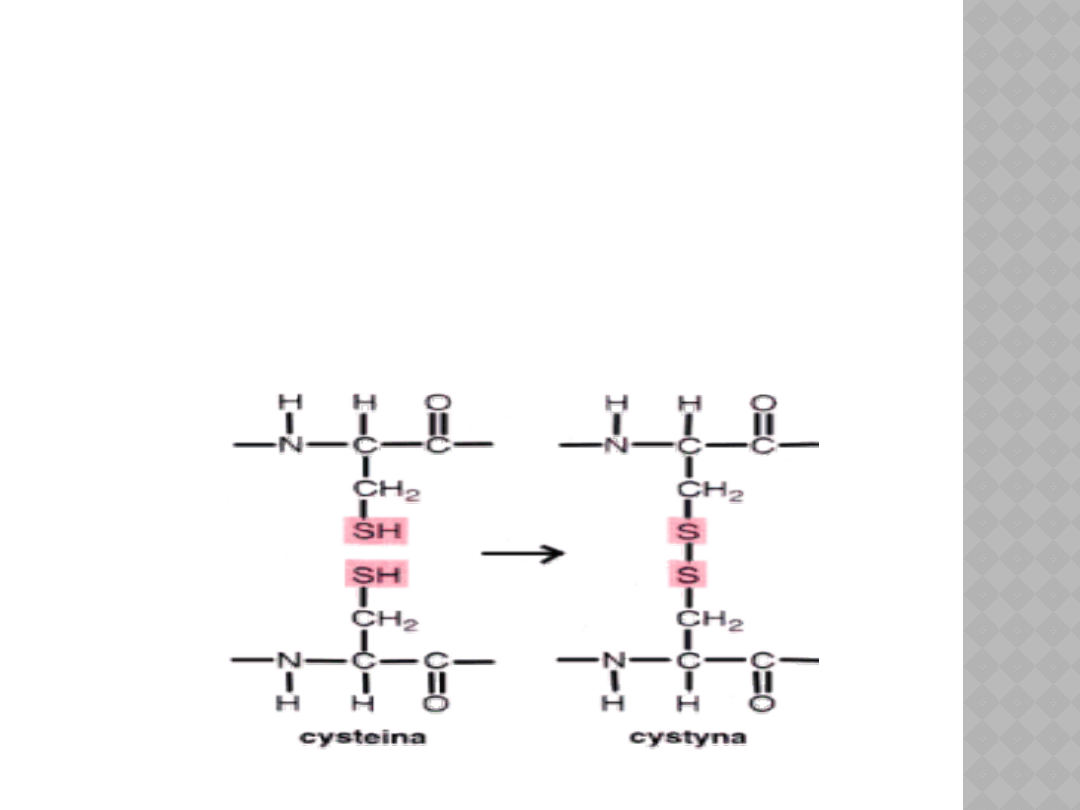
Bardzo charakterystycznym przykładem
wiązań stabilizujących trzeciorzędową
strukturę białek są tzw. "mostki
dwusiarczkowe",

BIAŁKA
Struktura czwartorzędowa – dotyczy
białek zbudowanych z dwóch lub więcej
łańcuchów peptydowych. Jest
charakterystyczna dla białek
oligomerycznych. (zawierających kilka
podjednostek). Podjednostki białek są to
niezależnie sfałdowane łańcuchy
polipeptydowe lub całe białka, będące
tylko składnikiem dużego kompleksu
białkowego.

STRUKTURA
CZWARTORZĘDOWA
Podobny zestaw oddziaływań reszt
aminokwasowych pomiędzy sobą oraz z
rozpuszczalnikiem jest
charakterystyczny dla czynników
stabilizujących strukturę
czwartorzędową białek
oligomerycznych. Często się zdarza, że
powierzchnie styku poszczególnych
podjednostek oligomeru zawierają dużą
ilość aminokwasów hydrofobowych.
Efektem tego jest "sklejenie"
podjednostek i "uszczelnienie" przed
wniknięciem rozpuszczalnika.
Hemoglobina składa się z czterech
podjednostek

REAKCJE
CHARAKTERYSTYCZNE BIAŁEK
Denaturacja – zmiana własności białka
spowodowana przez czynniki niszczące
struktury drugo-, trzecio- i
czwartorzędowe.
Denaturację białka spowodować
mogą:
podwyższona temperatura
promieniowanie rentgenowskie i
jonizujące
sole metali ciężkich
silne kwasy i zasady
rozpuszczalniki organiczne

REAKCJE
CHARAKTERYSTYCZNE BIAŁEK
Wysalanie – proces odwracalny nie
narusza przestrzennej struktury białka,
dlatego po dodaniu wody wytrącony
osad rozpuszcza się.
Czynnikiem powodującym wysalanie
jest NaCl
Proces wytrącania się osadu w
roztworze koloidalnym nazywamy
koagulacją a proces odwrotny to
peptyzacja.
Zol ↔ żel

REAKCJE
CHARAKTERYSTYCZNE BIAŁEK
Reakcja biuretowa – w reakcji białka z świeżo
strąconym wodorotlenkiem miedzi(II) tworzy się
związek kompleksowy o barwie niebieskofioletowej.
Reakcja ksantoproteinowa – pod wpływem
stężonego roztworu kwasu azotowego(V) zachodzi
nitrowanie pierścieni aromatycznych zawartych w
niektórych resztach aminokwasów białkowych.
Powstałe pochodne nitrowe mają żółte zabarwienie.
Procesem charakterystycznym dla białek jest ich
hydroliza w środowisku kwasowym lub
zasadowym, prowadzi ona do zerwania wiązań
peptydowych i rozpadu łańcucha polipeptydowego
na aminokwasy.
Document Outline
- Slide 1
- Aminokwasy
- Slide 3
- Właściwości ogólne aminokwasów
- Właściwości ogólne aminokwasów
- Właściwości ogólne aminokwasów punkt izoelektryczny
- Właściwości ogólne aminokwasów
- Amfoteryczność aminokwasów
- Podział aminokwasów
- Wiązanie peptydowe
- Powstawanie wiązania peptydowego
- Aminokwasy białkowe
- PRZYKŁADY AMINOKWASÓW BIAŁKOWYCH
- PRZYKŁADY AMINOKWASÓW BIAŁKOWYCH
- PRZYKŁADY AMINOKWASÓW BIAŁKOWYCH
- Konfiguracja aminokwasów
- Konfiguracja aminokwasów
- Konfiguracja aminokwasów
- peptydy
- peptydy
- białka
- białka
- białka
- Struktura helisy
- Struktura pofałdowanej kartki
- białka
- Slide 27
- Slide 28
- białka
- Struktura czwartorzędowa
- Reakcje charakterystyczne białek
- Reakcje charakterystyczne białek
- Reakcje charakterystyczne białek
Wyszukiwarka
Podobne podstrony:
01 Aminokwasy, peptydy, białka, enzymyid 3054 ppt
68 Aminokwasy peptydy i bialka(1)
68 Aminokwasy peptydy i bialka
Aminokwasy,peptydy,białka i inne
Aminokwasy, peptydy, białka
Chemia 6 Aminokwasy Peptydy i Białka
AMINOKWASY, PEPTYDY, BIAŁKA
Aminokw,peptydy,białka,enzymy
01 Aminokwasy, peptydy, białka, enzymyid 3054 ppt
Aminokwasy, peptydy, białka
Chemia 6 Aminokwasy Peptydy i Białka
Peptydy i białka
8 AMINOKWASY, PEPTYDY, BIA id 4 Nieznany (2)
Æwiczenie 7 Aminokwasy, peptydy i bia³ka
Peptydy i białka
AMINOKWASY I PEPTYDY
więcej podobnych podstron