
Immunoterapia
nowotworów.
Strategie i kliniczne zastosowanie.
Rafał Mazurek

Definicja nowotworu.
Nowotwór (łac. neoplasma)
- grupa chorób,
w których komórki organizmu dzielą się
w sposób niekontrolowany przez
organizm, a nowo powstałe komórki
nowotworowe nie różnicują się w typowe
komórki tkanki. Utrata kontroli nad
podziałami jest związana z mutacjami
genów kodujących białka uczestniczące
w cyklu komórkowym: protoonkogenami i
antyonkogenami. Mutacje te powodują,
że komórka wcale lub niewłaściwie
reaguje na sygnały z organizmu

• Powstanie nowotworu jest procesem
wieloetapowym
• Kancerogeny nie wywołują bezpośrednio
rozwoju nowotworu (indukują w
organizmie powstanie czynników
pośrednich, które uszkadzają DNA)
• W organizmie człowieka występują
naturalne czynniki antykancerogenne
(np. witaminy C i E, glutation, enzymy
[np. dysmutaza, katalaza], geny
kodujące białka, które hamują cykl
komórkowy [np. p53], enzymy
naprawiające DNA)

ŻADNEMU z wymienionych wcześniej
czynników chroniących przed rozwojem
nowotworu nie pomaga układ
immunologiczny!!!
Odgrywa on dość istotną rolę dopiero, kiedy
powstanie komórka nowotworowa.
Niemniej jednak w przypadku przewlekłej
immunosupresji zwiększa się ryzyko
zachorowań na różnego rodzaju nowotwory
(np. chłoniaki, mięsak Kaposiego) → układ
immunologiczny musi mieć duży udział w
odporności przeciwnowotworowej!

Antygeny nowotworów
• W przypadku choroby nowotworowej,
u pacjentów obserwuje się
podwyższoną aktywność
immunologiczną, która polega na:
Podwyższonym stężeniu przeciwciał
przeciwko komórkom nowotworowym
Aktywności immunologicznej limfocytów (np.
cytotoksyczność wobec własnych komórek
nowotworowych)
• Większość antygenów powstaje
spontanicznie i charakteryzuje się
brakiem swoistości

• Antygeny nowotworowe są bardzo
ważne w terapii; wykorzystywane są
w:
Wykrywaniu
Monitorowaniu
Leczeniu nowotworów (tworzenie przeciwciał
monoklonalnych, produkcja szczepionek)
• Bardzo ważna jest swoistość tych
antygenów (charakterystyczne dla
danego nowotworu)

Immunoterapia
Jest stosowana jako uzupełnienie
konwencjonalnych metod leczenia
(np. radio-, chemioterapii, czy
zabiegów chirurgicznych)
W przypadku niektórych nowotworów
może stanowić pierwszą metodę
leczenia!

• Często badania dotyczące immunoterapii
in vitro/na zwierzętach wychodzą
pomyślnie; w przypadku ludzi (badania
kliniczne) nie można w większości
uzyskać równie dobrych wyników, co jest
wynikiem:
a) Komórki nowotworowe człowieka są
bardzo mało immunogenne (przeżywają
tylko, te które potrafią obronić się przed
ludzkim układem immunologicznym)
b) Komórki nowotworowe u człowieka są
charakteryzują się heterogennością
(komórki różnią się fenotypowo – różna
ekspresja poszczególnych antygenów)

FAZY BADAŃ KLINICZNYCH
I.
Ocena toksyczności terapii; określenie
maksymalnej tolerowanej dawki leku;
ustalenie sposobu leczenia;
II.
Określenie typu nowotworu, który jest
najbardziej wrażliwy na badaną terpię
III.
Ocena przewagi nowej metody/leku nad
standardowymi metodami/lekami;
określenie śmiertelności

3 FORMY IMMUNOTERAPII:
1.Czynna
2.Bierna
3.Adoptywna

Immunoterapia CZYNNA
• Polega na wzmożeniu aktywności
immunologicznej pacjenta;
• Podaje się komórki nowotworowe lub
ich antygeny (czynna swoista)
• Można również osiągnąć taki efekt
stymulując układ immunologiczny
(np. cytokinami – czynna nieswoista)

Immunoterapia BIERNA
•Opiera się na podaniu
przeciwciał pacjentowi;
•Przeciwciała są swoiste,
monoklonalne;

Immunoterapia
ADOPTYWNA
•Polega na podaniu dożylnym
pacjentowi komórek układu
immunologicznego;
•Są one wcześniej
(pozaustrojowo) odpowienio
aktywowane

Metody immunoterapii:
I.
SWOISTE
Terapia „szczepionkami”
przeciwnowotworowymi
Terapia przeciwciałami
Immunoterapia adoptywna
II.
NIESWOISTE
Immunoterapia cytokinami
Terapia komórkami układu
immunologicznego
Terapia preparatami immunostymulującymi
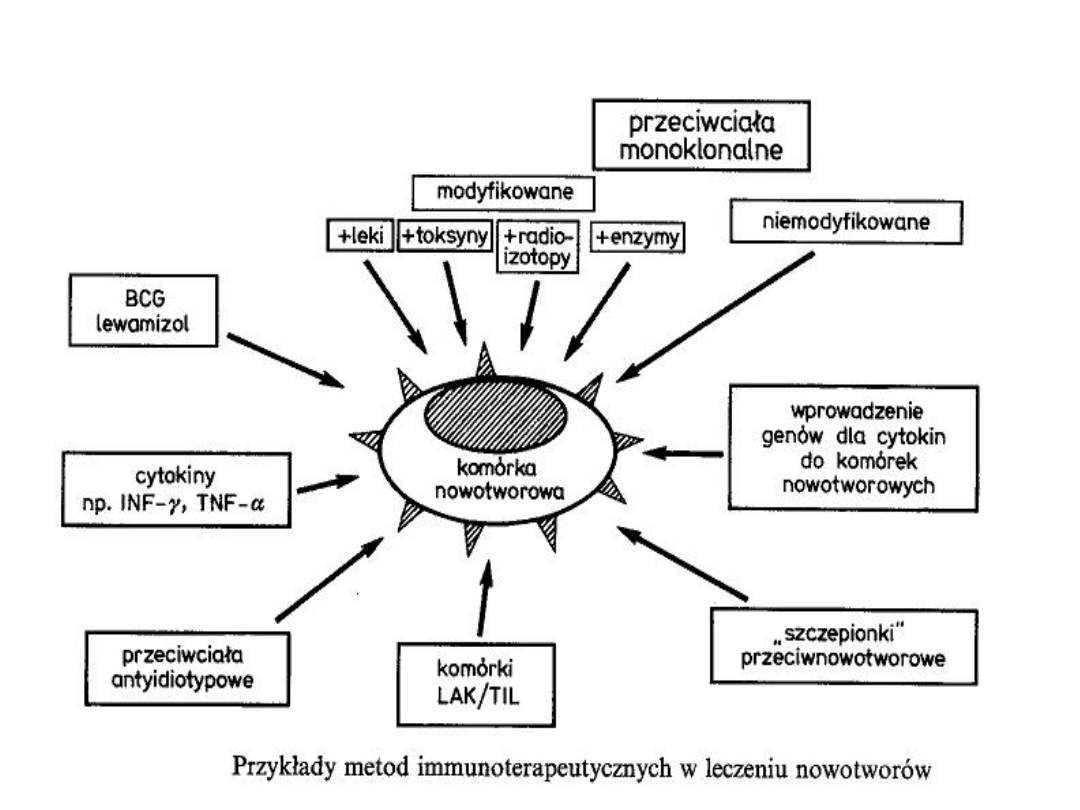

Immunoterapia nieswoista
Leczenie cytokinami
• Polega na nieswoistej aktywacji
mechanizmów obronnych
organizmu;
• Cytokiny – substancje zdolne do
modulowania proliferacji i funkcji
wielu rodzajów komórek (nie
tylko układu immunologicznego!)

Właściwości cytokin
(dzięki, którym możliwe jest ich stosowanie
w immunoterapii nowotworów)
• Bezpośredni efekt cytotoksyczny (np.
TNF-α)
• Wpływ na migrację limfocytów (np. IL-1)
• Zwiększenie wrażliwości komórek
nowotworowych (np. IFN-γ)
• Hamowanie proliferacji komórek (np. IFN)
• Efekt aktywujący komórki układu
immunologicznego [komórki NK] (np.
GM-CSF, IL-4)

• Białaczka włochatokomórkowa
• Przewlekła białaczka szpikowa
(IFN = uzupełnienie)
• Mięsak Kaposiego (uzupełnienie)
• Czerniak i rak nerki
(uzupełnienie)
Powodzenie terapii IFN-α:

Właściwości IFN-α determinujące jego
efekt p-nowotworowy:
• Wzmaganie ekspresji MHC na
komórkach nowotworowych
• Nasilenie róznicowania limfocytów
• Aktywacja komórek (NK, makrofagi)
• Nasilenie sekrecji innych cytokin
• Efekt antyangiogenny (hamowanie
tworzenia naczyń krwionośnych)

IL-2 → inna cytokina stosowana
w leczeniu nowotworów
• Stosowana w leczeniu (jest stosowana jako
uzupełnienie) raka nerki i czerniaka.
• Aktywuje komórki LAK lub TIL (dlatego
czasami podaje się ją jednocześnie z nimi)
LAK (Lymphokine activated killer cells) –
komórki NK aktywowane limfokinami
TIL (Tumor Infiltrating Lymphocytes) –
komórki T naciekające nowotwór

Immunoterapia nieswoista
Terapia komórkami układu
immunologicznego
• Lata 80’ pierwsze próby leczenia
nowotworów za pomocą komórek LAK.
• Podstawowa metoda leczenia polegała
na:
Podawanie dużych dawek IL-2 (co 8h przez 5 dni –
aktywacja prekursorów LAK)
Odzyskanie LAK z krwi w procesie leukaferezy
Hodowanie komórek in vitro + stymulacja IL-2
Wyhodowane komórki podawano pacjentom (od
których te komórki pochodziły)
Dodatkowe podanie IL-2
• Stosowano również inne warianty terapii

Skuteczność tej terapii nie
przyniosła zadowalających
efektów (uzyskano
niewielki efekt leczniczy
jedynie w przypadku
czerniaka, raka nerki i
wątroby)

• Kolejną grupą komórek wykorzystaną
w leczeniu nowotworów jest grupa
makrofagów
• Badania in vitro wykazały, że
charakteryzuje je bardzo silny efekt
cytotoksyczny w stosunku do
komórek nowotworowych (po
wcześniejszej aktywacji)
• Najsilniejszym ich aktywatorem jest
IFN-γ
• Źródłem makrofagów w badaniach
były monocyty izolowane z krwi

Czynniki stymulujące wzrost in
vitro:
1. IFN-γ
2. GM-CSF
3. 1,25-dihydroksywitamina D3
• Makrofagi podawano systemowo
(dożylnie) lub miejscowo (do jamy
otrzewnej) – drugi wariant okazywał
się być korzystniejszy

Immunoterapia nieswoista
Terapia preparatami immunostymulującymi
• Mechanizmy odporności (w tym
nowotworowej) są osłabione u
pacjentów z zaawansowanymi
postaciami nowotworów.
• Wyniki badań klinicznych były
dość zadowalające → włączenie
tej metody do standardów terapii
nowotworowej

•
Opracowano dwie metody, które
zasługują na zwrócenie uwagi:
I. Wlew zawiesiny BCG do pęcherza
moczowego; taki zabieg zmniejsza
odsetek pooperacyjnych nawrotów
nowotworu;
II. Dotyczy raka okreżnicy; połączenie
lewamizolu (immunostymulant) z 5-
fluorouracylem; uzupełnienie terapii
chirurgicznej; zmniejszenie
nawrotów i przedłuża przeżycie;

Leczenie czerniaka
(nieswoiste)
• W leczeniu czerniaka przy pomocy
immunoterapii nieswoistej jak dotąd
prowadzono badania wypróbowując
TNFα, interferony oraz interleukiny 2,
6, 10, 12 i 15. Jednak wyniki
zachęcające do dalszych prób
leczenia uzyskały jedynie interferon
alfa (INFα) oraz interleukina 2.

• Mechanizm działania interferonu alfa
związany jest z ekspresją genów,
których produkty aktywują komórki
prezentujące antygeny nowotworowe
oraz komórki zdolne do niszczenia
innych komórek (limfocyty T
cytotoksyczne). INFα był podawany
pacjentom podskórnie. Terapia ta wiąże
się z występowaniem objawów
paragrypowych (dreszcze, gorączka
brak łaknienia), co może być przyczyną
konieczności zmniejszenia dawki
podawanego interferonu i tym samym
zmniejszenia jego skuteczności.

• Drugi z modulatorów odpowiedzi
immunologicznej badany w terapii
nieswoistej, czyli IL2, jest odpowiedzialny
za migrację leukocytów poza naczynia.
Cytokina ta powoduje również aktywację
limfocytów T i komórek NK (ang. Natural
Killers) oraz LAK (ang. Lymphokine-
Activated Killer). Wśród kilkunastu
procent pacjentów (którzy odpowiedzieli
na leczenie) obserwowano także
długoletnie całkowite remisje. Jednak
terapia IL2 wiąże się z wysoką
toksycznością (!), co u części chorych
doprowadziło do konieczności przerwania
leczenia (udział zgonów wywołanych
leczeniem sięga 4%).

• Przy temacie immunoterapii
nieswoistej należy także wspomnieć o
immunostymulatorach pochodzących
z obcych organizmów. Ich przykładem
jest BCG (Bacillus Calmette-Guérin),
które może być wykorzystywane do
miejscowego leczenia. Szczepionkę
BCG podaje się jednorazowo do danej
zmiany, co powoduje zahamowanie
wzrostu guza. Należy podkreślić, że
jest to sposób leczenia zmian
powierzchownych, co powoduje, że
chorzy często umierają z powodu
przerzutów do narządów
wewnętrznych.

Leczenie czerniaka (swoiste)
• Immunoterapia swoista czerniaka złośliwego
opiera się– mówiąc w uproszczeniu- na
stymulowaniu organizmu do zwiększonej
prezentacji antygenów zlokalizowanych na
komórkach czerniaka i tym samym do
produkcji specyficznych przeciwciał
skierowanych przeciwko tym antygenom
(jest to tak zwana odpowiedź humoralna) czy
do powstania cytotoksycznych limfocytów T
(jest to tak zwana odpowiedź komórkowa).

• Komórki nowotworowe czerniaka
charakteryzują się występowaniem
antygenów będących potencjalnym
punktem uchwytu dla odpowiedzi układu
odpornościowego. Należą do nich fragmenty
białek np. MAGE (ang. melanoma antigen
gene), MART (ang. melanoma antigen
recognized by T-cells), tyrozynaza czy
gangliozydy GM2, GM3. Ponadto możemy
wykorzystać wzbudzenie odporności
przeciwko tzw. antygenom różnicowania
znajdującym się na komórkach czerniaka i
prawidłowych melanocytach (komórki
barwnikowe skóry) czy w nabłonku
barwnikowym siatkówki, a także przeciwko
antygenom embrionalnym występującym na
zdrowych komórkach tylko w stadium
embriogenezy (stadium zarodka).

• Najprostszą metodą swoistej immunoterapii jest
zastosowanie całych komórek nowotworowych
(uprzednio „unieszkodliwionych” najczęściej poprzez
napromieniowanie). Jedną z możliwości jest
stosowanie szczepionek opartych na komórkach
autologicznych (czyli pochodzących od samego
chorego). Terapia taka wymaga uzyskania
odpowiedniej liczby komórek, co w wielu przypadkach
okazuje się niemożliwe, zwłaszcza, gdy leczenie
uzupełniające jest prowadzone bezpośrednio po
zabiegu chirurgicznym. Rozwiązaniem problemu, a
zarazem drugą możliwością „tworzenia” szczepionek
komórkowych jest wykorzystanie komórek tzw. linii
ustalonych (szczepionki allogeniczne– opierające się
na komórkach pochodzących od innego chorego).
Przedstawicielem tej grupy jest szczepionka
„Cancervax” składająca się z trzech ustalonych linii
ludzkiego czerniaka. W badaniach obejmujących 157
chorych w IV stopniu zaawansowania choroby
odpowiedzi kliniczne uzyskano u 15-20% chorych
(badania II fazy).

• Genetycznie zmodyfikowane szczepionki
komórkowe (GMTV- ang. genetically
modifified tumor vaccines) są kolejną
możliwością w walce z nowotworami. Terapia
GMTF polega, tak jak terapia szczepionkami I
generacji, na podawaniu choremu komórek
nowotworowych, które mają za zadanie
pobudzić układ odpornościowy. Jednak
uprzednio są one wzbogacane o gen(y)
cząsteczek MHC koniecznych do prezentacji
antygenów, samych antygenów czerniaka,
czy wreszcie różnych cytokin jak interleukina
2, interleukina 6, których zadaniem jest
zwiększanie odpowiedzi
przeciwnowotworowej. Istnieje cały szereg
tego typu szczepionek będących w fazie
badań klinicznych.

• Jedną z nich jest szczepionka GMTV
modyfikowana kompleksem genów
interleukiny 6 ( IL-6) oraz agonistycznego
receptora (sI-6R). W badaniach II fazy
wykazano że u 22 chorych (54%)
zaobserwowano kliniczną korzyść z leczenia,
w tym u 5 chorych stwierdzono całkowitą
remisję, u 4 częściową odpowiedź, a u 13
stabilizację choroby. Natomiast u 19 chorych
(co stanowiło 46%) niestety nastąpiła
progresja. Objawy uboczne związane z jej
stosowaniem były minimalne i u żadnego z
chorych nie spowodowały przerwy w leczeniu.
U chorych stwierdzono wzrost aktywności
komórek CTL i NK, a także wzrost stosunku
limfocytów Th1 do Th2, co świadczy o
aktywizacji swoistej komórkowej odpowiedzi.
Obecnie przeprowadzane są badania III fazy.

DZIĘKUJĘ ZA UWAGĘ
Bibliografia:
„Immunologia” – J.Gołąb, M. Jaóbiskiak,
W. Lasek
Wikipedia.pl -http://pl.wikipedia.org/
Hylostet – „Immunoterapia czerniaka
złośliwego…” -
http://hylostet.pl/igm/article/41/
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
Wyszukiwarka
Podobne podstrony:
Immunologia nowotworów
Immunologia Nowotworów
Immunoterapia nowotworów
immunologia nowotworow
Immunologia nowotworow ok, Immunologia
immunologia nowotworów
IMMUNOLOGIA NOWOTWORÓW
199611 immunoterapia nowotworow
Immunohistochemia nowotworów
Immunologia nowotworów
Immunologia Nowotworów
Immunologia nowotworoTŽ w, niedobory odpornosTŽ ci, psychoneuroimmunologia
Immunologia Nowotworów
Immunoterapia nowotworów
immunologia nowotworow
więcej podobnych podstron