
2.4. Miareczkowanie
strąceniowe (precypitometria)
U podstaw metod miareczkowania strąceniowego
leży reakcja tworzenia trudno rozpuszczalnych osadów
z odpowiednich jonów.
Zalety metody:
• selektywna
• szybka w wykonaniu
• prostota
Precypitometria
____________________________________________________________________________________________________________________________________________
Titrant - roztwór odczynnika strącającego.
Od niego pochodzi nazwa metody:
1.Argentometria
(argentum łac. srebro)-
miareczkowanie
roztworem AgNO
3
lub AgClO
4
;
stosowana głównie do Cl
–
, Br
–
, I
–
.
2
. Merkurometria
– miareczkowanie solami
Hg
+
roztwór H
2
(NO
3
)
2
– głównie do Cl
–
, Br
–
,
szczególnie Cl
–
w wodach i ściekach
Hg
2
2+
+ 2X
–
Hg
2
X
2

Precypitometria
____________________________________________________________________________________________________________________________________________
Przykłady metod miareczkowania strąceniowego
1.Miareczkowanie bezpośrednie
– metoda Mohra
2. Odwrotne (odmiareczkowanie nadmiaru)
- metoda Volharda

Precypitometria
Przykłady metod
miareczkowania strąceniowego
____________________________________________________________________________________________________________________________________________
Miareczkowanie bezpośrednie –
metoda Mohra
X
–
+ Ag
+
=AgX
X=Cl
–
, Br
–
Wskaźnik PK - roztwór K
2
CrO
4
2Ag
+
+ CrO
4
2–
= Ag
2
CrO
4
początek
koniec (PK)
przemiareczkowanie

Precypitometria
Przykłady metod
miareczkowania strąceniowego
____________________________________________________________________________________________________________________________________________
Charakterystyka analityczna metody Mohra
1. Metoda miareczkowania bezpośredniego
2. Nadaje się tylko do oznaczania Cl
–
i Br
–
(AgI i
AgSCN silnie adsorbują jony CrO
4
2–
).
3. Nadaje się tylko dla roztworów o 6,5<pH
<10,5 gdyż:
•
w roztworach kwaśnych rozpuszcza się
Ag
2
CrO
4
2CrO
4
2–
+ 2H
+
= Cr
2
O
7
2–
+ H
2
O
•
w roztworach zasadowych wytraca się jon
Ag
+
2Ag
+
+ 2OH
–
= 2AgOH
2Ag
2
O
+
H
2
O

Precypitometria
____________________________________________________________________________________________________________________________________________
Charakterystyka analityczna metody Mohra, cd
c
4. W oznaczeniu
przeszkadzają:
•
inne jony tworzące trudno rozpuszczalne osady z
Ag
+
,
np.: CO
3
2–
, Br
–
, I
–
, PO
4
3–
, AsO
4
3–
• jony Fe
3+
lub Al
3+
, które wytrącają się w postaci
wodorotlenków
w stosowanym zakresie pH
• kationy Ba
2+
i Pb
2+
, tworzące trudno
rozpuszczalne chromiany
• jony Fe
2+
, które redukują Ag
+
do metalicznego Ag.

Precypitometria
____________________________________________________________________________________________________________________________________________
Charakterystyka analityczna metody Mohra, cd
5. Metoda wymaga ścisłego przestrzegania stężenia wskaźnika
6. Metoda ma mały skok krzywej miareczkowania (mały Ir
AgCl)
,
więc jest mało precyzyjna
7. Metodę można stosować do oznaczania Ag
+
przez
miareczkowanie odwrotne (nadmiar NaCl i odmiareczkowanie
chlorków)

Precypitometria
Przykłady metod
miareczkowania strąceniowego
____________________________________________________________________________________________________________________________________________
Miareczkowanie odwrotne – metoda Volharda
1.X
–
+ Ag
+
=AgX + Ag
+
(nadmiar)
2. Odmiareczkowanie nadmiaru Ag
+
Ag
+
+ SCN
–
= AgSCN
Wskaźnik PK – jony Fe
3+
SCN
–
+ Fe
3+
=
Fe(SCN)
2+
(krwistoczerwony
kompleks)
Reakcja przeszkadzająca:
Fe(SCN)
2+
+ AgX AgSCN + Fe
3+
+ X
–

Precypitometria
____________________________________________________________________________________________________________________________________________
Charakterystyka analityczna metody Volharda
1. Metoda argentometryczna oparta na miareczkowaniu
odwrotnym
2. Nadaje się do oznaczania w środowisku kwaśnym
3. Precyzja wyników gorsza niż w metodzie Mohra
Precypitometria
____________________________________________________________________________________________________________________________________________
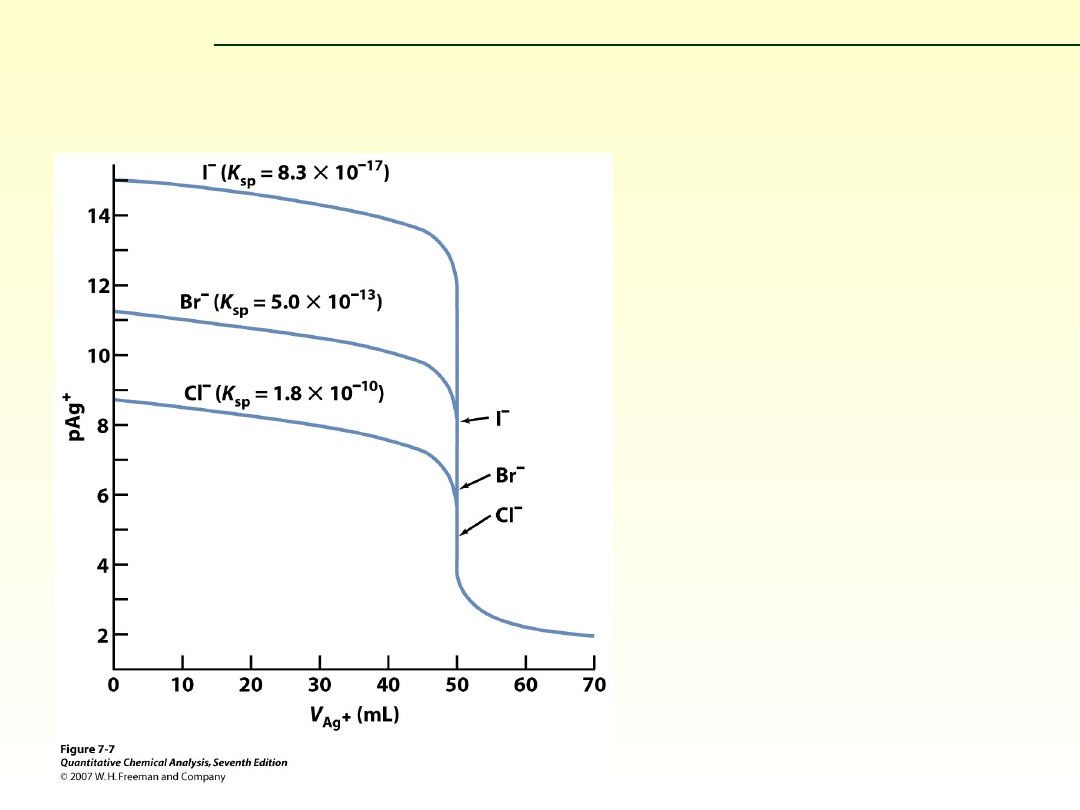
Krzywa miareczkowania argentometrycznego
Wpływ iloczynu rozpuszczalności na krzywe miareczkowania
Skok krzywej tym większy
im mniejsza wartość iloczynu
rozpuszczalności (im łatwiej
osad się wytrąca.
Precypitometria
Krzywa miareczkowania
argentometrycznego
____________________________________________________________________________________________________________________________________________
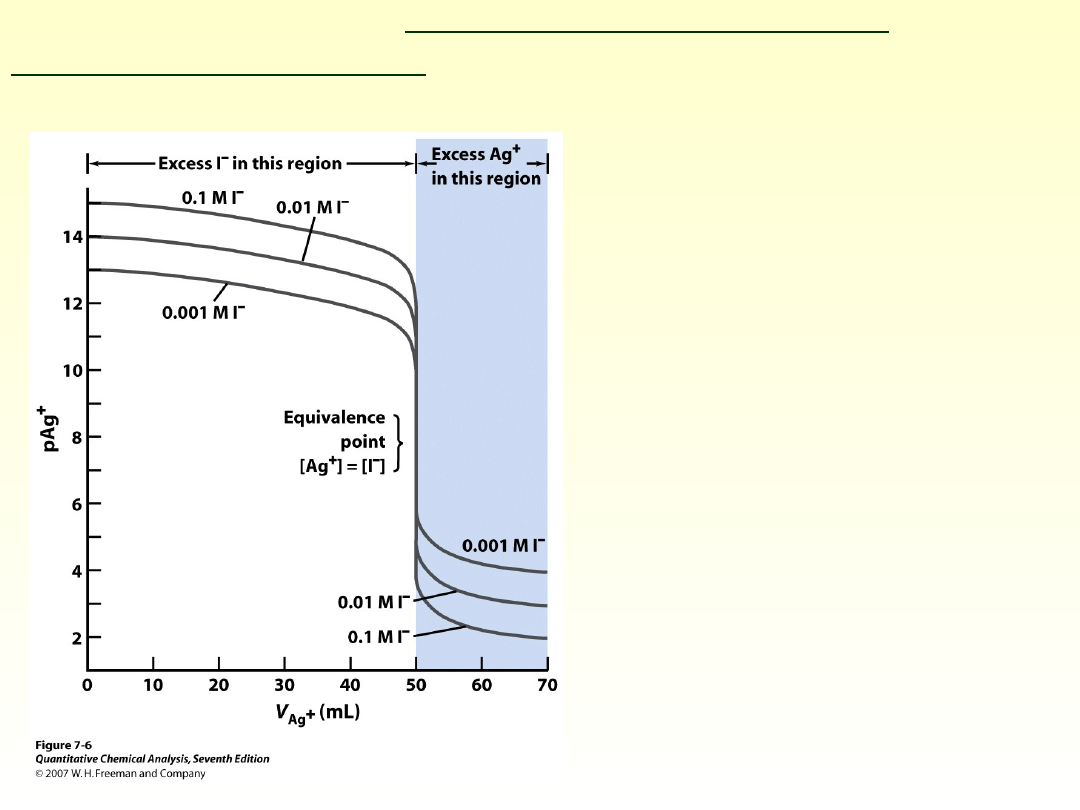
Im mniejsze stężenie
oznaczanego jonu,
tym większy skok
krzywej
miareczkowania
Krzywa miareczkowania jonów jodkowych za pomocą AgNO
3

Precypitometria
____________________________________________________________________________________________________________________________________________
Przykłady pytań:
1. Scharakteryzować krótko metodę Mohra oznaczania chlorków
(odpowiednie reakcje, warunki pH, jony przeszkadzające)
2. Scharakteryzować krótko metodę Wolharda oznaczania
halogenków(odpowiednie reakcje, wskaźnik)
Document Outline
Wyszukiwarka
Podobne podstrony:
Notatki precypitometria ikompleksonometria
Miareczkowanie precypitometryczne
kompeks precyp zadania
Precypitometria i kompleksometria (1), rok numero deux, chemia analityczna, I semestr
Aglutynacja i precypitacja, immunologia
KOMPLEKSONOMETRIA i precypitometria
Aglutynacja i precypitacja, Analityka Medycza Umed Łódź, II rok, Immunologia
5 Precypitometria
precypitatometria
10 analiza ilościowa miareczkowanie precypitometryczne
Miareczkowanie precypitometryczne
kompeks precyp zadania
więcej podobnych podstron