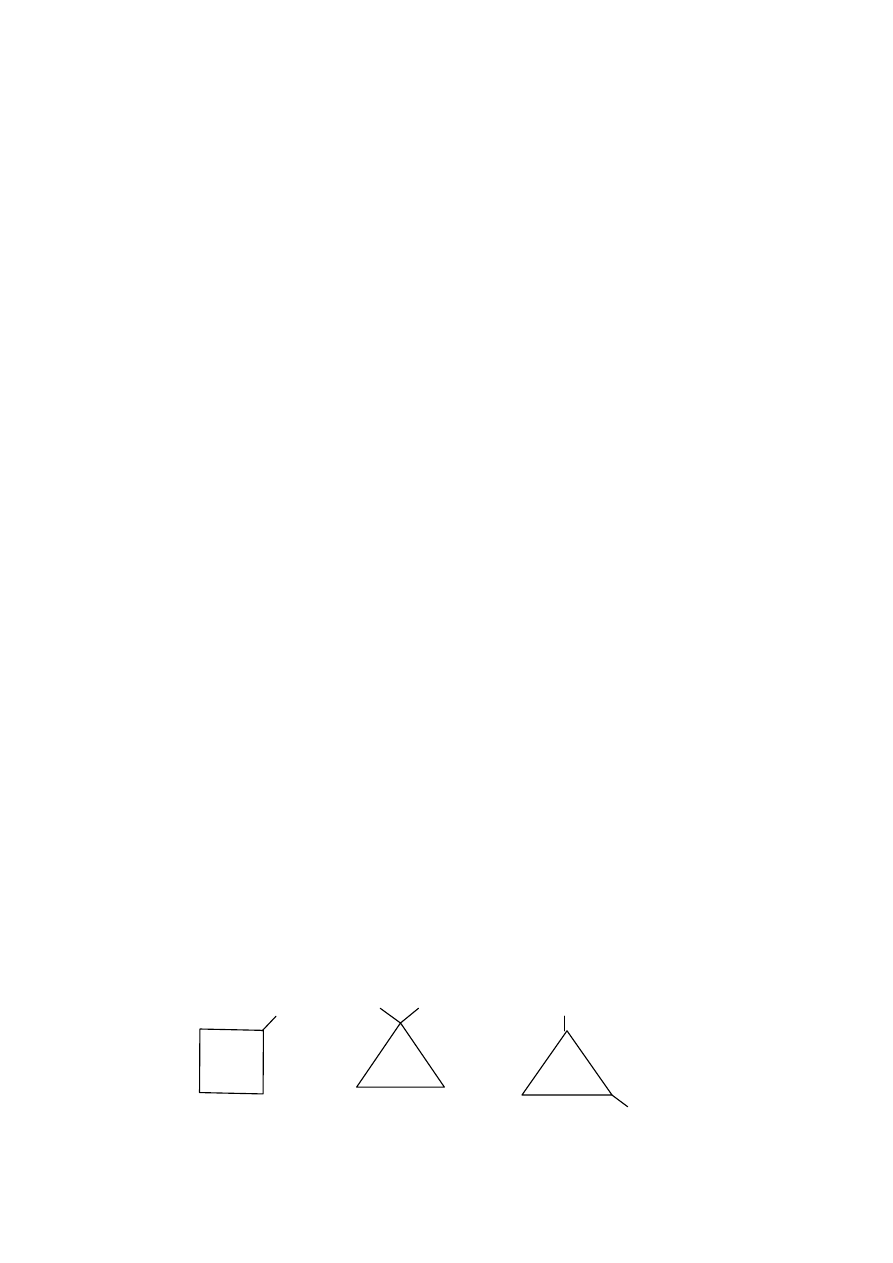
Cz. XXII - Alkohole monohydroksylowe
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą
hydroksylową (
- OH
).
1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Alkohole alifatyczne nasycone - pochodne alkanów R -
OH
, tworzą szereg
homologiczny alkanoli o ogólnym wzorze C
n
H
2n+1
-
OH
-
izomeria szkieletowa (łańcuchowa)
4
CH
3
-
3
CH
2
-
2
CH
2
-
1
CH
2
-
OH
; butan -
1
-
ol
(1
o
)
3
CH
3
-
2
CH -
1
CH
2
-
OH
;
2
-
metylo
propan-
1-
ol
(1
o
)
|
CH
3
-
izomeria położenia grupy funkcyjnej
4
CH
3
-
3
CH
2
-
2
CH
2
-
1
CH
2
-
OH
; butan -
1
-
ol
(1
o
)
1
CH
3
-
2
CH -
3
CH
2
-
4
CH
3
;
butan-
2
-
ol
(2
o
)
|
OH
Alkohole alifatyczne nienasycone (Uwaga: jeżeli grupa
-OH
związana jest
z węglem o hybrydyzacji
sp
2
lub
sp
to związki te
nie są alkoholami
)
- izomeria szkieletowa,
- izomeria położenia grupy funkcyjnej,
- izomeria położenia wiązania wielokrotnego
4
CH
2
=
3
CH
-
2
CH
2
-
1
CH
2
-
OH
; but-
3
-
en
-
1
-
ol
(1
o
)
4
CH
3
-
3
CH
=
2
CH
-
1
CH
2
-
OH
; but-
2
-
en
-
1
-
ol
(1
o
)
4
CH
≡
3
CH
2
-
2
CH
2
-
1
CH
2
-
OH
; but-
3
-
yn
-
1
-
ol
(1
o
)
4
CH
3
-
3
C
≡
2
C -
1
CH
2
-
OH
; but-
2
-
yn
-
1
-
ol
(1
o
)
Alkohole cykloalifatyczne
- izomeria pierścieniowa i izomeria położenia grupy funkcyjnej
OH
HO
CH
3
OH
1
1
1
2
CH
3
cyklo
butan
ol
(2
o
);
1
-
metylo
cyklo
propan-
1
-
ol
(3
o
);
2
-
metylo
cyklo
prapan-
1
-
ol
(2
o
)
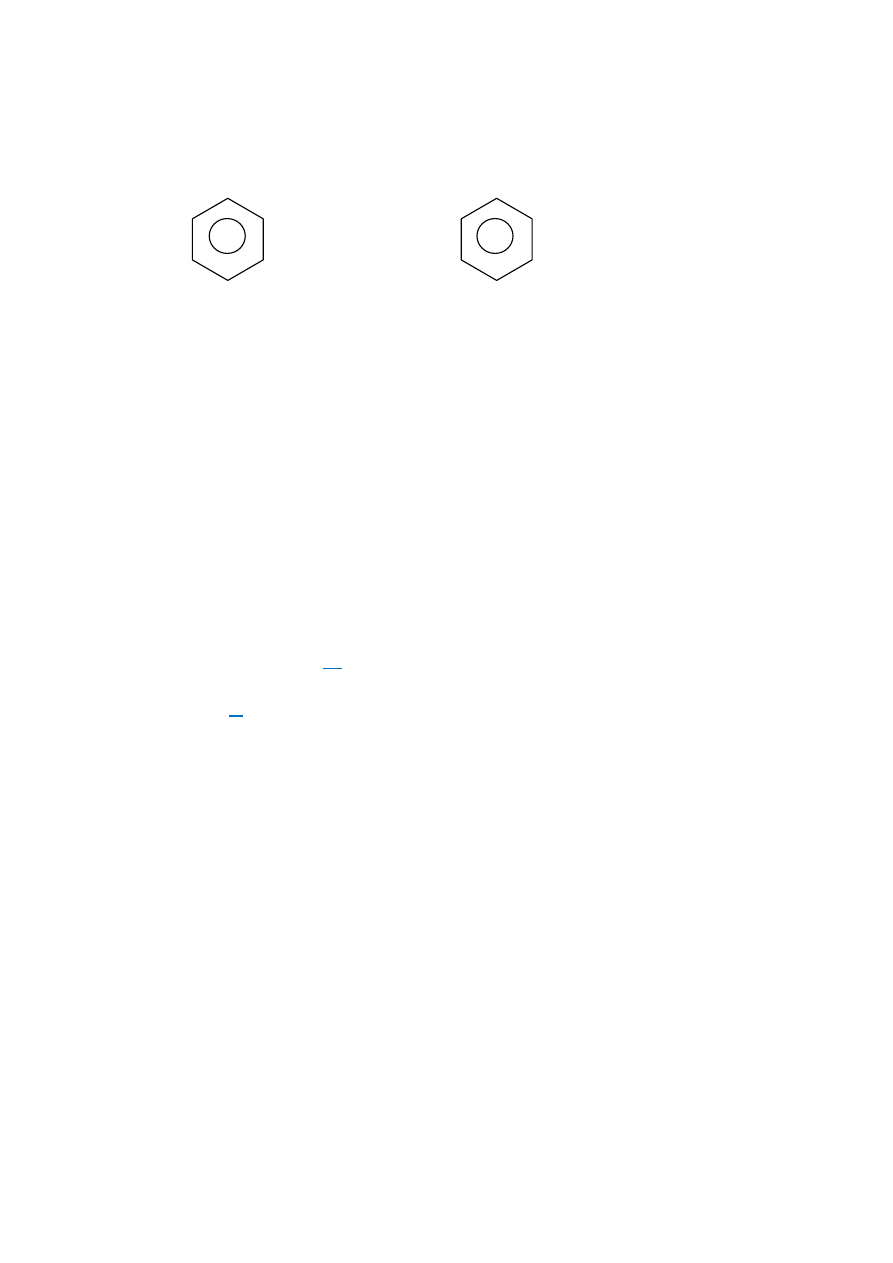
Alkohole aromatyczne
2
CH
2
-
1
CH
2
-
OH
(1
o
)
2
CH
3
-
1
CH
-
OH
(2
o
)
| |
2
-
fenylo
etan
ol
1
-
fenylo
etan
ol
2. Wybrane właściwości fizyczne
- do 12 at. C w cząsteczce są cieczami, od 12 at. C w cząsteczce są ciałami stałymi,
- wraz ze wzrostem masy cząsteczkowej wzrasta ich gęstość, maleje
rozpuszczalność w wodzie, od 11 at. C w cząsteczce są praktycznie
nierozpuszczalne, wzrasta T
t
i T
w
(w przypadku izomerów mogą wystąpić
odstępstwa),
Metanol: T
w
= 64,7
o
C, T
t
= - 97,8
o
C,
Etanol: T
w
= 78,3
o
C, T
t
= - 117,3
o
C,
- wysokie temp. wrzenia wynikają polarności grupy
-OH
, co prowadzi do
powstawania
wiązań wodorowych
i asocjacji cząsteczek alkoholu
R
\
R
δ-
O |
\ /
δ-
O|
- - - - -
H
δ+
/
H
δ+
- w trakcie rozpuszczania alkoholi w wodzie występuje
zjawisko kontrakcji
, tj.
zmniejszenia się objętości mieszanych cieczy o ok. 3%, zmniejszenie objętości
jest efektem powstawania krótszych wiązań wodorowych między dipolami
wody a cząsteczkami alkoholu (od wiązań wodorowych między cząsteczkami
alkoholu),
- gęstość alkoholi monohydroksylowych jest mniejsza niż gęstość wody,
3. Otrzymywanie alkoholi
Etanolu
da celów spożywczych i farmaceutycznych
- fermentacja alkoholowa
pod wpływem biokatalizatorów (enzymów), fermentacja zatrzymuje się po
osiągnięciu stężenia alkoholu etylowego ok. 18%
# fermentacja cukrów prostych: C
6
H
12
O
6
2C
2
H
5
OH + 2CO
2
↑,
# fermentacja dwucukrów: C
12
O
22
O
11
+ H
2
O 4C
2
H
5
OH + 4CO
2
↑,
# fermentacja skrobi: (C
6
H
10
O
5
)n + nH
2
O 2nC
2
H
5
OH + 2nCO
2
↑,

Dla celów technicznych i metodami laboratoryjnymi
I.
Hydroliza monohalogenoalkanów
w wodnych roztworach silnych
zasad [NaOH, KOH, Ca(OH)
2
], jest to reakcja
substytucji
nukleofilowej
(
Uwaga
: w środowisku stężonego alkoholu zachodzi
reakcja eliminacji halogenowodru i powstają
alkeny
)
CH
3
- CH
2
-
Cl
+
Na
-
OH
CH
3
- CH
2
-
OH
+
NaCl
H2O
Na
OH
↔
Na
+
+
OH
-
H
1/2
δ-
|
1/2
δ-
δ+
C
H
3
-
δ-
Cl
+
OH
-
HO
- - -
C
- - -
Cl
CH
3
-
OH
+
Cl
-
/ \
H H
stan przejściowy
- - -
; zdelokalizowane wiązanie wodorowe
- w przypadku halogenoalkanów II-rz (2
o
) reakcje przebiegają trudniej, niż
w przypadku I i III-rz,
- natomiast w przypadku halogenoalkanów III-rz (3
o
) reakcje zachodzą
znacznie łatwiej z tym, że dochodzi do heterolizy wiązania C -
X
(
X
podstawnik halogenowy) powstający karbokation atakuje grupę
OH
-
,
która jest lepszym elektrofilem niż
X
-
)
II.
Hydratacja alkenów w obecności H+ jako katalizatora (addycja wody) -
mechanizm karbokationu, zgodnie z regułą Markownikowa
CH
2
= CH
2
+ H-
OH
CH
3
- CH
2
-
OH
CH
3
- CH = CH
2
+ H -
OH
CH
3
- CH - CH
3
|
OH
III.
Hydroliza estrów
O
//
CH
3
- C -
O - CH
2
- CH
3
+ H-OH
CH
3
-COOH
+
CH
3
- CH
2
- OH
Etanian (octan) etylu Kwas etanowy(octowy) + etanol
4. Właściwości chemiczne alkoholi
Wodne roztwory alkoholi mają odczyn obojętny, nie ulegają dysocjacji
elektrolitycznej (jonowej), wykazują jeszcze słabsze właściwości kwasowe niż
woda,
Reagują z aktywnymi metalami (głównie litowce), produktem są
alkoholany
i wodór,
alkoholany
są związkami o charakterze soli słabych kwasów i
mocnych zasad, w roztworze wodnym ulegają
hydrolizie anionowej
, odczyn
wodnego roztworu jest
silnie zasadowy
;
2CH
3
- OH + 2Na 2CH
3
- ONa + H
2
↑; metanian sodu
CH
3
- ONa + H
2
O CH
3
-OH + Na
+
+ OH
-
CH
3
- O
-
+ H
2
O CH
3
- OH + OH
-

Nie reagują z zasadami (powstaje roztwór wodorotlenku w alkoholu),
W środowisku kwasowym reagują z kwasami karboksylowymi (w obecności
H
2
SO
4
, kationy wodorowe są katalizatorami reakcji), powstają estry i woda,
reakcje estryfikacyji są odwracalne;
O O
// //
CH
3
-C - OH
+
H - O
-
CH
3
- CH
3
↔
CH
3
- C -
O - CH
2
- CH
3
+ H
2
O
Etanian (octan) etylu
Alkohole tworzą również estry z kwasami nieorganicznymi (H
3
PO
4
, HNO
3
,
H
2
SO
4
), produktami są estry nieorganiczne;
CH
3
-
O - H
+
HO - SO
2
- OH
+
H - O
- CH
3
2H
2
O + CH
3
-
O
-
SO
2
-
O
- CH
3
Siarczan(VI) dimetylu
Alkohole są związkami palnymi,
Alkohole reagują z gazowym HCl, w reakcji bierze cała grupa funkcyjna
(-OH), reakcja przebiega w obecności H
2
SO
4
;
CH
3
- CH
2
-
OH
+
H
-
Cl
CH
3
- CH
2
-
Cl
+
H
2
O
Chloro
etan (pali się zielonym płomieniem)
Alkohole ulegają reakcji
dehydratacji (odwodnienia) - eliminacji wody
, reakcja
przebiega w obecności związków silnych odwadniających (np. stężony H
2
SO
4
i T > 140
o
C, w przypadku nadmiaru alkoholu i gdy T < 140
o
C powstają
odpowiednie etery:
H
2
SO
4
/T>140
o
C
CH
3
- CH
2
- OH CH
2
= CH
2
+ H
2
O
H
2
SO
4
/T<140
o
C
CH
3
- CH
2
-
O - H + HO
- CH
2
- CH
3
H
5
C
2
-
O
- C
2
H
5
+
H
2
O
Eter dietylowy
w obecności Al
2
O
3
i podwyższonej temperaturze, produktem są odpowiednie
alkeny, reakcja przebiega zgodnie z regułą Zajcewa;
T/Al
2
O
3
CH
3
- CH
2
- OH CH
2
= CH
2
+ H
2
O (eten)
T/Al
2
O
3
CH
3
- CH
2
- CH - CH
2
-
OH
CH
3
- CH
2
- CH = CH
2
+
H
2
O
| but-1-en
H

T/Al
2
O
3
CH
3
- CH - CH - CH
3
CH
3
- CH = CH - CH
3
+
H
2
O
| | but-2-en
H OH
Katalityczne utlenianie alkoholi: produktami katalitycznego utlenienia
alkoholi 1
o
są odpowiednie
aldehydy
, natomiast w przypadku alkoholi
2
o
są odpowiednie
ketony
, katalitycznymi utleniaczami mogą być: CuO,
KMnO
4
, K
2
Cr
2
O
7
;
O - H
O
|
T
//
CH
3
-
C
-
H
+
O = Cu
CH
3
-
C
-
H
+
Cu
+
H
2
O
|
H
Etanol (1
o
) etanal (aldehyd octowy)
O
-
H
|
T
CH
3
-
C
-
H
+
O = Cu
CH
3
-
C
- CH
3
+
H
2
O
+ Cu
| ||
CH
3
O
keton dimetylowy (propanon)
Propan-2-ol (2
o
)
Wykrywanie (identyfikacja) etanolu; odczynniki - K
2
Cr
2
O
7
+ H
2
SO
4
K
2
Cr
2
O
7
+ 4H
2
SO
4
+ 3
CH
3
- CH
2
- OH
barwa pomarańczowa etanol
K
2
SO
4
+
Cr
2
(SO
4
)
3
+ 3
CH
3
-CHO
+ 7H
2
O
barwa fioletowozielona etanal
Toksyczność alkoholi monohydroksylowych - maleje wraz ze wzrostem
długości łańcucha węglowego.
Wyszukiwarka
Podobne podstrony:
Alkohole polihydroksylowe id 58 Nieznany (2)
Alkohole i fenole 3 id 58102 Nieznany
Alkohole 13 id 58087 Nieznany (2)
alkohole i fenole 2 id 58101 Nieznany (2)
zestaw podstawowych drgan id 58 Nieznany
alkohol i kierowca id 58052 Nieznany
Zgloszenie zamiaru budowy id 58 Nieznany
alkohole i fenole 2 id 58114 Nieznany (2)
Alkohole 09 id 58086 Nieznany (2)
Alkohole i etery 3 id 58099 Nieznany
altera trex quarus72 ver2 id 58 Nieznany (2)
ZestawienieOcenElektrVer1 id 58 Nieznany
Zespol Turnera i Edukacja id 58 Nieznany
Alkohole i fenole 3 id 58102 Nieznany
58 2 id 41679 Nieznany (2)
Zi 58 id 590103 Nieznany
Alkohole id 58069 Nieznany (2)
58 id 41676 Nieznany
M W05 58 id 274845 Nieznany
więcej podobnych podstron