
Wydział Chemiczny Politechniki Gdańskiej
Katedra Technologii Leków i Biochemii
Kultury tkankowe i komórkowe roślin i zwierząt
PORÓWNANIE ILOŚCI I JAKOŚCI DNA WYIZOLOWANEGO Z KOMÓRKI
ROŚLINNEJ I ZWIERZĘCEJ
METODY BADANIA KWASÓW NUKLEINOWYCH:
1. TECHNIKI MIKROSKOPOWE
A. MIKROSKOPIA ELEKTRONOWA
Mikroskop elektronowy jest urządzeniem, którego zakres rozdzielczości wynosi
0,2-20 nm, co umożliwia oglądanie organelli komórkowych, wirusów i
makrocząsteczek biologicznych (np. DNA), niemniej jednak ograniczeniem
mikroskopu elektronowego jest brak możliwość oglądania próbek materii żywej.
Najbardziej popularną techniką uwidaczniania DNA jest metoda Klein-Schmidta.
W tej technice kroplę roztworu DNA w octanie amonu zawierającym cytochrom c,
nanosi się na powierzchnię octanu amonu. Po dotknięciu przez kroplę powierzchni,
tworzy się na niej cienki film zdenturowanego cytochromu c. Film ten zawiera pewną
ilość cząsteczek DNA, do której przyłącza się cienka warstwa cytochromu. Jeżeli do
tego filmu zostanie przyłożony mały obiekt kulisty, to dołączy się do niego kropla
zawierająca część filmu. Usunięcie fazy wodnej np. poprzez zanurzenie w alkoholu,
spowoduje stabilne przyleganie warstwy do filmu pokrywającego kulisty obiekt.
Technika ta zawiera wstępne barwienie pozytywne, np. octanem uranu. Metoda ta jest
stosowana do określania długości i formy DNA. Zmodyfikowana metoda Klein-
Schmidta pozwala natomiast zlokalizować specyficzne obszary w DNA m.in. określić
pozycje końców liniowego DNA w formie kolistej, identyfikować bardzo długie
cząsteczki izolowane z E.coli zainfekowanych fagiem
λ oraz określić kierunek
replikacji DNA faga
λ.
B. SKANINGOWA MIKROSKOPIA ELEKTRONOWA
Skaningowa mikroskopia elektronowa pozwala na badanie cech strukturalnych
obiektów biologicznych o wymiarach 3-20 nm w buforach czy w warunkach
zbliżonych do fizjologicznych. Znalazła ona zastosowanie w badaniach nad zginaniem
DNA na skutek różnych oddziaływań z białkami, oddziaływaniem przeciwciał z
różnymi formami DNA, w analizie relacji stechiometrycznych kompleksów białek z
kwasami nukleinowymi i badaniach struktury chromatyny.
C. MIKROSKOPIA SKANINGOWO-TUNELOWA
Mikroskopia skaningowo-tunelowa jest precyzyjną techniką charakteryzującą się
wysoką rozdzielczością - co najmniej 0,02
×0,3 nm, pozwalająca uzyskiwać obraz
trójwymiarowy. Za pomocą mikroskopu skaningowo-tunelowego bada się m.in.
kompleksy białek z kwasami nukleinowymi oraz topografię DNA.
2. ELEKTROFOREZA
1

Elektroforeza jest obecnie jedna z głównych metod identyfikacji, rozdzielania i
oczyszczania kwasów nukleinowych. W wersji podstawowej jest to prosta i szybka
technika używana do rozdzielania cząsteczek DNA, które nie mogą być rozdzielone
innymi technikami np. przez wirowanie w gradiencie gęstości.
Do fizycznego opisu elektroforezy służą takie parametry jak: wielkość
molekularna DNA - N
D
, średnia wielkość porów w żelu -
α, natężenie pola
elektrycznego -
ε;
T
k
Ea
Q
b
a
M
M
N
B
a
D
a
D
D
2
;
;
≡
≡
≡
ε
α
gdzie M
a
jest wielkością fragmentów DNA, które „pasują” do typowej wielkości porów
żelu
a,
Q
a
= M
a
l
D
λ
D
– ładunek cząsteczki o wielkości scharakteryzowanej przez M
a
.
A. ELEKTROFOREZA W ŻELU AGAROZOWYM
Agaroza to frakcja agaru oczyszczona z krasnorostów. Jest to polisacharyd
zbudowany z około 800 liniowo połączonych reszt heksozy (inaczej – 400 reszt
agarobioza). Agarobioza jest dwucukrem zbudowanym z D-galaktozy i 3,6-anhydro-L-
galaktozy. Powstawanie żelu agarozowego jest reakcją odwracalną, w wyniku której
pojedyncze, losowo zwinięte łańcuchy układają się w dwuniciową, helikalną strukturę
III-rzędową, które rozgałęziają się tworząc sieć. Wielkość porów żelu agarozowego
zależy od stężenia agarozy i określa zakres ciężaru makrocząsteczek np. DNA, RNA,
które można w niej elektroforetycznie rozdzielać.
Żel agarozowy stosuję się do rozdzielania DNA o szerokim zakresie mas
cząsteczkowych. Wadą elektroforezy w żelu agarozowym jest słaba rozdzielczość
frakcji DNA różniącego się poniżej 5% wielkości.
Stężenie agarozy [%] Zakres długości rozdzielanego liniowego DNA [kp.z]
0,3
0,6
0,7
0,9
1,2
1,5
2,0
5-60
1-20
0,8-10
0,5-7
0,4-6
0,2-3
0,1-2
Elektroforeza w żelu agarozowym prowadzona jest w aparatach ustawionych poziomo, a rozdział
elektroforetyczny prowadzony jest w buforze TBE
×1 (90 mM Tris-base, 90 mM kwas borowy, 2 mM
EDTA, pH 8) lub TAE
×1 (40 mM Tris-base, 40 mM lodowy kwas octowy, 1 mM EDTA, pH 8).
Cząsteczka DNA jest naładowana ujemnie w środowisku obojętnym i alkalicznym, a więc
umieszczona w polu elektrycznym, przemieszcza się w kierunku anody. DNA o tych samych masach
cząsteczkowych, ale różnych konformacjach charakteryzuje różna ruchliwość elektroforetyczna. Im
dłuższa jest cząsteczka DNA lub RNA tym dłużej odnajduje ona drogę poprzez pory żelu. Jeżeli
umieścimy DNA w żelu agarozowym i przyłożymy niskie napięcie to prędkość migracji DNA o różnych
ciężarach cząsteczkowych jest proporcjonalna do napięcia. Aby otrzymać optymalny rozdział DNA o
wielkości większej niż 2 kp.z, elektroforeza prowadzona jest w polu elektrycznym o natężeniu nie
większym niż 5V/cm. Powyżej tego napięcia fragmenty DNA przemieszczają się z prędkością
odwrotnie proporcjonalną do logarytmu ich ciężaru cząsteczkowego. Elektroforetyczne zachowanie
DNA w żelu agarozowym nie zależy od składu zasad azotowych i słabo zależy od temperatury. Jednak
2
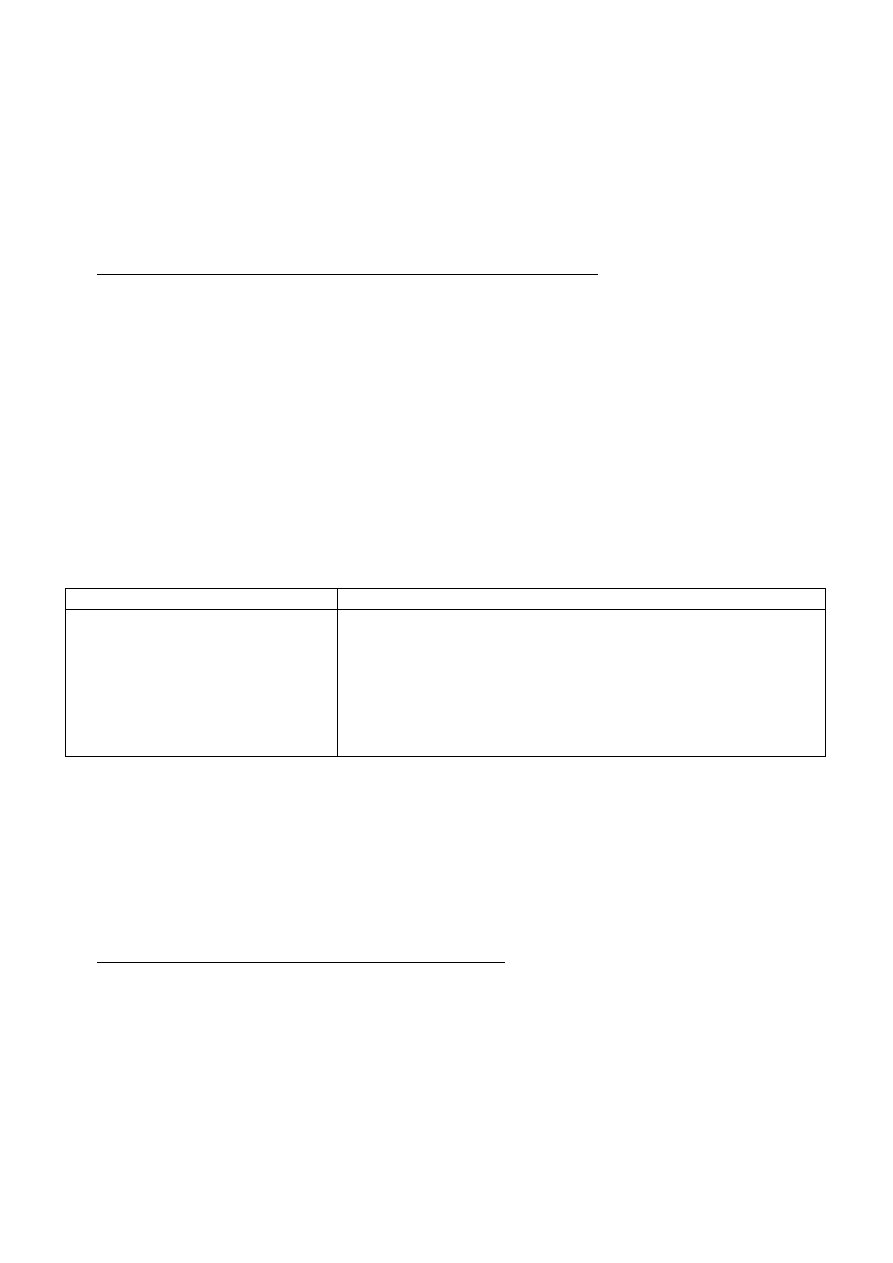
jeżeli stosuje się żele agarozowe o stężeniu mniejszym niż 0,5% należy elektroforezę prowadzić w
temperaturze około 4
°C.
Do uwidocznienia DNA po lub w trakcie elektroforezy stosowany jest rutynowo bromek etydyny
(EtBr), który interkaluje pomiędzy sąsiednie pary dwuniciowego DNA (powinowactwo EtBr do
jednoniciowego DNA jest znacznie słabsze). Należy pamiętać, że obecność związku interaklującego do
DNA w żelu agarozowym zmniejsza ruchliwość elektroforetyczną DNA o około 15%. Innym
barwnikiem DNA jest np. SYBR Green, którego czułość barwienia dwuniciowego DNA jest około 25
razy większa niż EtBr.
B. ELEKTROFOREZA W ŻELU POLIAKRYLAMIDOWYM (PAGE)
Elektroforeza w żelu poliakrylamidowym jest wykorzystywana do rozdzielania i analizy małych
fragmentów DNA lub białek. Najlepszy rozdział uzyskuje się dla DNA o długości mniejszej niż 1000
par zasad. W żelach tych można efektywnie rozdzielać także jednoniciowe fragmenty DNA i RNA.
Żel poliakrylamidowy powstaje w wyniku polimeryzacji N,N’-metylenobisakrylamidu z monomerami
akryloamidu w obecności wolnych rodników dostarczonych przesz nadsiarczan amonu i
stabilizowanych przez TEMED (N,N,N’,N’-tetrametylenodiamina). Stopień usieciowana żelu (udział
procentowy N,N’-metylenobisakrylamidu) stanowi czynnik wpływający na rozdzielenie fragmentów
jednoniciowego DNA.
Elektroforezę w żelach poliakrylamidowych prowadzona jest w aparaturze
ustawionej pionowo, a więc migracja cząsteczek DNA jest zgodna z kierunkiem siły
ciążenia, gdzie jednoniciowe DNA charakteryzują się spowolnioną, w stosunku do
dwuniciowego DNA, migracja w żelu. Rozdział elektroforetyczny prowadzony jest w
buforze TBE
×1. DNA w żelu poliakrylamidowym można wybarwiać za pomocą np.
EtBr lub Sybr Gold.
Stężenie poliakrylamidu [%] Zakres długości rozdzielanego liniowego DNA [kp.z]
3,5
5,0
8,0
12,0
15,0
20,0
1000-2000
80-500
60-400
40-200
25-150
6-100
Żele poliakrylamidowe mają przewagę nad żelami agarozowymi z kilku przyczyn:
- zdolność rozdzielcza żeli poliakrylamidowych jest tak duża, że można rozdzielać
cząsteczki DNA różniące się o 1 p.z.
- studzienkę żelu poliakrylamidowego można załadować znacznie większą ilością
DNA niż w żelu agarozowym
- DNA odzyskany z żelu poliakrylamidowego jest czysty (nie wymaga dodatkowego
czyszczenia przy stosowaniu w biologii molekularnej)
C. ELEKTROFOREZA W POLU PULSYJĄCYM (PFGE)
Elektroforeza w polu pulsującym jest stosowana do rozdzielania fragmentów DNA o bardzo
dużej masie cząsteczkowej, np. DNA chromosomalnego wyższych eukariota, którego długość wynosi
powyżej 7000 p.z. W metodzie tej zastosowano zmienne, pulsujące, wzajemnie prostopadłe pole
elektryczne. Cząsteczki DNA znajdujące się w żelu, do którego zostanie przyłożone takie pole,
potrzebuje czasu aby zmienić swoje ułożenie na zgodne z orientacją pola. Czas ten jest tym dłuższy im
większa jest masa cząsteczki, a DNA będzie rozdzielana według masy, ponieważ czas trwania impulsu
elektrycznego jest krótszy niż czas potrzebny na reorientacje cząsteczki DNA w żelu. Granica
rozdzielczości elektroforezy w pulsującym polu elektrycznym zależy m.in. od stopnia jednorodności
stosowanych pól elektrycznych, długości trwania impulsu, względnych wartości natężenia obydwu pól.
3

D. ELEKTROFOREZA W POLU INWERSYJNYM (FIGE)
Elektroforeza w polu inwersyjnym jest stosowana do rozdzielania fragmentów DNA o długości
20-2000 p.z., przy czym rozdzielczość tej metody jest około 100-krotnie wyższa niż w przypadku
zwykłej elektroforezy agarozowej. Zastosowano tu elektryczne pole inwersyjnym którego wektor
natężenia pola zmienia zwrot na przeciwny w określonych momentach. Stosunek czasu trwania impulsu
dodatniego do ujemnego wynosi 3:1, a wartości bezwzględne natężenia pola obydwu impulsów są
równe. Podczas elektroforezy w polu inwersyjnym łańcuchy DNA ulegają cyklicznym, synchronicznym
zmianom konformacyjnym, które trwają do chwili zmiany zwrotu wektora natężenia pola elektrycznego
na przeciwny.
E. ELEKTROFOREZA KAPILARNA (CE)
Elektroforeza kapilarna jest stosowana do analizy krótkich, jednoniciowych oligonukleotydów
oraz sekwencjonowania DNA. W elektroforezie kapilarnej stosuje się kolumny (kapilary), których
wewnętrzna średnica wynosi najczęściej 50-100
µm, natężenie prądu 10-20 µA, a natężenie pola
elektrycznego w żelu około 300 V/cm przy zastosowaniu buforu o niskiej przewodności. W tej
elektroforezie wykorzystano efekt elektrosomozy. Kapilary wykonane są ze stopionej krzemionki, która
zawiera wolne grupy silanolowe ulegające jonizacji pod wpływem działania elektrolitu o pH
<2, na
skutek czego wewnętrzna powierzchnia kapilar zostaje naładowana ujemnie, a gęstość jej ładunku
zależy od pH. Przylegająca warstwa jonów dodatnich z roztworu znajdującego się w kapilarze po
przyłożeniu pola elektrycznego porusza się, powodując przepływ cieczy z zewnętrznego zbiornika przez
kapilary. Detekcja odbywa się najczęściej przez monitorowanie absorbancji UV na kolumnie. Objętość
próbki jest rzędu nanolitrów, co pozwala analizować składniki pojedynczych komórek.
F. ELEKTROFOREZA W ŻELACH DENATURUJĄCYCH (CGGE)
Elektroforeza w żelach denaturujących jest głównie wykorzystywana do
wykrywania i analizy mutacji. Wykorzystuje się tu fakt, że temperatura topnienia
wiązań wodorowych między zasadami azotowymi DNA zależy od składu zasad
komplementarnych nici. Stosuje się tu czynnik denaturujący, głównie mocznika lub
formamidu. Elektroforeza prowadzona jest w temperaturze bliskiej temperaturze
topnienia danego DNA, zazwyczaj w 55-60
°C. Temperatura topnienia DNA zależy od
składu ilościowo puryn i pirymidyn w DNA (temperatura topnienia dla G i C jest
wyższa niż dla A i T).
3. SPEKTROSKOPIA ABSORPCYJNA
W pomiarach spektroskopowych zasadnicze znaczenie ma znajomość stężeń
molowych kwasów nukleinowych. Stężenie można otrzymać z pomiaru absorpcji przy
długości
fali
λ = 260 nm (maksymalna absorpcja promieniowania nadfioletowego przez DNA),
jeżeli znamy molowy współczynnik ekstynkcji
ε:
l
A
C
•
=
ε
260
gdzie l – to długość drogi optycznej w kuwecie. Przyjmuje się, ze wartości współczynnika ekstynkcji
wynosi 6600 M
-1
cm
-1
.
Widmo absorpcji może być wykorzystane do określenia stężenia i czystości próbki DNA. Pomiar
stężenia DNA w roztworze oznacza się poprze pomiar absorpcji przy długości fali
λ = 260 nm,
określanej często jako OD – gęstość optyczna. Idealny roztwór do pomiarów spektrofotometrycznych
DNA to bufor o niskim stężeniu jonów, np. bufor TE. Jeżeli A
260
równa się 1 to stężenie dwuniciowego
DNA (dsDNA) wynosi około 50
µg/ml, jednoniciowego DNA (ssDNA) 36 µg/ml, RNA - 40 µg/ml, a
oligonukleotydów 30
µg/ml. Należy jednak pamiętać, że jest to wartość przybliżona, ponieważ wartość
4

współczynnika ekstynkcji zależy od składu zasad azotowych w DNA. Stosunek A
260
/A
280
jest natomiast
często stosowna miarą czystości roztworu DNA, a ściślej miarą zanieczyszczenia DNA białkami
(maksimum absorpcji UV dla białek wynosi 280 nm). Ogólnie preparat DNA uznaje się za czysty jeżeli
A
260
/A
280
wynosi 1,8-2,0. Jeżeli próbka DNA zanieczyszczona jest RNA to wartość A
260
/A
280
jest
bliższa 2,0, natomiast jeżeli próbka zanieczyszczona jest białkami to wartość A
260
/A
280
jest niższa niż
1,8. Absorpcja mierzona przy długości fali 230 odzwierciedla zanieczyszczenia pochodzące od
węglowodorów, białek lub fenolu. W przypadku czystych próbek wartość A
260
/A
230
powinna wynosić
2,2. Absorpcja mierzona przy długości fali 325 nm może być wyznacznikiem wytrąceń w roztworze lub
zanieczyszczeń samej kuwety.
4. MAGNETYCZNY REZONANS JĄDROWY
Magnetyczny rezonans jądrowy ma zastosowanie w badaniach struktury Z-DNA,
obszarów przejść B
→Z-DNA oraz dynamiki tych przejść. NMR stosowany jest także w
badaniach nad oddziaływaniem DNA z różnymi ligandami np. w badaniach nad
oddziaływaniem m.in. leków przeciwnowotworowych z DNA.
5. SPEKTROSKOPIA PROMIENIOWANIA RENTGENOWSKIEGO
Spektroskopia promieniowania rentgenowskiego stosowana jest w badaniach
krystalograficznych struktury DNA, w szczegółową charakterystykę w tym błędnie
tworzone pary zasad czy zasady pozahelikalne. Za pomocą tej metody można także badać
kompleksy DNA z różnymi związkami jak substancje przeciwnowotworowe i antybiotyki.
6. SPEKTROSOKOPIA RAMANA
Spektroskopia Ramana opisuje rotacyjne i oscylacyjne widma cząsteczek.
Pozwala ona na poznanie struktury pojedynczych grup atomów w układach
biologicznych, a także pozwala na uzyskanie informacji o szybkich zmianach
strukturalnych zachodzących w cząsteczkach biologicznych. W klasycznej metodzie
Ramana do wzbudzenia stosowany jest laser argonowy, gdzie DNA można badać w
roztworze, w formie odwodnionego włókna lub postaci krystalicznej.
7. SPEKTROSKOPIA W PODCZERWIENI
Spektroskopia w podczerwieni była jednym z klasycznych narzędzi w badaniach
nad strukturą i oddziaływaniem małych cząsteczek takich jak jony metali czy leki
łączące się z DNA poprzez interkalację.
8. SPEKTROSKOPIA FLUORESCENCYJNA
DNA nie wykazuje mierzalnej fluorescencji wewnętrznej z wyjątkiem niskich
temperatur. Z DNA wiążą się natomiast znaczniki intekalatorowe jak EtBr czy
barwniki akrydynowe, które fluorescencję wykazują. Jednak mają one tę wadę, że
wiążą się z DNA niespecyficznie wzdłuż całej długości helisy. W przeciwieństwie do
DNA fluorescencję wykazują białka, których fluorescencja w wielu przypadkach nie
zmienia się po związaniu z DNA.
9. DICHROIZM KOŁOWY (CD)
5

Dichroizm kołowy jest zjawiskiem polegającym na zróżnicowanym
oddziaływaniu cząsteczek (chiralnych) ze światłem o różnej polaryzacji kołowej.
Kwasy nukleinowe ze względu na strukturę helikalną i określoną skręcalność, bardzo
dobrze nadają się do badań metodą CD. Metoda ta pozwala różnicować struktury
zawierające pętle oraz wykazujące różną skręcalność. Widmo CD zależy od siły
jonowej i rodzaju roztworu, w którym się znajduje. Zmiany konformacyjne w kwasach
nukleinowych można badać jako funkcje temperatury, pH, rozpuszczalnika. Technika
ta jest szeroko stosowana w badaniu przejść konformacyjnych DNA takich jak
denaturacja i zmiana form B
→A oraz B→A czy rozróżnienie DNA dwuniciowego od
trójniciowego. Spektroskopia znajduje także szerokie zastosowanie w badaniu
oddziaływań kwasów nukleinowych z substancjami małocząsteczkowymi jak
chromofory czy leki. Technika ta znalazła także zastosowanie w badaniu oddziaływań
typu: białko-białko czy białko-DNA.
6

WYKONANIE ĆWICZENIA
Materiały i sprzęt
1. Roztwór TE (10 mM Tris-base, 1mM EDTA, pH 8)
2. 1% roztwór agarozy
3. Roztwór bromku etydyny (50 mg/ml)
4. Roztwór buforu elektroforetycznego TBE
×1 (90 mM Tris-base, 90 mM kwas
borowy,
2 mM EDTA, pH 8)
5. Roztwór obciążający LB (50% glicerol, 0,25% błękit bromofenylowy, 1 mM
EDTA)
6. Kolba Erlenmeyer'a 25 ml
7. Cylinder miarowy
8.
Aparat
do
elektroforezy
9. Pipety automatyczne: 1 ml, 0,1 ml, 0,02 ml
10.Probówki
eppendorf
11.Spektrofotometr UV-Vis
12.Kuwety kwarcowe
a. Charakterystyka wyizolowanego DNA – widmo absorpcji UV
• Rozcieńczyć 1:10 roztwór DNA przy pomocy buforu TE; w razie potrzeby
przygotować rozcieńczenie 1:100.
• Zmierzyć z użyciem kuwet kwarcowych absorpcje roztworu DNA przy długości
fali 230, 260 i 280 nm, stosując bufor TE jako odnośnik.
• Wyznaczyć stężenie DNA.
b. Elektroforeza w żelu agarozowym
• Naważkę 0,3 g agarozy rozpuścić w 30 ml buforu elektroforetycznego TBE×1 poprzez jej
zagotowanie w kuchence mikrofalowej, tak aby agaroza nie tworzyła widocznych agregatów.
Ostudzić tak przygotowany roztwór do około 50
°C i dodać 1 µl bromku etydyny
• Wlać roztwór agarozy do uprzednio przygotowanej formy (stolik elektroforetyczny) z
umocowanym grzebieniem formującym studzienki do nanoszeni próbek.
• Po zastygnięciu agarozy zalać żel buforem elektroforetycznym TBE×1. Powierzchnia buforu
powinna znajdować się około 1 mm ponad górną powierzchnią żelu. Powoli wyjąć grzebień, tak
aby nie uszkodzić studzienek żelu.
• Wymieszać w probówce eppendorfa 10 µl wcześniej przygotowanego roztworu DNA i 5 µl
roztworu obciążającego LB. Dokładnie rozpipetować. Całość umieść w jednej studzience żelu.
• Podłączyć elektrody aparatu elektroforetycznego do zasilacza. Elektroforezę prowadzić przez 30-
60 min przy napięciu 90 V.
• Obejrzeć żel umieszczony na transiluminatorze emitującej światło nadfioletowe λ = 302-312 nm.
Opracowanie wyników
1) Obliczyć stosunek absorpcji roztworu DNA przy 230, 260 i 280 nm (A
2 6 0
/A
2 8 0 ,
A
2 6 0
/A
2 3 0
). Skomentować różnicę pomiędzy otrzymaną wartością a wielkością
charakterystyczną dla wysoce oczyszczonego DNA.
2) Obliczyć stężenie DNA (mg/ml) w roztworze TE i na tej podstawie całkowitą
ilość otrzymanego DNA i wydajność oczyszczania dla ludzkich komórek
nowotworowych (A
2 6 0
= 1 to C
d s D N A
= 50
µg/ml; 1 mln komórek ≈ 6 µg DNA)
3) Porównać wydajność i czystość DNA izolowanego z komórek eukarotycznych i
prokariotycznych na podstawie uzyskanego elektroforogramu.
7

Literatura
1. Bryszewska M., Leyko W.: Biofizyka kwasów nukleinowych dla biologów,
Warszawa: PWN 2000;
2. Techniki analizy i detekcji kwasów nukleinowych i białek, kurs zorganizowany
przez Katedrę Biotechnologii i Mikrobiologii Żywności Akademii Rolniczej w
Poznaniu, 2003
3. Techniki elektroforetyczne oraz produkcja i oczyszczanie białek rekombinowanych,
kurs organizowany przez DNA-Gdańsk, 1998
8
Wyszukiwarka
Podobne podstrony:
cw 7 porownanie metod sterowania i regulacji
Badania porównawcze metod obliczanaia obciązen
Porownanie metod dezintegracji komorek
5 1 6 Porownanie metod szacowan Nieznany
porównanie metod pod wzg dokładności
5 1 6 Porównanie metod szacowania rzetelności
Porównanie metod kierowania realizacją złożonych przedsięwzi
Peeling kawitacyjny + manualne oczyszczanie skóry - porównanie metod, Studium kosmetyczne, Pracownia
Porównanie metod antykoncepcji, Kolegium Nauczycielskie - materiały, Uczelnia, Biomedyka
Analiza porownawcza metod oceny JEE
POROWNANIE METOD OSTEOSYNTEZY P Nieznany
Porównanie metod wychowania językowego dzieci niesłyszących
cw 7 porownanie metod sterowania i regulacji
Badania porównawcze metod obliczanaia obciązen
cw 7 porownanie metod sterowania i regulacji
Porównanie metod
więcej podobnych podstron