ZESTAW 3
faza ciemna C4-przebieg 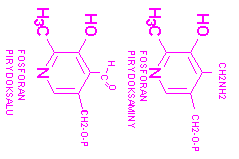
Fotosynteza C4 to proces fotosyntezy, wiązania dwutlenku węgla u roślin określanych nazwą rośliny C4. Proces wiązania CO2 przebiega w komórkach mezofilowych, gdzie dwutlenek węgla przyłączany jest do fosfoenolopirogronianu. W reakcji tej powstaje związek czterowęglowy - szczawiooctan. Jest on w zależności od gatunku rośliny przekształcany do asparaginianu lub jabłczanu i w tej postaci przenoszony do komórek pochew okołowiązkowych. Tam zachodzi reakcja dekarboksylacji i wydzielenie CO2, która jest włączany do cyklu Calvina-Bensona. Brak cyklu Calviana-Bensona w komórkach mezofilowych związany jest z brakiem enzymu, przyłączającego CO2 do cząsteczki rybulozo-1,5-bisfosforanu (RuBP,) określanego nazwą rubisco (karboksylaza oksygenaza rybulozo-1,5-bisfosforanu). Enzym ten może katalizować także reakcję przyłączenia do RuBP tlenu. Proces ten nosi nazwę fotooddychania i obniża on wydajność fotosyntezy roślin C3. Tlen i dwutlenek węgla konkurują o centrum aktywne enzymu rubisco. Dzięki zwiększonemu stężenie CO2 w komórkach pochew okołowiązkowych proces fotooddychania jest zahamowany,a tym samym wydajność fotosyntezy roślin C4 jest wyższa niż roślin C3. Rośliny Proces fotosyntezy u roślin C4 przebiega wydajniej, jednak nakład energetyczny na związanie jednej cząsteczki CO2 jest większy niż u roślin C3. Rośliny C4 podzielono na trzy podtypy: podtyp NADP-ME, podtyp NAD-ME i podtyp PEP-CK. Podstawą wydzielenia trzech podtypów jest enzym odpowiedzialny za przeprowadzenie reakcji dekarboksylacji w komórkach pochew okołowiązkowych. Jest to odpowiednio: enzym jabłczanowy zależny od NADP, enzym jabłczanowy zależny od NAD i karboksykinaza fosfoenolopirogronianu. Do roślin C4 należą gatunki z wielu rodzin np.: kukurydza, trzcina cukrowa, proso zwyczajne, sorgo, proso olbrzymie. Są to rośliny pochodzące z klimatu zwrotnikowego. Proces fotosyntezy u roślin C4 przebiega wydajniej, jednak nakład energetyczny na związanie jednej cząsteczki CO2 jest większy niż u roślin C3.
2. fosforan pirydoksolu- wzór, przykład reakcji z udziałem koenzymu
witamina B6 ma trzy formy: pirydoksynę, pirydoksamine, pirydoksal. Koenzymem B6 jest fosforan pirydoksaminy i pirydoksalu, które współdziałają z enzymami w przemianach aminokwasów i uczestniczą w: RACEMIZACJI OPTYCZNIE CZYNNYCH AMINOKWASÓW, TRANSMINACJI POMIĘDZY AMINOKWASEM I 2-OKSOKWASEM, DEKARBOKSYLACJI AMINOKWASÓW, ELIMINACJI TYPU 3,4 (ODWODNIENIE DERYNY DO PIROGRONIANU) SYNTEZA TRYPTOFANU Z SERYNY I INDOLU, FOSFOROLIZA SACHARYDÓW ZŁOŻONYCH reakcje zachodzą dzięki aktywności grupy aldehydowej 5-fosforanu pirydoksalu. Łatwo zachodzą w obrębie aminokwasów, które z tą grupą tworzą zasadę Schiffa o bardzo nietrwałym układzie elektronów. Sprzyja temu grupa OH, które chelatuje jony miedzi i glinu. Odmienna funkcję wykazuje on we współdziałaniu z fosforylazą glikogenową, do działania której jest niezbędny jako kofaktor. Funkcją fosforanu pirydoksalu jest reakcja transaminacji, kóra może przebiegac bez udziału białka enzymowego, a jedynie w obecności koenzymu i dwuwartościowego jonu metalu.
3. mechanizm działania koenzymów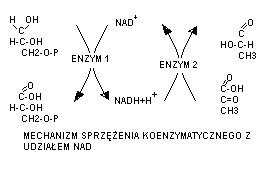
Dzialanie koenzymow polega na ich powiązaniu stechiometrycznym z substratem za pośrednictwem określonej jego grupy oraz z bialkiem enzymowym. W reakcji przeniesienia protonów i elektronów z jednego związku na inny może uczestniczyc jeden lub dwa enzymy; w drugim przypadku nastepuje tzw. Sprzężenie koenzymatyczne. Przykładem takiego sprzeżenia jest powiazanie z udzialem dinukleotydu nikotynoamidoadeninowego.
Enzym 1 (dehydrogenaza fosforanu gliceraldehydu, katalizuje przeniesienie atomow wodoru z wodzianu fosforanu triozy na NAD+, przy czym tworzy się 3-fosfoglicerynian i zredukowany NAD+. Reakcja jest sprzężona z druga w której regeneruje się NAD+ przez przekazanie atomów wodoru na pirogronian z udziałem innego enzymu- dehydrogenazy mleczajowej, w wyniku czego tworzy się mleczan. W tym przypadku koenzym jest lluxno powiązany z bialkiem enzymu i może współdziałać z róznymi apoenzymami. W innych reakcjach koenzym jest silniej powiązany z apoenzymem i wtedy jest on pośrednikiem w przekazaniu określonej grupy atomów z jednego substratu na drugi przy udziale tego samego enzymu.
Reakcja utlenienia β-D-glukopiranozy do laktonu kwasu glukonowego, katalizowana przez oksydazę glukozową, współdziałającą z FAD. Atomy wodoru odłączone z glukozy są tu przekazane za pośrednictwem FAD, współdziałającego z białkiem enzymu, na tlen cząsteczkowy, w wyniku czego tworzy się nadtlenek wodoru H2O2.
4. prebieg i znaczenie cyklu kwasu cytrynowego
cykl Krebsa, cykl kwasów trójkarboksylowych) zachodzi w macierzy mitochondrialnej. Polega na utlenieniu cząsteczki acetylokoenzymu A do dwóch cząsteczek dwutlenku węgla. Wytwarzana energia jest magazynowana w wysokoenergetycznych wiązaniach cząsteczek ATP, natomiast uwolnione atomy wodoru są przenoszone przez koenzymy NAD i FAD na enzymy łańcucha oddechowego. Cykl kwasu cytrynowego jest pośrednim etapem katabolizmu wielu związków chemicznych utlenianych w komórce.
Cykl rozpoczyna się od kondesacji szczawiooctanu z acetylo-CoA , w wyniku czego powstaje cytrynian, a następnie w drodze izomeryzacji jego powstaje izocytrynian. W następnej kolejności następuje dekarboksylacja izocytrynianu do a- ketoglutaranu, a ten po przez oksydacyjną dekarboksylację daje bursztynylo-CoA. Wiązanie tioestrowe w bursztynylo-CoA zostaje rozerwane przez fosforan, powstaje bursztynian i 1 cząsteczka GTP. W wyniku utleniania bursztynianu powstaje fumaran, który po uwodnieniu daje jabłaczan. Cykl kończy regeneracja szczawiooctanu, powstałego w wyniku utleniania jabłaczanu. Bilans energetyczny cyklu kwasu cytrynowego stanowi 10 wysokoenergetycznych wiązań fosforanowych powstałych z całkowitego utleniania każdego fragmentu dwuwęglowego do CO2 i H2O
5. Omów na dowolnym przykładzie proces syntezy kwasu tłuszczowego
Biosynteza kwasów tłuszczowych odbywa się w cytoplazmie komórek tłuszczowych. Do procesu potrzebny jest acetylokoenzym A. W biosyntezie kwasów tłuszczowych wyróżnić można kilka etapów:
1. acetylokoenzym A ulega karboksylacji do malonylokoenzymu A (malonylo-CoA).
2. Synteza kwasów tłuszczowych na kompleksie enzymatycznym - syntetazie kwasów tłuszczowych. W skład syntetazy wchodzi ACP, ktrory przenosi acyle. ACP zawiera z kolei panteteinę Tworzony kwas tłuszczowy jest związany kowalencyjnie z enzymem. reszta acetylowa jest przeniesiona na ACP. Następnie dochodzi do połączenia reszty malonylowej z resztą acetylową, powstaje 4-węglowa cząsteczka acetoacetylo-S-ACP. Wydzielony wówczas jest CO2 i HS-ACP. CO2 jest uwolniony w wyniku działania syntazy 3-oksoacylo-ACP.
3. Etap redukcji odbywa się przy udziale NADPH i reduktazy 3-oksoacylo-ACP. Dochodzi do redukcji grupy -okso. Powstaje reszta beta-hydroksyacylowa, która poddana jest dehydratacji przy udziale dehydratazy 3-hydroksy-ACP. Powstaje reszta alfa, beta-dehydro-acylowa, która zostaje poddana redukcji przy udziale NADPH i reduktazy enoilo-ACP. Powstaje 4-węglowy rodnik butyrylowy. W następnym obrocie reakcji powstaje kolejna jego cząsteczka, przy czym reszta acylowa z wcześniej wytworzonego rodnika jest przeniesiona na tę następna, wydzielony jest wówczas dwutlenek węgla i powstaje reszta beta-ketoacylowa. Ta znów podlega kondensacji z kolejną. W ten sposób tworzony kwas ulega wydłużaniu do odpowiedniej masy.
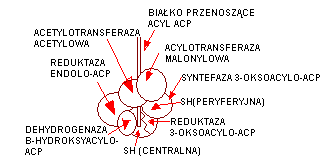
4. Uwalnianie gotowego łańcucha kwasu tłuszczowego odbywa się przy pomocy deacylazy. Odłącza ona kwas od HS-ACP,
CH3CO ~ S-CoA + 7HOOC-CH2CO~S-CoA + 14 NADPH + 14 H+ CH3(CH2)14CO~S-CoA + 7 CO2 + 7 HS-CoA + 14 NADP+ + 6H2O
Powstałe kwasy tłuszczowe są gromadzone w komórkach w postaci estrów glicerolu.
MODEL SYNTEZY KW. TŁUSZCZOWYCH
6. proces dekarboksylacji aminokwasow, rola otrzymanych produktów
Reakcje dekarboksylacji aminokwasów polegają na rozerwaniu wiązania między grupą karboksylową -COOH i resztą cząsteczki aminokwasu, w wyniku czego wydziela się CO2 i powstaje odpowiednia amina. Reakcję katalizują dekarboksylazy aminokwasowe. Dekarboksylacja aminokwasowa jest źródłem amin biogennych - substancji o dużej aktywności fizjologicznej, np. histamina (po dekarboksylacji histydyny), tyramina (po dekarboksylacji tyroksyny), tryptamina (po dekarboksylacji tryptofanu), serotonina = 5-hydroksytryptamina (po dekarboksylacji 5-hydroksytryptofanu). W Wyniku dekarboksylacji niektórych aminokwasów tworzą się ważne części składowe koenzymów, np. 2-propanolamina (składnik koenzymu B12), cysteamina (składnik koenzymu A). Z kwasu glutaminowego powstaje kwas gamma-aminomasłowy.
W wyniku dekarboksylacji aminokwasów obojętnych i zasadowych powstają aminy biogenne, które z wyjątkiem histaminy zwężają naczynia krwionośne i podwyższają ciśnienie krwi. Produkt dekarboksylacji histydyny - histamina rozszerza naczynia krwionośne, powodując spadek ciśnienia krwi oraz wywołując objawy alergiczne. Histamina jest stosowana do wydzielania soku żołądkowego w próbach czynnościowych. Natomiast produktem dekarboksylacji 5-hydroksytryptofanu jest serotonina. Serotonina zwęża naczynia krwionośne, powodując zwiększenie ciśnienia krwi, wywołując skurcz mięśni gładkich. Działa pobudzająco na ośrodkowy układ nerwowy.
5-hydroksytryptofan Serotonina
Rys. 16 Dekarboksylacja aminokwasów
Aminy biogenne można podzielić na aminy alifatyczne (monoaminy i poliaminy), katecholowe (fenolowe, o pierścieniach aromatycznych) i heterocykliczne. Aminy katecholowe (tyramina, dyzamina, adrenalina), imidazolowe (histamina) i indolowe (tryptamina, serotonina) powodują zmiany ciśnienia krwi. Aminy te są też neuroprzekaźnikami, odgrywają ważną role w przenoszeniu impulsów nerwowych przez zakończenia nerwowe (noradrenalina, a jako inhibitor dopamina) oraz poprzez synapsy komórek nerwowych (serotonina). Nadmiar serotoniny w krwi powoduje stany halucynacyjne, a niedobór depresje.
7.rola tranclacjii w biosyntezie bialek Translacja - to w biologii proces syntezy łańcucha polipeptydowego białek na matrycy mRNA. Proces ten katalizowany jest przez rybosomy. Translacja polega na interpretacji informacji zawartej w kolejności ułożenia nukleotydów mRNA, zgodnie z zasadami kodu genetycznego, na kolejność ułożenia reszt aminokwasowych w białku. Translacja odbywa się w kierunku od 5' do 3' mRNA, a syntetyzowane białko powstaje od końca aminowego do karboksylowego. Proces składa się z trzech etapów: inicjacji, elongacji i terminacji. Zakończenie odbywa się gdy w mRNA zostanie napotkany nonsensowny (stop) kodon nie odpowiadający żadnemu tRNA.
Etap translacji (odczytania, przetłumaczenia)- zachodzi w rybosomach.- biorą w nim udział cząsteczki tRNA. - aminokwas łącząc się z cząsteczką tRNA ulega uaktywnieniu:
tRNA + aminokwas = aminoacylo tRNA
- cząsteczki mRNA umiejscawiają się między dwiema podjednostkami rybosomu.- cząsteczki tRNA dostają się do rybosomu i jeśli maja antykodon komplementarny do kodonu w mRNA to zostawiają tam transportowany aminokwas.- między aminokwasami powstają wiązania peptydowi, rybosom przesuwa się wzdłuż nici mRNA, a łańcuch peptydowy wydłuża się.- translacja zaczyna się kodonem startowym- metionina (AUG), a kończy kodonem nonsensownym (UAA, UAG, ULG).- translacja wymaga: udziału rybosomów, mRNA, dostatecznej ilości aminokwasów, energii, tRNA. translacja jest zatem kluczowym procesem warunkujacym zycie organizmow
8. Omow znaczenie w przemianach metabolicznycha: jonu amonowego
Cykl ornitynowy, zwany też cyklem mocznikowym lub mocznikowym cyklem Krebsa to cykl przemian biochemicznych (reakcji enzymatycznych) trzech aminokwasów: ornityny, cytruliny i argininy. Do cyklu wprowadzany jest karbamoilofosforan powstały z amoniaku i dwutlenku węgla. Cykl przebiega w mitochondriach i cytoplazmie komórek wątroby (hepatocytów) i wymaga dostarczenia energii w postaci ATP, a jego produktem końcowym jest mocznik.
Reakcje zużywania aminokwasów rozpoczynają się od odłączenia grupy aminowej w procesie deaminacji. Produktami tych reakcji są łańcuchy węglowe (tzw. ketokwasy) oraz jon amonowy. W komórkach człowieka łańcuchy węglowe po przemianach mogą być włączone w glikolizę lub do cyklu Krebsa. Jon amonowy jest silnie toksyczny. W organizmie człowieka jest więc szybko przekształcany w substancję mniej toksyczną i dobrze rozpuszczalną w wodzie - mocznik. W ciągu doby człowiek wydala średnio kilkanaście gramów mocznika w postaci stężonego moczu.
b)Glukoneogeneza, zespół przemian biochemicznych zachodzących w wątrobie, prowadzący do wytworzenia glukozy lub glikogenu z substancji niecukrowych: aminokwasów, kwasu mlekowego, pirogronowego i in. Glukoneogeneza pobudzana jest i kontrolowana przez glikokortykoidy. Głównym substratem jest pirogronian. Glukoneogeneza ma miejsce głównie w komórkach wątroby, częściowo również w nerkach. W wyniku glukoneogenezy wydzielają się duże ilości energii.
Jest to proces syntezy glukozy z mleczanu i związków nie cukrowych. W warunkach tlenowych, pod wpływem dehydrogenazy mleczanowej, mleczan przechodzi w pirogronian. Właściwy proces glukoneogenezy rozpoczyna się pirogronianu i jest w dużej mierze odwróceniem procesu glikolizy. Jednak nie wszystkie etapy glikolizy można w prosty sposób odwrócić. Do takich etapów należy przejście:
- glukozy w glukozo-6-fosforan,
- fruktozo-6-fosforanu we fruktozo1,6-dwufosforan,
- fosfoenolopirogronianu w pirogronian,
to enzymatyczny proces tworzenia przez organizm glukozy z metabolitów nie będących węglowodanami. Większość czynników wpływających na aktywność szlaku glukoneogenezy to substancje powodujące zmniejszenie czynności wykorzystywanych w nim enzymów, jednak zarówno acetylo-CoA jak i cytrynian działają na nie aktywująco. Glukoneogeneza rozpoczyna się od wytworzenia α-ketoglutaranu przez karboksylację pirogronianu kosztem jedej cząsteczki ATP. Reakcja jest katalizowana przez odpowiednią karboksylazę. α-ketoglutaran jest następnie dekarboksylowany i równocześnie fosforylowany do fosfoenolopirogronianu przez odpowiednią karboksykinazę. W czasie tej reakcji jedna cząsteczka GTP jest hydrolizowana do GDP. Obie reakcje zachodzą w mitochondriach.
Wyszukiwarka
Podobne podstrony:
zestaw 6 biochemia, OGRODNICTWO UP LUBLIN, BIOCHEMIA, zestawy
Zestawy z biochemie co były na egzamnie, OGRODNICTWO UP LUBLIN, BIOCHEMIA
zestaw 2 biochemia, OGRODNICTWO UP LUBLIN, BIOCHEMIA, zestawy
zestaw 4 biochemia, OGRODNICTWO UP LUBLIN, BIOCHEMIA, zestawy
zestaw 1 biochemia, OGRODNICTWO UP LUBLIN, BIOCHEMIA, zestawy
zestaw 7 biochemia, OGRODNICTWO UP LUBLIN, BIOCHEMIA, zestawy
BIAŁKA, OGRODNICTWO UP LUBLIN, BIOCHEMIA, dodatkowe materiały
BIAŁKA ściąga, OGRODNICTWO UP LUBLIN, BIOCHEMIA
Gerbera nakolosanotatki 13-01-2014, OGRODNICTWO UP LUBLIN, ROŚLINY OZDOBNE, ozdobne II semestr
przech-sciagi, OGRODNICTWO UP LUBLIN, PRZECHOWALNICTWO
eko4, OGRODNICTWO UP LUBLIN, EKOLOGIA
Zielarstwo - wyk-ad 6 - 16.11.2010, OGRODNICTWO UP LUBLIN (buka), Semestr III, ZIELARSTWO
Ekonomia- wszystkie wykłady i ćwiczenia- ściaga, OGRODNICTWO UP LUBLIN, EKONOMIA
Sciagi warzywa, OGRODNICTWO UP LUBLIN (buka), Semestr III, WARZYWNICTWO OGÓLNE
Doniczki test, OGRODNICTWO UP LUBLIN, ROŚLINY OZDOBNE, ozdobne II semestr
botanika pytania, OGRODNICTWO UP LUBLIN, BOTANIKA
GLEBOZNAWSTWO - wykład 7 - 23.11.2009r, OGRODNICTWO UP LUBLIN, GLEBOZNAWSTWO, wykłady
szkółkarstwo 3 kolokwium, OGRODNICTWO UP LUBLIN (buka), Semestr III, SZKÓŁKARSTWO
Palmy, OGRODNICTWO UP LUBLIN, ROŚLINY OZDOBNE, ozdobne II semestr
więcej podobnych podstron