
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wyklad 4c. Chemia Ciała Stałego
37/47
8. Izomorfizm i polimorfizm
Substancje o :
-
tym samym typie wzoru chemicznego,
-
tym samym typie sieci,
-
takimi samymi lub zbliżonymi rozmiarami komórki
sieciowej
nazywamy substancjami izomorficznymi
Przykłady :
1) CaCO
3
(kalcyt)
FeCO
3
(syderyt)
MgCO
3
(magnezyt)
2) KClO
4
PbSO
4
KMnO
4
3) KAl(SO
4
)
2
⋅⋅⋅⋅
12H
2
O
KCr(SO
4
)
2
⋅⋅⋅⋅
12H
2
O
Uwaga!!! KAl(SO
4
)
2
⋅⋅⋅⋅
12H
2
O jest to sól podwójna, którą możemy zapisać
też inaczej: K
2
SO
4
⋅⋅⋅⋅
Al
2
(SO
4
)
3
⋅⋅⋅⋅
24H
2
O

Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wyklad 4c. Chemia Ciała Stałego
38/47
Substancje izomorficzne mają :
-
podobne właściwości chemiczne,
- poddane współkrystalizacji tworzą kryształy mieszane.
Przykłady kryształów mieszanych:
- oliwin
(Mg,Fe)
2
SiO
4
- apatyt
Ca
3
(PO
4
)
2
⋅⋅⋅⋅
Ca(F,Cl)
2
w jonowych sieciach
krystalicznych są
na przemian:
Mg
2+
, Fe
2+
- oliwin
F
-
, Cl
-
- apatyt
Czy KCl i KBr są izomorficzne???
KCl i KBr są izomorficzne (sieć typu NaCl) gdyż :
r
Cl-
= 167 pm
r
Br-
= 182 pm
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wyklad 4c. Chemia Ciała Stałego
39/47
Polimorfizm
Polimorfizm polega na tym, że jedna i ta sama substancja
chemiczna, zależnie od warunków, występuje w dwóch (lub
więcej) odmianach różniących się :
- postacią krystaliczną,
- strukturą sieci przestrzennej.
Przykłady :
1) ZnS - siarczek cynku:
wurcyt - heksagonalny
│ blenda cynkowa - regularny
2) CaCO
3
- węglan wapnia:
kalcyt - heksagonalny
│ aragonit - rombowy
Dla pierwiastków posługujemy się terminem ALOTROPIA
Węgiel : diament, grafit, fullereny
Tlen : tlen(O
2
) i ozon (O
3
)

Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wyklad 4c. Chemia Ciała Stałego
40/47
10. Związki niestechiometryczne. Defekty sieciowe
Prawo stosunków stałych, Proust (1799):
Każdy związek chemiczny ma stały i niezmienny
skład ilościowy (np. CO
2
, H
2
O).
Dzisiaj prawo to nadal obowiązuje dla substancji ciekłych lub
gazowych. Ale dla substancji w stanie stałym są pewne
odstępstwa. Dotyczy to związków chemicznych, w sieci których
nie można wyodrębnić oddzielnych cząsteczek.
Dla przykładu uzyskano tlenki tytanu o składzie :
od TiO
0,716
do TiO
1,250
przy czym wszystkie mają strukturę NaCl.
Są to związki o składzie niestechiometrycznym.
Tego typu związki tworzą pierwiastki d-elektronowe z tlenowcami.

Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wyklad 4c. Chemia Ciała Stałego
41/47
Przyczyna - kryształy rzeczywiste różnią się od idealnych (tj.
doskonale uporządkowanych) zaburzeniami, tj. defektami
sieci.
Defekty sieciowe są to nieprawidłowości w obsadzaniu
węzłów sieci przestrzennej :
- defekty punktowe,
- defekty liniowe,
- defekty powierzchniowe.
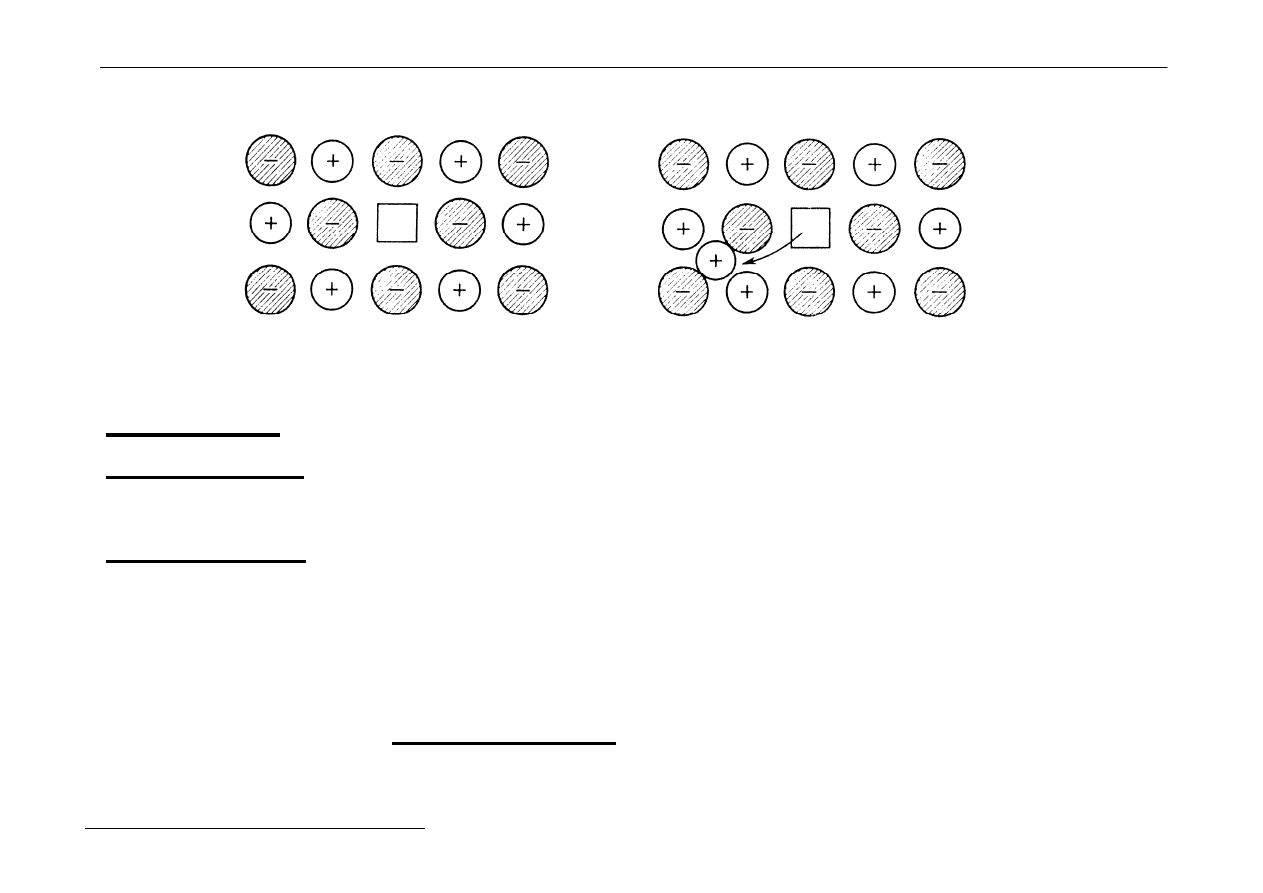
Defekty punktowe
Tak zwane defekty Schottky'ego polegają na występowaniu
luk kationowych lub anionowych.
Natomiast defekty Frenkla to przemieszczenia cząstek
w położenia międzywęzłowe.
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wyklad 4c. Chemia Ciała Stałego
42/47
Defekt Schottky'ego
Defekt Frenkla
Przykłady:
tlenek żelaza: Fe
0,93
O
1,00
- defekty kationowe - część jonów Fe
2+
jest
zastąpiona przez Fe
3+
tlenek cynku: Zn
1,05
O
1,00
- dodatkowe wbudowanie się jonów Zn
2+
w położenia międzywęzłowe.
W luki sieciowe mogą się wbudowywać elektrony.
W wyniku oddziaływania pomiędzy defektami jonowymi i elektronami
mogą powstawać centra barwne. I tak na przykład obserwuje się
zabarwione kryształy halogenków litowców (niebieska sól kamienna).
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wyklad 4c. Chemia Ciała Stałego
43/47
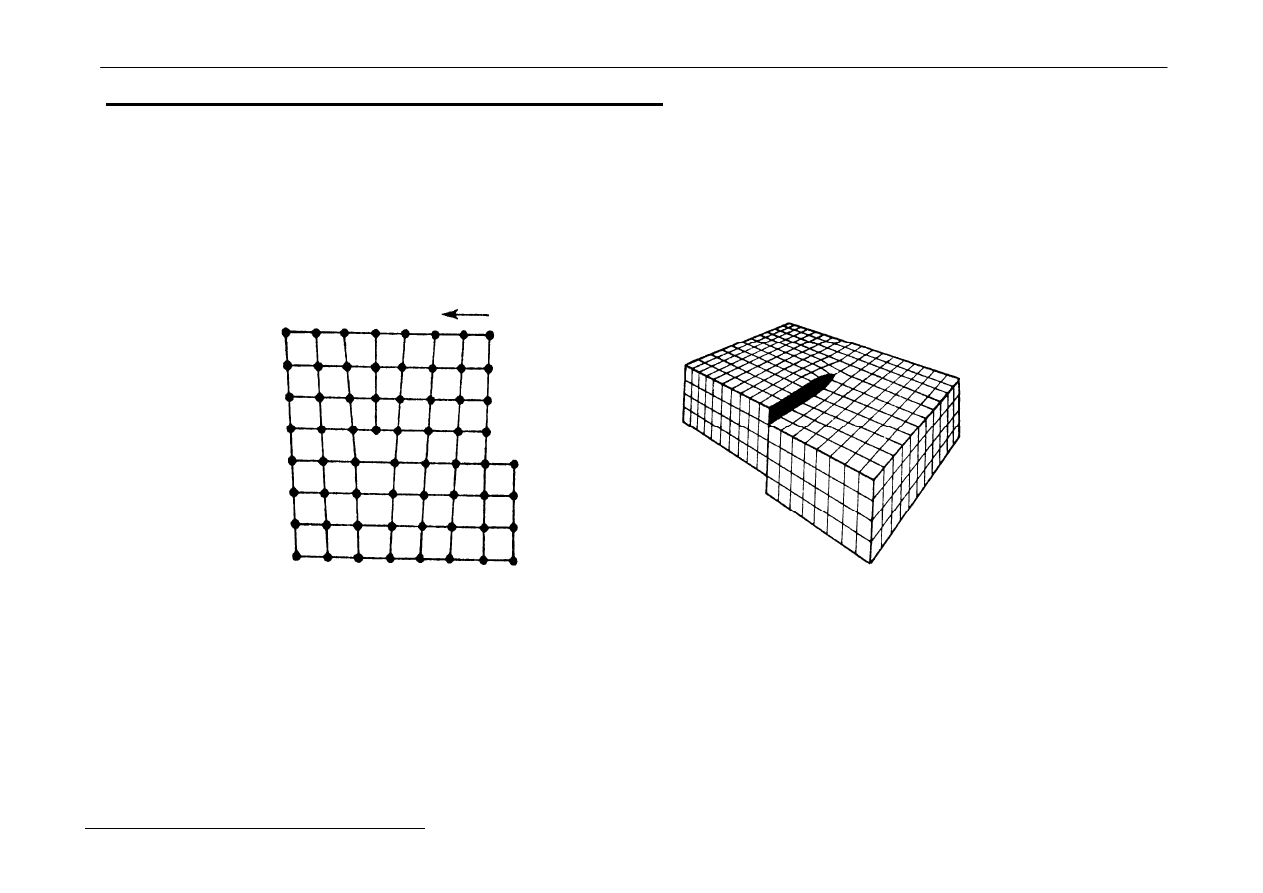
Defekty liniowe i powierzchniowe
Defekty liniowe to inaczej dyslokacja - całe szeregi elementów
strukturalnych przesuwają się względem siebie. Możliwe są
dyslokacje krawędziowe i śrubowe.
Istnieją też defekty powierzchniowe.

Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wyklad 4c. Chemia Ciała Stałego
44/47
Daltonidy, bertolidy
Fe
0,93
O
1,00
- jest to związek niestechiometryczny. Możemy to
inaczej zapisać jako Fe
93
O
100
. Uwzględniając obecność w tym
związku jonów Fe
3+
można napisać: Fe
79
II
Fe
14
III
O
100
Suma dodatnich stopni utlenienia ⇒
⇒
⇒
⇒
śelazo:(79 x 2 + 14 x 3) = 200
Suma ujemnych stopni utlenienia ⇒
⇒
⇒
⇒
Tlen: 100 x 2 = 200
Jest to skład stechiometryczny. Nie jest więc uzasadnione
wiązanie stechiometrii tylko z liczbami całkowitymi.
Unikamy określenia związek niestechiometryczny, zastępując
go terminem BERTOLID.
DALTONID-y odpowiadają zwykłym związkom chemicznym,
a ich skład można wyrazić używając niewielkich liczb
całkowitych (np. CO
2
).
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wyklad 4c. Chemia Ciała Stałego
45/47
11.
Rentgenograficzne
metody
badania
struktury
kryształów
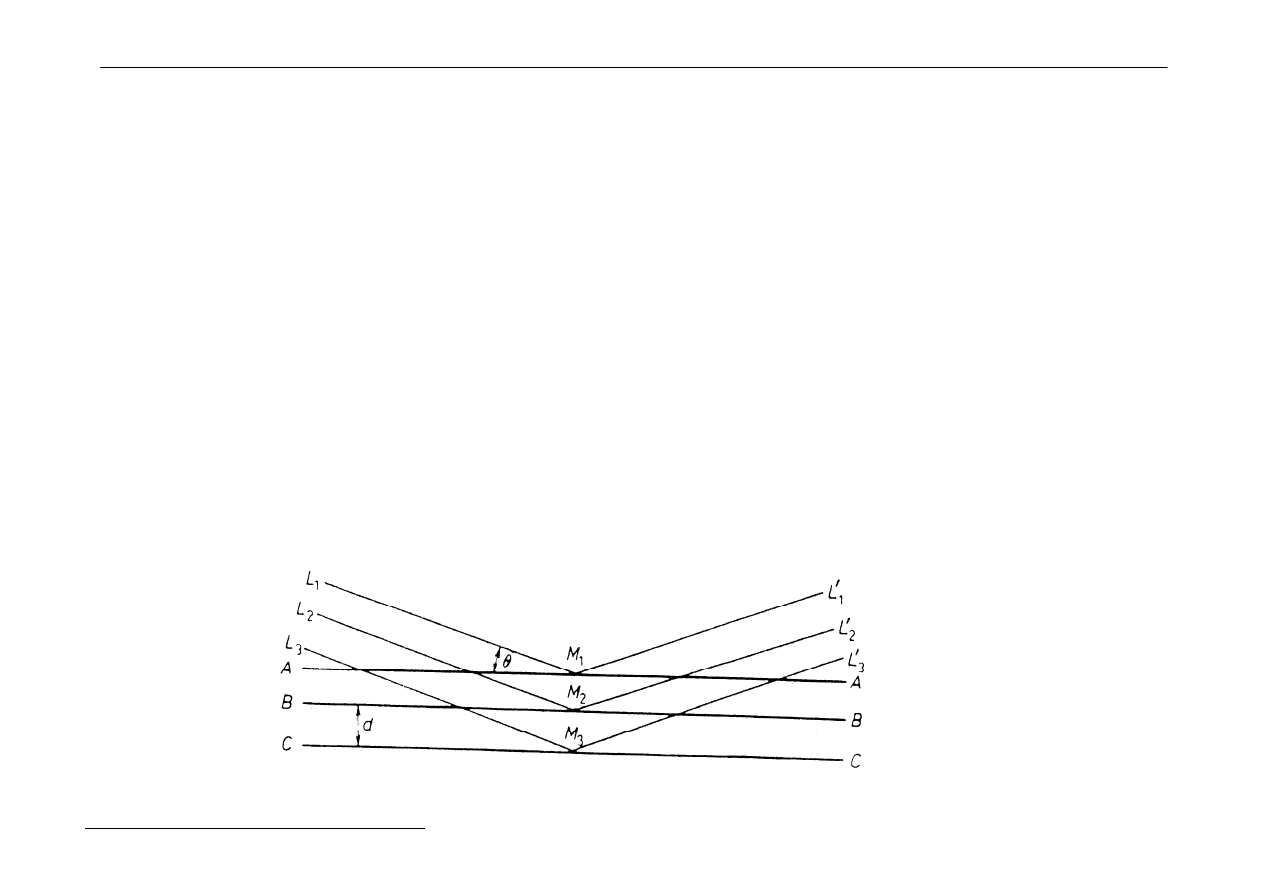
Dyfrakcja promieni rentgenowskich na kryształach - rolę siatki
dyfrakcyjnej pełnią tutaj płaszczyzny sieciowe kryształów.
Braggowie wykazali:
n
λλλλ
= 2d sin
θθθθ
n = 1,2,3
gdzie: d - odległość płaszczyzn,
λλλλ
- długość fali prom. rentgenowskich,
θθθθ
- kąt pomiędzy prom. padającym i płaszczyzną
sieciową (kąt odbłysku).
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wyklad 4c. Chemia Ciała Stałego
46/47
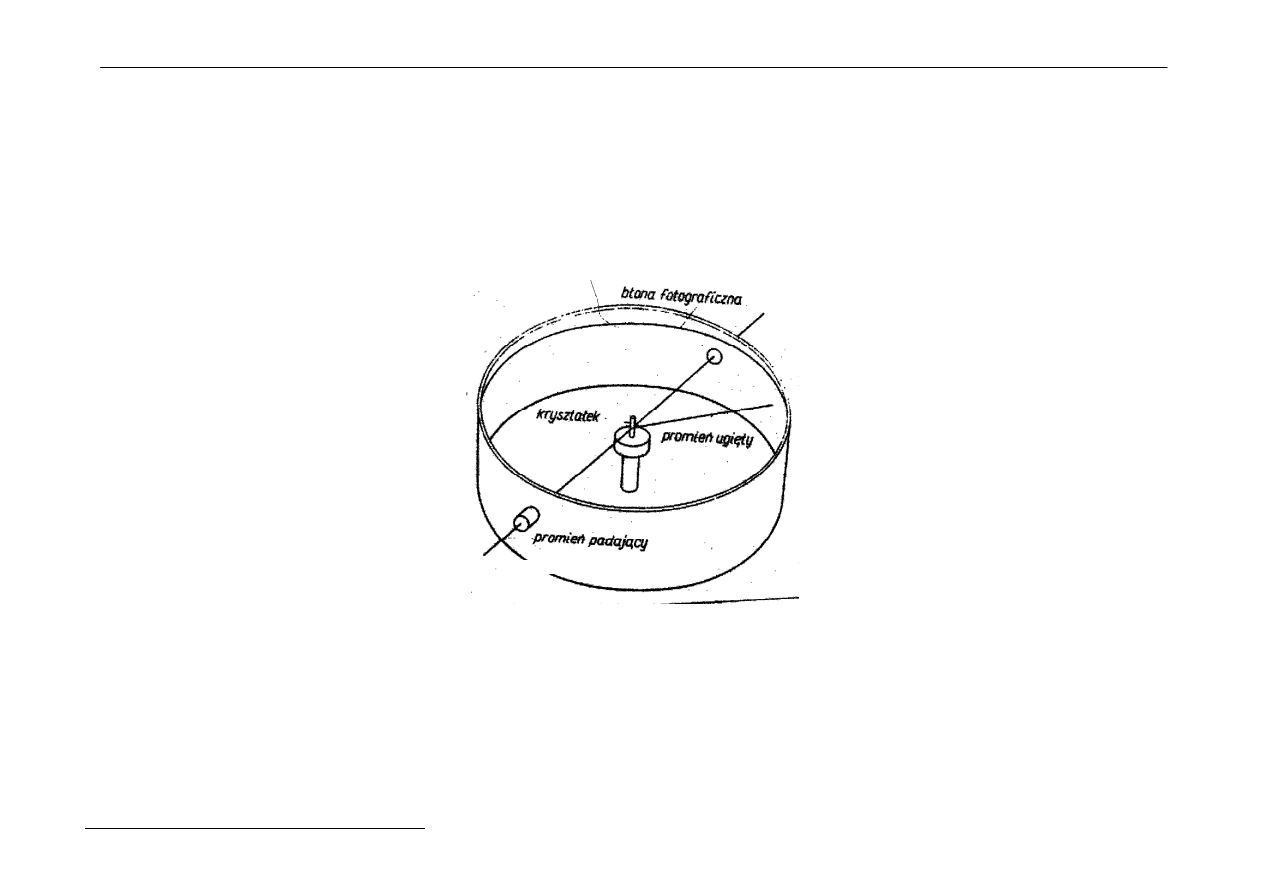
Jak mierzyć kąt odbłysku???
a) Metoda obracanego kryształu
W tej metodzie musimy dysponować pojedynczym kryształem,
zazwyczaj o wymiarach kilku milimetrów.
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wyklad 4c. Chemia Ciała Stałego
47/47
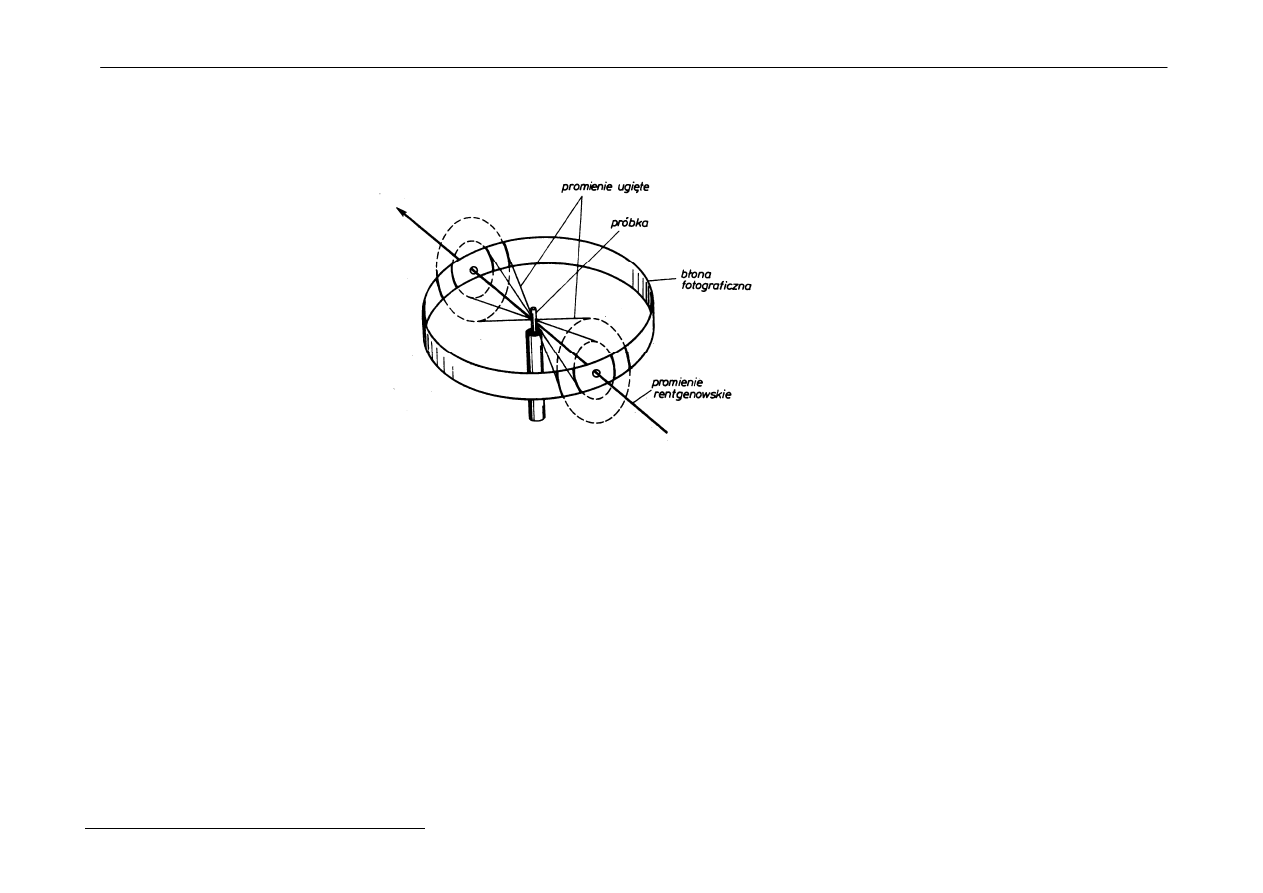
b) Metoda proszkowa Debye'a i Scherrera
W tym przypadku można badać substancje sproszkowane.
Koniec rozdz. IV-tego
Wyszukiwarka
Podobne podstrony:
Leszek wyklad9 teoria pasmowa ciala stalego
WYK-4c.Budowa ciala stalego
Wykład 5. Teoria pasmowa ciała stałego
Wykład 5 Teoria pasmowa ciała stałego
4. Budowa ciala stałego, pwr biotechnologia(I stopień), II semestr, Chemia nieorganiczna, Wykłady Ap
Chemia Wyklad 4c id 111678
Wyklad 1 Fizyka ciala stalego podstawy
wykład 8 budowa ciała stałego
Fizyka ciała stałego, STUDIA, SEMESTR I, Mechanika, Mechanika Wyklady, Mechanika net
wyklad z czwartku chemia fizycz dnia19 marca
28 Zjawiska towarzyszące bombardowaniu ciała stałego elektro
II 14 Fizyka ciala stalego
Ciżman, fizyka ciała stałego L, sprawozdanie dwójłomność spontaniczna
bryja, fizyka ciała stałego, Równanie kp
5 Teoria pasmowa ciala stalego Nieznany (2)
bryja, fizyka ciała stałego, Model ciasnego wiązania
więcej podobnych podstron