
WYKŁAD 8
1
PODSTAWY CHEMII
PODSTAWY CHEMII
PODSTAWY MECHANIKI KWANTOWEJ
PODSTAWY MECHANIKI KWANTOWEJ
WYKŁAD 8
2
PODSTAWY CHEMII
PODSTAWY CHEMII
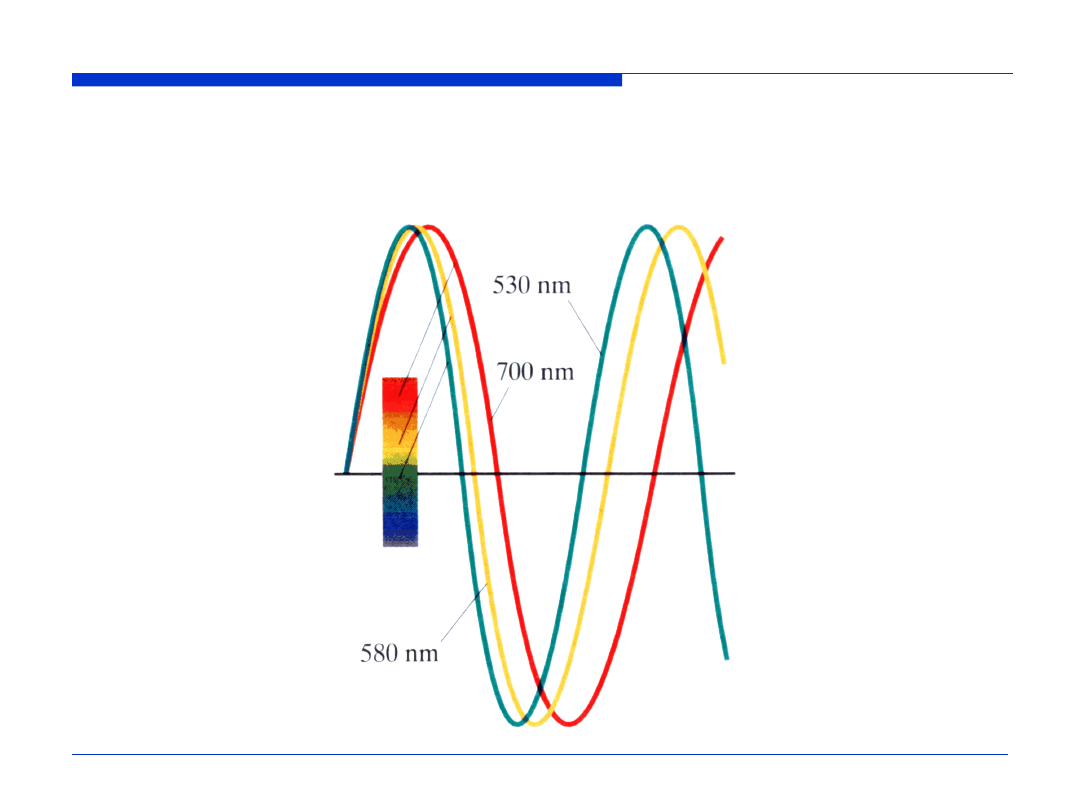
Barwa promieniowania elektromagnetycznego
Barwa promieniowania elektromagnetycznego
WYKŁAD 8
3
PODSTAWY CHEMII
PODSTAWY CHEMII
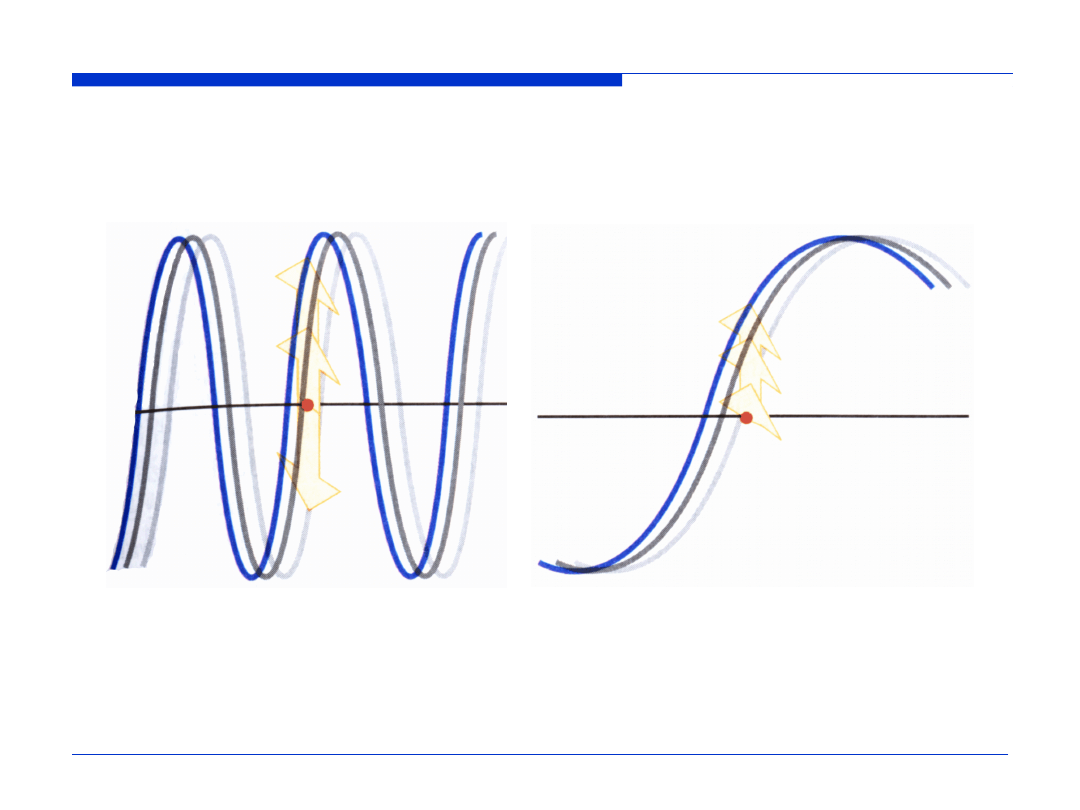
Długość fali i częstość są odwrotnie proporcjonalne
Długość fali i częstość są odwrotnie proporcjonalne
mała długość fali
mała długość fali
duża częstość
duża częstość
duża długość fali
duża długość fali
mała częstość
mała częstość
WYKŁAD 8
4
PODSTAWY CHEMII
PODSTAWY CHEMII
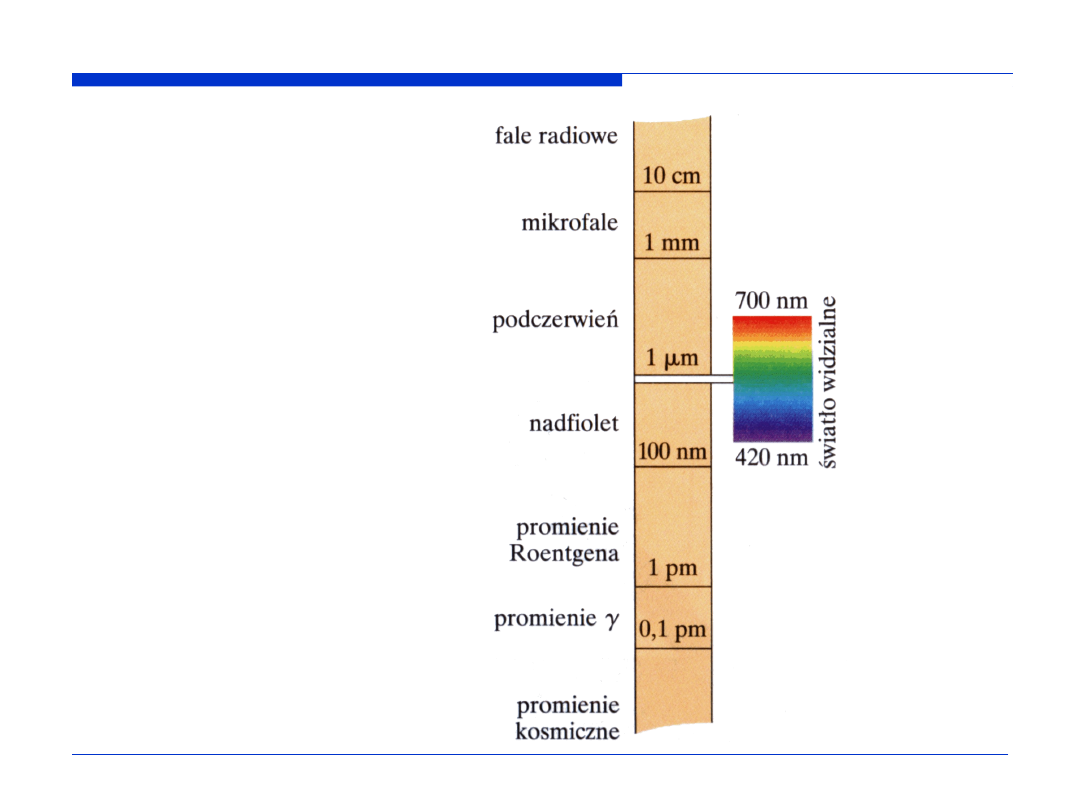
Widmo promieniowania
Widmo promieniowania
elektromagnetycznego
elektromagnetycznego
WYKŁAD 8
5
PODSTAWY CHEMII
PODSTAWY CHEMII
WYKŁAD 8
6
PODSTAWY CHEMII
PODSTAWY CHEMII
Kwantowanie (Max Planck)
Kwantowanie (Max Planck)
nh
E
1
34
10
626
,
6
Hz
J
h
Efekt fotoelektryczny (Albert Einstein)
Efekt fotoelektryczny (Albert Einstein)
h
m
e
2
2
1
v
WYKŁAD 8
7
PODSTAWY CHEMII
PODSTAWY CHEMII
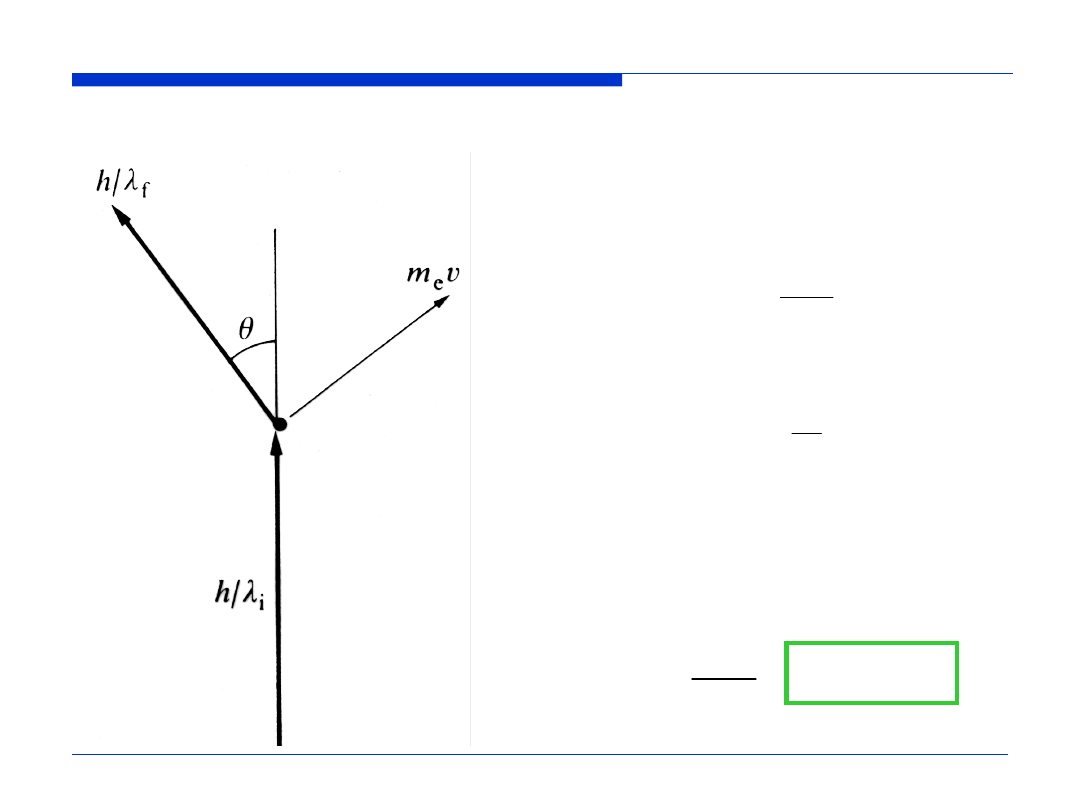
EFEKT COMPTONA
EFEKT COMPTONA
Relacja
Relacja
de Broglie
de Broglie
c
h
p
h
p
cos
1
c
pm
426
,
2
c
m
h
e
c
WYKŁAD 8
8
PODSTAWY CHEMII
PODSTAWY CHEMII
WŁAŚCIWOŚCI FOTONÓW
WŁAŚCIWOŚCI FOTONÓW
energia
energia
masa
masa
pęd
pęd
h
E
f
2
c
h
m
f
h
c
h
p
f
h
h
-
-
stała Plancka = 6,62
stała Plancka = 6,62
.
.
10
10
-34
-34
J
J
.
.
s
s
- częstość
- częstość
- długość fali
- długość fali
c
c
– prędkość światła 3
– prędkość światła 3
.
.
10
10
8
8
m/s
m/s
WYKŁAD 8
9
PODSTAWY CHEMII
PODSTAWY CHEMII
Równanie Schrödingera
Równanie Schrödingera
czyli zagadnienie własne operatora energii
czyli zagadnienie własne operatora energii
V
E
Η
ΕΨ
Ψ
Η
kin
ˆ
ˆ
ˆ
- operator energii (hamiltonian)
- funkcja falowa
- wartość własna energii
- operator energii kinetycznej
- energia potencjalna
V
E
E
Ψ
Η
kin
ˆ
ˆ
WYKŁAD 8
10
PODSTAWY CHEMII
PODSTAWY CHEMII
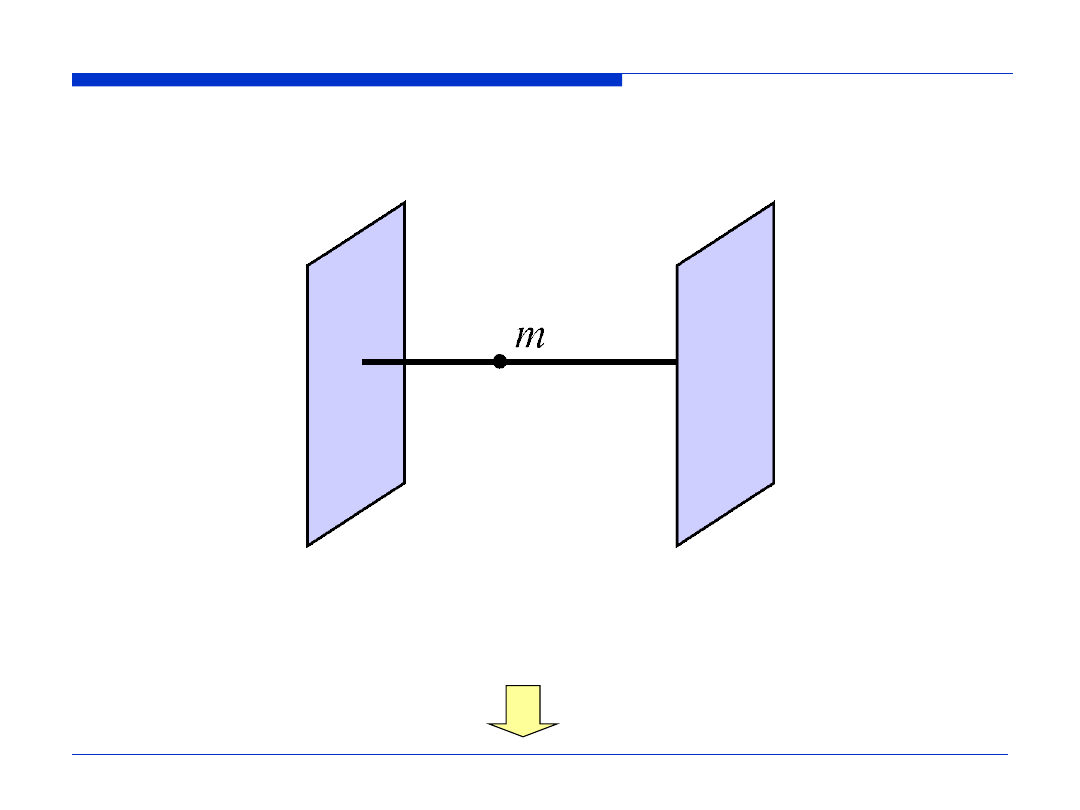
Cząstka w jednowymiarowym pudle potencjału
Cząstka w jednowymiarowym pudle potencjału
x = 0
x = L
(x)
(L) = 0
WYKŁAD 8
11
PODSTAWY CHEMII
PODSTAWY CHEMII
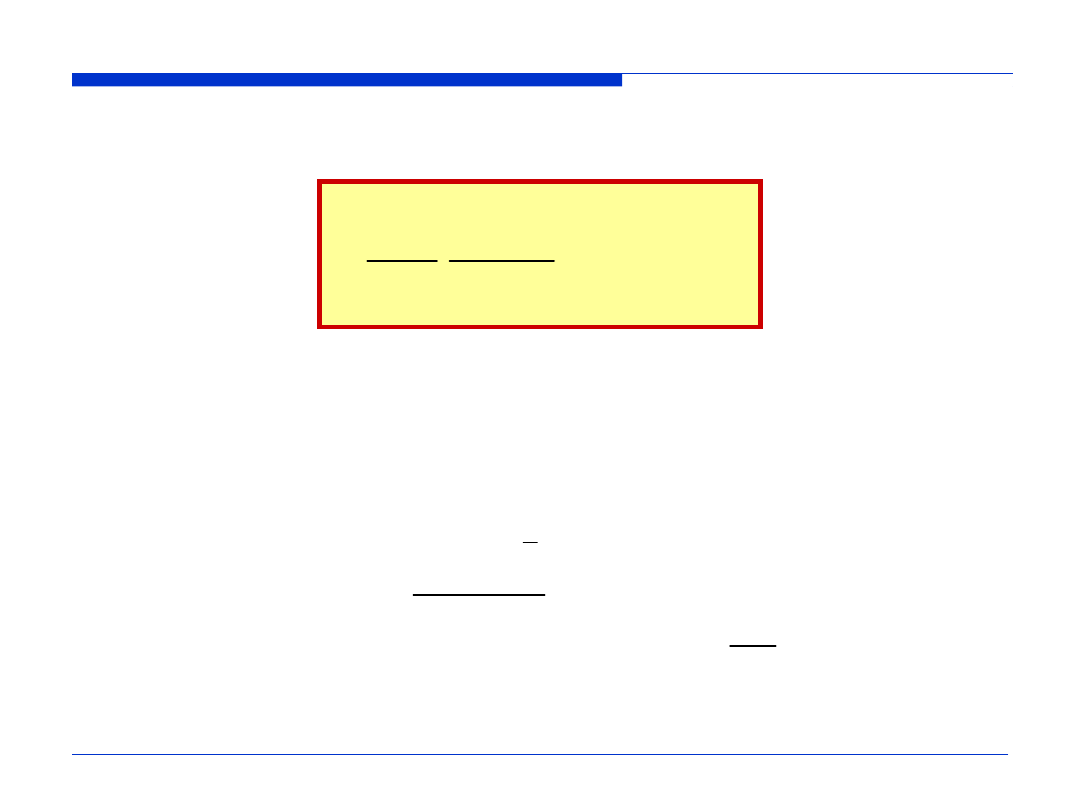
Równanie Schrödingera
Równanie Schrödingera
)
Ψ(
Ψ
2
2
2
2
x
E
dx
d
m
h
Jego ogólne rozwiązanie
Jego ogólne rozwiązanie
kx
B
kx
A
x
cos
sin
)
Ψ(
gdzie
gdzie
E
– energia cząstki
2
h
A, B
– stałe całkowania
2
1
)
2
( mE
k

WYKŁAD 8
12
PODSTAWY CHEMII
PODSTAWY CHEMII
Warunek brzegowy dla x = 0
Warunek brzegowy dla x = 0
(x) = 0
(x) = 0
sin
sin
kx
kx
= 0
= 0
cos
cos
kx
kx
= 1
= 1
(x)
(x)
x=0
x=0
=
=
B
B
= 0
= 0
(x) =
(x) =
A
A
sin
sin
kx
kx
Warunek brzegowy dla x =
Warunek brzegowy dla x =
L
L
(
(
L
L
) = 0
) = 0
(L) =
(L) =
A
A
sin
sin
kL
kL
= 0
= 0
a zatem
a zatem
albo
albo
A
A
= 0
= 0
albo
albo
sin
sin
kL
kL
= 0
= 0
Przypadek A=0 wykluczamy gdyż prowadzi on do wniosku, że
Przypadek A=0 wykluczamy gdyż prowadzi on do wniosku, że
cząstka nie istnieje
cząstka nie istnieje
(
(
(x)= 0 dla 0 < x<
(x)= 0 dla 0 < x<
L
L
)
)

WYKŁAD 8
13
PODSTAWY CHEMII
PODSTAWY CHEMII
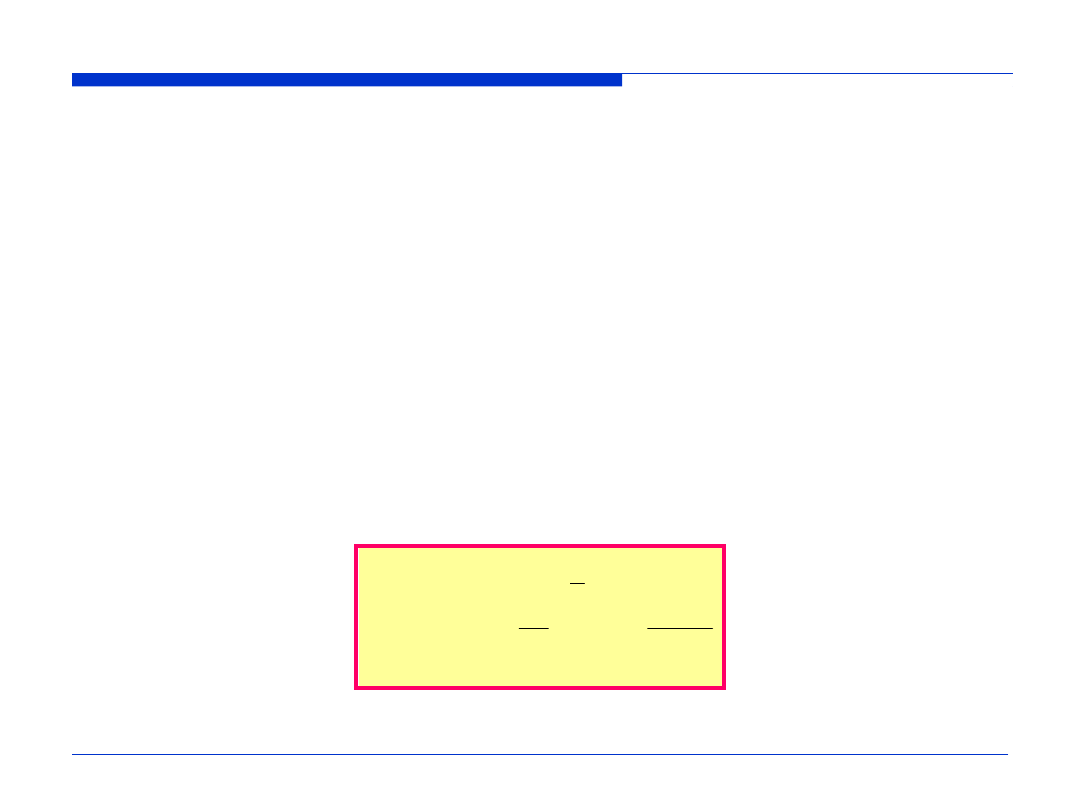
a zatem
a zatem
sin
kL
= 0
kL
=
n
n
n
– liczba całkowita
– liczba całkowita
2
2
2
8mL
h
n
E
n
mE
L
2
1
)
2
(
WYKŁAD 8
14
PODSTAWY CHEMII
PODSTAWY CHEMII
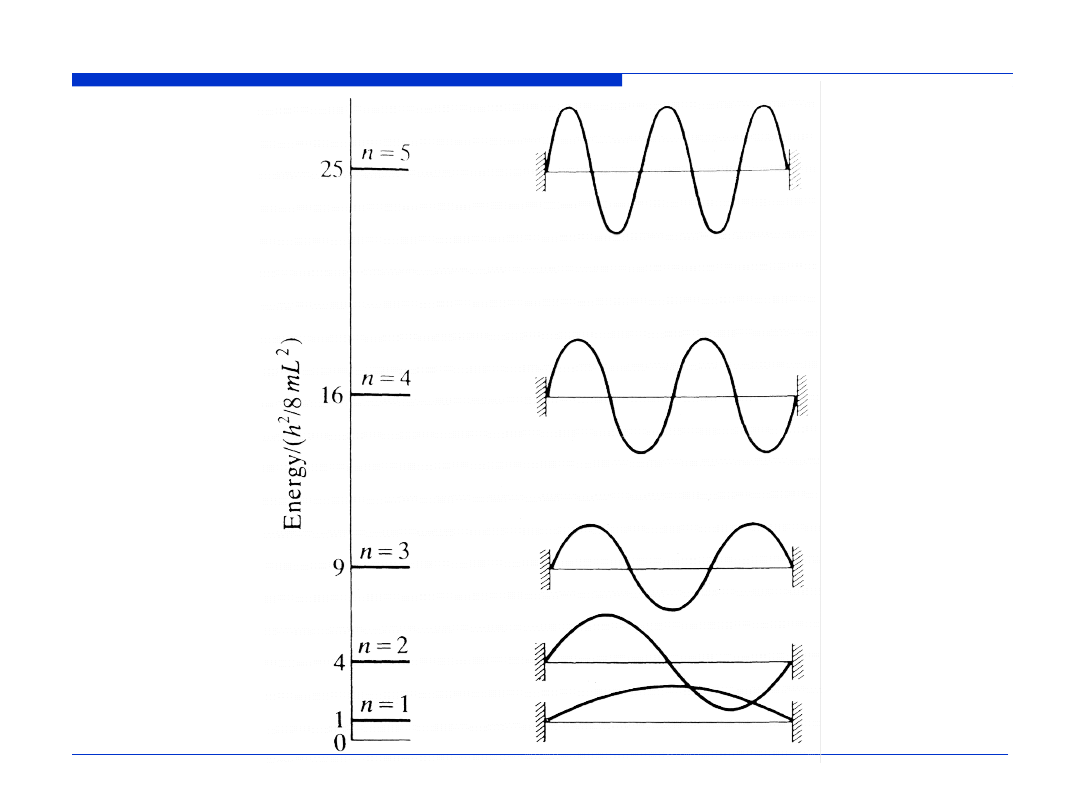
Energia jest kwantowana, a jej wartość zależy od liczby kwantowej
Energia jest kwantowana, a jej wartość zależy od liczby kwantowej
n
n
Dla stanu podstawowego
Dla stanu podstawowego
n
n
= 1
= 1
Dla stanu wzbudzonego
Dla stanu wzbudzonego
n
n
> 1
> 1
Można wykazać, że z warunku
Można wykazać, że z warunku
L
dx
x
0
2
1
)
(
wynika wzór
wynika wzór
L
x
n
L
x
n
sin
2
)
(
2
1
określający funkcję własną dla
określający funkcję własną dla
n
n
-tego poziomu energetycznego.
-tego poziomu energetycznego.
WYKŁAD 8
15
PODSTAWY CHEMII
PODSTAWY CHEMII
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
Wyszukiwarka
Podobne podstrony:
AGH e-Fizyka 11 Cząstki i fale - podstawy mechaniki kwantowe, Fizyka i Fizyka chemiczna
1) Podstawowe prawa mechaniki kwantowej
1) Podstawowe prawa mechaniki kwantowej
mechanika kwantowa
Ostwald M Podstawy mechaniki Mechanika techniczna
Przewłócki J Podstawy mechaniki budowli
maszyny proste, Technik BHP, CKU Technik BHP, CKU, Notatki szkoła CKU (BHP), Podstawy mechaniki, Mec
MECHANIKA KWANTOWA
Lista6, PWr WME Energetyka, Podstawy mechaniki i wytrzymałości Polko
Lista2, PWr WME Energetyka, Podstawy mechaniki i wytrzymałości Polko
Mechanika kwantowa
Neuronalne podstawy mechanizmu A Buzzelli 2010 id 317584
Mechanika kwantowa wstęp
Projekt 2 - Ewa Litwinek, Akademia Górniczo - Hutnicza, Technologia Chemiczna, Studia stacjonarne I
Przekładnia zębata gotowe, podstawy mechaniki
Podstawy Mechaniki i Konstrukcji Maszyn
7 Mechanika kwantowa 2
więcej podobnych podstron