
Środowisko
Morza
Bałtyckiego
Wersja „elektroniczna”
Toksykologia –
Wpływ Zanieczyszczeń
na Środowisko
Autor
Jan Erik Kihlström
Tłumaczenie
Andrzej Kędziorski
Zeszyt 6

P
RZEDMOWA
Kolejna część kursu traktuje o wpływie chemicznych zanieczyszczeń na
Morze Bałtyckie i jego otoczenie. Opisuje ich oddziaływanie na organiz−
my żywe, populacje i całe ekosystemy, oraz próbuje wyjaśnić czy i jeśli
tak to w jaki sposób zagrażają one życiu w Bałtyku. Na koniec przedsta−
wia możliwe sposoby zmniejszenia tych zagrożeń w omawianym regionie.
Zrozumienie działania czynników zanieczyszczających środowisko (tzw.
polutantów) wymaga pewnej podstawowej wiedzy z zakresu biologii.
Także przy ich charakterystyce przyjęto, że Czytelnik opanował podsta−
wy z zakresu chemii. Tym niemniej pochodzenie oraz wytwarzanie oma−
wianych związków zostało przedstawione zaledwie w krótkim podsu−
mowaniu. Bardziej wyczerpująco zagadnienia te omówiono w poprzednim
zeszycie (
Liczba substancji zanieczyszczających obecnych w regionie Bałtyku jest
ogromna. Chemiczna natura większości z nich pozostaje nieznana, po−
dobnie jak efekty ich działania. Sądzimy jednak, że posiadamy pewną
wiedzę o zjawiskach i procesach jakie tu zachodzą. Można bowiem przy−
jąć, że związki o podobnej strukturze oddziałują w podobny sposób. Za−
tem podane w tej broszurze przykłady dotyczące najlepiej poznanych
substancji można uznać za reprezentatywne także dla innych, podob−
nych związków chemicznych.
Toksyczne efekty związków chemicznych dla organizmów mieszczą się
w szerokim spektrum, poczynając od uszkodzeń DNA i struktury chro−
mosomów (tzw. efekty genotoksyczne) aż do zaburzeń w funkcjonowaniu
narządów, a nawet zmian na złożonym poziomie ekosystemu. W takim
zakresie oddziaływań efekty genotoksyczne można uważać za mało is−
totne. Wniosek taki potwierdzają znane własności głównych zanieczy−
szczeń, ich stężenia w środowisku oraz skutki ich obecności. W dalszej
części skupimy się zatem tylko na zmianach wywoływanych na pozi−
omie narządów, całych organizmów, populacji i ekosystemów.
Wiele z podanych tu przykładów odnosi się do Szwecji i przyległych czę−
ści Bałtyku. Wynika to z faktu, że obszary te są najlepiej przebadane
z punktu widzenia ekotoksykologii. Jednakże wnioski z tych badań są
z pewnością aktualne dla całego regionu.
Istotny wkład w powstanie tej broszury włożył Lars Rydén. Układ tek−
stu wykonał Benny Kullinger a nad poprawnością językową (wersji an−
gielskiej – przyp. tłum.) czuwał Donald MacQueen.
Uppsala, luty 1992
Jan Erik Kihlström

S
PIS
T
REŚCI
............................................................................................... 4
Chemiczne zanieczyszczenia Morza Bałtyckiego .......................................... 6
.................................... 10
Ze środowiska do organizmów żywych ......................................................... 13
Losy zanieczyszczeń w organizmie – akumulacja i biomagnifikacja ..... 14
Zatrucie wrodzone – przepływ toksyn od matki do dziecka .................... 16
Zwierzęta: czynności nerwów i mięśni .......................................................... 19
Układ odpornościowy i organogeneza ........................................................... 20
Fizjologia rozrodu jest bardzo wrażliwa na zanieczyszczenia ................ 20
Populacja fok w Bałtyku jest zagrożona ....................................................... 21
Wrażliwym stadium u ptaków jest jajo .......................................................... 22
Ryby w jeziorach są zagrożone przez metale ciężkie ................................. 23
................................................................... 24
Zanieczyszczenia wywołują efekty łańcuchowe w ekosystemach .......... 24
Przykład – ekosystem zmieniony przez zakwaszenie ................................ 25
Zmiany w sąsiedztwie zakładów metalurgicznych ..................................... 25
? ................................ 27
Pierwsze akcje – zakaz stosowania rtęci i DDT ........................................... 27
Chlorowane dwufenyle (PCB) – długotrwały problem .............................. 28
Model cykliczny – czy kiedyś znikną zanieczyszczenia? ........................... 30
............................................................................................. 33
............................................................................................. 34

Strona 4
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
1.
W
PROWADZENIE
1.1. Groźba dla życia w Bałtyku
Można zapytać czy rzeczywiście organizmy żyjące w Bałtyku są zagrożone. Obserwacje pro−
wadzone w latach 50 i 60 dostarczyły szeregu dowodów świadczących o zaburzeniach w eko−
systemach. Spośród najbardziej spektakularnych zmian jakie w tym okresie miały miejsce
w Morzu Bałtyckim należy wymienić dramatyczne zmniejszenie liczebności fok, zarówno foki
szarej (Haliochaerus grypus) jak i nerpy (Pusa hispida), oraz przypadki znajdowania martwych orłów
bielików. Liczebność innych gatunków także zmalała. Nieco później zaobserwowano tendencję
do częstszego występowania uszkodzeń płetw u okoni oraz deformacji szczęk u szczupaków
(
). Już w latach sześćdziesiątych pojawiły się wyraźne wskazówki, że przyczyną tych
zjawisk są chemikalia używane przez człowieka. W wielu przypadkach podejrzenia te potwier−
dziły się. Terminy „toksyczny bigos” lub „chemiczny bigos” wprowadzono na określenie mie−
szanin potencjalnie groźnych substancji, głównie pochodzenia antropogennego, obecnych w śro−
dowisku.
Całe zagadnienie należy jednak widzieć nieco szerzej. Bowiem nie tylko związki chemiczne
uwalniane w wyniku funkcjonowania społeczeństwa oddziałują na pojedyncze osobniki, popu−
lacje i całe ekosystemy. Wiele innych działań podjętych przez człowieka prowadzi do podobnych
konsekwencji. Gwałtowne zmiany krajobrazu są ważnym czynnikiem prowadzącym do zmia−
ny warunków w ekosystemach. Klasycznym przykładem tego typu jest niemal całkowite wy−
ginięcie bociana w południowej Szwecji. Ptak ten żyje na podmokłych łąkach, tymczasem już
w ubiegłym wieku zostały one osuszone i wykorzystane dla celów rolniczych. Kolejnym przykła−
dem jest kuropatwa zamieszkująca ekotony, skrawki terenu pomiędzy małymi polami. Aktu−
alnie w Szwecji gatunek ten jest niemal na wymarciu. Tradycyjne rolnictwo stwarzało dobre
warunki dla jego rozwoju,
natomiast nowoczesne, ra−
cjonalne i uprzemysłowione
rolnictwo ze swoimi olbrzy−
mimi polami drastycznie
ogranicza miejsca bytowa−
nia kuropatwy. Opisane
zmiany w krajobrazie nie
wszędzie zachodzą w jedna−
kowym stopniu, stąd też np.
w Polsce liczebność tych
ptaków jest nadal stosun−
kowo duża.
Gwałtowne fluktuacje licze−
bności populacji zachodzą
często z nieznanych powo−
dów. Mewa śmieszka była
rzadkim morskim ptakiem
jeszcze w pierwszej połowie
XX wieku. Później stała się
bardzo pospolita jako ptak
Ryc. 1.
Zniekształcone szczęki u szczupaka złowionego w odbiorniku ście−
ków pochodzących z zakładów przemysłu celulozowo–papierniczego w Nor−
rsundet na zachodnim wybrzeżu Zatoki Botnickiej. [fot. udostępnił Jan
Thulin].
Strona 5
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
lądowy najwyraźniej o zmienionych zwyczajach żywieniowych. Obecnie obserwujemy spadek
liczebności w populacji tych ptaków, jednak przyczyna tego stanu rzeczy pozostaje zagadkowa.
W samym Bałtyku również obserwujemy poważne zmiany. W ciągu ostatnich 20 lat wielkość
populacji szprota zmieniła się kilkunastokrotnie. Sądzimy, że przyczyną tego są fluktuacje
liczebności dorsza, który jest jego głównym drapieżnikiem. Z kolei wiemy, że rozród dorsza
zależy od poziomu tlenu w strefie przydennej, poniżej gradientu zasolenia wody. Wreszcie,
zawartość tlenu wzrasta wskutek napływu do Bałtyku słonej wody z Morza Północnego, ale
maleje w wyniku dodatkowego napływu substancji odżywczych. Ten przypadek ilustruje dość
złożony łańcuch przyczynowo–skutkowy, który często decyduje o losach poszczególnych popula−
cji w ekosystemie. W tym przypadku wpływ związków chemicznych, tj. składników odżywczych,
miał charakter pośredni.
W niniejszej broszurze skupimy się jednak na wpływie toksycznych chemikaliów, tj. na
toksykologii. Dziedzina nauki zwana ekotoksykologią zajmuje się wytworzonym przez czło−
wieka „chemicznym bigosem”, jego składem, przenoszeniem przez wiatry i wodę, pobieraniem
przez rośliny i zwierzęta, rozmieszczeniem w ekosystemie, metabolizowaniem i degradacją oraz,
co najważniejsze, oddziaływaniem na organizmy, populacje i całe ekosystemy.
1.2. Łańcuch zanieczyszczeń
Efekty „chemicznego bigosu” w środowisku można opisać ogólnie w oparciu o tak zwany łańcuch
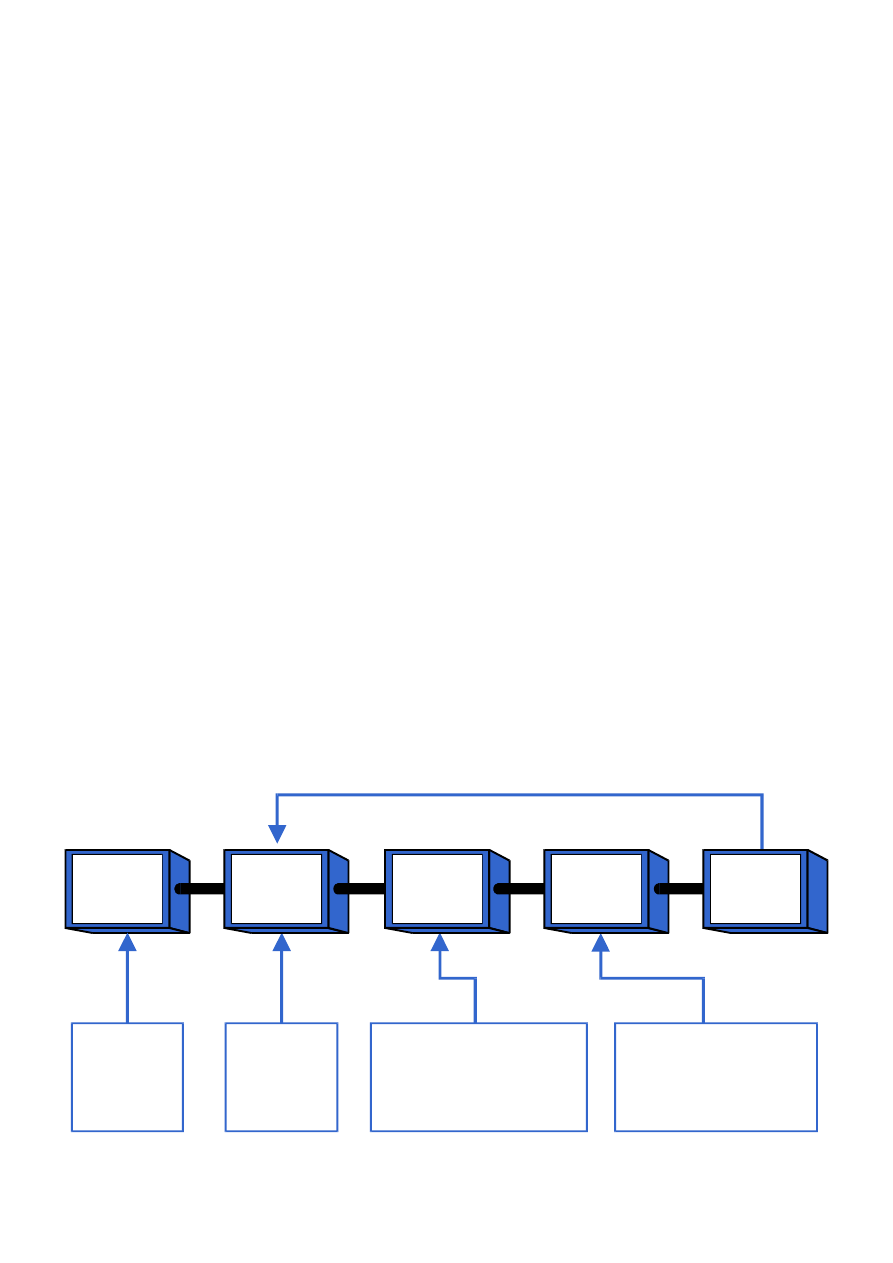
zanieczyszczeń. Jest to schemat przepływowy, przedstawiający losy związków począwszy od
ich powstania, przez rozprzestrzenianie się w środowisku, pobieranie przez organizmy żywe
aż do ich degradacji (
). Pierwsze ogniwo tego łańcucha przedstawia źródła zanieczyszczeń.
Należą tu substancje różnego pochodzenia w różnych ilościach uwalniane do środowiska, itp.
Ostatnie obliczenia wskazują, że w skali światowej mniej więcej codziennie znajduje się
w użyciu jakieś 70 do 80 tysięcy różnych związków. Oczywiście, w tej sytuacji istnieje ryzyko,
że tysiące z nich znajdą się w środowisku. Na szczęście część z nich jest szybko rozkładana
dzięki chemicznym procesom, zachodzącym w powietrzu, glebie i wodzie, tracąc tym samym
swoją toksyczność. Z drugiej strony chemicznie stabilne, lub trwałe, substancje pozostają
w środowisku, nieraz przez stosunkowo długi czas.
Wiele z tych związków ma zdolność przenikania przez błony biologiczne. Zatem mogą one być
pobierane przez bakterie, rośliny i zwierzęta. Takie związki określa się jako biologicznie
dostępne. W wielu przypadkach są one jednak rozkładane biologicznie do nieszkodliwych
Ryc. 2.
Łańcuch zanieczyszczeń opisuje losy zanieczyszczeń
chemicznych poczynając od źródła aż do ich rozkładu.
ród³a
Wytwarzanie
Substancje
chemiczne
Iloci
Woda
Powietrze
Gleba
Mechanizmy
Transport biologiczny
Kumulacja w organizmach
Biomagnifikacja
Osobniki
Gatunki i populacje
Ekosystemy
Transport
Pobieranie
Skutki
Rozk³ad

Strona 6
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
metabolitów a następnie (lub bezpośrednio) szybko wydalane przez organizmy. Jednak pomimo
tego nadal pozostają setki produktów trwałych i trudnych do wydalenia, które będą się
gromadziły lub akumulowały w różnych tkankach roślin i zwierząt. Głównym problemem
ekotoksykologii jest badanie różnych dróg, którymi te substancje, tak zwane ksenobiotyki lub
inaczej związki obce dla żywych komórek {gr. xénos = obcy, gr. bios = życie – przyp. tłum.}
uszkadzają organizmy i żywe komórki. Praktycznie biorąc, wszystkie trwałe substancje są
w pewnym stopniu toksyczne głównie dlatego, że organizm ma trudności z pozbyciem się ich.
W wielu przypadkach toksyczność jest wyraźnie widoczna, w związku ze sposobami
oddziaływania tych substancji na procesy biologiczne, takie jak wzrost, rozmnażanie i rozwój.
Ostatnie ogniwo łańcucha zanieczyszczeń stanowi rozkład. Związki organiczne zostają
ostatecznie przekształcone do dwutlenku węgla, wody i może jeszcze kilku innych
nieszkodliwych produktów końcowych, jak np. jonów chlorkowych, stanowiących naturalne
składniki biosfery. Degradacja może być wynikiem procesów fizycznych, np. wyzwalanych pod
wpływem światła ultrafioletowego, zwykle jednak zachodzi wskutek procesów biologicznych.
Najczęściej organizmami aktywnymi w tym działaniu są bakterie i mikroskopijne grzyby.
Posiadają one bogaty zestaw reakcji metabolicznych, a ich substratami często są również
ksenobiotyki. Zanim jednak to nastąpi może minąć długi czas. Okres półtrwania wielu
szkodliwych substancji w ekosystemach w regionie Bałtyku może wynosić dziesiątki lat.
W warunkach mniej typowych, jak obszary polarne, okres ten może być znacznie dłuższy, choć
brak jak dotąd precyzyjnych pomiarów tego rodzaju. Metale ciężkie stanowią oczywiście
przypadek szczególny. Jako pierwiastki nigdy nie ulegną przekształceniu do czegoś innego.
Zamiast tego wrócą ostatecznie do podłoża np. w osadach na akumulujących obszarach den−
nych Bałtyku i innych wód regionu. Tam pozostaną już na zawsze lub powrócą do obiegu, jeżeli
osady denne znajdą się ponownie jako zawiesina w wodzie, zaczynając w ten sposób nową podróż
przez łańcuch zanieczyszczeń.
1.3. Chemiczne zanieczyszczenia Morza Bałtyckiego
Z powyższego rozważania można wyciągnąć wniosek, że najbardziej niebezpiecznymi substan−
cjami w środowisku są te, które łączą w sobie trwałość z biologiczną dostępnością. Większość
związków posiadających ten zestaw cech należy do jednej z trzech głównych grup chemicznych
produktów:
●
metali i ich organicznych pochodnych, zwłaszcza metali posiadających gęstość większą od 5,
często zwanych metalami ciężkimi, jak np. rtęć (Hg), kadm (Cd), ołów (Pb) i inne
●
organicznych substancji, których jeden lub więcej atomów wodoru zostało podstawione
przez atomy chloru (lub bromu albo fluoru, czyli ogólnie przez halogeny) często zwanych
chlorowcowanymi węglowodorami (
●
wielopierścieniowe węglowodory aromatyczne (
PAH
– z ang. polycyclic aromatic hydro−
carbons lub krócej polyaromatic hydrocarbons – przyp. tłum.) czyli cząsteczki złożone z wielu
pierścieni aromatycznych.
Niektóre z chemicznych zanieczyszczeń obecnych w biosferze np. metale i niektóre z ich
związków powstają w procesach naturalnych, głównie wietrzenia skał. Dość wcześnie w historii
ludzkości działalność człowieka powiększała to naturalne dotąd zanieczyszczenie. Nawet
najbardziej prymitywne formy obróbki metali stosowane kilkanaście tysięcy lat temu
zwiększały uwalnianie metali i ich związków do środowiska. Obecnie działalność człowieka
stanowi daleko ważniejsze źródło zanieczyszczenia metalami niż wietrzenie skał i to zarówno
w skali globalnej jak i w regionie Bałtyku (
).
Chlorowane węglowodory częściowo również mogą być pochodzenia naturalnego, np. dioksyny
i substancje pokrewne (
) powstają, jak się przypuszcza, podczas naturalnych pożarów
lasów. Jednakże zdecydowana ich większość jest dziełem człowieka i znajduje zastosowanie
w przemyśle {np. wielochlorowane dwufenyle, czyli
PCB
– z ang. polychlorinated biphenyls –
Strona 7
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
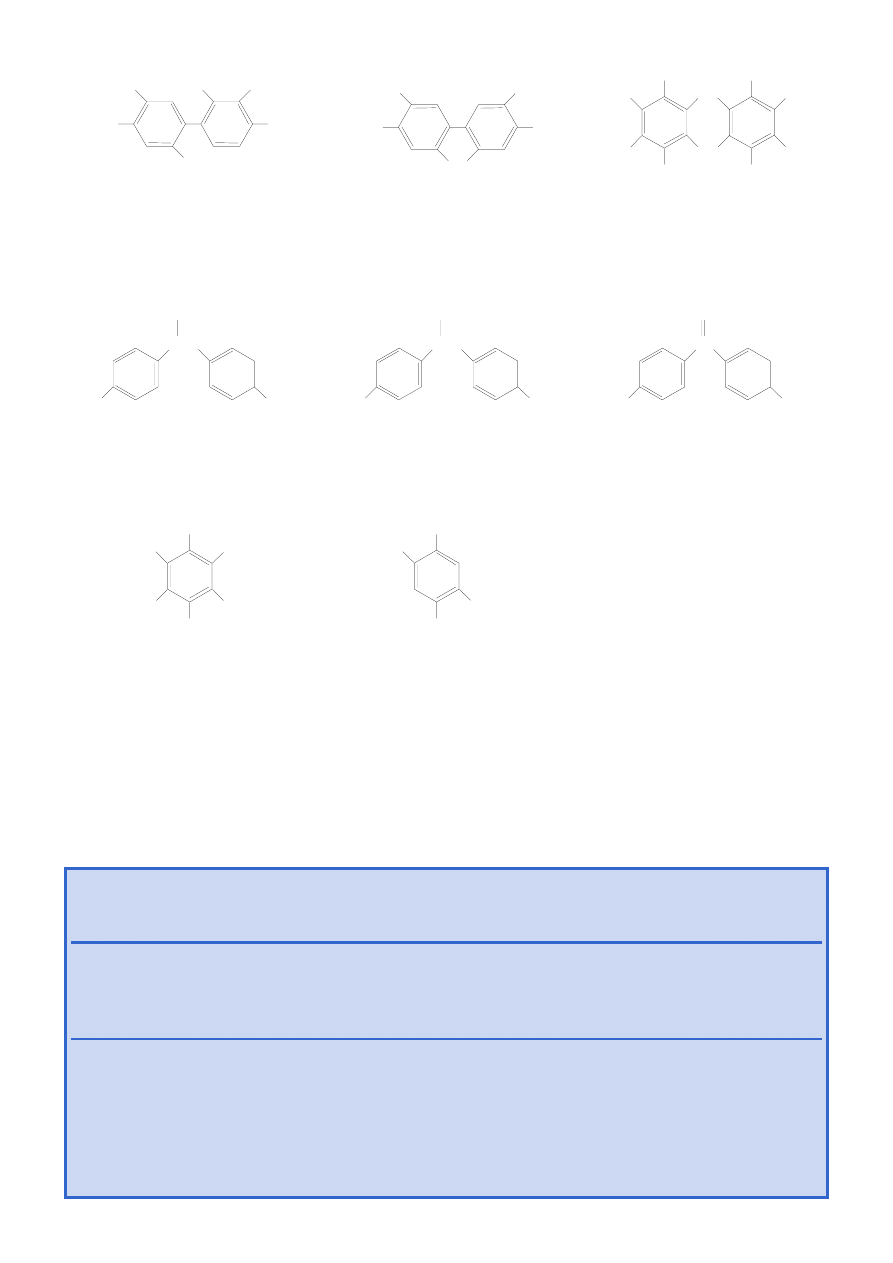
Ryc. 3.
Chlorowane węglowodory są toksycznymi związkami organicznymi, zbudowanymi z aromatycznych
pierścieni zawierających kilka lub więcej atomów chloru. Zidentyfikowano już kilka tysięcy takich związków.
Są wśród nich zarówno biocydy jak i zanieczyszczenia przemysłowe (zob.
Emisje przemysłowe
i zanieczyszczenia toksyczne
). Zwykle są one trwałe i dostępne dla organizmów żywych.
p,p- DDE
CCl
2
Cl
Cl
C
omiochlorodwubenzo-
-p-dioksyna
Cl
Cl
Cl
Cl
Cl
Cl
Cl
Cl
O
O
p,p- DDT
Cl
Cl
CH
CCl
3
szeciochlorodwufenyl
Cl
Cl
Cl
Cl
Cl
Cl
piêciochlorofenyl
Cl
Cl
Cl
Cl
Cl
OH
p,p- DDA
COOH
Cl
Cl
CH
czterochlorodwubenzofuran
Cl
Cl
Cl
Cl
O
2,4,5-T
Cl
Cl
Cl
OCH COOH
2
Tab. 1.
Ilości różnych metali (w tonach na rok) uwalnianych rocznie do Bałtyku
[wg danych Lithnera, 1990].
Metal
W wyniku procesów
W wyniku procesów
naturalnych (N)
antropogenicznych (A)
A/N
(dane szacunkowe)
(opad atmosferyczny
oraz wody ściekowe)
Cynk
8 530
21 154
2,5
Miedź
2 495
4 745
1,9
Kadm
41
210
5,1
Ołów
505
3 330
6,6
Rtęć
5,4
30,3
5,6

Strona 8
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
przyp. tłum.}, powstaje jako produkty uboczne w papierniach (np. chlorowane fenole) lub jest
rozpylana jako insektycydy (np. DDT czyli dwuchloro–dwufenylo–trójchloroetan) itp.
Obecnie poziom DDT w Bałtyku jest stosunkowo niski w porównaniu z tymi, które notowano
zanim, około 1970 roku, kilkanaście krajów wprowadziło zakaz stosowania DDT. Stężenia PCB
również uległy zmniejszeniu choć nie tak znacznemu jak DDT. Większa część PCB obecnego
w Bałtyku znajduje się w osadach dennych. Najprawdopodobniej ta ukryta pula będzie sto−
pniowo przenoszona do organizmów żywych tego regionu, co może trwać przez dziesiątki lat.
W czasie ostatniej dekady sporo
uwagi poświęcono chlorowanym
węglowodorom stanowiącym
produkty uboczne powstające
podczas bielenia masy papierni−
czej. W Zatoce Botnickiej jest to
największe źródło skażenia wo−
dy tymi związkami (
).
Jednakże większość wspomnia−
nych produktów ubocznych,
często oznaczanych skrótem
EOCl {z ang. extractable orga−
nic bound chlorine czyli chlor
w połączeniach organicznych
możliwy do odzyskania metodą
ekstrakcji – przyp. tłum.}, nie
została dotychczas chemicznie
zidentyfikowana.
Większość wielopierścieniowych węglowodorów aromatycznych powstaje w czasie niekomplet−
nego spalania. Zatem mogą one powstawać zarówno podczas pożarów naturalnych jak i tych
spowodowanych przez człowieka. Ponadto powstawanie ropy naftowej i naturalnego asfaltu
zachodzi dzięki podobnym procesom {tj. niekompletnego utleniania – przyp. tłum.}. Tak więc
PAH można znaleźć w takich produktach jak olej mineralny, smoła węglowa, smoła drzewna
(dziegieć) itp. Kilka przykładów tych substancji podano na
.
Zanieczyszczenia można również sklasyfikować w oparciu o ich pochodzenie. Z tego punktu
widzenia są trzy główne typy źródeł zanieczyszczenia, obejmujące olbrzymią większość
omawianych substancji, czyli:
1.
Źródła związane z produkcją energii, oprócz innych związków uwalniające takie istotne
zanieczyszczenia jak tlenki siarki (SO
x
), tlenki azotu (NO
x
), węglowodory, tlenek węgla,
pyły itp. Analizując te związki z punktu widzenia problemów środowiskowych i zdrowotnych
okazuje się, że zagrożenia nimi wywołane niekoniecznie są proporcjonalne do ich ilości.
Tlenek węgla jest uwalniany w największych ilościach. Pomimo to jest on najmniej szko−
dliwy ponieważ symptomy zatrucia czadem są łatwo odwracalne.
Ryc. 4.
Węglowodory wielopierścieniowe (w skrócie PAH) są toksycznymi związkami organicznymi
składającymi się z kilku połączonych pierścieni aromatycznych. Również i w tej grupie opisane związki
cechuje duża różnorodność. Często są one trwałe i łatwo dostępne dla organizmów.
Tab. 2.
Emisje do Bałtyku chlorowanych węglowodorów ulegających
adsorpcji (AOX). Kilka procent podanych wartości (tu przyjęto ok.
1–5%) stanowią rozpuszczalne w tłuszczach chlorowce organiczne
uważane za najgroźniejsze dla organizmów żywych. [Enell M.
i Johnsson P., informacja ustna].
Źródło
Ilości w tonach na rok
jako AOCl
rozpuszczalne
w tłuszczach
Spływ z rzekami
18–26 000
2–1 000
Opad atmosferyczny
5–6 000
50–250
Przemysł drzewny
>15 000
>150–750
Inne źródła
>1 000
>10–50

Strona 9
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
2.
Źródła przemysłowe, uwalniające bardzo wiele różnych zanieczyszczeń, w tym te wymie−
nione powyżej, jak również metale ciężkie, chlorowce, itp. Najbardziej niebezpieczne spo−
śród nich to np. chlorowane węglowodory, kadm, ołów, rtęć i inne metale ciężkie.
3.
Pestycydy używane w rolnictwie i gospodarce leśnej. Są one zasadniczo konstruowane w celu
zabicia specyficznych szkodników takich jak owady, chwasty, grzyby itp. Jednakże podsta−
wowe funkcje wszystkich organizmów są podobne. Stąd też nawet selektywne preparaty
mogą być groźne dla organizmów nie będących celem ich stosowania. Sprzedaż pestycy−
dów w Szwecji w przeliczeniu na tony substancji czynnych podano w
zużycie pestycydów jest takie, że ich poziom w środowisku w Szwecji jest dość niski. Naj−
prawdopodobniej podobna sytuacja panuje w większości krajów w regionie Bałtyku.
Tab. 3.
Biocydy sprzedane w Szwecji w 1990 r. (w tonach substancji czynnej)
[Źródło: Szwedzki Urząd Kontroli Związków Chemicznych].
Sadow−
Gospo−
Rol−
Leś−
nictwo
Przemysł dar stwa
Łącznie
Zastosowanie
nictwo nictwo i warzyw−
domowe
nictwo
ton
%
Zaprawy nasienne
97
0
0
0
0
97
0,0
Fungicydy
546
2
62
14
0
610
6,9
Herbicydy
1 631
6
28
16
66
1 743 19,6
Regulatory wzrostu
44
0
5
0
0
49
0,5
Insektycydy
25
3
11
29
14
83
0,9
Moluskocydy
0
0
0
130
0
130
1,5
Środki ochrony drewna
0
0
1
5 922
146
6 069 68,4
Inne
0
3
1
34
56
56
1,1
Razem:
ton
2 343
13
108
6 122
282
8875
%
26,4
0,1
1,2
69,1
3,2
100
100
Strona 10
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
2.
O
D
ŹRÓDŁA
ZANIECZYSZCZEŃ
DO
ŻYWEGO
ORGANIZMU
2.1. Przenoszenie przez wiatry
Drugie ogniwo w łańcuchu zanieczyszczeń symbolizuje fizyczny transport chemicznych za−
nieczyszczeń, czyli przenoszenie za pomocą wiatru i wody, oraz transport w glebie.
Wszystkie zanieczyszczenia emitowane do atmosfery z kominów fabrycznych, domowych, rur
wydechowych, itp. będą roznoszone przez wiatry. Ciężkie cząstki opadną na dół w pobliżu źródła,
natomiast gazy, para wodna i opary mogą być przenoszone na duże odległości. Na przykład
w 1966 roku znaleziono DDT w ciele pingwinów i fok w wodach otaczających Antarktykę a trzy
lata później również w lodowej skorupie Antarktydy. Oczywiście, nigdy nie było najmniejszego
powodu aby używać insektycydy na Antarktydzie. DDT obecny w ciele zwierząt musiał być
przeniesiony przez wodę. Jednakże jedynym możliwym sposobem dotarcia do pokrywy lodowej
był transport wraz z prądami powietrza. W regionie Bałtyku przeważające wiatry wieją
z południa i zachodu. Znajduje to odzwierciedlenie w dyspersji zanieczyszczeń, która jest
największa w kierunku dominujących wiatrów (
). Silne wiatry oznaczają, że zanieczysz−
czenia zostają wymieszane z dużymi masami powietrza, czego konsekwencją są ich niskie
stężenia. W obrębie mas powietrza występują nieuporządkowane ruchy, turbulencje, jeszcze
bardziej rozpraszające zanieczyszczenia. Te procesy mogą być jednym z powodów błędnego
stwierdzenia: „rozcieńczenie jest sposobem na zanieczyszczenie”
.
Różne zanieczyszczenia powie−
trza charakteryzują się różnym
czasem przebywania w atmosfe−
rze. W końcu jednak wszystkie
osadzają się na powierzchni zie−
mi. Osadzanie przebiega w opar−
ciu o trzy różne procesy, tj. sedy−
mentację, opad suchy i opad mo−
kry. Sedymentacja jest opadem
największych i najcięższych czą−
stek obcych w powietrzu i wystę−
puje raczej w pobliżu ich źródła.
Opad suchy oznacza, że małe czą−
steczki, gazy i opary przenoszone
w masach powietrza osiadają i są
bezpośrednio pobierane przez
glebę, rośliny i zwierzęta. Opad mokry wskazuje, że zanieczyszczenia rozpuszczają się podczas
opadów deszczu lub w kroplach tworzących chmury, spadając później wraz z deszczem lub śnie−
giem. Opad mokry stanowi skuteczny sposób usuwania z atmosfery takich zanieczyszczeń jak
związki siarki i azotu.
Z powodu przeważających kierunków wiatrów w północnej Europie, zanieczyszczenia emito−
wane w środkowej i zachodniej części kontynentu przenoszone są wraz z masami powietrza
w region Bałtyku. Zatem zanieczyszczenie tego regionu jest spowodowane nie tylko lokalnymi
emisjami ale i tymi z odległych części Europy. Istotne pytanie dotyczy czasu ich przeniesienia
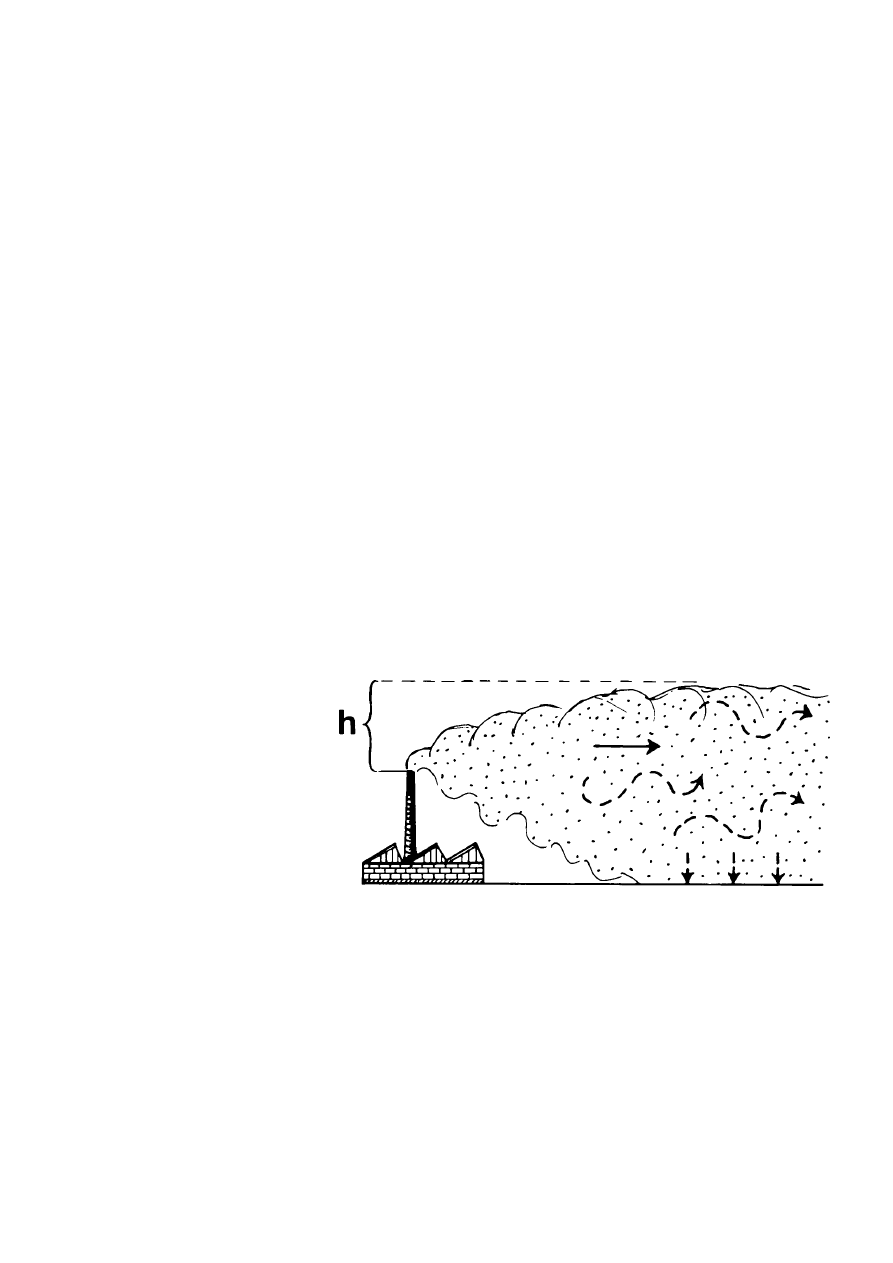
Ryc. 5.
Transport powietrzny zanieczyszczeń, ulatujących z wyso−
kiego komina, za pośrednictwem wiatrów. Strzałka pokazuje kie−
runek przenoszenia emisji; h — wysokość; strzałki przerywane fa−
lujące ilustrują turbulencje; strzałki pionowe – opad na
powierzchnię.
Strona 11
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
z wysoko uprzemysłowionych regionów, takich
jak Wielka Brytania, Zagłębie Ruhry, itp.
w rejon Bałtyku. Szybkość mas powietrza
często wynosi kilkanaście metrów na sekundę
co oznacza przejście z Wielkiej Brytanii do
Bałtyku w ciągu 12–36 godzin. Zatem trans−
port zanieczyszczeń z Wielkiej Brytanii lub
Zagłębia Ruhry w rejon Bałtyku zależy od
czasu przebywania zanieczyszczeń w powie−
trzu (ang. residence time – T) i szybkości wia−
tru (V). Duża szybkość wiatru i długi czas
utrzymywania się zanieczyszczeń zwiększają
odległość (D) jaką mogą one pokonać zanim
ulegną osadzeniu:
D = T × V
Odległość ta zależy również od wysokości emi−
sji nad poziomem gruntu. Zatem dym z wyso−
kiego komina fabrycznego będzie przenoszony znacznie dłużej niż z rury wydechowej samochodu
(
). Ogólna sytuacja meteorologiczna także wpływa na rozpraszanie zanieczyszczeń
w powietrzu. Na obszarach gdzie panuje niskie ciśnienie, zwłaszcza zimą, temperatura powie−
trza spada wraz z wysokością. Do wysokości około 10–11 km obniża się mniej więcej 1°C na
każde 100 m. W tych warunkach zanieczyszczenia są mniej więcej równomiernie rozproszone
w kierunku pionowym i dobrze wymieszane. Emisje z wysokiego komina zostaną daleko roz−
niesione. Z kolei na obszarach wysokiego ciśnienia, szczególnie popołudniami i w dolinach, czę−
sto ma miejsce inwersja temperatury w atmosferze. Oznacza to, że wraz z wysokością
temperatura rośnie zamiast spadać. Zimne, a zatem również ciężkie, powietrze poniżej inwersji
hamuje prądy wstępujące i turbulencje.
Innymi słowy cieplejsze powietrze powy−
żej warstwy inwersyjnej działa jak po−
krywa zatrzymująca zanieczyszczenia
wypuszczone na niskich poziomach, cza−
sami przez dość długi czas.
Załóżmy przykładowo, że na wysokości
1 000 m nad ziemią znajduje się war−
stwa inwersyjna. Przy szybkości wiatru
ok. 8 m/s dym z komina rozproszy się
równomiernie w kierunku pionowym
poniżej warstwy inwersyjnej i opadnie
na ziemię około 100 km dalej (
).
W odległości 1 000 km od emitora w po−
wietrzu nadal pozostaje 37% wypuszczo−
nego dwutlenku siarki opadającego
z szybkością 0,8 cm/s.
Z drugiej strony emisje powyżej war−
stwy inwersyjnej mają tendencje do
utrzymywania się na wysokim poziomie,
jako że pionowe ruchy powietrza są ha−
mowane przez pokrywę inwersyjną
(
). W takich warunkach istnieje
ryzyko tworzenia się smogu.
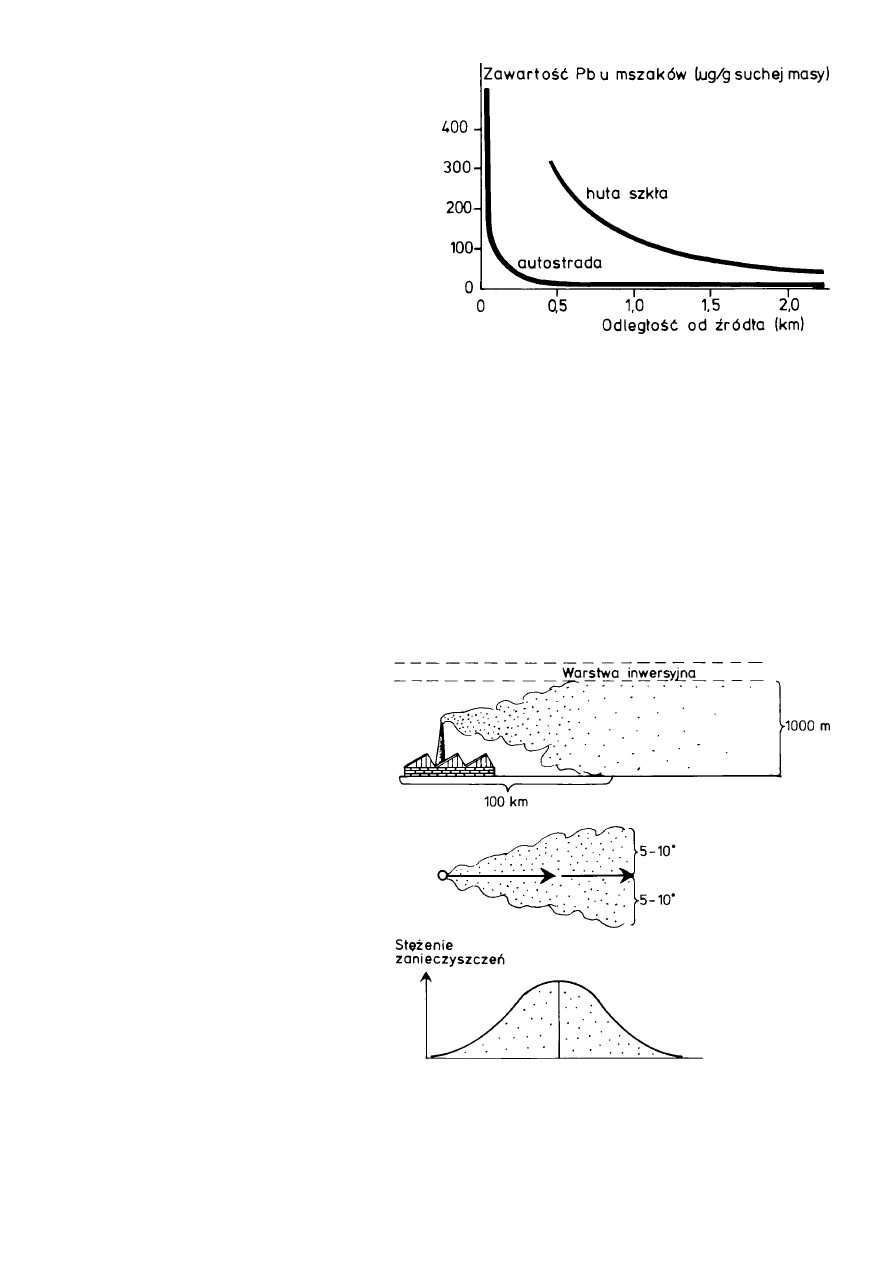
Ryc. 6.
Transport ołowiu z fabryki szkła i z autostra−
dy mierzony wielkością opadu ołowiu u mszaków (w
µg Pb/g suchej masy mchu [dane uzyskane przez
Ake Ruehling, Germind Tyler i Petera Göranssona].
Ryc. 7.
Rozmieszczenie zanieczyszczeń poniżej warstwy in−
wersyjnej, rozprzestrzenianie prostopadłe do kierunku
wiatru, i stężenia w różnych częściach smugi zanieczyszczeń
[w oparciu o dane z Monitora, 1984].
Strona 12
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
Powyższe rozważania odnoszą się do liniowego transportu zgodnie z kierunkiem przeważają−
cych wiatrów. Jednakże pióropusz dymu roznosi się także poziomo, prostopadle do kierunku
wiatru. Około 100 km od źródła emisji taki pióropusz zajmuje 10–20° okręgu, którego centrum
stanowi komin, a stężenia zanieczyszczeń maleją od linii środkowej na boki (
).
2.2. Przenoszenie przez wodę
Rozmieszczenie i transport związków chemicznych w wodzie jest bardziej złożony. Większość
toksycznych substancji obecnych w środowisku jest słabo rozpuszczalna w wodzie ale
rozpuszcza się w tłuszczach i ich rozpuszczalnikach, np. olejach, eterach, itp. Rośliny i zwierzęta
są częściowo zbudowane ze związków tłuszczowych, a zatem mogą pobierać wiele toksycznych
substancji. Niektóre z tych toksyn pozostają nawet w szczątkach szkieletów, odchodów, liści
itp. znajdywanych w jeziorach i rzekach. Takie cząstki mogą unosić się w wodzie lub też osadzać
się na dnie. Największe ilości substancji lipofilowych zwykle stwierdza się w osadach, które
funkcjonują jako pułapka dla wielu zanieczyszczeń. Wysokie stężenia związków toksycznych
są również obecne na granicy faz woda–powietrze. We wszystkich wodach pochodzenia
naturalnego obecne są substancje pochodzenia biologicznego, których cząsteczki zawierają
fragmenty rozpuszczalne w wodzie {hydrofilowe – przyp. tłum.} i rozpuszczalne w tłuszczach
{lipofilowe, a zarazem hydrofobowe – przyp. tłum.}, np. kwasy tłuszczowe (
). Takie
molekuły skupiają się na granicy faz, zanurzone częścią hydrofilową w wodzie, a lipofilową
w powietrzu. W ten sposób na powierzchni wody tworzy się cienka błona lipidowa. W jej obrębie
będzie zachodziła akumulacja substancji rozpuszczalnych w tłuszczach, które mogą osiągać
wysokie stężenia. Na przykład w niektórych przypadkach stężenie PCB w takiej błonie jest
ponad 1 000 razy wyższe niż w całej masie wody, nawet jeśli całkowita ilość zanieczyszczeń
w błonie jest niska.
W jeziorze można zatem wy−
różnić cztery przedziały lub
frakcje, różniące się stężenia−
mi zanieczyszczeń:
1.
woda,
2.
organizmy i zawiesina
materii organicznej,
3.
osady, oraz
4.
błona powierzchniowa.
Te frakcje oddziałują ze sobą
na wiele sposobów. Na przy−
kład zwierzęta ryjąc w mule
dennym powodują transport
zawartych w nim zanieczy−
szczeń w górę, z kolei martwe
organizmy zawierające zanie−
czyszczenia opadają na dno
itp. Wysokie stężenia w błonie
powierzchniowej mają istotne
konsekwencje biologiczne, ja−
ko że wiele organizmów żyje
w ścisłym związku z tą strefą. Na przykład larwy komarów żyją przez długi czas tuż pod po−
wierzchnią, wystawiając grzbietową część odwłoka ponad wodę, wiele roślin wyrasta ponad
powierzchnię a liście unoszą się na niej itp.
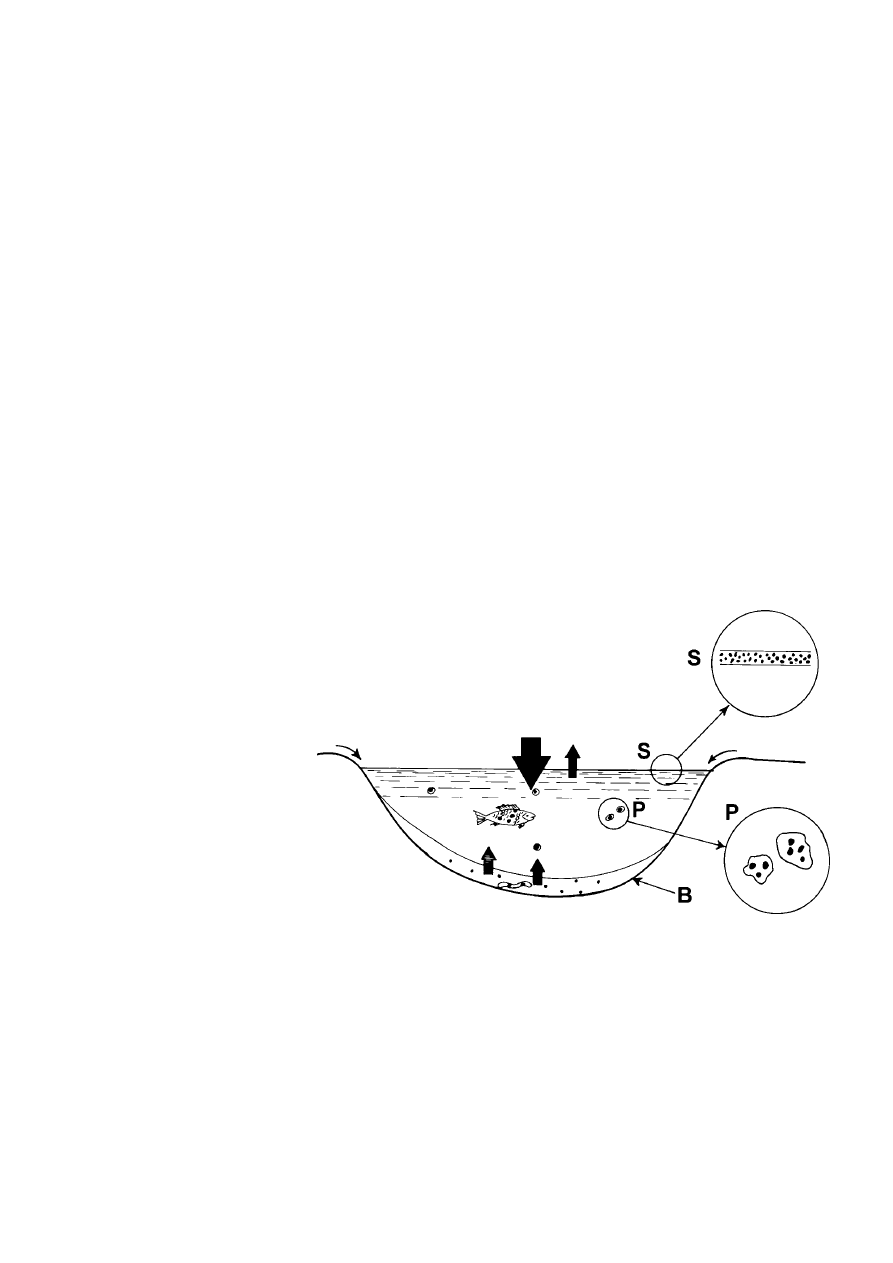
Przeważająca część zanieczyszczeń wodnych znajduje się w osadach. W połączeniu z wielkimi
ruchami wody na płytkich obszarach, np. w czasie wiosennych powodzi, zanieczyszczenia te
są częściowo transportowane do wody wraz z osadami. Poza tymi ruchami zanieczyszczeń
Ryc. 8.
Rozmieszczenie zanieczyszczeń lipofilowych (kropki) w jeziorze.
Zagęszczenie kropek oznacza stężenie zanieczyszczeń, natomiast strzałki
ilustrują transport. Poszczególne frakcje oznaczono następująco:
(S)
błona powierzchniowa;
(B)
osady denne;
(P)
cząsteczki w wodzie [z
Kihlströma, 1986].

Strona 13
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
w kierunku pionowym istnieje oczywiście transport poziomy w obrębie jezior, rzek i mórz.
Jednakże to przenoszenie na duże odległości jest w wodzie znacznie wolniejsze niż w powietrzu.
Transport zanieczyszczeń w glebie zależy od ich właściwości, cząsteczek gleby oraz tzw. wody
kapilarnej. Substancje rozpuszczalne w wodzie są przenoszone szybko wraz z przemieszczającą
się wodą kapilarną. Z drugiej strony, związki rozpuszczalne w tłuszczach ulegają mniej lub
bardziej trwałej adsorpcji na organicznych cząsteczkach gleby. Tak więc transport tych sub−
stancji jest powolny w warstwie gleby bogatej w materię organiczną, taką jak pleśń, ale szyb−
szy w glebie piaszczystej o niskiej zawartości składników organicznych. Również w glebie gru−
boziarnistej transport jest szybszy niż w materiale silnie rozdrobnionym.
Procesy fizyczne zachodzące w atmosferze, wodzie i glebie wpływają na substancje toksyczne
w różny sposób. Na przykład światło ultrafioletowe może zmienić wiele typów cząsteczek
(fotoliza). W eksperymencie z pentachlorofenolem (
) po 7 dniach napromieniowania ultra−
fioletem pozostało tylko 12% początkowej ilości tego fungicydu. W podobnym eksperymencie
z DDT (
) pozostałości stanowiły 66%. Postępujące zakwaszenie gleby i wody wpływa na
rozpuszczalność metali, przez co np. zwiększa się poziom kadmu i aluminium w jeziorach i rze−
kach. Tak więc mieszanina zanieczyszczeń, z którą stykają się rośliny, zwierzęta i mikroorga−
nizmy ma skład inny od tej emitowanej ze źródeł. Ostateczną degradację pewnych związków
przeprowadzają mikroorganizmy, głównie bakterie. Jednak wiele zanieczyszczeń nie poddaje
się takiej degradacji i pozostaje w środowisku.
2.3. Ze środowiska do organizmów żywych
Związek, który nie może przeniknąć ze środowiska abiotycznego do roślin i zwierząt nie może
działać jako czynnik toksyczny. Pobieranie z otoczenia do żywego organizmu jest warunkiem
zarówno toksycznego działania jak i transportu biologicznego. Bardzo ważną właściwością sub−
stancji jest więc jej dostępność biologiczna
. Oczywiście dla oceny zagrożenia wielce użyteczna
byłaby możliwość przewidywania tej dostępności. Jako ogólną regułę można przyjąć, że do−
stępność związku dla organizmów żywych wzrasta wraz ze wzrostem rozpuszczalności w lipi−
dach. Tak więc w celu oceny tej właściwości wyznacza się rozpuszczalność danej substancji
w rozpuszczalniku dla tłuszczowców w porównaniu do rozpuszczalności w wodzie. Uzyskany
współczynnik nosi nazwę Kow, gdzie o oznacza oktanol – rozpuszczalnik lipidowy, a w – wodę.
Najczęściej jako miara używany jest logarytm Kow. Ogólnie mówiąc, log Kow większy od 3–4
(co oznacza, że substancja jest 1 000–10 000 razy bardziej rozpuszczalna w oktanolu niż w wo−
dzie) wskazuje na łatwą dostępność dla organizmów.
Najważniejsze drogi, którymi substancje toksyczne wnikają do roślin biegną przez korzenie
i przez liście. Korzenie są wyspecjalizowane w pobieraniu wody i jonów z wody znajdującej się
w glebie. Mogą zatem równie skutecznie pobierać zanieczyszczenia. Niektóre z nich są maga−
zynowane w korzeniach, inne mniej lub bardziej efektywnie transportowane są do łodygi i liści.
Nadziemne części rośliny są pokryte woskowatymi substancjami. W tej warstwie uwięzione
zostają zanieczyszczenia opadające z powietrza szczególnie te rozpuszczalne w tłuszczach.
Niektóre z nich przenikają następnie w głąb liści, inne pozostają w kutikuli. Z kolei gazy i pary
mogą przejść bezpośrednio przez szparki do liści z pominięciem warstwy woskowej.
Zwierzęta mogą pobierać zanieczyszczenia różnymi drogami, a więc przez żołądek i jelita, przez
płuca lub skrzela, przez skórę, a w pewnych wypadkach bezpośrednio do krwi. Zwierzęta
oddychające powietrzem „łapią” większość zanieczyszczeń środowiska wraz z pokarmem i wodą
tj. przez żołądek i jelito. Nie oznacza to jednakże, że mieszanina toksyn obecnych w pożywieniu
zostanie całkowicie zaabsorbowana w jelicie. Część tej mieszaniny może przejść nie wchłonięta
i opuścić ciało wraz z odchodami; część zostanie chemicznie rozłożona przez soki trawienne.
Zanieczyszczenia powietrza mogą być wchłaniane oczywiście przez płuca ale tylko wtedy, gdy
średnica cząstek nie przekracza kilku mikrometrów. Zatem u zwierząt lądowych dominuje po−
bieranie toksyn przez przewód pokarmowy.

Strona 14
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
U ludzi skóra jest wystawiona na bezpośrednie oddziaływanie środowiska i niektóre zanieczysz−
czenia rzeczywiście przez nią przenikają. Większość zwierząt ma jednak pokrycie ciała w postaci
futra, piór, łusek, itp. co oznacza, że zanieczyszczenia obecne w ich otoczeniu rzadko docierają
do warstwy komórek, gdzie zachodzi wchłanianie. Wyjątkiem są niektóre zwierzęta żyjące w wil−
gotnych środowiskach, takie jak żaby i dżdżownice, których skóra jest podobna do błony ślu−
zowej.
Zwierzęta wodne oddychające skrzelami, włącznie z wszystkimi rybami, znajdują się w odmien−
nej sytuacji. Skrzela są wyspecjalizowane w pobieraniu tlenu z wody oraz przenoszeniu jonów
i innych rozpuszczonych substancji między wnętrzem ciała a otoczeniem. Aby mogły efektywnie
pełnić tą rolę mają one często budowę blaszkowatą, co oznacza dużą powierzchnię kontaktu
z wodą. Zasadniczo więc zwierzęta skrzelodyszne większość zanieczyszczeń pobierają właśnie
tą drogą.
2.4. Losy zanieczyszczeń w organizmie –
akumulacja i biomagnifikacja
Większość niebezpiecznych zanieczyszczeń środowisko−
wych jest pod względem chemicznym bardzo trwała.
Ponadto większość z nich jest również słabo rozpu−
szczalna w wodzie i w konsekwencji trudna do wyda−
lenia z organizmu wraz z moczem, który jest roztworem
wodnym. W czasie trawienia posiłku zwierzęta rozkła−
dają pokarm, wykorzystując go następnie jako mater−
iał budulcowy lub jako źródło energii. Jednakże zanie−
czyszczenia trwałe nie mogą ulec degradacji. W rezul−
tacie ilość takich zanieczyszczeń w ciele nieco rośnie
wraz z każdym kęsem pokarmu a także wiekiem zwie−
rzęcia. Taki wzrost zanieczyszczeń wraz z wiekiem
(
) nosi nazwę akumulacji lub bioakumulacji.
W porównaniu z transportem z udziałem wiatrów i wo−
dy, transport biologiczny z jednego miejsca do drugiego
jest znikomy i ograniczony do zwierząt migrujących na
dalekie odległości, takich jak: migrujące ptaki, łososie,
węgorze, itp. Transport biologiczny ma jednak inne
właściwości. Gdy roślinożercy zjadają rośliny i trawy
kumulują trwałe toksyny z pożywienia. Ponieważ roślinożercy nie mogą rozłożyć zanieczyszczeń
w sposób efektywny, wędrują one w dalszej kolejności do ciała drapieżników, żywiących się
roślinożercami. W konsekwencji transportowane są od jednego gatunku do drugiego. Tak więc
transport biologiczny ma zupełnie inny wymiar aniżeli fizyczny.
Transport pomiędzy gatunkami oznacza także przeniesienie z jednego do drugiego poziomu
w sieci pokarmowej. Skutkiem tego jest wzrost stężenia czynników toksycznych w kolejnych
poziomach. Przypuśćmy, że zwierzę roślinożerne zjada w ciągu swego życia dziesięć razy wię−
cej pożywienia niż samo waży. Główna część tego pożywienia ulega rozłożeniu, a reszta jest
usuwana wraz z odchodami i moczem. Jednakże zanieczyszczenia z trudem ulegają rozkładowi
co oznacza, że niełatwo je wydalić. W rezultacie gromadzą się one w ciele zwierzęcia i tym
samym ich stężenia osiągają wartości około 10–krotnie wyższe niż w pokarmie. Na tej zasadzie
koncentracja tych związków wzrośnie jeszcze bardziej u zwierząt drapieżnych, itd. To zjawi−
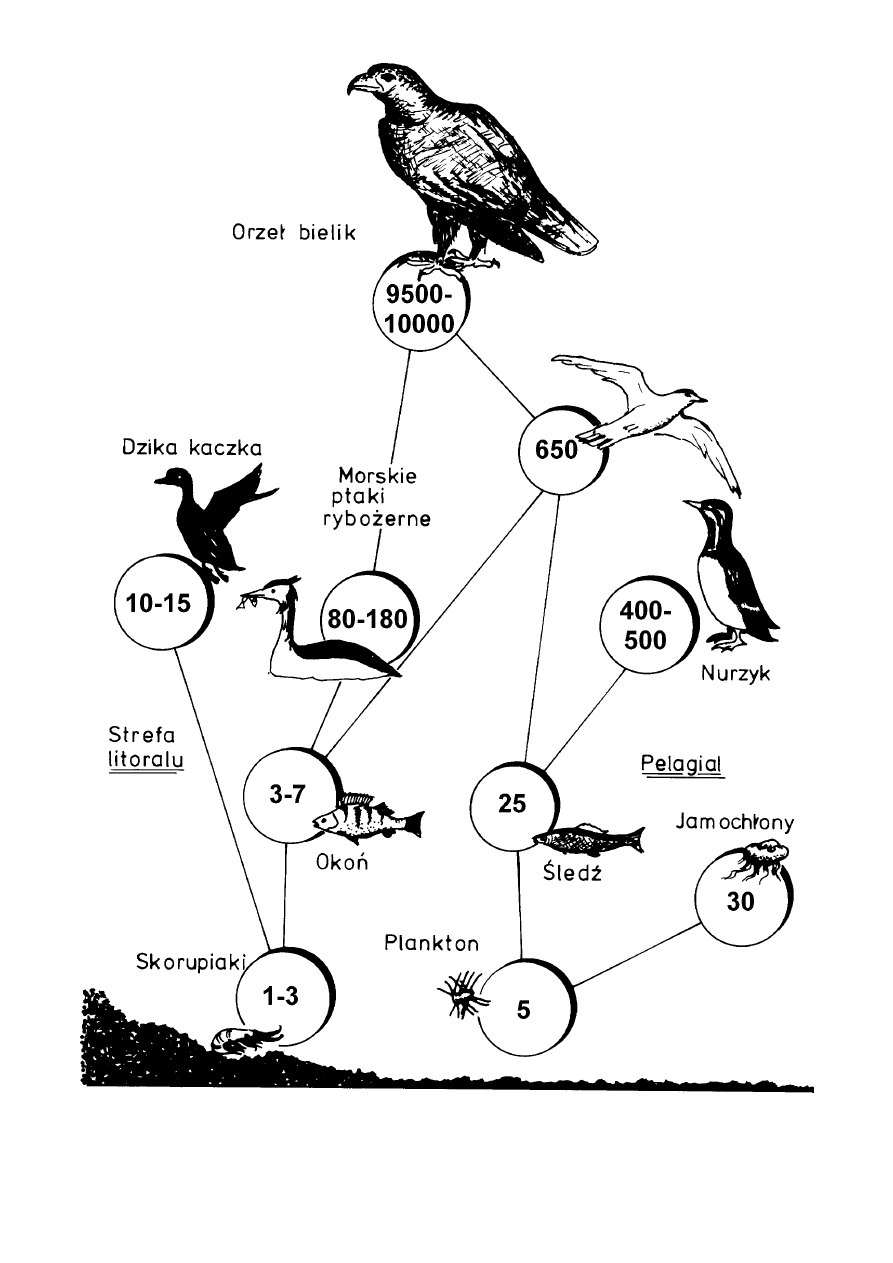
sko nosi nazwę biomagnifikacji. Jego przykład obserwowany w Bałtyku ilustruje
.
Można ogólnie stwierdzić, że w lądowej sieci pokarmowej następuje około 10–krotny wzrost
stężenia w obrębie każdego poziomu natomiast w wodnej około 3–5 krotny.
Ryc. 9.
Stężenie zanieczyszczeń rozpuszczal−
nych w tłuszczach u szczupaków w różnym
wieku, ilustrujące akumulację wraz
z upływem czasu [Johnels i in. 1967].
Strona 15
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
Ryc. 10.
Akumulacja toksycznych zanieczyszczeń z grupy PCB i ich biomagnifikacja w ekosystemie Bał−
tyku. Dla każdego gatunku w sieci pokarmowej podano stężenie PCB w mg/g tkanki tłuszczowej [z Olsson
i in., 1972].

Strona 16
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
2.5. Zatrucie wrodzone –
przepływ toksyn od matki do dziecka
Transport biologiczny oznacza także przeniesienie toksyn z jednej generacji do następnej, co
również odróżnia go od transportu fizycznego. U ssaków ten rodzaj transportu przebiega dwoma
różnymi drogami. Z zasady wydaje się nieprawdopodobne żeby zanieczyszczenia obecne
w środowisku mogły przenikać bezpośrednio do naczyń krwionośnych. Jednak tak właśnie
zdarza się w kilku szczególnych sytuacjach i w tych przypadkach efekty występują szybciej i są
wyraźniejsze niż wtedy, gdy toksyny są pobierane na innej drodze. U ciężarnej samicy ssaka
krew matki i płodu są od siebie oddzielone zaledwie kilkoma błonami. Dzięki temu płód ma
zagwarantowane dobre zaopatrzenie w tlen i substancje odżywcze. Jednak szereg zanieczysz−
czeń może przenikać z krwi matki do krwi płodu. W rezultacie, pod koniec ciąży często osiągają
one u niego stężenia podobne do tych jakie występują u matki.
Inną drogą przenoszenia substancji od matki do jej potomstwa jest ich pobieranie wraz z mle−
kiem. Mleko zawiera tłuszcz, np. mleko kobiece 3–4%, a mleko foki około 30%. Zanieczyszcze−
nia rozpuszczalne w tłuszczach łatwo opuszczają ciało matki wraz z tłuszczem mleka. Przynaj−
mniej u niektórych gatunków większe ilości zanieczyszczeń docierają do młodych osobników
w okresie karmienia mlekiem niż w czasie ciąży. Jednakże młode w tym okresie szybko rosną,
co oznacza rozcieńczenie substancji toksycznych obecnych w ich tkankach. Tym samym stężenia
zanieczyszczeń mogą się zmniejszać pomimo wzrastającej ich ilości
.
Podobna sytuacja występuje w jajach składanych przez ptaki, gady, ryby, itp. W jaju ptaka
rosnący zarodek stanowi zaledwie niewielką plamkę na powierzchni żółtka, reszta to materiał
zapasowy. Bardzo wcześnie w okresie wysiadywania naczynia krwionośne zarodka docierają
do żółtka. Ich rola polega na pobieraniu z niego składników odżywczych. Jednakże od początku
jajo jest częścią ciała matki i zawiera ten sam poziom zanieczyszczeń środowiskowych co inne
podobne tkanki. Zatem za pośrednictwem naczyń krwionośnych zarodek pobiera również zanie−
czyszczenia obecne w żółtku. W rezultacie tylko nieliczne młode osobniki, o ile takie są,
rozpoczną swe życie wolne od zanieczyszczeń środowiskowych.
Strona 17
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
3.
W
JAKI
SPOSÓB
ZANIECZYSZCZENIA
WPŁYWAJĄ
NA
ORGANIZMY
3.1. Dawki i efekty
Trzecie ogniwo w łańcuchu zanieczy−
szczeń symbolizuje skutki zanieczy−
szczeń. Nie jest jednak możliwe omó−
wienie setek rozmaitych efektów jakie
w eksperymentach laboratoryjnych wy−
wołują te substancje. Ponadto nie wszy−
stkie z nich mają istotne znaczenie w śro−
dowisku. W dalszej części ograniczymy
się zatem tylko do tych, które wiążą się
z konsekwencjami ekologicznymi, tj.
mają wpływ na przeżycie osobników, ga−
tunków i/lub całych ekosystemów. Na
wstępie konieczne będzie zapoznanie się
z niektórymi podstawowymi pojęciami
używanymi w ekotoksykologii.
Termin ekspozycja (ang. exposure –
przyp. tłum.) oznacza, że organizm jest
w kontakcie z czynnikiem toksycznym.
Charakterystyka ekspozycji oraz jej sku−
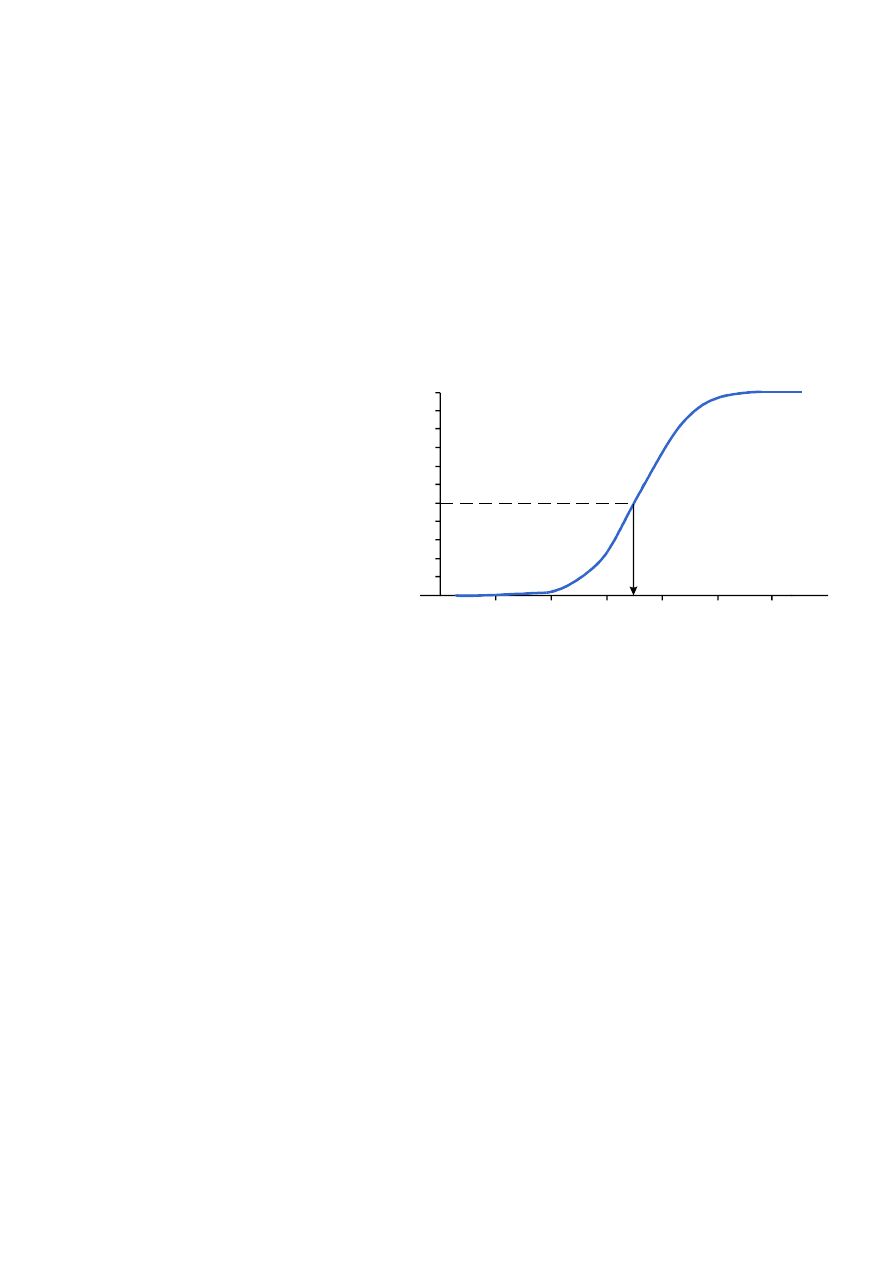
tki są związane zależnością określaną
jako zależność dawka–efekt (ang. dose–
effect relationship – przyp. tłum.) (
). Jej zrozumienie jest niezbędne dla uświadomienia
sobie efektów toksycznych. Skutki wywołane przez dany związek są często określane jako
toksyczność tego związku. Toksyczność ostra (ang. acute toxicity – przyp. tłum.) obejmuje efekty
występujące bardzo krótko po jednorazowej ekspozycji. Efekty te mogą być zróżnicowane
poczynając od zwykłego zaczerwienienia skóry na śmierci osobnika kończąc. W tym drugim
przypadku mówimy o efekcie letalnym. W przyrodzie przeważają jednak efekty wywołane
chronicznym {lub przewlekłym – przyp. tłum.} działaniem toksycznym. Toksyczność przewlekła
przejawia się efektami występującymi po dłuższym okresie ciągłego podawania niewielkich
dawek bez wystąpienia ostrych objawów.
Powszechnie przyjętym sposobem ilościowego wyrażania toksyczności ostrej jest podawanie wartości
LD
50
(dawki letalnej), która oznacza dawkę powodującą śmierć (czyli letalność) 50 procent zwie−
rząt spośród tych, które ją otrzymały.
LD
0
jest więc najwyższą dawką nie powodującą żadnej śmier−
telności. Warto zauważyć, że wysoka wartość
LD
50
oznacza niską toksyczność i vice–versa
to pojęcie jest uogólniane jako
ED
50
itp., gdzie ED oznacza dawkę efektywną, która może określać
dowolne objawy od podrażnienia skóry aż do śmierci zwierząt. W przypadku zwierząt wodnych
zamiast LD i ED często używa się pojęć
LC
i
EC
, co oznacza odpowiednio stężenie letalne i stężenie
efektywne substancji toksycznej w otaczającej wodzie.
100
50
0,030 0,040 0,050 0,060 0,070 0,080
ED 50
Procent upionych much
ml eteru etylowego na litr powietrza
Ryc. 11.
Krzywa zależności dawka–odpowiedź ukazująca
wpływ eteru na sen muszek owocowych. Oś pozioma – il−
ość eteru w naczyniu z muszkami. Oś pionowa – procent
uśpionych owadów. W stężeniach niższych niż 0,03 ml eteru
na litr powietrza żadna z much nie została uśpiona, przy
0,07 ml eteru na litr wszystkie zostały uśpione. Przy
stężeniu 0,055 ml efekt ten wystąpił u 50% much. Takie
stężenie nosi nazwę ED50 [dawka skuteczna w 50%].

Strona 18
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
Zasadniczo wszystkie związki toksyczne wywierają swoje pierwotne efekty biologiczne na
komórki i ich funkcje. Mogą to być np. zaburzenia w transporcie jonów przez błony komórkowe,
zmieniona aktywność enzymów, zmniejszone lub podwyższone wydzielanie hormonów, itp.
W zależności od typu zaatakowanych komórek, efekty obserwowane u poszczególnych osob−
ników zmieniają się w szerokich granicach.
Obecnie letalne skutki zanieczyszczeń w Morzu Bałtyckim są raczej rzadkie. Jednak na przeło−
mie lat 50. i 60. często znajdywano martwe zwierzęta, głównie ptaki. Aktualnie, z powodu niż−
szych stężeń toksyn, większość efektów stanowią zmiany subletalne, które często są bardzo
trudne do wykrycia. Nawet w takim przypadku gdy zmiany te w niewielkim stopniu wpływają
na osobniki ich skutkiem często są zaburzenia, które na dłuższą metę zmniejszają przeżywal−
ność.
3.2. Oddziaływanie na rośliny
Powszechnie znaną jest obserwacja, że niektóre rośliny doniczkowe źle rosną w sąsiedztwie
choinki. Najwidoczniej drzewko to wydziela jedną lub kilka substancji, które oddziaływują
negatywnie na inne gatunki. W rzeczywistości wiele roślin znajduje się pod wpływem szeregu
związków obecnych w atmosferze. W bardzo niskich stężeniach wiele z nich nawet pobudza
wzrost ale w wyższych spowalnia lub wręcz hamuje. To zjawisko, że niskie stężenia danej sub−
stancji wywierają pozytywne skutki, a wysokie – negatywne nie jest wcale rzadkie. Nosi ono
nazwę hormezy. Ujemnymi skutkami są np. opadanie liści, zmniejszona produkcja nasion, itp.
Jednakże wrażliwość roślin różni się w zależności od gatunku. Niektóre porosty są skrajnie
wrażliwe na dwutlenek siarki. Najprawdopodobniej ta wrażliwość wyjaśnia nieobecność po−
rostów nadrzewnych na najbardziej zanieczyszczonych terenach miast i obszarów przemysło−
wych. Porosty są również wrażliwe na fluor, który ulatnia się do atmosfery podczas produkcji
aluminum. Z tego względu zaledwie kilka gatunków tych organizmów możemy spotkać w są−
siedztwie huty aluminium. Niektóre paprocie i grzyby najwyraźniej także są wrażliwe na dwu−
tlenek siarki. Ogólnie rośliny zielne są bardziej wrażliwe na zanieczyszczenia powietrza niż
trawy, a szpilkowe są bardziej wrażliwe od drzew liściastych. Podaje się, że smog w rejonie
San Francisco oddziałuje na drzewa szpilkowe w promieniu 100 km i uniemożliwia uprawę
drzew cytrusowych w promieniu 50 km.
Już w starożytności roślinność wokół kopalni wykazywała różne zaburzenia, wskazując, że nie−
które metale są toksyczne dla roślin. Przy wysokich stężeniach następuje zahamowanie wzrostu
przypuszczalnie spowodowane gromadzeniem się metali w korzeniach, co z kolei wpływa na
pobieranie składników odżywczych. Objawem działania jeszcze wyższych stężeń są blade i biało
nakrapiane liście, co wskazuje na zmniejszoną syntezę chlorofilu. Rezultatem tego będzie oczy−
wiście zakłócenie procesu wytwarzania cukru i skrobi. Najprawdopodobniej najbardziej wrażli−
wymi stadiami życiowymi są kiełkujące nasiona i młode rośliny. Szczególnie silnie hamowany
jest wzrost młodych korzeni, nawet przy niskich dawkach metali.
Wiele gatunków drzew żyje w symbiozie z grzybami. Te mikoryzowe grzyby są często bardzo
wrażliwe na metale. Konsekwencje tego są dla zaatakowanych drzew zwykle bardzo poważne
.
Wiele porostów, grzybów i drobnoustrojów wykazuje dużą wrażliwość na metale. Szereg mikro−
organizmów glebowych pełni istotną rolę w rozkładzie substancji organicznych. Zatem wzrost
zawartości metali w glebie powoduje zwolnienie procesów rozkładu martwych szczątków roś−
lin i zwierząt.
Niektóre gatunki roślin już od dawna są używane jako wskaźniki (lub inaczej indykatory) tok−
sycznych efektów zanieczyszczeń lub ich obecności, co pozwala na wczesne wykrycie proble−
mu. Liczebność niektórych porostów i mchów jest wykorzystywana jako wskaźnik długotrwa−
łej emisji zanieczyszczeń do atmosfery, głównie dwutlenku siarki i metali ciężkich. W pewnych
przypadkach tkanki liścia używane są rejestrowania emisji fluorków z hut aluminium. W jesz−
cze innych rośliny hoduje się w kontrolowanych warunkach a następnie przenosi w teren i okre−
sowo poddaje analizie pod kątem silnych zanieczyszczeń (ang. acute air pollution – przyp. tłum.).

Strona 19
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
3.3. Zwierzęta: czynności nerwów i mięśni
U zwierząt nawet niewielkie zaburzenia funkcji mięśni mogą zmniejszyć szansę na przeżycie,
zwłaszcza w sytuacjach krytycznych. Osłabienie funkcji mięśni oznacza ich obniżoną wydolność
roboczą
. Z tego względu dorosłe ptaki z zaburzeniami w czynności mięśni mogą nie podołać
głównemu zadaniu rodzica, jakim jest zdobycie dostatecznej ilości pożywienia dla swoich piskląt.
W tym przypadku rodzice mają względnie duże szanse na przeżycie, jednak ich młode są za−
grożone. Dobrze znany jest fakt, że niektóre chemiczne zanieczyszczenia, np. organiczne związki
rtęci, DDT i kilka innych, mogą powodować zaburzenia w czynności mięśni. Zaburzenia tra−
wienia, metabolizmu lub zmniejszenie pobierania pokarmu również mogą zakłócić funkcje
mięśni przez obniżenie zasobów dostępnej energii. Zmiany takie obserwowano jako skutek obec−
ności rtęci, PCB i pięciochlorofenolu w pokarmie.
Do swej właściwej pracy mięśnie potrzebują prawidłowego impulsu nerwowego. Stwierdzono,
że wysoki poziom DDT i podobnych substancji działa tłumiąco na czynność nerwów, czego kon−
sekwencją może być zaburzona wydolność robocza mięśni.
Znalezienie pokarmu zimą wymaga od roślinożerców dużego wysiłku, który czasem trzeba wy−
konać w głębokiej śnieżnej pokrywie. Tym samym wiele czynników składa się na zwiększone
ryzyko śmiertelnego wygłodzenia jeleni i innych gatunków roślinożernych. Niektóre ptaki omi−
jają ten problem wędrując na południe. Jednakże migracja także wiąże się z olbrzymią pracą
mięśni. Ich zmniejszona wydolność może uniemożliwić ptakom osiągnięcie celu i tym samym
zagrozi ich przetrwaniu. Wędrówki ptaków oznaczają również konieczność skomplikowanej
nawigacji na dużych odległościach. Do jej sprawnego przeprowadzenia niezbędna jest doskonała
współpraca pomiędzy narządami zmysłów, nerwami i mięśniami. Nieprawidłowe funkcjono−
wanie tego systemu może pociągnąć za sobą różne konsekwencje jak np. niemożność znalezienia
miejsca lęgowego i zagrożenie przeżywalności jako że, najprawdopodobniej, do rozrodu w ogóle
nie dojdzie.
Można zapytać czy takie efekty są wyłącznie spekulacjami czy też istnieją niezbite fakty świad−
czące, że mają one miejsce w przyrodzie? Ptaki przygotowują się do wędrówki przez groma−
dzenie zapasów tłuszczu, który następnie jest wykorzystywany jako źródło energii podczas lotu.
Tłuszcz ten zawiera szereg zanieczyszczeń, które się w nim rozpuszczają. Eksperymenty wy−
kazały, że równocześnie z zużywaniem tłuszczu uwalniane są zawarte w nim toksyny, które
następnie gromadzą się w mięśniach i w układzie nerwowym. Tam mogą zaburzać zarówno
funkcje nerwowe, mięśniowe jak i sensoryczne. Przynajmniej u jednego gatunku stwierdzono,
że ptaki którym podawano PCB rozpoczynały lot w ciągu całego dnia, natomiast osobniki kon−
trolne tylko rano, co wskazuje na zaburzenie czynności nerwowych i czuciowych.
Za pomocą specjalnego sprzętu można mierzyć podobne zmiany u ryb. Główną częścią tego urzą−
dzenia jest długa, pozioma i przezroczysta rura, którą obraca się wokół długiej osi. Za pomocą
specjalnej techniki wodę przepływającą przez tę rurę także wprawia się w ruch wirowy. Ryba
umieszczona w tej rurze próbuje utrzymać normalną pionową pozycję pomimo obracającej się
wokół niej wody. Zwiększając szybkość obrotu można osiągnąć taką, przy której ryba nie jest
dłużej w stanie skorygować swej pozycji. Okazuje się, że ta szybkość krytyczna jest ujemnie
skorelowana z poziomem DDT, PCB i rtęci w tkankach ryby, to znaczy, że wysoka zawartość
tych zanieczyszczeń zmniejsza zdolność ryby do radzenia sobie w warunkach stworzonych przez
wirującą wodę. Może to być spowodowane zaburzoną funkcją narządów zmysłów rejestrujących
położenie ciała, zmniejszoną wydolnością roboczą mięśni, oraz (lub też) nieprawidłowym prze−
kazem sygnałów nerwowych pomiędzy narządami zmysłów a mięśniami (czyli zaburzeniami
funkcjonowania układu nerwowego – przyp. tłum.).

Strona 20
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
3.4. Układ odpornościowy i organogeneza
Wiadomo, że wiele spośród chlorowanych
zanieczyszczeń organicznych np. dioksy−
ny, niektóre związki z grupy PCB, być mo−
że również DDT obniżają sprawność ukła−
du odpornościowego. W istocie jednym
z pierwszych zaobserwowanych skutków
działania PCB była zmniejszona odpor−
ność u ptaków zaatakowanych przez wi−
rusa. Na skutek takiej obniżonej odporno−
ści nawet stosunkowo błahe infekcje stają
się śmiertelne. Groźna sytuacja populacji
fok w Bałtyku może częściowo wynikać
z osłabionej bariery odpornościowej.
Wskazuje na to np. duża ilość wolno goją−
cych się ran na skórze i w jelitach, prze−
rośnięte nadnercza itp. Podczas przepro−
wadzania pośmiertnych badań zaobserwowano takie zmiany u ponad połowy osobników.
Oczywiście taka sytuacja oznacza, że stan zdrowia populacji fok bałtyckich jest bardzo zły.
Stwierdzono, że chlorowane związki organiczne powodują deformacje twardych tkanek takich
jak szkielet i płetwy. Wymienione związki są uwalniane np. z papierni jako produkt uboczny
w procesie bielenia masy papierniczej. W pobliżu takich zakładów często spotyka się deformacje
szczęk u szczupaków. Nietrudno sobie uświadomić, że takie osobniki mają trudności w zdobyciu
dostatecznej ilości pożywienia. Na tych samych obszarach niektóre okonie pozbawione są czę−
ści płetw. Płetwy używane są głównie do wykonywania drobnych ruchów, co wymaga dużej
precyzji. W rezultacie wykonywanie takich czynności jak łapanie ofiary lub składanie mleczu
w miejscu złożenia ikry podczas kopulacji może być znacznie utrudnione. Eksperymenty wy−
kazały, że rozcieńczone ścieki z papierni mogą powodować skrzywienia kręgosłupa u dorsza
i kura rogacza
). To zniekształcenie oznacza, że połączenia pomiędzy kręgosłupem
a dużymi mięśniami ogona są nieprawidłowe, co może pociągać za sobą zaburzenia ruchów.
3.5. Fizjologia rozrodu
jest bardzo wrażliwa na zanieczyszczenia
Rozmnażanie i wzrost okazują się niestety procesami wyjątkowo wrażliwymi na działanie sub−
stancji toksycznych. W wielu przypadkach zaburzenia tych procesów występują już w stęże−
niach zbyt niskich dla wywołania innych objawów. Mimo licznych badań przyczyny tego stanu
rzeczy są nadal nieznane. Jedną z nich może być zmiana, pod wpływem zanieczyszczeń, stężenia
hormonów regulujących czynności rozrodcze. W obecności wielu obcych substancji wątroba pra−
cuje intensywnie w celu zniszczenia chemicznego intruza. Okazuje się jednak, że te same lub
podobne enzymy aktywne są w procesach degradacji zarówno zanieczyszczeń jak i hormonów
płciowych
. Zatem zwiększony poziom zanieczyszczeń może pociągać za sobą obniżenie stężenia
tych hormonów.
Niektóre skutki powodowane przez zanieczyszczenia środowiskowe mogą być rezultatem zmian
w poziomie hormonów. Na przykład pomyślne zagnieżdżenie zapłodnionego jaja w błonie ślu−
zowej macicy musi być poprzedzone procesem jej przygotowania, który zachodzi pod wpływem
hormonów płciowych. Jeśli zwierzę ma zbyt niski poziom hormonów indukujących omawiane
procesy może nie dojść do implantacji. Takie nieudane zagnieżdżenia zaobserwowano w eks−
perymentach laboratoryjnych u myszy, którym podawano PCB i DDT. Zaburzenia w przebiegu
cyklu miesiączkowego u kobiet i samic małp narażonych na działanie PCB również można wy−
jaśnić zmienionymi poziomami hormonów. Oczywiście zwierzę jest w stanie, w przeciągu
Ryc. 12.
Uszkodzenia kręgów u dorsza
[udostępnił Jan Thulin].

Strona 21
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
zaledwie kilku dni, skompensować obniżenie poziomu hormonów, wywołane pojedynczą dawką
PCB. Ponieważ jednak w środowisku powszechne jest raczej ciągłe narażenie na niskie dawki
zanieczyszczeń należy sądzić, że muszą istnieć również inne przyczyny zaburzeń w czynnościach
rozrodczych.
Można odtworzyć rzeczywistą sytuację w laboratorium przez podawanie zwierzętom doświad−
czalnym niskich dawek w sposób ciągły przez określony czas, np. podczas całego okresu ciąży.
Przeprowadzone eksperymenty wykazały, że w takich warunkach niektóre z zagnieżdżonych
płodów umierały jeszcze w obrębie macicy. Oczywiście poszczególne gatunki różnią się stopniem
wrażliwości. Bardzo wrażliwym gatunkiem jest norka, używana jako zwierzę doświadczalne,
jak się zdaje również i wydra. Niewiele jednak wiadomo o przyczynach tego zjawiska. Stężenia
związków chemicznych w tkankach płodów nie są śmiertelne, ani też transport substancji od−
żywczych przez łożysko nie jest znacząco upośledzony.
Wykazano, że u niektórych gatunków ptaków i ryb stężenie zanieczyszczeń środowiskowych
w jajach jest dostatecznie wysokie aby spowodować śmierć zarodków. Stwierdzono to np. u ry−
bołowów (PCB i DDT) i łososia atlantyckiego (DDT).
Wzrost zarodków i młodych także zależy od wpływu rozmaitych zanieczyszczeń. Szczenięta
norek, które otrzymywały w czasie ciąży PCB miały niższą masę urodzeniową niż szczenięta
niezatruwanych matek. Z kolei u gryzoni takich jak szczury, myszy i świnki morskie, uzyskano
odmienne rezultaty. Co najmniej w kilku eksperymentach młode tych gatunków rosły szybciej,
gdy otrzymywały wraz z mlekiem DDT lub PCB.
3.6. Populacja fok w Bałtyku jest zagrożona
W warunkach krytycznych zmniejszone możliwości rozrodu mogą wyeliminować całe populacje
danego gatunku. Foki, żyjące w Bałtyku omal nie wyginęły z powodu poważnych zaburzeń roz−
rodu, najprawdopodobniej wywołanych przez PCB. W Bałtyku żyją trzy gatunki fok: foka szara
(Halichaerus grypus), foka obrączkowana, inaczej nerpa, (Pusa hispida) i foka pospolita (Phoca vitu-
lina). Przynajmniej do pierwszej wojny światowej wszystkie trzy gatunki występowały w ży−
wotnych populacjach. W tym czasie najprawdopodobniej żyło sto tysięcy fok szarych, dzisiaj
zostało jakieś 1500. Bardzo kiepsko rozmnaża się również nerpa, której liczebność w północnych
częściach Bałtyku wynosi aktualnie około 6000 osobników. Wydaje się, że tylko około 30% samic
jest płodnych. W ich tkankach stężenia PCB są niższe niż u pozostałych samic.
Pośmiertne badania zmian patologicznych u martwych samic fok bałtyckich ujawniły występo−
wanie nieznanego typu uszkodzeń macicy. Około połowa z przebadanych zwierząt miała zro−
śnięty przynajmniej jeden róg macicy
. Obecnie takie uszkodzenia występują u ponad 60%
samic nerpy. Zrośnięcie macicy uniemożliwia połączenie się plemnika i komórki jajowej, w wy−
niku czego zwierzę staje się bezpłodne. Co więcej, stwierdzono wysoką częstość występowania
raka macicy. U niektórych zwierząt pojawiają się uszkodzenia skóry przypominające ropnie
lub trądzik chlorowy występujące u ludzi zatrutych PCB i związkami pokrewnymi; ich pazury
często są zdeformowane a w jelicie obserwuje się uszkodzenia na tle zapalnym. Ponadto poja−
wiają się patologiczne zmiany w nerkach i nadnerczach, czasami także w szkielecie.
Warunki panujące w Morzu Bałtyckim bardzo się zmieniły w ostatnich kilku dekadach. Oprócz
odpadów zawierających chlorowane związki organiczne wzrosło stężenie metali ciężkich i in−
nych zanieczyszczeń. Jest zatem niemożliwe jednoznaczne określenie przyczyny lub przyczyn
wszystkich tych zaburzeń i dysfunkcji. Aby odpowiedzieć na to pytanie przeprowadzono eks−
perymenty, używając norki amerykańskiej (Mustela vison) jako gatunku modelowego. Norka,
podobnie jak foki, żywi się rybami i ma taki sam przebieg wczesnej ciąży z opóźnionym za−
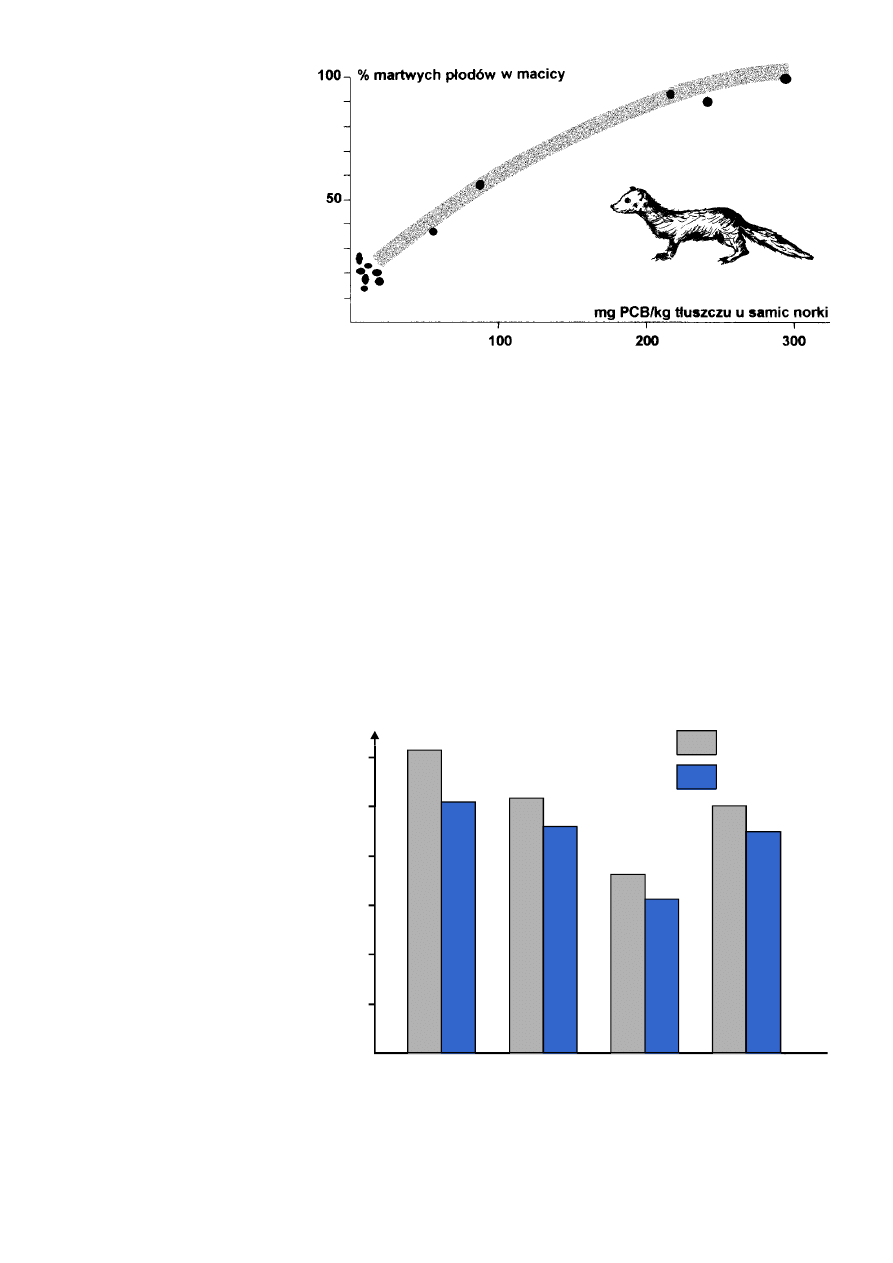
gnieżdżeniem się zapłodnionych jaj. Wyniki pokazują wyraźną zależność pomiędzy ilością mar−
twych płodów w macicy a poziomem PCB w tkance tłuszczowej matki (
). Dokładniejsze
eksperymenty wykazały, że najniższe stężenia PCB wywołujące opisaną zmianę (porównaj
) wynoszą w przybliżeniu 10 mg technicznie czystej substancji na kilogram tłuszczu matki.
Jak dotąd eksperymenty potwierdzają pogląd, że PCB są główną przyczyną obniżonej płodności
Strona 22
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
fok bałtyckich. Jednakże ani
u norek ani u innych gatun−
ków nie stwierdzono zrostów
w macicy tak jak u fok. W isto−
cie technicznie czysty PCB jest
mieszaniną 60–70 różnych po−
krewnych związków, różnią−
cych się nieco właściwościami.
W celu ustalenia względnego
zagrożenia każdego z nich mie−
szaninę tę rozdzielono na kil−
kanaście grup obejmujących
ściśle spokrewnione związki,
po czym badano efekty każdej
z nich. Żadna z tych grup po−
dawana osobno nie wywierała
wpływu na norki, nawet jeśli
w danej grupie były tak toksyczne składniki jak dwubenzofurany (zob.
), które są za−
nieczyszczeniami technicznych preparatów PCB. Jednakże, gdy podawano je razem lub łączono
dwie grupy, wyniki były takie same jak przy działaniu czystego technicznie PCB.
3.7. Wrażliwym stadium u ptaków jest jajo
W 1967 zaobserwowano, że skorupki jaj niektórych gatunków ptaków są cieńsze niż w latach
poprzednich (
). Zmniejszenie grubości, u wszystkich przebadanych gatunków
przekraczało 10%. Może się wydawać nieistotne czy grubość skorupki wynosi 0,5 czy 0,35 mm.
Jednak taka zmiana oznacza, że jest ona bardziej krucha i zwiększa się ryzyko, że jaja ulegną
zniszczeniu zanim wylęgną się z nich pisklęta. Wysunięto przypuszczenie, że przyczyną tego
jest DDT. Ponieważ skorupki jaj zbieranych we wcześniejszych latach są przechowywane
w muzeach przyrodniczych można było dokonać pomiarów porównawczych ich grubości na
przestrzeni lat. Pierwsze obja−
wy ścienienia zaobserwowano
w 1947 kiedy to wprowadzono
DDT. Skorupki ptasich jaj zbu−
dowane są z węglanu wapnia,
a ich wytwarzanie przebiega
pod kontrolą hormonów płcio−
wych samicy. Przypuszczano
zatem, że to obniżony poziom
hormonów u ptaków zatru−
wanych DDT jest powodem
zmniejszonej grubości sko−
rupki. Okazało się jednak, że
problem jest bardziej skompli−
kowany. Bezpośrednią przy−
czyną wydaje się być niedo−
stateczna absorpcja wapnia
z krwi przez gruczoł wytwa−
rzający skorupkę, oraz jego
wydzielanie do jaja. Proces ten
regulowany jest przez kilka
hormonów, nie tylko hormony
Ryc. 13.
Śmiertelność płodowa u norki (w % martwych płodów) wy−
wołana przez PCB podane ciężarnym samicom [Jensen i in., 1977].
0,6
0,5
0,1
0,2
0,3
0,4
-17%
-11%
-14%
-13%
przed 1947 r.
po 1947 r.
Orze³ bielik
Jastrz¹b
B³otniak
stawowy
Alka
krzywonosa
Gr
ub
oæ
sk
or
up
ki
ja
ja
(m
m
)
Ryc. 14.
Zmniejszenie grubości skorupek u niektórych gatun−
ków ptaków w zależności od poziomu DDT w środowisku, wy−
rażone grubością skorupki przed i po roku 1947, kiedy to DDT
został wprowadzony jako biocyd [Johnels i Odsjö, 1972].

Strona 23
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
płciowe. Wykazano również, że to nie DDT lecz jeden z produktów jego degradacji zwany DDE
(patrz
) odpowiada za ścienienie skorupek. Różne gatunki wykazują oczywiście odmienną
wrażliwość na ten związek. Sokół wędrowny jest wyjątkowo wrażliwy, natomiast kura domowa
jest praktycznie niewrażliwa.
Stosunkowo niedawno zaobserwowano odmienny typ ścienienia skorupek ptasich jaj. Wraz
z zakwaszeniem gleby i wody rośnie rozpuszczalność wielu metali, m.in. aluminium. Wysokie
dawki tego metalu wpływają na wytwarzanie zmineralizowanych tkanek takich jak skorupki
jaj, muszle ślimaków i szkielety kręgowców. Badając muchołówkę żałobną, żywiącą się wodnymi
owadami zamieszkującymi zakwaszone wody jeziora, stwierdzono, że istnieje wyraźny związek
pomiędzy stężeniem aluminium w ciele samic a grubością skorupek w składanych przez nie
jajach. Co więcej, skorupki nie tylko były cieńsze ale także bardziej porowate niż w jajach nie−
uszkodzonych
. Porowata skorupka umożliwia zwiększone parowanie wody z jaja, skutkiem
czego zarodki giną zarówno z odwodnienia jak i pękania skorupek.
3.8. Ryby w jeziorach są zagrożone przez metale ciężkie
Zwiększony poziom metali w wodzie prowadzi także do innych poważnych konsekwencji.
W wielu jeziorach regionu bałtyckiego, zwłaszcza w oligotroficznych zbiornikach na obszarach
leśnych, zakwaszenie wody doprowadziło do wzrostu zawartości rtęci w rybach czyniąc je nie−
przydatnymi do celów konsumpcyjnych. Innym skutkiem zwiększonego poziomu metali ciężkich
w jeziorach i rzekach są uszkodzenia skrzel u ryb. Przy wysokich stężeniach aluminium złożone
związki metali osiadają na ich powierzchni co utrudnia pobieranie tlenu z otaczającej wody.
Ponadto aluminium, podobnie jak kadm, tytan i miedź, mogą być pobierane przez komórki
skrzeli. Na silnie zanieczyszczonych obszarach Morza Bałtyckiego kadm spowodował uszko−
dzenia kręgów u ryb.
W celu prawidłowego oszacowania jakie zagrożenia niesie ze sobą zanieczyszczenie metalami
ciężkimi, bardzo ważna jest znajomość dostępności biologicznej różnych związków tych metali.
Co najmniej kilkanaście metali ciężkich jest łatwiej dostępnych w postaci związków organicz−
nych, np. dwumetylortęci czy czteroetylenku ołowiu niż jako jony nieorganiczne. Tym samym
u wielu gatunków ryb pobieranie nieorganicznych soli metali jest ograniczone.

Strona 24
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
4.
O
DDZIAŁYWANIE
NA
EKOSYSTEMY
4.1. Zanieczyszczenia wywołują
efekty łańcuchowe w ekosystemach
Zanieczyszczenia mogą powodować rozległe i nieoczekiwane skutki w całych ekosystemach.
Częściowo wymyślony przykład może posłużyć do zilustrowania tych procesów. Myszołów jest
ptakiem żywiącym się głównie małymi gryzoniami. Przypuśćmy, że na obszarze gdzie żyje sporo
myszołowów ktoś rozsypał rodentycyd, który z definicji jest najbardziej szkodliwy dla gryzoni
,
a względnie nieszkodliwy dla innych gatunków. W krótkim czasie liczba gryzoni gwałtownie
spadnie. Zmusi to myszołowy do uzupełniania diety wężami, żabami, dżdżownicami, ślimakami
itp. wskutek czego ich liczebność także się zmniejszy. W tej sytuacji nasuwa się wniosek, że
także węże, żaby itd. zostały zatrute a nie tylko gryzonie. Ponadto istnieją gatunki, które kon−
kurują z małymi gryzoniami o niektóre zasoby środowiska. Niektóre trzmiele i osy często pre−
ferują porzucone nory nornic jako miejsce do budowy gniazda. Redukcja liczebności gryzoni
będzie więc dla nich czynnikiem sprzyjającym i ich liczba najpewniej szybko wzrośnie. Nie mając
pełnego rozeznania można w takiej sytuacji wyciągnąć fałszywy wniosek, że zaprzestano stoso−
wania insektycydu na tym obszarze, podczas gdy w istocie zastosowano inny pestycyd – środek
gryzoniobójczy.
Zgromadzono wiele obserwacji w jaki sposób zanieczyszczenia środowiskowe pośrednio zmieniły
warunki życia jakiegoś gatunku, pomimo braku bezpośredniego oddziaływania czynnika to−
ksycznego. Brak niestety dobrze udokumentowanych przypadków tego typu z regionu Bałty−
ku, kilkanaście znanych jest z obszaru USA i dwa z nich zostaną krótko omówione. W celu zwal−
czenia komara malarycznego powierzchnie jezior, w których żyły larwy tych owadów, spryskano
DDT. Oprócz komarów, w większości jezior wytępiono tym sposobem także skorupiaki. Szopy
pracze, żywiące się głównie skorupiakami także zostały wyeliminowane, mimo że były prak−
tycznie niewrażliwe na bezpośredni wpływ tego pestycydu. Szereg obserwacji ilustruje mody−
fikujący wpływ konkurencji międzygatunkowej na spodziewane efekty substancji chemicznych.
Dominującym szkodnikiem na dużych plantacjach kapusty w USA był owad. Na tych samych
polach występował także roztocz – również szkodnik ale o niewielkim znaczeniu. Wprowadzając
DDT farmerzy mieli nadzieję na pozbycie się owada, jako że środek ten okazał się bardzo sku−
teczny właśnie przeciw owadom. Z kolei roztocza nie są nań szczególnie wrażliwe. Po spryskaniu
pól DDT owady wyginęły tak jak przypuszczano. Plony jednak nie wzrosły, gdyż pozbawiony
konkurenta roztocz stał się szkodnikiem równie groźnym jak ten pierwszy.
4.2. Pomiary liczebności
Łatwo przyjąć, że zmniejszona liczba urodzonych młodych osobników, wywołana obecnością związ−
ków zakłócających czynności rozrodcze musi oznaczać zmniejszoną liczbę dorosłych w kolejnym
pokoleniu. Niekoniecznie jednak musi tak być, co ilustrują poniższe dwa przykłady. Przypuśćmy,
że w małym jeziorze zawierającym dostateczną ilość pożywienia urodziło się 1 000 sztuk narybku.
Załóżmy dalej, że 900 spośród nich zostanie zjedzonych przez drapieżniki i jedynie 100 osobników
przeżyje. Jeśli rozrodczość dorosłych ryb obniży się o 10% to urodzi się tylko 900 rybek. Przy nie
zmienionej liczbie drapieżców wszystkie ofiary zostaną złapane i żadna nie pozostanie przy życiu.

Strona 25
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
W tym teoretycznym przykładzie zmniejszenie zdolności rozrodczej o 10% wystarczyło do wyeli−
minowania całego pokolenia. W drugim przykładzie ponownie załóżmy, że urodziło się 1 000
rybek. Przypuśćmy dalej, że tym razem nie ma drapieżców a ilość pożywienia pozwoli przeżyć
zaledwie 100 osobnikom. Załóżmy także, że rozrodczość dorosłych obniży się aż o 90%. Zatem
urodzi się tylko 100 rybek i wszystkie przeżyją ze względu na dostateczną ilość pożywienia
oraz brak drapieżników. Podane przykłady są oczywiście skrajne i raczej nie mają miejsca w rze−
czywistym świecie. Wskazują jednakże na fakt, że w ekosystemie ostateczne zmiany w roz−
rodczości populacji są wypadkową współdziałania bardzo wielu czynników.
4.3. Przykład – ekosystem zmieniony przez zakwaszenie
Zakwaszenie jest wynikiem rozprzestrzeniania się dwutlenku siarki i tlenków azotu na dużych
obszarach. Aktualne zakwaszenie wód śródlądowych spowodowało zubożenie fauny i flory w do−
tkniętych nim jeziorach. Pierwsze objawy pojawiają się gdy pH obniży się do 5,5 – zanikają
skorupiaki i obniża się rozrodczość łososia i płoci, które są najbardziej wrażliwymi gatunkami
ryb. Przy pH w granicach 5,5–5,0 giną ślimaki i niektóre gatunki planktoniczne, a aktywność
bakterii obniża się. Poniżej dolnej wartości tego przedziału spada rozrodczość golca, szczupaka
i okonia, a dno zbiornika porasta niemal wyłącznie mech torfowiec. W jeszcze niższym pH (po−
niżej 4) maleje liczebność niektórych roślin naczyniowych, zagrożone są także dorosłe ryby,
gdyż ich nerki nie są w stanie prawidłowo funkcjonować w tak niskim pH. Poniżej tej wartości
ryby giną, poczynając od łososia i gatunków pokrewnych, które są najbardziej wrażliwe.
Zmniejszona rozrodczość wynika głównie z zaburzonego rozwoju zarodkowego. Przy pH<5,0
jaja nie mogą utrzymać fizjologicznego stężenia jonów wodorowych, a w zakwaszonym środowi−
sku wewnętrznym wzrost zarodków przebiega nieprawidłowo. Nawet przy nieco wyższym pH
jaja nie pęcznieją wystarczająco. W konsekwencji, w obrębie jaja jest zbyt mała przestrzeń aby
narybek rósł prawidłowo, skutkiem czego zagina się, co prowadzi ostatecznie do różnych jego
zniekształceń. Dodatkową przyczyną obniżonej zdolności reprodukcyjnej jest zmniejszona ilość
larw opuszczających jaja. Powodem tego jest zaburzenie funkcji enzymów, odpowiedzialnych
za rozerwanie osłon jajowych podczas wylęgu, wywołane zakwaszeniem środowiska.
Jak już wspomniano zakwaszenie zwiększa stężenie metali, zwłaszcza metali ciężkich, w wodzie
a tym samym również w organizmach. Tym samym dotknięte zostają nie tylko organizmy wodne
ale również te, które w wodzie szukają pożywienia. Skutki zakwaszenia jeziora będą się więc
rozprzestrzeniały także na sąsiednie ekosystemy. W małym jeziorze Tjulträsk, położonym
w szwedzkich górach, stwierdzono wysokie stężenia aluminium. Przy brzegach żyje mnóstwo
muchołówek. Niektóre, gnieżdżące się blisko brzegu, żywią się wodnymi owadami i składają
jaja otoczone bardzo cienką skorupką lub w ogóle jej pozbawione. Analizy wykazały, że ich szpik
kostny zawiera wysokie stężenia aluminium. Z kolei ptaki, gnieżdżące się w pewnej odległości
od brzegu i żywiące się głównie owadami lądowymi, składają normalne jaja. Widać więc jak
aluminium obecne w wodzie rozprzestrzenia się na sąsiadujące tereny ekosystemów lądowych.
4.4. Zmiany w sąsiedztwie zakładów metalurgicznych
Skutki działania zanieczyszczenia w ekosystemie, np. jonów wodorowych, jak w podanym wyżej
przykładzie, można podsumować jako spadek liczby gatunków, czyli zmniejszenie różnorodności,
oraz zmniejszenie biomasy. Przedstawia to również
, prezentujący rezultaty badań orga−
nizmów glebowych wokół huty miedzi w Walii. Z diagramu po prawej stronie wynika, że licz−
ba gatunków maleje wraz ze wzrostem stężenia miedzi w glebie, co oznacza malejącą różno−
rodność. Diagram po lewej przedstawia różne pośrednie i bezpośrednie pomiary biomasy jako
funkcje stężenia miedzi w glebie. Większość zmiennych obniża się liniowo wraz ze wzrostem
stężenia metalu.
Otoczenie huty w Rönnskär położonej na wybrzeżu w Zatoce Botnickiej (Szwecja) jest silnie
zanieczyszczone ołowiem, miedzią, cynkiem, arsenem i kadmem. Las rosnący w pobliżu huty

Strona 26
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
przestał istnieć, muchołówki nie mogą się rozmnażać, wśród ryb częste są przypadki deformacji
kręgosłupa itp. Podobna sytuacja z pewnością występuje na wielu innych silnie uprzemysło−
wionych terenach w regionie Bałtyku.
Ryc. 15.
Wpływ obecności miedzi na ekosystem gleby. Po lewej: całkowita biomasa grzybów, aktywność
enzymu fosfatazy i zależna od grzybów mineralizacja maleje wraz ze wzrostem stężenia miedzi. Po prawej:
liczba gatunków (bioróżnorodność) także się zmniejsza ze wzrostem poziomu metalu [Oparte na danych F.
Moriarty].
2
4
6
10
15
0
20
50 100 200
500 1000 2000
5000 10000 20000
0
2
1
0,5
1,0
1,5 3
mied [µg·g gleby]
-1
Te
mp
o r
ozk
³a
du
[m
g·
g
·d
]
-1
-1
Ca
³k
owit
a b
iom
asa
gr
zy
bó
w [
km·g
]
-1
Te
mp
o m
in
era
liz
ac
ji
az
ot
u [
m
m
ol·
l]
-1
Ak
ty
wno
æ f
os
fat
az
y
Rozk³ad
Mineralizacja
azotu
Aktywnoæ
fosfatazy
Biomasa
grzybów
20
50 100 200
0
500 1000 2000 5000 10000 20000
mied
[µg·g gleby]
-1
40
30
20
10
Liczba taksonów
Pozosta³e grzyby
G
rzy
by
o
wo
cn
iko
we
Msz
aki
Ro
lin
y
nac
zyniowe
Por
osty n
a sonie
Sk¹po
szczety
Por
osty z r
odzaj
u
Cladon
ia
(Chrobotek)
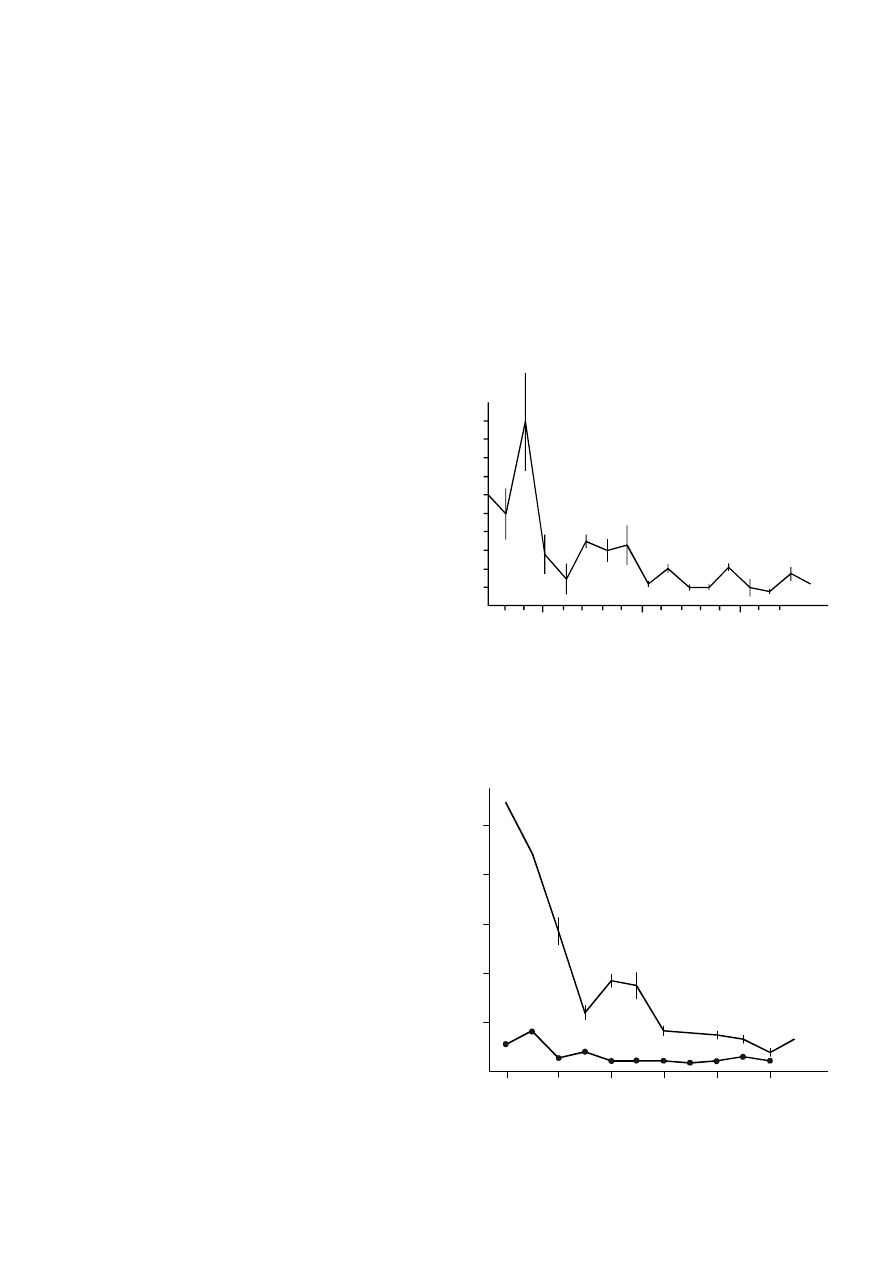
Strona 27
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
5.
P
RZYSZŁOŚĆ
–
C
ZY
PODJĘTE
DZIAŁANIA
SĄ
SKUTECZNE
?
5.1. Pierwsze akcje – zakaz stosowania rtęci i DDT
Na początku lat 60. szkodliwe skutki chemicz−
nych zanieczyszczeń zaczęły być oczywiste dla
wielu ludzi. Słynna książka Rachel Carson –
„Milcząca wosna”, opublikowana w 1962 ro−
ku rozpoczęła bardziej ogólną debatę na temat
problemów środowiska oraz stała się istotną za−
chętą do podjęcia konkretnych działań dla wielu
zatroskanych aktualnym stanem rzeczy ludzi.
Znacznie wcześniej jednak sami naukowcy
ostrzegali przed skutkami działania różnych
związków wprowadzonych do środowiska. Naj−
wcześniejsze prace ukazujące poważne skutki
wywołane przez DDT pojawiły się już około
1950 r., a na przełomie lat 50. i 60. wykazano
szkodliwość pestycydów zawierających rtęć. Stąd
też pomiędzy 1965 a 1972 r. wiele krajów wpro−
wadziło zakaz stosowania większości tych
związków.
Można zapytać co się działo w regionie Bałtyku
w okresie mniej więcej 20 lat, które upłynęły od
tamtego czasu. W 1966 w Szwecji zakazano sto−
sowania organicznych związków rtęci jako zapra−
wy do nasion. Spowodowało to obniżenie stężenia
rtęci u wielu organizmów, co zilustrowano na
przykładzie szpaków (
). Oczywiście
proces ten zachodził stopniowo. Najprawdopo−
dobniej powodem tego był stosunkowo długi
okres życia szpaków, który wynosi kilkanaście
lat. Gwałtowne zmniejszenie poziomu rtęci mo−
gło nastąpić dopiero po całkowitej wymianie po−
koleń. Jednak już od początku lat 70. zawartość
metalu w ciele tych ptaków pozostaje niska i nie
ulega większym zmianom. W środowisku wod−
nym sytuacja jest nieco odmienna. Najczęstszym
sposobem służącym do oceny stopnia skażenia je−
ziora rtęcią jest ocena jej zawartości w ciele
szczupaka. Niestety, okazuje się, że w wielu jezio−
rach Szwecji poziom Hg nadal wzrasta. Przyczy−
0
50
100
0
1970
1975
1980
lata
Zawartoæ Hg u szpaków
z okolic Krankensjön
ng/g
¿ywej wagi
Ryc. 16.
Zmiana poziomu rtęci u szpaków po wpro−
wadzeniu w 1966 r. zakazu stosowania zapraw na−
siennych zawierających organiczną rtęć. [Monitor,
1985].
50
40
30
20
10
0
Karlskrona
Ä
ä
ngsk rsklubb
[mg/kg]
1970 1972
1974
1976
1978
1980 Lata
Zawartoæ DDT
w miêniach ledzi
Ryc. 17.
Zmiany poziomu DDT u śledzia bałtyckie−
go po wprowadzeniu około 1970 r. zakazu jego stoso−
wania. [Monitor, 1985].

Strona 28
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
na tego nie jest całkiem jasna, choć
jedną z możliwości jest zwiększona
rozpuszczalność rtęci pod wpływem
zakwaszania, co z kolei prowadzi do
nasilonego jej wymywania ze skał
i gleby.
Po wprowadzeniu, około 1970 r.,
w wielu krajach zakazu stosowania
DDT, stężenia tego związku oraz
produktów jego degradacji, DDE
i DDD, łącznie oznaczanych jako
sDDT
(co oznacza sumę substancji
typu DDT), gwałtownie spadły
(
i
). Ten znacząco
szybki spadek odzwierciedla fakt, że
DDT dostaje się do środowiska bez−
pośrednio podczas jego stosowania.
Poczynając od około 1972 r. stężenia tego związku rejestrowane u bałtyckich śledzi są stosunko−
wo niskie (
). Rysunek ten wskazuje na jeszcze jeden istotny fakt. Po wprowadzeniu
zakazu, stężenia DDT u śledzi łowionych w południowej części Bałtyku oscylowały wokół prze−
działu 8–9 ppm (górny wykres). Jednak u ryb łapanych w Zatoce Botnickiej nie stwierdzono
takiego poziomu nawet przed wprowadzeniem zakazu. Ta obserwacja wskazuje, że istnieją róż−
nice geograficzne w zawartości sDDT przy czym, ogólnie mówiąc, jest ona wyższa w południo−
wych częściach Bałtyku. Gwałtowne obniżenie stężeń tych związków w organizmach żyjących
w tym regionie widoczne jest również na
, przedstawiającym zmiany poziomu sDDT
jajach nurzyka podbielałego zbieranych na wyspie Stora Karlsö na zachód od Gotlandii.
5.2. Chlorowane dwufenyle (PCB) – długotrwały problem
W warunkach przemysłowych PCB używano do izolacji przewodów elektrycznych, jako sub−
stancje stabilizujące do farb, itp. Taki sposób ich wykorzystania pociąga za sobą fakt, że jako
składniki innych materiałów PCB nie dostaną się do środowiska dopóki materiały te nie zostaną
zniszczone. Konsekwencje tego ilustruje
, przedstawiający stężenia wielochlorowanych
dwufenyli w jajach nurzyka podbielałego zbieranych w okolicach Stora Karlsö. Zakaz stosowa−
nia tych związków wprowadzono w wielu krajach około 1970 r. Jednakże ich poziom w jajach
nurzyka obniżył się dopiero po kilkunastu latach. Opóźnienie to ilustruje średni odstęp czasowy,
jaki upływa od powstania produktu zawierającego PCB do jego destrukcji, czemu towarzyszy
uwalnianie tych toksyn.
Odkrycie PCB jako zanieczyszczeń środowiskowych nastąpiło z powodu drastycznych skutków
przez nie wywoływanych u drapieżników na szczycie łańcucha pokarmowego, w tym przypad−
ku orła bielika. Znaleziony w 1966 r. na archipelagu Sztokholmskim martwy okaz bielika pod−
dano analizie na obecność DDT, za pomocą kombinowanej chromatografii gazowej i spektro−
metrii masowej, przeprowadzonej przez pracującego w Sztokholmie skandynawskiego chemika
Sörena Jensena. Analiza wykazała obecność wielu innych chlorowanych węglowodorów. Poziom
tych toksyn w tkance tłuszczowej orła był szokujący, przekraczał 10 000 ppm.
5.3. Ołów – przyczyny i zmiany
Zmiany stężenia ołowiu wskazują wyraźnie, że działania podjęte w celu zmniejszenia chemicz−
nego zagrożenia w środowisku mogą być skuteczne. Na
grubą linią oznaczono ilości
ołowiu użyte do produkcji benzyny ołowiowej w Stanach Zjednoczonych w okresie 1975–1980,
a linią cienką średni poziom ołowiu we krwi mieszkańców w tym samym okresie. Bezpośrednia
Ryc. 18.
Zmiany poziomu DDT i PCB w jajach nurzyka pod−
bielałego po wprowadzeniu około 1970 r. zakazu ich stosowania
[Monitor, 1985].
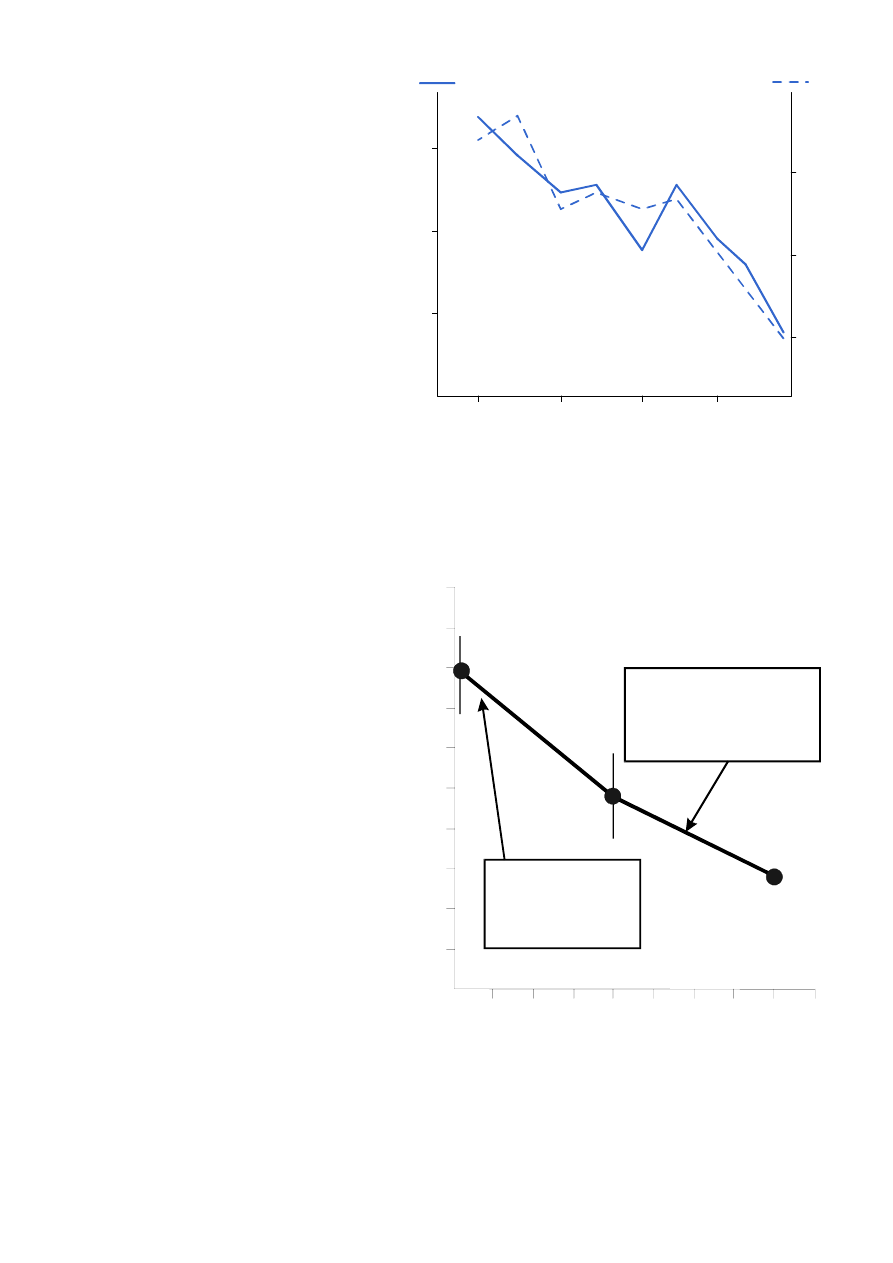
Strona 29
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
korelacja tych parametrów wręcz rzuca
się w oczy. Podobne pomiary przeprowa−
dzono również w Szwecji (
) wy−
kazując, że średnia zawartość ołowiu we
krwi dorosłych mieszkańców Sztokholmu
obniżała się równolegle z przedsięwzię−
ciami podejmowanymi przez władze
w celu ograniczenia użycia benzyny oło−
wiowej.
A co z ołowiem w środowisku? Czy jego
poziom również się obniżył. Wiercenia
w pokrywie lodowej na Grenlandii dostar−
czyły szeregu długich rdzeni wiertni−
czych. Jest możliwe określenie wieku róż−
nych części tych rdzeni. Jak widać na
pierwszy gwałtowny wzrost za−
wartości ołowiu w opadach osiadającego
śniegu przekształcanego następnie w lód
stwierdzono we wczesnym okresie uprze−
mysłowienia, a wyraźne nasilenie tego
procesu zaznacza się od momentu wpro−
wadzenia, pod koniec lat 40., benzyny
ołowiowej. Zmniejszenie zużycia benzyny
ołowiowej z pewnością przyczyniło się do
gwałtownego obniżenia poziomu ołowiu
w lodzie, tworzącym się od lat 70. Można
zapytać czy te globalne zmiany zanie−
czyszczenia ołowiem widoczne są także
w regionie Bałtyku?
pokazuje
stężenia ołowiu w muzealnych okazach
jednego z gatunków mchów zebranych
w Szwecji, z których najstarszy pochodził
z 1868 r. Mchy nie mają prawdziwych ko−
rzeni i nie pobierają mikroelementów
i wody z gleby, natomiast bardzo łatwo
pobierają je z opadów atmosferycznych.
Jak widać na rysunku, opad ołowiu
z powietrza zwiększał się powoli mniej
więcej aż do okresu I wojny światowej, po
czym – aż do roku 1947 kiedy to nastąpił
gwałtowny jego wzrost – nie ulegał
większym zmianom. Podobnie jak w po−
przednim przykładzie widać, że wprowa−
dzenie benzyny ołowiowej stało się głów−
ną przyczyną zwiększonego poziomu tego
metalu w środowisku w okresie powojen−
nym. Widać również, że ograniczenie
zużycia ołowiu do produkcji benzyny, na
początku lat 70. znalazło odzwierciedle−
nie w odpowiednim zmniejszeniem jego
stężenia w środowisku, także w regionie
Bałtyku.
60
80
100
140
120
100
1976
1977
1978
1979
[µg/l krwi]
( )
[kilotony]
( )
Zawartoæ o³owiu
Ryc. 19.
Zależność pomiędzy ilością ołowiu użytego do
produkcji benzyny w USA a średnim poziomem tego met−
alu we krwi mieszkańców tego kraju [Hubendick, 1985].
100
90
80
70
60
50
40
30
20
10
0
80 81 82
84
86
88 89
83
85
87
Zawartoæ o³owiu we krwi
doros³ych mieszkañców
Sztokholmu [µg Pb/l krwi]
zmniejszenie
iloci o³owiu
do produkcji
wprowadzenie
benzyny
bezo³owiowej
Ryc. 20.
Obniżenie poziomu ołowiu we krwi mieszkań−
ców Sztokholmu po wprowadzeniu ograniczeń w stosowa−
niu Pb do produkcji benzyny.
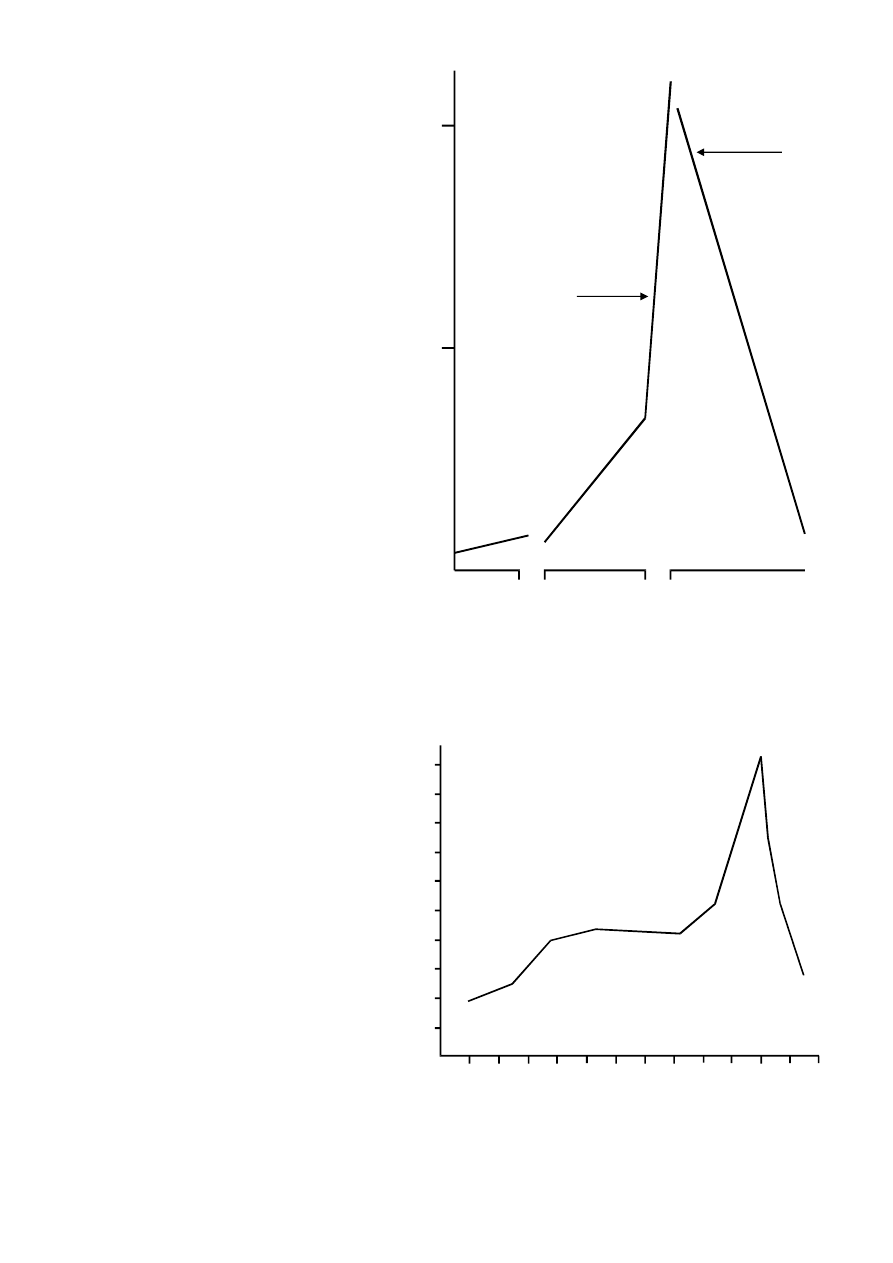
Strona 30
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
5.4. Model cykliczny –
czy kiedyś znikną
zanieczyszczenia?
Źródła zanieczyszczeń, ich transport,
przemiany, skutki działania itp. zostały
już przedstawione jako elementy łańcu−
cha zanieczyszczeń na
, który pod−
sumowuje najważniejsze aspekty oma−
wiane w tekście. Ostatnie ogniwo tego
łańcucha oznacza rozkład. Po śmierci
organizmów zarówno roślinnych i zwie−
rzęcych ich ciała ulegają rozkładowi
wskutek działania mikroorganizmów. Za−
tem przynajmniej niektóre z zanieczysz−
czeń obecnych w ich tkankach dostaną się
ponownie do środowiska. Tak więc mar−
twe organizmy stanowią dodatkowe ich
źródło. Oznacza to, że zanieczyszczenia
będą dotąd krążyły w obiegu materii do−
póki nie zostaną całkowicie rozłożone do
dwutlenku węgla i wody. Tym samym
najpoważniejsze zagrożenie wiąże się
z metalami, które jako pierwiastki są
trwałe i na zawsze już pozostaną w obie−
gu. Z tego wniosek, że emisje toksycznych
metali muszą być utrzymywane na mo−
żliwie najniższym poziomie w celu
zmniejszenia zagrożenia dla środowiska.
A co z gatunkami, które były zagrożone? Na
przełomie lat 50. i 60. często znajdywaliśmy
martwe zwierzęta zabite przez zanieczysz−
czenia. Wśród gatunków najbardziej dot−
kniętych znalazły się bażant, trznadel, so−
kół wędrowny i orzeł bielik, czyli ziarnojady
zatrute przez zaprawy nasienne zawiera−
jące alkilortęć, oraz konsumenci ostatniego
rzędu. W 1964 r obserwacje trznadli nale−
żały do rzadkości. Jednak wkrótce po
wprowadzeniu zakazu stosowania rtęci
w 1966 r. liczebność populacji wróciła do
normy. Podobna sytuacja ma miejsce
w przypadku sokoła wędrownego i orła bie−
lika. Około 1970 r. w Szwecji pozostały przy
życiu jedynie nieliczne osobniki. Obecnie,
wskutek zakazu stosowania DDT oraz in−
tensywnych działań na rzecz restytucji tych
gatunków, ich liczebność rośnie. Odbudowa
słabych populacji jest więc możliwa, ko−
nieczne jest jednak podjęcie odpowiednich
kroków administracyjnych i praktycznych.
Ryc. 21.
Poziom ołowiu w rdzeniach wiertniczych pocho−
dzących z pokrywy lodowej na Grenlandii.
200
100
2500
p.n.e.
1750
1950 1970
1990
Benzyna
o³owiowa
Benzyna
bezo³owiowa
Czasy
rzymskie
[pikogramy Pb/g]
Ryc. 22.
Zawartość ołowiu u jednego z gatunków mchów
w Szwecji w okresie 1868–1985 [Oparte na danych Szwedz−
kiej Agencji Ochrony Środowiska].
1860 70 80 90 1900 10 20 30 40 50 60 70 80 85
100
90
80
70
60
50
40
30
20
10
0
Lata
O³ów
[mg/g]
Zawartoæ o³owiu w mszakach
z prowincji Skäne
w latach 1860-1985

Strona 31
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
Podobne obserwacje poczynione zostały w środowisku morskim. Na przykład kilka lat temu
pasy morszczynu, rosnącego wokół wybrzeży Bałtyku, zostały w niektórych miejscach mocno
przerzedzone. Aktualnie wiele populacji tego gatunku wróciło do normy, odzyskując pierwotną
liczebność. Zubożałe zbiorowiska morszczynu można obecnie znaleźć najczęściej u wylotów
odprowadzających ścieki, np. z zakładów celulozowo–papierniczych, których wody są bardziej
żyzne a jednocześnie zawierają trujące zanieczyszczenia.
5.5. Czy człowiek także jest zagrożony?
Człowiek zajmuje miejsce na szczycie sieci pokarmowej stąd też istotne jest pytanie czy rów−
nież i on jest zagrożony przez zanieczyszczenia środowiskowe. Odpowiedź na nie jest dość
złożona.
Z jednej strony człowiek nie jest typowym drapieżnikiem, gdyż spożywa bardzo różne rodzaje
pokarmów, natomiast wiele zwierząt jest bardziej ograniczonych w swej diecie. Jest bardziej
prawdopodobne, że skutkiem stosowania diety urozmaiconej będzie niższy poziom zanieczy−
szczeń niż w przypadku pobierania jednorodnego pokarmu. Większość zanieczyszczeń ląduje
ostatecznie w zbiorowiskach jezior i mórz, stąd też skrajni konsumenci ryb mogą należeć do
grupy ryzyka. Szwedzka Narodowa Agencja ds. Żywności wydała pewne zalecenia dotyczące
spożycia ryb. I tak, ryb łowionych w Öresund
oraz w okolicach Sztokholmu, Göteborga
i Sundsvall nie należy spożywać częściej niż dwa razy w tygodniu, natomiast okonia, szczupaka,
sandacza i miętusa – raz w tygodniu. Kobiety w ciąży nie powinny jeść żadnego z wymienionych
gatunków z powodu wysokiej zawartości organicznych związków rtęci. Ktoś mógłby również
zapytać, czy pozostałości pestycydów np. w warzywach są szkodliwe dla człowieka. Nie ma,
jak na razie, dobrze udokumentowanego przypadku wywołania choroby u człowieka przez takie
pozostałości.
W sytuacjach skrajnych pojawiają się oczywiście szkodliwe skutki. Kilkanaście dobrze
udokumentowanych przypadków dotyczy wypadków, w których doszło do masowej emisji che−
mikaliów. Pierwszy znany przypadek tego typu wydarzył się w miejscowości Minamata
w Japonii w 1953 r., gdzie duże ilości organicznej rtęci zostały wypuszczone z fabryki i stały
się przyczyną śmierci wielu mieszkańców, żywiących się rybami łowionymi w pobliskiej zatoce
Stosunkowo niedawny tragiczny wypadek w fabryce chemicznej w Bhopalu w Indiach w 1986 r.
spowodował śmierć ponad 2 000 osób.
Znaczna ekspozycja na związki chemiczne często ma także miejsce w warunkach pracy
zawodowej. Dlatego pracownicy mający kontakt ze stężonymi roztworami np. biocydów w celu
ich rozpylenia na polach muszą zachować szczególną ostrożność aby nie zostać samemu
narażonym na ich działanie. Skutkiem nieodpowiednich środków ostrożności były poważne
obrażenia a nawet śmierć. Podobnie, niewłaściwe obchodzenie się z chemikaliami w fabrykach
może pociągnąć za sobą choroby i śmierć. Zostało to dobrze udokumentowane przez ekspertyzy
medyczne zarówno w Szwecji jak i innych krajach regionu bałtyckiego. Bardzo dokładnie
przebadany przypadek dotyczył zakładu metalurgicznego Rönnskärsverken położonego nad
Zatoką Botnicką. Najprawdopodobniej złe warunki pracy są przyczyną złego stanu zdrowia
pracowników w wielu silnie uprzemysłowionych regionach Polski, takich jak regiony Śląska
i Łodzi, gdzie zarówno spodziewana długość życia jak i śmiertelność są wyższe niż gdziekolwiek
indziej w Europie (średnia śmiertelność w Katowicach wynosi 1 900 osób na 100 000, natomiast
spodziewana długość życia mężczyzn wynosi 66 lat a kobiet 74; dane te należy porównać
z rokiem 1972 i 1978 dla Europy zachodniej – zob.
Zeszyt 5
tej serii). Dzieci z tych regionów
cierpią najbardziej mimo, że nie są aktywne zawodowo. Liczby dotyczące śmiertelności i zdrowia
dzieci są alarmujące. Szkodliwy wpływ zanieczyszczonego środowiska jest tutaj wyraźnie
widoczny.
Na koniec musimy wspomnieć o wpływie czynników środowiskowych na nowotwory. Ogólnie
biorąc, czynniki te są odpowiedzialne za około 75% wszystkich przypadków raka u ludzi. Bardzo
trudno jest określić co to są za czynniki choć wiadomo, że znaczącą rolę odgrywa pokarm. Dobrze

Strona 32
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
udokumentowanym czynnikiem jest oczywiście palenie papierosów będące przyczyną raka płuc.
Innym, także dobrze znanym, jest promieniowanie spowodowane przez np. radon, obecny
w wielu materiałach budowlanych, czy też wpływ katastrofy w Czarnobylu na niektórych
obszarach Ukrainy i Białorusi. Jasne jest także, że efekty łączone, inaczej synergizm, odgrywają
istotną rolę, w wyniku czego palacze są bardziej wrażliwi na szereg innych zagrożeń
zawodowych w swoim środowisku niż niepalący.
Dobrze udokumentowane oddziaływania czynników środowiskowych na zdrowie człowieka
należy i można zmienić poprzez poprawę warunków pracy i życia, a przede wszystkim zdrowszy
styl życia. Reszta świata ożywionego nie ma wyboru. Oto zadanie dla nas aby zmniejszyć
szkodliwe wpływy w celu zachowania przy życiu biologicznej różnorodności populacji, gatunków
i całej przyrody ożywionej.

Strona 33
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
6.
P
ODSUMOWANIE
●
Ekotoksykologia zajmuje się losem zanieczyszczeń chemicznych w środowisku,
tak jak to zestawiono w łańcuchu zanieczyszczeń.
●
Spośród wielu związków chemicznych uwalnianych do środowiska najbardziej za−
grażające są te, które łączą w sobie trwałość z dostępnością biologiczną.
●
Większość zagrażających substancji należy do trzech grup: chlorowcowanych węglo−
wodorów, węglowodorów wielopierścieniowych oraz metali ciężkich i ich związków.
●
Głównymi źródłami zanieczyszczeń są: produkcja energii, działalność przemysłu
i stosowanie pestycydów. Zanieczyszczenia są szeroko roznoszone w środowisku
abiotycznym za pośrednictwem wiatrów i wody. Podczas tego transportu niektóre
z nich ulegają częściowej lub całkowitej degradacji.
●
Niektóre substancje są dostępne dla organizmów żywych i są przez nie pobierane.
W ich ciałach niektóre z nich ulegają rozkładowi i wydaleniu. Inne mogą być groma−
dzone w narządach, zwłaszcza tkance tłuszczowej.
●
Zanieczyszczenia mogą być przenoszone z jednego osobnika do drugiego, zwłasz−
cza od ofiary do drapieżcy w obrębie sieci pokarmowej. W tych przypadkach stężenie
wzrasta na kolejnych poziomach sieci – zjawisko to nazywamy biomagnifikacją.
●
Transfer między matką a dzieckiem może zachodzić za pośrednictwem łożyska
u ssaków i przez jajo u ptaków i gadów. Z tego powodu młode mają takie same
stężenia zanieczyszczeń jak matka już w momencie urodzenia.
●
Istnieje ścisła zależność zwana zależnością dawka–reakcja pomiędzy ilością zwią−
zku docierającą do organizmu a nasileniem skutków przez nią wywołanych. Za−
leżność tą często określa się ilościowo wartością LD50.
●
Najbardziej szkodliwymi ale nie powodującymi śmierci skutkami zanieczyszczeń
jest zmniejszona produkcja u roślin {chodzi o produkcję pierwotną – przyp. tłum.}
oraz zaburzenia w funkcjonowaniu mięśni, układu nerwowego i odpornościowego
a także czynnościach rozrodczych u zwierząt. Te ostatnie są często najbardziej
podatne na działanie zanieczyszczeń.
●
Niektóre efekty wywołane u pojedynczych osobników mogą zagrozić istnieniu całych
populacji. Przykładem jest populacja fok w Bałtyku znajdująca się na progu zagłady,
podobnie jak populacje niektórych ptaków, z powodu niepowodzeń reprodukcji.
●
Skutki działania zanieczyszczeń na poziomie całych ekosystemów można określić
jako zmniejszenie ich bioróżnorodności i biomasy.
●
Aktualne poziomy zanieczyszczeń w regionie Bałtyku wymagają rozwagi w dzia−
łaniach w celu uniknięcia poważnych zagrożeń dla człowieka.
●
Zakazy i ograniczenia, wprowadzone przez władze w różnych krajach wokół Mo−
rza Bałtyckiego, zaowocowały zmniejszeniem stężeń niektórych zanieczyszczeń,
jednak aktualny stan Bałtyku w dalszym ciągu wymaga podejmowania dodatko−
wych działań.

Strona 34
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
7.
P
IŚMIENNICTWO
1.
Hubendick B., Människoekologi. Gidlunds, 1985.
2.
Jensen S., Kihlström J.E., Olsson M., Lundberg C. Örberg J., Ambio 6:239, 1977.
3.
Johnels A.G., Westermark T., Berg W., Persson P.I. Sjöstrand B., Oikos 18:323, 1967.
4.
Johnels, A.G. Odsjö T., Ambio Special Report Nr 1, 1972.
5.
Kihlström, J.E., Gifter i naturen. Liber, 1986.
6.
Monitor,1984, Langväga transport av luftföroreningar. Swedish Environmental Protection Agen−
cy, ss. 134.
7.
Monitor 1985,PMK: Pa vakt i naturen. Swedish Environmental Protection Agency, ss. 208.
8.
Olsson M., Jensen S., Rehnberg L., Ambio Special Report Nr 1, 1972.
Ze względu na niewielką dostępność dla Czytelnika polskiego
wymienionych wyżej pozycji, poniżej podano wybrane piśmiennictwo
w języku polskim poszerzające problematykę toksykologiczną:
O
PRACOWANIA
OGÓLNE
1.
Kulisz I., Kwaśne opady i ich wpływ na środowisko. Przegląd literatury światowej. Wyd. Geolog−
iczne, Warszawa 1988.
2.
Migula P., Kiedy metale ciężkie są szkodliwe. Fundacja Ekologiczna „Silesia”, Katowice
1993.
3.
Przeździecki Z., Biologiczne skutki chemizacji środowiska. PWN, Warszawa 1980.
4.
Umiński T., Ekologia, Środowisko, Przyroda. WSiP, Warszawa 1995.
5.
Zakrzewski S.F., Podstawy toksykologii środowiska. PWN, Warszawa 1995.
O
PRACOWANIA
SZCZEGÓŁOWE
1.
Ciszewska I. (red.), Międzynarodowy Monitoring Biologiczny Morza Bałtyckiego. Instytut Ochrony
Środowiska, Warszawa 1993.
2.
Gumińska M. (red.), Chemiczne substancje toksyczne w środowisku i ich wpływ na zdrowie czło−
wieka. Ossolineum, Wrocław 1990.
3.
Praca zbiorowa, Życie drzew w skażonym środowisku. Seria: Nasze drzewa leśne. Tom 21. PWN,
Warszawa–Poznań 1989.
4.
Różański L., Przemiany pestycydów w organizmach żywych i środowisku. PWRiL, Warszawa
1992.

Strona 35
Ś
RODOWISKO
M
ORZA
B
AŁTYCKIEGO
Toksykologia – Wpływ Zanieczyszczeń na Środowisko
8.
P
RZYPISY
1
Ta „optymistyczna” sytuacja wywołana jest nie tyle faktem znacznego ograniczenia stosowania pesty−
cydów, ile wprowadzeniem nowych generacji niezwykle silnych preparatów (np. syntetycznych py−
retroidów) pozwalających na znaczne zmniejszenie ilości środka użytego do zabiegu (rzędu kilku–
kilkunastu gramów substancji czynnej na hektar) przy zachowaniu wysokiej skuteczności. Te niewielkie
ilości są jednak toksyczne także dla organizmów nie będących szkodnikami – przyp. tłum.
2
W oryginale: „The solution of the pollution is dilution”. W żargonie toksykologów funkcjonuje równie
zgrabna korekta tego stwierdzenia: „Dilution is not solution to pollution” co można przetłumaczyć
jako: „rozcieńczenia nie rozwiązują problemu zanieczyszczenia” – przyp. tłum..
3
W języku angielskim oprócz terminu „biological availability” czyli dostępność biologiczna używany
jest skrót „bioavailability”, co można tłumaczyć jako biodostępność. Jednak określenie to nie funkcjo−
nuje w polskiej terminologii stąd też nie będzie używane w niniejszym opracowaniu – przyp. tłum.
4
Stężenia zanieczyszczeń wyrażamy na jednostkę masy ciała lub narządu (zwykle suchej masy) nato−
miast ich ilość określamy w przeliczeniu na osobnika, stąd przyrost masy ciała szybszy niż ilości
zanieczyszczeń powoduje obniżenie ich stężenia. Nota bene opisana sytuacja może mieć miejsce wte−
dy, gdy oprócz mleka młode pobierają także inny, mniej skażony pokarm – przyp. tłum.
5
Mówiąc o śmiertelności należy zawsze mieć na uwadze czas, w którym ją analizujemy. W praktyce
LD
50
określa się najczęściej dla 24 godzin ale mogą być stosowane i inne okresy zarówno dłuższe − np.
48 godz., 72 godz. lub krótsze − np. 1 godz. – przyp. tłum.
6
Grzybnia oplatająca korzenie drzew pełni m.in. rolę rozbudowanej, dodatkowej „strefy włośnikowej”
umożliwiającej lepsze pobieranie wody i soli mineralnych. Zanik grzybni prowadzi więc do znacznego
upośledzenia transportu tych substancji z gleby do korzeni – przyp. tłum.
7
Wydolność robocza mięśni (ang. working capacity) jest pochodną funkcjonowania aparatu kurczliwe−
go (miofilamenty) oraz enzymatycznego, dostarczającego energii niezbędnej do skurczów (uzyskiwa−
nej zarówno w procesach tlenowych jak i beztlenowych). Oznacza ona zatem zdolność mięśni do kon−
tynuowania wysiłku przez pewien czas – przyp. tłum.
8
Myoxocephalus quadricornis − ryba z rodziny głowaczowatych żyjąca w wodach przybrzeżnych Morza Ar−
ktycznego i niektórych wodach śródlądowych. W Bałtyku jest gatunkiem reliktowym.
9
Chodzi tu głównie o tak zwane oksydazy o funkcji mieszanej (lub monooksygenazy), metabolizujące
różne substraty zarówno endo− jak i egzogennego pochodzenia. Hormony płciowe są sterydami, pochod−
nymi cholesterolu a więc nie są rozkładane przez „zwykłe” hydrolazy, działające w środowisku wod−
nym komórki (a także jelita) – przyp. tłum.
10
U fok obie macice − przedłużenie parzystych jajowodów − łączą się ze sobą na pewnej długości tworząc
w ten sposób macicę dwurożną z dwoma, częściowo połączonymi komorami, w których rozwijają się
zarodki. U naczelnych, z człowiekiem włącznie, połączenie to jest całkowite i powstaje macica poje−
dyncza z jedną komorą – przyp. tłum.
11
Skorupka jaja zawiera mnóstwo maleńkich porów (np. w jaju kury jest ich ok. 7 000) umożliwiających
wymianę gazów między zarodkiem a otoczeniem. Ich ilość jest kompromisem pomiędzy koniecznością
oddychania a koniecznością ograniczenia strat wody – przyp. tłum.
12
Łacińska nazwa rzędu gryzoni brzmi Rodentia, (ang. rodents) stąd środki gryzoniobójcze to rodentycy−
dy, podobnie dla owadów (łac. Insecta, ang. insects) będą to insektycydy, dla mięczaków (łac. Mollusca,
ang. molluscs) − molluskocydy itp. Nazwa pestycydy pochodzi od ang. słowa pest oznaczającego szkodni−
ka – przyp. tłum.
13
Cieśnina graniczna między Szwecją i Danią – przyp. tłum.
14
W istocie związki rtęci obecne w ściekach przemysłowych ulegały metylacji do silnie toksycznych
pochodnych głównie w środowisku wodnym, pod wpływem bakterii obecnych w osadach dennych.
Stamtąd dopiero trafiały one na wyższe poziomy sieci troficznej, w tym i do ludzi. W okresie kilku lat
zatruciu uległo kilka tysięcy ludzi, z czego ponad 100 zmarło. Z powodu neurotoksycznego i terato−
gennego działania metylortęci wielu chorych – zwłaszcza dzieci – zostało kalekami – przyp. tłum.
Document Outline
- Spis Treœci
- Przedmowa
- 1. Wprowadzenie
- 1.1. GroŸba dla ¿ycia w Ba³tyku
- 1.2. £añcuch zanieczyszczeñ
- 1.3. Chemiczne zanieczyszczenia Morza Ba³tyckiego
- 2. Od Ÿród³a zanieczyszczeñ do ¿ywego organizmu
- 2.1. Przenoszenie przez wiatry
- 2.2. Przenoszenie przez wodê
- 2.3. Ze œrodowiska do organizmów ¿ywych
- 2.4. Losy zanieczyszczeñ w organizmie - akumulacja i biomagnifikacja
- 2.5. Zatrucie wrodzone - przep³yw toksyn od matki do dziecka
- 3. W jaki sposób zanieczyszczenia wp³ywaj¹ na organizmy
- 3.1. Dawki i efekty
- 3.2. Oddzia³ywanie na roœliny
- 3.3. Zwierzêta: czynnoœci nerwów i miêœni
- 3.4. Uk³ad odpornoœciowy i organogeneza
- 3.5. Fizjologia rozrodu jest bardzo wra¿liwa na zanieczyszczenia
- 3.6. Populacja fok w Ba³tyku jest zagro¿ona
- 3.7. Wra¿liwym stadium u ptaków jest jajo
- 3.8. Ryby w jeziorach s¹ zagro¿one przez metale ciê¿kie
- 4. Oddzia³ywanie na ekosystemy
- 4.1. Zanieczyszczenia wywo³uj¹ efekty ³añcuchowe w ekosystemach
- 4.2. Pomiary liczebnoœci
- 4.3. Przyk³ad - ekosystem zmieniony przez zakwaszenie
- 4.4. Zmiany w s¹siedztwie zak³adów metalurgicznych
- 5. Przysz³oœæ - Czy podjête dzia³ania s¹ skuteczne?
- 5.1. Pierwsze akcje - zakaz stosowania rtêci i DDT
- 5.2. Chlorowane dwufenyle (PCB) - d³ugotrwa³y problem
- 5.3. O³ów - przyczyny i zmiany
- 5.4. Model cykliczny - czy kiedyœ znikn¹ zanieczyszczenia?
- 5.5. Czy cz³owiek tak¿e jest zagro¿ony?
- 6. Podsumowanie
- 7. Piœmiennictwo
- 8. Przypisy
Wyszukiwarka
Podobne podstrony:
Eutrofizacja morza bałtyckiego
CHARAKTERYSTKA MORZA BAŁTYCKIEGO, Liceum, Geografia liceum
Główne ogniska zanieczyszczeń w zlewisku Morza Bałtyckiego
Ochrona morza Bałtyckiego
POCHODZENIE I EWOLUCJA EKOSYSTEMÓW MORZA BAŁTYCKIEGO ORAZ ICH ZMIANY ANTROPOGENICZNE, Ochrona Środow
charakterystyka morza bałtyckiego
żegluga bliskiego zasięgu w rejonie morza bałtyckiego
Historia Morza Bałtyckiego
Środowisko Morza Bałtyckiego
Współpraca transnarodowa Region Morza Bałtyckiego
05 GEOLOGIA jezior iatr morza
toksykologia 4
Analiza toksykologiczna
Toksykologia sądowo lekarska
TOKSYKOLOGIA 8
więcej podobnych podstron