
03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
1/18
Postępowanie w zaburzeniach gospodarki
lipidowej
Rola lipoprotein w powstawaniu miażdżycy 1
Spośród licznych czynników patogenetycznych miażdżycy lipoproteiny wydają się odgrywać
najważniejszą rolę w powstawaniu ogniska miażdżycowego, poprzez penetrację do ściany
tętnicy i wprowadzanie cholesterolu. Zaburzenia gospodarki lipidowej wiążą się ponadto z
upośledzeniem funkcji śródbłonka i do pewnego stopnia z zaburzeniami krzepnięcia i
fibrynolizy, które mają swój udział w patogenezie miażdżycy, a w szczególności w rozwoju
niedrożności tętnic. Główne zaburzenia lipidowe zwiększające ryzyko chorób sercowo
naczyniowych to hipercholesterolemia i aterogenna dyslipidemia. Trzeci rodzaj zaburzeń
lipidowych, to rzadziej występujący zespół chylomikronemii, który nie odgrywa istotnego
znaczenia w chorobach układu krążenia, ale może zwiększać ryzyko ostrego zapalenia
trzustki.
Rodzaje zaburzeń lipidowych:
hipercholesterolemia,
aterogenna
dyslipidemia
(hiperlipidemia mieszana),
zespół chylomikronemii.
Najczęstsza przyczyną hipercholesterolemii jest zwiększone stężenie LDL w osoczu.
Lipoproteiny te przenikają do błony wewnętrznej w wyniku filtracji osocza pod wpływem
ciśnienia krwi. Proces ten jest ułatwiany przez czynniki uszkadzające błonę wewnętrzną
tętnicy, do których należy nadciśnienie tętnicze, palenie tytoniu, homocysteina i in. W ścianie
tętnicy LDL są oksydacyjnie modyfikowane pod wpływem kontaktu z komórkami ściany
naczynia (śródbłonek, makrofagi, komórki mięśni gładkich), wytwarzającymi wolne rodniki
tlenowe. To powoduje, że nabierają one właściwości aterogennych. Zmodyfikowane LDL
wykazują silne powinowactwo do niepodlegającego sprzężeniu zwrotnemu receptora
zmiatającego (scavenger receptor) na makrofagach (komórki pochodzące od monocytów),
które po przyswojeniu dużej liczby cząsteczek zmodyfikowanych LDL przeistaczają się w
komórki piankowate – ważny element ogniska miażdżycowego. Tak więc intensywność
filtracji LDL do ściany tętniczej zależy od ich ilości w krążeniu, od przepuszczalności tętnicy
oraz od ciśnienia tętniczego.
Rola lipoprotein w powstawaniu miażdżycy 2

03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
2/18
Za aterogenne, oprócz LDL, uważa się również tzw. lipoproteiny resztkowe (remnanty) tj.
częściowo skatabolizowane lipoproteiny o bardzo małej gęstości (VLDL) i chylomikrony.
W celu przypomnienia warto dodać, że VLDL przenoszą w osoczu głównie trójglicerydy (TG)
wytworzone w wątrobie z wolnych kwasów tłuszczowych, uwolnionych przez tkankę
tłuszczową oraz z węglowodanów pokarmowych. Chylomikrony są natomiast syntetyzowane
w nabłonku jelitowym i transportują w osoczu trójglicerydy i cholesterol pochodzenia
pokarmowego.
W wyniku hydrolizy TG zawartych w VLDL i chylomikronach, pod wpływem lipazy
lipoproteinowej obecnej w śródbłonku naczyniowym, powstają remnanty tych lipoprotein.
Mają one znacznie mniejsze rozmiary niż lipoproteiny macierzyste, utraciły bowiem znaczną
część trójglicerydów i łatwo przenikają do ściany tętnicy, wprowadzając cholesterol.
Odmienną rolę w aterogenezie odgrywają lipoproteiny o dużej gęstości (HDL). Mają
właściwości odbierania cholesterolu z tkanek, transportując go następnie do wątroby
(transport zwrotny). W ten sposób mogą odgrywać ważną rolę w hamowaniu powstawania
ognisk miażdżycowych. Jest to najważniejszy, chociaż nie jedyny, z postulowanych
mechanizmów przeciwmiażdżycowego działania HDL. Inne właściwości HDL to działanie
przeciwzapalne i antyoksydacyjne.
Rozwój miażdżycy zależy w znacznym stopniu od stosunku lipoprotein aterogennych do
HDL w osoczu. Małe stężenie cholesterolu HDL ma różne przyczyny, w 4060% jest jednak
determinowane genetycznie. Może ono również występować wtórnie w następstwie chorób,
przyjmowania niektórych leków i określonego stylu życia.
Do czynników odpowiadających za małe stężenie cholesterolu HDL należą:
zespół metaboliczny,
cukrzyca typu 2,
otyłość,
hipertrójglicerydemia,
przewlekła niewydolność nerek,
zespół nerczycowy,
AIDS,
przyjmowanie tiazydów moczopędnych,
leków betaadrenolitycznych, steroidów anabolicznych i progestagenów,
palenie papierosów,
dieta bogatowęglowodanowa (60% dziennego spożycia energii),
brak aktywności fizycznej (unieruchomienie).
Zaburzenie lipidowe, jakim jest małe stężenie HDL, występuje albo samodzielnie, albo
łącznie z innymi nieprawidłowościami, takimi jak hipertrójglicerydemia i obecność w osoczu
wspomnianych już małych, gęstych LDL (dyslipidemia aterogenna), o których pisano
wcześniej.
Rola lipoprotein w powstawaniu miażdżycy 3
Jak wskazują badania epidemiologiczne i obserwacje kliniczne złożone zaburzenia
lipidowe, występujące niezależnie od podwyższonego stężenia cholesterolu LDL, również

03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
3/18
zwiększają ryzyko chorób sercowonaczyniowych. Zaburzenia te, charakteryzujące się
podwyższonym stężeniem trójglicerydów (głównie efekt wzmożonej produkcji VLDL),
obniżonym stężeniem cholesterolu HDL i obecnością tzw. małych gęstych cząsteczek LDL
nazywane są aterogenną dyslipidemią. Małe gęste LDL są bardziej aterogenne niż normalne
cząsteczki LDL, przede wszystkim ze względu na szczególną podatność na oksydacyjną
modyfikację (mają mało antyoksydantów).
Poza opisaną „triadą lipidową” w aterogennej dyslipidemii występuje w osoczu retencja
remnantów VLDL i chylomikronów. Inny rodzaj zaburzeń lipidowych charakteryzujący się
dużą aterogennością, to mieszana (złożona) hiperlipidemia, cechująca się podwyższonym
stężeniem cholesterolu LDL i aterogenną dyslipidemią.
Odosobnione zwiększone stężenie TG w surowicy nazywane jest hipertrójglicerydemią. Jest
ona najczęściej wynikiem zwiększonego stężenia VLDL (zwykle duże cząsteczki) lub rzadko
obecności chylomikronów w osoczu na czczo, przeważnie w skojarzeniu ze zwiększonym
stężeniem VLDL. Zaburzenie to określa się mianem zespołu chylomikronemii.
Podwyższone stężenie trójglicerydów może być determinowane genetycznie oraz może
występować w formie w przebiegu niektórych chorób, bądź przyjmowania leków.
Główne przyczyny wtórnej hipertrójglicerydemii to:
otyłość,
zespół metaboliczny,
cukrzyca (głównie typu 2),
nadmierne spożycie alkoholu,
brak aktywności fizycznej,
niedoczynność tarczycy,
choroby nerek (zwłaszcza mocznica, kłębkowe zapalenie nerek),
ciąża (fizjologiczny dwukrotny wzrost w III trymestrze ciąży),
choroby autoimmunologiczne (np. lupus erythematosis),
niektóre leki: kortykosteroidy, estrogeny (głównie podawane doustnie), tamoksifen,
nieselektywne ßblokery, tiazydy, leki psychotropowe.
W badaniach epidemiologicznych (Prospective Cardiovascular Münster Study, PROCAM)
wykazano, że hipertrójglicerydemia jest niezależnym czynnikiem ryzyka chorób sercowo
naczyniowych. Zwiększenie TG o 1 mmol/L podwyższa to ryzyko o 32% u mężczyzn i o 76%
u kobiet.
Hipercholesterolemia
Hipercholesterolemia oznacza zwiększone stężenie w osoczu lipoprotein o małej gęstości,
czyli LDL. Zaburzenie to jest najczęściej następstwem nakładania się czynników
żywieniowych (dieta bogata w nasycone kwasy tłuszczowe i cholesterol) na podatność
genetyczną. Tę powszechnie występującą hipercholesterolemię nazywa się wielogenową.
Oprócz niej rzadko spotykana hipercholesterolemia rodzinna (monogenowa). Przyczyną
jej jest brak lub nieprawidłowe funkcjonowanie wszystkich receptorów lipoprotein LDL w
wątrobie (postać homozygotyczna) albo tylko połowy receptorów, podczas gdy druga połowa
działa prawidłowo (postać heterozygotyczna). Przypomnijmy, że receptory LDL, obecnie
głównie na powierzchni komórek wątrobowych, odpowiadają za przyswajanie i rozkładanie

03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
4/18
LDL. Zatem od prawidłowego ich działania zależy utrzymanie prawidłowych stężeń
cholesterolu LDL.
W homozygotycznej hipercholesterolemii rodzinnej stężenia cholesterolu całkowitego i
cholesterolu LDL są nadzwyczaj duże (na ogół cholesterol całkowity 7001200 mg/dL), a
zaawansowana miażdżyca występuje już we wczesnym dzieciństwie. Na szczęście ta
ciężka choroba dotyczy tylko 1 osoby na 1 milion osób w populacji.
W heterozygotycznej hipercholesterolemii rodzinnej stężenia cholesterolu całkowitego i
cholesterolu LDL są duże (zazwyczaj cholesterol całkowity 350500 mg/dl), miażdżyca w
postaci choroby wieńcowej objawia się na ogół w 4. lub 5. dekadzie życia. Heterozygotyczna
hipercholesterolemia rodzinna występuje znacznie częściej niż homozygotyczna, bo u 1
osoby na 500 osób w populacji.W celu rozpoznania rodzinnej hipercholesterolemii, po
stwierdzeniu u osoby badanej wysokich stężeń cholesterolu, konieczne jest wykazanie tej
nieprawidłowości u bliskich krewnych w rodzinie. Potwierdzenie rozpoznania na poziomie
molekularnym wymaga badania DNA, aby wykryć mutację genu receptora LDL. Jednak w
codziennej praktyce lekarskiej nie jest to niezbędne.
Do hipercholesterolemii pierwotnych zalicza się również rodzinny defekt apolipoproteiny
B100, spowodowany upośledzonym wiązaniem cząsteczek LDL z receptorami na skutek
defektu apo B.
W hipercholesterolemiach występujących rodzinnie mogą występować zmiany skórne
(ksantelazmy, ksantelatozy) u chorych oraz u członków jego rodziny.
Hipercholesterolemia może być wtórna, czyli wywołana niektórymi chorobami (najczęściej
jest to niedoczynność tarczycy, może to być także żółtaczka zastoinowa, zespół nerczycowy,
porfiria) lub lekami (tiazydy moczopędne, progestageny).
Zespół chylomikronemii
Zespół chylomikronemii jest dość rzadkim zaburzeniem lipidowym, wykrywanym najczęściej
przypadkowo, przy okazji wystąpienia ostrego zapalenia trzustki (charakterystyczne
powikłanie) lub wykrycia dużych stężeń cholesterolu całkowitego. Doświadczony lekarz
zawsze sprawdzi w takich przypadkach stężenie trójglicerydów, zleci wykonanie tak
zwanego testu zimnej flotacji i wdroży odpowiednie postępowanie. Jakkolwiek w zespole
chylomikronemii stężenie cholesterolu całkowitego jest duże, to nie zależy ono od dużego
stężenia cholesterolu LDL, tylko od dużej liczby chylomikronów, które oprócz trójglicerydów
zawierają także trochę cholesterolu. Duża liczba chylomikronów jest więc przyczyną dużego
stężenia cholesterolu całkowitego i bardzo dużego stężenia trójglicerydów (>1000 mg/dL tj.
11 mmol/L).
Charakterystycznym objawem zespołu chylomikronemii jest dodatni test zimnej flotacji. To
proste badanie należy obowiązkowo wykonywać w przypadku silnej hipertrójglicerydemii.
Polega ono na przechowywaniu surowicy krwi, pobranej od osoby badanej na czczo, w
lodówce w temperaturze +4
o
C przez 24 godziny. Surowica zaraz po pobraniu krwi ma barwę
mleczną z powodu dużego stężenia trójglicerydów, a w przypadku obecności chylomikronów
po 24 godzinach na jej powierzchni powstaje warstwa tłuszczu różnej grubości. Są to
chylomikrony.
Zespół chylomikronemii może być zaburzeniem rodzinnym, a więc genetycznie
uwarunkowanym (niedobór enzymu rozkładającego trójglicerydy, jakim jest lipaza

03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
5/18
lipoproteinowa lub niedobór apoproteiny C II, która aktywuje ten enzym), bądź wtórnym,
powstałym z powodu nadużywania alkoholu lub źle kontrolowanej cukrzycy. Ludzie
chorującym na zespół chylomikronemii nie są bardziej narażeni na chorobę wieńcową niż
reszta populacji, są natomiast szczególnie zagrożeni ostrym zapaleniem trzustki. Z tego
względu stężenie trójglicerydów należy u nich szybko zmniejszyć do wartości mniejszej niż 6
mmol/L.
Docelowe stężenia lipidów
W leczeniu zaburzeń lipidowych najważniejsze jest osiągnięcie docelowego stężenia
cholesterolu LDL. Związek redukcji tego lipidu ze zmniejszeniem ryzyka zawału serca jest
najlepiej udokumentowany w badaniach klinicznych, dotyczy to w szczególności badań z
zastosowaniem statyn. Co więcej, badanie takie wiąże się ze spadkiem liczby zgonów
spowodowanych chorobą wieńcową i ogólnej liczby zgonów. Stężenie cholesterolu LDL,
jakie należy osiągnąć określa się na podstawie oceny ryzyka zgonu z powodu chorób
sercowonaczyniowych w okresie 10 lat. Cele terapeutyczne wynikają z ryzyka choroby
sercowonaczyniowej, tj. im jest ono większe tym większe również wymaganie pod tym
względem.
Jeśli zagrożenie zgonem sercowonaczyniowym w ciągu 10 lat jest małe, tzn. mniejsze niż
5%, to docelowe stężenie LDLC powinno być mniejsze niż 115 mg/dl (<3,0 mmol/L), a
cholesterolu całkowitego < 190 mg/dL (5,0 mmol/L).
W przypadku dużego zagrożenia, wynikającego z obecności choroby wieńcowej, choroby
innych tętnic na tle miażdżycy, cukrzycy, lub ryzyka zgonu sercowonaczyniowego ≥5%
stężenie cholesterolu LDL powinno być mniejsze niż 100 mg/dL (<2,5 mmol/L), a
cholesterolu całkowitego <175 mg/dL (<4,0 mmol/L).
W ostatnich wytycznych Europejskiego Towarzystwa Kardiologicznego i innych towarzystw
(2007) zaproponowano dodatkowo, dla pacjentów z dużym ryzykiem, stężenie LDLC <80
mg/dl (<2,0 mmol/L), jako opcję terapeutyczną.
Należy podkreślić, że tabela ryzyka SCORE służy do oceny ryzyka zgonu sercowo
naczyniowego wyłącznie u osób bez objawowych (prewencja pierwotna). Chorzy na
chorobę wieńcową, chorobę innych tętnic, niż wieńcowe lub cukrzycę mają a priori duże
ryzyko i nie potrzeba w takich przypadkach korzystać do jego oceny z tabeli SCORE.
Istnieją dwie Karty Ryzyka, osobna dla mężczyzn i osobna dla kobiet, które uwzględniają
wiek, palenie papierosów, stężenie cholesterolu całkowitego i wartość ciśnienia
skurczowego.
Po wybraniu Karty Ryzyka odpowiedniej dla płci należy znaleźć pole odpowiadające
wiekowi pacjenta i dotyczące palenia lub niepalenia papierosów. Następnie w obrębie pola
trzeba odszukać kratkę odpowiadającą wartości ciśnienia skurczowego oraz stężenia
cholesterolu całkowitego i odczytać stopień ryzyka wyrażony w procentach.
Jak z tego widać, Karta Ryzyka uwzględnia pięć klasycznych czynników ryzyka płeć, wiek,
palenie papierosów, stężenie cholesterolu i skurczowe ciśnienie tętnicze. Trzeba zdawać
sobie sprawę z tego, na co zwracają uwagę autorzy Karty Ryzyka, że u pacjentów, u których
można stwierdzić cechy miażdżycy (co wykazuje badanie ultrasonograficzne czy tomografia
komputerowa), pomimo braku objawów klinicznych choroby, oraz u tych, którzy pochodzą z
rodzin odznaczających się częstym występowaniem chorób sercowonaczyniowych lub mają
03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
6/18
na przykład zwiększone stężenie trójglicerydów, małe stężenie cholesterolu HDL, bądź
upośledzoną tolerancję glukozy, zagrożenie zgonem sercowonaczyniowym w ciągu 10 lat
może być większe niż odczytane z Karty. Dotyczy to także ludzi otyłych i prowadzących
siedzący tryb życia.
Leczenie niefarmakologiczne 1
Nie ma leczenia zaburzeń lipidowych bez zmiany stylu życia, ze szczególnym
uwzględnieniem poprawy zachowań żywieniowych. Dla redukcji stężenia cholesterolu LDL
kluczowe znaczenie ma
ograniczenie spożycia nasyconych kwasów tłuszczowych < 7% ogółu energii, co w
praktyce oznacza mniej niż 20 g dziennie;
zminimalizowanie spożycia izomerów trans nienasyconych kwasów tłuszczowych.
Powstają one w czasie uwodornienia tłuszczów roślinnych. Zarówno nasycone kwasy
tłuszczowe, jak i izomery trans nienasyconych kwasów tłuszczowych zwiększają stężenie
cholesterolu LDL. Dla realizacji pierwszego zalecenia potrzebna jest znajomość zawartości
nasyconych kwasów tłuszczowych w produktach spożywczych, zwłaszcza tych, które w nie
obfitują. Celowi temu służą Tabele Składu i Wartości Odżywczej Produktów, autorstwa H.
Kunachowicz i wsp. W diecie hipolipemizującej nadal we wszystkich wytycznych
postępowania zaleca się ograniczenie spożycia cholesterolu pokarmowego poniżej 200
mg/dzień.
W praktyce najważniejszym źródłem cholesterolu w diecie są jajka.
Z tego względu należy ograniczać ich spożycie do 2 sztuk tygodniowo. Trzeba także
wiedzieć, że dużo cholesterolu zawierają podroby i wędliny podrobowe, które mają ponadto
dużo nasyconych kwasów tłuszczowych. Jednonienasycone (MUFA), a szczególnie
wielonienasycone (PUFA) kwasy tłuszczowe z rodziny omega6, zastępując nasycone
kwasy tłuszczowe, zmniejszają stężenie cholesterolu LDL. Bogatym źródłem MUFA są oleje
oliwkowy i rzepakowy, zaś PUFA oleje słonecznikowy, sojowy, kukurydziany, krokoszowy.
Właściwość redukcji cholesterolu LDL ma też błonnik rozpuszczalny (nasiona roślin
strączkowych, produkty zbożowe z owsa i jęczmienia, owoce).
Leczenie niefarmakologiczne 2
Ostatnio zwraca się uwagę na korzystną rolę stanoli i steroli roślinnych w obniżaniu
stężenia cholesterolu LDL. Związki te bowiem hamują wchłanianie cholesterolu
pokarmowego i cholesterolu wydzielonego z żółcią do jelita. W stanole i sterole roślinne
wzbogacane są niektóre margaryny i/lub jogurty (żywność funkcjonalna).
Umiarkowana hipertrójglicerydemia może być następstwem otyłości brzusznej i jednym z
objawów zespołu metabolicznego. W takich przypadkach kluczowe znaczenie dla redukcji
stężenia trójglicerydów ma spadek masy ciała.
03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
7/18
Ważnym zaleceniem w hipertrójglicerydemii, o czym często się zapomina, jest unikanie
alkoholu (dotyczy to również piwa), gdyż alkohol nasila hipertrójglicerydemię.
Pacjenci ze zwiększonym stężeniem trójglicerydów powinni ograniczyć spożycie
węglowodanów, zwłaszcza łatwo przyswajalnych. Jest to ważne z tego samego powodu co
unikanie alkoholu. Dla zwiększenia stężenia cholesterolu HDL, spośród zmian stylu życia,
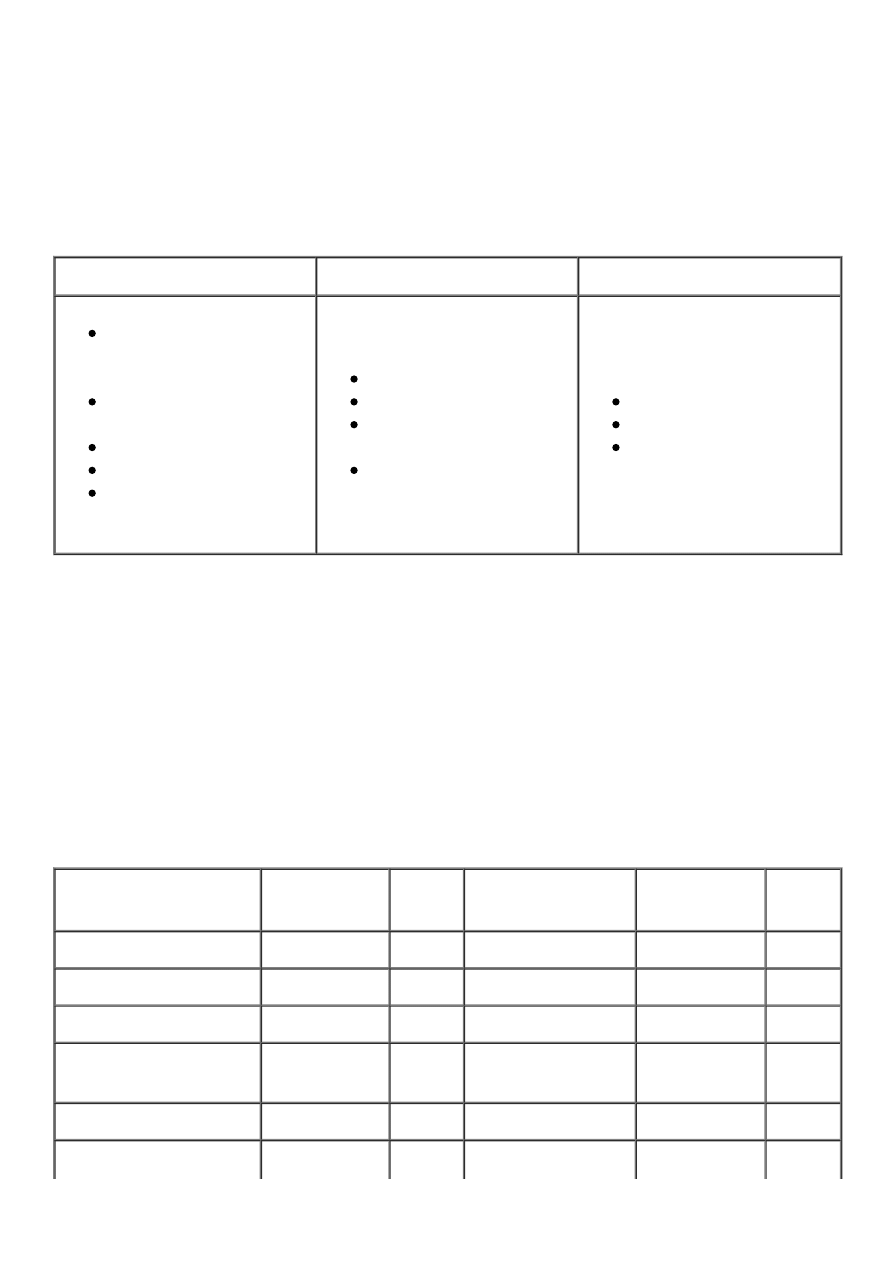
największe znaczenie ma zwiększenie wysiłku fizycznego. W Tabeli 1 przedstawiono wpływ
zmian stylu życia na korektę zaburzeń lipidowych.
.
Tabela 1. Zalecane zmiany stylu życia w zależności od rodzaju zaburzeń lipidowych.
Podwyższone LDLC
Podwyższone TG
Małe HDLC
↓ nasyconych kwasów
tłuszczowych
i
izomerów „trans”
↓
cholesterolu
pokarmowego
↓ masy ciała
błonnik
sterole
i
stanole
roślinne
↓ masy ciała
unikanie alkoholu
↓ węglowodanów łatwo
przyswajalnych
↑ wysiłku fizycznego
↑ wysiłku fizycznego
masy ciała
zaprzestanie palenia
Dla zobrazowania, jakie produkty żywnościowe należy wybierać, a jakich unikać podano
zawartość nasyconych kwasów tłuszczowych w przykładowych produktach, biorą pod
uwagę ich ilości zalecane dla dziennego spożycia.
Leczenie niefarmakologiczne 3
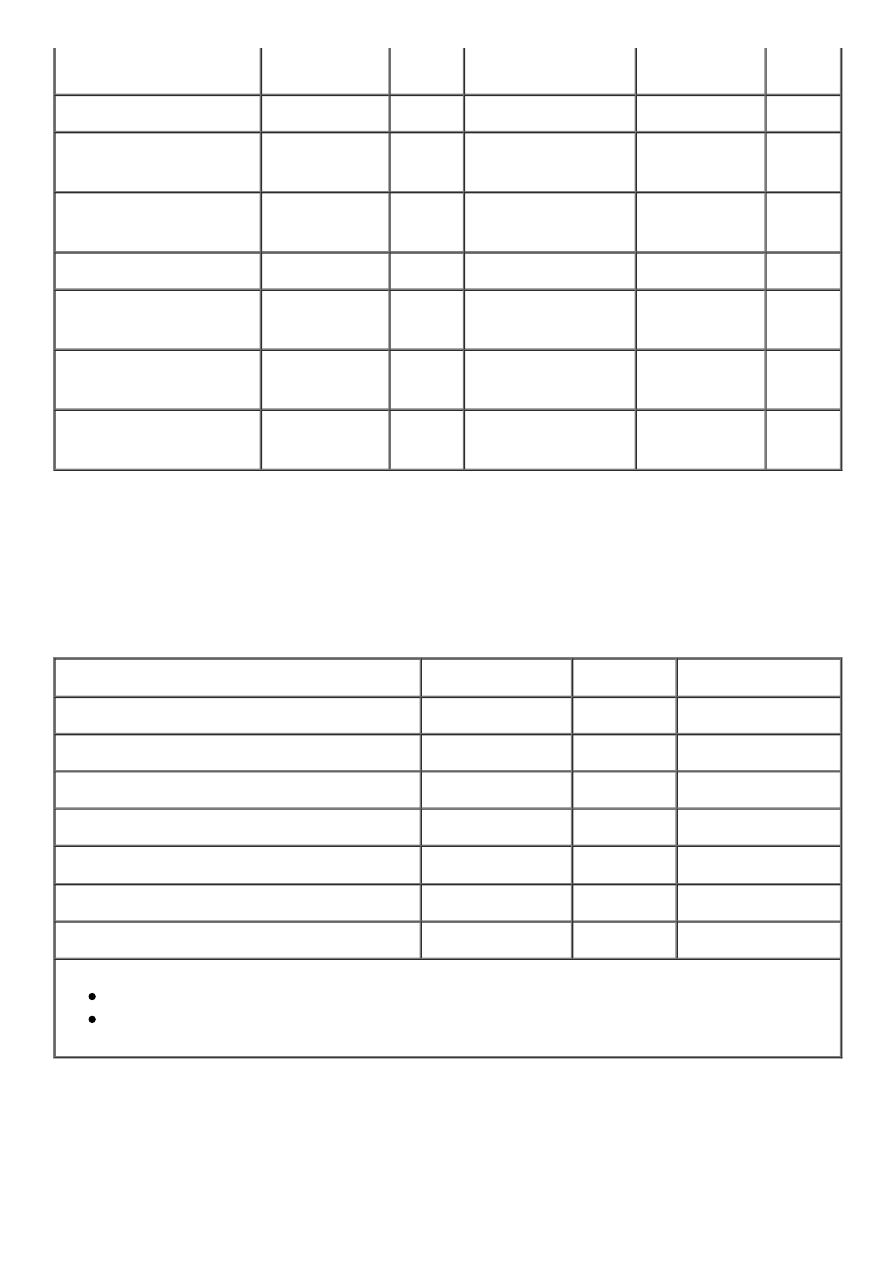
Tabela 2. Zawartość nasyconych kwasów tłuszczowych (NKT) w porcjach wybranych
produktów spożywczych (H. Kunachowicz i wsp. Tabele składu i wartości odżywczej
produktów. PZWL 2005)
Produkt
Ilość (ml lub
g)
NKT
(g)
Produkt
Ilość (ml lub
g)
NKT
(g)
mleko
.
.
morszczuk
100
0,3
0,5% tł.
500
1,6
mintaj
100
0,1
1,5% tł.
500
4,8
pasztetowa
50
6,2
3,2% tł.
500
9,6
parówki
popularne
50
5,8
masło
25
13,7
salceson włoski
50
5,7
margaryna
miękka
03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
8/18
60% tł.
25
3,4
baleron gotowany 50
3,5
smalec
30
14,0
szynka
50
3,2
słonina
50
13,8
polędwica
sopocka
50
1,6
olej rzepakowy
30
2,1
polędwica
z
indyka
50
0,6
wieprzowa łopatka
100
7,6
ser tylżycki tłusty
50
8,3
wołowa polędwica
100
1,7
ser
edamski
topiony
50
4,0
cielęcina udziec
100
1,2
ser
twarogowy
tłusty
50
3,0
pierś indyka
100
0,2
ser
twarogowy
chudy
50
0,14
.
Jak wynika z badań Instytutu Żywności i Żywienia w Polsce głównym źródłem izomerów
trans nienasyconych kwasów tłuszczowych w diecie są wyroby czekoladowe i wyroby
przemysłu cukierniczego. Zwraca uwagę duża ich zawartość w zupach w proszku i sosach.
Należy wiedzieć, że chociaż w mniejszych ilościach to występują one w żywności typu fast
food i w niektórych twardych margarynach.
Tabela 3. Zawartość izomerów trans nienasyconych kwasów tłuszczowych w produktach
żywnościowych (Mojska H. i wsp., 2006)
Grupa produktów
Liczba prób
NKT (g)
Q1 Q4
Zupy w proszku i sosy
20
18,86
(5,32 ÷ 28,66)
Wyroby przemysłu cukierniczego
15
10,14
(1,23 ÷ 30,36)
Wyroby czekoladowe
12
7,86
(1,54 ÷ 14,76)
Chipsy ziemniaczane
15
1,75
(0,57 ÷2,03)
Fast foods*
15
1,56
(0,31 ÷ 9,75)
Margaryny twarde
15
0,14
(0,00 ÷ 20,51)
Margaryny miękkie
15
0,00
(0,00 ÷ 6,45)
* frytki, hamburgery, cheesburgery, pizza
Q1Q4 (kwartyle)
.
Należy podkreślić, iż u chorych z zaburzeniami lipidowymi, u których występuje również
nadwaga i otyłość niezbędne jest obniżenie masy ciała.
Redukcja masy ciała o 10 kg pozwala obniżyć ciśnienie krwi i stężenia glukozy oraz na
poprawienie profilu lipidowego, co wyraża się zmniejszeniem stężenia trójglicerydów o 30%,

03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
9/18
cholesterolu całkowitego o 10%, cholesterolu LDL o 15% oraz zwiększeniem stężenia
cholesterolu HDL o 8%.
Te wyniki wskazują, iż u osób z zaburzeniami lipidowymi oraz z towarzyszącą temu
nadwagą i otyłością w pierwszej kolejności konieczna jest redukcja masy ciała. Jeżeli
mimo schudnięcia pacjenta zaburzenia lipidowe nadal utrzymują się, niezbędne jest
wprowadzenie diety hipolipemicznej (powodującej zmniejszenie stężenia lipidów w osoczu),
a następnie zastosowanie leków.
U osób ze złożonymi zaburzeniami lipidowymi, do których należy aterogenna dyslipidemia i
hiperlipidemia mieszana, oprócz zaleceń obowiązujących w hipercholesterolemii należy
wprowadzić dalsze ograniczenia. Aterogenna dyslipidemia jest często elementem zespołu
metabolicznego, którego istotnym objawem jest otyłość brzuszna, stąd bierze się zalecenie
redukcji masy ciała.
Leczenie niefarmakologiczne 4
W postępowaniu niefarmakologicznym bardzo ważne miejsce zajmuje dieta mająca na celu
utrzymanie małego stężenia cholesterolu LDL lub jego zmniejszenia w razie potrzeby.
Dotyczy to w szczególności hiperlipidemii mieszanej. Dlatego zaleca się spożycie
nasyconych kwasów tłuszczowych <7% ogółu energii, izomerów trans <1% energii, oraz
cholesterolu <200 mg/dzień.
Ograniczeniu podlegają nasycone kwasy tłuszczowe, podczas gdy spożycie tłuszczu
ogółem może być większe (35% ogółu energii). Powinien to być jednak tłuszcz roślinny,
przede wszystkim obfitujący w jednonienasycone kwasy tłuszczowe (olej rzepakowy i
margaryna z tego oleju, olej oliwkowy).
Oczywiste jest, że nie oznacza to diety bogato tłuszczowej w sensie ilościowym, tylko
większy udział procentowy tłuszczu w diecie o odpowiedniej dla pacjenta wartości
energetycznej. Dopuszczenie większego odsetkowego udziału tłuszczu w diecie pacjentów
z aterogenną dyslipidemią wynika z potrzeby ograniczenia spożycia węglowodanów, które
jak wiadomo nasilają hipertrójglicerydemię i zmniejszają stężenie cholesterolu HDL.
Dodatkowa korzyść wynika ze zmniejszania hiperinsulinemii i hiperglikemii, ważnych
elementów zespołu metabolicznego, którego częścią często jest także aterogenna
dyslipidemia. Pacjenci z aterogenną dyslipidemią powinni unikać alkoholu (nasilanie
hipertrójglicerydemii). Ponadto uzasadnienie, zwłaszcza w przypadku stężenia
trójglicerydów ≥500 mg/dL, ma stosowanie suplementów oleju rybnego.
Modelowym przykładem diety zalecanej w profilaktyce chorób sercowonaczyniowych jest
dieta śródziemnomorska. W jej skład wchodzą: warzywa, owoce, produkty zbożowe,
nasiona roślin strączkowych, orzechy, oliwa z oliwek, którą w naszych warunkach można
zastąpić olejem rzepakowym (traktowanym jako główne źródło tłuszczów dodawanych), oraz
produkty mleczne.
Ponadto dieta ta zawiera ryby (2 posiłki tygodniowo), drób (23 razy w tygodniu), ziemniaki.
Mięso czerwone spożywane jest kilka razy w miesiącu.
Korzystne działanie diety śródziemnomorskiej wiąże się z tym, iż jest ona bogatym źródłem
witamin przeciwutleniających (witamina E, betakaroten, witamina C), flawonoidów,
składników mineralnych (wapń, potas), błonnika oraz kwasów tłuszczowych
jednonienasyconych (oliwa z oliwek) i kwasów tłuszczowych omega3 (ryby). Podkreślić
03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
10/18
należy ponadto, że ten model żywienia charakteryzuje się małym spożyciem nasyconych
kwasów tłuszczowych.
Stosowanie diety śródziemnomorskiej wpływa korzystnie na profil lipidów, stężenie glukozy i
ciśnienie krwi. Prowadzi to do ewidentnych korzyści klinicznych, co wykazano w badaniu
Lyon Study. Po 27 miesiącach stosowania diety śródziemnomorskiej u ludzi po zawale serca
zaobserwowano redukcję zgonów ogółem o 70%, zgonów sercowych o 76% i zawałów
serca bez zgonu o 70%, w porównaniu z dietą kontrolną charakterystyczną dla krajów
zachodnich. Pomimo osiągania tak dobrych wyników badanie zaplanowane na 5 lat zostało
przerwane po 27 miesiącach ze względów etycznych, gdyż nie można było dłużej
kontynuować „szkodliwej” diety kontrolnej.
Jak wskazuje nazwa, dieta śródziemnomorska jest charakterystyczna dla krajów basenu
Morza Śródziemnego. Zagrożenie chorobami sercowonaczyniowymi w tych krajach jest
znacznie mniejsze niż w krajach Europy Północnej i Wschodniej.
Jak wynika z innych badań klinicznych zastosowanie diety bogatej w warzywa (Indian
Study), bądź bogatej w ryby (DART Study) przynosi ewidentne korzyści w postaci redukcji
zgonów ogółem, zgonów sercowych i zawałów serca.
.
Tabela 4. Efekty badań klinicznych z zastosowaniem diety (prewencja wtórna)
Incydenty
DART
Indian Study
Lyon Study
Wszystkie zgony
29%
45%
70%
Zgony sercowe
33%
42%
76%
Zawały serca bez
zgonu
38%
70%
Farmakoterapia zaburzeń lipidowych 1
Do leków obecnie stosowanych w praktyce klinicznej zaliczamy statyny (główna grupa leków
hipolipemizujących) oraz fibraty, kwas nikotynowy i ezytymib. Dobór leku zależy od rodzaju
zaburzeń lipidowych.
.
Tabela 5. Farmakoterapia w kontroli zaburzeń lipidowych
↓ LDLC
↓ TG
↑ HDLC
statyny
inhibitory
wchłaniania
cholesterolu (ezetymib)
żywice
fibraty
kwas nikotynowy
fibraty
kwas nikotynowy
statyny
suplement oleju rybnego
24 g/dzień
kwas
nikotynowy
fibraty
estrogeny*
statyny
*zwiększają stężenie TG

03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
11/18
.
Lekami zmniejszającymi najskuteczniej stężenie cholesterolu LDL, jak dobrze wiadomo,
pozostają statyny (atorwastatyna, fluwastatyna, lowastatyna, simwastatyna, prowastatyna,
rosuwastatyna). Do leków redukujących stężenie tego lipidu, w słabszym stopniu niż statyny,
należą inhibitory wchłaniania cholesterolu i żywice jonowymienne. Statyny hamują syntezę
cholesterolu w wątrobie, inhibitory wchłaniania cholesterolu, hamują wchłanianie
cholesterolu pokarmowego i wydzielonego z żółcią do jelit, zaś żywice jonowymienne
przerywają wchłanianie zwrotne kwasów żółciowych. Ostatecznym efektem działania tych
wszystkich leków jest nasilenie aktywności receptorów LDL na hepatocytach, a tym samym
katabolizmu tych lipoprotein.
Przedstawicielem inhibitorów wchłaniania cholesterolu jest ezetymib, a żywic
jonowymiennych, cholestyramina, kolestipol i kolesewelam. Ezetymib i żywice
jonowymienne
pełnią
funkcję
pomocniczą
wspierając
statynę
w
działaniu
hipocholesterolemicznym. Pozwala to u pacjentów z dużym i bardzo dużym ryzykiem łatwiej
osiągnąć niskie docelowe stężenie cholesterolu LDL. Żywice są ponadto w monoterapii
stosowane u dzieci z hipercholesterolemią rodzinną.
Do leków umiarkowanie redukujących stężenie cholesterolu LDL należą fibraty (zwłaszcza
fenofibrat) i kwas nikotynowy.
Stężenie trójglicerydów najsilniej zmniejszają fibraty i kwas nikotynowy. Leki te również
zwiększają stężenie cholesterolu HDL. W hipertrójglicerydemii, szczególnie ze znacznie
zwiększonym stężeniem trójglicerydów (≥500 mg/dl), zastosowanie mają także suplementy
oleju rybnego w dawce farmakologicznej 24 g/dzień, w skojarzeniu z fibratami. Skuteczność
poszczególnych leków hipolipemizujących zależy od rodzaju leku i jego dawki, co
przedstawiono poniżej w tabelach.
.
Tabela 6. Wpływ farmakoterapii i innych związków o działaniu hipolipemizującym na lipidy
(wg H.Bays i E.A.Stein, 2003)
Leki
LDLC (zmiana %)
TG (zmiana %)
HDLC (zmiana %)
Statyny
↓ 18 55
↓ 7 30
↑ 5 15
Ezetymib
↓ 17 22
↓ 4 11
↑ 2 5
Żywice
↓ 15 30
0 ↑
↑ 3 5
Fitosterole/ fitostanole
↓ 10 15
0 ↑
0 ↑
Fibraty*
↓ 5 20
↓ 20 50
↑ 10 20
Kwas nikotynowy**
↓ 5 25
↓ 20 50
↑ 15 3
* mogą
LDLC u niektórych pacjentów z HTG
**zmniejsza także Lp(a)
.
Tabela7. Porównanie wpływu różnych statyn na spadek stężenia LDLC (%) u pacjentów z
hipercholesterolemią. Badanie STELLAR* (wg P.H.Jones, M.H.Davidson, E.A.Stein i wsp.,
2003)
Dawka statyny mg/dzień
Rosuwa
Atorwa
Simwa
Prawa
10
45,8
36,8
28,3
20,1

03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
12/18
20
52,4
42,6
35,0
24,4
40
55,0
47,8
38,8
29,7
80
brak danych
51,1
45,8
brak danych
*6 tygodni leczenia; LDLchol ≥160 mg/dL do 250 mg/dL, TG < 400 mg/dL
Farmakoterapia zaburzeń lipidowych 2
Efekt hipolipemizujący statyn zależy od rodzaju statyny i stosowanej dawki. Jak widać poza
fibratami i kwasem nikotynowym, które silnie zmniejszają stężenie trójglicerydów, również
statyny mają pewne działanie pod tym względem. Statyny najwięcej obniżające stężenie
cholesterolu LDL, również najlepiej zmniejszają stężenie trójglicerydów.
Uwagę zwraca umiarkowana redukcja stężenia cholesterolu LDL pod wpływem
przyjmowania steroli lub stanoli roślinnych w ilości 2 g/dzień. Związki te jednak nie mogą być
przyjmowane samodzielnie, jako leki, tylko w produktach żywnościowych, takich jak
margaryny lub jogurty. Należy dodać, że nie można łączyć stosowania ezetymibu z
przyjmowaniem steroli lub stanoli roślinnych.
Jak wspomniano poprzednio stężenie cholesterolu HDL zwiększają fibraty i w większym
stopniu kwas nikotynowy. Ten ostatni lek w formie krystalicznej jest rzadko stosowany, ze
względu a nieprzyjemne objawy uboczne, wynikające z rozszerzenia naczyń skóry (uczucie
gorąca, zaczerwienienie skóry twarzy, szyi). Za granicą dostępny jest wolnouwalniający się
kwas nikotynowy, a tym samym o ograniczonych objawach ubocznych (do stosowania raz na
dzień), a w badaniach klinicznych jest preparat kwasu nikotynowego skojarzony ze
związkiem o nazwie laropiprant, który blokuje wiązanie się prostaglandyny D2 (PGD2) z
receptorami w skórze i tym samym efekt naczynioworozkurczowy. Spośród statyn,
przebadanych w STELLAR pod względem wpływu na stężenie cholesterolu LDL,
najsilniejsza okazała się rosuwastatyna, lek w Polsce nie zarejestrowany. Kolejne miejsce
zajęła atorwastatyna.
Godne zauważenia jest, że podwojenie dawki statyny nie podwaja efektu
hipolipemizującego. Uznaje się tzw. „regułę 6”, która oznacza uzyskanie dodatkowego
spadku cholesterolu LDL o 6%.
Farmakoterapia zaburzeń lipidowych 3
Leki hipolipemizujące są lekami zarówno skutecznymi jak i bezpiecznymi. Jednakże należy
pamiętać, że mogą wywoływać objawy uboczne, które zmuszają do zmniejszenia dawki
leku, bądź przerwania terapii.
Objawy uboczne, które mogą towarzyszyć terapii statynami to:
bóle brzucha, wzdęcia, nudności, biegunka lub zaparcie, wysypka,

03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
13/18
wzrost stężenia ALAT i/lub AsPAT w surowicy,
bóle lub osłabienie mięśni z lub bez wzrostu CK,
wzrost stężenia CK z lub bez bólów mięśni,
miopatia (objawy mięśniowe i wzrost CK >10krotności górnej granicy normy)*,
rabdomioliza z niewydolnością nerek,
neuropatia obwodowa (parestezje),
proteinuria (znaczenie kliniczne nieznane).
Statyny wchodzą w interakcje z wieloma lekami nasilając ryzyko miopatii. Wynika to ze
wspólnej drogi metabolicznej w wątrobie, za pośrednictwem enzymu 3A4 cytochromu 450.
W rezultacie tego wzrasta znacznie stężenie statyny, co zwiększa ryzyko miopatii. W tym
miejscu należy wspomnieć o soku grejpfrutowym, który również powoduje wzrost stężenia
statyny i nasila niebezpieczeństwo miopatii.
Poniżej przedstawiono wykaz leków, z którymi statyny mogą wchodzić w interakcję nasilając
ryzyko miopatii:
fibraty (szczególnie gemfibrozyl),
kwas nikotynowy,
warfaryna,
digoksyna,
werapamil,
amiodaron,
azolowe leki p/grzybicze,
erytromycyna, azytromycyna, klarytromycyna,
inhibitory proteazy HIV,
nefazodon,
fluoksetyna,
leki p/histaminowe,
benzodypiny.
Najpoważniejszym powikłaniem leczenia statyną jest miopatia, która może przejść w
rabdomiolizę z mioglobinurią i niewydolnością nerek. Generalnie nie ma zalecenia,
odnośnie potrzeby oznaczenia poziomu kinazy kreatyny (CK) przed wdrożeniem statyny.
Uważa się, że aktywność tego enzymu należy zbadać, jeśli podczas leczenia wystąpią
objawy mięśniowe (tkliwość, bolesność, sztywność mięśni). Częstość miopatii wśród
leczonych statynami ocenia się na 1 przypadek na 1000 pacjentów.
Farmakoterapia zaburzeń lipidowych 4
Zwiększone stężenie aminotransferazy alaninowej i/lub asparaginowej, ale poniżej 3xGGN
(górna granica normy), nie jest przeciwwskazaniem do wdrożenia terapii statyną. Należy
jednak w czasie leczenia monitorować ten parametr bezpieczeństwa. Statyny zwiększają
stężenie aminotransferaz. Im większa dawka leku tym większe prawdopodobieństwo tego
zjawiska. Nie ma zgodności, co do tego, że wzrost stężenia enzymów wątrobowych jest
objawem hepatotoksyczności. Hepatolodzy uważają, że niekoniecznie. Tym niemniej jeśli
ten wzrost przekracza trzykrotność GGN, leczenie należy przerwać (1% leczonych statyną).

03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
14/18
Schemat postępowania mający na celu zmniejszenie ryzyka powikłań po statynach podano
poniżej.
.
Tabela 8. Bezpieczeństwo leczenia statynami.
Przeciwwskazania
ciężkie uszkodzenie wątroby, wiek rozrodczy bez stosowania antykoncepcji, ciąża,
laktacja, nadużywanie alkoholu
UWAGA! Przed leczeniem ocenić ALAT, ASPAT. W niektórych zaleceniach także TSH i
funkcja nerek.
Jeśli ALAT lub ASPAT > 3 x GGN (około 1% leczonych) przerwać leczenie.
Jeśli wystąpią objawy mięśniowe (bóle, sztywność, skurcze) ocenić CK:
CK > 5 x GGN zmniejszyć dawkę
CK> 10x GGN przerwać leczenie (miopatia dotyczy 0,1 – 0,2% leczonych)
Jeśli konieczne są azolowe leki p/grzybicze czasowo przerwać leczenie statyną lub
zmniejszyć dawkę.
Jeśli konieczny jest antybiotyk makrolidowy czasowo przerwać leczenie statyną lub
zmniejszyć. dawkę
GGN górna granica normy
.
Statyny są lekami, które dowiodły w wielu dużych badaniach klinicznych skuteczność w
zmniejszaniu ryzyka incydentów wieńcowych, zgonów wieńcowych, zgonów ogółem,
udarów mózgu i zabiegów rewaskularyzacyjnych. Skuteczność statyn wykazano u obu płci,
niezależnie od wieku, u chorych na cukrzycę oraz na nadciśnienie tętnicze. Na podkreślenie
zasługuje zmniejszanie ryzyka chorób sercowonaczyniowych niezależnie od wyjściowego
stężenia cholesterolu LDL. Korzyść odnoszą pacjenci po incydencie sercowonaczyniowym
(prewencja wtórna) i bez objawowej choroby sercowonaczyniowej (prewencja pierwotna).
Powinny być podawane również w ostrym zespole wieńcowym, nie tylko ze względu na efekt
hipolipemizujący, ale także z powodu działania plejotropowego, w tym efekt przeciwzapalny.
Jak wykazano w badaniach angiograficznych statyny hamują progresję miażdżycy tętnic
wieńcowych. Działanie to potwierdza ultrasonografia wewnątrzwieńcowa. Silne statyny,
redukując bardzo znacznie stężenie cholesterolu LDL, zmniejszają objętość blaszek
miażdżycowych, co również wykazano tą metodą. Leki te hamują progresję miażdżycy także
w tętnicach szyjnych, co stwierdzono w badaniach ultrasonograficznych.
Farmakoterapia zaburzeń lipidowych 5
Lekiem niedawno wprowadzonym do terapii hipolipemizującej jest ezetymib. Jak już
uprzednio powiedziano hamuje on wchłanianie cholesterolu pochodzenia pokarmowego i

03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
15/18
zawartego w żółci. Ograniczenie dostępności cholesterolu w wątrobie powoduje wzrost
aktywności receptorów LDL na hepatocytach i w rezultacie zwiększa przyswajanie tych
lipoprotein z osocza. Ezetymib słabiej zmniejsza stężenie cholesterolu LDL niż statyny, ale
bardzo nasila efekt hipolipemizujący tych leków. Podwajając dawkę statyny, jak już
poprzednio wspomniano uzyskuje się spadek stężenia cholesterolu LDL o dodatkowe 6%,
natomiast dodanie ezetymibu do statyny skutkuje dodatkową redukcją tego lipidu o 1824%.
Ezetymib (stosowany w dawce 10 mg/d) znajduje najwłaściwsze zastosowanie w terapii
skojarzonej ze statyną, jako lek wspomagający statynę, u pacjentów z grup dużego i bardzo
dużego ryzyka, którzy nie osiągają docelowego stężenia cholesterolu LDL w wyniku
monoterapii statyną. Terapia ezetymibem jest bezpieczna, jednak opisano pojedyncze
przypadki miopatii. W leczeniu aterogennej dyslipidemii uwzględnia się statyny, fibraty i
kwas nikotynowy. Fibrat lub kwas nikotynowy są odpowiednimi lekami w aterogennej
dyslipidemii, gdyż zmniejszają stężenie trójglicerydów, zwiększają stężenie cholesterolu
HDL i normalizują wielkość i skład cząsteczek LDL. W praktyce klinicznej w Polsce
niedostępny jest preparat wolno uwalniającego się kwasu nikotynowego, wobec czego
stosowany jest wyłącznie fibrat.
W aterogennej dyslipidemii można rozważyć zastosowanie farmakoterapii skojarzonej
(statyna+ fibrat; statyna+kwas nikotynowy) dla normalizacji stężeń wszystkich lipidów.
Jak wspomniano, fibraty zmniejszają stężenie trójglicerydów, zwiększają cholesterolu HDL i
redukują zawartość w osoczu małych gęstych LDL (normalizacja składu i wielkości
cząsteczek tych lipoprotein). Leki te wpływają na stężenie lipidów i lipoprotein osocza
poprzez modyfikację (aktywację lub hamowanie) ekspresji genów biorących udział w
syntezie enzymów i białek kluczowych dla metabolizmu lipoprotein. W modyfikacji ekspresji
genów pośredniczą specyficzne czynniki transkrypcyjne zwane jądrowymi receptorami,
aktywowanymi przez proliferatory peroksysomów α (PPAR α, peroxisome proliferator
activated receptor α). Fibraty są proliferatorami peroksyzomów, wiążąc się z receptorami
jądrowymi powodują ich aktywację. Aktywowane PPAR α łączą się ze specyficznymi
miejscami genów, regululąc ich ekspresję, a tym samym produkcję enzymów i białek
kluczowych dla metabolizmu lipidów i lipoprotein.
Farmakoterapia zaburzeń lipidowych 6
Fibraty zmniejszają ryzyko incydentów sercowonaczyniowych, w tym wieńcowych
(gemfibrozil – prewencja pierwotna i wtórna) brak jest jednak dowodów na redukcję ryzyka
zgonów z tego powodu. Najszerzej obecnie stosowany spośród fibratów fenofibrat
mikronizowany spowodował po 5 latach w badaniu FIELD spadek incydentów sercowo
naczyniowych i wieńcowych u chorych na cukrzycę bez choroby sercowonaczyniowej
(prewencja pierwotna). Nie było redukcji zgonów wieńcowych. Leczenie zahamowało postęp
mikroangiopatii (zwolnienie progresji albuminurii oraz retinopatii). Z drugiej strony wiadomo
jednak, że fibraty zwiększają stężenie kreatyniny, tak było też w FIELD. Fibraty hamują
progresję miażdżycy tętnic wieńcowych. Wykazano to w badaniach angiograficznych, w
odniesieniu do gemfibrozylu i fenofibratu mikronizowanego.
Podczas stosowania fibratów mogą wystąpić objawy uboczne. Są to:
dyspepsja, bóle brzucha, biegunka, wysypka, wypadanie włosów, osłabienie libido,
wysycenie żółci cholesterolem, wzrost ryzyka kamicy żółciowej (12% leczonych),
03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
16/18
wzrost stężenia kreatyniny,
wzrost stężenia ALAT,
rzadko wzrost stężenia CK i możliwość miopatii,
rzadko niedokrwistość, spadek liczby leukocytów i płytek krwi,
upośledzenie wiązania z białkami doustnych antykoagulantów, wymagające redukcji ich
dawki.
Aby zmniejszyć ryzyko powikłań należy pamiętać o przeciwwskazaniach do stosowania
fibratów, co podano niżej.
.
Tabela 9. Bezpieczeństwo leczenia fibratami.
Przeciwwskazania
Ciężkie uszkodzenie wątroby lub nerek, ciąża
Kamica żółciowa (względne)
UWAGA! Przed leczeniem ocenić ALAT, ASPAT i kreatyninę.
Jeśli upośledzona funkcja nerek rozpocząć leczenie od małej dawki.
Jeśli wystąpią objawy mięśniowe ocenić CK.
Jeśli leczenie przeciwkrzepliwe ściśle monitorować INR i w razie potrzeby
zmniejszyć dawkę antykoagulantu
Farmakoterapia zaburzeń lipidowych 7
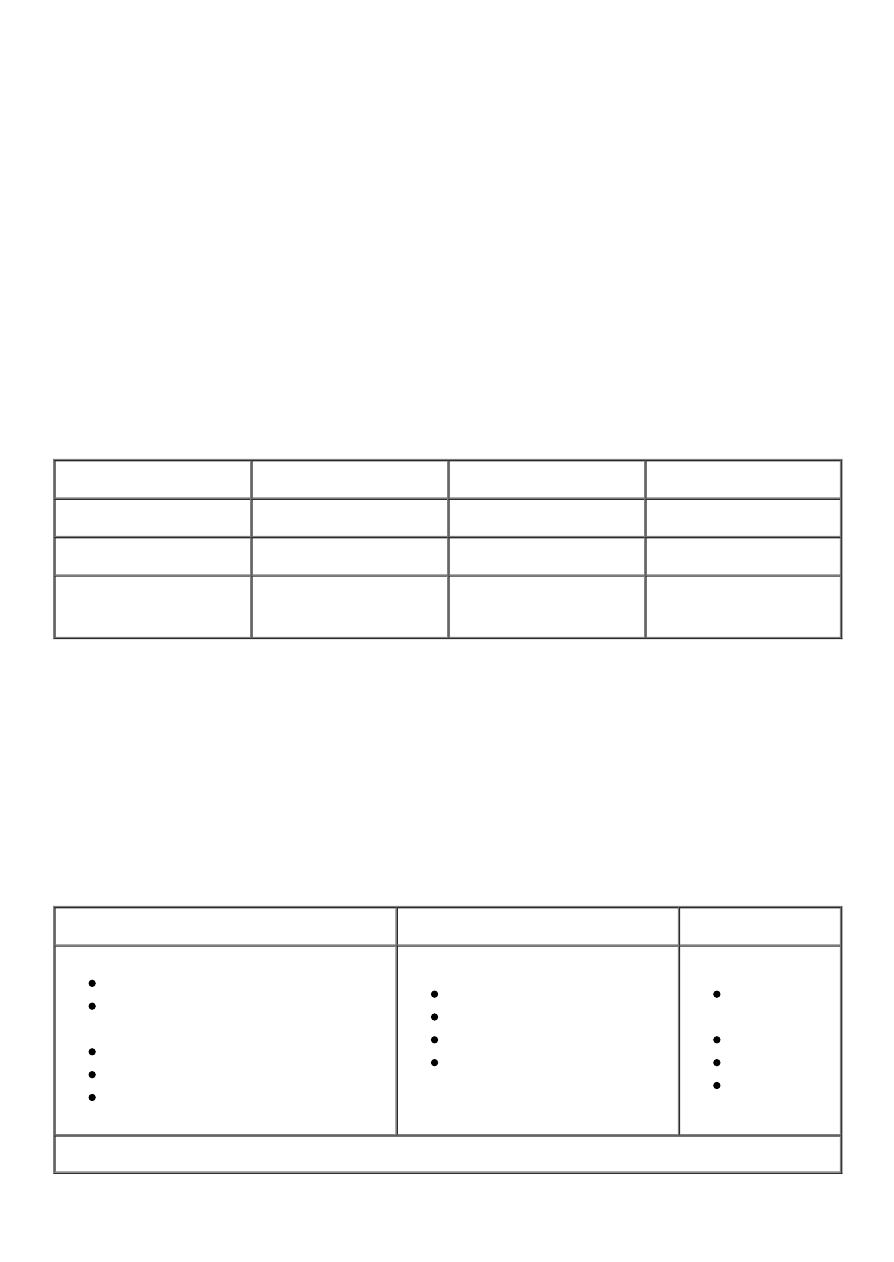
W ciężkich przypadkach hipercholesterolemii oraz w aterogennej dyslipidemii, bądź w
zespole chylomikronemii zastosowanie jednego leku hipolipemizującego może być
niewystarczające. Można wtedy rozważyć dwa leki, co przedstawiono poniżej.
.
Tabela 10. Terapia skojarzona w zaburzeniach lipidowych.
Hipercholesterolemia
Aterogenna dyslipidemia
Zespół chylomikronemii
statyna + ezetymib
(jeśli
statyna
nie
spowodowała ↓ LDLC
do wartości docelowej)
statyna + żywica (jak
wyżej)
statyna + fibrat
statyna
+
kwas
nikotynowy
fibrat + olej rybny (24
g/dzień)
Terapia skojarzona w aterogennej dyslipidemii stwarza możliwość dobrej korekty wszystkich
nieprawidłowości w stężeniu lipidów. Przykładem tego jest rycina przedstawiająca efekty
rocznego stosowania razem fenofibratu 200M i simwastatyny (20 g/d) w dwóch modelach

03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
17/18
leczenia:
dodanie simwastatyny do fenofibratu po rocznym stosowaniu monoterapii fenofibratem,
dodanie fenofibratu do simwastatyny po rocznym stosowaniu monoterapii
simwastatyną.
Jak widać dodanie simwastatyny do fenofibratu spowodowało dodatkową redukcję
cholesterolu całkowitego, cholesterolu LDL i trójglicerydów, w porównaniu z monoterapią
fenofibratem, odpowiednio o 14,5%, 23,4% i 19,2%, zaś dodanie fenofibratu do simwastatyny
stężeń tych lipidów odpowiednio o 15%, 20,3% i 30,9%. Ryc. 1. Efekt stosowania terapii
skojarzonej (fenofibrat mikronizowany plus simwastatyna w hiperlipidemii mieszanej (wg L.
KłosiewiczLatoszek i in., Kardiol. Pol. 2003) Należy jednak pamiętać, iż terapia skojarzona
w porównaniu ze stosowaniem jednego leku może nasilać ryzyko wystąpienia objawów
niepożądanych – uszkodzenia wątroby, a zwłaszcza miopatii. Dlatego też terapia skojarzona
powinna być prowadzona tylko u osób z wysokim ryzykiem i współpracujących z lekarzem.
Należy stosować małe dawki obu leków, to jest statyny i fibratu. Przeciwwskazania do
farmakoterapii skojarzonej statyną i fibratem przedstawiono poniżej: • starszy wiek (>70 lat) •
upośledzona czynność nerek (kreatyninemia >2,0 mg/dl) • upośledzona czynność wątroby •
niedoczynność tarczycy • przyjmowanie wielu leków • długotrwała terapia antybiotykiem
makrolidowym • leczenie cyklosporyną lub azolowym lekiem przeciwgrzybiczym Uwaga!
Przy stosowaniu obu leków: statyna – wieczorem, a fibrat – rano lub naprzemiennie co 2.
dzień.
Wskazania do stosowania leków hipolipemizujących
Jasne jest, że statyny są najważniejszymi lekami dla osiągnięcia docelowego stężenia
cholesterolu LDL. Spadek stężenia tego lipidu jest wymiernym parametrem skuteczności
tych leków. Jednak ich wartość polega głównie na redukcji incydentów wieńcowych, udarów
mózgu, zgonów wieńcowych i zgonów ogółem, co oznacza przedłużenie życia. Leki te zatem
wypełniają do końca wymagania medycyny opartej na faktach. Skuteczność statyn pod tym
względem jest największa u pacjentów z dużym ryzykiem (prewencja wtórna). Zależy ona
także od osiągniętego stężenia cholesterolu LDL i od wielkości spadku tego stężenia (im
niżej tym lepiej im większa redukcja tym lepiej). Istnieją jednak pewne granice poniżej,
których nie powinno się zmniejszać stężenia cholesterolu LDL. Taką wartością w opinii
ekspertów amerykańskich jest 60 mg/dl. Należy jednak dodać, że problem ten nie jest do
końca wyjaśniony. Najlepiej udokumentowaną skuteczność w wielu dużych badaniach
klinicznych, w odniesieniu do zmniejszania ryzyka, mają simwastatyna i atorwastatyna.
Aktualnie prowadzonych jest wiele badań z najsilniejszą rosuwastatyną. Wiadomo już, że
lek ten powoduje regresję miażdżycy tętnic wieńcowych, co wyraża się zmniejszeniem
objętości blaszki miażdżycowej. Jaką dawkę statyny należy zastosować u konkretnego
pacjenta? Taką, która pozwoli osiągnąć docelowe stężenie cholesterolu LDL, wyznaczone
przez indywidualne ryzyko. Nie u wszystkich pacjentów udaje się osiągnąć docelowe
stężenie LDL przy pomocy samej statyny, nie zawsze też można stosować maksymalną
dawkę leku. Dlatego w przypadkach dużego i bardzo dużego ryzyka, gdzie wymagania, co
do docelowego stężenia tego lipidu są duże, można do statyny dodać ezetymib. Jak już
powiedziano, lekami zwiększającymi stężenie cholesterolu HDL i redukującymi trójglicerydy

03.04.2013
Do druku: Postępowanie w zaburzeniach gospodarki lipidowej
www.docedu.klrwp.pl/print.php?id=163
18/18
są fibraty i kwas nikotynowy. Należy mieć na uwadze, że redukcja ryzyka sercowo
naczyniowego, w wyniku leczenia statynami, jest ograniczona do około 3035%. Zwolennicy
farmakoterapii skojarzonej statyną i fibratem lub statyną i kwasem nikotynowym sugerują, że
w aterogennej dyslipidemii działanie nie tylko w kierunku spadku stężenia cholesterolu LDL,
ale także wzrostu małego stężenia cholesterolu HDL może przynieść dodatkową korzyść w
postaci większej redukcji ryzyka. Szczególnie byłoby to pożądane u pacjentów z dużym
ryzykiem. Odpowiednie badanie kliniczne (ACCORD) z simwastatyną i fenofibratem, w
porównaniu z monoterapią simwastatyną, jest w toku realizacji. Schemat obejmujący
wskazania do stosowania leków wpływających na stężenie lipidów można przedstawić
następująco. Tabela 11. Wskazania do leków hipolipemizujących. Statyny Ezetymib Fibraty
Kwas nikotynowy • Leki pierwszego rzutu dla osiągnięcia docelowego LDLC (ChNS,
choroby innych tętnic, cukrzyca, duże ryzyko z innych przyczyn) • Lek uzupełniający statynę
dla osiągnięcia docelowego stężenia LDLC • Leki do zwiększenia HDLC i redukcji
trójglicerydów w aterogennej dyslipidemii
monoterapia, jeśli LDLC odpowiada
zaleceniom
ze statyną, jeśli LDLC powyżej zalecanej wartości (ChNS, choroby innych
tętnic, cukrzyca, duże ryzyko z innych przyczyn)
Wyszukiwarka
Podobne podstrony:
Zaburzenia gospodarki lipidowej
1. Zaburzenia gospodarki lipidowej, FARMAKOLOGIA
FARMAKOLOGIA, 42 Leki w zaburzeniach gospodarki lipidowej
07 Patofizjologia zaburzeń gospodarki lipidowej zespół metaboliczny
genetyczne zaburzenia gospodarki lipidowej
zaburzenia gospodarki lipidowej referat
zaburzenia gospodarki lipidowej
W08 Patofizjologia zaburzeń gospodarki węglowodanowej
Patomechanizmy zaburzeń gospodarki wapniowo fosforanowej; osteoporoza
Diagnostyka laboratoryjna zaburzen gospodarki lek 2010
Zaburzenia gospodarki węglowodanowej u kobiet w ciąży
Zaburzenia gospodarki wodno-elektrolitowej, Prywatne(1)
Gospodarka lipidowa i potem już tylko zaliczenie
Choroby przytarczyc i zaburzenia gospodarki wapniowo fosforanowej
5 ZABURZENIA GOSPODARKI WODNO ELEKTROLITOWEJ
Zaburzenia gospodarki wodno elektrolitowej, Patofizjologia, Ćwiczenia 1-2 (zapalenie, wstrząs, RKZ)
więcej podobnych podstron