1. Równanie stanu gazu doskonałego.
![]()
2. Równanie van der Waalsa.
![]()
a,b-korekty na siły międzycząsteczkowe
3. Definicja pracy.
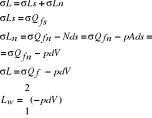
4. Entalpia i energia wewnętrzna.
Entalpia jest to funkcja stanu i ma
różniczkę zupełną.
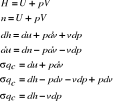
5. Termodynamiczne równania stanu.
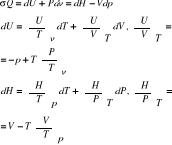
a) gaz doskonały
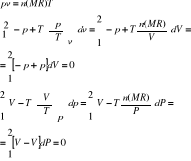
b) gaz van der Waalsa
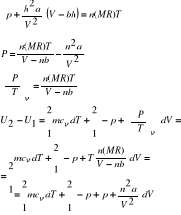
6. Ciepło całkowite.
7. I zasada dynamiki.
a) układ adiabatyczny
L1-2=U(p2,V2)-U(p1,V1) - energia wew.
![]()
b) układ nie adiabatyczny
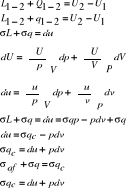
8.Ciepło właściwe.
Współczynnik, który informuje o
ile należy zwiększyć temp. danego
ciała, aby jego temp. Zwiększyła
się o jeden stopień.
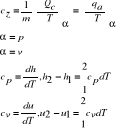
dla gazu doskonałego
cp=f(T,p)
cv=f(T,v)
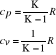
ciepło właściwe przy stałym ciśnieniu
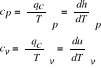
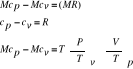
9. Roztwory gazów doskonałych.
10. Liczba postępu reakcji.
![]()
dni - (dn - liczba moli) nieskończenie
mała zmiana liczby moli reagenta,
i - numer reagenta,
ν - współczynnik stechiometryczny
11. Ciepło reakcji.
Ilość ciepła wymienionego między
układem, a otoczeniem w czasie
przebytego izotermiczno-izochorycznej
reakcji, w której liczba postępu zmienia
się o jedność jest równa różnicy energii
wew. układu w stanie końcowym
(produkty)- minus i w stanie początkowym
(substraty reakcji).
a) izochoryczn-izotermiczna: dT=0, dV=0
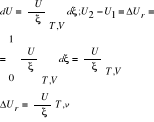
b) izobaryczno-izotermiczna, dP=0,dT=0
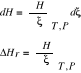
12. Prawo Hessa.
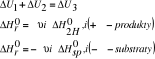
Ciepło tworzenia - to ciepło reakcji syntezy
1 mola danego związku pod ciśnieniem
1 atm. Fizycznej z pierwiastków w najtwardszej
postaci alotropowej w danych warunkach
ciśnienia i temp. Ciepło tworzenia pierwiastka
chemicznego w najtwardszej, w danych
warunkach odmianie fazowej jest równe 0.
Ciepło spalania - to ciepło reakcji spalania w
tlenie 1 mola związku przy ciśnieniu 1 atm. Fiz.
(efektem musi być CO2, H20, SO2, N2).
13. Prawo Kirchhoffa.
![]()
T=298K
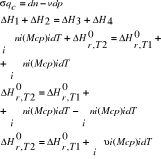
a) wpływ temperatury na ciepło reakcji
![]()
b) wpływ ciśnienia
14. II zasada termodynamiki
Cel II zasady:
-optymalizacja procesów termodynamiki
-znajduje rozwiązania trudno rozwiązywalne
![]()
dS.=![]()
, dS>0
rys
![]()
- przyrost entropi
![]()
-wartości >0
rys
ds.=![]()
dS.=![]()
dS=![]()
,
dU=![]()
dS=![]()
dH=![]()
dS=![]()
dS=![]()
ds.=![]()
ds.=![]()
ds.=![]()
ds.= ![]()
![]()
![]()
ds.=![]()
ds.=![]()
![]()
![]()
![]()
![]()
15. Entropia standardowa
fun. S![]()
-entropia standardowa
fun. S![]()
-entropia właściwa
S![]()
![]()
Planck - Nerst
T=ok. S(=0)=0
ds.=![]()
ds.=![]()
ds.=![]()
ds.=![]()
![]()
![]()
![]()
[ST=S298+![]()
a)ds.= ![]()
b) ds.=![]()
![]()
a)dG=(![]()
a) dF=(![]()
b) dP=0 , dT=0
dS=(![]()
, ![]()
![]()
dG=(![]()
, ![]()
![]()
a) dV=0 , dT=0
dS=(![]()
, ![]()
![]()
![]()
, ![]()
![]()
G= H -Ts
F=U -Ts
dG=dH-Tds-sdT
dV=dU-Tds-sdT
![]()
![]()
![]()
![]()
![]()
jeżeli:
a)![]()
,to reakcja zachodzi od strony lewej
do prawej (np N![]()
+3H![]()
=2NH![]()
)
b)![]()
, to reakcja zachodzi od strony prawej do lewej
c)![]()
, występuje stan równowagi
d)![]()
, to reakcja zachodzi od strony lewej do prawej
e)![]()
, to reakcja zachodzi od strony prawej do lewej
f)![]()
, występuje stan równowagi
16. Energia swobodna i entalpia swobodna.
H=U+pV
F=U - ST [J]
G=H - ST [J]
dF=dU - sdT - Tds ![]()
du=dF + sdT+Tds
dG=dH - sdT - Tds ![]()
dH=dG+sdT+Tds
ds=![]()
ds=![]()
![]()
Tds=du+pdv , Tds=dF+sdT+Tds+pdv
Tds=dH - vdp , Tds=dG+sdT+Tds - vdp
dF= - sdT - pdV
dG= - sdT+Vdp
Przejmowanien ciepła
Rys
- współczynnik przejmowania ciepła
Q=![]()
, ![]()
17. Potencjał chemiczny
![]()
18. II zasada termodynamiki w odniesieniu
do reakcji chemicznej.
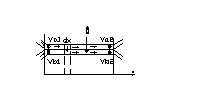
du=![]()
du=![]()
d![]()
ds.=![]()
ds.=![]()
dF=![]()
a)przemiana izotermiczno-izobaryczna
ds.=![]()
dG=![]()
b)izotermiczno - izochoryczna
ds.=![]()
dF=![]()
19. Izobara van`t Hoffa
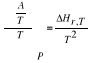
20. Powinowactwo chemiczne
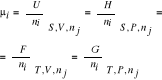
gdzie ![]()
21. Stałe równowagi
![]()
![]()
![]()
22. Równanie Fouriera
![]()
![]()
![]()
gdzie ![]()
- przewodnictwo cieplne [W/m*K]
23. Równanie przewodnictwa cieplnego.
![]()
![]()
- f(x, y, z,![]()
)=const
![]()
-warunki jednoznaczności:
-warunek początkowy T= f(ł0, x, y, z )
-warunek brzegowy Ts= f (ł, x, y, z ) - warunek Dirichleta
![]()
f (![]()
, x, y, z )- warunek Neumana(gradient temperatury)
![]()
, to ![]()
- równanie Laplace`a
24. Przewodzenie ciepła przez przeponę
płaską wielowarstwową
![]()
![]()
![]()
![]()
![]()
![]()
25. Przewodzenie ciepła przez przeponę
płaską wielowarstwową
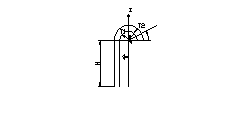
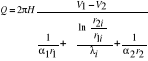
26. Przejmowanie ciepła.
-współczynnik przejmowania ciepła
![]()
27. Przenikanie ciepła (przepona płaska
i wielowarstwowa). rys
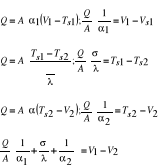
![]()
- dla wielu przepon płaskich
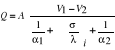
- dla wielu przepon kołowych
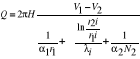
28. Zdolność emisyjna (E).
![]()
Q - strumień (ilość ciepła emitowana na
sekundę na pow. Ciała),
A - powierzchnia
29. Model ciała doskonale czarnego i
doskonale białego (zdolność, odbijania,
pochłaniania i przepuszczania).
Model ciała doskonale czarnego - ciało
to tylko absorbuje, promień stamtąd się
nie wydostaje)
a=1 (V=p=0)
Model ciała doskonale białego
V=1 (a=p=0)
ciało doskonale przeźroczyste
p=1 (a=V=0)
ciało doskonale czarne
![]()
- zdolność emisyjna
c1=0,374[Wm2]
c2=0,01438[m/K]
30. Prawo Viena.
![]()
![]()
![]()
![]()
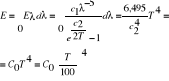
![]()
-stała Boltzmana
Wraz ze zwiększeniem temp. energia przypada
na coraz krótszą falę.
31. Prawo Stefana-Boltzmana.
32. Emisyjność.
Emisyjność jest to zdolność ciała badanego do
zdolności emisyjnej ciała doskonale czarnego.
![]()
33. Wymiana ciapła przez promieniowanie
pomiędzy dwoma równoległymi płytami
o różnych temp.
- promień emisyjny płyty 1
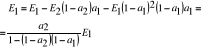
- promień emisyjny płyty 2
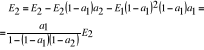
![]()
-czynna wymiana ciepła między dwiema
równoległymi płytami
![]()
34. Ekrany izolujące (wprowadzamy je w celu
wyeliminowania ciepła)..rys
![]()
![]()
![]()
![]()
![]()
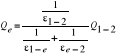
![]()
35. Promieniowanie gazów.
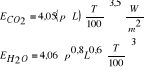
gazy dwuatomowe nie absorbują i nie emitują
36. Liczby podobieństwa.
Teoria podobieństwa
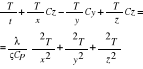
![]()
, ![]()
, ![]()
, ![]()
![]()
, ![]()
, ![]()
![]()
, ![]()
![]()
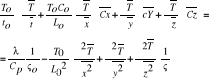
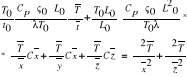
![]()
- liczba Fouriera
![]()
- liczba Pecleta
![]()
- liczba Strouchala
![]()
- liczba Frouole`a
![]()
- liczba Reynoldsa
![]()
- liczba Macha
![]()
- liczba Eulera
![]()
- liczba Prandtla
37. Lokalna i średnia liczba Nusselta.
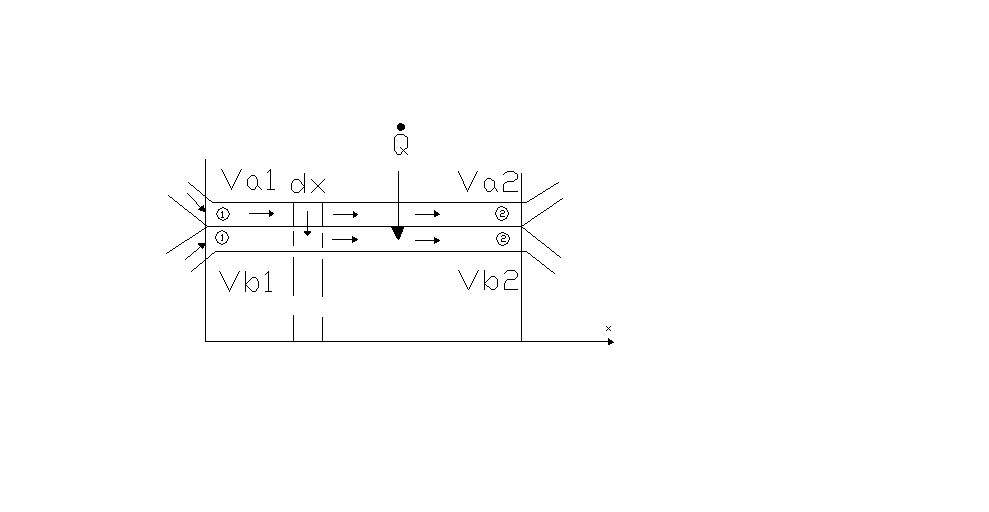
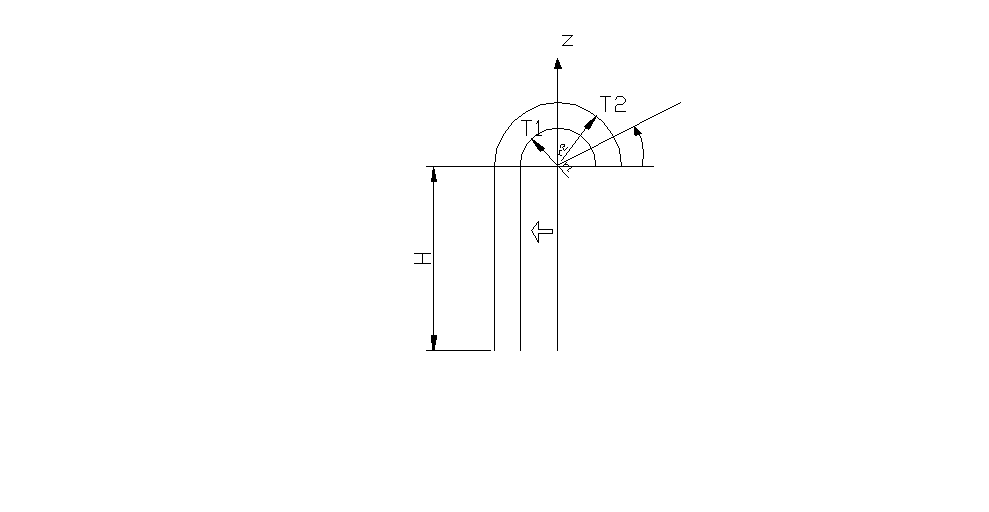
38. Konwekcja wymuszona w przepływie
wzdłuż płyty płaskiej.
![]()
![]()
-liczba krytyczna Reynoldsa
Wyszukiwarka
Podobne podstrony:
16 Kinetyczna teoria gazow i termodynamika I (10)
termodynamika 10
10 termodynamika (2)
10 Zasady termodynamiki 3
10 Zasady termodynamiki
10. termodynamika
10 Zasady termodynamiki
7 Termodynamika 1 SLA 10
10 termodynamikaid 10641
10 Zasady termodynamiki 2
10 termodynamika
10 termodynamika
10 Zasady termodynamiki 2
W5 II zas termod(29 10 15)
10 termodynamika
10 Zasady termodynamiki
10 Zasady termodynamiki 3
10 Metody otrzymywania zwierzat transgenicznychid 10950 ppt
10 dźwigniaid 10541 ppt
więcej podobnych podstron