Rodzaje wiązań
chemicznych
Wiązania chemiczne są to charakterystyczne
oddziaływania występujące pomiędzy
atomami, grupami atomów, jonami lub
cząsteczkami. Wiązania chemiczne powstają
w wyniku oddziaływania, przyjmowania lub
uwspólniania elektronów walencyjnych
reagujących ze sobą atomów.
Każdy atom pierwiastka składa
się z jądra atomowego oraz
elektronów znajdujących się na
tzw. powłokach elektronowych
wokół jądra. W tworzeniu
wiązania bierze udział głównie
ostatnia powłoka tzw.
walencyjna.
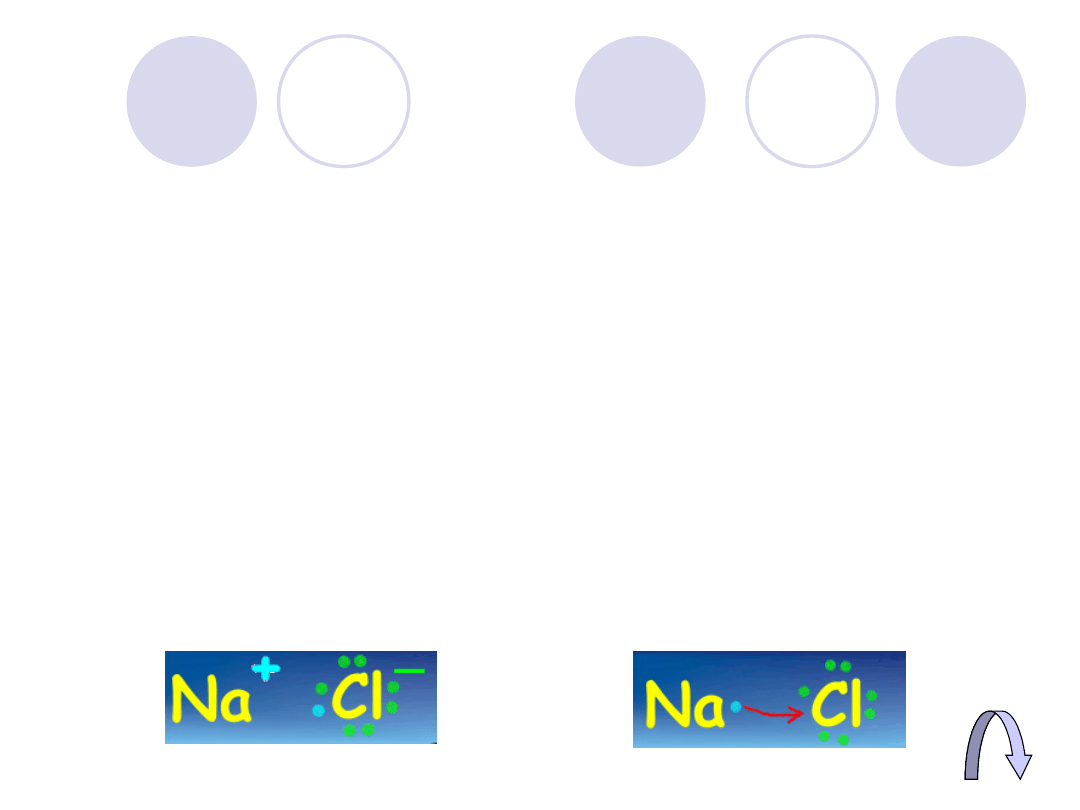
Wiązanie jonowe
Polega na przeniesieniu jednego lub
kilku elektronów z atomami o mniejszej
elektroujemności do atomu o większej
elektroujemności. Powstają wówczas jony,
które przyciągają się elektrostatycznie.
Jest to wiązanie słabe, a subdtancje je
zawierające są aktywne chemicznie.
Różnica elektroujemności musi być
większa niż 1,7.
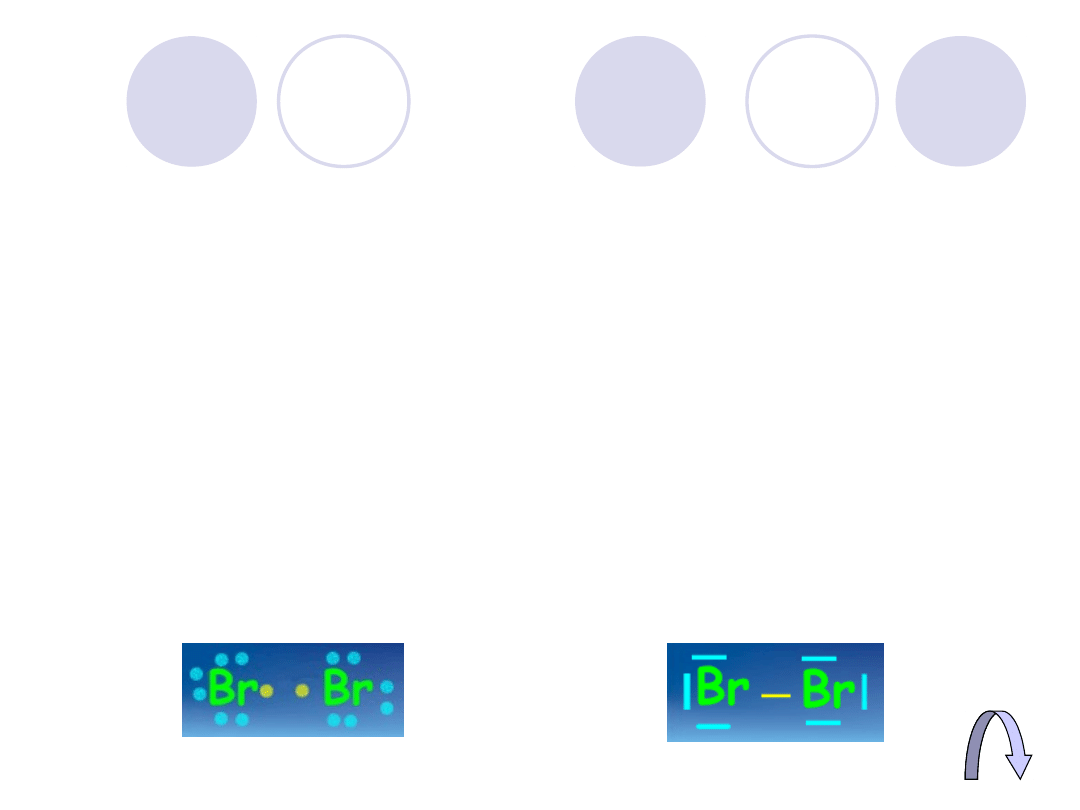
Wiązanie kowalencyjne
Polega na uwspólnianiu
(współużytkowaniu) jednej lub kilku par
elektronowych, które znajdują się w ‘mniej
więcej’ jednakowej odległościach między
atomami. Jest to wiązanie trwałe, mocne,
trudno jest je rozerwać, a więc substancje
je posiadające są mało aktywne
chemicznie.
Różnica elektroujemności musi być
mniejsza niż 0,4.
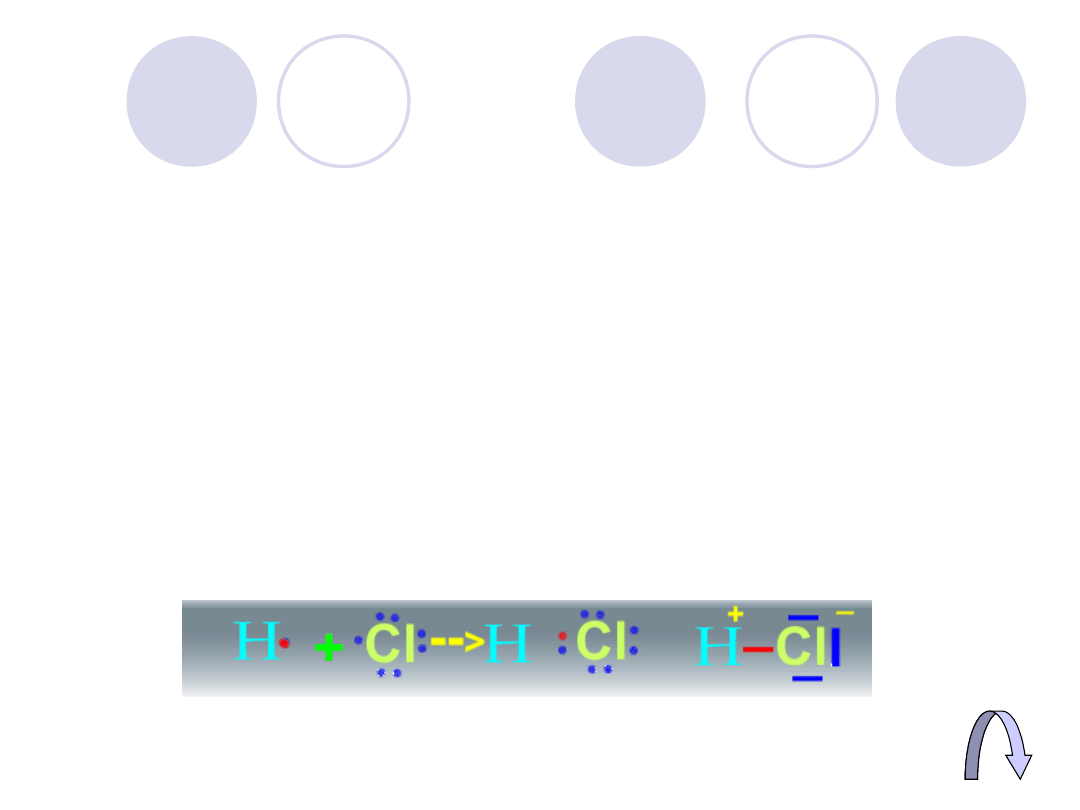
Wiązanie kowalencyjne
spolaryzowane
Tworzy się tak samo jak wiązanie
kowalencyjne, ale wspólne pary
elektronowe są przesunięte, mają większą
elektroujemność. Jest to wiązanie słabsze
od kowalencyjnego, a więc substancje je
posiadające są aktywniejsze niż w
kowalencyjnym.
Różnica elektroujemności musi być
większa niż 1,4 ale mniejsza niż 1,7.
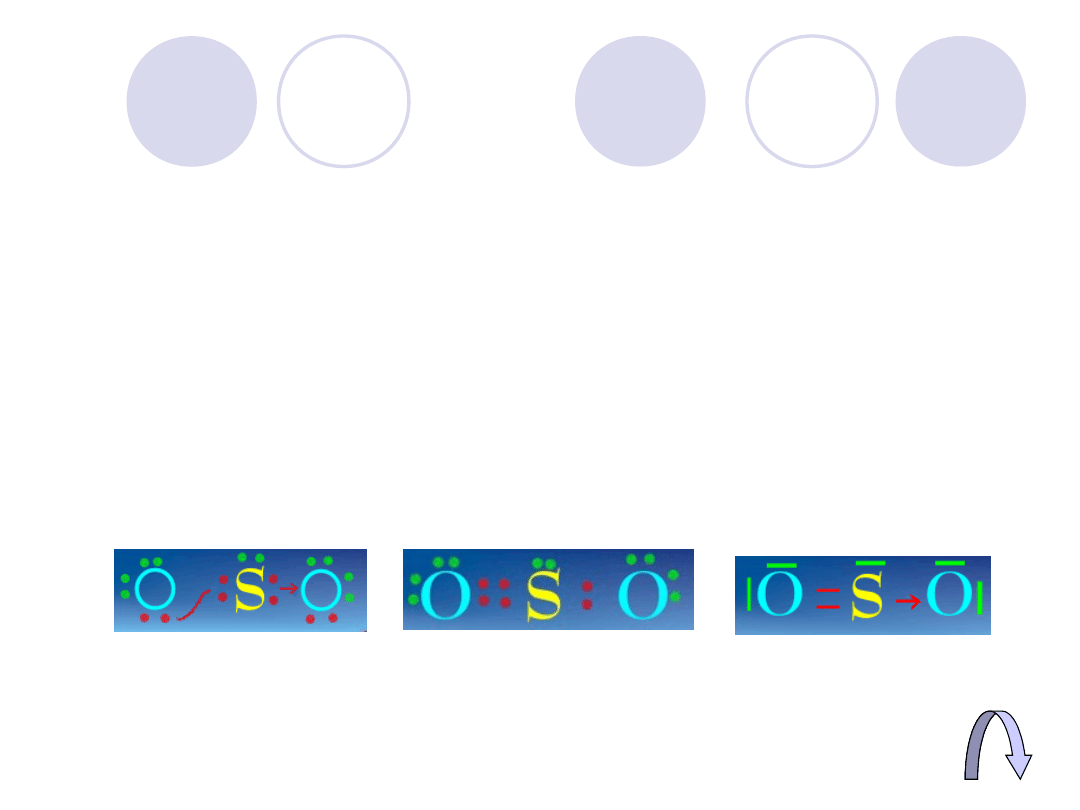
Wiązanie koordynacyjne
Inaczej donorowo-akceptorowe, polega
na uwspólnianiu pary elektronowej w
całości pochodzącej od jednego atomu. W
wiązaniach koordynacyjnych wyróżnia się
atom donora (dostarczyciela) i akceptora
(przyjmującego) elektronów.
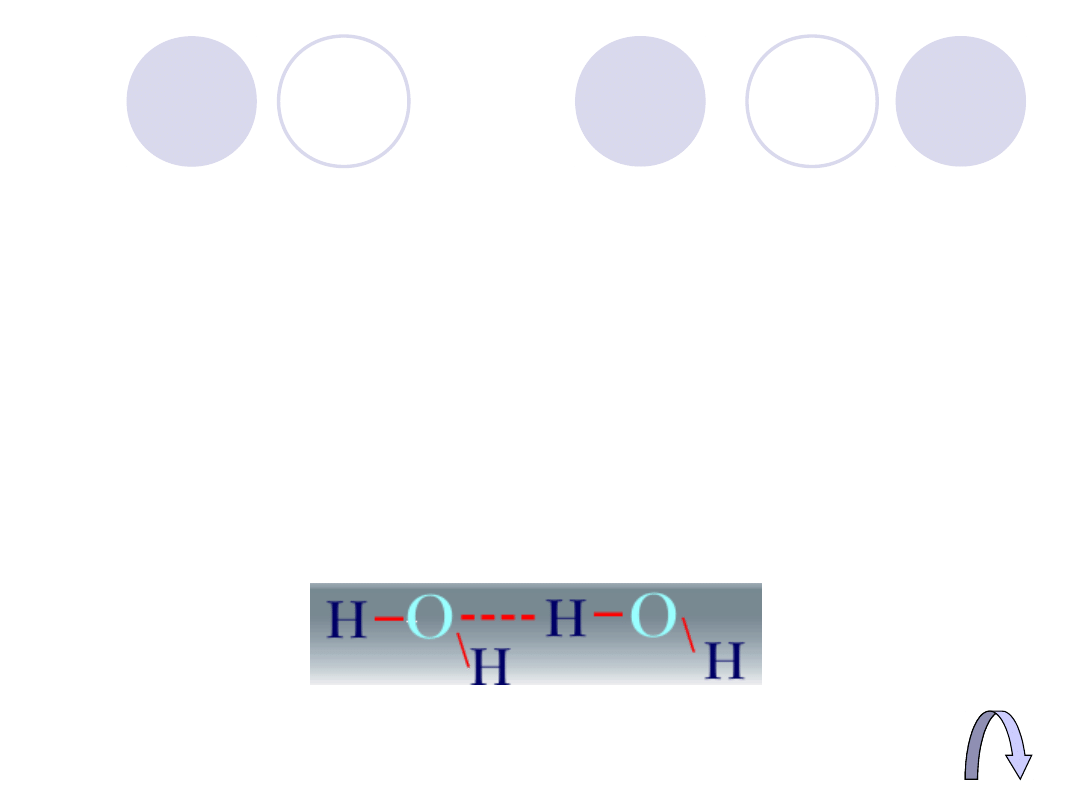
Wiązanie wodorowe
Powstaje pomiędzy wodorem związanym
z silnie elektroujemnym atomem
praktycznie pozbawiającym go
elektronów, a wolną parą elektronową
należącą do atomu z sąsiedniej cząsteczki.
Jest to najsłabsze wiązanie, powoduje
wzrost temperatury wrzenia.
KONIEC
Document Outline
Wyszukiwarka
Podobne podstrony:
wypisać i wymienić rodzaje wiązań chemicznych
ściąga rodzaje wiązań chemicznych
6 Zależność właściwości substancji od rodzaju wiązania chemicznego, Budownictwo PK, Chemia, Chemia n
chemia zaleznosc wlasciwosci substancji od rodzaju wiazania chemicznego
Wyklad 4 Wiazania chemiczne w cialach stalych
Wiązania chemiczne (II)
6 wykad WiĄzania chemiczne[F]
Wykład 1, budowa atomu, wiązania chemiczne
2 Atom i cząstka Wiązania chemiczne klucz
2 Atom i cząstka Wiązania chemiczne
7 układ okresowy pierwiastków, wiązania chemiczne
RODZAJE WIĄZAŃ
Budowa atomu i wiązania chemiczne test odpowiedzi
WIĄZANIA CHEMICZNE
Atom, cząsteczka, wiązanie chemiczne
Wiązania chemiczne
Chemia wiązania chemiczne
więcej podobnych podstron