
Marian Cholewa
Katedra Fizyki
Politechnika Rzeszowska
Semestr zimowy, rok 2011/2012
Lekcja 10 Strona 1
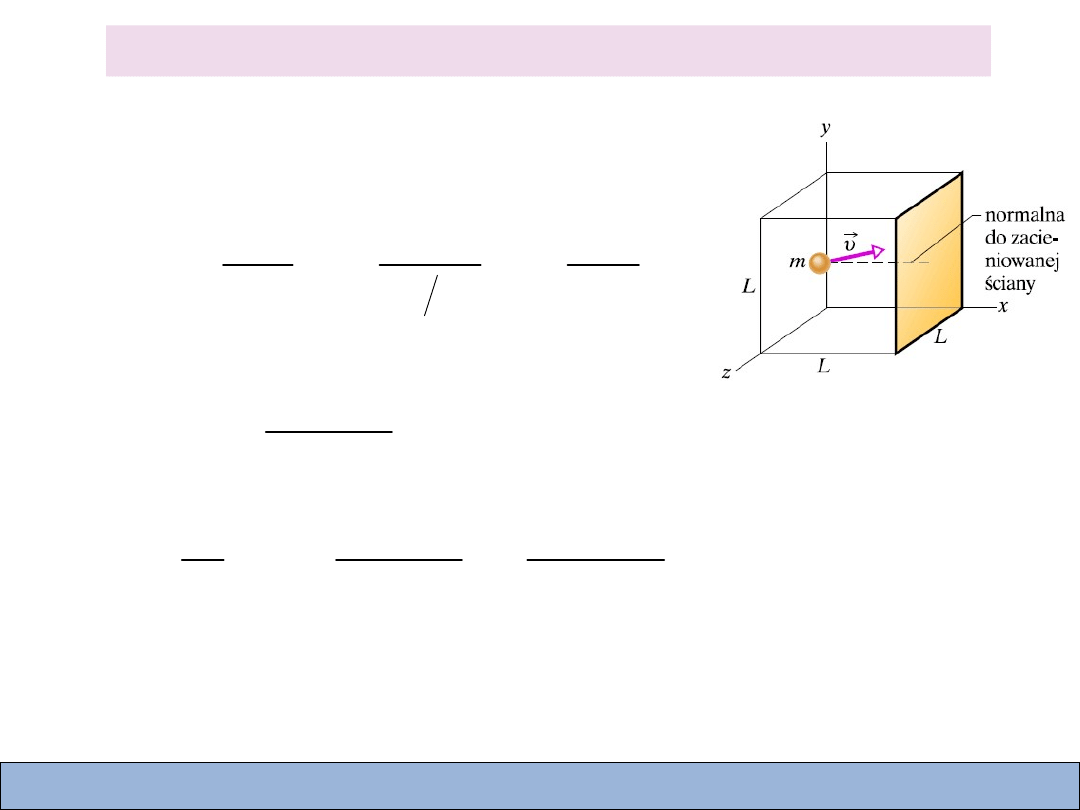
Prędkość średnia kwadratowa
(
)
2
x
x
x
x
p
mv
mv
mv
D = -
-
=-
2
2
2
xi
xi
xi
x
i
i
i
xi
p
mv
mv
F
t
L v
L
D
=
=
=
D
�
�
�
( )
2
x sr
x
A
m v
F
nN
L
=
( )
( )
2
2
2
3
x
x
x
sr
sr
A
m v
M v
F
p
nN
n
L
L
V
=
=
=
A
M mN
=
- molowa masa gazu
Lekcja 10 Strona 2
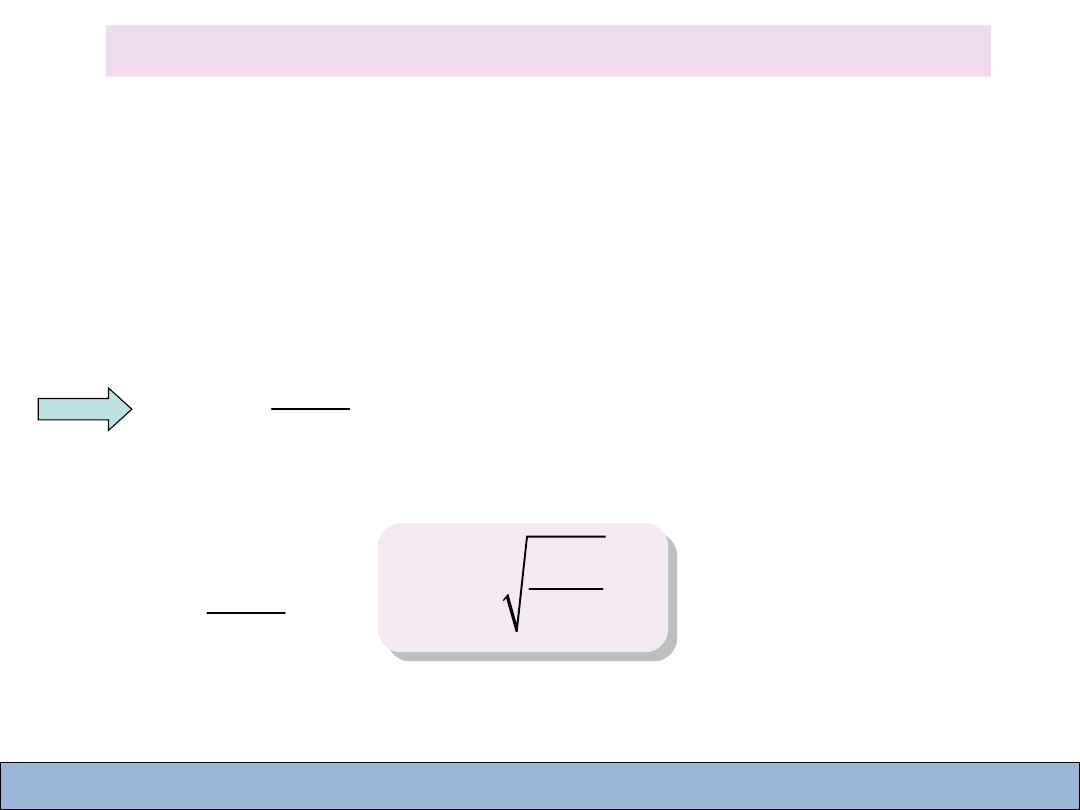
Prędkość średnia kwadratowa
( ) ( ) ( )
2
2
2
x
y
z
sr
sr
sr
v
v
v
=
=
( ) ( ) ( )
( )
2
2
2
2
2
3
sr
x
y
z
x
sr
sr
sr
sr
v
v
v
v
v
=
+
+
=
2
3
sr
Mv
p n
V
=
pV nRT
=
2
3
sr
Mv
RT =
3
sr
RT
v
M
=
Lekcja 10 Strona 3
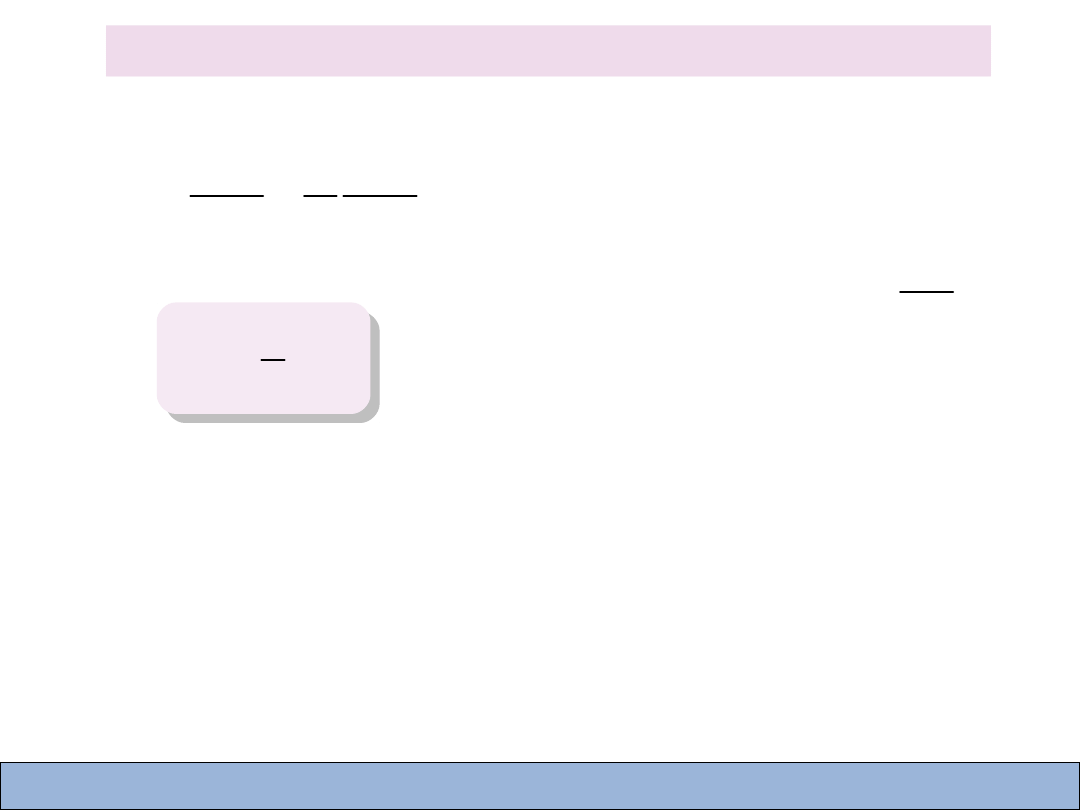
Energia kinetyczna cząsteczki
2
3
2
2
sr
k
mv
m RT
E
M
=
=
A
M N m
=
A
R
k
N
=
3
2
k
E
kT
=
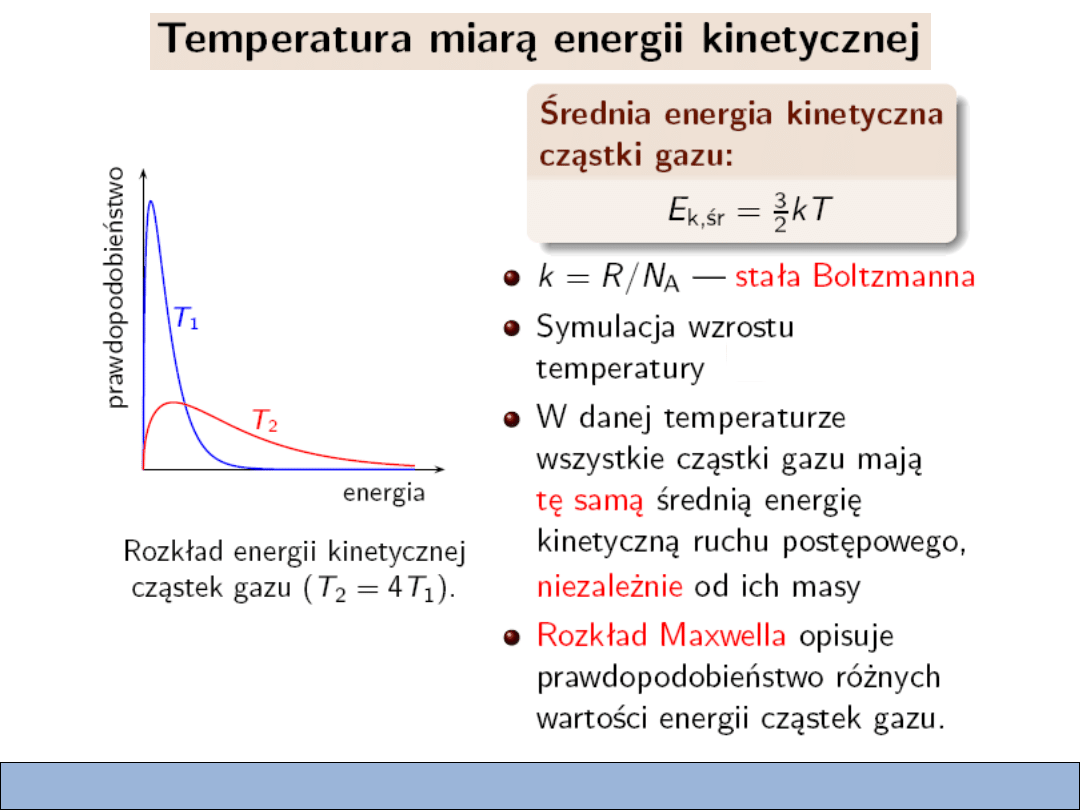
W danej temperaturze T wszystkie cząsteczki gazu doskonałego
mają taką samą średnią energią ruchu postępowego.
Lekcja 10 Strona 4
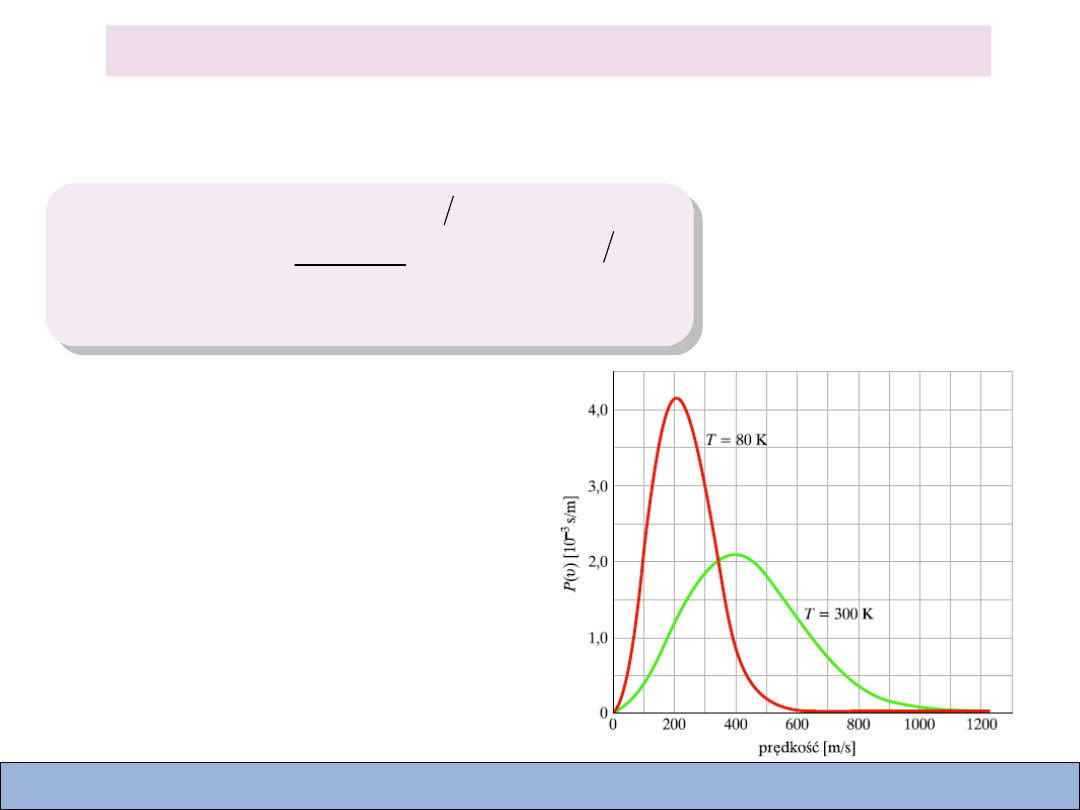
Rozkład prędkości cząsteczek
Funkcja rozkładu prawdopodobieństwa:
2
3 2
2
2
( ) 4
3
mv
kT
m
P v
v e
kT
p
p
-
�
�
=
�
�
�
�
rozkład Maxwella
Lekcja 10 Strona 5
0
( )
1
P v dv
�
=
�
2
2
0
( )
sr
v P v dv v
�
=
�

Energia wewnętrzna gazu
Energia n moli gazu:
3
2
w
A
kT
E
nN
=
3
2
w
E
nRT
=
– gaz jednoatomowy!
Lekcja 10 Strona 6
A
R
k
N
=
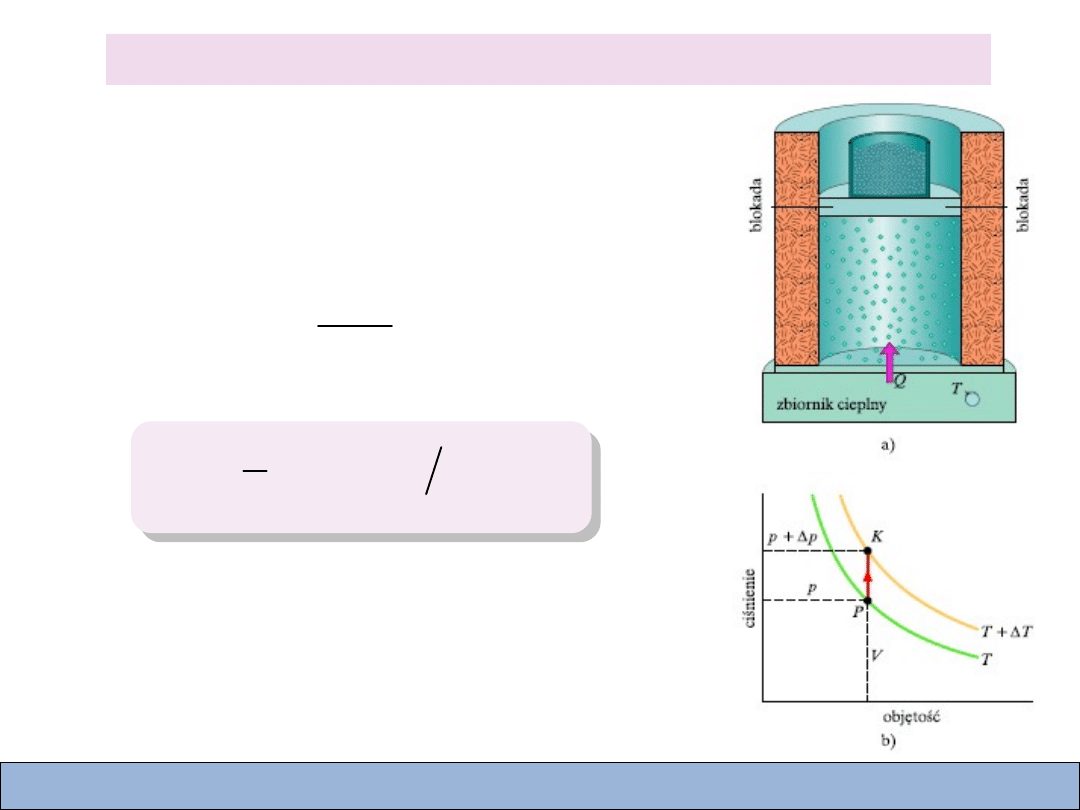
Molowe ciepło właściwe
Molowe ciepło właściwe gazu przy stałej
objętności:
w
V
E
C
n T
D
=
D
(
)
3
12,5J mol K
2
V
C
R
=
=
Lekcja 10 Strona 7
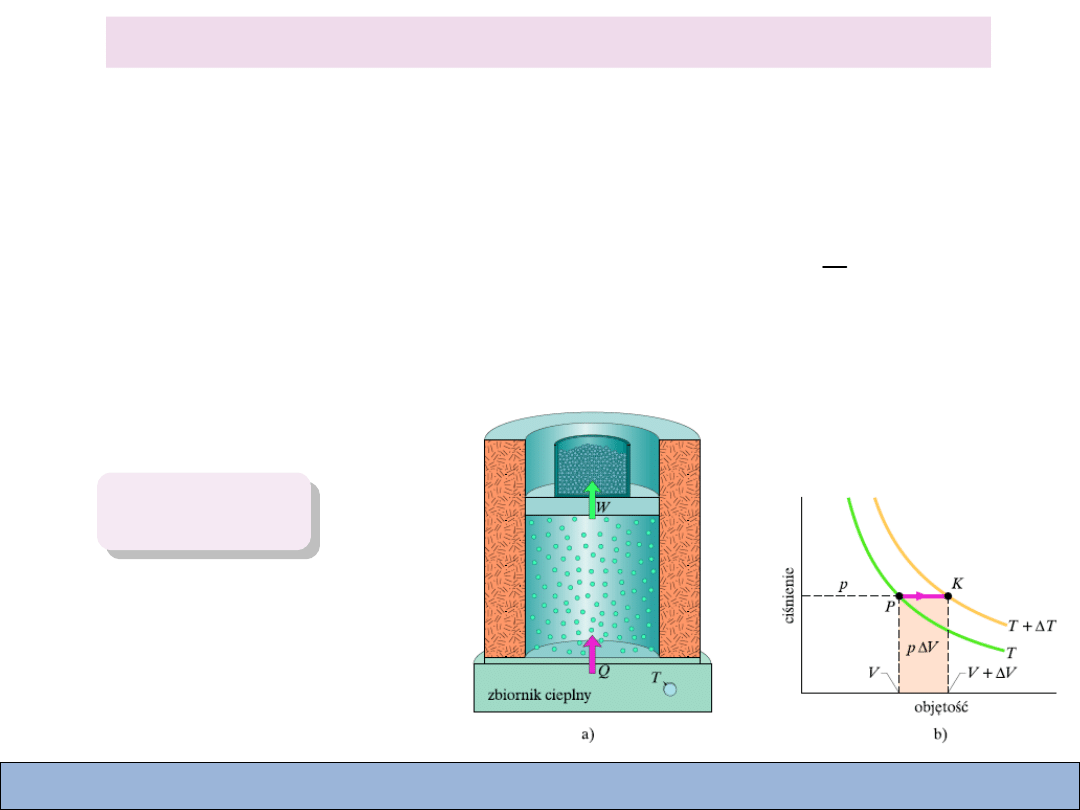
Molowe ciepło właściwe
Zmiana energii przy stałym ciśnieniu:
w
p
E
Q
W nC T p V
D =D - D =
D - D
pV nRT
=
w
p
E
nC T nR T
D
=
D -
D
V
p
nC T nC T nR T
D =
D -
D
3
2
w
V
E
nRT nC T
=
=
p
V
C
C
R
=
+
Lekcja 10 Strona 8
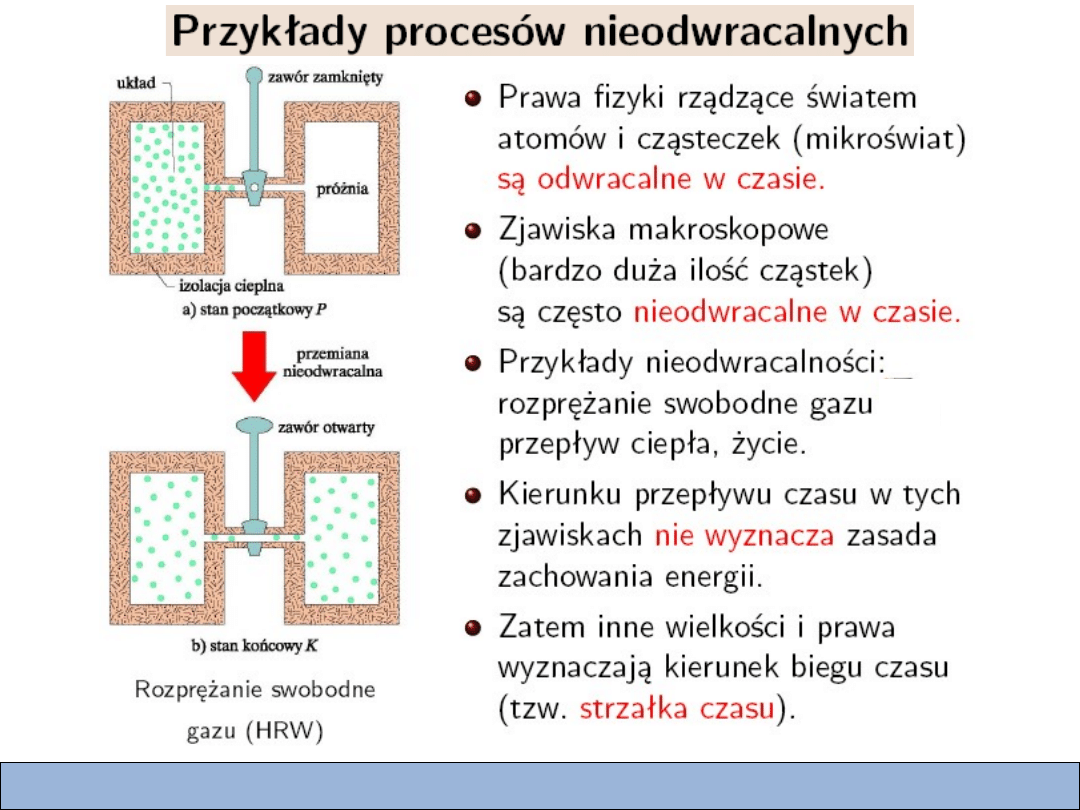
Lekcja 10 Strona 9

Lekcja 10 Strona 10

Lekcja 10 Strona 11

Lekcja 10 Strona 12
Lekcja 10 Strona 13
Lekcja 10 Strona 14

Lekcja 10 Strona 15

Lekcja 10 Strona 16
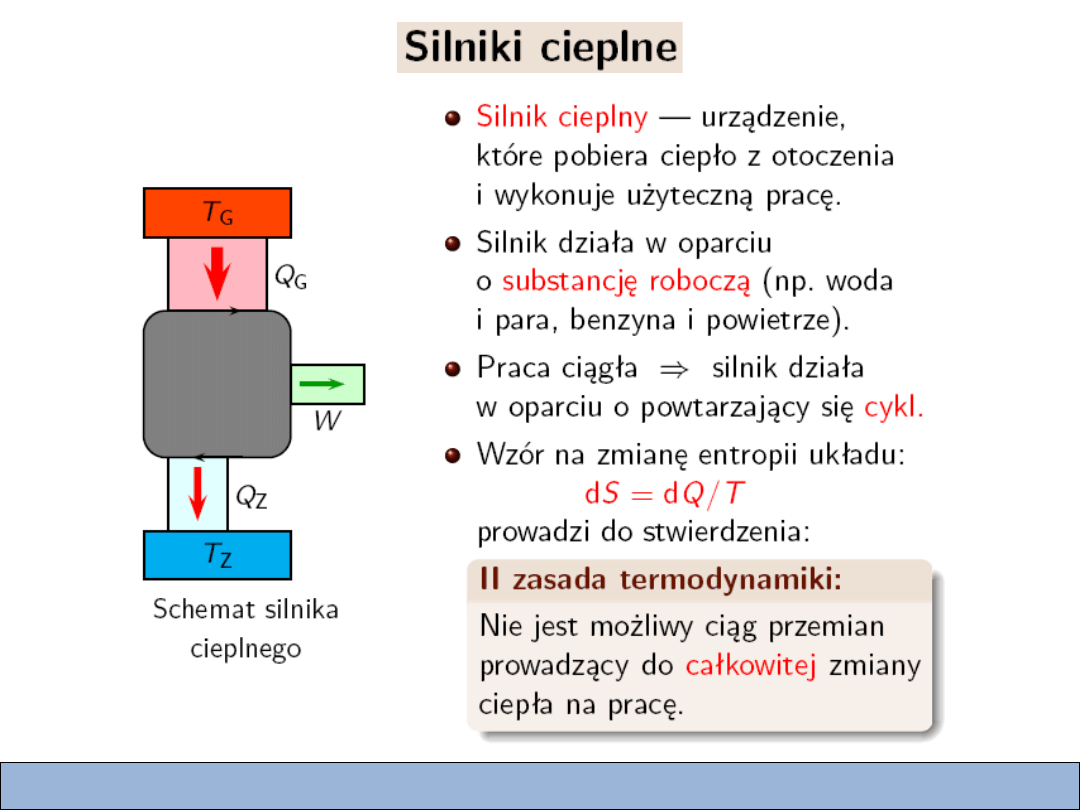
Zmiana entropii
Definicja zmiany entropii:
konc
konc
pocz
pocz
dQ
S S
S
T
D =
-
=
�
W wypadku małej zmiany temperatury:
sr
T
Q
S
Lekcja 10 Strona 17
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
Wyszukiwarka
Podobne podstrony:
Fizyka 4 9 10
Fizyka82 (10)
Fizyka 10
FIZYKA (10)
fizyka 10+
Fizyka 10 PP
Fizyka 2 10 czastki elementarne
Fizyka W 10 Uz a
Fizyka 10
AGH e-Fizyka 10 Relatywistyka i fizyka jądrowa, Fizyka i Fizyka chemiczna
fizyka! 10 09
Fizyka81 (10)
Fizyka 4 9 10
FIZYKA1 (10) DOC
Fizyka 10
więcej podobnych podstron