

Temperatura
Temperatura wód powierzchniowych
zależy od:
Ich pochodzenia
Strefy klimatycznej
Pory roku
Od dopływu
ścieków
przemysłowych i
miejskich

Temperatura
Wzrost
temperatury
powoduje
zmniejszenie ilości rozpuszczonego tlenu,
zwiększenie
biologicznego
zapotrzebowania na tlen, przyspieszenie
procesów
chemicznych
oraz
mikrobiologicznych.
Temperatura wody ma duży wpływ na współistnienie
organizmów wodnych oraz przebieg procesów fizycznych,
chemicznych i biologicznych zachodzących w wodach.

Temperatura
Stratyfikacja termiczna wody w
jeziorze:
• Temperatura wody obniża się w kierunku
od powierzchni zwierciadła wody do dna w
jeziorze i tworzy trzy warstwy (układ letni):
• Epilimnion – górna warstwa mieszana, o
dość wyrównanej temperaturze
• Metalimnion – warstwa przejściowa
• Hypolimnion– dolna warstwa, ok. 4°C

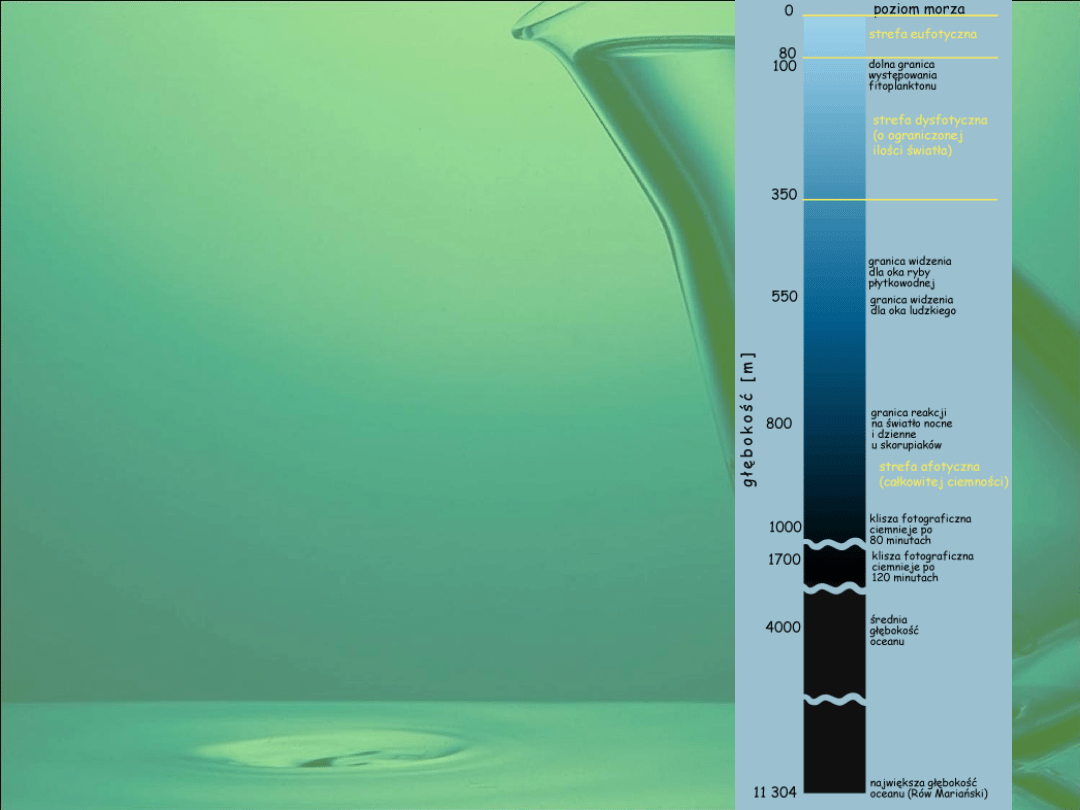
Przezroczystość
Przezroczystość jest to
wskaźnik który określa
zdolność przepuszczania
promieni świetlnych przez
warstwę wody. O stopniu
przezroczystości decyduje
ilość występujących w wodzie
zdyspergowanych cząsteczek
koloidalnych lub zawiesin.
Przezroczystość mierzy się
krążkiem Secchiego .
Barwa
• Wpływa ona na
przezroczystość.
• Barwa wynika z obecności w
wodzie rozpuszczonych
substancji mineralnych
(jonów żelaza czy manganu)
lub substancji organicznych,
np. związków humusowych.
• Wpływa na pochłanianie
promieniowania słonecznego,
przez co kształtuje się
pionowy gradient termiczny.

pH
Odczyn wód naturalnych waha się w granicach pH 4
- 9 i zależy od wielu czynników:
•
Zawartości węglanów,
wodorowęglanów i dwutlenku węgla
•Charakteru podłoża glebowego,
które może zawierać związki o
charakterze kwaśnym lub
zasadowym
• Zanieczyszczeń ściekami
•Opadów atmosferycznych, które
mogą powodować wzrost stężeń
słabych i mocnych kwasów w
wodach.

pH
Odczyn wody ma duże znaczenie dla
organizmów żywych i przebiegu
procesów biochemicznych oraz
przemysłowego użytkowania wody. W
wodach
zbyt kwaśnych lub zbyt
zasadowych zamiera życie
biologiczne.
Niskie pH wody
przyspiesza wymywanie metali
ciężkich z osadów dennych. Wody o
odczynie kwaśnym mają właściwości
korozyjne.
Przewodnictwo
Przewodnictwo elektrolityczne wody jest możliwe
dzięki obecności w niej jonów pochodzących ze
zdysocjowanych cząsteczek soli, zasad i kwasów.
Główną rolę w przewodnictwie odgrywają
jony dodatnie (kationy) wapnia, magnezu,
sodu i potasu oraz ujemne jony (aniony)
chlorkowe, siarczanowe, wodorowęglanowe i
azotanowe. Jednostką przewodnictwa jest
mS/cm.
Przewodnictwo
Wody powierzchniowe w
Polsce charakteryzują
się najczęściej
przewodnictwem
mieszczącym się w
zakresie od 100 do 500
mS/cm.
Przewodnictwo jest często używane jako
pierwszy wskaźnik mineralizacji i
zanieczyszczenia wody.

Tlen
• Tlen w wodzie pochodzi z dwóch źródeł:
– z atmosfery
– z produkcji pierwotnej zachodzącej w wodzie
Rozpuszczaniu tlenu sprzyja niska temperatura
i mieszanie wód.
Jest niezbędny do życia organizmom żywym,
bierze udział w procesie samooczyszczania
mineralizując substancje organiczne przy
udziale bakterii.

Tlen
Ilość tlenu w
wodzie określa
się w
jednostkach
wagowych
(mg/l), lub jako
względne
nasycenie
tlenem (%).

Chlorofil a
Zielony barwnik biorący
udział w procesie
fotosyntezy u
autotrofów,
zlokalizowany w
chloroplastach. Energia
świetlna pochłaniana
przez chlorofil warunkuje
fotosyntezę.
• Na podstawie chlorofilu
a ocenia się warunki
rozwoju fitoplanktonu.

BZT5
Proces samooczyszczania wód zanieczyszczonych
substancją organiczną polega na utlenianiu substancji
organicznych przy współudziale mikroorganizmów
tlenowych.
Podczas tego procesu wymagany jest
dopływ tlenu.
Zapotrzebowanie na ten tlen określa się
mianem
biologicznego zapotrzebowania na tlen (BZT).
Parametr
BZT5
określa ile
tlenu zostało by zużyte do
mineralizacji substancji
organicznej w warunkach
nieograniczonej jego
dostawy przez 5 dni
ponieważ wtedy te procesy
zachodzą najintesywniej.

ChZT
Chemiczne zapotrzebowanie na tlen
jest to parametr używany do oceny
stanu wody lub ścieków,
interpretowany jako ilość tlenu
potrzebna do utlenienia zawartych
związków organicznych i
nieorganicznych. Utlenianie odbywa
się za pomocą silnych związków
utleniających takich jak dwuchromian
potasu.
BZT jest częścią ChZT, a ich
proporcja jest istotną wskazówką
odnośnie biodegradowalności
ścieków.
Fosfor
Źródła fosforu w wodzie:
• Wietrzenie i rozpuszczanie minerałów, erozja
gleby, opady atmosferyczne, spływy
powierzchniowe, nawozy fosforowe, fosforany w
środkach piorących, ścieki komunalne.
Fosfor, który trafia do zbiornika wodnego, krąży
między poszczególnymi warstwami wody w
rozmaity sposób, co jest zależne od typu
miktycznego jeziora i od jego stanu troficznego.

Fosfor
Pojawienie
się
w
wodzie
dodatkowych
ilości
fosforu
(pochodzących
głównie
ze
spływów powierzchniowych z
pól) powoduje intensyfikację
przebiegu
fotosyntezy,
nadmierny
wzrost
ilości
biomasy w wodzie i zakłócenie
naturalnej
równowagi
(eutrofizację).
Fosfor jest uznawany za
najważniejszy z biogenów !!!

Azot
• Źródłem azotu w wodzie w naturalnym
zbiorniku wodnym jest azot
atmosferyczny, który dostaje się do niej
poprzez wiązanie go przez bakterie i
niektóre gatunki sinic.
• Azot pochodzi również z nawozów
azotowych czy ścieków miejskich .
Jest on podobnie jak fosfor w
większości magazynowany w osadach
dennych.
W zależności od warunków tlenowych
dochodzi do jednego z dwóch
fundamentalnych procesów związanych
z przemianami azotu w wodzie – przy
obecności tlenu zachodzi nitryfikacja,
natomiast w przypadku jego braku –
denitryfikacja.

Formy Azotu
Amoniak (
NH
3
) oraz jony amonowe(
NH
4+
)
Azotyny (
NO
2-
)
Azotany(
NO
3-
)
Azot (
N
2
)

Dziękujemy za uwagę
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
Wyszukiwarka
Podobne podstrony:
Prezentacja fizyko UV
Prezentacja z fizykoterapii UV
Prezentacja fizyko LASEROTERAPIA
Prezentacja fizyko UV
sem III GWiOW prezentacja Bilans Wód Zlewni
milosc jest jak bezmiar wod www prezentacje org
prezentacja działalność przedsiębiorstw wod kan
Prezentacja kompetencje organów administracji samorządowej w zakresie korzystania z wód
prezentacja na fizykoterapie
sem III GWiOW prezentacja konspekt Bilans Wód Zlewni
milosc jest jak bezmiar wod www prezentacje org
milosc jest jak bezmiar wod www prezentacje org
prezentacja finanse ludnosci
prezentacja mikro Kubska 2
więcej podobnych podstron