
Infection in the neonatal
period
Iwona Maroszyńska
Polish Mother’s Health Centre

Classification
• Early onset
– 24 hours - 85%
– 24 - 48 hours - 5%
– 48 hours-6 -days 10%
• Late onset
– After 6 day
– After 3 day

Classification
• Very early infection
– 12 hours
• Early infection
– 12-72 hours
• Late infection

Pathogenesis of early
infection
• Acquisition of microorganisms from the
mother
– Transplacental infection
– Ascending
•Colonisation of the mother's
genitourinary tract
•Colonisation of birth canal at
delivery

Etiology of early infection
• B Streptococcus (GBS)
• Escherichia coli
• Haemophilus influenzae
• Listeria monocytogenes

Sexually Transmitted
Diseases
• Gonorrhea
• Syphilis
• Herpes simplex virus (HSV)
• Cytomegalovirus (CMV)
• Hepatitis
• HIV
• Trichomonas vaginalis
• Candida species

TORCH Infections
• T – Toxoplasmosis
• O – Other
• R – Rubella
• C – Cytomegalovirus
• H - Herpes


Pathogenesis of the late
infection
• Colonisation of the neonates from the
environment :
– The infant's skin
– Respiratory tract
– Conjunctivae
– Gastrointestinal tract
– Umbilicus

Vectors for the colonization
• Vascular or urinary catheters
• Intubation tube
• Chest tube
• Contact from caregivers with bacterial
colonization

Etiology
• The infectious agents associated with neonatal
sepsis have changed over the past 50 years
• S aureus and E coli were the most common
infectious hazards for neonates in the 1950s in
the United States
• GBS then replaced S aureus as the most
common gram-positive agent, causing early-
onset sepsis during the next decades
• During the 1990s, GBS and E coli continued to
be associated with neonatal infection;
however, coagulase-negative S epid. and S
aureus are now observed more frequently

Etiology
• Gram positive germs
– Coagulase-negative staphylococci
• Staphylococcus epidermidis
– Staphylococcus aureus
– GBS
• Gram negitive germs
– E coli
– Klebsiella
– Pseudomonas
– Enterobacter
– Serratia, Acinetobacter
• Fungi
– Candida

Late Viral Infection
• Meningoencephalitis and neonatal
sepsis syndrome
– Adenovirus
– Enterovirus
– Coxsackievirus
– RSV

• Bacterial organisms with increased
antibiotic resistance have emerged and
have further complicated the
management of neonatal sepsis
• Infants with lower birth weight and
infants who are less mature have
increased susceptibility to these
organisms

Coagulase negative strains
• Increasingly seen as a cause of nosocomial or
late-onset sepsis, especially in the premature
infant
• It is considered the leading cause of late-
onset infections for preterm babies
• Its prevalence is related to its preference for
the plastic mediums found in cannulas and
shunts, which increases its introduction via
umbilical catheters and other indwelling lines

Coagulase negative
staphylococci
• The bacterial capsule polysaccharide
adheres well to the plastic polymers of
the catheters
• Proteins found in the organism [AtlE and
SSP-1] enhance attachment to the
surface of the catheter
• The adherence creates a capsule
between microbe and catheter, which
prevents C3 deposition and phagocytosis

Coagulase negative
staphylococci
• The toxins formed by this organism have
been associated with necrotizing
enterocolitis
• Coagulase-negative Staphylococcus is a
frequent contaminate of blood and
cerebrospinal fluid (CSF) cultures;
therefore, it can be a false indicator of
coagulase-negative staphylococcal
septicemia

Frequency - early infection
USA
• Frequency 7-
13%
• Positive blood culture 3-8%
– Gram (+) 60%
– Gram (-) 14%
– Other 26%
ICZMP
11,5%
28%
57%
29%
Fungi 14%
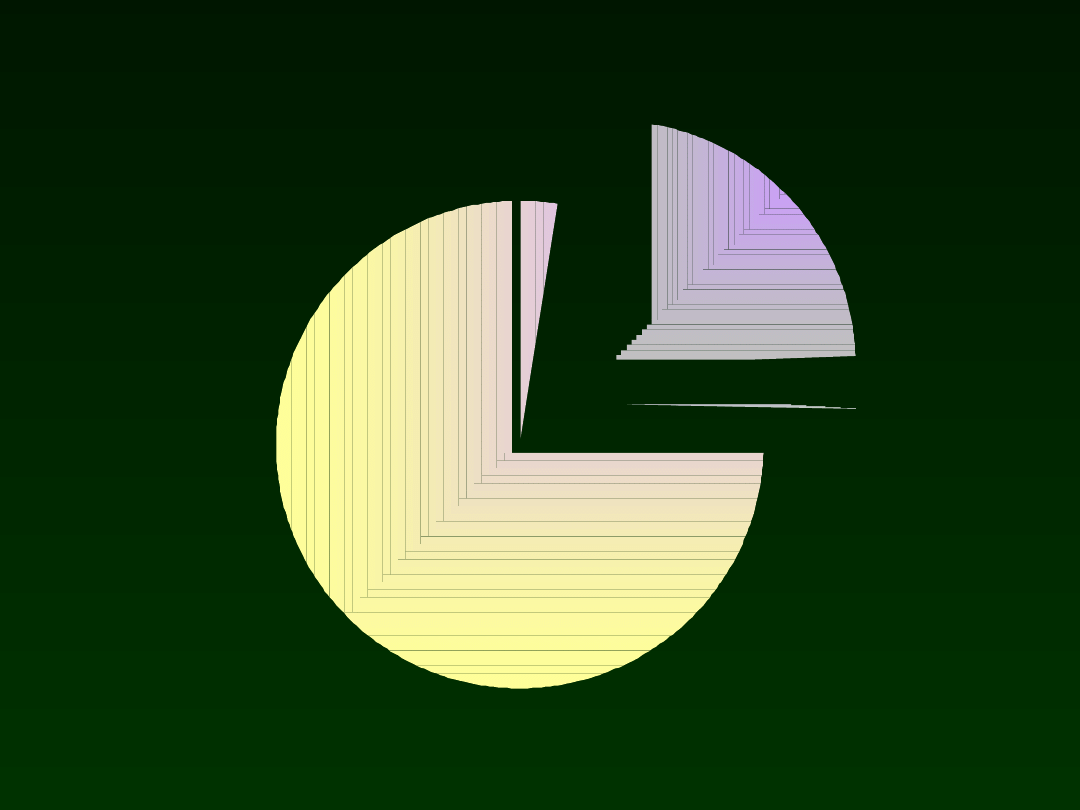
28%
0,9%
N of patients in
NICU.
infection
CNS infections

Frequency of late infection
• USA 5,2% - 30,4%
• Europe 8% – 10%
• ICZMP
– Sepsis - 28%
• Positive blood culture – 82%
• Sepsis complcated by CNS infection -
11%
– CNS infection – 0,9%
• with sepsis 78%
– Serious infections – 29%
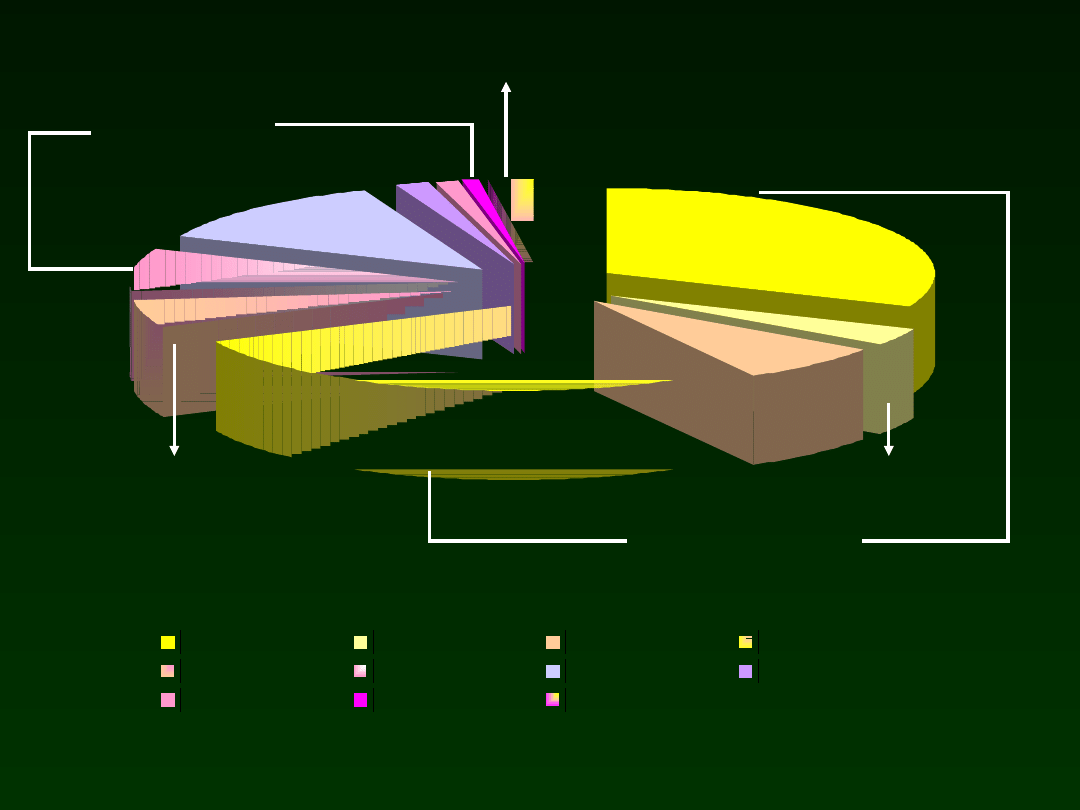
Staph. epid. 31
Strept. B 3,5
Staph. aureus 7
Staph. sp. 26
Ent. faec. 5,3
E. coli 8
Klebsiella 12
Enerobacter 1,8
Pseudomonas 1,2
Acinetob. 0,6
Grzyby 2,3
Gram (+) – 73%
S. Epi
31%
Strept.-
3,5%
Gram (-) –
24%
Fungi
2,3%
Staph. sp.
Enterococcus
faec. 5,3%
Klebsiella
sp. 12%
7%
S.aure
us
8% E. coli

Mortality/Morbidity
• The mortality rate - 50%
• Infection is a major cause of fatality during
the first month of life, contributing to 13-15%
of all neonatal deaths
• Neonatal meningitis occurs in 2-4 cases per
10,000 live births
• Mortality in the NICU related to the sepsis
– USA 11%
– ICZMP 7%

Risk factors – early infection
• Maternal GBS colonization (especially if
untreated during labor)
• Premature rupture of membranes
(PROM) Prolonged rupture of
membranes
• Prematurity
• Chorioamnionitis

Predisposing factors – early
infection
• Low Apgar score (<6 at 1 or 5 min),
• Maternal fever greater than 101°F (38.4°C)
• Maternal urinary tract infection
• Poor prenatal care
• Poor maternal nutrition
• Low socioeconomic status
• Recurrent abortion
• Maternal substance abuse
• Low birth weight
• Difficult delivery
• Birth asphyxia
• Meconium staining amniotic fluid

Maternal GBS status
Colonisation of the maternal gastrointestinal
tract and birth canal
Approximately 30% of women have
asymptomatic GBS colonisation during
pregnancy
Neonatal GBS infection - 2 neonates per 1000
live births
The highest risk of perinatal transmission
Heavy GBS colonisation
Chronically positive cultures for GBS have

Maternal GBS status
Heavy colonization at 23-26 weeks of
gestation is associated with prematurity
and low birth weight
Intrapartal chemoprophylaxis of women
with positive cultures for GBS has been
shown to decrease the transmission of
the organism to the neonate during
delivery

PROM
Response to an untreated infection of the
urinary tract or birth canal
Association with previous preterm delivery,
uterine bleeding in pregnancy, and heavy
cigarette smoking during pregnancy
Rupture of membranes without other
complications for more than 24 hours prior to
delivery is associated with a 1% increase in
the incidence of neonatal sepsis
PROM accompanying the chorioamnionitis the
incidence of neonatal infection is quadrupled

Prematurity
Preterm infants are more likely to require
invasive procedures, such as umbilical
catheterization and intubation
Premature infants have less immunologic
ability to resist infection
Prematurity is associated with infection from
CMV, HSV, hepatitis B, toxoplasmosis,
Mycobacterium tuberculosis, Campylobacter
fetus, and Listeria species

Chorioamnionitis
• The relationship between chorioamnionitis
and other risk variables is strong.
• Suspect chorioamnionitis in the presence
of:
– fetal tachycardia,
– uterine tenderness,
– purulent amniotic fluid,
– elevated maternal WBC count,
– unexplained maternal temperature above
100.4°F (38°C)

• IV, IA kaniula
• Mechanical ventilation
• TPN
• Treatment of hydrocephalus
• High humidityty in incubators
• Chest tube
• Vesicle catheterisation
Predisposing factors – Late
infection

Clinical presentation
• Nonspecific and associated with
characteristics of the causative
organism and the body's response to
the invasion
• These nonspecific clinical signs of early
sepsis syndrome are also associated
with other neonatal diseases, such as
RDS, metabolic disorders, intracranial
hemorrhage, and a traumatic delivery

Congenital pneumonia
• Aspiration of the microorganisms during
the delivery process
• Tachypnea, irregular respirations,
moderate retracting, apnea, cyanosis,
grunting
• Neonates with intrauterine pneumonia
may also be critically ill at birth and
require high levels of ventilatory
support

Congenital pneumonia
The colonization of the expiratory tract
Infection with pulmonary changes
Infiltration
Destruction of bronchopulmonary tissue
Inhibition of pulmonary surfactant
function
Respiratory failure with an RDS-like
presentation

Congenital pneumonia
x-ray
Segmental or lobar
atelectasis
Diffuse reticulogranular
pattern
Pleural effusions may be
observed
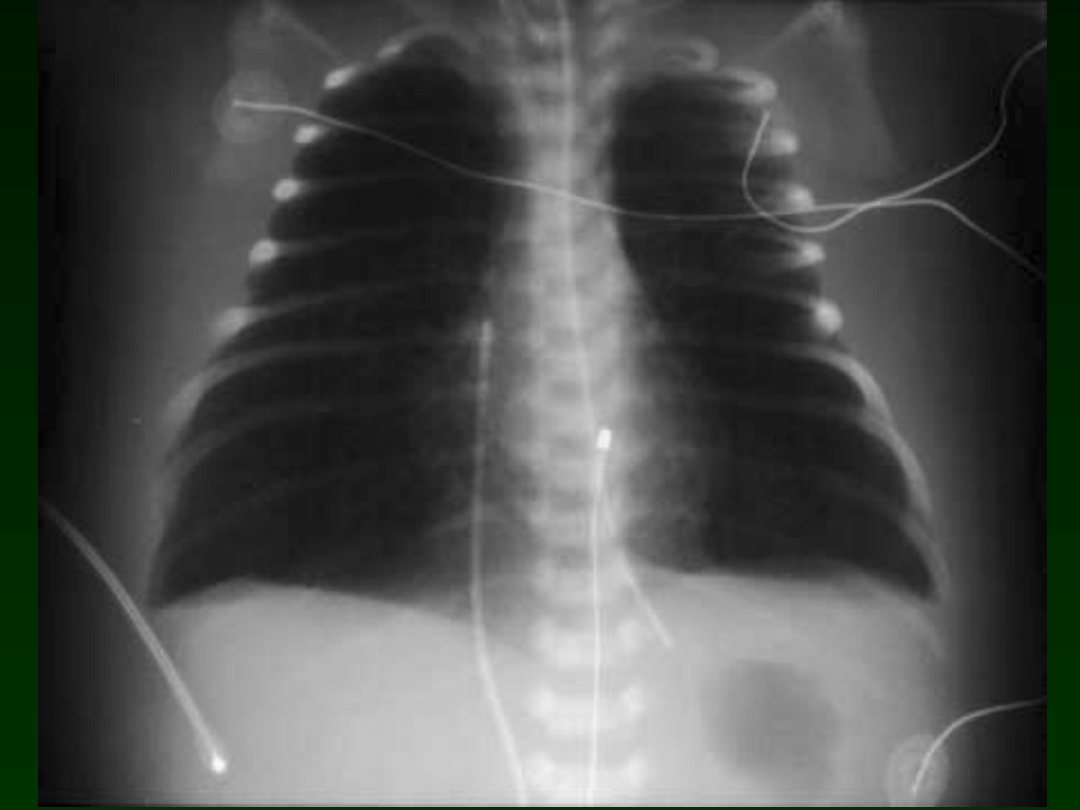
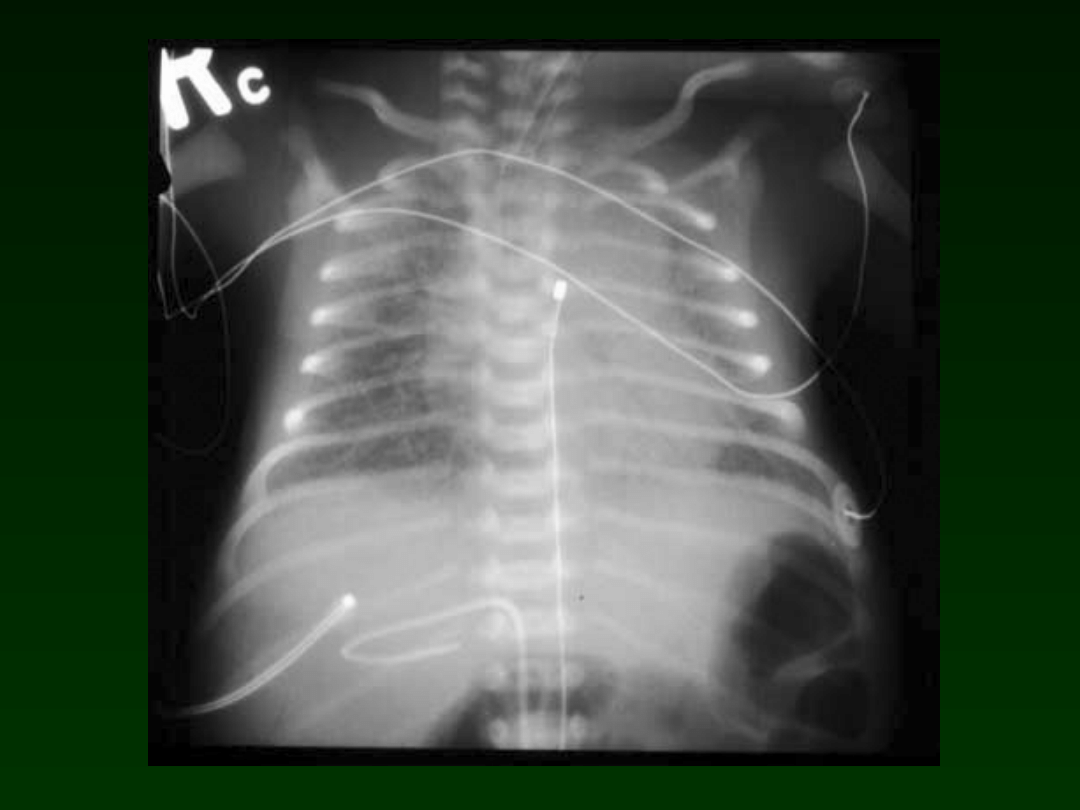

Acquired pneumonia
Infectious agents exist in the
environment
Risc factors
Endotracheal intubation
mechanical ventilation,
Etiology
Staphylococcus
Pseudomonas species

Cardiac signs
• Initial early phase
• Pulmonary hypertension
– hydroxyl radicals
– thromboxane B2
– polysaccharide capsule of type III
Streptococcus
• Decreased cardiac output
• Hypoxemia is postulated to occur

Septic shock
• Clinical signes
– Pallor
– Poor capillary perfusion
– Oliguria
– Hypotension
– Edema
• These signes of shock are indicative of
severe compromise and are highly
associated with mortality

Metabolic problems
• Hypoglycemia
• Metabolic acidosis
– Conversion to anaerobic metabolism
• Increased oxygen requirements
• Increased metabolic rate
• Hyperactivity, respiratory effort
• Jaundice
• Increased glucose requirement

Neurologic signs - Meningitis
Etiology
GBS - 36%
E coli -31%)
Listeria species -5-10%
Other organisms:
S pneumoniae, S aureus, Staphylococcus
epidermis, Haemophilus influenzae, and species of
Pseudomonas, Klebsiella, Serratia, Enterobacter,

Neurologic signs - Meningitis
Early-onset neonatal sepsis - 24-48 hours
nonneural signs dominat.
Neurologic signs
stupor
irritability.
Overt signs of meningitis occur in 30% of
cases
Even culture-proven meningitis may not
demonstrate white cell changes in the CSF

Neurologic signs - Meningitis
Late-onset infection - 80-90% neurologic signs
Impairment of consciousness (ie, stupor with
or without irritability)
Coma
Seizures
Bulging anterior fontanel
Extensor rigidity
Focal cerebral signs
Cranial nerve signs

Neurologic signs - Meningitis
The CSF findings
Elevated WBC count (predominately PMNs)
within the reference range in 29% of GBS
meningitis and 4% of gram-negative meningitis
Elevated protein level, decreased CSF
glucose concentration
Present in about 50% of GBS meningitis and
15 - 20% of gram-negative infections
Positive cultures.

Neurologic signs - Ventriculitis
Inflammation of the ventricular surface
Exudative material at the choroid plexus externaly to
the plexus
Ependymitis
Disruption of the ventricular lining
Projections of glial tufts into the ventricular lumen
Glial bridges may develop by these tufts causing
obstruction, particularly at the aqueduct of Sylvius
The lateral ventricles become multiloculated
Isolation of the organisms

Neurologic signs - Arachnoiditis
• Next phase and the hallmark of meningitis
The arachnoid is infiltrated with
inflammatory cells producing an exudate
• Arachnoid fibrosis is responsible for
obstruction and hydrocephalus
• Early-onset GBS meningitis is
characterized by much less arachnoiditis
than late-onset GBS meningitis

Neurologic signs - Vasculitis
• Next phase of the arachnoiditis and
ventriculitis
• Appears within the first days of meningitis,
and become more prominent during the
second and third weeks
• Occlusion of the venous (phlebitis,
thrombosis) and arteries
– Hemorrhagic infarction

Hematologic signs
Thrombocytopenia - 10-60% of
cases
< 100 000/mm3
< 50 000/mm3 - more diagnostic
Duration - 1-3 weeks

Hematologic signs - WBC
• Normal WBC counts may be observed in as
many as 50% of cases of culture-proven
sepsis
• Not infected infants may demonstrate
abnormal WBC counts related to the stress of
delivery.
• Total neutrophil count (PMNs and immature
forms) is slightly more sensitive in
determining sepsis than total leukocyte count

Hematologic signs - Neutrofils
• Abnormal neutrophil - observed in two
thirds of infants
• Does not provide adequate confirmation
of sepsis
• Neutropenia is observed with maternal
hypertension
– severe perinatal asphyxia
– periventricular or intraventricular
hemorrhage

Hematologic signs - Neutrofils
• Neutrophil ratios - the immature-to-total
(I/T) ratio
– Immature neutrophil forms/ all neutrophils
– Tthe most sensitive indicator of sepsis
• Maximum acceptable ratio for excluding
sepsis during the first 24 hours is 0.16
• In most newborns, the ratio falls to 0.12
within 60 hours of life.
• The sensitivity - 60-90%

Gastrointestinal signs
• Colonization of the gut by organisms in
utero or at delivery by swallowing infected
amniotic fluid
• The immunologic defenses of the gut are
not mature, especially in the preterm
infant
• Bacterial overgrowth in the neonatal lumen
is a component of the multifactorial
pathophysiology of NEC

Diagnostic tests - cultures
Blood, CSF, and urine cultures
Aerobic cultures are appropriate for most of the
bacterial etiologies associated with neonatal
sepsis
Anaerobic cultures are indicated in neonates
with
Abscess formation,
Processes with bowel involvement,
Massive hemolysis,
Refractory pneumonia

Diagnostic tests - cultures
A Gram stain provides early
identification of the gram-negative or
gram-positive status of the organism
for preliminary identification
Bacterial cultures should generally
reveal the organism of infection within
36-48 hours
The initial identification occurs within
12-24 hours of the growth

Diagnostic tests - cultures
Urine cultures are most appropriate
when investigating late-onset sepsis
Blood and CSF cultures are appropriate
for early and late-onset sepsis
Because of the low incidence of
meningitis in the newborn infant with
negative cultures, clinicians may elect
to culture the CSF of only those infants
with documented or presumed sepsis

Diagnostic tests - CBC
May be ordered serially to determine changes
associated with the infection, such as
Thrombocytopenia
WBC
neutropenia
left shift of leukocytes
I/T ratio

Diagnostic tests - C-reactive
protein
• CRP - an acute phase protein associated with
tissue injury
• Rises within 24 hours of infection, peaks within
2-3 days, and remains elevated until the
inflammation is resolved
• Not recommended as a sole indicator of
neonatal sepsis,
• Part of a sepsis workup
• Serial study during infection to determine
response to antibiotics, duration of therapy

Imaging studies
Chest radiographs - segmental or lobar
atelectasis, diffuse, fine, reticulogranular pattern,
and pleural effusions may also be observed.
A CT scan - neonatal meningitis
Blocks to CSF flow,
Infarctions
Abscesses
Ventricular dilation
Multicystic encephalomalacia
Atrophy

Imaging studies
• Head ultrasonograms in neonates with
meningitis
– Ventriculitis,
– Abnormal parenchymal echogenicities
– Extracellular fluid
• Serially, head ultrasonograms can
demonstrate the progression of
complications

Procedures
• Lumbar puncture is warranted for early-
and late-onset sepsis
• Difficulties with obtaining sufficient or
clear fluid for all the studies
• Infants shold be positioned on their side
or sitting with support, adequate
restraint is needed to avoid a traumatic
tap.
• Because the cord is lower in the spinal
column in infants, the insertion site
should be between L3 and L4

Procedures
• If positive cultures are demonstrated, a
follow-up lumbar puncture is often
performed within 24-36 hours after
antibiotic therapy to document CSF sterility
• If organisms are still present, modification
of drug type or dosage may be required
• An additional lumbar puncture within 24-
36 hours is necessary if organisms are still
present

Treatment
• Begin antibiotics as soon as diagnostic tests are
performed
• Additional therapies have been investigated for
the treatment of neonatal sepsis; however, no
unequivocal proof that these treatments are
beneficial exists.
• These additional therapies include:
– granulocyte transfusion
– intravenous immune globulin (IVIG)
replacement
– exchange transfusion,
– use of recombinant cytokines

Treatment - early onset
infection
• Antibiotic: aminoglycoside and penicillin
• This provides coverage for:
– Gram-positive organisms, especially GBS
– Gram-negative bacteria, such as E coli.
• The specific antibiotics to be used are
chosen on the basis of maternal history
and prevalent trends of organism
colonization in individual nurseries

Treatment - late onset
infections
• Direct coverage at organisms implicated
in hospital-acquired infections,
– S aureus
– S epidermis
– Pseudomonas sp.
– Klebsiella sp.

Treatment - late onset
infection
• Most strains of S aureus produce beta-
lactamase, which makes them resistant
to penicillin G, ampicillin, carbenicillin,
and ticarcillin
• Vancomycin has been favored for this
coverage
• Overuse of this drug may lead to
vancomycin-resistant organisms

Treatment - late onset
infections
• Cephalosporins - attractive in the
treatment of nosocomial
infection
• Lack of dose-related toxicity
• Adequate serum and CSF concentration
• Resistance by gram-negative organisms
has occurred with their use

Treatment
• Sids effect of Aminoglycosides and Vancomycin
– Ototoxicity
– Nephrotoxisity
• Have caution when using them
• Check the serum level after 48 hours of treatment
to determine if levels are above those required
for a therapeutic effect
• The dosage amount or interval may need to be
changed to ensure adequate but nontoxic
coverage

Treatment
• A serum level may be warranted when
the infant's clinical condition has not
improved to ensure that a therapeutic
level has been reached
• In addition, perform renal function and
hearing screening to determine any
short- or long-range toxic effects of
these drugs

Treatment
• Negative Cultures + Significant risk for sepsis
and/or clinical signs,
– The clinician must decide whether to
provide continued treatment
– Three days of negative cultures should
provide confidence in the data
• A small number of infants with proven sepsis
at postmortem had negative cultures during
their initial sepsis workup

Treatment
•
Mother received antibiotic
therapy before delivery,
especially close to delivery
•
This may result in negative cultures in the infant who
is still ill
•
Review all diagnostic data, including cultures,
maternal and intrapartal risk factors, CSF results, the
CBC and differential radiographs, and the clinical
picture to determine the need for continued therapy
•
Treatment for 7-10 days may be appropriate, even if
the infant has negative cultures at 48 hours.

Treatment
• Bacterial meningitis
– Different antibiotic choice
– Different dosage
– Different treatment time
•14 - 21 days

Treatment - Meningitis
• Perform a follow-up lumbar puncture within 24-36
hours after antibiotic therapy has been initiated
to determine if the CSF is sterile
• If organisms are still present, modification of drug
type or dosage is required to adequately treat the
meningitis
• Continue antibiotic treatment for 2 weeks after
sterilization of the CSF or for a:
– minimum of 2 weeks for gram-positive
meningitis
– 3 weeks for gram-negative meningitis

Treatment - Meningitis
• Chloramphenicol or trimethoprim-
sulfamethoxazole has been shown to be
effective in the treatment of highly
resistant bacterial meningitis

Treatment
Indications:
Depletion of the storage neutrophil pool
Difficulties
Granulocyte transfusion - remains an
experimental treatment
Documentation of storage pool depletion requires a
bone marrow aspiration,
Must be administered quickly to be beneficial
Potential adverse effects
Graft versus host reaction
Transmission of CMV or hepatitis B
Pulmonary leukocyte sequestration

Treatment - IVIG
Has been considered to provide type-
specific antibodies to improve
opsonization and phagocytosis of bacterial
organisms
complement activation
chemotaxis of neonatal neutrophils
The effect has been transient,
Adverse effects associated with the
infusion of any blood product can occur

Treatment
Recombinant human cytokine
Stimulation of granulocyte progenitor cells
Benefit in animal models, especially for GBS
sepsis,
Require pretreatment or immediate treatment
to demonstrate efficacy
Granulocyte-macrophage colony-stimulating
factor (GM-CSF) and granulocyte colony-
stimulating factor (G-CSF) has been studied in
clinical trials, but their use in clinical
neonatology remains experimental
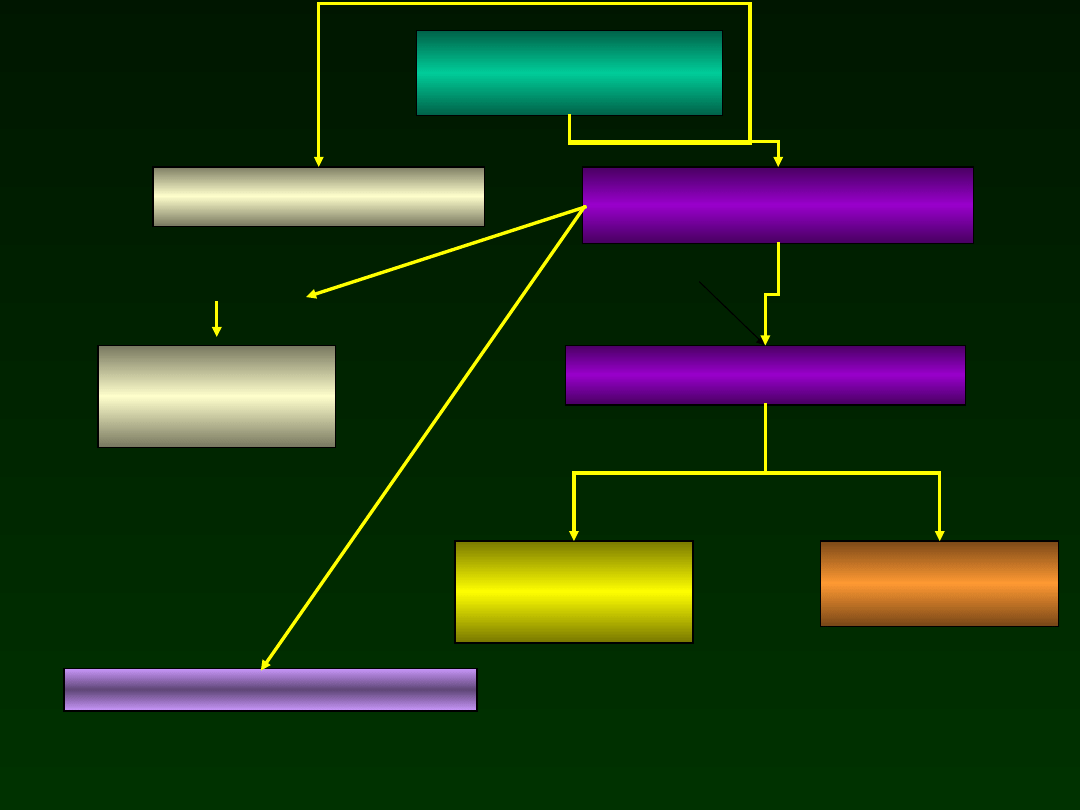
Suspected
early infection
CBC, CRP,Cultures
blood, gastric aspirate
Penicylin + aminoglikosid
Repeat CRP after 24-48 H.
LP
Continue antibiotics
Modification of antibioticotherapy
CRP (-)
CRP
(+)
CRP
(+)
LP
Contune antibiotics
CRP (-)
DC
antibiotics
Culture
(+)
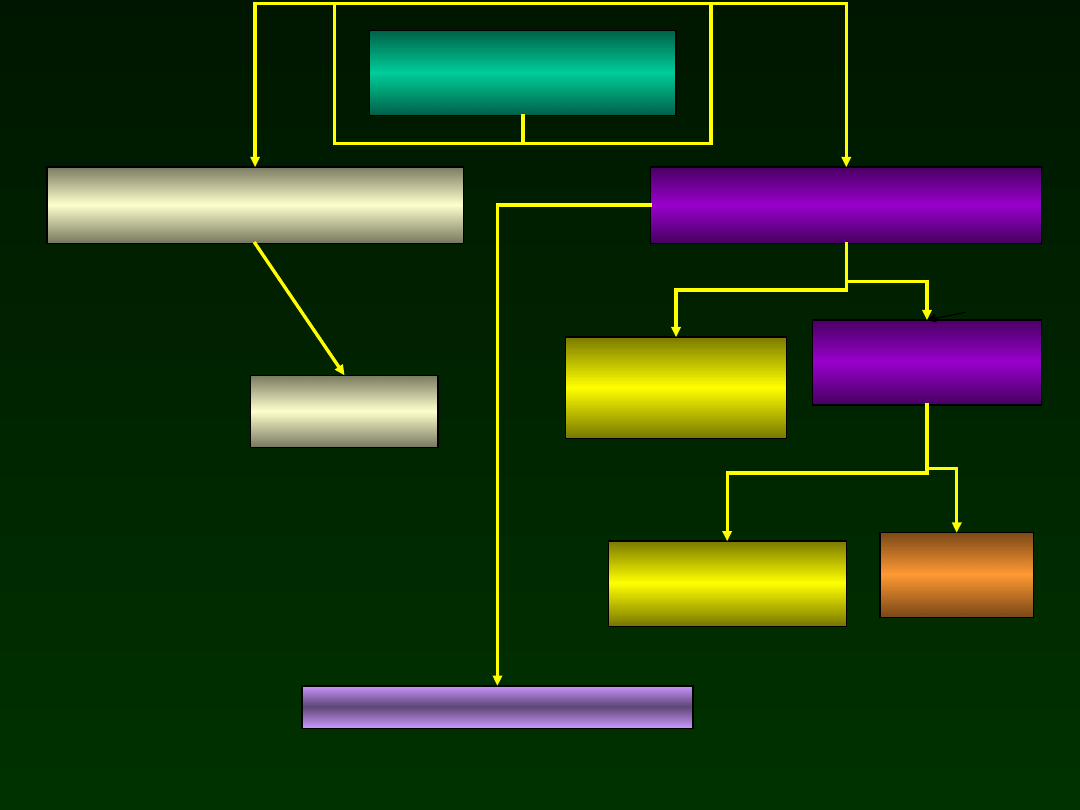
Suspected late infection
CBC, CRP, Cultures
Blood, Urine
Penicilin + betalactamase inhibitor
aminogliside
Repeat CRP after
24-28 godz.
LB
Antibitics
Modify anitibiotics
CRP (-)
CRP (+)
CRP (+)
Continue antibiotics
CRP (-)
DC
antibiotics
Posiew (+)
Imipenem +
aminoglikozyd
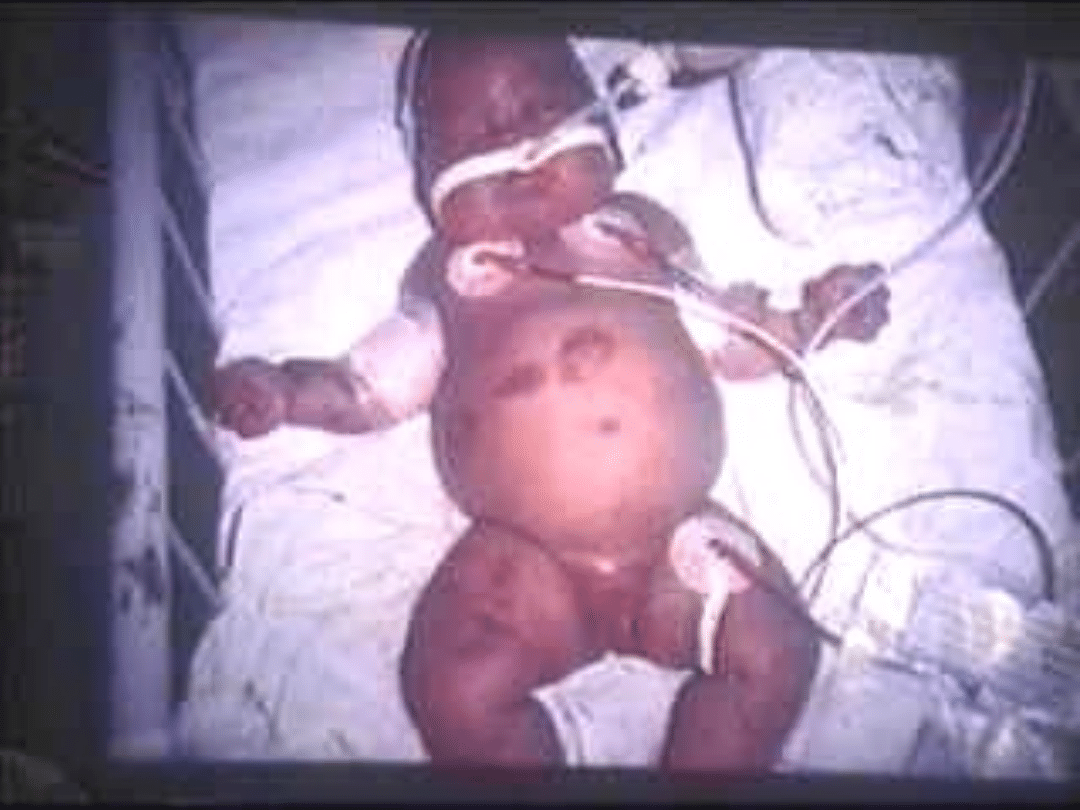
Septic shock
Severe gastrointestinal symtoms

Indications for Carbapenems
• Rapid progression of infection symptoms
• Sever gastrointenstinal problems
• Septic shock
• Symptoms of DIC
• Result of blood culture – strain ESBL

Wankomycin - indication
• Blood culture – strain MRS
– Lack of improvement
– Increase of CRP

Rational antibiotic therapy
• Restrictive
– Length of therapy
• Decision within the 48-72 H
• Therapy 4-10dni
– Avoid large spectrum antibiotics
– According to the blood culture result
– Do not use prophylactic antibiotic
therapy

Supportive care
Monitoring of blood pressure, vital signs
Minimal touching
Thermal comfort
Cardiopulmonary support
Katecholamine
Mechanical ventilation
Intravenous nutrition
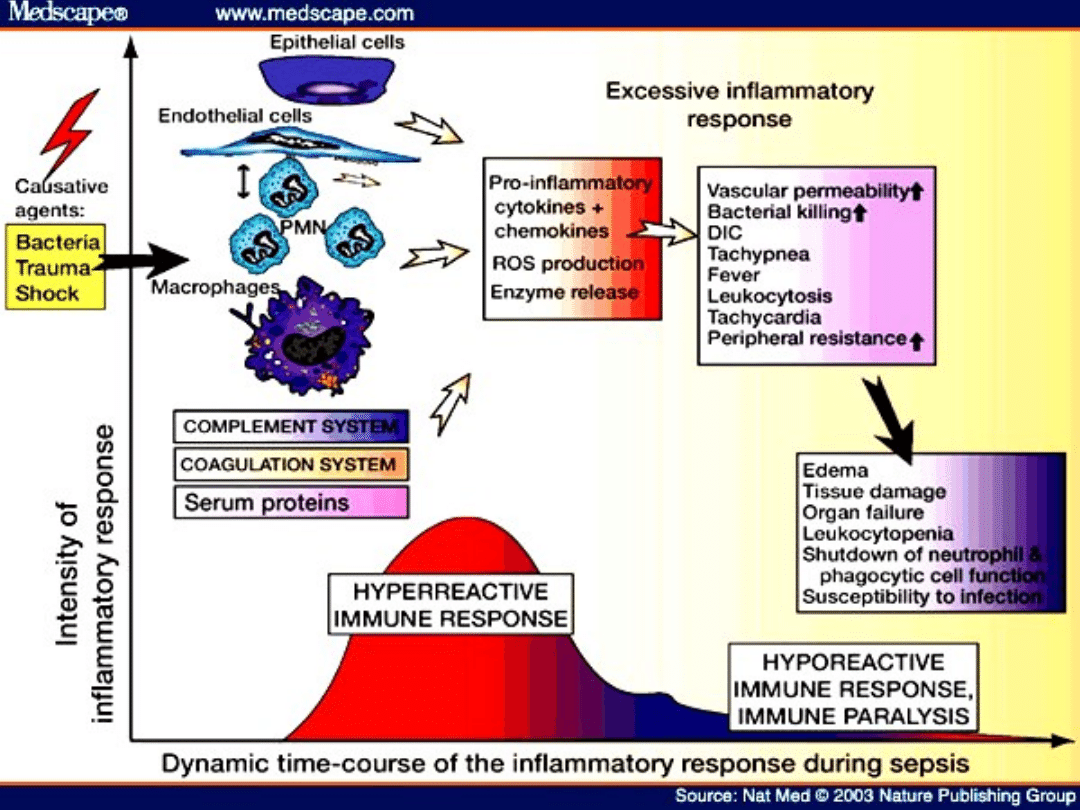
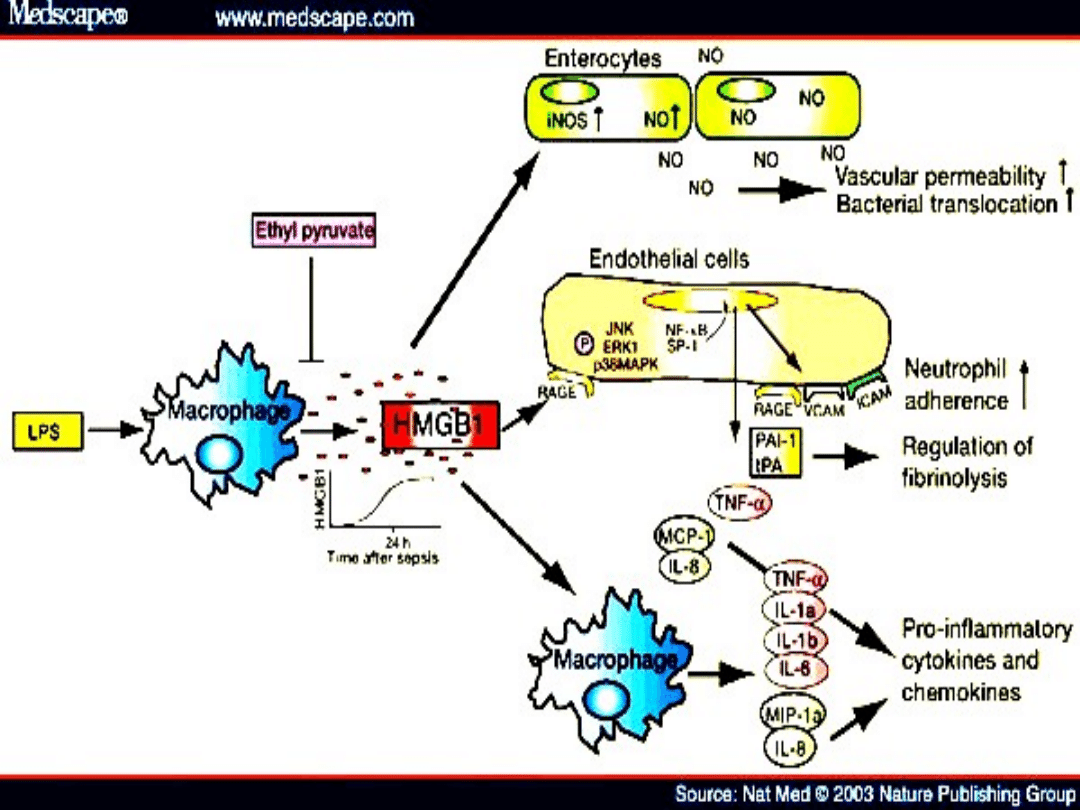
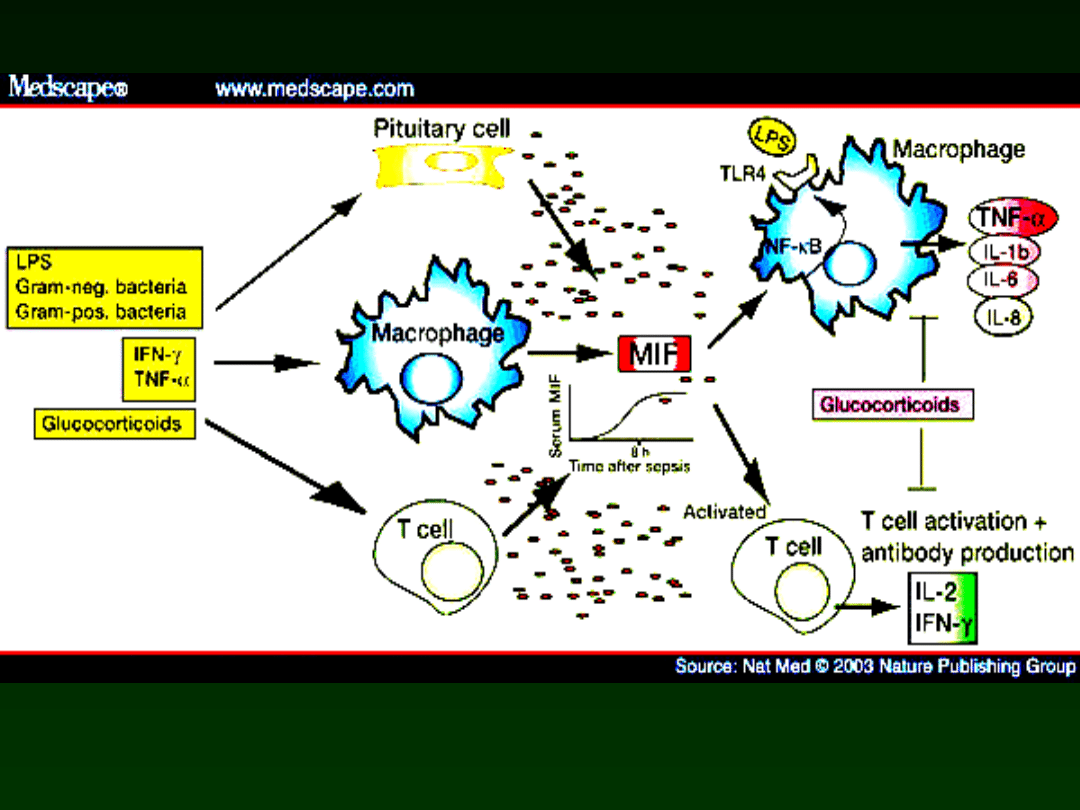
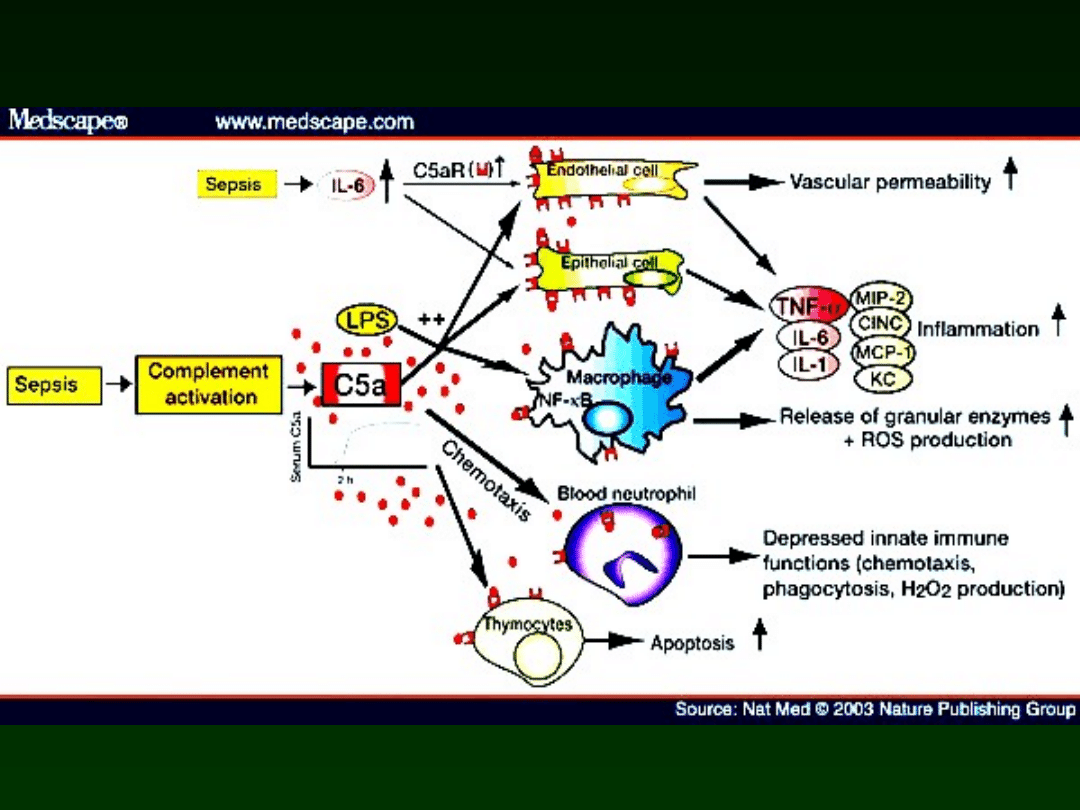
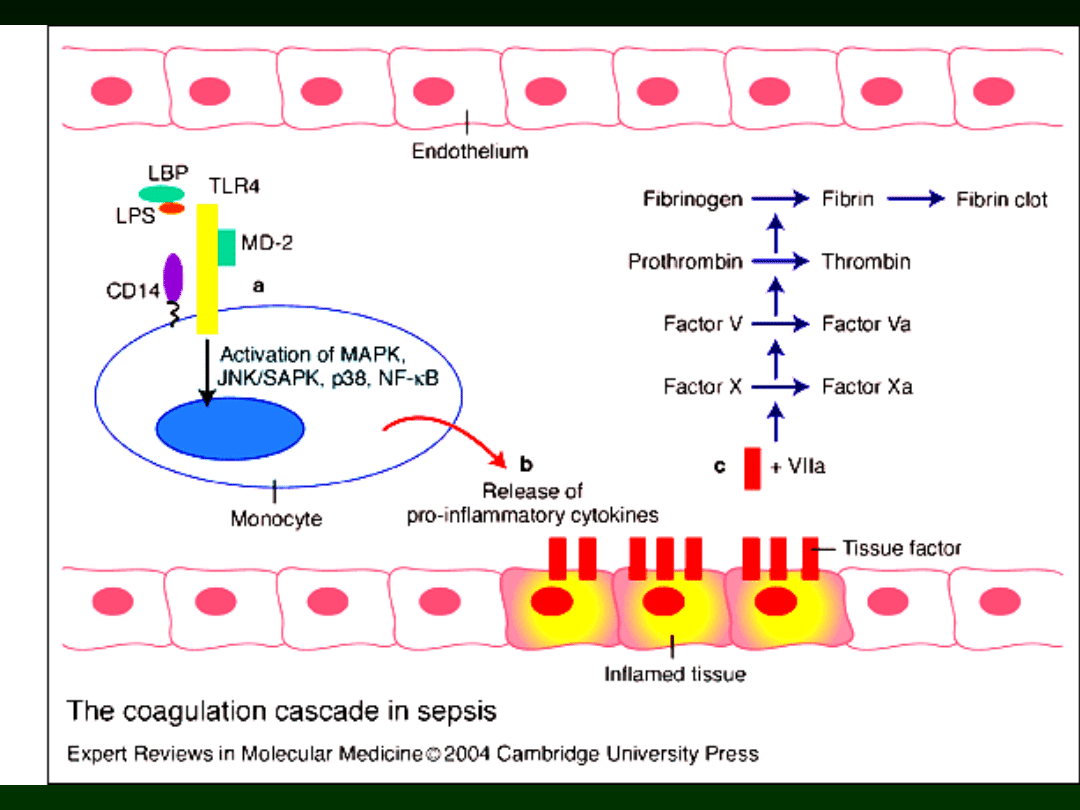

Immunity of the neonate

Neutrophils
• Immature chemotaxis and killing capacity
• Decreased adherence to the endothelial
lining of blood vessels
• Reduced ability to marginate and leave
the intravascular area to migrate into the
tissues
• Decreased deformability
• Depresed migration

Neutrophils
• Impaired phagocytosis and killing of
bacteria especialy in clinically ill infant
• Lastly, neutrophil reserves are depleted
easily because of the diminished
response of the bone marrow, especially
in the premature infant

Macrophages
• Neonatal monocyte concentration and function
are at adult levels
• Macrophage chemotaxis is impaired and
continues to exhibit decreased function into early
childhood
• Macrophages are decreased in the lungs, in the
liver and spleen.
• The chemotactic and bacteriocidal activity and
the antigen presentation are not fully competent
• Cytokine production is decreased, which may be
associated with a corresponding decrease in T-cell
production

Limphocytes T
• Decreased number of T cells with the memory
cell surface phenotype
• The antigenically naive cells do not proliferate
as readily as adult T cells when activated
• Decreased production of cytokines
– B-cell stimulation and differentiation
– Bone marrow stimulation to granulocyte/monocyte
proliferation
• A delay of the formation of antigen specific
memory function following primary infection

Limphocytes B
• Decreased production of immunoglobulin
• Transfer of immunoglobulins (IgG) from
the mother 16 week of gestation
• The infant born prematurely has less IgG
due to the shorter period of placental
transmission of immunoglobulin
• Immunosuppressed mother
– less IgG can be transmitted to the infant

Limphocytes B
• Low level of IgM at birth
– Intrauterin infection - stimulation of IgM production
• IgG and immunoglobulin E (IgE) may be
synthesized in utero; however, only traces are
found in cord blood
• Immunoglobulin A (IgA)
– Transfer by breastfeeding
– Lack of secretion of IgA until 2-5 weeks after birth.
• Diminished response to bacterial polysaccharide
(2 years)

Natural killers
• Natural killer (NK) cells are found in
greater concentration in the peripheral
blood of neonates than in that of adults
• Diminished expression of the
membrane’s receptors
– Reducing cytolytic activity

Complenet system
• Synthesis of complement protein - 6 week of
gestational age
• Wide variability among individual neonates in the
concentration of the components of the
complement system
• Classic pathway - comparable to adult
• Decreased activity of the alternative pathway
• Decreased the terminal activity for complement
• Maturation of complement activity until 6-10
months

Opsonic properties
• Lower concentration of the proteins of
alternative pathway of complement
system
• Lower concentration of Fibronectin,
• Reduced opsonic efficiency against GBS,
E coli, and S pneumoniae

The natural barriers
• Skin and mucus membranes are broken
down easily in the premature infant
• Neonates who are ill and/or premature are
additionally at risk because of the invasive
procedures that breach their physical
barriers to infection
• Immaturity of the respiratory and
gastrointestinal system
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
- Slide 78
- Slide 79
- Slide 80
- Slide 81
- Slide 82
- Slide 83
- Slide 84
- Slide 85
- Slide 86
- Slide 87
- Slide 88
- Slide 89
- Slide 90
- Slide 91
- Slide 92
- Slide 93
- Slide 94
- Slide 95
- Slide 96
- Slide 97
- Slide 98
- Slide 99
Wyszukiwarka
Podobne podstrony:
Cardivascular problems in the neonates
20 Seasonal differentation of maximum and minimum air temperature in Cracow and Prague in the period
Żurawski vel Grajewski, Przemysław Poland in the Period of Partitions 1795–1914 (2015)
DANN Changing patterns of violence at Qustul and Ballana in the post Meroitic period Part One The Hu
The Fate of Psychiatrie Patients During the Nazi Period in Styria Austria; Part I, German Speaking
The Fate of Psychiatrie Patients During the Nazi Period in Styria Austria; Part 2, The Yugoslav Reg
A Study of Detecting Computer Viruses in Real Infected Files in the n gram Representation with Machi
Dyson, Rebecca M i inni Interactions of the Gasotransmitters Contribute to Microvascular Tone (Dys)
Mettern S P Rome and the Enemy Imperial Strategy in the Principate
Early Variscan magmatism in the Western Carpathians
Applications and opportunities for ultrasound assisted extraction in the food industry — A review
In the end!
Cell surface in the interaction Nieznany
Post feeding larval behaviour in the blowfle Calliphora vicinaEffects on post mortem interval estima
Aftershock Protect Yourself and Profit in the Next Global Financial Meltdown
Multiple Intelligences in the Elementary Classroom
Fascia in the Lateral Upper Arm tapeSP
A Guide to the Law and Courts in the Empire
Functional improvements desired by patients before and in the first year after total hip arthroplast
więcej podobnych podstron