Program ćwiczeń z mikrobiologii dla biotechnologów
(II rok)
Ć
wiczenie 1
Metody sterylizacji szkła laboratoryjnego i pożywek mikrobiologicznych.
Podłoża i pożywki mikrobiologiczne.
Praca w warunkach jałowych.
Ć
wiczenie 2
Formy morfologiczne bakterii.
Podział bakterii na gram ujemne i gram dodatnie. Barwienie komórek bakteryjnych.
Budowa komórki bakteryjnej.
Ć
wiczenie 3
Wpływ czynników fizykochemicznych na bakterie.
Ć
wiczenie 4
Metody hodowli bakterii – w podłożu płynnym, hodowla beztlenowców
Posiew na szereg biochemiczny- badanie właściwości biochemicznych wybranych
pałeczek jelitowych
Morfologia kolonii bakteryjnych na różnych podłożach mikrobiologicznych.
Ć
wiczenie 5
Oznaczanie wrażliwości bakterii na chemioterapeutyki (antybiotyki, sulfonamidy, fitoncydy,
bakteriocyny)
Bakteriofagi- oznaczanie wrażliwości bakterii na bakteriofagi, miano lizatu fagowego,
streak-test.
Ć
wiczenie 6
Podstawowe odczyny serologiczne.
Baketrie z rodzajów Neisseriae i Corynebacterium
Ziarniaki α,β,γ-hemolizujące.
Ć
wiczenie 7
Zaliczenie – kolokwium (wspólne dla wszystkich grup)

Ćwiczenie 1
Przygotowanie do pracy w laboratorium mikrobiologicznym
Zapoznanie studentów z instrukcją BHP
I. Metody hodowli mikroorganizmów - rodzaje podłoży mikrobiologicznych
(
DEMONSTRACJA):
a) podłoża płynne i stałe
b) podłoże zwyczajne (LA - Luria agar), wybiórczo-różnicujące (MacConkey’a,
Chpmana), wybiórcze (selektywne; Sabouroda).
II. Sterylizacja w autoklawie i aparacie Kocha
Mamy do dyspozycji sześć probówek z jałowym bulionem.
probówki: 1, 2, 3 należy zaszczepić hodowlą nocną Escherichia coli (po 100µl),
probówki: 4, 5, 6 zaszczepić hodowlą nocną Bacillus subtilis (po 100µl).
a) probówki 1 i 4 jałowić w autoklawie przez 30 min. w temp. 121
o
C
b) probówki 2 i 5 jałowić w aparacie Kocha przez 30 minut.
c) probówki 3 i 6 - nie jałowić (kontrola).
Probówki inkubować w wytrząsarce w 37
o
C przez 24 godziny, a następnie schować do
lodówki. Wyniki doświadczenia będą omówione na następnych ćwiczeniach. Hodowle
wyjściowe badanych bakterii również zostaną przechowane do następnych ćwiczeń w
celu wybarwienia przetrwalników i wykonania preparatów mikroskopowych.
III. Sterylizacja przez sączenie (DEMONSTRACJA)
IV. Posiew bakterii na podłoże stałe:
a) posiew redukcyjny Escherichia coli - każdy student wykonuje posiew na podłożu
LA
b) posiew w postaci murawy – każda para wysiewa na podłoże LA
- 0,1 ml hodowli E. coli
- 0,1 ml hodowli Bacillus subtilis (do wyboru bakterie po autoklawowaniu, po
gotowaniu w aparacie Kocha, hodowle kontrolne)
c) łapanie bakterii z powietrza każda para ma do dyspozycji 1 płytkę
d) posiew na skos E. coli.
e) posiew na słupek E. coli.
Każda para ma do dyspozycji 6 płytek LA
V. Obserwacja wzrostu mikroorganizmów, morfologia kolonii na podłożach stałych i
płynnych
a) podłoże Chapmana - (Staphylococcus, Micrococcus sp.)
b) podłoże McConkeya (E. coli - lac
+
,
Serratia marcescens).
c) podłoże Sabourouda (Candida sp., E. coli).
d) Agar wzbogacony
Pałeczki
E.coli, Erwinia lejąca się, Serratia marcescens, Proteus vulgaris, Salmonella anatum,
Klebsiella oxytoca, Flavobacterium okeanokoites, Enterobacter spp. Pseudomonas
opalić ezę
opalić ezę
Inkubacja w odpowiednich warunkach
opalić ezę
Posiew redukcyjny
Wzrost bakterii

aeruginosa, Pseudomonas spp. Brunatny, Pseudomonas spp.( Fluoryzujący),
Xanthomonas,
Laseczki
Bacillus subtilis, Bacillus cereus, Bacillus stearothermophilus, Bacillus spp.
Ziarniaki
Micrococcus sp, Micrococcus luteus, Staphylococcus aureus, Staphylococcus
epidermidis, Gafkya tetragena, Sarcina spp.
Drożdzaki
Candida sp. Candida albicans.
Bakterie dnia:
Escherichia coli, Bacillus subtilis, Bacillus cereus, Bacillus stearothermophilus,
Bacillus spp.
WIADOMOŚCI TEORETYCZNE.
1. Mycie i sterylizacja szkła laboratoryjnego.
a) szkło nowe - posiada odczyn zasadowy - eliminacja przez zanurzenie w 1% HCl lub 15
minutowe gotowanie.
b) szkło używane - 24h moczenie w chromiance (dwuchromian potasu, kwas siarkowy i
woda).
Sterylizacja - (łac. sterylis - jałowy) - proces zabicia drobnoustrojów (formy wegetatywne i
przetrwalnikowe).
Metody sterylizacji:
a) fizyczne - sterylizacja cieplna (sucha) lub z parą wodną,
sterylizacja UV,
sterylizacja promieniami jonizującymi,
sterylizacja ultradźwiękami.
b) mechaniczne (filtracja),
c) chemiczne (dezynfekcja).
Ad a) Sterylizacja cieplna-sucha:
* wyżarzanie (ezy, igły, skalpele)
* opalanie (brzeg probówki, bagietki)
* suszenie (szkło laboratoryjne)
140oC - 2,5h, 170oC - 1,0h
Sterylizacja parą wodną
* gotowanie (strzykawki, instrumenty chirurgiczne)
* autoklawowanie (pożywki)
0,7 atm. - 117oC; 3,0 atm - 134oC
* jałowienie w aparacie Kocha (pożywki do 100oC).
Pasteryzacja - stosowana w celu zniszczenia form wegetatywnych w płynnych środkach
spożywczych (np. w mleku) - jednorazowe podgrzanie do 60-80oC.
Tyndalizacja - pasteryzacja frakcjonowana. Niszczy formy wegetatywne i przetrwalnikowe
–
3-krotna pasteryzacja w odstępach 24h.
Sterylizacja UV (długość fali 250nm) - uszkadza strukturę kwasów nukleinowych (DNA) -
stosowana do sterylizacji pomieszczeń, naczyń z tworzyw sztucznych i plastikowych.
Najmniej odporne są zarodniki pleśni.
Ultradźwięki - fale dźwiękowe powyżej 20 tys. Hz - metoda oparta na zjawisku kawitacji.
Polega na rozrywaniu roztworu przez powstanie w nim pęcherzyków gazów, co prowadzi

do mechanicznego rozerwania komórek od wewnątrz. Metodą tą nie można zabić
przetrwalników.
Ad b) Filtracja (podłoża płynne np. surowica, roztwór mocznika, witaminy) - przy filtracji
często stosuje się podciśnienie.
* filtry z ziemi okrzemkowej (Berkefelda),
* filtry z porcelany (Chamberlanda),
* filtry teflonowe
* filtry ze spiekanego szkła (schotta),
* filtry membranowe (molekularne) - z pergaminu, żelatyny, błon zwierzęcych
(zatrzymują wirusy).
Ad c) Dezynfekcja (chemiczna metoda sterylizacji) - jest to proces oczyszczania
powierzchni stołów, narzędzi od drobnoustrojów zdolnych wywołać zakażenie (nie niszczy
form przetrwalnych).
Na siłę działania środków bakteriobójczych (dezynfekujących) mają wpływ następujące
czynniki:
* rodzaj i wrażliwość drobnoustrojów,
* czas działania środka chemicznego,
* temperatura środowiska,
* stężenie środka dezynfekującego.
Ś
rodki dezynfekujące pomieszczenia i przedmioty:
* kwasy i zasady - 10% roztwory zasad, mleko wapienne - niszczą przedmioty
* środki utleniające - po zetknięciu z komórkami drobnoustrojów wydzielają zjonizowany
tlen, w wyniku czego następuje uszkodzenie struktury błon cytoplazmatycznych (niszczą
też przetrwalniki - działają tak jak ozon). Podchloryny, chloraminy, jodyna (10% roztwór
jodu), 3% woda utleniona.
* sole metali ciężkich (głównie srebra i rtęci) - precypitacja i inaktywacja białek.
* organiczne związki dezynfekujące:
- alkohole - denaturacja białek.
- fenole i krezole - trucizny protoplazmatyczne - wchodzą w reakcje ze ścianą komórkową
(niszczą formy wegetatywne bakterii i grzybów, na przetrwalniki oddziaływają słabo).
Przykłady: fenol, lizol, formaldehyd.
* detergenty - czwartorzędowe związki amoniowe (posiadają dużą aktywność
powierzchniową) - łączy się je z chlorowcami. Uszkadzają błony komórkowe, ale nie
niszczą spor. Przykłady: Zephirol, Desogen, Sterinol.
Ś
rodki dezynfekujące powietrze - gazy, para, aerozole - glikol propylenowy, trietylenoglikol,
podchloryn sodu, sterinol, kwas mlekowy.
Siłę działania związku dezynfekcyjnego określa się przez porównanie jego działania do
działania fenolu - tzw. współczynnik fenolowy (stosunek największego rozcieńczenia
badanego związku zabijającego mikroorganizmy w ciągu 10 min. do największego
rozcieńczenia fenolu zabijającego mikroorganizmy w 10 min.
2. Pożywki i podłoża mikrobiologiczne.
Pożywki (podłoża) - płynne lub zestalone mieszaniny złożone z odpowiednio dobranych
składników, służących hodowli drobnoustrojów in vitro (w szkle).
Pożywki muszą:
a) zawierać związki odżywcze (pierwiastki biogenne C,N,O,H,S,P). Jako Źródła węgla,
azotu, aminokwasów i witamin stosuje się pepton. Jest to produkt enzymatycznej
hydrolizy białek za pomocą pepsyny i HCl. Jest to mieszanina proteaz, polipeptydów i

aminokwasów.
b) mieć odpowiednie pH (z reguły 7,2-7,4).
c) być jałowe,
d) obyć izotoniczne (podobne ciśnienie jak w komórkach drobnoustrojów, zwykle uzyskuje
się przez dodanie soli NaCl). Podłoże hipotoniczne (o niższym ciśnieniu osmotycznym,
niż w komórkach) powoduje pęcznienie komórek, a nawet ich pękanie. W podłożu
hipertonicznym (o wyższym ciśnieniu osmotycznym, niż w komórkach) następuje
kurczenie się plazmy komórkowej i oddzielanie od ściany komórkowej (plazmoliza).
e) być jednorodne.
Podział pożywek ze względu na charakter składników:
* naturalne (wyciąg z krwi, z tkanek roślinnych i zwierzęcych, mleko),
* syntetyczne (mieszanina substancji organicznych i nieorganicznych),
* półsyntetyczne (mieszane).
Podział pożywek ze względu na wymagania odżywcze drobnoustrojów:
* proste - bulion odżywczy, agar odżywczy.
* złożone - jak wyżej plus witaminy, substancje wzrostowe itp. Wśród nich wyróżnia się:
- podłoża selektywne (wybiórcze) - które zawierają 1 lub 2 składniki hamujące rozwój
drobnoustrojów, które chcemy wyeliminować z hodowli.
- podłoża różnicujące (identyfikacyjne) - zawierają charakterystyczną substancje, która jest
enzymatycznie rozkładana wyłącznie przez określone gatunki drobnoustrojów.
Autotrofy - nie wymagają do wzrostu związków organicznych.
Prototrofy - wymagają do wzrostu 1 związku organicznego (rosną na ubogich pożywkach).
Heterotrofy - wymagają do wzrostu obecności w pożywce związków organicznych: (cukry -
Ź
ródło węgla), (aminokwasy - żądło azotu), witamin i innych.
Auksotrofy - to heterotrofy, które potrzebują poza jednym stosunkowo prostym związkiem
organicznym, jeszcze co najmniej jednego związku organicznego, jak np. aminokwasy lub
witaminy.
Hypotrofy - bezwzględne pasożyty - bytują w organizmie gospodarza.
Podział pożywek ze względu na konsystencję:
- płynne (bulion, podłoże mineralne, brzeczka).
- stałe (zestalone) - agar, podłoże żelatynowe.
- półpłynne - zawierają 0,15-0,2% agaru.
Agar - wielocukier zawierający galaktozę, resztę siarczanową, jony Ca+2 i Mg+2
(uzyskuje się go z krasnorostów). Rozpuszczalny w wodzie w temperaturze 95 - 99oC,
krzepnie zaś w temperaturze 45 - 49oC. Tylko nieliczne bakterie morskie i glebowe go
rozkładają. W środowisku kwaśnym ulega hydrolizie i traci zdolność do tworzenia żelu.
ż
elatyna - białko proste otrzymywane z chrząstek. Rozpuszcza się w ciepłej wodzie, a w
temperaturze 25oC tworzy galaretowaty żel. Jest upłynniana i rozkładana przez bakterie i
grzyby wytwarzające enzymy proteolityczne (hydrolizujące białko). Nie nadaje się do
hodowli drobnoustrojów, ale ma zastosowanie do badania proteolitycznych właściwości
drobnoustrojów.
Podłoże McConkey - zawiera sole żółci, które hamują rozwój większości bakterii. Na
bazie tego podłoża przygotowuje się pożywkę wybiórczą i różnicującą.
*wybiórcza - dezoksycholan sodu pozwala na rozwój pałeczek z rodzaju Enterobacteriae
(żyjące w przewodzie pokarmowym człowieka) i Enterocoki.
*różnicująca - zawiera laktozę i wskaźnik barwny - czerwień obojętną. Bakterie lac+
(rozkładają laktozę - zmiana zabarwienia pożywki na kolor fioletowy), bakterie lac- (bez

zmian).
Podłoże Chapmana - dla gronkowców.
*wybiórcza - wysokie stężenie NaCl (7,5%) - hamuje rozwój większości drobnoustrojów
(rosną gronkowce).
*różnicująca - mannitol 1% - substancja diagnostyczna i różnicująca. Część gronkowców
rozkłada mannitol i następuje zmiana pH pożywki, a w efekcie obserwujemy zmianę
zabarwienia (wskaźnik barwny - czerwień fenolowa).
Podłoże Sabourouda - podłoże do hodowli drożdży i grzybów.
*wybiórcza - niskie pH (4,4 - 4,5) i obecność glukozy.
OBSERWACJE I WNIOSKI.
Zagadnienia teoretyczne.
Czym są drobnoustroje? Organizmy prokariotyczne i eukariotyczne. Do czego służą podłoża mikrobiologiczne. Czym jest czysta
kultura danego drobnoustroju, czym jest kultura mieszana. Rodzaje pożywek mikrobiologicznych: płynne i stałe; naturalne,
syntetyczne i półsyntetyczne; minimalne, pełne, wzbogacone i specjalne (różnicujące, wybiórcze = selektywne, wybiórczo-
różnicujące); Czym jest i do czego służy agar. Jakie warunki powinna spełniać pożywka mikrobiologiczna, aby zapewnić warunki,
optymalne dla wzrostu badanych mikroorganizmów? Autotrofy i heterotrofy; prototrofy i auksotrofy.
Co oznacza: sterylizacja = jałowienie, pateryzacja, tyndalizacja, dezynfekcja, sanityzacja, aseptyka, antyseptyka - w
jakim celu je się wykonuje? Jakie są sposoby sterylizacji (fizyczne, chemiczne, mechaniczne?. Do czego służą: autoklaw
i aparat Kocha. W jaki sposób jałowi się: wodę i roztwory soli i pożywki (lub składniki pożywek) termostabilne (odporne
na wysoka temperaturę); w jaki sposób sterylizuje pożywki lub składniki pożywek wrażliwe na wysoką temperaturę
(termolabilne). W jaki sposób sterylizuje się szkoło laboratoryjne, narzędzia metalowe, pomieszczenia laboratoryjne.
Przykłady zastosowania dezynfekcji. Rodzaje posiewów bakteriologicznych. W jakim celu wykonuje się posiew
redukcyjny. Co oznacza termin „inokulacja”. Co wiesz o bakteriach Escherichia coli i Bacillus sp.
Ćwiczenie 2
Formy morfologiczne bakterii.
Podział bakterii na gram ujemne i gram dodatnie. Barwienie komórek bakteryjnych.
Budowa komórki bakteryjnej.
Materiał do ćwiczeń
Pałeczki
E.coli, Erwinia chrysanthemii - lejąca się, Serratia marcescens, Proteus vulgaris,
Salmonella anatum, Klebsiella oxytoca, Flavobacterium okeanokoites, Enterobacter
spp. Pseudomonas aeruginosa, Pseudomonas spp. Brunatny, Pseudomonas spp.(
Fluoryzujący), Xanthomonas,Citrobacter freundii
Laseczki
Bacillus subtilis, Bacillus cereus, Bacillus stearothermophilus, Bacillus spp.
Ziarniaki
Micrococcus sp, Micrococcus luteus, Staphylococcus aureus, Staphylococcus
epidermidis, Gafkya tetragena, Sarcina spp.
Krętki
Vibrio harveyi, Vibrio fischeri,
Drożdzaki
Candida glabrata. Candida albicans., Sacharomuces cerevisiae
I. Wygląd kolonii różnych gatunków bakterii, wyrosłych na podłożach agarowych
Każdy student samodzielnie dokonuje opisu wyglądu kolonii bakteryjnych, z
uwzględnieniem ich: zabarwienia; kształtu (okrągły, nieregularny, owalny); brzegu
kolonii (gładki, falisty, poszarpany); przekroju (płask, stożkowa, wypukła);

powierzchni (lśniąca, matowa, pomarszczona, grudkowata); konsystencji (miękka,
sucha, śluzowata,); zapachu
II. Barwienie złożone bakterii metodą Grama
1. Bakterie nanieść na szkiełko podstawowe.
•
W przypadku wykonywania preparatu z hodowli płynnej, wystarczy nanieść na szkiełko
kroplę hodowli, pobraną ezą i rozprowadzić zawiesiną na powierzchni szkiełka.
•
W przypadku wykonywania preparatu z bakterii, wyrosłych na podłożu stałym,
należy pobrać materiał jałową ezą, a następnie zawiesić bakterie w kropli soli
fizjologicznej (0,85% NaCl), naniesionej na szkiełko podstawowe.
2. Po wyschnięciu, preparat utrwalić poprzez przeciągnięcie szkiełka podstawowego
nad płomieniem palnika. Nie trzymać szkiełka w płomieniu!
3. Na utrwalone bakterie nanieść fiolet krystaliczny, tak aby całkowicie pokrył
powierzchnię z bakteriami. Barwnik pozostawić przez 2 minuty.
4. Zmyć fiolet krystaliczny wodą destylowaną.
5. Nanieść płyn Lugola i pozostawić przez 1 minutę. Spłukać wodą destylowaną.
6. Spłukać obficie alkoholem etylowym (odbarwianie), a następnie wodą destylowaną.
7. Nanieść roztwór fuksyny zasadowej i pozostawić na 40 sekund. Spłukać wodą i
pozostawić preparat do wyschnięcia.
Po barwieniu fioletem i dobarwianiu płynem Lugola wszystkie komórki bakteryjne są zabarwione na fioletowo. Pod wpływem
alkoholu z acetonem odbarwiają się wyłącznie bakterie Gram-ujemne. Ściana komórkowa bakterii Gram-dodatnich zatrzymuje
kompleks filetu z jodem i komórki pozostają zabarwione na fioletowo. Odbarwione komórki bakterii Gram-ujemnych wybarwiają się
fuksyną na kontrastowy, różowoczerwony kolor.
III.
Barwienie proste bakterii błękitem metylenowym.
1. Bakterie nanieść na szkiełko podstawowe.
2. Po wyschnięciu, preparat utrwalić poprzez przeciągnięcie szkiełka podstawowego
nad płomieniem palnika. Nie trzymać szkiełka w płomieniu!
3. Nanieść roztwór błękitu metylenowego i pozostawić na 5 minut.
4. Delikatnie spłukać wodą destylowaną i pozostawić preparat do wyschnięcia.
IV.
Barwienie pozytywno-negatywne w celu uwidocznienia otoczek bakteryjnych
(met. Manevala)
1. Na szkiełku przedmiotowym zmieszać 1 kroplę odczynnika Maneval A (1% r0ztwór
wodny czerwieni Kongo z 1 kroplą hodowli badanych bakterii.
2. Po rozprowadzeniu próby na szkiełku przedmiotowym pozostawić preparat do
wyschnięcia.
3. Następnie nakroplić na szkiełko odczynnik Maneval B (5% roztwór fenolu, 20%
kwas octowy, 30% chlorek żelazowy, 1% kwaśna fuksyna) i pozostawić na 5
minut.
4. Preparat spłukać wodą i wysuszyć.
W wyniku barwienia komórki bakteryjne wybarwiają się na czerwono, tło
preparatu jest niebieskie, zaś otoczki bakteryjne pozostają bezbarwne.
Barwimy Klebsiella oxytoca i cyanobakterie

V.
Barwienie przetrwalników metodą Dornera
1. W probówce zmieszać 0.3 ml zawiesiny bakteryjnej w soli fizjologicznej oraz 0.3 ml
stężonej fuksyny karbolowej.
2. Probówkę umieścić w łaźni wodnej o temperaturze 70
o
C i inkubować przez 20 minut.
3. Pobrać ezą zawiesinę bakteryjną i umieścić ją na szkiełku przedmiotowym.
4. Dodać kroplę roztworu nigrozyny, zmieszać ją z zawiesiną bakteryjną a następnie
rozprowadzić na szkiełku przedmiotowym.
5. Preparat wysuszyć na wolnym powietrzu,
6. Dodać kroplę olejku immersyjnego i oglądać w mikroskopie.
W wyniku barwienia obserwuje się na ciemno-szarym od nigrozyny tle czerwone
przetrwalniki i najczęściej bezbarwne komórki bakterii.
VI.
Obserwacja mikroskopowa preparatów barwionych.
1. Barwione preparaty bakterii oglądamy pod dużym powiększeniem, stosując
obiektywy imersyjne.
2. Przed umieszczeniem preparatu na stoliku mikroskopu, na szkiełko nanosimy
kroplę olejku imersyjnego
.
3. Preparat umieszczamy na stoliku i zanurzamy obiektyw mikroskopu w olejku.
Olejek, wypełniający przestrzeń pomiędzy preparatem a obiektywem mikroskopu,
zapewnia lepsze warunki oświetlenie preparatu, gdyż jego współczynnik załamania
ś
wiatła jest zbliżony do współczynnika szkła.
4. Ustawiamy ostrość, najpierw przy użyciu śruby makrometrycznej, a nastepnie
mikrometrycznej.
5. Po zakończeniu pracy, obiektyw mikroskopu należy przetrzeć bibułką, nasączoną
ksylenem, w celu oczyszczenia z olejku imersyjnego.
6. Należy przestrzegać zasady, iż oświetlenie włączamy WYŁĄCZNIE podczas
obserwacji preparatu.
Bakterie dnia:
Sacharomyces cerevisiae, Candida albicans, Candida glabrata, Candida
parapsilosis, Candida thermophilus
WIADOMOŚCI TEORETYCZNE.
1. Rodzaje mikroskopów:
- prosty,
- ultrafioletowy - ma lepszą zdolność rozdzielczą,
- ciemnego pola - wyraźniejszy obraz dzięki zwiększonemu kontrastowi,
- fluorescencyjny,
- kontrastowo-fazowy,
- elektronowy.
Powiększenie mikroskopu - iloczyn powiększenia okularu i obiektywu.
Zdolność rozdzielcza - najmniejsza odległość między dwoma punktami, przy której
widoczne są oddzielnie.
Imersja - wypełnienie przestrzeni między preparatem a obiektywem płynem o wyższym
współczynniku załamania niż powietrze (olejek imersyjny). Usuwa zjawisko załamania się
promieni świetlnych przy przechodzeniu ze środowiska optycznie gęstszego (szkło) do
ś
rodowiska optycznie rzadszego (powietrze).
2. Formy morfologiczne bakterii:
- kuliste: ziarniak (Micrococcus), dwoinka (Diplococcus), czworaczki (Tetracoccus),
sześcianka-pakietowiec (Sarcinia), paciorkowce, gronkowce (Staphylococcus).
- cylindryczne: pałeczki (Bacterium), laseczki (Bacillus).
- spiralne: krętki, śrubowce (Spirillum), przecinkowce (Vibrio).
Opisując morfologię (wygląd) kolonii bakteryjnych zwracamy uwagę na następujące cechy:
kształt - okrągły, nieregularny, promienisty, korzonkowaty, koncentryczny
wielkość - średnica kolonii oceniana w milimetrach
wzniesienie nad powierzchnię podłoża - kolonie mogą być płaskie, wzniesione, soczewkowate,
pępkowate, stożkowate
struktura - bezpostaciowa, drobno- lub gruboziarnista, włóknista
powierzchnia - gładka, matowa, błyszcząca, szorstka, brodawkowata, pomarszczona, sucha, wilgotna
brzegi - równe, faliste, ząbkowane, postrzępione, poszarpane
barwa - zależy od barwników wytwarzanych przez bakterie
przezroczystość - przezroczyste, półprzezroczyste, nieprzezroczyste
zróżnicowanie - możliwość wyodrębnienia w kolonii części centralnej i brzegowej
zmiany podłoża wokół kolonii - zabarwienie podłoża, zmętnienie, hemoliza podłoża krwawego
zapach - może być nieswoisty, podobny dla wielu gatunków bakterii, może też być swoisty,
charakterystyczny dla danego gatunku, związany z produktami metabolizmu bakterii (zapach miodu,
jaśminu, zjełczałego tłuszczu, gnilny)
3. Metody barwienia:
Celem barwienia jest ułatwienie obserwacji.
Odczyn zasadowy barwników wykazuje powinowactwo do kwaśnego odczynu składników
chemicznych ściany komórkowej.
Podział:
- barwienie proste: błękit metylowy (5), fuksyna (30).
- barwienie złożone:
- pozytywne - zabarwienie wnętrza komórki.
- negatywne - zabarwienie tła (nigrozyna, tusz chiński, czerwień Kongo).
- negatywno-pozytywne
Barwienie przyżyciowe - odróżnienie komórek żywych od martwych, które się zabarwiają
(błękit metylowy, saponina). Barwnik jest pochłaniany tylko przez komórki żywe.
Różnice i podobieństwa w budowie komórek prokariotycznych i eukariotycznych.
PROKARYOTA
EUKARYOTA
1. błona cytoplazmatyczna
1. błona cytoplazmatyczna
2. ściana komórkowa
2. ściana komórkowa (wyłącznie
w
w komórkach roślinnych)
3. nukleoid (funkcjonalny odpowiednik
jądra) -
nagi zawieszony w cytoplażmie
splątek DNA - podwójna helikoida.
3. jądro komórkowe z jąderkiem
i
chromosomami osłonięte
błoną
jądrową.
4. mezosomy oraz wpuklenia błony
cytoplazmatycznej
4. mitochondria - centra
procesów
energetycznych
5. ziarna chromatoforowe
5. plastydy

6. rybosomy
6. rybosomy
7. brak
7. lizosomy
8. brak
8. reticulum endoplazmatyczne
9. brak
9. aparat Golgiego
U PROCARIOTA brak również:
- centromeru,
- wrzeciona mitotycznego,
- fazy diploidalnej,
- podziału redukcyjnego.
4. Ściana komórkowa:
Bakterie G (+) - kw. tejchojowe:
* fosforan glicerolu,
* fosforan rybitolu,
- wielocukry,
- białka,
- za swoistość antygenową odpowiada białko,
- grubość ściany komórkowej wynosi 15-50 nm.
Bakterie G (-) - lipolisacharyd - LPS,
- lipoproteina - LP,
- białka,
- lipidy,
- za swoistość antygenową odpowiada wielocukier wchodzący w skład LPS,
- białka działają jako enzymy autolityczne,
- grubość ściany komórkowej wynosi 2-10 nm.
5. Skład chemiczny komórek bakteryjnych:
73 - 85% stanowi woda
W suchej masie:
- 40-60% s.m. stanowią białka. Występuje charakterystyczny dla bakterii kwas
-
dwuaminopimelinowy oraz jego D-izomery. Brak lub prawie brak białek zasadowych
(arginina, lizyna), protamin i histonów.
- 17% kw. nukleinowe (stosunek A+T / G+C nie jest równy 1).
- 10% cukry - materiałem zapasowym jest granuloza (podobna do skrobi), glikogen
bakteryjny, mukopeptyd, kwasy tejchoinowe. Nie występuje celulozy (wyjątkowo u
Acetobacter występuje).
- 10% lipidy - materiałem zapasowym jest polimer kwasu -hydroksymasłowego, LPS
(lipolisacharyd), LP (lipoproteina), rzadko mat. zapasowym są glicerydy, brak jest
kwasów nienasyconych, steroli, cholesterolu.
- Witaminy i czynniki wzrostowe - nie wymagają do wzrostu witaminy C, A, D.
6. Przetrwalniki - formy spoczynkowe bardzo oporne na wysuszenie dzieki obecności
dużej ilości kwasu dwupikolinowego), temperaturę oraz działanie czynników chemicznych.
Powstają w procesie sporulacji, w którym następuje aktywacja szeregu genów. Sporulacja
rozpoczyna się od izolacji końcowej części DNA bakteryjnego przez błonę rosnącą do
wewnątrz. Dwie błony przetrwalnika rozpoczynają czynną syntezę specjalnych warstw,
które będą stanowiły osłony komórkowe. Całkowicie ukształtowany przetrwalnik posiada:
- rdzeń - protoplast przetrwalnika posiadający chromosom i wszystkie elementy do
syntezy białek,
- ścianę przetrwalnika,
- korę - najgrubszą warstwę przetrwalnika,
- płaszcz - zbudowany z białka keratynopodobnego,

- egzosporium - błonę lipidową.
Zagadnienia teoretyczne.
Budowa komórki bakteryjnej: formy morfologiczne bakterii, wielkość komórek bakteryjnych,
budowa komórki bakteryjnej. Różnica pomiędzy organizmami prokariotycznymi a
eukariotycznymi. Budowa ściany komórkowej bakterii gramdodatnich i gramujemnych Co to jest
endotoksyna? Co to jest antygen somatyczny? Budowa błony zewnętrznej bakterii gramujemnych.
Co to jest przestrzeń periplazmatyczna, mureina, pseudomureina, otoczka, glikokaliks, warstwa S,
protoplast, sferoplast. Enzymy występujące w przestrzeni periplazmatycznej oraz błonie
zewnętrznej, dlaczego bakterie gramujemne są oporne na penicylinę
Barwienie bakterii i przygotowanie preparatów mikroskopowych – dlaczego barwi się
bakterie w celu przygotowania preparatów, barwienie proste, złożone, pozytywne,
negatywne? Jakie sposoby barwienia stosuje się w celu uwidocznienia komórek
bakteryjnych, przetrwalników oraz otoczek. Jaka grupa substancji pozwala na wybarwienie
komórek bakteryjnych? Na czym polega barwienie metodą Grama?
Obserwacja mikroskopowa preparatów – rodzaje mikroskopów, budowa mikroskopu
ś
wietlnego, obiektyw immersyjny
ĆWICZENIE 3
WPŁYW CZYNNIKÓW FIZYKO-CHEMICZNYCH NA BAKTERIE
Materiał do badań: hodowle płynne bakterii Escherichia coli i Bacillus subtili,
Staphylococcus aureus, Pseudomonas aeruginosa, Sacharomyces lub Candida
Podłoża: podłoże stałe LA (płytki: 4 duże - (śmierć cieplna) + 20 małych (UV; dezynfekcja
- po 2 na parę)
Odczynniki: 3% woda utleniona, jodyna, 70% alkohol, 2% sterinol, 1,5% chloramina,
40%
formalina
Każda para wykonuje wszystkie doświadczenia dla jednego z gatunków tak by cała grupa
przetestowała wszystkie gatunki bakterii.
I. Wpływ temperatury na przeżywalność drobnoustrojów - Wyznaczanie czasu
ś
mierci cieplej w temperaturze 60°°°°C i 100°°°°C dla badanych gatunków bakterii
Czas śmierci cieplej – czas potrzebny do zabicia wszystkich drobnoustrojów danego
gatunku, w określonych warunkach, w danej temperaturze.
Punkt śmierci cieplnej –
najniższa temperatura, w której dany organizm ginie w ciągu 10 minut.
Do dwóch probówek wprowadzamy po 1 ml hodowli nocnej bakterii,
Probówki umieszczamy w łaźni wodnej o temperaturze, odpowiednio 60°C oraz
100°C.
W czasie: 0, 5, 10, 20, 30 i 40 minut od momentu rozpoczęcia inkubacji, hodowle
wysiewamy na płytki z podłożem agarowym.
Po 24-godzinnej inkubacji płytek w temperaturze 37°C określamy czas śmierci cieplnej
w temperaturze 60°C oraz 100°C, dla obu badanych gatunków bakterii.

II. Wpływ promieniowania UV na hodowle bakterii.
a) Na płytki agarowe (2 płytki na parę) wysiewamy murawą po 0,2 ml hodowli nocnych
badanych bakterii
b) Płytki z wysianymi bakteriami eksponujemy na promieniowanie UV przez 0,5, 1, 5,
10, 20, 30 minut (każda para przez inny okres czasu). W trakcie naświetlania płytki
przykrywamy wieczkiem do połowy (ponieważ promieniowanie UV nie przenika
przez szkło, okryta część płytki posłuży jako kontrola)
c) Płytki inkubujemy 24 godziny w temperaturze 37°C.
III. Skuteczność działania wybranych środków dezynfekcyjnych na bakterie
70% etanol, 2% sterinol, 1,5% chloramina, 3% H
2
O
2
, Sefril.
a) Każda para bada wpływ wszystkich środków dezynfekcyjnych na badany gatunek
bakterii.
b) Płytki dzielimy 6 sektorów, opisanych: 0, 5, 10, 30, 45 i 60 minut.
c) Do 2 jałowych probówek (na parę) wprowadzamy 2 ml wybranego środka
dezynfekcyjnego, po czym zawieszamy w nich bakterie każdego z badanych
gatunków, pobrane z podłoża stałego. Zawartość probówek dokładnie mieszamy.
d) W czasach 0, 5, 10, 30 i 60 minut od momentu rozpoczęcia inkubacji, zawiesiny
bakterii wysiewamy ezą na płytkę agarową.
e) Płytki inkubujemy 24 godziny w temperaturze 37°C.
IV. Badanie wpływu pH na wzrost bakterii.
Na płytki z agarem wzbogaconym o pH 5, 6, 7, 8, 9, i 10 wysiewamy badany gatunek bakterii i
pozostawiamy do inkubacji 24godziny.
WIADOMOŚCI TEORETYCZNE.
1. Wpływ temperatury na drobnoustroje.
Temperatura jest najważniejszym czynnikiem zewnętrznym wpływającym na wzrost
bakterii (aktywność enzymów i szybkość reakcji metabolicznych zależy od temperatury).
Podział drobnoustrojów ze względu na tolerancję temperatury:
a) Psychrofile - zimnolubne (temperatura optymalna 15-20
o
C)
b) Mezofile (temperatura optymalna 20-40
o
C)
c) Termofile - ciepłolubne (temperatura optymalna 45-60
o
C)
Psychrofile - saprofity i drobnoustroje chorobotwórcze dla ryb. Występują w glebie, w
zimnych jeziorach i morzach. Znoszą niską temperaturę dzięki ewolucyjnemu
przystosowaniu do specyficznych warunków. Drobnoustroje te posiadają enzymy, które
aktywują się w niskiej temperaturze. Zmiana przepuszczalności błon cytoplazmatycznych
wiąże się z wyższym poziomem nienasyconych kwasów tłuszczowych w błonach
komórkowych. Dzięki temu błony komórkowe psychrofili nie tracą elastyczności w niskich
temperaturach.
Mezofile - są najbardziej rozpowszechnione. W tej grupie występuje większość saprofitów
bytujących w glebie i w wodzie. W tej grupie znajdują się również wszystkie bakterie
chorobotwórcze. Gdy temperatura spada poniżej minimum, to zachodzi represja

gromadzenia w komórkach aminokwasów i włączania ich do białek. Gdy temperatura
wyższa od optymalnej, to następuje degradacja RNA.
Termofile - występują w nawozie, fermentujących resztkach roślinnych, w jelitach
niektórych zwierząt, w gorących Ÿródłach. Należą do tej grupy głównie bakterie z rodzaju
Bacillus (przetrwalnikują
ce, G(+)). Termofile posiadają białko o dużej termostabilności i
mają zdolność do szybkiej regeneracji białka, które utraciło aktywność.
2. Bakteriobójcze działanie wysokiej temperatury:
a) Pod wpływem wysokiej temperatury następuje denaturacja białek (skuteczniejsze jest
gorące i wilgotne powietrze, nią gorące i suche).
b) Obecność w podłożu cukrów, białek i soli stwarza barierę ochronną dla drobnoustrojów.
c) Ochronne działanie ma również obojętne pH podłoża (za wyjątkiem bakterii
kwasoopornych, które posiadają osłonę woskową).
d) Starsze komórki są bardziej oporne na działanie wysokiej temperatury.
e) Bakterie nie tworzące endospor i formy wegetatywne bakterii przetrwalnikujących giną
w temperaturze 60-70
o
C, endospory w 100
o
C.
f) Przetrwalniki zawierają enzymy ciepłooporne. Pod wpływem wysokiej temperatury
racemaza L-alaniny, przekształca ją w D-alaninę, która hamuje kiełkowanie endospor.
Enzymy ciepłooporne związane są z kompleksem cząsteczkowym, który zawiera kwas
dwupikolinowy.
3. Wpływ promieniowania UV na drobnoustroje.
Fale o długości 230-270nm wywierają silne działanie biologiczne. Są one absorbowane
przez kwasy nukleinowe i białka (kwasy 25-50 razy więcej).
a) Po naświetleniu cytozyna ulega hydratacji i powstają dimery tyminy, cytozyny i
mieszane dimery cytozyno-tyminowe. Zmiany te mogą uniemożliwiĆ replikację DNA i
mogą spowodowaĆ śmierĆ lub błędne podstawianie zasad w czasie replikacji (mutanty).
b) W bakteriach fotoreaktywowanych powstają specjalne enzymy zdolne do wycinania z
łañcucha polinukleotydowego dimerów timiny, a brakujące zasady są ponownie
wbudowywane.
c) Fotodynamiczne uczulenie występuje w przypadku, gdy doda się do hodowli bakterii
barwniki (błękit toluidynowy, eozynę, safraninę). Po wystawieniu bakterii na działanie
ś
wiatła (lub części widma słonecznego) - bakterie giną.
d) UV ma małą przenikliwość. Działa powierzchniowo. Pod wpływem UV występują
zmiany w podłożu (tworzy się nadtlenek wodoru i wolne rodniki OH), które to związki mają
właściwości utleniające, a więc toksyczne dla bakterii - działanie pośrednie.
4. Wpływ środków dezynfekcyjnych na drobnoustroje.
- Alkohole - denaturacja białek i rozpuszczanie lipidów.
- Chloraminy - chloramid sodowy kwasu p-toulenosulfonowego (30% czynnego chloru),
działa odkażająco, odwadniająco i utleniająco. Chlorowce, jod, inaktywują białka (reagują
z tyrozyną). Chlor reaguje z wodą tworząc kwas podchlorowy, który ma właściwości
utleniające.
- Formalina - roztwór aldehydu mrówkowego, silny środek bakterio- i wirusobójczy (służy
do odkażania narzędzi laboratoryjnych i hirurgicznych).
- Sterinol - detergent hamujący rozwój bakterii, mykoplazm, pierwotniaków, grzybów
chorobotwórczych i niektórych wirusów). Jest to czwartorzędowy związek amoniowy, który
rozrywa błony komórkowe.
- Lizol - ciekłe mydło krezolowe (czyste krezole rozpuszczone w równej części w
obojętnym mydle potasowym z oleju lnianego). Lizol jest środkiem dezynfekującym,
niszczy formy wegetatywne bakterii, prątki gruŸlicy, wszy. Krezole są to trucizny

protoplazmatyczne, które wchodzą w reakcje ze ścianą komórkową i białkami.
- H
2
O
2
- nadtlenek wodoru wydziela zjonizowany tlen po zetknięciu z komórką i powoduje
denaturację białek, uszkadza błonę cytoplazmatyczną i zlokalizowane w nie enzymy.
Zagadnienia.
Przygotowanie do pracy w laboratorium mikrobiologicznym. Wpływ czynników
fizyko-chemicznych na bakterie:
Metody sterylizacji (rodzaje i mechanizmy działania); dezynfekcja – przykłady środków
dezynfekcyjnych i sposób ich działania; czas i punkt śmierci cieplnej; Praca w warunkach
jałowych – pojęcia: aseptyka, antyseptyka, sanityzacja. W jaki sposób sterylizuje się szkło
laboratoryjne, pipety, narzędzia metalowe, podłoża bakteriologiczne itp...? Na czym polega
i do czego służy dezynfekcja, przykłady środków dezynfekcyjnych i sposób ich działania),
na czym polega działanie promieniowania ultrafioletowego, co to jest punkt oraz czas
ś
mierci cieplnej.
Podłoża bakteriologiczne – do czego służą, jakie mikroorganizmy można hodować w
warunkach in vitro Jakie warunki powinny spełniać pożywki mikrobiologiczne? Co to jest
podłoże proste, wzbogacone, minimalne, wybiórcze, róznicujące (przykłady tych podłóż)?
Przykłady czynników wybiórczych i różnicujących. Co to jest czysta kultura? do czego
służy podłoże Chapmana? jaki to rodzaj podłoża? Co jest czynnikiem wybiórczym a co
różnicującym w tym podłożu? Do czego służy podłoże MacConkeya? Jaki to rodzaj
podłoża? Co jest czynnikiem wybiórczym i różnicującym? Jak odróżnić kolonie Escherichia
coli od kolonii Salmonella sp. przy wykorzystaniu podłoża MacConkeya?
Ć
wiczenie 4
Metody hodowli bakterii.
Metody hodowli bakterii – w podłożu płynnym, hodowla beztlenowców
Fizjologia mikroorganizmów.
Posiew na szereg biochemiczny- badanie właściwości biochemicznych wybranych
pałeczek jelitowych
Morfologia kolonii bakteryjnych na różnych podłożach mikrobiologicznych.
Bakterie dnia rodzaj Salmonella, rodzaj Klebsiella
a)
Hodowla E. coli na podłożu płynnym - wykreślanie krzywej wzrostu
bakterii.
b) Zaszczepić 1 ml hodowli nocnej E. coli w 50 ml pożywki płynnej. – dwie hodowle
c) 1 Kolbę umieścić w wytrząsarce, w temperaturze 37
o
C druga w temp. pokojowej na
stole
d) Bezpośrednio po zaszczepieniu bakterii oraz w odstępach czasowych co 20 minut
wykonać pomiar OD
575
hodowli. Przed pomiarem kazda kolbke dobrze zamieszac.
e) Na papierze milimetrowym wykreślić krzywą wzrostu bakterii (oś Y – OD; oś X –
czas inkubacji).
f) Wykonać seryjne rozcieńczenia z hodowli na poszczególnych etapach wzrostu
(każda para próba pobrana w innym czasie) i określić ilość komórek bakteryjnych

w poszczególnych fazach wzrostu (wysiewamy na murawę ostatnie 3 seryjne
rozcieńczenia) na początku hodowli i na końcu hodowli w każdej grupie
g)
Metody hodowli bakterii beztlenowych
W doświadczeniach prowadzona będzie hodowla bakterii beztlenowych z rodzaju
Clostridium. Kontrolnie prowadzona będzie hodowla bakterii tlenowej, jaką jest
Serratia marescens.
e) hodowla w próżni, z wykorzystaniem anaerostatu – DEMONSTRACJA
f)
metoda fizyczna – odtlenianie pożywki przez zagotowanie i szybkie schłodzenie
h) Podłoże płynne VL (2 probówki na całą grupę) odtlenić poprzez zagotowanie i szybkie schłodzenie w łaźni lodowej.
i) Do jednej z probówek wprowadzić bakterię beztlenową Clostridium sp., do
drugiej szczep kontrolny bakterii tlenowej S. marcescens.
j) Na powierzchnię pożywek wprowadzić cienką warstwę parafiny (w celu
utrudnienia dostępu powietrza).
k) Probówki z bakteriami inkubować przez 24 godz. w temp. 37°C.
metoda biologiczna Fortnera
(równoległa hodowla bakterii beztlenowej oraz tlenowej; bakteria tlenowa,
zużywając tlen, tworzy środowisko beztlenowe)
l)
Płytkę z podłożem agarowym podzielić na dwie części, wcinając przez środek, przy pomocy jałowego skalpela, pasek
pożywki.
m) Na jednej części wysiać bakterię Clostridium sp., na drugiej bakterię tlenową
S. marcescens.
n) Płytkę uszczelnić i inkubować w temp. 37°C przez 24 godz.
metoda chemiczna - odtlenianie przy pomocy substancji chemicznych
1. Na dwóch płytkach agarowych wysiać niezaleznie: Clostridium sp. oraz
Serratia marcescens.
2. Przygotować koperty z bibuły, napełnione mieszanką odtleniającą, które
następnie należy przykleić do wewnętrznej strony wieczka płytek agarowych.
3. Płytki uszczelnić i inkubować w temp. 37°C przez 24 godz
•
Obserwacje wzrostu i morfologii hodowli bakteryjnych na podłożach
stałych:
Agar wzbogacony- Bacillus subtilis, E.coli lac
-
, Proteus vulgaris, Pseudomonas
aeruginosa, Klebsiella oxtyoca,
Podłoże Mac Conkeya E.coli lac
-
, E.coli lac
+
, Salmonella anatum, Klebsiella oxytoca
Podłoże Chappmana Staphylococcus aureus, Staphylococcus epidermidis, Micrococus sp,
Podłoże z krwią , Paciorkowce hemolizujące i niehemolizujace
Agar SS Salmonella, Shigella
Podłoże Sabuouda Candida glabrata. Candida albicans., Sacharomuces cerevisiae
Podłoże Ejmhejlena bakterie halofilne Halobacterium
Podłoże Bg Cyanobakterie
Wła
ściwości hemolityczne bakterii. Typy hemolizy (rodzaj Streptococcus) demonstracja:
a)
hemoliza ∝
b)
hemoliza β
c)
hemoliza γ.

•
Badanie właściwości biochemicznych drobnoustrojów - szereg
biochemiczny
Przy pomocy jałowej ezy posiać bakterie - pałeczki z rodziny Enterobacteriaceae na
następujące podłoża:
(Każdy student wykonuje posiew jednego gatunku bakterii, który powinien
zidentyfikować w oparciu o jego właściwości biochemiczne).
VII.
podłoże Kliglera - badanie zdolności bakterii do rozkładu cukrów (glukoza, laktoza) oraz właściwości
proteolitycznych (wydzielanie siarkowodoru) – posiew kłuty i na powierzchnię skosu
VIII.
podłoże Singera - badanie zdolności bakterii do rozkładu mocznika (obecnosć ureazy) i wytwarzania
indolu
IX.
podłoże półpłynne z mannitolem - badanie zdolności bakterii do rozkładu mannitolu oraz do ruchu
X.
podłoże z laktozą - badanie zdolności bakterii do rozkładu laktozy
XI.
podłoże z fenyloalaniną - badanie zdolności bakterii do dezaminacji fenyloalaniny
XII.
podłoże Simmonsa – wykorzystanie cytrynianu sodu jako jedynego źródła węgla
XIII.
podłoże z żelatyną – badanie obecności enzymów proteolitycznych
XIV. podłoże do badania ruchu bakterii i obecności azotanów
XV.
podłoże z malonianem sodowym - badanie zdolności bakterii do rozkładu malonianu
WIADOMOŚCI TEORETYCZNE.
1. Hodowla stała - stacjonarna.
a) Faza przygotowania (lag faza) - faza przystosowawcza. Wzrasta ilość RNA (nawet 12
razy), wzrost liczby białka i rybosomów, wydatnie powiększają się komórki. OpóŸnienie w
liczbie, a nie w masie hodowli. W fazie tej następuje przestrojenie aparatu
enzymatycznego.
b) Faza logarytmicznego wzrostu - zaczynają się podziały komórkowe. Liczba komórek
wzrasta w postępie geometrycznym - logarytm liczby bakterii jest proporcjonalny do czasu.
c) Faza zwolnionego wzrostu - następuje na skutek wyczerpania w pożywce substratów
niezbędnych dla wzrostu lub w wyniku nagromadzenia produktów toksycznych. Synteza
RNA i białka gwałtownie maleje.
d) Faza równowagi - stała liczba żywych bakterii. Sporadyczne podziały równoważą ubytki
spowodowane zamieraniem. W tej fazie hodowli największe nagromadzenie biomasy.
e) Faza zamierania - wzrasta liczba komórek martwych, procesy autolizy komórek,
zmniejsza się biomasa hodowli.
f) Faza zamierania logarytmicznego.
V= n/t
V - stała szybkości podziałów
n - liczba podziałow
t - czas
g = t/n
g - czas generacji (wiek osobniczy)
rys.
2. Hodowla ciągła.
Jest to hodowla, w której faza wzrostu logarytmicznego jest przedłużona i może trwaĆ
(teoretycznie) przez nieograniczony czas. Trzeba jednak zapewniaĆ dopływ świeżej
pożywki oraz usuwaĆ szkodliwe metabolity. Hodowle takie prowadzi się w chemostacie i
turbidostacie - kontrola składników podłoża prowadzona jest przez układ fotokomórki i
przekaŸników.
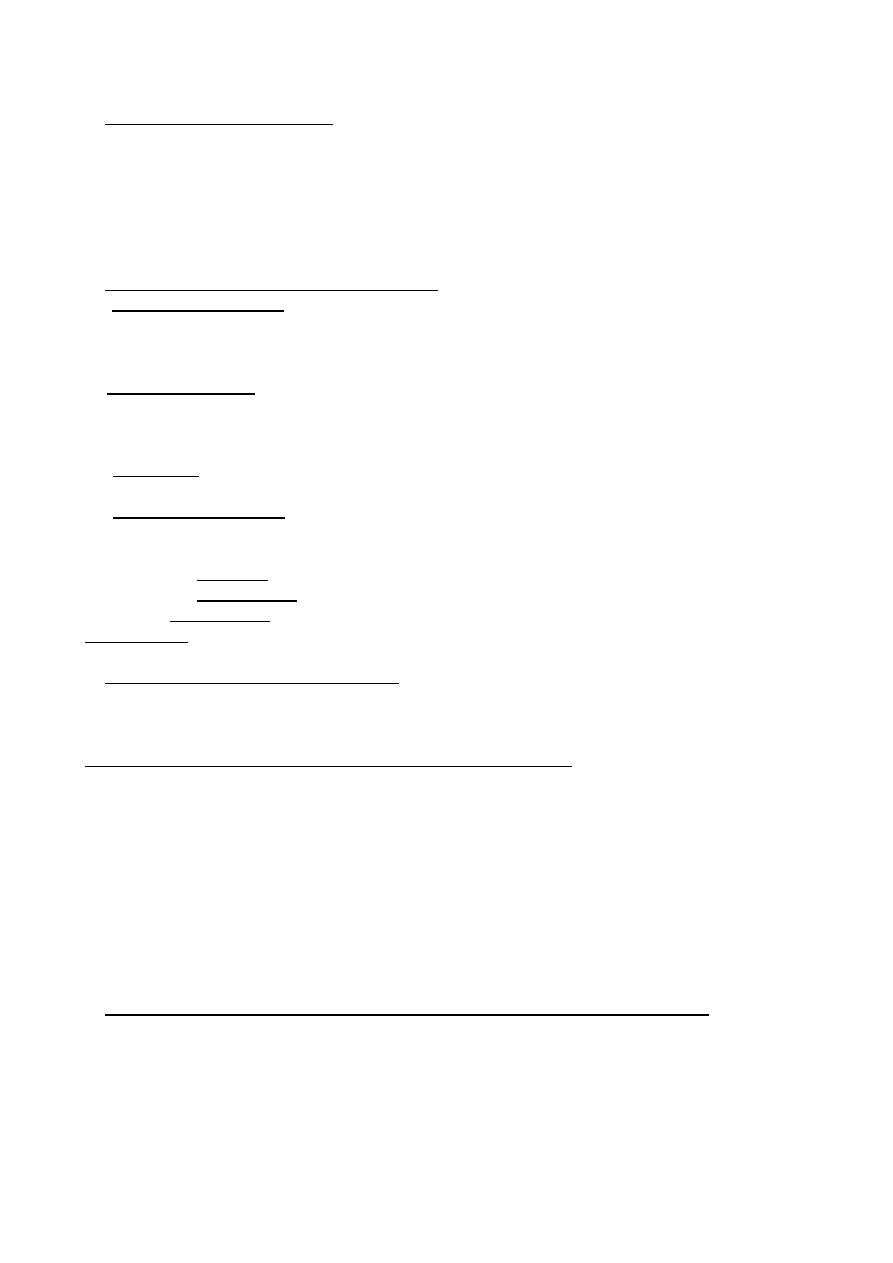
3. Hodowle zsynchronizowane.
Wszystkie osobniki dzielą się prawie jednocześnie. Synchronizację hodowli otrzymuje się
poprzez:
- okresową zmianę temperatury hodowli (zahamowanie podziałów, wzrost kontynuowany).
- chwilowe usunięcie z podłoża niezbędnego składnika pokarmowego,
- mechaniczną selekcję na filtrach,
- rozdział hodowli na podstawie podobnej gęstości komórek.
4. Metody oznaczania liczby drobnoustrojów.
A. Metody bezpośrednie:
- w preparacie barwionym (szereg rozcieñczeñ zawiesiny bakterii),
- w hemocytometrze,
- metoda ultrafiltracji (filtrów membranowych).
B. Metody pośrednie:
- metoda płytkowa,
- automatyczny licznik kolonii,
- metoda nefelometryczna
a) chemiczna - intensywność zmętnienia pożywki podczas inkubacji - porównanie
zmętnienia z probówkami standartowymi (chlorek baru + kwas siarkowy).
b) spektrofotometryczna - porównanie gęstości pożywki a przepuszczalności światła
(600nm).
Bezwzględne
tlenowce - bezwzględne aeroby.
Bezwzględne
beztlenowce - bezwzględne anaeroby.
Względne
beztlenowce - względne anareoby.
Mikroaerofile
- lepiej rosną, gdy jest mniej tlenu.
5. Hodowla w warunkach beztlenowych.
Bezwzględne beztlenowce mogą się rozwijaĆ tylko w środowisku pozbawionym tlenu.
Tlen jest dla nich czynnikiem szkodliwym (wręcz zabójczym).
Warunki beztlenowe można stworzyĆ w następujący sposób:
- zagotowanie pożywki przed posiewem,
- wprowadzenie na powierzchnię pożywki płynnej warstewki oleju parafilmowego,
- podłoże zestalone i posiew wgłębny (kłuty),
- dodanie do pożywki substancji w formie zredukowanej, które szybko zuzywają tlen,
- specjalne hodowle w płytkach Petriego bakterii beztlenowych (na denku płytki), z
dodatkowym posiewem drobnoustrojów tlenowych zużywających tlen do swego rozwoju
na wewnętrznej stronie przykrywki. Przed dopływem tlenu z zewnątrz płytkę zabezpiecza
się za pomocą przylepca,
- różne aparaty do hodowli beztlenowców (zwykły anaerostat, hodowle w eksykatorze).
6. Badanie zdolności bakterii do utylizacji określonych związków chemicznych.
Zdolność bakterii do degradacji różnych substancji jest uzależniona od spektrum
wytwarzanych przez nie enzymów. Enzymy to substancje białkowe pełniące funkcję
biokatalizatorów. Enzymy katalizują procesy biosyntezy i biorozkładu związków
chemicznych oraz wiązanie lub uwalnianie energii. Przy identyfikacji bakterii wykorzystuje
się przede wszystkim zdolność do biologicznego rozkładu związków organicznych
(substratów). Podczas procesu rozkładu powstają produkty, zwane metabolitami.
Obecność metabolitów w środowisku reakcji wykrywa się za pomocą odczynników

chemicznych (część z nich należy do grupy indykatorów). Wyniki prób biochemicznych
decydują często o zaliczeniu danego drobnoustroju do rodzaju, gatunku lub odmiany.
Szczególnie duże znaczenie mają próby biochemiczne przy identyfikacji bakterii o
podobnej morfologii komórki (np: pałeczki jelitowe E. coli, Salmonella, Shigella i inne są
gramujemne, mają kształt pałeczkowaty, mniej więcej podobne rozmiary i pochodzą z tego
samego źródła).
Do powszechnie występujących reakcji biochemicznych, katalizowanych przez enzymy
bakteryjne należą:
a) reakcja utleniania (odłączenie wodoru lub przyłączenie tlenu),
b) reakcja odwodnienia (odłączenie cząsteczki wody),
c) reakcja hydrolizy (przyłączenie cząsteczki wody),
d) reakcja dezaminacji (odłączenie grupy anionowej -NH
2
z powstaniem po redukcji
cząsteczki amoniaku),
e) reakcja dekarboksylacji (odłączenie CO
2
),
f) reakcja fosforylacji (włączenie reszty kwasu fosforowego),
g) reakcja defosforylacji (hydrolityczne odłączenie reszty kwasu fosforowego z
powstaniem kwasu fosforowego).
2.
Hemoliza.
Niektóre bakterie wytwarzają substancje, które nie działają bezpośrednio toksycznie, lecz
odgrywają ważną rolę w procesie zakażania. Hemolizyny - rozpuszczają krwinki czerwone.
Wytwarzają je: Clostridium, gronkowce i liczne pałeczki G (-).
Rodzaj Streptococcus (paciorkowce), na podłożu agarowym z krwią mogą się tworzyć następujące
strefy:
a) hemolizy ∝ - częściowe rozpuszczenie krwinek, zazielenienie otaczającego podłoża i niewielka
przejrzystość,
b) hemolizy β - całkowite rozpuszczenie krwinek,
c) hemolizy γ - brak przejaśnienia (nie wykazują hemolizy).
Zagadnienia. Metody hodowli bakterii. Fizjologia mikroorganizmów.
Na czym polega hodowla stacjonarna bakterii? Kolejne fazy wzrostu bakterii w hodowli
stacjonarnej. Co to jest faza logarytmicznego wzrostu? Dlaczego w hodowli stacjonarnej
komórki ostatecznie zamierają? Co to jest czas generacji bakterii. Czy jest on taki sam dla
wszystkich bakterii? Co to jest miano bakterii? Co to jest OD. Przy jakiej długości fali
mierzymy OD hodowli bakteryjnej? Jakie są metody bezpośrednie określania liczby
drobnoustrojów? Jakie są metody pośrednie określania liczby drobnoustrojów? W jaki
przygotowuje się seryjne rozcieńczenia? W jaki sposób można uzyskać pojedyncze
kolonie bakteryjne (podaj co najmniej dwie metody)? Na czym polega hodowla ciagła
drobnoustrojów? Czy w hodowli tej występuje faza logarytmicznego wzrostu? Na czym
polega hodowla zsynchronizowana? Która z metod hodowli drobnoustrojów: stacjonarna
czy ciągła, jest bardziej przydatna w przemyśle biotechnologicznym (np. przy produkcji
różnych związków)? Co oznacza termin „czysta kultura” bakteryjna. Enzymy bakteryjne
(proteolityczne, amylazy) – w jakim celu są wytwarzane prze bakterie. Co to są
bakteriocyny – spektrum ich działania.
Ćwiczenie 5
Fizjologia mikroorganizmów – cd.
Oznaczanie wrażliwości bakterii na chemioterapeutyki (antybiotyki, sulfonamidy, fitoncydy,

bakteriocyny)
Bakteriofagi- oznaczanie wrażliwości bakterii na bakteriofagi, miano lizatu fagowego,
streak-test.
Bakterie dnia: Proteus, Pseudomonas, Citrobacter, Flavobacterium
Odczyt szeregu biochemicznego
XVI.
podłoże Kliglera - badanie zdolności bakterii do rozkładu cukrów (glukoza, laktoza) oraz właściwości
proteolitycznych (wydzielanie siarkowodoru) – posiew kłuty i na powierzchnię skosu
XVII.
podłoże Singera - badanie zdolności bakterii do rozkładu mocznika (obecnosć ureazy) i wytwarzania
indolu - do odczytu wyniku do podłoża należy dodać odczynnuk
Kowacsa
XVIII.
podłoże półpłynne z mannitolem - badanie zdolności bakterii do rozkładu mannitolu oraz do ruchu.
Po odczytaniu wyniki wykonujemy badanie rozkładu azotanów do azotynów do odczytu wyniku należy
dodać odczynniki
roztwór A- Kwas sulfanilowy
roztwór B α-naftyloamina
XIX.
podłoże z laktozą - badanie zdolności bakterii do rozkładu laktozy
XX.
podłoże z fenyloalaniną - badanie zdolności bakterii do dezaminacji fenyloalaniny do odczytu wyniku
dodajemy roztworu 10% FeCl
3
XXI.
podłoże Simmonsa – wykorzystanie cytrynianu sodu jako jedynego źródła węgla
XXII.
podłoże z żelatyną – badanie obecności enzymów proteolitycznych
XXIII.
podłoże do badania ruchu bakterii i obecności azotanów
XXIV.
podłoże z malonianem sodowym - badanie zdolności bakterii do rozkładu malonianu
Test na oksydazę cytochromową – enzym łańcucha oddechowego (DEMONSTRACJA)
Na murawy E. coli oraz Pseudomonas sp. (wysiane na podłożu agarowym) nanieść kroplę
odczynnika
na
oksydazę
cytochromową
(mieszania
chlorowodowrku
dimetylofenylodiaminy i α-naftolu).
II.
Wytwarzanie enzymów proteolitycznych - hydroliza kazeiny przez bakterie
(DEMONSTRACJA)
Studenci mają ocenić, które z poniższych gatunków bakterii, posiadają zdolność
hydrolizy kazeiny:
Bacillus cereus - Pseudomonas fluorescens - Escherichia coli
III.
Wytwarzanie α
α
α
α-amylazy przez bakterie.
1. Studenci maja do dyspozycji płytki (1 zestaw na całą grupę) z podłożem
zawierającym skrobię, na którą wcześniej wysiano następujące bakterie:
Bacillus subtilis – Bacillus cereus – Escherichia coli
2. Na powierzchnię płytki należy nakropić płyn Lugola. Zabarwienia podłoża będzie
zależało od rodzaju obecnych w nim cukrów: mono- i disacharydów – brak
zabarwienia; dekstryn – kolor brązowy; skrobii – kolor fioletowo-czarny
3. Określić, który z badanych szczepów posiada zdolność hydrolizy skrobii.
DODAC JESZCZE DEMONSTRACJI CECH BIOCHEMICZNYCH skonsultowac z
Sylwia
•
Wytwarzanie bakteriocyn przez bakterie

Kolicyny
Studenci mają do dyspozycji bakterie E. coli [col] A56, A78, które wcześniej wysiano
na podłoże agarowe.
1.
Na powierzchnię płytek z bakteriami wylać 4 ml agaru górnego (0,6%),
zawierającego 0,2 ml hodowli szczepu kontrolnego.Salmonella anatum,
Staphylococcus aureus, E.coli bez plazmidu
2.
Płytki inkubować przez 24 godz. w temperaturze 37C
Staphylokokcyny - na agar wzbogacony z wysianym szczepem Staphylococcus
sp.T należy wykonać streak test z wykorzystaniem następujących bakterii:
E.coli,
Micrococcus luteus, Sarcina, Staphylococcus aureus, Staphylococcus epidermidis.
Wykonanie antybiogramów dla wybranych gatunków bakterii – 1 zestaw na
parę kazda para wykonyje doswiadczenie dla jednego rodzaju bakterii
Materiał do badań - nocne hodowle E.coli, Bacillus subtilis, Salmonella anatum, Klebsiella oxytoca,
Staphylococcus aureus Candida albicans,
antybiogram
Z 0,1ml hodowli wykonać posiew murawą na podłoże Mueller-Hinton
Na powierzchni podłoża z posianymi bakteriami umieścić krązki bibuły,
nasycone różnymi antybiotykami – odległość między krążkami nie powinna
być mniejsza niż 2 cm
Płytki inkubować przez 2 godz. w temp. 4°C a następnie w temperaturze 37°C
Test wrażliwości na sulfonamidy
Z 0,1ml hodowli wykonać posiew murawą na podłoże Mueller-Hinton
Na powierzchni podłoża z posianymi bakteriami umieścić krązki bibuły,
nasycone sulfonamidami – odległość między krążkami powinna wynosić 2
cm
Płytki inkubować przez 2 godz. w temp. 4°C a następnie w temperaturze 37°C
Test wrażliwości na fitoncydy
Z 0,1ml hodowli wykonać posiew murawą na podłoże Mueller-Hinton
Na powierzchni podłoża a na środku płytki wyciąć krążek agaru. W tak przygotowanej
studzience umieścić posiekany czosnek lub cebulę.
Płytki inkubować przez 2 godz. w temp. 4°C a następnie w temperaturze 37°C
Plazmidowa oporność na antybiotyki
każda para studentów posiewa 4 szczepy bakterii posiadające plazmidy na podłoża z
dodatkiem antybiotyków:
Agar wzbogacony z ampicyliną
Agar wzbogacony z ampicyliną i tetracukliną
Agar wzbogacony z tetracykliną
E.coli [pSC101], E.coli[pBR322], E.coli [pJG7], E.coli A17 bez plazmidu
Bakteriofagi
Oznaczanie wrażliwości na bakteriofagi – Streaktest
Lizaty fagowe λcb2, T4
1.
Oznaczanie wra
żliwości bakterii na bakteriofagi.

WykonaĆ streak-test szczepów E. coli A17 λ
-
λ
S
, A135 λ
-
λ
R
, L2 λ
+
λ
R
, E. coli oraz Salmonella
anatum
wobec faga λ (łagodny) i T4 (zjadliwy). Za pomocą jałowych wykałaczek po pobraniu
materiału z kolonii, przeciągnąć wykałaczkę przez linię z naniesionym wcześniej przez
prowadzącego, lizatem fagowym (0,1ml). Strefa lizy bakterii świadczy o wrażliwości danego
szczepu bakterii na odpowiedniego faga.
Naniesione lizaty fagowe: A17 λ
-
λ
S
- wrażliwy, ma miejsca receptorowe na błonie,
A135 λ
-
λ
R
- oporny,
L2 λ
+
λ
R
- lizogenny.
A142 λdV
A40 dnaB
Salmonella anatum
Oznaczanie miana fagów – miareczkowanie
0,2ml Bakterii indykatorowych ezawieszamy w płynnym agarze górnym ogrzanym w łaźni wodnej,
dodajemy 0,1 ml Rozcieńczenia bakteriofagów i po wymieszaniu wylewamy na płytkę.
M
f
= n
*
10
x
*
10
M
f
- miano faga (ilość cząstek fagowych w objętości 1ml)
n - ilość łysinek fagowych
10
x
- rozcieńczenie lizatu fagowego
10 - wysiewamy 0,1ml, a nie 1,0 ml, a miano faga to ilość cząstek faga w 1ml.
Posiew materiałów własnych.
Każdy student wykonuje posiew materiałów własnych (wymazy z gardła, jamy
ustnej lub nosowej) na następujące podłoża: agar wzbogacony, podłoże
MacConkey’a, podłoże Chapmana,podłoże z krwią. (Wyrosłe bakterie będą
następnie oglądane pod mikroskopem)
WIADOMOŚCI TEORETYCZNE.
2. Szereg biochemiczny.
Szereg biochemiczny stosuje się do identyfikacji bakterii. Najlepiej jest przygotować gęstą
zawiesinę bakterii z jałowo pobranej, pojedynczej kolonii bakteryjnej. Bakterie zawiesiĆ w
roztworze soli fizjologicznej.
Przykłady podłóż stosowanych w szeregu biochemicznym:
- podłoże Kliglera
- (rozkład glukozy, laktozy, wydzielanie H
2
S) - posiew powierzchniowy
tzw. rysowy na powierzchnię skosu i kłuty.
- podłoże Singera - (obecność ureazy, tryptofanazy) - zawiesinę lub masę komórkową
rozetrzeć na ściankach probówki tuż przy powierzchni podłoża.
- podłoże z 10% laktozą - zawiesinę lub masę komórkową rozetrzeć na ściankach
probówki tuż przy powierzchni podłoża, następnie pokryĆ je około 1cm warstwą płynnej
parafiny.
- podłoże z fenyloalaniną
- posiew powierzchniowy.
- podłoże na „ruch i azotany” - posiew przez wkłucie.
- podłoże z malonianem sodowym
- zawiesinę lub masę komórkową rozetrzeć na
ś
ciankach probówki tuż przy powierzchni podłoża.
- podłoże z żelatyną - posiew przez wkłucie.
- podłoże z mannitolem
- (rozkład cukru).
- podłoże Simmonsa - posiew jałową ezą na podłoże.
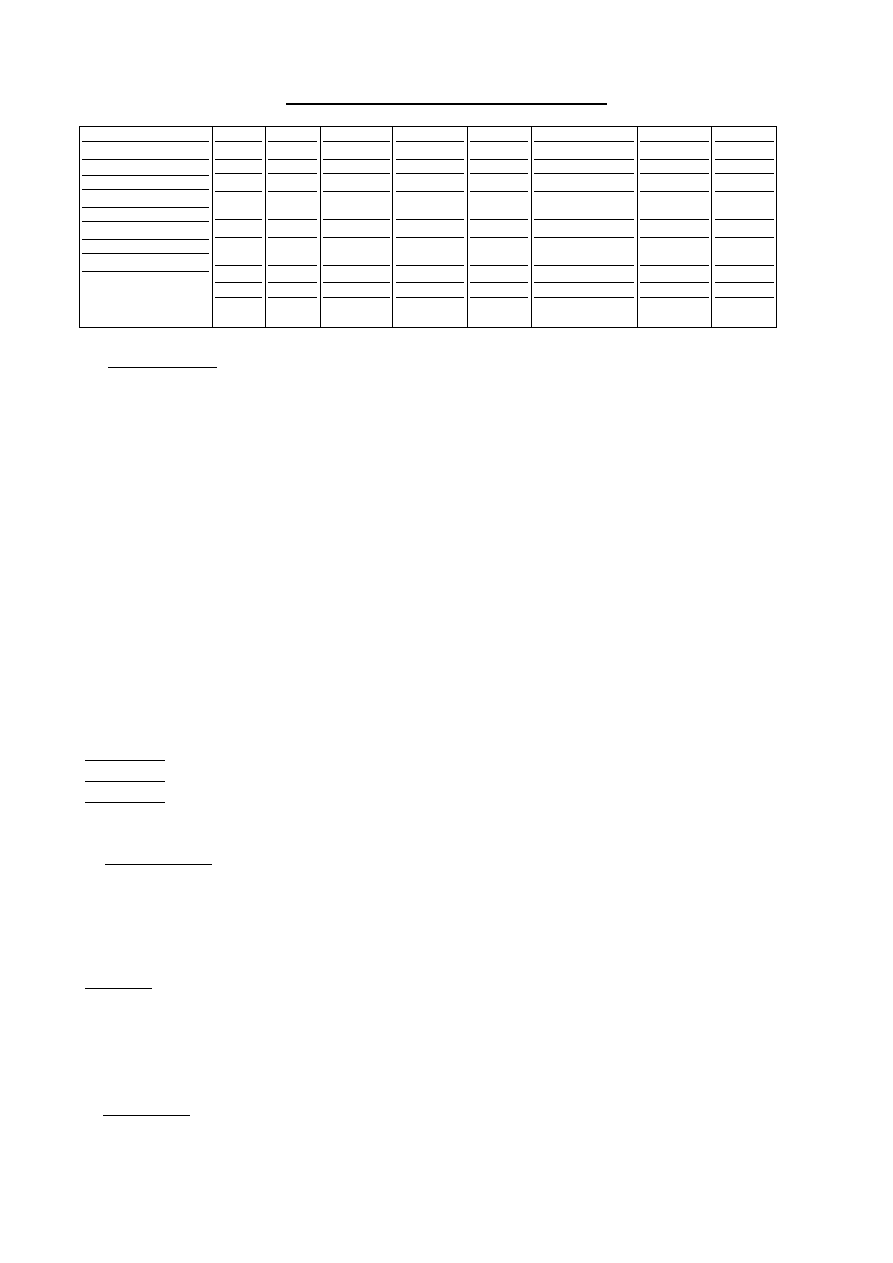
Odczytywanie szeregu biochemicznego.
Escherichia coli
Enterobacter sp.
Klebsiella oxytoca
Serratia marcescens
Salmonella anatum
Citrobacter freundii
Proteus mirabilis
Proteus vulgaris
Pseudomonas
aeruginosa
H
2
S
--
--
--
--
+
+
+
+
(+/--)
indol
+
--
--
--
--
--
--
+
(--/+)
mocznik
--
--
+
--
--
--
+
+
(--/+)
mannitol
+
+
+
+
+
+
(+/--)
(+/--)
--
laktoza
+
+
+
(+/--)
(+/--)
(+/--)
--
--
--
fenyloalanina
--
--
--
--
--
--
+
+
+
oksydaza
--
--
--
--
--
--
--
--
+
ruch
(+/--)
+
--
+
+
+
+
+
+
7. Test API 20E - mikrometoda do różnicowania bakterii z rodzaju Enterobacteriaceae i
innych G(-).
Metoda ta opiera się na różnicowaniu pałeczek na podstawie ich właściwości
metabolicznych. Pojedynczy zestaw mikroprobówek pozwala na wykonanie 20 oznaczeñ i
dodatkowo możliwe jest oznaczenie aktywności:
- oksydazy cytochromowej (OXI),
- redukcji azotanów do azotynów,
- uwalniania N
2
z azotanów.
W efekcie pozwala to na identyfikację jednego szczepu.
W każdej mikroprobówce znajduje się substrat i wskaŸnik umożliwiający odczytanie
wyniku reakcji, np: probówka 6 - (H
2
S) - zawiera 80 g tiosiarczanu sodowego. Jeśli
bakterie wytwarzają H
2
S z tiosiarczanu to H
2
S reaguje z solami żelaza tworząc czarny
osad (odczyt); probówka 7 - (URE) zawiera 0,8 mg mocznika. Bakterie wytwarzające
enzym ureazę, rozkładają mocznik z uwolnieniem amoniaku (pH zmienia się z kwaśnego
na zasadowe i następuje zmiana zabarwienia czerwieni fenolowej z żółtej na czerwoną).
W sumie otrzymuje się 21 prób. Te 21 prób podzielono na triady zgodnie z kolejnością
odczynów na pasku. Ostatni 21 odczyn stanowi próba na oksydazę. w efekcie uzyskuje się
7 grup. W każdej triadzie reakcje dodatnie są notowane i oznaczane we właściwych
wartościach numerycznych.
Wartość 1
- gdy próba dodatnia w pierwszym szeregu triady,
Wartość 2
- gdy próba dodatnia w drugim szeregu triady,
Wartość 4
- gdy próba dodatnia w trzecim szeregu triady.
Zapis kodowy 7-cyfrowy uzyskuje się przez dodanie wszystkich pozytywnych wartości
cyfrowych oddzielnie dla każdej triady.
5. Bakteriocyny.
Bakteriocyny są to substancje antybiotyczne o charakterze białkowym i wąskim spektrum
działania. łysinki fagowe - lakuny.
Bakteriocyny:
a) upostaciowione - duża masa cząsteczkowa,
b) nieupostaciowione - mała masa cząsteczkowa.
Kolicyny - bakteriocyny wytwarzane przez pałeczki jelitowe E. coli (najczęściej).
Biosynteza uwarunkowana jest genetycznie, a najczęściej determinanty genetyczne
kolicynogenii mają charakter plazmidów. Czynniki col są cząsteczkami DNA o strukturze
kolistej i wielkości 1/100 chromosomu bakteryjnego.
Wytwarzanie kolicyn można indukowaĆ UV, nitromycyną.
6.
Antybiotyki.
Antybiotyki są to substancje wytwarzane przez drobnoustroje (Streptococcus lactis, Bacillus, grzyb
Penicillum
i Aspergillus, promieniowce Streptomyces) i działające hamująco na wzrost, albo

litycznie czy niszcząco na inne mikroorganizmy. Wyróżniamy antybiotyki:
- interferujące z biosyntezą ściany komórkowej (hamują biosyntezę peptydoglikanu) -
Penicylina, Novobiotyna, Wankomycyna.
-
działające na błonę cytoplazmatyczną (działają silniej na G (-), dezorganizują LPS) -
Polimyksyna B, Kolistyna).
- hamujące syntezę białek (chloramfenicol, tetracykliny, neomycyna, streptomycyna).
- hamujące syntezę kwasów nukleinowych (sulfonamidy, nowobiocyna).
7.
Mechanizmy odporności na antybiotyki.
a) Modyfikacja enzymatyczna antybiotyku.
b) Modyfikacja rybosomu (antybiotyk, który wnika do komórki nie może połączyĆ się z
rybosomem).
c) Ominięcie szlaku metabolicznego.
d) Wypompowanie antybiotyków, które wniknęły do komórki.
e) Zmiana w budowie ściany komórkowej, która uniemożliwia wniknięcie antybiotyków.
8.
Sulfonamidy.
Sulfonamidy są to środki bakteriostatyczne, pochodne kwasu sulfanilowego, które włączają się do
metabolizmu drobnoustrojów w miejsce kwasu para-aminobenzoesowego, uniemożliwiając
namnażanie. Przerywają syntezę kwasu foliowego, który dla bakterii jest składnikiem wzrostowym.
Sulfonamidy:
- działające krótko - Sulfamidyna,
- działające długo i średnio - Madrixon,
- nierozpuszczające się w jelicie - Sulfaguanidyna,
- dobrze rozpuszczające się w moczu - Urenil.
WIADOMO
ŚCI TEORETYCZNE.
BAKTERIOFAGI.
1.
Ze względu na rodzaj materiału genetycznego (cząstka faga zawiera tylko białko i jeden rodzaj
kwasu nukleinowego) bakteriofagi dzielimy na:
a) zawierające DNA w postaci jednoniciowej (X174, M13),
b) zawierające DNA w postaci podwójnej nici (T2,T4, T6 itd, Mu, λ),
c) zawierające RNA (MS2, f2, QB).
2.
Ze względu na model namnażania bakteriofagi dzielimy na:
a) zjadliwe,
b) łagodne,
c) filamentne.
3.
Budowa faga przed wniknięciem jego DNA do bakterii.
a) główka z kwasem nukleinowym,
b) rdzeñ (może być kołnierz przy wstrzykiwaniu DNA),
c) rozciągnięta pochewka,
d) w dolnej części pochewki występuje białko bogate w grupy sulfhydrylowe (SH) biorące udział w
wprowadzaniu DNA do bakterii,
e) płytka podstawowa w postaci szeregu kolców,
f) w płytce podstawowej może znajdowaĆ się białko o charakterze enzymatycznym, rozpuszczające
ścianę komórkową.

4.
Budowa faga po wniknięciem DNA do komórki bakterii.
a) pusta główka (bez kwasu nukleinowego),
b) rdzeñ,
c) skurczona pochewka (białkowa otoczka),
d) nici ogonka.
5.
Cykl życiowy układu fag - komórka gospodarza.
1. Nie zakażona komórka.
2. Adsorpcja wolnego faga - komórka wrażliwa na faga - zawiera na powierzchni komórki
receptory.
3. Zakażenie lityczne - cząstka faga wegetatywnego może się namnażaĆ wytwarzając liczne kopie,
które dojrzewają wskutek otaczania się płaszczem białkowym. Komórka ulega lizie.
4. Redukcja faga wegetatywnego do profaga - fagi łagodne. Bakterie zawierające profagi zwane są
lizogennymi. Po nieokreślonej liczbie podziałów komórkowych jedna z komórek potomnych może
ulec lizie i uwolniĆ zakaŸnego faga.
5. Utrata profaga - czasami bakterie lizogenne spontanicznie tracą profagi, pozostają żywe, są
normalnymi, nie zakażonymi komórkami.
6.
Powstawanie profaga (połączenie profaga i chromosomu gospodarza).
1. DNA faga wnika do komórki gospodarza.
2. Koñce DNA faga łączą się wiązaniami kowalencyjnymi w strukturę kolistą.
3. Parowanie zachodzi między sekwencją zasad przylegającą do miejsca „gal” a homologiczną
sekwencją DNA faga.
4. W wyniku pęknięcia i krzyżowego połączenia się (crosing-over) w obszarze parowania następuje
połączenie dwóch kolistych struktur DNA. Przyłączony do DNA chromosowego, DNA faga zwany
jest profagiem.
7.
Odporność.
Bakterie lizogenne są odporne na zakażenie fagiem tego typu, którego profagi zawierają. Fagi
łagodne powodują pojawienie się w cytoplazmie substancji represorowej, która hamuje namnażanie
fagów wegetatywnych.
8.
Liza.
Liza (w przeciwieñstwie do lizogenii) zachodzi w warunkach korzystnych dla wzrostu faga (np.:
bogata pożywka).
1. Fag przytwierdza się niĆmi do powierzchni komórki.
2. Kurczy się pochewka.
3. Rdzeñ przebija ścianę komórkową.
4. DNA faga jest wstrzykiwane do komórki bakteryjnej (na zewnątrz komórki pozostaje tzw
„cieñ”).
5. Infekcja wywołuje następujące zmiany w komórce - zanik DNA gospodarza (fag wytwarza tzw.
wczesne geny - nukleazy degradujące DNA gospodarza). Genom wirusowy ma pełną kontrolę nad
metabolizmem gospodarza.
6. DNA wirusowy ulega wczesnej transkrypcji (transkrypcja mRNA na matrycy DNA). Pojawiają
się wczesne wirusowe mRNA, które indukują syntezę wczesnych białek wirusowych - nukleon.
Nukleony degradują DNA komórkowe, a uwolnione nukleotydy są substratami do syntezy DNA
fagowego. Jednocześnie następują zmiany właściwości aparatu transkrypcyjnego i translacyjnego.
7. Następnym etapem jest wczesna replikacja DNA (fagowa polimeraza, topoizomeraza, białka
topiące, ligaza polinukleotydowa, białka kompleksu replikacyjnego). Wczesna replikacja prowadzi
do pojawienia się kilkunastu kopii wirusowego DNA w komórce.
8. W trakcie replikacji następuje druga faza transkrypcji: rozpoczyna się powstawaniem wczesno-
późnego mRNA, a koñczy się utworzeniem późnych wirusowych mRNA, które kierują syntezą

białek strukturalnych wirusa.
9. Jednocześnie rozpoczyna się późna replikacja DNA, pojawiają się konkatamery (wiele kopii
genomu połączonych kowalencyjnie).
10. Cykl rozwojowy faga koñczy utworzenie wironów potomnych i synteza lizozymu - białka
degradującego ścianę komórki.
9.
Bakterie chorobotwórcze.
d)
Bordetella pertusis
G(-)
krztusiec - pałeczka
e)
Clostridium botulinum
G(+)
jad kiełbasiany - laseczka
f)
Clostridium perfringens
G(+)
zgorzel gazowa - laseczka
g)
Clostridium tetani
G(+)
tężec - laseczka
h)
Corynebacterium diphteriae
G(+), G(-)
błonica - dyfteryt - pałeczka
(maczugowiec)
i)
Eschericha coli
G(-)
zatrucie pokarmowe - pałeczka
j)
Neisseria gonorrhoe
G(-)
rzeżączka - ziarniak
k)
Neisseria meningitidis, Haemophilus influenzae
zapalenie opon mózgowych - ziarniak /
pałeczka
l)
Salmonella typhi
G(-)
dur brzuszny - pałeczka
m)
Shigella shigae
G(-)
czerwonka - pałeczka
n)
Staphylococcus aureus
G(+)
ropieñ, czyrak - ziarniak
o)
Streptococcus pneumoniae
G(+)
zapalenie płuc - ziarniak
p)
Streptococcus pyogenes
G(+)
angina - ziarniak
q)
Treponema pallidum
G(-)
kiła - krętek
r)
Vibrio cholerae
G(-)
cholera - przecinkowiec
s)
Yersinia pestis
G(-)
dżuma - pałeczka
Zagadnienia. Fizjologia mikroorganizmów – cd.
Metody hodowli bakterii beztlenowych. Co to są mikroorganizmy tlenowe (aeroby), beztlenowe (anaeroby), względnie beztlenowe i
mikroaerofile. Przykłady mikroorganizmów, należących do powyższych grup. Na czym polega oddychanie tlenowe oraz beztlenowe;
fermentacja. W jakim rodzaju oddychania uczestniczy oksydaza cytochromowa. Co wywołują bakterie Clostridium botulinum,
Clostridium perfingens i Clostridium tetani. Czym są: endotoksyna, enterotoksyny, endotoksyny. W jakim celu wykonuje się szereg
biochemiczny. Jakie właściwości bakterii bada się na podłożach: stosowanych podczas ćwiczeń. Do czego służą podłoża:
MacConkey'a, Chapmana, krwawe, Sabourauda, Eimhjellen. Jakie testy należy wykonać aby odróżnić: E.coli od Salmonella typhi;
Bacillus subtilis od E. coli; Proteus vulgaris od E.coli; Staphylococcus aureus od Micrococcus sp.; zakażenie bakteryjne od zakażenia
drożdżakami. Co to są i do czego służą testy API
Ć
wiczenie 6
Podstawowe odczyny serologiczne.
Baketrie z rodzajów Neisseria i Corynebacterium
Ziarniaki α
α
α
α,β
β
β
β,γγγγ-hemolizujące.
Bakterie dnia
f)
Aglutynacja szkiełkowa
o) Na szkiełko podstawowe nanieść kroplę surowicy wieloważnej HM oraz,
obok, kroplę soli fizjologicznej

p) Z podłoża stałego pobrać ezą niewielką ilość masy bakteryjnej Salmonela sp.
i rozprowadzić w kropli surowicy oraz soli fizjologicznej (kontrola negatywna)
Salmonella anatum
Salmonella heidelberg,
Salmonella london
Salmonella reading
Salmonellapanama
Salmonella tennesse
Identyfikacja paciorkowców grup A,B,C,D,E,F i G z wykorzystaniem Strepto-kit
zestawu firmy Bio-merieux
Wykonanie preparatów mikroskopowych met Grama Streptococcus, Enterococcus,
Neisseria, Corynebacterium,
Wykonanie preparatów z wymazów z gardła.
Barwienie bakterii z powietrza.
3.
Obronność (ochrona) przed infekcją:
a)
Obronność wrodzona, dziedzicznie przekazywana i niezależna od tego, czy organizm zetknął się
z zarazkiem, czy też nie - oporność.
b)
Obronność kształtująca się w czasie osobniczego życia i zależna jest od uprzedniego zetknięcia
się organizmu z zarazkiem - odporność.
Odporność naturalna (nieswoista) - wrodzona.
Odporność swoista - nabyta.
naturalna fizjologiczna ← odporność nieswoista → nabyta sztuczna
* cechy genotypowe,
* bariery fizyczno-chemiczne,
* system komórkowy (wielo- i jednojądrzaste fagocyty),
* nieswoista stymulacja (lizozym, dopełniacz, bakteriocydyny, przeciwciała naturalne).
humoralna ← odporność swoista nabyta → komórkowa
humoralna czynna - przechodzenie choroby, szczepienie.
humoralna bierna, sztuczna - podanie surowicy odpornościowej.
humoralna bierna, naturalna - otrzymanie przeciwciał z siarą lub przez łożysko.
komórkowa czynna - powstawanie aktywnych makrofagów zdolnych do fagocytozy.
komórkowa bierna - przeniesienie komórek limfoidalnych lub ich ekstraktów.
Jeśli organizmowi stałocieplnemu wprowadzi się do organizmu drogą pozajelitową
(zastrzyk dożylny, podskórny itp.) obce białka, wówczas zajdą w organizmie charakterystyczne
zmiany. Przede wszystkim w krwi (a zatem i w surowicy), pojawiają się w zwiększonej ilości białka
typu gamma-globulin (czasem też beta-globulun), zdolne do reagowania z substancją, jaką
wprowadziliśmy uprzednio do organizmu. Takie swoiście reagujące białka, powstające jako
odpowiedŸ na wspomniany bodziec, to przeciwciała. Wielkocząsteczkowe substancje, które
wprowadzone do organizmu drogą pozajelitową pobudzają ten organizm do wytwarzania
przeciwciał to - antygeny. Antygenami są białka oraz sprzężone z białkami makromolekuły innego

typu (np: wielocukry, kwasy nukleinowe), a nawet związki stosunkowo proste. Przeciwciała są
zdolne do reagowania z antygenami. Jeśli do organizmu, któremu uprzednio wprowadzono
pozajelitowo antygen, pobierzemy krew, pozwolimy jej skrzepnąć lub oddzielimy ciałka krwi , to
od skrzepu zawierającego komórki krwi oddzieli się złotawy płyn - surowica. W surowicy tej są
przeciwciała wytworzone przez organizm. Używając teraz surowicy zawierającej przeciwciała i
roztworu antygenu jako reagentów, możemy prześledzić in vitro przebieg reakcji pomiędzy nimi,
tzw. reakcję serologiczną.
Charakter reakcji pomiędzy przeciwciałem, a antygenem bywa różny, zależnie od stanu
fizykochemicznego używanego antygenu. Surowica nawarstwiona na rozpuszczony antygen tworzy
strąt przeciwciała i antygenu - precypitat, a reakcja ta nosi nazwę precypitacji.
Jeśli surowicę zawierającą przeciwciała zmieszać z antygenem złożonym np: z zawiesiną
komórkową bakterii, dojdzie do ich zlepienia, czyli aglutynacji. Reakcja między przeciwciałem a
antygenem jest bardzo swoista. Przeciwciało reaguje zwykle z antygenem, pod wpływem którego
zostało wytworzone przez organizm.
4.
Budowa antygenowa komórki Enterobacteriae:
- torebka (K),
- lipopolisacharydowe łañcuchy boczne (O) - antygen somatyczny,
- otoczka komórkowa (błona cytoplazmatyczna, peptydoglikan, błona zewnętrzna).
Za przynależność do grupy odpowiada obecność antygenu (O), a za przynależność do serotypu -
obecność antygenu (H).
5.
Aglutynacja szkiełkowa.
Do orientacyjnych badañ serologicznych Salmonella używa się hodowli 24 godzinnej na agarze.
Oznaczanie przeprowadza się na szkiełku podstawowym, używając surowic przechowywanych w
temperaturze 4
o
C. Na szkiełko przenosi się pipetą kroplę surowicy HM, zawierającą przeciwciała
przeciw wszystkim znanym antygenom H Salmonella, a inną pipetą umieszcza się obok na tym
samym szkełku kroplę jałowego 3% roztworu NaCl. Masę bakteryjną pobiera się ezą i zawiesza
osobno w kropli NaCl i surowicy. Za pomocą lupy sprawdza się czy nie występuje odczyn
aglutynacji w kontroli i szkiełko umieszcza się w płytce Petriego, wyścielonej wilgotną ligniną. Po
5-10 minutach szkiełko wyciąga się, lekko porusza w celu wymieszania płynu w każdej kropli i
odczytuje wynik przez lupę. Występowanie ziarnistości lub kłaczków w próbie badanej świadczy o
dodatnim wyniku.
1. Flora fizjologiczna i flora patogenna
.
a)
Wykonanie preparatów mikroskopowych z materiałów własnych barwionych matodą Grama.
3.
Aglutynacja szkiełkowa. Poj
ęcie serotypu.
a)
Na szkiełko nanieść kroplę surowicy wieloważnej HM.
b)
Z podłoża stałego pobraĆ ezą niewielką ilość masy bakteryjnej Salmonella sp. i rozprowadziĆ w
kropli surowicy.
c)
Kontrola - zawiesina bakterii w roztworze soli fizjologicznej.
WIADOMO
ŚCI TEORETYCZNE.
1.
Flora fizjologiczna - normalna mikroflora organizmu.
Komensale - tworzą normalną mikroflorę organizmu. Część komensali nie odgrywa żadnej roli, ich
obecność może byĆ obojętna dla organizmu. W większości przypadków odgrywają one pewną rolę.
a)
Jama ustna - w osadzie nazębnym i przy krawędzi dziąseł zawsze występują bakterie.
Najliczniejsze to:
- ziarniaki,
- G (+) pałeczki pokrewne Lactobacillus i paciorkowce (tworzą śluzy za pomocą których przylegają
do szkliwa) - wytwarzają z węglowodanów kwas mlekowy, odpowiedzialne są również za
uszkodzenia szkliwa i próchnicę zębów.
- krętki,
- G (-) pałeczki z rodzaju Enterobacteriae,
- pełzaki,
- pozostałe to komensale.
Usunięcie tej mikroflory (np: antybiotykami), powoduje masowy rozwój infekcji grzybowej.
b)
żołądek - środowisko silnie zakwaszone (HCl), nie pozwala na wzrost i rozwój bakterii. Gdy
występuje niedokwasota, to występują bakterie z rodzajów:
- Lactobacillus,
- Sarcinia ventriculi.
c)
Jelita - rodzaj mikroflory zależy od rodzaju pokarmu. U niemowląt karmionych naturalnym
mlekiem - Lactobacillus bifidus, karmionych mlekiem sztucznym - Lactobacillus acidophilus. U
dorosłych:
- w górnych partiach - enterokoki (Streptococcus faecalis),
- niżej - Clostridium perfringens i inne gatunki tego rodzaju,
- pałeczki Enterobacteriae (E. coli),
- liczne beztlenowce,
- nie przetrwalnikujące pałeczki i laseczki.
Mikroflora ta dostarcza dużych ilości witaminy B i nie dopuszcza do rozwoju szkodliwych
drobnoustrojów. Gdy nastąpi wyjałowienie antybiotykami, to rozwijają się grzyby, a u niemowląt
gronkowce wytwarzające enterotoksynę.
d)
Błona śluzowa jamy nosowej:
- gronkowce (Staphylococcus aureus i Staphylococcus albus),
- bakterie zbliżone do Corynebacterium (tzw. dyfteroidy).
e)
Jama nosowo-gardłowa:
- hemolizujące paciorkowce,
- G(-) ziarniaki.
f)
Cewka moczowa:
- Staphylococcus albus
-
dyfteroidy,
- kwasooporny, saprofityczny prątek Mycobacterium smegmatis.
g)
Pochwa:
- Lactobacillus, zwany pałeczką Döderleina (daje kwaśny odczyn).
h)
Skóra:
- Staphylococcus albus,
- Staphylococcus aureus -
u niektórych ludzi.
Zatoki nosowe, tchawica i oskrzela w zasadzie powinny byĆ wolne od bakterii.
Wyszukiwarka
Podobne podstrony:
Program ćwiczeń z mikrobiologii dla biotechnologów, Mikrobiologia, Mikrobiologia
Ćwiczenia ortograficzne dla uczniów klasy III
ZESTAW ĆWICZEŃ DOMOWYCH DLA DZIECI Z PŁASKOSTOPIEM I KOŚLAWOŚCIĄ KOLAN, korektywa(1)
Ćwiczenie 5, Mikrobiologia i immunologia
Ćwiczenia Kegla dla mężczyzn, dla mężczyzn, Ćwiczenia
Cwiczenia MATERIALY dla UP
63 zbior cwiczen metafonologicznych dla nauczycieli nauczania poczatkowego
ćwiczenia 1-2, Mikrobiologia
Ćwiczenie 3, Mikrobiologia
Konspekt ćwiczeń psychologicznych dla dzieci z problemami koncentracji uwag1, Autyzm
rzeczowniki do cwiczen w odmianach dla prawa, Prawo, Łacina
Ćwiczenia i zabawy dla dzieci agresywnych i nadpobudliwych
więcej podobnych podstron