LABORATORIUM 5
Temat: WPŁYW INHIBITORÓW I CZYNNIKÓW FIZYCZNYCH NA
PRZEBIEG REAKCJI ENZYMATYCZNYCH
Inwertaza, sacharaza, ß-D-fruktofuranozydaza, enzym z klasy hydrolaz i podklasy
glikozydaz, rozkładający cukier sacharozę na glukozę i fruktozę. Występuje głównie w
komórkach roślinnych, gdzie związany jest ze ścianą komórkową. Najłatwiej uzyskuje się ten
enzym z komórek drożdży.
Sacharoza disacharyd, złożony z fruktozy i glukozy, będący zasadniczym składnikiem cukru
trzcinowego i cukru buraczanego. W temperaturze pokojowej sacharoza jest bezbarwnym,
krystaliczny ciałem stałym. Jest nietoksyczna, ma słodki smak i bardzo dobrze rozpuszcza się
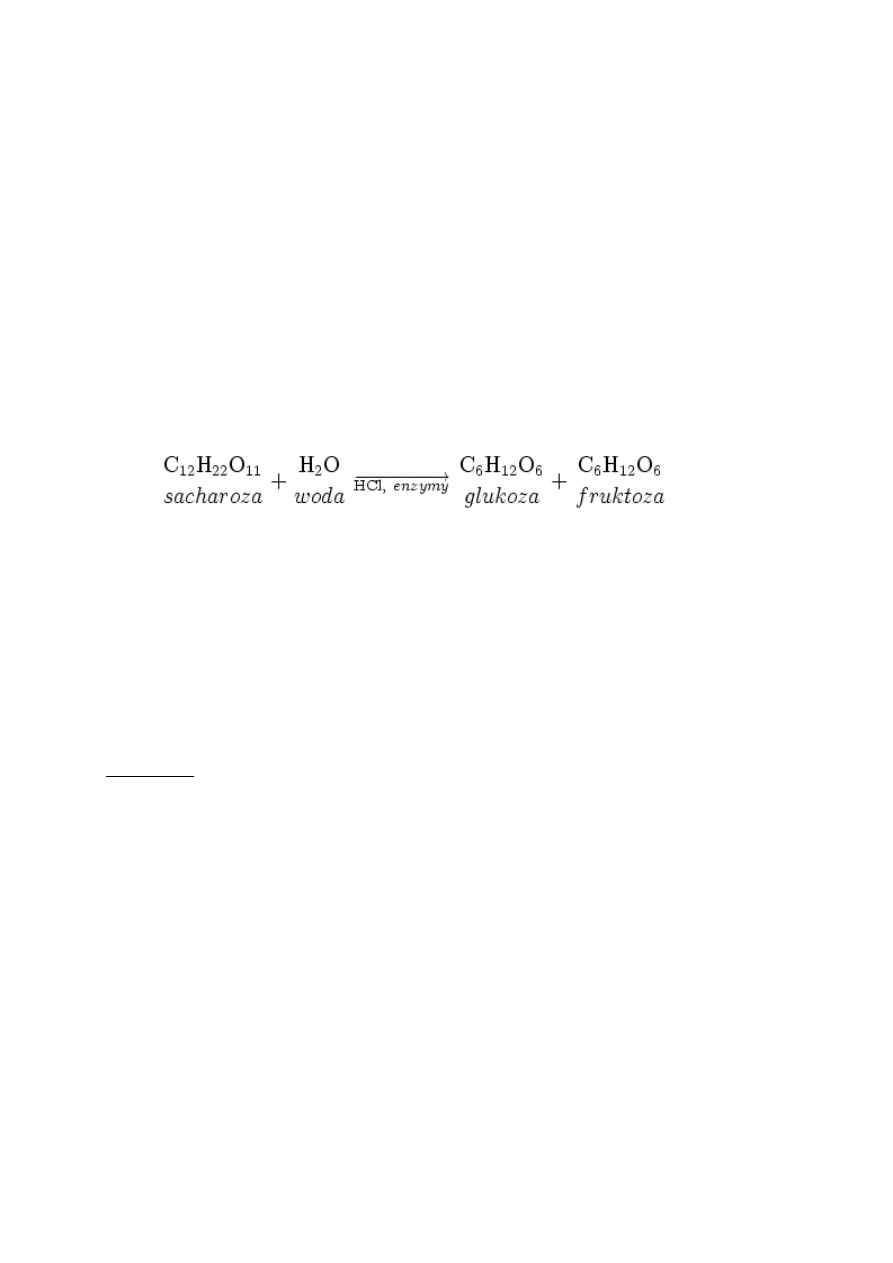
w wodzie. Należy do cukrów nieredukujących. W kwaśnych warunkach hydrolizuje do
fruktozy i glukozy wg schematu:
Zadanie 1. Wpływ pH na aktywność inwertazy z drożdży
Szybkość reakcji katalizowanej przez enzym jest maksymalna przy określonej wartości pH, a
maleje w miarę oddalania się od niej (zbyt kwasowe lub zasadowe środowisko może
powodować denaturację białek). Zmiany aktywności enzymatycznej przy różnym pH są
wywołane zmianami w stopniu zjonizowania składników układu: enzymu, substratu i
kompleksu enzym- substrat.
Inwertaza jest enzymem aktywnym w szerokim kwasowym zakresie pH od 4 do 6.
Optymalne pH ma wartość 4,7. Przy pH 2 i 9 jest już praktycznie nieaktywna.
Wykonanie:
Przygotować 7 probówek. Do 6 probówek wprowadzić po 1 ml odpowiedniego buforu o pH
3; 4,7; 5; 7; 9 i 11. Następnie do każdej probówki dodać 1 ml 0,3M sacharozy oraz 1 ml
inwertazy o optymalnym stężeniu. Przygotować także próbę kontrolną w 7-mej probówce
zawierającą 1ml buforu o pH 4,7; 1ml 0,3M sacharozy i 1 ml wody zamiast enzymu. Po
wymieszaniu wszystkich składników mieszaniny inkubacyjne zostawić na 30 minut. Po tym
czasie zalkalizować próby paroma kroplami 1M roztworu NaOH (sprawdzić pH !), a
następnie we wszystkich mieszaninach wykonać próbę Benedicta. W tym celu do siedmiu
czystych probówek dodać po 1 ml odczynnika Benedicta i do każdej z nich dodać 0,2 ml
mieszaniny reakcyjnej. Probówki umieścić na ok. 1-2 minuty we wrzącej łaźni wodnej.
Zanotować wyniki i zinterpretować je.
Zadanie 2. Wpływ temperatury na aktywność inwertazy z drożdży
Ze wzrostem temperatury zwiększa się szybkość reakcji enzymatycznej. Po osiągnięciu
pewnego optimum w danych warunkach szybkość reakcji zaczyna maleć w następstwie
denaturacji cieplnej enzymu. Większość enzymów traci nieodwracalnie aktywność po
przekroczeniu temperatury 65
0
C i tylko nieliczne wytrzymują krótkie gotowanie

(rybonukleaza, żelatyna czy pepsyna w pH 1). W zakresie temperatur, w których denaturacja
enzymu jest praktycznie nieistotna, a więc ok. 37
0
C, podniesienie temperatury o 10
0
C
zwiększa szybkość reakcji mniej więcej 2- krotnie.
Wykonanie:
Przygotować 6 probówek, a następnie do wszystkich dodać po 0,5 ml sacharozy w buforze
octanowym o pH 4,7 oraz do pięciu z nich 0,5 ml inwertazy drożdżowej o optymalnym
stężeniu. Do szóstej probówki zamiast inwertazy dodać 0,5 ml wody. Próby umieścić na 30
minut w temperaturze: 4, 20, 37, 60, 100
0
C, a próbę kontrolną w temperaturze 20
0
C. Po
zakończeniu inkubacji zalkalizować próby paroma kroplami 1M roztworu NaOH (sprawdzić
pH !), a następnie we wszystkich mieszaninach wykonać próbę Benedicta. W tym celu do
sześciu czystych probówek dodać po 1 ml odczynnika Benedicta i do każdej z nich dodać 0,2
ml mieszaniny reakcyjnej. Probówki umieścić na ok. 1-2 minuty we wrzącej łaźni wodnej.
Zanotować wyniki i zinterpretować je.
Zadanie 3. Wpływ promieniowana UV na aktywność inwertazy z drożdży
Aminokwasy aromatyczne występujące w białkach mają zdolność do absorbowania
promieniowania ultrafioletowego, co powoduje wzrost energii w obrębie cząsteczki białka, a
tym samym zaburzenia w jego strukturze.
Wykonanie:
Na szkiełko zegarkowe wlać 6 ml inwertazy z drożdży i poddać ją naświetlaniu promieniami
ultrafioletowymi. Po czasie naświetlania: 0 sek., 10 sek., 20 sek., 30 sek., 1 min., 2 min., 3
min., 4 min. pobierać do kolejnych probówek po 0,5 ml roztworu inwertazy i do wszystkich
ośmiu prób dodać 0,5 ml roztworu sacharozy w buforze octanowym o pH 4,7. Próby
wymieszać i umieścić na 30 minut w temperaturze pokojowej. Po tym czasie zalkalizować
próby paroma kroplami 1M roztworu NaOH. Następnie we wszystkich mieszaninach
wykonać próbę Benedicta. W tym celu do ośmiu czystych probówek dodać po 1 ml
odczynnika Benedicta i do każdej z nich dodać 0,2 ml mieszaniny reakcyjnej. Probówki
umieścić na ok. 1-2 minuty we wrzącej łaźni wodnej. Zanotować wyniki i zinterpretować je.
Wyszukiwarka
Podobne podstrony:
II OŚ Biochemia ćwiczenie 3
II OŚ Biochemia ćwiczenie 2
II OŚ Biochemia ćwiczenie 1
II OŚ Biochemia ćwiczenie 7
II OŚ Biochemia ćwiczenie 4
II OŚ Biochemia ćwiczenie 7
II OŚ Biochemia ćwiczenie 4
II OŚ Biochemia ćwiczenie 5
II OŚ Biochemia ćwiczenie 3
II OŚ Biochemia ćwiczenie 6
II OŚ Biochemia ćwiczenie 6
II OŚ Biochemia ćwiczenie 3
więcej podobnych podstron