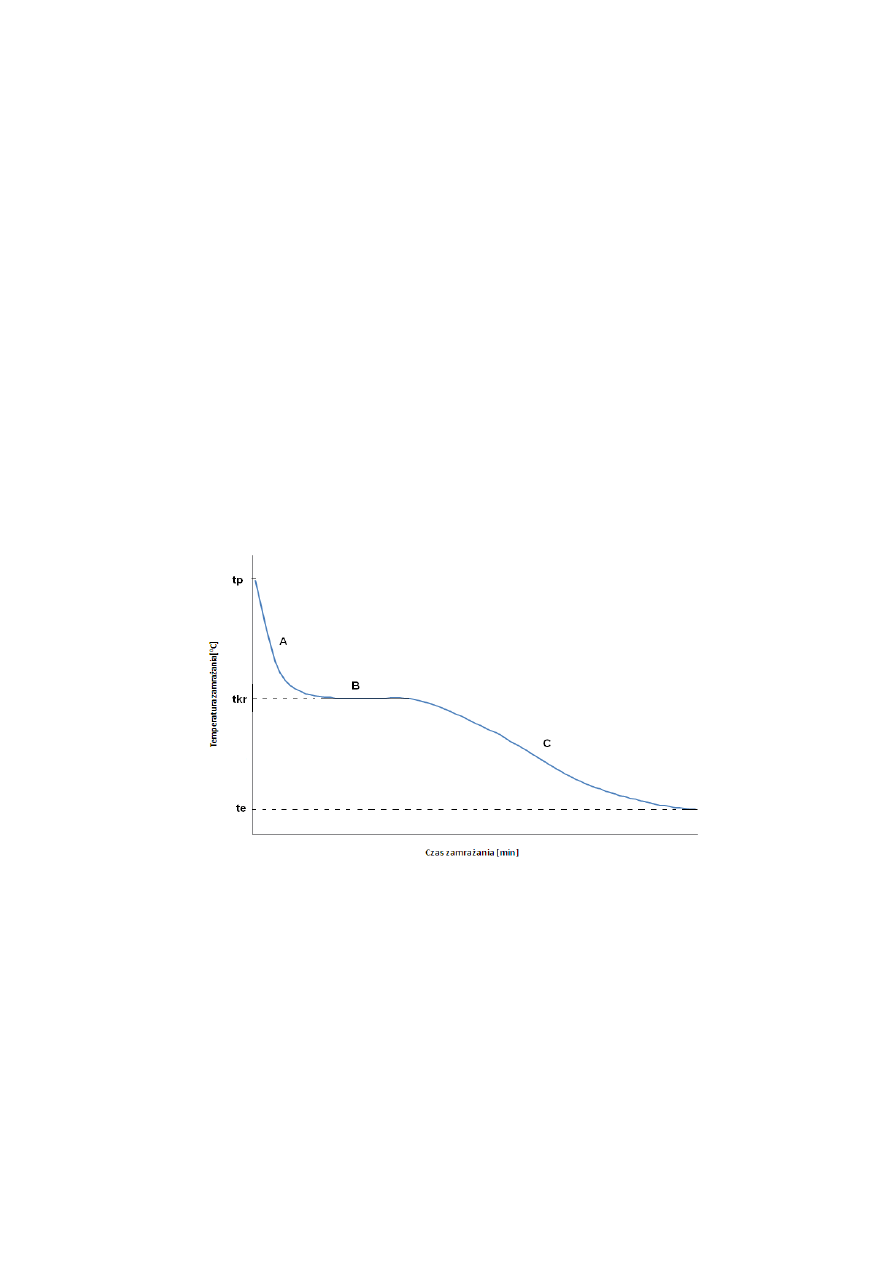
Autor: mgr inż. Urszula Ulanicka
Temat: Ocena procesu zamrażania produktów spożywczych na przykładzie roztworów
sacharozy
Wstęp teoretyczny
Zamrażanie jest specyficznym procesem w przetwórstwie żywności polegającym na obniżaniu
temperatury zamrażanego produktu, poniżej temperatury krioskopowej. Zjawiskiem towarzyszącym
temu procesowi jest przemiana fazowa wody w lód, związana z oddawaniem ciepła (335,2 kJ/kg). W
wyniku uwalniania się tak znacznych ilości ciepła dochodzi do obniżenia energii kinetycznej
cząsteczek wody (zawartych w produkcie spożywczym) powodując jednocześnie uporządkowanie ich
w zwartą sieć krystaliczną. Ponadto należy zwrócić uwagę na fakt iż woda zmieniając swój stan
skupienia, zmienia także swoje właściwości termofizyczne takie jak ciepło właściwe, przewodność
cieplną, dyfuzyjność cieplną czy też gęstość.
Celem stosowania procesu zamrażania jest przede wszystkim utrwalenie żywności, a także
zagęszczanie soków oraz produkcja lodów. Ponadto proces zamrażania wykorzystywany jest jako
pierwszy etap suszenia sublimacyjnego czyli tzw. Liofilizacji, służącej utrwaleniu materiałów
biologicznych termo labilnych o delikatnej strukturze (np. drożdże spożywcze).
Proces zamrażania interpretowany jest na podstawie tzw. krzywych mrożenia. Są to wykresy
ilustrujące zależność zmian temperatury zamrażanego materiału od czasu trwania całego procesu.
Analizując przebieg krzywej mrożenia (rysunek 1), można wyodrębnić trzy charakterystyczne
elementy odpowiadające etapom zamrażania:
Schładzanie – (odcinek A) etap obniżania temperatury zamrażanego materiału od temperatury
początkowej t
p
, do temperatury krioskopowej t
kr
;
Właściwe zamrażanie – (odcinek B) prostoliniowy odcinek krzywej charakteryzujący etap
przemiany fazowej wody w lód, która odbywa się bez zmiany temperatury. Temperaturą, w
której tworzone są pierwsze kryształy lodu czystej wody wynosi -0,5 do -0,8°C, z kolei w
Rysunek 1. Przykładowa krzywa mrożenia produktu spożywczego.
przypadku zamrażania produktów spożywczych w miarę wymrażania wody dochodzi do
wniosku stężenia soku komórkowego przy jednoczesnym obniżaniu temperatury
krioskopowej. Według Rjutowa temperatura właściwego zamrażania wynosząca -4°C
powoduje wymrożenie 73% wody wolnej w materiale;
Domrażanie – (odcinek C) etap termicznej dyfuzji ciepła, temperatura jest w dalszym ciągu
obniżana, do czasu uzyskania temperatury zadanej w całym procesie.
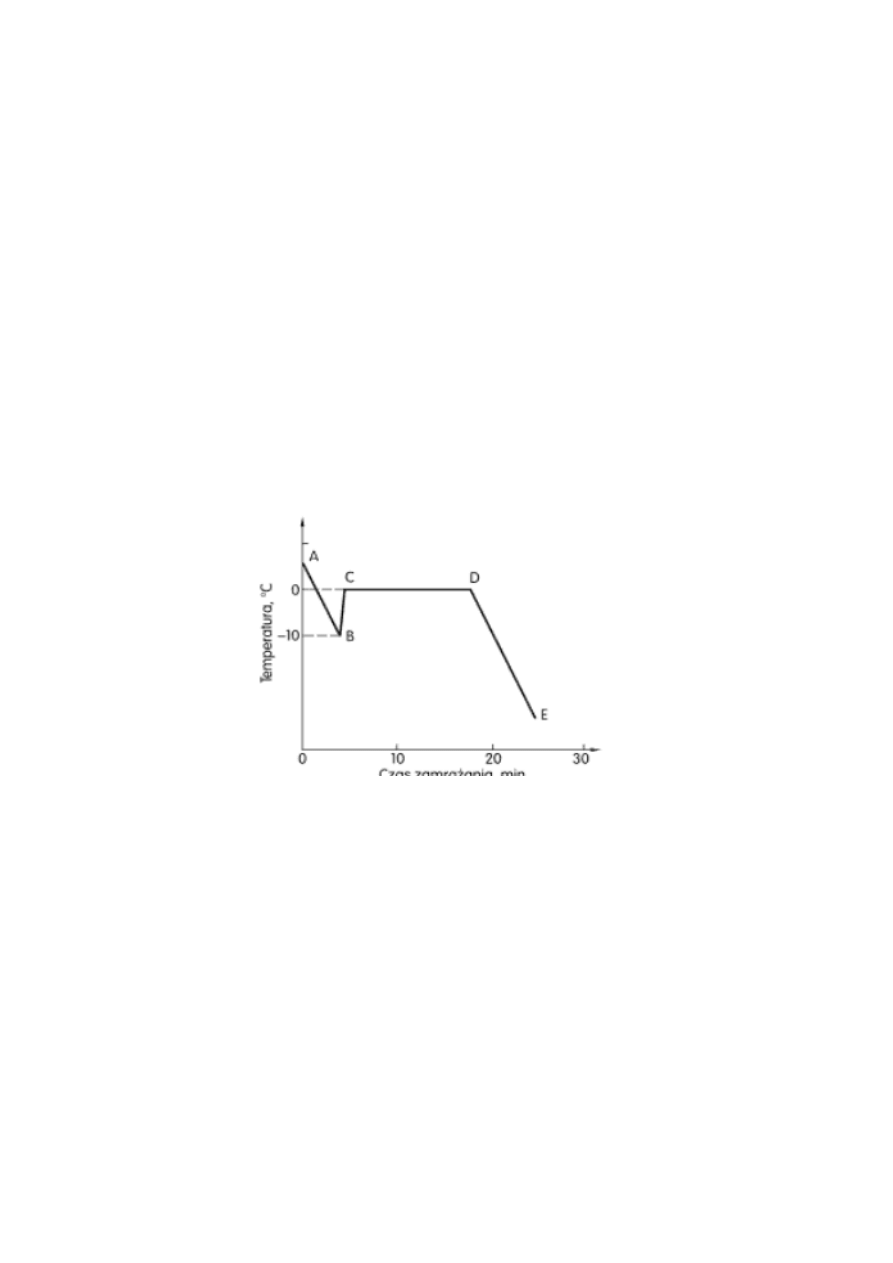
W przypadku zamrażania czystej wody może dojść do tzw. przechłodzenia. Jest to niestabilny
stan, w którym woda występuje w stanie ciekłym przy temperaturze niższej niż 0°C. Stan ten zakłócić
może pojawienie się zarodka kryształu lodu, którym mogą być między innymi szron zgromadzony na
powierzchni zamrażanego roztworu lub cząsteczka kurzu. W wyniku pojawienia się zarodka kryształu
lodu dochodzi do gwałtownego wydzielenia się ciepła powodującego charakterystyczny – widoczny
na krzywej jako pik ( odcinek AB i BC na rysunku 2) – wzrost temperatury do temperatury
zamarzania wody. Istnieje zależność mówiąca, że im wolniej jest zamrażana woda tym większe
występuje przechłodzenie.
Każdy zamrażany produkt lub roztwór charakteryzuje się specyficznym kształtem krzywej
mrożenia, zależnym między innymi od metody zamrażania, charakteru zamrażanego produktu (kształt,
wielkość, skład chemiczny, właściwości fizyczne) oraz obecności opakowania.
Jak już wspomniano woda zmieniając stan skupienia zmienia swoje właściwości. Ciepło
właściwe wody wynosi 4,187 kJ/(kg*K) zaś lodu jest prawie 2 razy mniejsze i wynosi 2,093
kJ/(kg*K). Odwrotną zależność obserwuje się przy współczynniku przewodzenia ciepła λ, dla wody
wynosi on 0,59 zaś dla lodu 2,24 W/(m*K). W temperaturze 0°C gęstość lodu jest mniejsza od
gęstości czystej wody (1000 kg/m
3
) i wynosi 917 kg/m
3
. Bardzo istotną właściwością jest również
współczynnik wyrównania temperatury, który dla czystej wody wynosi 0,14*10
-6
m
2
/s zaś dla lodu
1,16*10
-6
m
2
/s.
Zamrażanie materiałów biologicznych (tkanek roślinnych i zwierzęcych) znacznie różni się od
zamrażania czystej wody gdyż produkty żywnościowe są skomplikowanym układem, w którym woda
nie występuje w stanie czystym lecz tworzy roztwory zawierające sole mineralne, białka, cukry.
Ponadto układy biologiczne charakteryzują się tym, że wszystkie roztwory komórkowe zamknięte są
Rysunek 2. Schemat krzywej mrożenia czystej wody (Dłużewska, 2008).

w wyspecjalizowanych błonach, przez co łatwiej je uszkodzić podczas zamrażania. Zarodki
kryształów lodu powstają najpierw w przestrzeniach międzykomórkowych, a krystalizacja
wewnątrzkomórkowa następuje dopiero przy intensywnym oziębianiu.
Na podstawie krzywych mrożenia można wyznaczyć wartość tzw. temperatury
krioskopowej dla zamrażanego produktu. Jest ona początkową temperaturą, w której
rozpoczyna się właściwa przemiana fazowa wody w lód. Jej wartość, dla większości
naturalnych produktów żywnościowych, waha się w granicach od -0,5 do -2°C. Temperatura
zamarzania produktów jest zależna przede wszystkim od stężenia roztworu, masy
cząsteczkowej oraz od stopnia dysocjacji substancji w nim rozpuszczonych. Bardzo ważne są
również właściwości samego rozpuszczalnika. Obniżenie temperatury krioskopowej, opisane
jest wzorem Raoulta:
, gdzie
– współczynnik charakterystyczny dla danego rozpuszczalnika, tzw. stała krioskopowa
(dla wody wynosi 1,86 K/mol);
– stężenie molowe roztworu, [ mol/kg].
Na wartość temperatury krioskopowej ma wpływ rodzaj substancji rozpuszczonych
w roztworze, a w szczególności ich masa cząsteczkowa. Substancje o małej masie
cząsteczkowej np. cukry takie jak glukoza, fruktoza czy sacharoza oraz rozpuszczalne białka
wpływają na obniżenie punktu zamarzania. Najbardziej znaczące jest ich stężenie
w zamrażanym roztworze, gdyż istnieje zależność mówiąca, że wraz ze wzrostem stężenia
substancji rozpuszczonych w roztworze, spada punkt jego zamarzania. Podobna zależność jest
zaobserwowana przy zwiększonym stężeniu chlorku sodu, a także alkoholu.
Przeprowadzając proces zamrażania dąży się do maksymalnego skrócenia czasu tego procesu
przy optymalnym wykorzystaniu dostępnej technologii oraz uwzględnieniu aspektów
finansowych. Z przeprowadzonych analiz wynika, że czas zamrażania zależy od takich
czynników jak:
geometria zamrażanego produktu,
czynna różnica temperatur,
współczynnik wnikania ciepła pomiędzy produktem, a medium,
obecność opakowania,
współczynnik przewodzenia ciepła produktu.
Jeżeli chodzi o geometrię cząsteczki to największy wpływ na czas zamrażania ma
grubość zamrażanego ciała. Bardzo istotnie wpływa również kształt ciała i tak przy tych
samych grubościach najkorzystniejszy jest kształt kuli, a następnie walca i prostopadłościanu
(oziębianego ze wszystkich stron) – najmniej korzystna jest postać płyty.
Grubość materiału zamrażanego ma największy wpływ w nowoczesnych aparatach
zamrażania tzn. kontaktowych i kriogenicznych ze względu na duży współczynnik wnikania
ciepła, jednak dąży się do redukcji grubości materiału.
Według przeprowadzonych doświadczeń stwierdzono, że czas zamrażania jest odwrotnie
proporcjonalny do różnicy temperatur między zamrażanym produktem i czynnikiem
chłodzącym. Jest to bardzo istotne przy zamrażaniu owiewowym gdzie małe są
współczynniki wnikania ciepła.
Wpływ współczynnika przewodzenia ciepła rośnie wraz ze wzrostem grubości
zamrażanego ciała i ogólnie jest on zdeterminowany przez właściwości fizyczne produktu.
W procesie zamrażania chodzi przede wszystkim o poprawę współczynnika wnikania ciepła
oraz o maksymalne rozwinięcie i wykorzystanie powierzchni czynnej wymiany ciepła.

Współczynniki wnikania ciepła mają różne wartości zależne od typu aparatu oraz metody
mrożenia. Aby skrócić czas mrożenia należy uzyskać jak największe współczynniki wnikania
ciepła, jednak jest to bardzo energochłonne.
Czynnikiem utrudniającym warunki przepływu ciepła od powierzchni produktu do
medium jest opakowanie, jednocześnie można ten czynnik przyrównać do pogorszenia
współczynnika wnikania ciepła. Poza tym opakowanie (w szczególności wielowarstwowe)
znacznie wydłuża czas zamrażania, co wynika z dużego współczynnika przewodzenia ciepła
samego opakowania lub obecnej warstewki powietrza zawartej między opakowaniem,
a produktem. Aby zapobiec temu stosuje się odpowiednie dociski np. w aparatach
kontaktowych stosuje się hydrauliczny docisk płyt wynoszący ok. 7000 N/m
2
lub pakowanie
próżniowe i stosowanie folii termokurczliwych np. przy pakowaniu produktów nieforemnych
jak drób czy ryby.
Szybkość zamrażania jest stosunkiem grubości zamrażanej warstwy do czasu,
w którym dochodzi do zamrożenia. Uważa się, że prowadzenie procesu zamrażania z dużą
prędkością gwarantuje zachowanie najlepszych cech jakościowych żywności. Powoduje ono
powstawanie w mrożonym materiale wielu, drobnych kryształów lodu, które nie niszczą jego
struktury wewnętrznej.
Wykonanie ćwiczenia
Celem ćwiczenia jest sporządzenie krzywych mrożenia roztworów sacharozy o
różnym stężeniu, wyznaczeniu temperatury krioskopowej badanych roztworów oraz
teoretycznego i praktycznego czasu zamrażania. Ponadto ćwiczenie ma na celu wyznaczenie
bilansu cieplnego procesu zamrażania.
Materiał i metodyka badań
Materiał badawczy stanowić będą roztwory sacharozy o stężeniu odpowiednio 10, 20 i
30% sporządzone w ilości 35 ml każdy. Dodatkowo dla porównania zamrożona zostanie także
próbka czystej wody. Roztwory zamrażane będą w trzech wariantach temperatury medium
chłodzącego:
-10°C;
-20°C;
-30°C.
Proces prowadzony będzie do czasu uzyskania przez roztwory temperatury bliskiej
temperaturze medium chłodzącego, utrzymującej się na stałym poziomie przez minimum 3
minuty. Zaleca się aby średnia końcowa temperatura dla danego wariantu temperaturowego
była stała dla wszystkich zamrażanych próbek.
Wyznaczane dane
1. Wyznaczenie krzywych mrożenia
Krzywe mrożenia sporządzone zostaną na podstawie rejestracji zmian temperatury w
czasie trwania procesu. Na jednym wykresie przedstawione powinny być 4 krzywe
odpowiadające zamrażaniu czystej wody, roztworowi sacharozy 10, 20 i 30%, w
danym wariancie temperatury.
2. Wyznaczenie temperatury krioskopowej
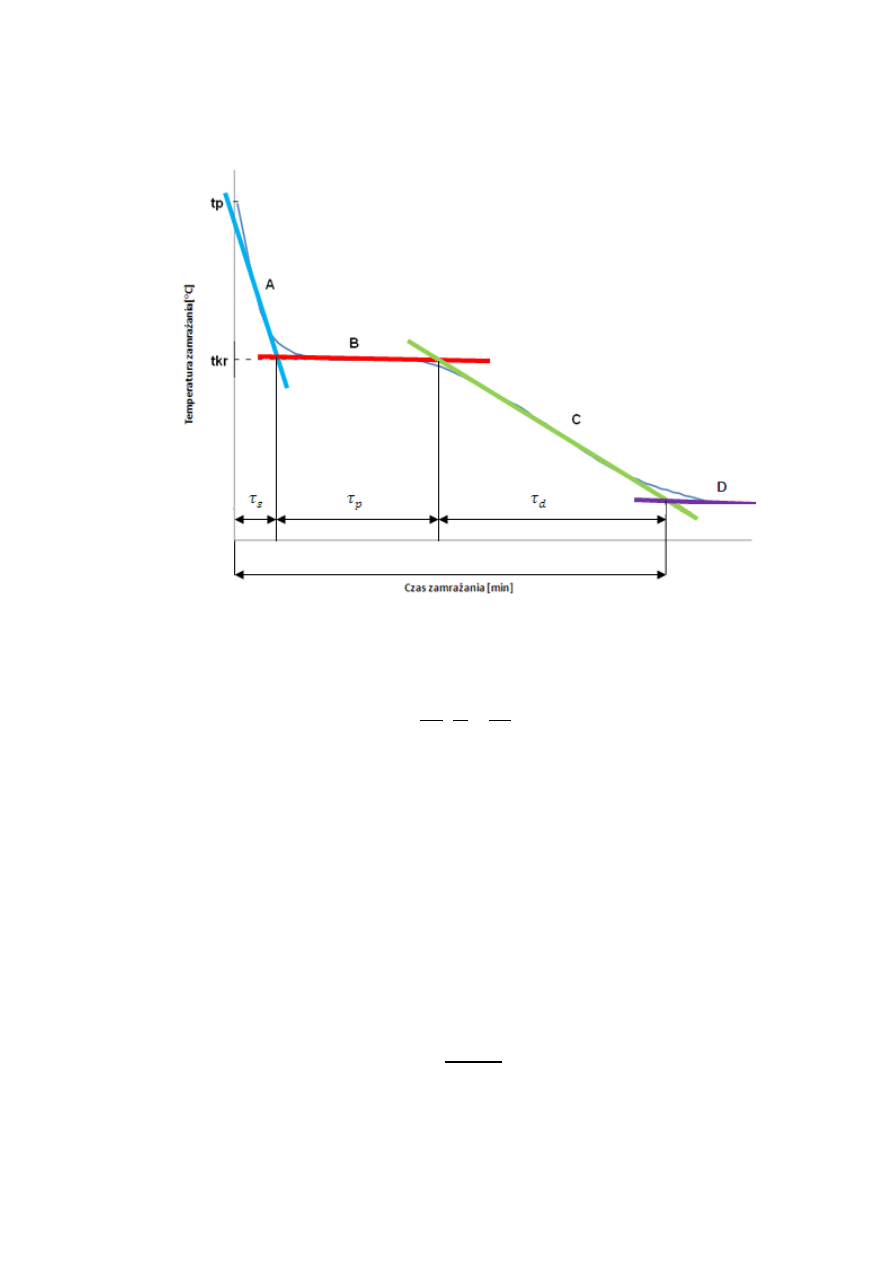
Z uzyskanych krzywych mrożenia wyznaczyć należy temperaturę krioskopową dla
danego roztworu. Sposób wyznaczenia temperatury krioskopowej ilustruje poniższy
rysunek:
3. Wyznaczenie teoretycznego i praktycznego czasu zamrażania
Teoretyczny czas zamrażania (τ
t
) wyznaczamy z poniższego wzoru:
g
dzie,
d
e
– średnica oziębianej powierzchni [m];
α – współczynnik wnikania ciepła (dla tuneli owiewowych o silnej wentylacji
40W/(m
2
*K));
λ
e
– przewodność cieplna produktu (wyliczana ze wzoru λ
e
=0,581(1-0,54s) gdzie, s
jest koncentracją sacharozy), [W/(m*K)];
ρ – gęstość roztworu sacharozy w T=293K (wyliczana ze wzoru
ρ=30,9s
3
+144,1s
2
+384,1s+1000), [kg/m
3
];
q
z
– ciepło zamarzania (przemiany wody w lód) [kJ/kg];
Δt – czynna różnica temperatur, między produktem, a medium [°C];
Czynna różnica temperatur obliczana jest z poniższego wzoru:
gdzie,
t
mp
– temperatura początkowa medium [°C];
t
mk
– temperatura końcowa medium [°C].

Czas praktyczny (τ
p
) jest czasem zmierzonym, w trakcie którego temperatura
zamrażanego roztworu niemalże równa temperaturze czynnika chłodzącego. Czas
praktyczny trwania procesu jest sumą czasów trwania poszczególnych etapów
zamrażania, które można wyznaczyć na podstawie krzywych mrożenia. Stąd
praktyczny czas zamrażania równy jest:
gdzie,
- czas schładzania od temperatury początkowej do temperatury krioskopowej [s];
- czas właściwego zamrażania [s];
- czas domrażania produktu do założonej temperatury końcowej [s]
4. Wyznaczenie bilansu cieplnego procesu zamrażania
Należy policzyć ilość ciepła odebraną w trakcie procesu zamrażania od roztworu:
gdzie,
q
1
– ciepło schładzania produktu od temperatury początkowej do temperatury
krioskopowej [kJ/kg];
q
2
– ciepło przemiany fazowej wody w lód [kJ/kg];
q
3
– ciepło obniżania temperatury lodu do temperatury końcowej [kJ/kg].
gdzie,
c
o
– ciepło właściwe produktu niezamrożonego [kJ/(kg*K)];
gdzie,
s – koncentracja sacharozy w roztworze [kg/kg];
T – temperatura niezamrożonego roztworu [K].
gdzie,
W – zawartość wody w produkcie [kg/kg];
ω – udział wody wymrożonej w produkcie [kg/kg];
q
zw
– ciepło zamarzania wody ( 333 kJ/kg) [kJ/kg];
Udział wody wymrożonej w produkcie można obliczyć ze wzoru Raoulta:
gdzie,
c
L
– ciepło właściwe lodu (2,1 kJ/(kg*K)) [kJ/(kg*K)].

Sprawozdanie powinno zawierać:
Cel i opis doświadczenia
Schemat i opis stanowiska pomiarowego
Wykresy z wyznaczonymi krzywymi mrożenia
Wyznaczone temperatury krioskopowe
Obliczone i przedstawione wyniki dotyczące praktycznego i teoretycznego
czasu zamrażania
Bilans cieplny procesu zamrażania
Spostrzeżenia i wnioski
Bibliografia
1. Praca zbiorowa pod red. Lewicki P. P. 2005. Wydanie 4. Inżynieria procesowa
i aparatura przemysłu spożywczego. Wydawnictwo Naukowo – Techniczne.
Warszawa. s. 300 – 345;
2. Mazur P. 1963. Kinetics of water loss from cells AT subzero temperatur es and the
likelihood of intracellular freezing. The Journal of General Physiology. Nr 47. s. 347
– 369;
3. Gruda Z., Postolski J. 1999. Zamrażanie żywności. Wydanie 3. Wydawnictwo
Naukowo – Techniczne. Warszawa. s. 73 – 137, 81 – 86, 123 – 134 ;
4. Dłużewska A., Dłużewska M. 2008. Część II. Technologia Żywności. Podręcznik dla
technikum. Wydawnictwo Szkolne i Pedagogiczne. Warszawa. s. 241 – 251;
5. Cziżow G. B. 1974. Procesy cieplne w technologii chłodniczej produktów
żywnościowych. Wydawnictwo Naukowo – Techniczne. Warszawa. s. 16-29;
6. Grabowska B., Kasperski J. 2006. Wymiana ciepła w procesie zamrażania
kontaktowego produktów w izolacji warstwowej. Chłodnictwo. Nr 45 (12). s. 38 –
45;
7. Kamińska A., Lewicki P. P. 2008. Metody ograniczania krystalizacji lodu w procesie
zamrażania. Przemysł Spożywczy. Nr 9 (62). s. 24 – 28;
8. Filin S. 2005. Niezwykłe właściwości zwykłej wody. Technika Chłodnicza
i Klimatyzacyjna. Nr 8 (114). s. 276 – 285;
9. Khadatkar R. M., Kumar S., Pattanayak S. C. 2004. Cryofreezing and Cryofreezer.
Cryogenics. Nr 44 (9), s. 661 – 678;
10. Kluza F. 1997. Zakres zamrażania owoców, warzyw oraz soków owocowo –
warzywnych jako wynik oddziaływania warunków ich chłodzenia i właściwości
fizycznych oraz modyfikacji składu produktu. Chłodnictwo. Nr 32 (1). s. 35 – 37;
11. Miles Ch. A., Mayer Z., Morley M. J., Hauska M. 1997. Estimation of initial freezing
point of foods from composition data. International Journal of Food Science and
Technology. Nr 32. s. 389 – 400;

12. Raventós M., Hernández E., Auleda J., Ibarz A. 2007. Concentration of aqueous
sugar solutions in a multi – plate cryoconcentrator. Journal of Food Engineering. Nr
79. s. 577 – 585;
13. Kozłowicz K., Kluza F. 2009. Wpływ dodatków napojów alkoholowych na proces
zamrażania sorbetów owocowych. Żywność. Nauka. Technologia. Jakość. Nr 1 (62).
s. 65 – 72;
14. James C., Lejay I., Tortosa N., Aizpurua X., James S. J. 2005. The effect of salt
concentration on the freezing point of meat stimulants. International Journal of
Refrigeration. Nr 28. s. 933 – 939;
15. Auleda J.M., Raventós M., Sánchez J., Hernández E. 2011. Estimation of the freezing
point concentrated fruit juices for application in freeze concentration. Journal of Food
Engineering. Nr 105. s. 289 – 294;
Wyszukiwarka
Podobne podstrony:
badanie procesu zamrażania produktów spozywczych(1)
8 BADANIE PROCESU ZAMRAŻANIA PRODUKTÓW SPOŻYWYCZYCH
8 BADANIE PROCESU ZAMRAŻANIA PRODUKTÓW SPOŻYWYCZYCH
OCENA MIKROBIOLOGICZNA PRODUKTO Nieznany
OCENA MIKROBIOLOGICZNA PRODUKTO Nieznany
ANALIZA I OCENA PROCESU PRODUKCYJNEGO SOKU JABŁKOWEGO
Analiza i ocena procesu produkcyjnego więźby dachowej
procesy fotochemiczne i reakcje Nieznany
IMW W01 Wstepny System produkc Nieznany
Ocena zgodnosci wynikow sondazy Nieznany
02 Charakteryzowanie produkcji Nieznany (2)
ocena ryzyka 3 id 329416 Nieznany
03 Stosowanie norm w produkcji Nieznany (2)
Ocena zgodnosci wyklad 4 akredy Nieznany
janus, procesy i techniki wytwa Nieznany
Ocena procesu kompostowania z udziałem odpadów poch zwierz
Procesybiznesowe id 393952 Nieznany
wykłady procesy i techniki produkcyjne
więcej podobnych podstron