Chemia Fizyczna: Ćwiczenia laboratoryjne nr 4
„Wyznaczanie energii aktywacji reakcji zmydlania estru”
Celem zadania jest wyznaczenie Ea reakcji zmydlania octanu etylu na podstawie znajomości stałych szybkości reakcji k w temperaturach 22°C, 32°C.
Literaturowa energia zmydlania estru wynosi 59,3 kJ/mol.
Energię zmydlania estru wyznaczamy z równania:
k1 Ea 1 1
(♦) log —— = - ——— — - —
k2 2,303R T1 T2
k1 - średnia szybkość reakcji w T1 = 25°C
k2 - średnia szybkość reakcji w T2 = 35oC
R - stała gazowa
Stałe szybkości reakcji znajdujemy ze wzoru:
2,303 coes(coz - cx)
k = ————— log ——————
t( coz - coes) coz(coes - cx)
gdzie oznaczenia i wartości są podane w tabeli dla odpowiednich temperatur.
Tabela wyników
T=22oC |
Czas[min] |
mS |
Χ |
cx |
k |
log y |
coz=0,05M
coes=0,0487M |
|
0.5 |
9,47 |
9,3 |
0,006237 |
0,009941 |
0,011026 |
|
|
2,0 |
7,561 |
7,42 |
0,018913 |
0,042702 |
0,019988 |
|
|
4,0 |
6,541 |
6,42 |
0,025685 |
0,074599 |
0,034489 |
|
|
6,0 |
5,904 |
5,8 |
0,029915 |
0,105807 |
0,05039 |
|
|
8,0 |
5,483 |
5,38 |
0,03271 |
0,135152 |
0,066607 |
|
|
10,0 |
5,185 |
5,09 |
0,034689 |
0,162698 |
0,083846 |
|
|
12,0 |
4,961 |
4,87 |
0,036176 |
0,188863 |
0,102067 |
|
|
14,0 |
4,79 |
4,70 |
0,037311 |
0,213201 |
0,120572 |
|
|
16,0 |
4,655 |
4,57 |
0,038208 |
0,23593 |
0,140184 |
|
|
18,0 |
4,547 |
4,47 |
0,038925 |
0,256937 |
0,160699 |
|
|
20,0 |
4,455 |
4,37 |
0,039536 |
0,277264 |
0,181356 |
|
|
|
|
|
|
kśr=0,1548
|
|
K=9,82 m-1 |
|
|||||||
T=32oC |
0,5 |
8,052 |
7,91 |
0,024216 |
0,066216 |
0,001655 |
coz=0,05M
coes=0,0487M |
|
2 |
6,811 |
6,69 |
0,031378 |
0,120032 |
0,007111 |
|
|
4 |
5,829 |
5,72 |
0,037046 |
0,207115 |
0,012422 |
|
|
6 |
5,282 |
5,19 |
0,040204 |
0,302605 |
0,017619 |
|
|
8 |
4,954 |
4,86 |
0,042097 |
0,399989 |
0,022506 |
|
|
10 |
4,728 |
4,64 |
0,043401 |
0,503514 |
0,027093 |
|
|
12 |
4,564 |
4,48 |
0,044348 |
0,612934 |
0,03145 |
|
|
14 |
4,444 |
4,36 |
0,04504 |
0,724059 |
0,035503 |
|
|
16 |
4,349 |
4,27 |
0,045589 |
0,841837 |
0,039288 |
|
|
18 |
4,273 |
4,2 |
0,046027 |
0,96503 |
0,042786 |
|
|
20 |
4,213 |
4,14 |
0,046374 |
1,089083 |
0,046171 |
|
|
|
|
|
|
kśr=0,316
|
|
|
Obliczyłem χ ze wzoru χt=K x Ro-1
Χ0,5=0,0982 x 9,47 = 0,929954
Obliczyłem stężenia estru w każdym punkcie pomiaru czasu ze wzoru
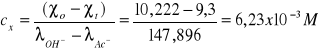
Następnie obliczam stałą reakcji ze wzoru:
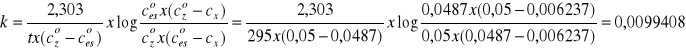
4) Następnie wyliczam średnią stałą szybkości i podstawiam do wzoru (♦) :
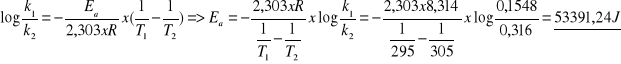
Błąd względny i bezwzględny:
Błąd względny: 5,909
Błąd bezwzględny: 0,09965
Dyskusja wyników:
Korzystając ze wzoru (♦) obliczyliśmy, że Ea wynosi 53,391kJ/mol podstawiając za k1 i k2 wartości średnie.
Wyznaczona wartość Ea jest mniejsza od literaturowej, co zapewne jest spowodowane:
-wyznaczona przez nas Ea jest wartością średnią dla danego przedziału temp.
-mogły wystąpić błędy podczas wykonywanych operacji matematycznych
Współczynnik temperaturowy czyli stosunek stałej szybkości w temp.32 st. Do stałej szybkości w temp. 22 st. Wynosi 2.
Stałe szybkości różnią się od siebie dość znacznie i mają tendencje wzrostu wraz z czasem.
Wyszukiwarka
Podobne podstrony:
Fizyczna ćw 6, fizyczna, chemia fizyczna, Fizyczna, CH. FIZYCZNA, laborki sprawozdania fizyczna
cw 2, fizyczna, chemia fizyczna, Fizyczna, CH. FIZYCZNA, laborki sprawozdania fizyczna
Korelacja liniowa, fizyczna, chemia fizyczna, Fizyczna, CH. FIZYCZNA, laborki sprawozdania fizyczna
Ćw. 17, chemia fizyczna, Nowy folder
Dane, fizyczna, chemia fizyczna, Fizyczna, CH. FIZYCZNA, laborki sprawozdania fizyczna
Ćw. 20, chemia fizyczna, Nowy folder
Ćw. 29, chemia fizyczna, Nowy folder
Ćw. 16, chemia fizyczna, Nowy folder
Ćw. 14, chemia fizyczna, Nowy folder
Ćw. 13, chemia fizyczna, Nowy folder
Ćw. 21, chemia fizyczna, Nowy folder
Ćw. 31, chemia fizyczna, Nowy folder
Ćw. 30, chemia fizyczna, Nowy folder
Wyznaczanie charakterystyki elektrod, fizyczna, chemia fizyczna, Fizyczna, CH. FIZYCZNA, laborki spr
Ćw. 25, chemia fizyczna, Nowy folder
Ćw. 11, chemia fizyczna, Nowy folder
Ćw. 12, chemia fizyczna, Nowy folder
Ćw. 27, chemia fizyczna, Nowy folder
więcej podobnych podstron