WYKŁAD 1
DROBNOUSTROJE
Cechą charakterystyczną drobnoustrojów są cechy chemiczne i fizyczne. Skład chemiczny jest podobny do składu chemicznego innych żywych organizmów.
Wahania w składzie chemicznym są związane z podłożami, na których odbywa się wzrost drobnoustrojów oraz od wieku hodowli.
WŁAŚCIWOŚCI CHEMICZNE
Podstawowym składnikiem chemicznym jest WODA (70 - 85 % wszystkich składników chemicznych). Pochodzi ze środowiska zewnętrznego i dostaje się do komórki na drodze osmozy, podczas procesu metabolizmu komórkowego - oddychania (biologiczne utlenianie). Może występować w postaci wolnej (uniwersalny rozpuszczalnik) oraz związanej.
Cząsteczka wody ma charakter dipolowy. Stwarza możliwość przeprowadzania do roztworu substancji o charakterze jonowym i polarnym. Dzięki temu mogą powstawać roztwory rzeczywiste i koloidalne. Substraty ulegające rozpuszczeniu w wodzie mają zdolność otaczania się dipolami wody, czyli płaszczem wodnym. Są to substraty HYDROFILNE, np. węglowodory (rzeczywiste), kwasy nukleinowe, białka (koloidalne). Substraty, które nie wykazują takich właściwości, to substraty HYDROFOBOWE. Są to substancje nierozpuszczalne w wodzie.
Stan uwodnienia komórki jest charakterystyczny dla danego gatunku. Jeżeli komórka traci wodę, to dochodzi do zmian w jej metabolizmie. Zasadnicze znaczenie ma tutaj oddziaływanie wody na reakcje enzymatyczne. Enzymy tylko wówczas pełnią swoją funkcję katalityczną, kiedy występują w stanie ROZPROSZENIA CZĄSTECZKOWEGO, co jest możliwe dzięki uwodnieniu komórki. Jeżeli enzymy są w stanie uwodnienia komórki, to mają wolne centrum aktywne enzymu. Przy właściwym uwodnieniu również substraty reakcji chemicznych są w odpowiednim rozproszeniu. Jeżeli enzym i substrat jest w stanie rozproszenia i centrum aktywne jest wolne, to może dojść do prawidłowego połączenia substratu z enzymem (zajście reakcji enzymatycznej).
Wszystkie enzymy są białkami. Na swojej powierzchni mają ładunki różnoimienne. Jeżeli komórka traci wodę, to dochodzi do oddziaływań elektrostatycznych pomiędzy cząstkami enzymu. Prowadzi to do zmiany konfiguracji przestrzennej białka.
Niedobór wody powoduje:
zatężenie substancji rozpuszczalnych, toksycznych. Substancje te (szczególnie metale ciężkie) reagują z grupami tiolowymi kwasów, przez co dochodzi do inaktywacji białek - najważniejsze to białka enzymatyczne.
wzrost substratów wchodzących w reakcje enzymatyczne. Substrat staje się bardziej dostępny dla enzymów.
zakłócenia w przepuszczalności membran komórkowych, przede wszystkim membran błony cytoplazmatycznej. Stan uwodnienia błony cytoplazmatycznej zależy od uwodnienia części hydrofilowej składników błony.
Woda występuje w stanie rozproszonym i związanym. Jest związana z makrocząsteczkami komórki (białka, lipidy, lipoproteidy).
W skład komórki mikroorganizmu wchodzą BIAŁKA. Należą do stałych składników komórki (41 - 56 (60)%). Mogą występować w postaci rozproszonej i są to: albuminy, globuminy, białka enzymatyczne oraz w postaci nierozproszonej.
Budują struktury komórkowe i biorą udział w reakcjach chemicznych jako enzymy. Bardzo często występują w postaci połączonej z innymi makrocząsteczkami i tworzą takie połączenia, jak: nukleoproteidy, glikoproteidy, lipoproteidy, chromoproteidy.
Z obecnością wiązań związane są własności:
antygenowość
toksyczność
wrażliwość na działanie czynników fizycznych, zwłaszcza temperatury
wrażliwość na działanie środków dezynfekujących
wrażliwość na działanie antybiotyków.
Skład peptydoglikanu:
pochodne i kwas diaminopikolinowy
pochodne i kwas dwuaminopimelinowy
aminokwasy w izomerii D.
KWASY NUKLEINOWE
U wirusów występuje tylko jeden kwas. U procariota kwasy nukleinowe nigdy nie są złączone z białkami, z histonami. U bakterii są złączone z jonami: wapnia i magnezu oraz z polaminami - kationy organiczne (spermina i spermidyna).
U bakterii podstawowymi zasadami są: adenina, guanina, cytozyna, puryna. Spotykane są również nietypowe zasady azotowe:
5 - hydroksymetylocytozyna
5 - hydroksymetylouracyl
5 - metylocytozyna
6 - metyloaminopuryna.
Ważnym czynnikiem pozwalającym określić skład kodów w DNA jest stosunek guaniny do cytozyny. U wszystkich organizmów żywych, wyższych niż procariota, stosunek ten wynosi około 50%. U bakterii są duże zróżnicowania - średnio 25 - 35%. Jest to charakterystyczna cecha.
U procariota występują wolne nukleotydy. Nie wchodzą one w skład kwasów nukleinowych, ale biorą udział w przemianie materii.
WITAMINY
Występują witaminy z grupy B: B1, B2, B6, B12; PP (kwas nikotynowy), M lub Bc (kwas foliowy), kwas pantotenowy, witamina H (biotyna).
Są częściami składowymi enzymów. Witaminy z grupy B są koenzymami enzymów.
POLISACHARYDY (9 - 11%).
Ta ilość uzależniona jest od składu ilościowego i jakościowego podłoża, na którym odbywa się wzrost drobnoustrojów.
Wielocukry charakterystyczne dla bakterii to polimery utworzone z kwasu muraminowego oraz polimery z kwasu tejchojowego.
Występują dwudezoksycukry:
Paratoza Tywetoza Askaryloza
Kolitoza Abekwoza
Charakterystyczne dla procariota, dla bakterii z polisacharydami związane są własności antygenowe i toksyczne. O własnościach tych decydują: układ przestrzenny cząsteczek oraz końcowy grupy chemicznej.
Przykładem bakterii wykazującej własności antygenowe i toksyczne jest dwoinka zapalenia płuc (Diplococcus pneumoniae). Ma zdolność wytwarzania otoczek, które pod względem chemicznym są polisacharydami. Znaleziono w nich 30 antygenów - u człowieka powodują odpowiedź immunologiczną.
ENDOTOKSYNY - związki polisacharydowo - białkowo - lipidowe.
TŁUSZCZE
Są to przede wszystkim tłuszcze właściwe. W komórce procariota ulegają połączeniu ze składnikami mineralnymi i organicznymi i tworzą substancje lipidowe:
woski
fosfolipidy
glikolipidy.
U wirusów - 0 - 60%
U bakterii - do 40%.
Przykładem bakterii zawierającej dużą ilość lipidów są prątki gruźlicy (Mycobacterium tuberculosis) - 40% tłuszczu.
Niektóre lipidy charakterystyczne dla bakterii:
kwas ftionowy i kwas mikolowy.
U bakterii nigdy nie występują sterole oraz nienasycone kwasy tłuszczowe. U drobnoustrojów lipidy wchodzą w skład związków tworzących endotoksyny. Połączenie organizmu - z białkami i polisacharydami.
SKŁADNIKI MINERALNE (1,3 - 14%)
Wpływają na ciśnienie osmotyczne komórki. Mają własności buforujące. Wchodzą w skład elementów struktury komórki. Mają znaczenie w reakcjach biochemicznych, bo budują tzw. grupę prostetyczną (część niebiałkowa) enzymu.
Istnieją enzymy metalozależne - ich aktywność jest związana z obecnością niektórych jonów metali.
Najważniejszymi pierwiastkami mineralnymi budującymi komórkę są jony: potasu, sodu, fosforu, wapnia, magnezu, siarki.
WŁAŚCIWOŚCI FIZYCZNE
Niektóre z nich nie dotyczą żadnych organizmów wyższych.
RUCH
Podstawowym narządem ruchu jest rzęska. Inny sposób to ruch bierny - ruch powietrza, przepływ wód, ścieków, ruch Browna (bombardowanie komórek bakteryjnych przez makrocząsteczkę rozproszoną w powietrzu). Ruch ślizgowy - nie opisany.
ZDOLNOŚĆ DO TWORZENIA ZAWIESIN
Zawiesina bakteryjna zachowuje się podobnie jak roztwór koloidalny. Bakterie mogą tworzyć ją dzięki mikronalnym rozmiarom i ładunkom elektrostatycznym na swojej powierzchni.
Nabój elektrostatyczny ulega zmianom zależnie od pH:
obojętne, zasadowe - ładunek ujemny
kwaśne - ładunek dodatni.
REAGOWANIE NA ZMIANY CIŚNIENIA OSMOTYCZNEGO W ŚRODOWISKU
Roztwory:
izotoniczne - ciśnienie osmotyczne w komórce i na zewnątrz jest takie samo
hipertoniczne - ciśnienie osmotyczne jest niż panujące w komórce. Roztwory dążą do wyrównania stężeń, dochodzi do wypływania wody. Konsekwencją jest kurczenie protoplastu i powstaje zjawisko noszące nazwę PLAZMOLIZA.
hypotoniczne - ciśnienie osmotyczne w komórce jest wyższe. Roztwory dążą do wyrównania stężeń. Woda wnika do komórki. Komórka pęcznieje i dochodzi do PLAZMOPTYZY. Konsekwencją jest rozerwanie powłok i pęknięcie komórki.
PRECYPITACJA
Bakterie mogą ulegać wytrącaniu w postaci strontu, np. w postaci elektrolitu zachowują się jak roztwory koloidalne.
Innym czynnikiem jest niska temperatura (-2°) - białka ulegają precypitacji.
AGLUTYNACJA
Bakterie w obecności elektrolitu ulegają zlepianiu.
Ma ona wykorzystanie w diagnostyce.
ODŻYWIANIE
Sposób pobierania substancji ze środowiska:
osmoza - roztwory izotoniczne, hipertoniczne, hypotoniczne.
Dzięki składnikom chemicznym drobnoustrojów i ich własnościom fizycznym można dokonać składu podłóż i wykorzystać ich własności w celach diagnostycznych.
WYKŁAD 2
METABOLIZM KOMÓRKOWY
Każdy ustrój ulega ciągłym zmianom, bo przepływa przez niego materia i energia.
METABOLIZM KOMÓRKOWY - stan ciągłego ruchu. Zachodzi tu też przepływ informacji genetycznej, bo wszystkie reakcje biochemiczne zachodzące w komórce są kontrolowane enzymami, z kolei wszystkie enzymy są białkami, a synteza białek odbywa się pod bezpośrednią kontrolą genów.
Na reakcje metabolizmu składają się dwie grupy procesów:
reakcje anaboliczne (anabolizm) - wszystkie reakcje syntez. Są to reakcje wymagające dostarczenia energii przez komórkę, czyli są reakcjami endoergicznymi.
reakcje kataboliczne (katabolizm) - wszystkie reakcje rozkładu - oddychania. Są to reakcje dostarczające komórkom energii - reakcje egzoergiczne.
Energia, która wydziela się podczas procesów katalizy zostaje zamieniona na energię chemiczną i zmagazynowana jest w związkach wysokoenergetycznych. Podstawowym związkiem jest ATP - adenozynotrójfosforan. Inne to:
GDP - guanidynodwufosforan
UTP - uracylotrójfosforan
GTP - guanidynotrójfosforan.
Procesy zachodzące w komórce polegają na oddawaniu elektronów i na przyłączaniu elektronów przez substraty. Substrat przyłączany ulega redukcji, a oddawany - utlenianiu.
Przenośniki elektronów:
NAD - dwunukleotyd nikotyn adenoadenilowy
NADP - fosforan dwunukleotydu nikotyn adenoadenilowy.
Wszystkie enzymy są białkami i są syntetyzowane pod kontrolą genów. Liczne enzymy zawierają w swoich cząsteczkach jony metali: Fe, Cu, Zn. Obecność tych jonów jest konieczna dla prawidłowego funkcjonowania enzymów. Część niebiałkowa enzymu nosi nazwę grupy prostetycznej. Działanie enzymu ma charakter wybitnie wybiórczy - jeden enzym katalizuje jedną reakcję biochemiczną lub katalizuje zespół reakcji bardzo podobnych.
Niektóre enzymy mogą występować w kilku odmianach, z których każda ma takie same własności katalityczne, ale różni się taki enzym od innych np. rozpuszczalnością, własnościami fizykochemicznymi i własnościami immunochemicznymi. Takie enzymy noszą nazwę IZOENZYMÓW.
Wszystkie poznane enzymy zostały sklasyfikowane przez Komisję Enzymatyczną. Zostały podzielone na kilka grup w zależności od tego jakie czynności w komórce pełnią:
Oksydoreduktazy - enzymy katalizujące reakcje odłączania atomów H+ od cząsteczki substratu.
Enzymy katalizujące przyłączanie tlenu do cząsteczki substratu.
Enzymy przenoszące elektrony na atom lub cząsteczkę tlenu.
Transferazy - enzymy katalizujące odłączanie grup funkcyjnych i przenoszenie ich z jednej cząsteczki na inną.
Hydrolazy - enzymy katalizujące reakcję hydrolizy.
Liazy - katalizują niehydrolityczne rozrywanie wiązań pojedynczych i podwójnych.
Izomerazy - katalizują wszelkie przemiany w obrębie tej samej cząsteczki (są to więc przemiany wewnątrzcząsteczkowe, np. izomeryzacja, recymizacja, przenoszenie grup).
Ligazy - katalizują powstawanie wiązań chemicznych w reakcjach biosyntez. Są to wiązania C - O,
C - S, C - C.
W każdej cząsteczce białka enzymatycznego występuje obszar mający decydujące znaczenie dla działalności katalitycznej. Własności fizykochemiczne tego obszaru, jego struktura oraz lokalizacja w obrębie cząsteczki białka enzymatycznego warunkują swoistość enzymu względem określonego substratu. Są one również źródłem zmian wiązań kowalencyjnych w obrębie cząsteczki substratu. Miejsce to nosi nazwę CENTRUM AKTYWNE ENZYMU.
Podczas reakcji enzym łączy się z substratem w centrum aktywnym enzymu. Szybkość reakcji enzymatycznych zależy od poziomu enzymów w komórce oraz od ich aktywności. Poziom enzymów w komórce zależny jest od ich degradacji w stanie równowagi dynamicznej. W komórce taka sama ilość enzymów jest syntetyzowana co i ulega rozkładowi (degradowaniu). Z kolei aktywność enzymów jest regulowana w komórce tzw. SPRZĘŻENIEM ZWROTNYM. Polega ono na tym, że enzym katalizujący pierwszą reakcję cyklu biochemicznego jest inhibowany (hamowany) przez produkt tego cyklu.
Aktywność enzymu w komórce oprócz sprzężenia zwrotnego zależy także od dostępności substratu i koenzymu, warunków środowiska (temperatura, pH) oraz od działania modulatorów allosterycznych. Przyjmuje się, że reakcja zachodzi pod wpływem enzymu 106 razy szybciej niż by zachodziła bez enzymu.
KOENZYM - wchodzi w skład enzymów, jest substancją niskocząsteczkową i niebiałkową, która może się odszczepiać od białka enzymatycznego. Jest przyłączany w sposób odwracalny. Są nim: witaminy z grupy B i związki o strukturze nukleotydowej.
MODULATORY ALLOSTERYCZNE - cząsteczki związków chemicznych przyłączające się do enzymu w miejscach innych niż centrum aktywne enzymu powodując zmianę konfiguracji i konformacji enzymu.
INHIBITORY - aktywne enzymy, które mogą być w komórce hamowane przez określone cząsteczki lub jony.
INHIBICJA (hamowanie) - może polegać na tym, że inhibitor może łączyć się z enzymem w sposób trwały lub odwracalny. Ponadto inhibitor może łączyć się również z innymi elementami reakcji enzymatycznych. Może też blokować ich współdziałanie. W związku z tym możemy mówić o inhibicji nieodwracalnej (trwałej) i odwracalnej.
Inhibicja nieodwracalna - jeżeli inhibitor połączy się z którymś z elementów układu enzymów w sposób trwały.
Inhibicja odwracalna (kompetycyjna) - polega na przyłączeniu inhibitora w centrum aktywnym enzymu. Jest to możliwe dlatego, że inhibitor podobny jest pod względem budowy chemicznej do substratu. Inhibitor, który przyłączył się w centrum aktywnym enzymu uniemożliwia przyłączanie się substratu. Powoduje to spadek szybkości katalizy. Jest to spowodowane tym, że spada ilość enzymów, które mają wolne centrum aktywne.
WYKŁAD 3
Inhibicja niekompetycyjna - rodzaj inhibicji odwracalnej. Proces polega na jednoczesnym powiązaniem się z cząsteczką enzymu zarówno substratu jak i inhibitora. Takie zjawisko powoduje spowolnienie reakcji katalizy. Następuje wolniejsze przejście substratu w produkt reakcji.
Rodzaje inhibitorów
Niektóre enzymy są produkowane w komórce w postaci połączonej z odpowiednim inhibitorem. Są to PROENZYMY lub ENZYMOGENY. Zamiana proenzymu w enzym polega na odszczepieniu inhibitora przez odpowiedni aktywator.
AKTYWATORY - czynniki powodujące przekształcenie nieaktywnej formy enzymu (proenzym = enzymogen). Zamiana proenzymu w enzym aktywny polega na odszczepieniu naturalnego inhibitora przez odpowiedni aktywator.
Rodzaje aktywatorów:
INNY ENZYM
Trypsyna + Wal - Asp - Asp - Asp - Asp - Liz
CZYNNIKI REGULUJĄCE POTENCJAŁ OKSYDACYJNOREDUKCYJNY
(substancje o niskim potencjale oksydacyjnoredukcyjnym, np. cysteina, glutation)
Enzymy, które w swojej cząsteczce zawierają grupę tiolową - SH wykazują własności katalityczne, jeżeli grupa tiolowa jest nieutleniona. Jeżeli w komórce znajdują się substancje utleniające to grupa tiolowa zostaje utleniona do grupy dwusiarczkowej
SH → - S - S -
i enzym traci własności katalityczne. Żeby temu zapobiec w komórce są syntetyzowane czynniki o niskim potencjale oksydacyjnoredukcyjnym. Do nich należy cysteina i glutation.
KOFAKTORY
KOFAKTORY - związki niskocząsteczkowe współdziałające z białkiem enzymu, np.:
witaminy i ich pochodne (szczególnie z grupy B)
aniony:
Cl- - aktywuje amylazę (rozkłada skrobię)
SO
- aktywuje enzymy proteolityczne (rozkładają białko)
kationy:
Mg2+ - aktywizuje fosfohydrolazy i fosforylazy
Mn2+ - aktywizuje arginazę
Co2+ - aktywizuje karboksylany
Fe2+ i Cu2+ - aktywizują cytochromy i oksydazę cytochromową (może zajść dzięki nim proces oddychania tlenowego wewnątrzkomórkowego).
RÓWNANIE MICHAELISA - MANTEN
Kinetyczne własności niektórych enzymów dają się opisać modelem Michaelisa - Manten. Zgodnie z tym modelem enzym (E) łączy się z substratem (S) i tworzy kompleks Enzym - Substrat (ES), który rozpada się na Enzym (E) i Produkt (P). kompleks Enzym - Substrat może dysocjować z powrotem do E + S.
k1 - przedstawia stałą szybkość powstawania ES
ES może ze stałą szybkością k2 dysocjować na E+S albo przekształcać się w E + P ze stałą szybkością k3
Szybkość reakcji katalizowanych V zmienia się wraz ze stężeniem substratu i osiąga maksymalną wartość Vmax w chwili, gdy wszystkie cząsteczki enzymu są wysycone substratem. Dalsze zwiększenie substratu poza tą wartość nie powoduje przyspieszenia reakcji.
Vmax
Km S
Km - stała Michaelisa - oznacza takie stężenie substratu, przy którym połowa miejsc aktywnych jest wysycona substratem.
Reakcje, które zachodzą w organizmie są katalizowane przez enzym.
Wszystkie organizmy żywe można podzielić na kilka grup ze względu na sposoby zdobywania energii:
aeroby - organizmy tlenowe
fakultatywne aeroby - względne tlenowce
fakultatywne anaeroby - względne beztlenowce
obligatoryjne anaeroby - bezwzględne beztlenowce.
Można je spotkać wyłącznie u bakterii czyli mikroorganizmów.
PROCES ODDYCHANIA WEWNĄTRZKOMÓRKOWEGO
Proces oddychania jest procesem wewnątrzkomórkowym. Opiera się tylko na reakcjach biochemicznych. Taki proces zachodzi u wszystkich organizmów wyższych, które są tlenowcami.
Po raz pierwszy mechanizm tego procesu opisał Krebs. W 1953 r. otrzymał za to nagrodę Nobla. Podzielił on oddychanie wewnątrzkomórkowe na trzy etapy.
Etapy oddychania tlenowego
Białka
aminokwasy |
Lipidy
Glicerol + kwasy tłuszczowe |
cukry proste (Glukoza) |
Acetylo - CoA
CO2 ATP
ATP H2O
Substratami do procesów metabolizmu komórkowego są polisacharydy, lipidy. W sytuacjach ekstremalnych komórka może wykorzystać białka. Związki wielkocząsteczkowe ulegają przemianom (degradacji) do substancji prostych: polisacharydy do cukrów prostych (każda komórka dąży do wytworzenia cukru 6 - węglowego - glukozy, ponieważ jest ona substratem najłatwiej przyswajalnym i najłatwiej włączanym w reakcje metabolizmu komórkowego), lipidy do glicerolu (alkohol trójwodorotlenowy) oraz kwasów tłuszczowych, białka do określonych aminokwasów.
Jest to I etap oddychania tlenowego. Nie dostarcza on komórce energii.
Najczęstszym etapem, który prowadzi do wytworzenia glukozy i dalej do jej przemian jest proces zwany GLIKOLIZĄ, który również wchodzi w I etap oddychania.
Te substancje proste zostają w organizmie w reakcji metabolizmu przekształcane. Kwasy tłuszczowe są przekształcane na drodze β - oksydacji, aminokwasy ulegają procesom transaminacji, D - aminacji i D - kaboksylacji. Glukoza - ulega glikolizie. Organizm tak prowadzi procesy przemian, aby powstał związek, który skupia wszystkie szlaki metabolizmu komórkowego (Acetylo - koenzym A).
Jest to II etap oddychania.
Acetylo - CoA jest włączany w cykl reakcji, które noszą nazwę cyklu Krebsa lub cyklu kwasów trójkarboksylowych lub cyklu kwasu cytrynowego. Jest to 8 reakcji, których celem jest wytworzenie energii, która jest zgromadzona w ATP, a produktem ubocznym jest CO2. Elektrony są przekazywane do łańcucha oddechowego, w którym dochodzi do wytworzenia energii (ATP) oraz drugiego produktu ubocznego - wody.
Jest to III etap oddychania.
Oddychanie to jest oddychaniem, które dostarcza komórce najwięcej energii ponieważ substraty użyte do reakcji oddychania ulegają całkowitemu spaleniu (do CO2, wody), a najważniejszym produktem procesu jest energia. Inne sposoby oddychania dostarczają komórce zdecydowanie mniej energii, bo proces spalania jest niecałkowity. Energia zostaje związana w produktach organicznych i np. w procesie fermentacji może być związana w etanolu, kwasie masłowym, kwasie mlekowym.
Proces oddychania tlenowego dostarcza komórce z jednej cząsteczki glukozy 38 cząsteczek ATP. Jest to proces najbardziej wydajny energetycznie. Proces np. fermentacji alkoholowej dostarcza 2 cząsteczki ATP.
Etapem najczęściej zachodzącym w każdej komórce jest proces GLIKOLIZY. Polega na przekształceniu glukozy do kwasu pirogronowego.
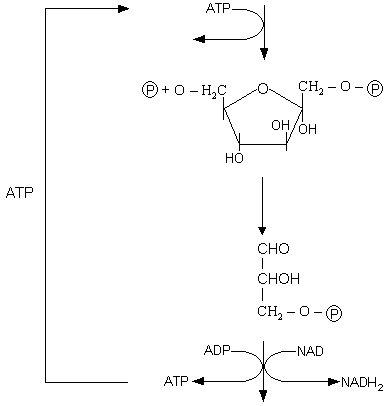
Najważniejsze etapy glikolizy:
WYKŁAD 4
Glikoliza jest głównym procesem oddychania, wspólnym dla oddychania tlenowego i beztlenowego.
W procesie tym glukoza ulega utlenieniu na drodze odwodorowania, czyli dochodzi do dehydrogenacji.
I etap procesu polega na wytworzeniu przy udziale ATP związku fruktozo 1,6 - dwufosforan. ATP redukuje się do ADP. Następnie dochodzi do powstania związku o 3 atomów węgla i ten etap jest kilkuczłonowy. Aby doszło do wytworzenia związku o 3 atomach węgla musi dojść do rozszczepienia pierścienia (łańcucha) 6 - węglowego. W wyniku tego procesu powstają dwie cząsteczki związku trójwęglowego. W wyniku procesu zostaje wytworzony aldehyd, z którego odłączony zostaje wodór, który przeniesiony jest następnie na NAD. Dochodzi do wytworzenia ATP i powstania końcowego produktu glikolizy jakim jest kwas pirogronowy. Proces ten nosi nazwę fosforylacja substratowa (wytworzenie ATP).
II etap procesu - Acetylo koenzym A (Acetylo CoA)
Żeby mógł powstać musi być substrat. Jest nim kwas pirogronowy, który powstał np. w glikolizie.
Acetylo - CoA powstaje w przypadku katabolizmu białek i węglowodanów przez oksydacyjną dekarboksylację pirogronianu
W przypadku katabolizmu kwasów tłuszczowych Acetylo - CoA tworzy się przez tiolizę.
III etap procesu - cykl Krebsa
Acetylo - CoA wchodzi w reakcje zwane cyklem Krebsa. Żeby zaszła reakcja muszą być dwa substraty do reakcji. Drugim substratem jest kwas szczawiooctowy
Możliwości uzupełniania szczawiooctanu w komórce:
karboksylacja pirogronianu
karboksylacja fosfoenolopirogronianu (powstaje w procesie glikolizy)
cykl Krebsa
Kwas szczawiooctanowy ma cechy kwasu α - lub β - ketokwasu. Są one nie trwałymi związkami, ulegają spontanicznej dekarboksylacji. W wyniku tego procesu powstaje pirogronian.
Kwasy 4 - węglowe są wykorzystywane w metabolizmie komórkowym (np. w procesie przemian aminokwasów, kwasów tłuszczowych i porfiryn).
CYKL KREBSA
kondensacja Acetylo - CoA ze szczawiooctanem
izomeryzacja cytrynianu
CH4 - metan
H3C
- karboanion metylowy
CH3 - jon dodatni, tzw. jon karboniowy, czyli jon z usuniętymi
utlenianie izocytrynianu
grupa HO - CH utleniona do C = O
dekarboksylacja szczawiobursztynianu
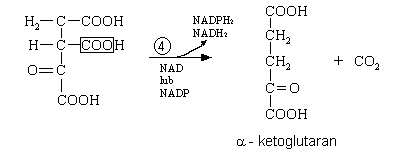
Pierwsze miejsce, w którym powstaje produkt uboczny - CO2 |
WYKŁAD 5
oksydacyjna dekarboksylacja α - ketoglutaranu
I etap - α - ketoglutaran pod wpływem kompleksu enzymów (dehydrogenaz), które współdziałają z witaminą B1 w postaci biologicznie czynnej, amidem kwasu liponowego i CoA. Powstaje bursztynylo - CoA.
II etap - jako produkt uboczny uwalnia się CO2. Oddziela się CoA z wolną grupą tiolową. Dochodzi do fosforylacji substratowej - wydziela się energia na skutek rozkładu substratu. Uwalnia się fosforan, przyłącza do GDP i powstaje GTP.
GDP - guanozynodwufosforan (guanozynodifosforan)
GTP - guanozynotrójfosforan
GTP oddaje swoją grupę fosforanową, która przyłącza się do ATP. GTP redukuję się do GDP i powstaje ATP.
utlenianie bursztynianu
Bursztynian ulega utlenieniu, działa enzym, który odbiera od bursztynianu protony wodoru, redukuje się do FADH2. W wyniku tego powstaje fumaran.
FAD - dwunukleotyd flawinoadeninowy
Jeśli dochodzi do zaburzeń w cyklu Krebsa, to może powstać kwas maleinianowy kwas w izomerii cis. Cykl Krebsa zostaje przerwany. Są bowiem inhibitory procesów oddechowych. Jeżeli powstanie fumaran - kwas w izomerii trans - proces przebiega dalej.
uwodnienie fumaranu
Pod wpływem cząsteczki H2O fumaran ulega hydratacji, w wyniku czego pęka podwójne wiązanie i powstaje kwas jabłkowy (jabłczan).
utlenianie jabłczanu
Proces zachodzi na drodze odwodorowania. Atomy H zostają przyjęte przez nukleotyd NAD (może być także NADP - reakcja przebiega wtedy wolniej). W wyniku reakcji odwodorowania powstaje ketokwas - szczawiooctan.
Cykl Krebsa jest trzecim czynnikiem, który uzupełnia szczawiooctan.
Komórka prowadzi ten proces, żeby uzyskać energię.
Bilans cyklu Krebsa
jedna fosforylacja substratowa
1 * 1 ATP
trzy odwodorowania z udziałem NAD lub NADP
3 * 3 ATP
jedno odwodorowanie z udziałem FAD
1 * 2 ATP
RAZEM 12 moli ATP = 96 kcal
oraz usunięcie 2 cząsteczek CO2
ŁAŃCUCH ODDECHOWY (Fosforylacja)
Atomy H, które zostały odłączone od substratu w cyklu Krebsa, a wcześniej w glikolizie, zostają przeniesione na tlen atmosferyczny. Dzieje się to za pomocą specjalnego mechanizmu przenoszenia zwanego łańcuchem oddechowym. Komórka zabezpiecza się i wytworzony zostaje łańcuch oddechowy. Składa się on z szeregu związków będących układem oksydacyjno - redukcyjnym.
Ogniwa łańcucha oddechowego
nukleotydy nikotynamidoadeninowe
nukleotydy flawinowe
FMN i FAD +
(z NADH2 i NADPH2 oraz z - CH2 - CH2 - ) FMNH2 i FADH2
np. bursztynian
FMN - mononkleotyd flawinowy
W skład nukleotydu FMN wchodzi ryboflawina (witamina B2) i fosforan nieorganiczny, natomiast w skład FAD - witamina B2, fosforan nieorganiczny i AMP.
AMP - adenozynomono fosforan
Koenzymy te przyjmują atomy wodoru od NADH2 lub NADPH2. Mogą również bezpośrednio przyjmować protony wodoru od konfiguracji typu bursztynianowej - CH2 - CH2 - . Następnie przekazują ją dalszym ogniwom łańcucha oddechowego.
Chinony
Jednym z chinonów jest ubichinon, który zawiera w swoim składzie reszty izoprenowe. Oprócz niego (koenzym Q) w skład chinonów wchodzi witamina K1. Są to związki zawierające pierścień aromatyczny oraz łańcuch boczny składający się z reszt izoprenowych. Chinony przejmują atomy wodoru od flawin. Redukują się, w związku z czym dochodzi do połączenia wodoru i tlenu.
Z chinonów elektrony są przeniesione na cytochromy.
Cytochromy
Istnieje wiele rodzajów cytochromów. U bakterii pierwszym jest cytochrom „b”. On przekazuje elektrony na cytochrom c1 i cyt c, a następnie na a i a3 (oksydaza cytochromowa). Z niej elektrony są bezpośrednio przekazywane na tlen atmosferyczny.
Pod względem chemicznym cytochromy są układami porfirynowymi - centralne miejsce zajmuje atom Fe. Fe przyjmując elektrony redukuje się z +3 na +2.
Cytochromy mają zdolność przenoszenia tylko elektronów. W wyniku kolejnego przenoszenia
przez kolejne ogniwa łańcucha oddechowego następuje utlenianie jednych substratów, gdy oddaje elektrony oraz redukcja innych substratów, gdy przyjmuje elektrony. Kolejne ogniwa łańcucha oddechowego są uszeregowane według wzrastającego powinowactwa elektronów, czyli wzrastającego potencjału oksydacyjno - redukcyjnego. Dzięki temu wzdłuż tego łańcucha płynie strumień elektronów lub atomu wodoru.
Atomy wodoru składają się z dodatnio naładowanego jądra (protony) i krążącego jednego elektronu. Rola części składowych atomu wodoru nie jest jednakowa. Energia zawarta w jądrze atomu jest dla komórki niedostępna. Zasadnicze znaczenie ma energia elektronu i jego transport wzdłuż łańcucha oddechowego. Cytochromy przenoszą same elektrony, reszta zaś atomu wodoru (proton) przechodzi do środowiska jako jony H+. Oksydaza cytochromowa (kompleks cyt a + a3) przenosi
na tlen atomowy, który bardzo łatwo je przyłącza. Powstaje wówczas bardzo nietrwały jon tlenkowy O2-, który natychmiast łączy się z protonem H+. W wyniku tego w środowisku tworzy się woda. Jest to drugi produkt uboczny oddychania:
O2- + 2 H+ H2O
Transport atomów wodoru jest procesem wtórnym po przeniesieniu elektronów i nie jest związany z przeniesieniem energii.
Energia związana jest z transportem elektronów. W łańcuchu oddechowym zachodzi fosforylacja oksydatywna. W łańcuchu oddechowym powstają 24 cząsteczki ATP (24 mole ATP).
Bilans oddychania tlenowego:
z 1 cząsteczki glukozy
38 cząsteczek ATP
Jest to proces najbardziej wydajny energetycznie ze wszystkich procesów oddechowych.
WYKŁAD 6
Innym sposobem zdobywania energii są procesy fermentacyjne.
FERMENTACJA - proces biochemiczny służący odtworzeniu ATP. Produkty rozkładu substratów organicznych pełnią rolę donorów i akceptorów wodoru i elektronów. Reakcje fosforylacji ADP mają charakter utlenienia. Poszczególne etapy utleniania przebiegają na drodze odwodorowania. W procesach tych wodór zostaje przekazany do kofaktora jakim jest NAD. Związki węgla, które ulegają utlenianiu podczas fermentacji opuszczają komórki w postaci CO2. Produkty pośrednie, które powstają w procesie degradacji substratowej służą jako akceptory wodoru, który pochodzi ze zredukowanego NADH2. Zredukowane produkty utworzone są w wyniku regeneracji NAD i są wydzielane.
Podczas procesu fermentacji stale odbywa się przenoszenie elektronów i protonów wodoru. Gdy substraty ulegają redukcji, NADH2 regeneruje się (NAD) i odwrotnie.
Podczas fermentacji węglowodorów powstaje bardzo wiele produktów: etanol, mleczan, maślan, bursztynian, octan, kapronian, n - butanol, 2,3 - butanodiol, aceton, izopropanol, CO2, wodór cząsteczkowy. Poszczególne reakcje fermentacji mają nazwy pochodzące od dominującego produktu końcowego, np.
fermentacja alkoholowa - etanol
fermentacja masłowa - kwas masłowy.
Fermentację można podzielić na:
homofermentację - powstaje tylko jeden produkt reakcji
heterofermentację - powstaje więcej niż jeden produkt.
Odtworzenie ATP na drodze fermentacji:
Jedynie kilka reakcji uczestniczy w przekazywaniu energii na drodze fosforylacji substratowej.
Bakterie mają trzy możliwości odtwarzania ATP:
|
|
|
|
|
|
Bakterie beztlenowe mają zdolność utleniania pirogronianu. Utleniają pirogronian w trzech następujących reakcjach:
Pirogronian + CoA + NAD
Acetylo - CoA + NADH2 + CO2
Enzym: wieloenzymatyczny kompleks dehydrogenazy pirogronianowej
W reakcjach fermentacji zachodzą:
Pirogronian + CoA + 2 Fd
Acetylo - CoA + 2 Fd H + CO2
Enzym: oksydoreduktaza pirogronian: ferredoksyna
FERREDOKSYNA - białko, które w swoim składzie zawiera Fe
Pirogronian + CoA
Acetylo - CoA + mrówczan
Enzym: liaza pirogronian: mrówczan.
Reakcja nr 2 jest reakcją charakterystyczną dla bakterii z rodzaju Clostridium, a reakcja nr 3 - dla bakterii z rodziny Enterobackteriacea.
Wodór i elektrony są jeszcze związane. Pozwalają je uwolnić dwie reakcje (dostarczają bezpośrednio czynników redukujących):
1.
2 Fd H
2 Fd + H2
Enzym: hydrogenaza lub oksydoreduktaza ferredoksyna i H2
2.
mrówczan
H2 + CO2
Enzym: liaza wodorowa.
W ten sposób w fermentacji 1 mola glukozy bakterie mogą uzyskać do 4 moli ATP. Reakcje te wyjaśniają proces fermentacji.
FERMENTACJA ALKOHOLOWA
Proces fermentacji alkoholowej jest procesem szeroko rozpowszechnionym u drobnoustrojów. W warunkach beztlenowych głównie produkowany jest etanol, a głównym producentem są grzyby, szczególnie należące do gatunku Saccharomyces Cerevisiae (drożdże).
Oprócz drożdży proces fermentacji alkoholowej mogą prowadzić grzyby z rodzaju Mucor sp., bakterie, np. Sarcina ventriculi, Zymomonas molibis (Pseudomonas linduceri), rodzina Enterobacteriaceae.
Głównymi organizmami są drożdże. W I etapie fermentacji z glukozy wytwarzają pirogronian. Następnie pirogronian zostaje przekształcony do aldehydu octowego. Reakcja ta zachodzi z wydzieleniem produktu ubocznego fermentacji alkoholowej i jest nim CO2. Następnie aldehyd octowy jest redukowany do etanolu. Donorami wodoru we wszystkich tych reakcjach są zredukowane nukleotydy, zwłaszcza NADH2.
Fermentacja alkoholowa:
C6H12O6
2 C2H5OH + 2 CO2
|
|
Sumaryczna reakcja fermentacji alkoholowej - RÓWNANIA NEUBERGA
pierwszy wzór fermentacji alkoholowej - I równanie Neuberga
C6H12O6
2 C2H5OH + 2 CO2
Neuberg wykazał, że drożdże mogą fermentować nie tylko glukozę, ale także pirogronian. Poza tym wykazał powstawanie produktu pośredniego: aldehydu octowego, dzięki zadozowaniu do zaczynu drożdżowego wodorosiarczynu sodu (nie jest toksyczny dla drobnoustrojów prowadzących proces fermentacji). Po dodaniu wodorosiarczynu sodu aldehyd octowy ulega precypitacji. W wyniku tego powstaje siarczyn sodowy aldehydu octowego. Proces fermentacji w obecności kwaśnego aldehydy sodu został wykorzystany w przemyśle do produkcji glicerolu. Zablokowany wodorosiarczynem sodu aldehyd octowy nie może funkcjonować jako akceptor wodoru. Miejsce aldehydu zajmuje fosforan dihydroksyacetonu, który ulega redukcji do glicerolo - 3 - fosforanu. Następnie związek ten ulega defosforylacji i powstaje glicerol.
CH3CHO + NaHSO3
CH3 - CHOH - SO3Na
drugi wzór fermentacji alkoholowej - II równanie Neuberga
I i II reakcja są wykorzystywane na skalę przemysłową:
I - do otrzymywania alkoholu
II - do otrzymywania glicerolu (gliceryna).
Jeżeli do zaczynu drożdżowego dodamy związek o charakterze zasadowym, to wówczas powstanie CO2, glicerol, kwas octowy, etanol.
trzeci wzór fermentacji alkoholowej - III równanie Neuberga
Aldehyd octowy ulega dysmutacji - równocześnie się utlenia i redukuje:
C2H5OH (redukcja)
CH3CHO
CH3COOH (utlenianie)
Z równań tych wynika, że proces fermentacji alkoholowej jest procesem heterofermentacji.
WYKŁAD 7
Proces fermentacji glukozy przez drożdże jest procesem, który jest stosowany w historii ludzkości od setek, a nawet tysięcy alt.
Fermentacja jest procesem beztlenowym. Drożdże, które prowadzą proces fermentacji alkoholowej są organizmami tlenowymi. Przy braku tlenu drożdże fermentują, ale nie rosną. W środowisku, jeżeli pojawi się tlen proces fermentacji intensywnie maleje. Wzrasta natomiast oddychanie tlenowe.
Paster odkrył, że silne napowietrzanie powoduje zanik fermentacji - EFEKT PASTERA. Proces napowietrzania podtrzymuje wzrost organizmów i równocześnie prowadzi do zmniejszenia zużycia glukozy. Spada również ilość wytworzonego etanolu i CO2. Ma to duże znaczenie, jeżeli chodzi o energetykę procesu.
W warunkach beztlenowych 1 mol glukozy daje 2 mole ATP. Natomiast podczas oddychania tlenowego 1 mol glukozy daje 38 moli ATP. Ta energetyka procesu wyjaśnia proces fermentacji. Zawsze najbardziej energetycznym procesem jest oddychanie tlenowe.
W procesie fermentacji nie dochodzi do całkowitego spalania substratu, bo część energii jest związana w produkcie energetycznym - etanolu. Drożdże rosną (rozmnażają się) tylko podczas oddychania tlenowego, bo potrzebna jest duża ilość energii, której dostarcza oddychanie tlenowe. Dlatego jeżeli fermentują, to nie rosną.
Istnieje selekcja drożdży, która służy potrzebom człowieka:
drożdże denne - słabo oddychają, a dobrze fermentują. Są wykorzystywane do ważenia piwa.
drożdże fermentacji górnej - służą do produkcji wina i etanolu, a także używane są w piekarnictwie.
Wszystkie płyny, które powstają w procesie fermentacji zawierają substancje uboczne - fuzle.
FUZLE - mieszaniny propanolu, alkoholi pentanoli i butanoli. Są to produkty uboczne przemian aminokwasów: izoleucyny, leucyny i waliny.
Wśród wszystkich znanych organizmów żywych fermentację taką, jaką prowadzą Saccharomyces Cerevisiae prowadzi jedna bakteria Sarcina ventriculi - wytwarza etanol w takich samych procesach fermentacyjnych jak drożdże.
Inną bakterią, która została wyizolowana z fermentacji soku agawy jest bakteria Zymomonas mobilis. Prowadzi proces fermentacji podobny do drożdży. W procesie powstaje CO2, etanol, ale również w niewielkich ilościach kwas mlekowy.
Jednak na skalę przemysłową wykorzystywane są drożdże.
FERMENTACJA MLEKOWA
Wszystkie bakterie mlekowe zostały zakwalifikowane do rodziny Lactobacteriaceae. Grupa ta obejmuje bakterie o zróżnicowanej morfologii. Należą tutaj laseczki oraz ziarniaki typu paciorkowcowatego. Wszystkie są gram+, nie wytwarzają przetrwalników, z wyjątkiem jednej bakterii Lactobacillus inulinus. W decydującej przewadze wszystkie bakterie z tej rodziny są bakteriami nieruchliwymi. Zależne są od węglowodanów, jako źródła energii, wytwarzają one kwas mlekowy.
Do wzrostu na podłożach mineralnych wymagają czynników i witamin (z grupy B), dostarczają określonych aminokwasów oraz puryn i pirimidyn. Bakterie te, jeżeli są hodowane na podłożu wzbogaconym krwią, tworzą cytochromy i są zdolne do fosforylacji w łańcuchu oddechowym.
Bakterie z rodziny Lactobacteriaceae można uznać za formy ułomne pod względem syntetyzowania wielu składników. To, że zatraciły zdolność syntezy wielu związków wynika ze środowiska, w którym żyją. Bakterie te bardzo dobrze rozmnażają się w mleku oraz w środowiskach bogatych w czynniki wzrostowe i odżywcze. Mogą one rozkładać i wykorzystywać laktozę. Taką zdolność posiadają tylko bakterie należące do rodziny Enterobacteriaceae.
Laktoza praktycznie nie występuje w królestwie roślin, jest wykorzystywana jedynie przez ssaki, u których znajduje się w mleku. Wykorzystywanie laktozy przez bakterie tych rodzin jest wynikiem przystosowania ich do warunków, w których żyją.
Laktoza jest dwucukrem, który musi zostać rozłożony:
enzym β - galaktozydaza
Tylko nieliczne drobnoustroje zawierają ten enzym.
Drobnoustroje należące do tej rodziny bardzo rzadko występują w wodzie i glebie. Naturalnym ich siedliskiem są mleko i produkty mleczne, zdrowe i gnijące rośliny, układ pokarmowy i błony śluzowe ludzi i zwierząt.
W zależności od tego, czy bakteria z tej rodziny fermentuje glukozę do jednego produktu (kwas mlekowy) lub kilku produktów, mogą prowadzić homofermentację lub heterofermentację.
Proces homofermentacji mlekowej:
C6H12O6
2 CH3CHOH - COOH
Proces ten prowadzą:
Paciorkowce:
Lactococcus lactis
Lactococcus casei
Streptococcus pyogenes
Streptococcus salivarius
Enterococcus feacalis
Laseczki:
Lactobacillus acidophilus
Proces homofermentacji mlekowej bardzo wydajnie zachodzi w temperaturze ok. 40°C. Niektóre bakterie prowadzą wydajnie ten proces w temperaturze 30 - 37°C.
Kwas mlekowy może występować w izomerii D jak i L. O tym czy powstanie izomer D czy L decyduje stereoswoistość enzymu dehydrogenazy mleczanowej oraz obecność lub brak enzymu racemazy mleczanowej.
Bakterie należące do rodziny Lactobacteriaceae mogą prowadzić również proces heterofermentacji mlekowej. Jednakże bakterie prowadzące heterofermentację nie mają czynnych enzymów, które mogłyby przeprowadzić glukozę w pirogronian w szlaku glikolizy. Jest tzw. szlak pentozofosforanowy.
Proces heterofermentacji mlekowej:
Powstaje więcej niż jeden produkt:
Lactobacillus bifidum
Bifidobacterium bifidum
2 C6H12O6
2 CH3 - CHOH - COOH + 3 CH3COOH
glukoza kwas mlekowy
Leuconostoc mesenteroides
C6H12O6
CH3 - CHOH - COOH + C2H5OH + CO2
glukoza
C5H10O5
CH3 - CHOH - COOH + CH3COOH
ryboza
Bakterie te mają znaczenie w gospodarstwach domowych jak i w przemyśle. Służą do zakwaszania i nadawania smaku produktom mleczarskim - twarogi, masło, kefir, jogurt, kwas mlekowy, zsiadłe mleko, wyrób wędlin (salami).
WYKŁAD 8
Transport elektronów w warunkach beztlenowych u bakterii.
W osadach dennych jezior i stawów oraz w mokrych glebach, czyli w ekosystemach pozbawionych tlenu rozwijają się bakterie, które otrzymują energię do procesów metabolicznych drogą ODDYCHANIA ANOKSYCZNEGO (akceptorami elektronów są związki nieorganiczne, które w swojej budowie chemicznej mają tlen). Obecnie tylko procesy fermentacji są uznawane za procesy striktobeztlenowe.
Bakterie oddychające anoksycznie wykorzystują związki, które są wytwarzane przez bakterie w procesach fermentacji, czyli związki powstałe w fermentacjach są donorami elektronów i protonów wodoru.
Te anoksycznie oddychające organizmy wykorzystują jako akceptory związki: azotany, azotyny, tlenek azotu, podtlenek azotu, siarczany, siarczyny, siarkę elementarną, węglan, żelazo na +3 stopniu, inne związki. Przez przyłączenie elektronów do w/w związków powodują one ich redukcję:
azotan redukuje się przez kolejne związki do azotu cząsteczkowego lub do amoniaku (
)siarczany, siarczyny i siarkę elementarną redukują do tiosiarczanów, siarczków i siarkowodoru
węglany i CO2 redukują do kwasu octowego lub metanu
żelazo z +3 redukują do żelaza na +2.
Przenoszenie elektronów pochodzących z substratów organicznych do wymienionych związków nieorganicznych lub nieorganicznych jonów pozwala na fosforylację na poziomie transportu elektronów, czyli jest to fosforylacja oksydatywna. Wynikiem procesu fosforylacji oksydatywnej jest zysk energetyczny.
Organizmy, które oddychają anoksycznie mają ogromne znaczenie dla poszczególnych cykli obiegu pierwiastków w przyrodzie oraz w utrzymaniu równowagi w biosferze. Wszystkie bez wyjątku organizmy oddychające anoksycznie należą do Procaryotów. Produkty oddychania anoksycznego są zazwyczaj bardzo charakterystyczne i mogą być to substancje gazowe - azot cząsteczkowy, tlenek i podtlenek azotu, gazy palne (np. metan), siarkowodór, diamagnetyczny tlenek żelaza (Fe3O4).
Jednym ze sposobów jest ODDYCHANIE AZOTANOWE. U bakterii oddychających w ten sposób elektrony są przekazywane do azotanu. Azotan ulega redukcji. W trakcie transportu elektronów dochodzi do zysku energetycznego i proces ten nosi nazwę dysymilacyjna redukcja azotanu (oddychanie azotanowe).
Ze względu na energię i rolę biochemiczną wyróżnia się dwa typy bakterii i dwa rodzaje metabolizmu:
denitryfikacja (szlak asymilacyjny)
amonifikacja azotanów.
Bakterie denitryfikacyjne to tlenowce. Rosną w warunkach beztlenowych w obecności azotanu, natomiast nie rosną w warunkach tlenowych przy braku azotanu. Koniecznym warunkiem denitryfikacji jest obecność azotanów.
W warunkach beztlenowych przy obecności azotanów związek ten jest jedynym akceptorem elektronów. Następuje redukcja tego związku przez kolejne etapy:
Denitryfikacja
10[H] + 2[H+] + 2NO
N2 + H2O
Enzymy: reduktazy
DENITRYFIKACJA - przekształcenie azotu związanego w postaci azotanów do wolnego azotu. Jest jedynym biologicznym procesem, w wyniku którego azot związany w związkach organicznych i nieorganicznych może zostać uwolniony i ponownie włączony w obieg.
Każdy etap redukcji azotanów i redukcji kolejnych przenośników elektronów jest katalizowany przez enzymy: Reduktazy. Są one związane z błoną cytoplazmatyczną.
W zależności od warunków środowiska redukcja azotanu może przebiegać bez akumulacji związków pośrednich lub z akumulacją związków pośrednich. Azotyn, tlenek azotu lub azot są wydzielane kiedy jest nadmiar azotanu, a stężenie donorów wodoru jest czynnikiem ograniczającym, czyli w takich warunkach nie ma kumulacji produktów pośrednich redukcji azotanów w komórce.
Wszystkie bakterie prowadzące denitryfikację to tlenowce, ponieważ mają pełny zestaw składników (enzymów) łańcucha oddechowego. Enzymy biorące udział w oddychaniu azotowym są indukowane lub hamowane w warunkach niedoboru lub braku tlenu. Kolejnym warunkiem indukcji lub inhibicji enzymatycznej jest obecność azotanu. Wiele bakterii denitryfikacyjnych rośnie wówczas, kiedy w środowisku nie ma azotanów, ale są inne akceptory elektronów: azotyny, podtlenek azotu. O tym, że tak bakterie mogą żyć i rosnąć w takich warunkach świadczy obecność reduktaz.
Denitryfikacja jest procesem powszechnym w środowisku pozbawionym tlenu i łatwo zachodzi w wodach stojących, szczególnie wtedy, gdy równocześnie stosowane są nawozy organiczne i azotany. Prowadzić to może do nagromadzenia azotynów, zanieczyszczenia wody pitnej toksycznymi azotynami.
Zależność między utratą azotu a jego zaleganiem wynika z metabolizmu enzymów redukujących azotan, bowiem enzymy te ulegają indukcji w obecności azotanu jedynie w warunkach beztlenowych. Tlen hamuje tworzenie się reduktazy azotanowej, a także reduktazy azotynowej, współzawodniczy też z azotanem o elektrony.
Do bakterii prowadzących proces denitryfikacji należą:
Rodzaje
Bacillus
Agrobacterium
Acinetobacter
Alcaligenes
Propiobacterium
Corynobacterium
Cytoplyga
Spirillum
Hyphomicrobium
Rhizobium
Gatunki
Pseudomonas denitryficans
Pseudomonas aeruginos
Bacillus licheniformis
Paracoccus denitryficans
Thiobacillus denitryficans
Znaczenie denitryfikacji w przyrodzie
Jest jedynym biologicznym procesem, w którym azot w formie związanej zostaje przeprowadzony w azot cząsteczkowy. W skali globalnej proces ten ma znaczenie w utrzymywaniu życia na Ziemi. W normalnie napowietrzonych ekosystemach azotany są końcowym produktem procesu mineralizacji. Ponieważ azotany są bardzo dobrze rozpuszczalne w wodzie, a słabo adsorbują się do cząsteczek gleby mogłyby być wymywane i ulegałyby kumulacji w oceanach. W ten sposób azot ciągle byłby tracony z atmosfery i gleb, co doprowadziłoby do zahamowania wzrostu roślin, produkcji biomasy i procesu tlenu.
Proces denitryfikacji jest kontrolowany głównie przez temperaturę. Bakterie prowadzące denitryfikację należą do bakterii mezofilnych - najlepiej rosną w temperaturze 20 - 40°C.
Denitryfikacja najlepiej zachodzi, gdy:
temperatura = 20°C
pH = 7
tlen rozpuszczony - mniej niż 0,5 mg O2/l
obecność metali, które aktywizują powstawanie enzymów: reduktazy azotanowej, a także dehydrogenaz (selen, molibden).
WYKŁAD 9
AMONIFIKACJA AZOTANU
Prowadzą ją bakterie fakultatywne, których zasadnicze procesy oddechowe to fermentacja - Escherichia coli, Enterobacter aerogenes. Wykorzystują one azotan, jako akceptor elektronów. Elektrony i wodór są przenoszone na azotan z substratów pochodzących z procesów fermentacji. Azotan przyjmując elektrony i protony wodoru ulega redukcji i redukuje się wpierw do azotynu. Reakcja ta katalizowana jest przez enzym - reduktazę azotanową A.
Proces redukcji azotanów związany jest z fosforylacją oksydatywną, czyli daje zysk energetyczny komórce. I etap zachodzi wewnątrz komórki i dostarcza zysku energetycznego:
Azotany są toksyczne dla komórki i zostają z komórki wydzielone do środowiska zewnętrznego. W środowisku zewnętrznym pod wpływem enzymów wydzieliny zewnątrzkomórkowe redukują się do amoniaku:
Proces ten odbywa się poza komórką i nie dostarcza jej energii.
NO
- tzw. egzogenny akceptor elektronów, poza komórkowy.
Końcowym produktem amonifikacji azotem jest amon - amonifikacja nie prowadzi do powstania wolnego azotu.
Podstawową różnicą między denitryfikacją (wolny azot) i amonifikacją (amon) jest produkt końcowy.
Niektóre drobnoustroje mają zdolność asymilacji azotu. Najpowszechniejszym źródłem azotu dla bakterii i roślin jest azotan, amon.
Większość bakterii wytwarza enzymy potrzebne do asymilacji azotanu. Enzymy te ulegają indukcji w warunkach tlenowych i beztlenowych, gdy brak jest innego źródła azotu. Proces ten przebiega przez kilka związków pośrednich i prowadzi do uwolnienia azotu w postaci amoniaku lub amonu. Akceptorami elektronów są NO
- w skutek przyjęcia 2
redukuje się do NO
, przyjmuje 2
i powstaje HNO:
Redukcja NO
do NO
wymaga dostarczenia 2
. Dalszy etap to dostarczenie 6
. Proces katalizowany jest przez enzymy:
I etap - reduktaza azotanowa B - NO
do NO
pozostałe etapy - reduktaza azotynowa.
Elektrony są przenoszone na poszczególne przenośniki przy pomocy nukleotydów: NADH2, NADPH2. u roślin przenośnikami są jeszcze związki zawierające Fe, np. ferodoksyna. Powstający azot w postaci NH3 lub NH
ulega wbudowaniu do aminokwasów i innych związków zawierających azot w formie amonu.
Inną możliwością oddychania w warunkach beztlenowych jest PROCES DESULFURYKACJI.
Jest grupa bakterii o zdolności redukowania siarczanów, przekazów wodoru do siarczanu, jako ostatecznego akceptora elektronów. Siarczan w wyniku tej redukcji redukuje się do siarczku lub H2S. Proces ten zachodzi przy współudziale cytochromu C, a zysk energetyczny w warunkach beztlenowych pochodzi z fosforylacji oksydatywnej. Donory wodoru i elektronów są produktami fermentacji.
Proces fosforylacji
Ten typ reakcji to ODDYCHANIE SIARCZANOWE (dysymilacyjna redukcja siarczanu). Głównym produktem tego procesu jest H2S lub siarczki. Bakterie redukujące siarczany to obligatoryjne beztlenowce - są ściśle uzależnione od warunków beztlenowych.
Proces denitryfikacji - beztlenowy, a bakterie tlenowe.
Desulfurykacja - proces beztlenowy, bakterie to bezwzględne beztlenowce.
Bakterie desulfurykacyjne:
Bakterie właściwie urzęsione i nie urzęsione
Rodzaje:
Desulfovibria
Desulfomonas
Desulfobacterium
Desulfosarcina
Thermosulfobacterium
Bakterie właściwe gram + wytwarzające endospory
Rodzaj:
Desulfatomaculum
Bakterie gram - poruszające się ruchem ślizgowym
Rodzaj:
Desulfonema
Archebacterie
Rodzaj:
Archeaglobus.
Donorami wodoru i elektronów dla poszczególnych grup bakterii mogą być różne związki niskocząsteczkowe: maślan, metanol, etanol, wyższe kwasy tłuszczowe, związki aromatyczne, wodór cząsteczkowy, mleczan, octan, pirogronian. Są to produkty procesu fermentacji. Żaden pojedynczy gatunek nie ma możliwości wykorzystania wszystkich związków i żaden związek nie jest wykorzystywany przez wszystkie mikroorganizmy.
Proces redukcji siarczanów jest skomplikowany. Akceptorami elektronów są siarczany. Przyjmowane elektrony redukują się i jednocześnie aktywizuje się ATP. W tym procesie działa enzym sulfurylaza ATP. W wyniku aktywacji ATP redukuje się do AMP, uwalniają się dwie grupy fosforanowe. Siarczan staje się APS na wyższym poziomie energetycznym.
Gdy proces zachodzi w tzw. Dysymilacyjnej redukcji siarczanów to APS redukuje się i podczas tego procesu uwalnia się AMP. Czynnikiem redukującym są elektrony i wodór w ilości: 2 atomy wodoru i 2
. AMP zredukowany uwalnia siarczyny. One redukują się do jonu kwasu wielotionowego. On redukuje się do tiosiarczanów, a one do siarczków lub siarkowodoru.
Proces w wyniku asymilacyjnej redukcji siarczanów, to związek, czyli siarczany są dwukrotnie podnoszone na wyższy poziom energetyczny.
Siarczany
APS - wspólny etap dla asymilacyjnej i dysymilacyjnej redukcji siarczanu.
Potem APS ulega aktywizacji. Dawcą energii jest ATP redukujący się do APS.
Oddychanie siarczanowe
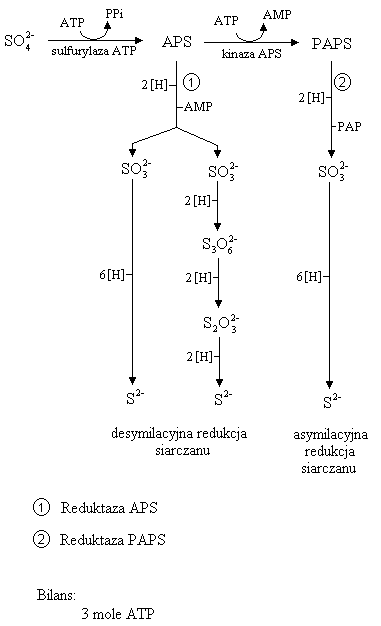
APS - adenozyno - 5′ - fosfosiarczan
PAPS - fosfoadenozyno - 5′ - fosfosiarczan
PAP - fosfoadenozyno - 5′ - fosforan
WYKŁAD 10
Każdy organizm prowadzi proces oddychania w celu uzyskania energii. Oddychanie siarczanowe dostarcza energii dzięki fosforylacji oksydatywnej.
Dlaczego możliwa jest fosforylacja na poziomie transportu
:
występowanie cytochromów CB i b (niski potencjał
= - 205 mV) oraz białek żelazo - siarkowychobecność konstytutywnej hydrogenazy biorącej udział w pobieraniu i aktywacji wodoru oraz w jego uwalnianiu
zdolność redukcji SO
przy udziale cząsteczkowego wodoru z akumulacji H2S (ale bez wyraźnego wzrostu).
Bakterie oddychające siarczanowo mogą prowadzić fermentację. Substrat to kwas pirogronowy.
Fermentacja bakterii desulfurykacyjnych - heterofermentacja:
Mogą też wykorzystywać mleczan.
Rola bakterii desulfurykacyjnych w przyrodzie:
Występują głównie w rozkładających się osadach i tzw. czarnym błocie - zachodzi tu również degradacja związków organicznych. Związki ulegające rozkładowi to głównie kwasy tłuszczowe, ketokwasy, alkohole. Bakterie te powodują degradację związków powstałych wcześniej w procesie fermentacji. Donorami dla tych bakterii są zawsze produkty fermentacji. Produktem degradacji są: siarczki, H2S.
Bakterie te przyczyniają się do wytworzenia złóż siarki pochodzenia bakteryjnego, bo bakterie redukujące siarczany redukują je w etapie pośrednim do siarki elementarnej. Siarkowodór i siarka powstaje też przez redukcję osadów morskich - udział bakterii.
Beztlenowa korozja żelaza - uszkodzenia rurociągów, wycieki substancji zachodzą głównie przy udziale bakterii z rodzaju Desulfovibrio sp.:
utlenianie Fe - na powierzchni tworzy się błonka z utlenionego Fe i wodoru
4 Fe0 + 8 H+
4 Fe2+ + 4 H2.
Błonka ta częściowo zabezpiecza przed korozją, ale gdy w środowisku są bakterie Desulfovibrio sp. dochodzi do
redukcja siarczanu
4 H2 + SO
H2S + 2 H2O + 2 OH-
Elektrony potrzebne tu do redukcji SO
pochodzą z wodoru. Fe dalej utlenia się, nawet przy braku tlenu.
dalsze utlenianie Fe
4 Fe2+ + H2S + 2 OH- + 4 H2O
FeS + 3 Fe(OH)2 + 6 H+.
Beztlenowa korozja Fe - reakcja sumaryczna:
4 Fe0 + SO
+ 2 H2O + 2 H+
FeS + 3 Fe(OH)2.
Procesy korozji spowodowane są nie tylko samym utlenianiem Fe, ale oddychaniem bakterii desulfurykacyjnych.
Na dnie mórz (Morze Czarne) jest dużo H2S powstającego w drodze pracy bakterii desulfurykacyjnych. Bakterie te powodują korozję Fe na dnie morza. Powstaje siarczek żelaza (czarny - stąd nazwa Morze Czarne). Jest to spowodowane dużą ilością bakterii, korozją Fe, wytwarzaniem siarczku Fe.
Bakterie te występują w przewodzie pokarmowym zwierząt przeżuwających. U nich w żuwaczu powstaje siarkowodór.
NIEORGANICZNE DONORY WODORU
Wiele bakterii w wodach i glebie potrafi wykorzystać nieorganiczne związki i jony - amon, azotyn, siarczyny, tiosiarczan, siarczek, F2+, siarka elementarna, wodór, tlenek węgla - jako donory elektronów lub wodoru. W wyniku ich utleniania uzyskują energię i elektrony konieczne dla reakcji syntezy. Ten typ życia, w którym związki nieorganiczne są wykorzystywane jako donory wodoru i elektronów nosi nazwę chemolitotrofii.
Jest kilka grup bakterii prowadzących proces z transportem elektronów:
bakterie utleniające amoniak NH3
NO
Nitrosamonas europea
bakterie utleniające azotyn NO
NO
Nitrobacter winogradskyi
bakterie siarkowe S0, S2-, S2O
SO
Thiobacillus thiooxidans
bakterie żelazowe Fe2+
Fe3+
Thiobacillus ferrooxidans
bakterie utleniające wodór H2
H2O
Alcaligenes eutrophus
karboksylobakterie CO
CO2
Pseudomonas carcoxidovorans.
Bakterie chemolitotroficzne wykorzystują też węgiel z CO2, rzadziej z octanu. Bakterie te mają zdolność asymilacji CO2 w cyklu rybulozobisfosforanowym (cykl Celvina, faza ciemna fotosyntezy). Glukoza najczęściej powstaje w reakcjach wiążących CO2 i przetwarzających go w związki organiczne. Są to bakterie autotroficzne - asymilują CO2, bakterie chemolitoautotroficzne.
Chemolitotrofia- utlenianie nieorganicznych związków.
Chemolitoautotrofia - asymilacja CO2.
NITRYFIKACJA
Jedną z tych reakcji jest proces nitryfikacji zachodzący dwuetapowo:
utlenianie amonu do azotynów
utlenianie azotynów do azotanów.
W tych reakcjach zawsze uczestniczą dwie grupy bakterii. Do tej pory nie stwierdzono obecności bakterii utleniających amon bezpośrednio do azotynów.
I.
Nitrosamonas europea
Nitrosococcus oceanus
II.
Nitrobacter winogradskyi
Nitrobacter agilis
Nitrobacter hamburgensis
Drugi etap nitryfikacji może zajść, bo bakterie pierwszego etapu zmieniają pH z zasadowego na kwaśny. Odczyn zasadowy hamuje drugi etap, bo jest toksyczny dla bakterii przeprowadzających ten etap.
Bakterie prowadzące nitryfikację to nitryfikatory: bakterie gram ujemne, autotroficzne, należące do rodziny Nitrobacteriaceae - są to bezwzględne tlenowce.
Od ilości O2 zależy szybkość utleniania przez nie związków. Bakterie te można hodować w warunkach laboratoryjnych na podłożach mineralnych, przy pH = 7,7 - 8,0.
Proces nitryfikacji zachodzi już w temperaturze 5°C, optimum przypada na temperaturę 24 - 29°C. Bakterie te są szczególnie wrażliwe na temperaturę - giną w temperaturze 55°C. W temperaturze 55 - 62°C bakterie giną normalnie. Bakterie te wykorzystują jako źródło węgla CO2, rzadziej octan. Octan wykorzystują Nitrobacter winogradskyi.
Szlak utleniania amonu przebiega przez etapy pośrednie. Amon utlenia się do hydroksyloaminy - etap wymagający dostarczenia energii (endoergiczny). Dalej zachodzi utlenianie hydroksyloaminy do azotynów, jest to proces egzoergiczny - komórka otrzymuje 66 kcal. Ogólnie cały proces dostarcza 17 kcal.
Szlak utleniania amonu:
Proces nitryfikacji zachodzi również u heterotrofów, np. bakterie z rodzaju Arthobacker. Bakterie te wytwarzają azotan z azotynów. Inne organizmy mogą też prowadzić ................................ Procaryota - promieniowce, eucaryota - grzyby. Grzyby utleniają azot aminowy NH2 do azotynu i dalej do azotanu.
Proces utleniania związków zredukowanych u heterotrofów zachodzi powoli ze słabą wydajnością. Proces utleniania nie jest sprzężony ze wzrostem organizmów i produkcją biomasy - to tylko jeden ze sposobów dodatkowego utleniania amonu i związków organicznych. Pozyskiwanie energii nie służy im do wzrostu, produkcji biomasy. Energię czerpią z oddychania tlenowego.
WYKŁAD 11
W procesach takich jak utlenianie związków azotu, siarki, żelaza proces zachodzi z niewielką wydajnością energetyczną. Substraty biorące udział charakteryzują się bardzo wysokim potencjałem redoks:
NH
/ NH2OH ε0 = + 889 mV
Fe2+ / Fe3+ ε0 = + 770 mV
NAD / NADH2 ε0 = - 320 mV
Taka różnica potencjałów powoduje, że nukleotydy i substraty nie mogą być bezpośrednio sprzężone z redukcją NAD lub NADP. Zredukowane nukleotydy są niezbędne do redukcji CO2 w fazie ciemniej fotosyntezy - szlak rybulozobisfosforanowy.
Powody niskiego zysku energetycznego komórki:
Redukcja CO2 to inaczej asymilacja CO2.
Elektrony włączane są do łańcucha oddechowego z procesu utleniania substratu na poziomie cytochromu A lub C, czyli w łańcuchu oddechowym zachodzi tylko jedna fosforylacja oksydatywna. Elektrony z utlenianego substratu są włączane w ostatnim etapie łańcucha oddechowego.
Część energii wykorzystywana jest do redukcji nukleotydów pirymidynowych. Proces ten nosi nazwę transportu elektronów w kierunku przeciwnym i jest on niezbędnym mechanizmem do uzyskania równoważników redukujących (elektrony) koniecznych do reakcji syntez.
Niewielka ilość energii pozwala na bardzo niewielką wydajność komórkową.
Rola nitryfikacji w procesach środowiskowych.
Jony amonowe wyzwalające w mineralnych związkach azot w dobrze napowietrzonym środowisku szybko ulegają utlenieniu.
Zastąpienie kationu anionem prowadzi do zakwaszenia środowiska - rozpuszczenia się minerałów.
Wytworzenie środowiska kwaśnego przez utlenienie amonu do azotynów umożliwia zajście drugiej fazy nitryfikacji.
Duże stężenie amonu jest toksyczne dla bakterii utleniających azotyny do azotanów.
Bakterie nitryfikacyjne uczestniczą bezpośrednio w niszczeniu wapienia i cementu - niszczenie dróg, budynków. Utleniają one amon z atmosfery lub odchody zwierzęce do kwasu octowego.
Gleby potraktowane nawozami azotowymi uwalniają tlenek azotu, szczególnie przy braku tlenu, bo bakterie Nitrosamonas też mogą przeprowadzać denitryfikację i wtedy tlenek lub dwutlenek azotu pochodzi z utlenionego amoniaku.
Stwierdzono też, że organizmy utleniające amon, metan, etylen, propylen charakteryzują się bardzo silnym potencjałem utleniającym. Występują one przede wszystkim w środowisku glebowym i w zanieczyszczonych wodach i należą do tzw. autochtonicznej flory tych środowisk. Uczestniczą one w powolnym utlenianiu produktów powstających w rozpadzie związków organicznych.
Zdolność utleniania amonu mają też bakterie metanowe, ale nie wykorzystują one tego procesu do wzrostu. Prowadzona prze nie reakcja to nitryfikacja heterotroficzna. Utlenianie amonu przez bakterie metanogenne i utlenianie przez nie metanu zachodzi przy udziale enzymu - monooksygenazy (ten sam enzym, który utlenia pierwszy etap nitryfikacji).
Czynniki kontrolujące w procesie nitryfikacji:
temperatura - optymalna to 24 - 29°C. W procesie technologicznym to około 30°C. Proces nitryfikacji zachodzi w temperaturze 5 - 50°C. W 55°C bakterie giną
pH - technologiczne to 7,5 - 8,5. Jeżeli pH jest na poziomie 6,5 i jest stałe to nitryfikacja zachodzi z dobrą wydajnością. Jeżeli spada poniżej 6,5 to proces jest słabo wydajny, a przy pH 6,0 ustaje. Również pH wyższe niż 8,5 powoduje obniżenie wydajności.
odpowiednia zasadowość ścieków - przy utlenianiu 1 mg amonu spadek zasadowości jest o 7,14 mg CaCO3
tlen - żeby nitryfikacja zachodziła z dobrą wydajnością to minimum tlenu powinno wynosić 2 mg O2/l. Jeżeli tlenu rozpuszczonego jest mniej to nitryfikatory mogą wykorzystać jako akceptory elektronów azotany (Nitrobacter), ale wtedy wydajność jest mniejsza
obecność substancji toksycznych - cyjanki, tiomocznik, fenole, pochodne halogenowe węglowodorów, krezole, anilina. Powinno ich być mniej niż 20 mg/l
metale ciężkie - miedź, cynk, kadm, nikiel, ołów, chrom. Stężenie nie powinno przekraczać 5 mg/l
materia organiczna - jeżeli jest nadmiar materii organicznej dochodzi do rozwoju flory heterotroficznej. Rozwój uniemożliwia rozwój nitryfikatorów, bo heterotrofy oddychają tlenowo, wykorzystują więc tlen. Ich procesy życiowe zachodzą intensywnie, bo w oddychaniu z 1 cząsteczki glukozy zyskują 38 cząsteczek ATP (bardzo szybko się mnożą). Nitryfikatory ze względy na niski zysk energetyczny prowadzą proces powoli. Dlatego bardzo ważne jest obciążenie (BZT5 - 0,2 kg) i wiek osadu.
Inną możliwością pozyskiwania energii są PROCESY UTLENIANIA ZREDUKOWANYCH ZWIĄZKÓW SIARKI.
Siarka organiczna wchodzi w skład substratów organicznych - aminokwasy siarkowe: cysteina, cystyna, metionina.
Do środowiska naturalnego (woda, gleba) siarka dostaje się z resztkami roślinnymi i zwierzęcymi w postaci połączeń organicznych. W środowiskach tych żyją drobnoustroje, które redukują organiczne połączenia siarki, a następnie mają zdolność redukcji siarczanów do siarczku i siarkowodoru. Obok tych organizmów znajdują się też drobnoustroje, które prowadzą proces odwrotny - utleniają zredukowane związki siarki. Zawsze bakteriom denitryfikacyjnym towarzyszą bakterie, które utleniają związki siarki - bakterie siarkowe. Celem jest pozyskiwanie energii.
Zdolność utleniania zredukowanych związków siarki ma grupa polarnie urzęsionych bakterii gram (-), które należą do rodzaju Thiobacillus (pałeczka). Obecnie odkryto bakterię spiralną z rodzaju Thiomicrospira oraz bakterię termofilną (gorące źródła) z rodzaju Sulfolobus. Bakterie te utleniają związki siarki i mogą utleniać siarczki, siarkę elementarną, tiosiarczany.
Utlenianie zredukowanych związków siarki
S2- + 2 O2
SO
S + H2O +
O2
SO
+ 2 H+
S2O
+ H2O + 2 O2
2 SO
+ 2 H+
Thiobacillus thiooxidans (CO2)
Thiobacillus ferrooxidans
Thiobacillus thioparus (CO2)
Thiobacillus denitryficans (CO2)
Thiobacillus novellus
Thiobacillus intermedius
Thionicrispira pelophila
Sulfolobus acidocaldarius
Formy nitkowate:
Beggiatoa sp.
Thiothrix sp.
Thioploca sp.
(CO2) - bakterie te są zasadniczo autotrofiami uzależnionymi od wiązania CO2. są też bakterie, które wykorzystują jako źródło węgla związki organiczne.
Bakterie utleniające związki siarki wykorzystywane są do zmniejszenia alkalicznego odczynu gleb (gleby kredowe). Stosuje się wprowadzenie do nich siarki elementarnej. Kwas siarkowy, który powstaje wskutek działalności tiobakterii przeprowadza węglan wapnia w związki lepiej rozpuszczalne w CaSO4. Szybko ulega on wypłukaniu z gleb. Można również pomagać uprawom - choroba zwana parchem ziemniaka - opyla się siarką i powstaje kwaśny odczyn, którego ta choroba nie znosi.
Wszystkie wymienione bakterie żyją w warunkach tlenowych. Istnieje jedna, która może żyć w warunkach pozbawionych tlenu: Thiobacillus denitryficans - wykorzystuje jako akceptor elektronów azotany (redukcja azotanów do azotu cząsteczkowego).
Bakterie, które żyją w ekstremalnych warunkach - Sulfolobus acidocaldarius - zamieszkują gorące źródła, w których utleniają siarkowodór i siarkę pochodzenia wulkanicznego. Bakterie te wykazują optymalny wzrost przy pH = 2 - 3 (w środowisku silnie kwaśnym). Większość bakterii Thiobacillus żyje w temperaturze około 30°C, a gatunki ciepłolubne w temperaturze 70 - 75°C (temperatura optymalna), a spotyka się je w temperaturze 90°C. Szczególną bakterią jest Thiobacillus thiooxidans - wybitnie kwasowa. Toleruje ona jednonormalny kwas siarkowy i bardzo dobrze rozwija się w pH = 1. Thiobacillus ferrooxidans ma zdolność utleniania zredukowanych związków siarki, ale energię do życia czerpie z utleniania żelaza z +2 na +3 stopień.
WYKŁAD 12
Podstawową reakcją, która dostarcza komórce energii jest proces utleniania siarczanów - zysk na drodze fosforylacji substratowej
APS - adenozyno - 5 - fosfosiarczan
Procesy utleniania zredukowanych związków mogą prowadzić bakterie Thiobacillus thiooxidans, Thiobacillus ferrooxidans, ale również bakterie nitkowate. Występują one w osadach dennych jezior lub w wolno płynących wodach - Beggiatoa, Thiothrix sp.
Procesy utleniania zredukowanych związków siarki zostały wykryte przez Winogradzkiego. Stwierdził on, że bakterie nitkowate utleniają siarkowodór do siarki elementarnej, a dalej do kwasu siarkowego. Wykazał, że proces ten jest rodzajem oddychania, w którym komórki czerpią energię.
GENETYKA MIKROORGANIZMÓW
Jednostką funkcjonalną dziedziczności i zmienności jest GEN. Są to odcinki DNA rozmieszczone liniowo. Pojedynczy gen spełnia rolę zapisu genetycznego o pojedynczej funkcji, np. o syntezie białka. Białka są białkami strukturalnymi jak i enzymatycznymi. Geny wpływają bezpośrednio na katalizowanie komórki, a w organizmach wyższych na procesy katalityczne całego układu.
Określono hipotezę: „Hipoteza jeden gen - jeden enzym”.
Bakterie (Escherichia coli) maja zdolność z prostych składników pożywki syntetyzować wszystkie złożone związki organiczne.
PROTOTROF - organizm, zdolny do syntetyzowania potrzebnych mu do życia metabolitów, ale nie mogący asymilować CO2.
MUTANT AUKSOTROFICZNY - mutacje powstające u bakterii często polegają na utracie zdolności syntetyzowania pojedynczych związków, które są konieczne do wzrostu (witaminy, aminokwasy, zasady organiczne). Mutanty takie nie rosną na pożywce mineralnej, a wzrost ich jest uwarunkowany obecnością w pożywce gotowego produktu, którego zdolność syntezy mutant utracił.
Według tej hipotezy pojedynczy den umożliwia syntezę w organizmie pojedynczego enzymu. Mutacje w genach powodują brak syntezy białka enzymatycznego albo też dochodzi do syntezy białka, które nie ma własności katalitycznych. Enzymy w całości lub części są białkami. Część białkowa decyduje o specyficzności enzymu. Geny decydują o syntezie białek w organizmie.
Hipoteza „jeden gen - jeden enzym” była bardzo doniosła w genetyce i doprowadziła do wyjaśnienia roli DNA w syntezie białek. Została ona zmodyfikowana, bo wykryto, że niektóre białka i niektóre enzymy zbudowane są nie z jednego łańcucha polipeptydowego, ale z dwóch, trzech, a synteza jednego łańcucha polipeptydowego jest uwarunkowana odpowiednim genem. Każdy polipeptyd ma zakodowaną syntezę w genach.
Geny determinują syntezę wszystkich białek i biolog o nazwisku Benzer zdefiniował jednostkę funkcjonalną DNA pod względem genetycznym i nazwał ją cistronem.
CISTRON - fragment cząsteczki DNA, który kontroluję syntezę jednego łańcucha polipeptydowego, jednego enzymu lub jednego białka.
Zasadniczą funkcją kwasu DNA jest przekazywanie do komórek potomnych informacji genetycznej. Jest ona zakodowana w kolejności nukleotydu (sekwencji zasad organicznych).
Kwas DNA jest jednostką wzorcową przekazującą informacje zasadniczo dwoma odrębnymi szlakami. Pierwszy szlak prowadzi od DNA macierzystego do DNA potomnego (replikacja DNA). Drugi szlak obejmuje przekazywanie informacji z DNA do miejsca syntezy białka, czyli do rybosomu. Nośnikiem tej informacji jest kwas m - RNA (transkrypcja). U organizmów wyższych (tkankowe) istnieje jeszcze jeden szlak dotyczący różnicowania się komórek z zygoty w tkanki, narządy.
Wszystkie organizmy żywe, za wyjątkiem wirusów RNA, posiadają w komórce kwas DNA, w którym zakodowana jest informacja genetyczna. Geny spełniają w życiu organizmów i komórek rolę nadrzędną, gdyż:
umożliwiają podczas replikacji kopiowanie wszystkich swoistych cech w nowych cząsteczkach DNA
przekazują tę cechę organizmom potomnym
umożliwiają i kontrolują biosyntezę wszystkich białek komórkowych, czyli za pośrednictwem wymienionych funkcji geny kontrolują wszystkie procesy życiowe komórki.
Informacja genetyczna w rybosomie jest przepisywana na język aminokwasów. W informacji genetycznej zapisana jest kolejność aminokwasów w syntetyzowanym łańcuchu polipeptydowym. Odkąd stwierdzono, że DNA jest strukturą liniową o określonej sekwencji nukleotydów, stało się jasne, że kod genetyczny polega na kolejnym występowaniu zasad w łańcuchu. Ta kolejność zasad jest tłumaczona na język aminokwasów.
Przyjmuje się, że w skład białek wchodzi 20 aminokwasów (budują białka). Więcej niż 20 aminokwasów to aminokwasy, które nie budują struktur komórkowych - są to metabolity procesu przemiany materii. W skład cząsteczek DNA wchodzą cztery zasady: adenina, guanina, cytozyna, tymina.
Podstawową jednostką kodu genetycznego nie jest jedna zasada, dwie zasady tylko trzy zasady (43 = 64).
Cechy kodu genetycznego:
kod genetyczny jest trójkowy - podstawowa cecha
Doświadczenie Crick'a. Badano fag Escherichia coli. Robiono modyfikacje w strukturze DNA: wycinano trójkę zasad (delecja) lub dodawano trójkę zasad (addycja). Te dwa procesy powodują zmianę wszystkich następnych trójek, o ile delecja i addycja dotyczą tylko jednej zasady. Konsekwencją tego procesu było wytworzenie nieaktywnego białka o zupełnie innej sekwencji aminokwasów. Powstawało białko mające własności enzymatyczne. Potrojona addycja i potrojona delecja powodują zmiany w obrębie mutacji. Dalsze trójki są prawidłowe i może powstać prawidłowe białko. Są to dowody, że kod genetyczny jest trójkowy.
uniwersalny charakter. Bez względu na rodzaj organizmu jego konstrukcja i mechanizm działania są jednakowe. Budowa DNA i mechanizm działania jest taki sam u wszystkich organizmów. W miarę rozwoju genetyki zaczęto się starać, aby wyjaśnić ilość możliwości kodowania aminokwasów. Do roku 1961 wyjaśniono to i stwierdzono, że 61 trójek koduje aminokwasy, a 3 pozostałe kodony (cistrony) nie kodują żadnych aminokwasów. Zostały one nazwane kodonami nonsensownymi. Na podstawie nadmiaru zasad w stosunku do ilości aminokwasów wykazano, że kod genetyczny ma kodony synonimowe - poszczególny aminokwas może być kodowany przez kilka trójek zasad. Kod genetyczny ma charakter zdegenerowany - nie jest wadliwy.
ma charakter ciągły. Cały czas są sekwencje trójek. Jego system działania jest wyposażony w tzw. znaki przestankowe. Znaczy to, że w kodzie genetycznym są informacje dotyczące rozpoczęcia i zakończenia syntezy łańcucha polipeptydowego. Jeżeli na nici kwasu m - RNA znajdą się takie kodony o sekwencji UAA, UAG, UGA to proces biosyntezy białka rozpoczyna się. Jeżeli w pewnym momencie na nici m - RNA pojawi się kodon AUG, GUG to proces biosyntezy białka zostanie zakończony. Są to znaki przestankowe w kodzie genetycznym.
WYKŁAD 13
Geny podlegają procesom regulacyjnym. Mechanizm regulujący działanie genów polega na ich włączaniu i wyłączaniu. Został on wykryty u bakterii Escherichia coli. Odkrywcami byli Francuzi. Każda komórka zawiera tysiące genów, które kontrolują wytwarzanie białek nieaktywnych (strukturalnych) i aktywnych (enzymów).
W określonych warunkach żywa komórka jest zdolna do wyboru produkcji takich białek, jakie w danym momencie metabolizmu są jej najbardziej przydatne. Natomiast potrafi zahamować produkcję białek, które w określonym momencie metabolizmu nie są przydatne. Regulacja genetyczna polega na tym, iż komórka uruchamia bądź wstrzymuje syntezę danego białka, czyli w komórkach DNA muszą znajdować się geny regulujące.
Francuzi wykazali, że pod koniec łańcucha DNA (pod koniec zespołu genów) występuje zespół genów działających włączająco lub wyłączająco na syntezę białek. Takie geny noszą nazwę geny operatory, a teoria, która wyjaśnia działanie tych genów nosi nazwę TEORII OPERONU. Dotyczy ona zarówno procesów katabolicznych, jak i anabolicznych.
W procesach katabolicznych gen regulator wytwarza aktywny represor, który bezpośrednio pasuje do genu operatora i powoduje jego zablokowanie (wyłączenie) i nie ma syntezy białka i DNA.
Rys. Schemat działania genu - regulatora na kataboliczny operon; a) bez induktora, b) z induktorem;
GR - gen - regulator, Ra - aktywny represor, Rx - nieaktywny represor, O - operator, GS - kontrolowane geny strukturalne, i - induktor, m - m - RNA, E - enzym.
W reakcjach anabolizmu geny - regulatory produkują represor, ale jest to tzw. represor nieaktywny, który swoją strukturą nie pasuje do operatora - nie może go zablokować. Na genach struktury syntetyzowany jest m - RNA i białko enzymatyczne. Jeżeli w środowisku znajdują się czynniki mogące zmienić strukturę (korepresor), to represor staje się aktywny i pasuje do genu - operatora powodując jego zablokowanie. Nie ma syntezy białka.
Rys. Schemat działania genu - regulatora na anaboliczny operon; a) bez korepresora, b) z korepresorem;
r - korepresor, GR - gen - regulator, Ra - aktywny represor, Rx - nieaktywny represor, O - operator, GR - kontrolowane geny strukturalne, m - m - RNA, E - enzym.
Represor jest syntetyzowany w formie nieaktywnej - możliwa jest synteza białka.
W komórce mikroorganizmu możliwa jest REKOMBINACJA MATERIAŁU GENETYCZNEGO. U bakterii i innych prokariotów występuje kwas DNA zawsze w formie pojedynczej (haploidalnej) - należą do haplobiontów. Nigdy u procaryota nie pojawia się stadium diploidalne - nie ma powielenia materiału genetycznego. Proces rekombinacji materiału genetycznego u procaryota jest inny niż u organizmów diploidalnych.
U organizmów prokariotycznych istnieją różne możliwości genetycznych zmian o charakterze rekombinacji. Są to: koniugacja, transdukcja, transformacja, transfekcja, transpozycja.
KONIUGACJA - przełomowym momentem było wykazanie, że dwa mutanty Escherichia coli wytwarzają rekombinanty gdy są hodowane razem. Następnie wykazano, że istnieje specyficzny system koniugacji komórek i rekombinacji genów między koniugującymi partnerami. System ten opiera się na bardzo specyficznych zróżnicowaniu komórek bakteryjnych zwanym zróżnicowaniem płciowym. Komórki, które mają specyficzny czynnik F (czynnik płciowy) oznaczone są jako komórki (F+) i mogą przekazać ten czynnik komórkom nie mającym czynnika F - są to komórki (F-). Przekazanie tego czynnika jest procesem rekombinacji. Częstość jej zachodzenia pomiędzy komórkami (F+) a (F-) jest zjawiskiem rzadkim i przypada w jednej komórce na 104 - 105 komórek.
Przenoszenie czynnika płciowego (rekombinacja) jest zawsze jednokierunkowy - odbywa się z komórki dawcy (F+) do komórki biorcy (F-). Można tutaj mówić o pewnym zróżnicowaniu płciowym - typ biorcy to komórka żeńska, a typ dawcy - komórka męska.
CZYNNIK F - zawiera małą kolistą cząsteczkę DNA i jest zdolny do autonomicznej replikacji, która nie jest zsynchronizowane z replikacją kwasu DNA wchodzącego w skład genomu.
W czasie koniugacji między komórką (F-) i (F+) wytwarza się mostek cytoplazmatyczny, a czynnik F zostaje przekazany z komórki (F+) do komórki (F-).
Komórki (F+) różnią się szeregiem własności od komórki (F-):
zawierają specyficzny antygen (f +)
są wrażliwe na niektóre fagi
wytwarzają wypustki cytoplazmatyczne zwane pili (fimbrie).
Komórka, która nabędzie czynnik F nabiera pewnych własności wraz z przejściem tego czynnika - nabiera nowych cech genetycznych.
TRANSDUKCJA - jest to proces przenoszenia bakteryjnego materiału dziedzicznego z jednej komórki na drugą za pośrednictwem fagów (wirusów). W wyniku przeniesienia przez fagi DNA bakteryjnego (DNA dawcy) i następnie jego integracji do DNA komórki biorcy na drodze rekombinacji zachodzi przekazywanie własności dziedzicznych ze szczepu dawcy do szczepu biorcy.
Badacze stwierdzili, że fag P22 ma zdolność rozwijania się w komórce Salmonella typhimurium. Ten fag może przenieść własności dziedziczne z jednego szczepu Salmonella typhimurium na drugi. Jeżeli fagi wyizolujemy z zakażenia komórki po lizie Salmonelli to taki fag może przenieść materiał genetyczny na kolejne zainfekowane komórki, czyli wówczas fagi te stają się fagami transdukującymi. Część komórek Salmonelli ulegnie zainfekowaniu, lizie (zniszczeniu), a część będzie rekombinantami. Jeżeli szczep biorcy był auksotroficzny, a dawcy - prototroficzny to transduktanty (rekombinanty) będą prototrofami. Łatwo je wyizolowane wysiewać na pożywki mineralne nie uzupełnione odpowiednimi składnikami pokarmowymi.
Fragment DNA, który przenosi fag jest bardzo mały i zazwyczaj stanowi 0,01 genomu bakteryjnego. Fagi, które mają zdolność przenoszenia DNA bakteryjnego przenoszą ten fragment w kapsydzie. W trakcie wytwarzania płaszcza białkowego faga cząsteczki białka otaczają odcinek DNA bakteryjnego równy długości DNA fagowego, czyli fag może przenieść taki odcinek DNA, jaki sam ma.
Tylko od 10 - 12% fagów, które przenoszą bakteryjne DNA infekuje komórkę bakteryjną, bo żeby doszło do zainfekowania i transdukcji, to DNA przenoszone przez faga musi zostać włączone w DNA bakterii. Czasami zdarza się, że transdukujące fagi zawierają DNA bakteryjne i DNA fagowe. Wówczas DNA bakteryjne pochodzi z procesu, w którym fag zostaje wycięty częściowo z DNA bakteryjnym, a częsciowo ze swoim. Fagi, które mają zdolność wycinania całego odcinak DNA bakteryjnego lub jego części przenoszą informację genetyczną zawartą w DNA z jednej komórki bakteryjnej na drugą.
Z badań nad koniugacją i transdukcją wynika, że między bakteriami przekazywany jest kwas DNA, czyli odgrywa on decydujące znaczenie w przekazywaniu dziedziczności. Najbardziej bezpośrednim dowodem na rolę DNA w przekazywaniu własności dziedzicznych stanowi proces transformacji.
TRANSFORMACJA - proces przenoszenia z jednych komórek do drugich informacji genetycznych przy pomocy fragmentu DNA wyizolowanego z komórki dawcy i pobranego oraz zintegrowanego prze komórkę biorcy. W wyniku zastąpienia fragmentu DNA biorcy fragmentem DNA dawcy o odrębnych własnościach komórka biorcy nabiera nowych cech, jakie miały komórki dawcy.
Transformacja polega na pobraniu fragmentu DNA, powstaniu przejściowej formy, tzw. MEROZYGOTY (postać komórki, w której DNA nowy jest już w komórce, ale nie ulega integracji z DNA starym), rekombinacji genetycznej prowadzącej do integracji do genomu biorcy fragmentu DNA pochodzącego do dawcy.
Do transdukcji i koniugacji transformacja różni się tym, że DNA zostaje aktywnie pobrany przez komórkę ze środowiska bez pośrednictwa fagów, jak to ma miejsce w transdukcji, ani bez kontaktu dwóch typów komórek, jak w przypadku koniugacji.
Transformacja została opisana przez Griffith'a, który wykazał, że bakterie, które tworzą tzw. gładki typ kolonii, tj. Diplococcus pneumoniae (dwoinka zapalenia płuc) oznaczył jako S i stwierdził, że te bakterie są wirulentnymi (zakaźnymi) i inwazyjnymi. Mają one otoczki, w skład których wchodzą wielocukry i nadają poszczególnym szczepom specyficzne własności antygenowe. Ze szczepów S mogą w specyficznych warunkach na drodze mutacji powstać szczepy tzw. szorstkie R. Szczepy te nie wytwarzają otoczek i są nie wirulentne (nie zakaźne).
Wykazał on, że jeżeli do hodowli bakterii szczepu R doda się cząsteczkę DNA z bakterii szczepu S uzyska się pewien niewielki procent komórek R stransformowanych. Oznacza to, że jedynie DNA ma własności transformujące. Jeżeli chcielibyśmy stransformować dwie cechy i transformować je jednocześnie, to bakterie, które ulegną transformacji zazwyczaj nabywają tylko jedną cechę dawcy.
Komórka podczas transformacji ma zdolność transformacji bardzo niewielkiej części łańcucha DNA (0,01 długości). Wobec tego dwa geny leżące daleko od siebie w genomie bakteryjnym będą zawsze znajdowały się w odrębnych fragmentach DNA wbudowywując się do genomu biorcy i dlatego komórka nabiera tylko jednej cechy. Wspólnej transformacji ulegają geny tzw. sprzężone, mające szanse znaleźć się w jednym fragmencie stransformowanego DNA. Geny sprzężone leżą bardzo blisko siebie i komórka może nabyć dwie lub więcej cech.
Na wydajność transformacji mają wpływ cechy hodowlane: pH, temperatura i skład pożywki.
TRANSFEKCJA - polega na tym, że bakteriofagi zawierające DNA mogą w komórce bakteryjnej występować w stanie autonomicznym lub mogą być zintegrowane z genomem bakterii. Takim fagiem jest fag umiarkowany λ oraz czynnik płciowy F. Mogą one występować w komórce bakteryjnej w stanie autonomicznym w cytoplazmie - jest nie zależny od DNA bakteryjnego. Może być włączony do DNA bakteryjnego, jako stały jego składnik i wówczas nosi postać profaga. Replikuje się on wtedy synchronicznie wraz z DNA bakteryjnym. W obu przypadkach obecność zintegrowanego wirusa czy czynnika F powoduje nieobecność na terenie cytoplazmy autonomicznych fagów czy czynników F. Tego rodzaju cząsteczki, które występują w komórce w dwóch postaciach alternatywnych (autonomicznej i zintegrowanej z DNA bakterii) noszą nazwę EPISOM. Proces integracji faga λ lub czynnika F jest procesem odwracalnym. Profagi mogą być na skutek indukcji uwalniane z DNA bakteryjnego i mogą stać się fagiem wegetatywnym.
Okazało się również, że integracja czynnika F do DNA bakteryjnego w pewnych typach bakterii oznaczanych Hfr jest odwracalna, czyli czynnik F może być oddzielony od DNA bakterii i może być czynnikiem autonomicznym w cytoplazmie. Przypuszcza się, że mechanizm włączania episomów do DNA bakterii jak i przechodzenie ich w stan autonomiczny jest procesem zbliżonym do zjawiska występującego u organizmów eukariotycznych zwanym procesem crossing - over (wymiana fragmentów genów).
„Odłączone” episomy mogą czasami wymieniać odcinek własnego DNA na DNA bakteryjne. Jeżeli tego rodzaju episom, fag lub czynnik F dostanie się do następnej komórki to przenosi on także znajdujące się w nim fragmenty DNA poprzedniego gospodarza bakteryjnego. Episomy mogą być czynnikami przenoszącymi materiał genetyczny z jednych szczepów do drugich.
TRANSPOZYCJA - polega na przeniesieniu genu z jednego genoforu na inny lub na przeniesieniu genu z jednego miejsca na inne w obrębie tego samego genoforu. Prowadzi to do powstania nowych genoforów i innych genomów o odmiennej niż pierwotna sekwencji nukleotydów.
KLONOWANIE
KLON - potomstwo jednego osobnika o identycznym składzie genotypowym i powstałym na drodze rozmnażania bezpłciowego.
Klonowanie bakterii wykorzystuje rekombinację w warunkach laboratoryjnych. Polega to na tworzeniu zupełnie nowych kombinacji genów. Utworzone geny są następnie wprowadzane do odpowiednich komórek, są wielokrotnie powielane w komórce gospodarza przez syntezę DNA.
40
Cykl Krebsa
Łańcuch
Oddechowy
(fosforylacja
oskydatywna)
I etap
II etap
III etap
Wyszukiwarka
Podobne podstrony:
Ściąga PLP wykład, ZIP sem VI, PLP
WYKŁADY-fabian-sem-VI, mm005
Zagadnienia egzaminacyjne wg wykładówz KB sem VI inż r ak 14 15
Mechanika Budowli Sem[1][1] VI Wyklad 04
VI- Małopolska, LEŚNICTWO SGGW, MATERIAŁY LEŚNICTWO SGGW, Urządzanie, Wykłady, PROJEKTY sem 8 Rok Ak
Mechanika Budowli Sem[1][1] VI Wyklad 02 color
Konstrukcje metalowe Sem VI Wyklad 02
pijarski, Politechnika Lubelska, Studia, Studia, sem VI, VI-semestr, SJESJA, Sieci-wyklady, sieci-ma
odpowiedzi nie wszystkie, Politechnika Lubelska, Studia, Studia, sem VI, VI-semestr, SJESJA, Sieci-w
Zarządzanie jakością w projektowaniu QFD, Uczelnia, sem VI, zarządzanie jakością produkcji, wykład
Mechanika Budowli Sem[1][1] VI Wyklad 01
wyklad 2 (28.11.2010), Zarządzanie, sem VI marketing, Zarządzanie projektami, wykłady
Konstrukcje metalowe Sem VI Wyklad 04
Silnki, AM Gdynia, Sem. V,VI, Okrętowe silniki spalinowe - wykład
Konstrukcje metalowe Sem VI Wyklad 03
wyklad 4 (29.01.2011), Zarządzanie, sem VI marketing, Zarządzanie projektami, wykłady
Wykład praca impulsowa T, Politechnika Lubelska, Studia, Studia, sem VI, energoelektronika, Energoel
Mechanika Budowli Sem[1][1] VI Wyklad 05
więcej podobnych podstron