
1
Wydział Inżynierii Materiałowej i Ceramiki
Akademii Górniczo-Hutniczej w Krakowie
kierunek: Technologia Chemiczna
Materiały pomocnicze do zajęć seminaryjnych z przedmiotu
„CHEMIA ORGANICZNA”
Opracowanie:
dr inż. Edyta Stochmal
Kraków 2011

2
SPIS TREŚCI
Str.
1. Wskazówki dotycz
ące nazewnictwa wybranych grup
zwi
ązków organicznych ............................................................................... 3
2. Seminarium, cz
ęść I: Budowa i nazewnictwo związków organicznych ..... 17
3. Seminarium, cz
ęść II: Reakcje związków organicznych ............................ 36

Zasady nazewnictwa
3
1. WSKAZÓWKI DOTYCZĄCE NAZEWNICTWA
WYBRANYCH GRUP ZWIĄZKÓW ORGANICZNYCH
1. Alkany
(zawieraj
ą jedynie wiązania pojedyncze C-H i C-C)
Nazwy alkanów maj
ą końcówkę –an. Ich ogólny wzór to C
n
H
2n+2
(n-dowolna liczba
całkowita).
Nazwy pierwszych dziesi
ęciu alkanów normalnych (o strukturze prostołańcuchowej):
Liczba atomów
Nazwa
Wzór C
n
H
2n+2
w
ęgla (n)
1
metan
CH
4
CH
4
2
etan
C
2
H
6
CH
3
CH
3
3
propan
C
3
H
8
CH
3
CH
2
CH
3
4
butan
C
4
H
10
CH
3
CH
2
CH
2
CH
3
5
pentan
C
5
H
12
CH
3
CH
2
CH
2
CH
2
CH
3
6
heksan
C
6
H
14
CH
3
CH
2
CH
2
CH
2
CH
2
CH
3
7
heptan
C
7
H
16
CH
3
CH
2
CH
2
CH
2
CH
2
CH
2
CH
3
8
oktan
C
8
H
18
CH
3
CH
2
CH
2
CH
2
CH
2
CH
2
CH
2
CH
3
9
nonan
C
9
H
20
CH
3
CH
2
CH
2
CH
2
CH
2
CH
2
CH
2
CH
2
CH
3
10
dekan
C
10
H
22
CH
3
CH
2
CH
2
CH
2
CH
2
CH
2
CH
2
CH
2
CH
2
CH
3
Nazwy niektórych grup alkilowych:
–CH
3
metyl (Me)
–CH
2
CH
3
etyl (Et)
–CH
2
CH
2
CH
3
propyl (Pr)
–CH
2
CH
2
CH
2
CH
3
butyl (Bu)
|
CH
3
CHCH
3
izopropyl (i-Pr)
CH
3
CH
3
CH
3
C
tert-butyl (t-Bu)
Zasady nazewnictwa
4
Alkany rozgałęzione
Ogólne zasady nazewnictwa alkanów rozgał
ęzionych:
1. Nale
ży znaleźć najdłuższy łańcuch węglowy – łańcuch główny.
2. Ponumerowa
ć atomy węgla w łańcuchu głównym rozpoczynając od końca najbliższego
rozgał
ęzienia. W przypadku usytuowania pierwszych rozgałęzień w równych
odległo
ściach od obydwu końców kierować się pozycją kolejnego rozgałęzienia.
3. Poda
ć położenie i nazwę podstawników wymieniając je w kolejności alfabetycznej.
4. Dla identycznych podstawników poda
ć krotność ich występowania za pomocą
odpowiednich przedrostków: di-, tri-, tetra- itd.
5. Podstawnikom alkilowym nada
ć odpowiednie nazwy reszt węglowodorowych:
etylo-, metylo- itp.
6. Podstawnik zło
żony nazywany jest tak, jak gdyby sam był związkiem, zgodnie
z powy
ższymi regułami, rozpoczynając numerowanie od punktu dołączenia do łańcucha
głównego. Nazw
ę tego podstawnika umieszcza się w nawiasie poprzedzonym zapisem
numeru okre
ślającego jego położenie w łańcuchu głównym.
2. Cykloalkany
Do nazwy macierzystego w
ęglowodoru o budowie łańcuchowej dodaje się przedrostek cyklo-.
Podstawniki wymienia si
ę w kolejności alfabetycznej ze wskazaniem ich położenia podając
numer w
ęgla, przy którym są położone.
CH
3
CH
2
CCH
2
CHCH
3
CH
3
CH
3
CH
2
CH
3
4-etylo-2,4-dimetyloheksan
CH
3
CH
2
CHCHCH
2
CHCH
2
CH
3
CH
3
CH
2
CH
3
CH
2
CH
3
3,6-dietylo-4-metylooktan
CH
3
CH
2
CH
3
1-etylo-3-metylocykloheksan

Zasady nazewnictwa
5
3. Alkeny
(zawieraj
ą wiązanie podwójne C=C)
(Reguły podobne jak dla alkanów)
Nazwy alkenów maj
ą przyrostek –en poprzedzony numerem atomu węgla wskazującego
poło
żenie wiązania podwójnego i są pochodnymi nazw alkanów. Ich ogólny wzór to C
n
H
2n
.
Przy numerowaniu ła
ńcucha głównego pierwszeństwo ma położenie wiązania podwójnego.
Atomy w
ęgla przy podwójnym wiązaniu otrzymują możliwie najniższe numery, a pozycję
wi
ązania podwójnego wskazuje się umieszczając w nazwie numer atomu węgla o niższym
indeksie.
Nazwy zwi
ązków z dwoma podwójnymi wiązaniami mają końcówkę –dien, z trzema
–trien z okre
śleniem położenia.
4. Cykloalkeny
(Reguły podobne jak dla cykloalkanów)
Numerowanie rozpoczyna si
ę tak, by wiązanie podwójne było miedzy węglem C1 i C2 i aby
pierwszy podstawnik miał jak najni
ższy numer.
5. Alkiny
(zawieraj
ą wiązanie potrójne C
≡
C)
(Reguły podobne jak dla alkanów i alkenów)
Nazwy alkinów maj
ą przyrostek –in lub –yn poprzedzony numerem atomu węgla
wskazuj
ącego położenie wiązania potrójnego i są pochodnymi nazw alkanów. Ich ogólny
wzór to C
n
H
2n-2
.
CH
2
CHCHCH
3
CH
3
3-metylobut-1-en
CH
3
CH
CHCH
2
CH
2
CH
3
heks-2-en
CH
3
1-metylocyklopenten
CH
3
C
CCH
3
but-2-yn
CH
3
CHCH
2
CH
2
C
CH
CH
3
5-metyloheks-1-yn

Zasady nazewnictwa
6
W przypadku zwi
ązków zawierających wiązanie podwójne i potrójne numerowanie łańcucha
rozpoczyna si
ę od końca bliższego pierwszego wiązania wielokrotnego, bez różnicy, czy jest
to wi
ązanie podwójne, czy potrójne.
6. Halogenki alkilowe, R-X
(X = F, Cl, Br, I)
(Reguły podobne jak dla węglowodorów alifatycznych)
Fluorowiec traktowany jest jako podstawnik. Numerowanie ła
ńcucha głównego rozpoczyna
si
ę od końca bliższego pierwszego podstawnika, obojętne czy jest to alkil, czy fluorowiec.
Je
żeli w cząsteczce obecne jest wiązanie podwójne lub potrójne, to musi ono znaleźć się
w ła
ńcuchy głównym.
Halogenki alkilowe mo
żna również nazywać traktując atom fluorowca jako grupę funkcyjną;
wówczas zamiast np. chlorometanu b
ędzie chlorek metylu, chloroetanu – chlorek etylu, 2-
bromobutanu – bromek izopropylu, itp.
7. Związki aromatyczne
(w
ęglowodory aromatyczne, halogenki arylowe i inne pochodne
benzenu)
Nazwy zwi
ązków aromatycznych jednopierścieniowych tworzy się w zależności od liczby
podstawników w pier
ścieniu.
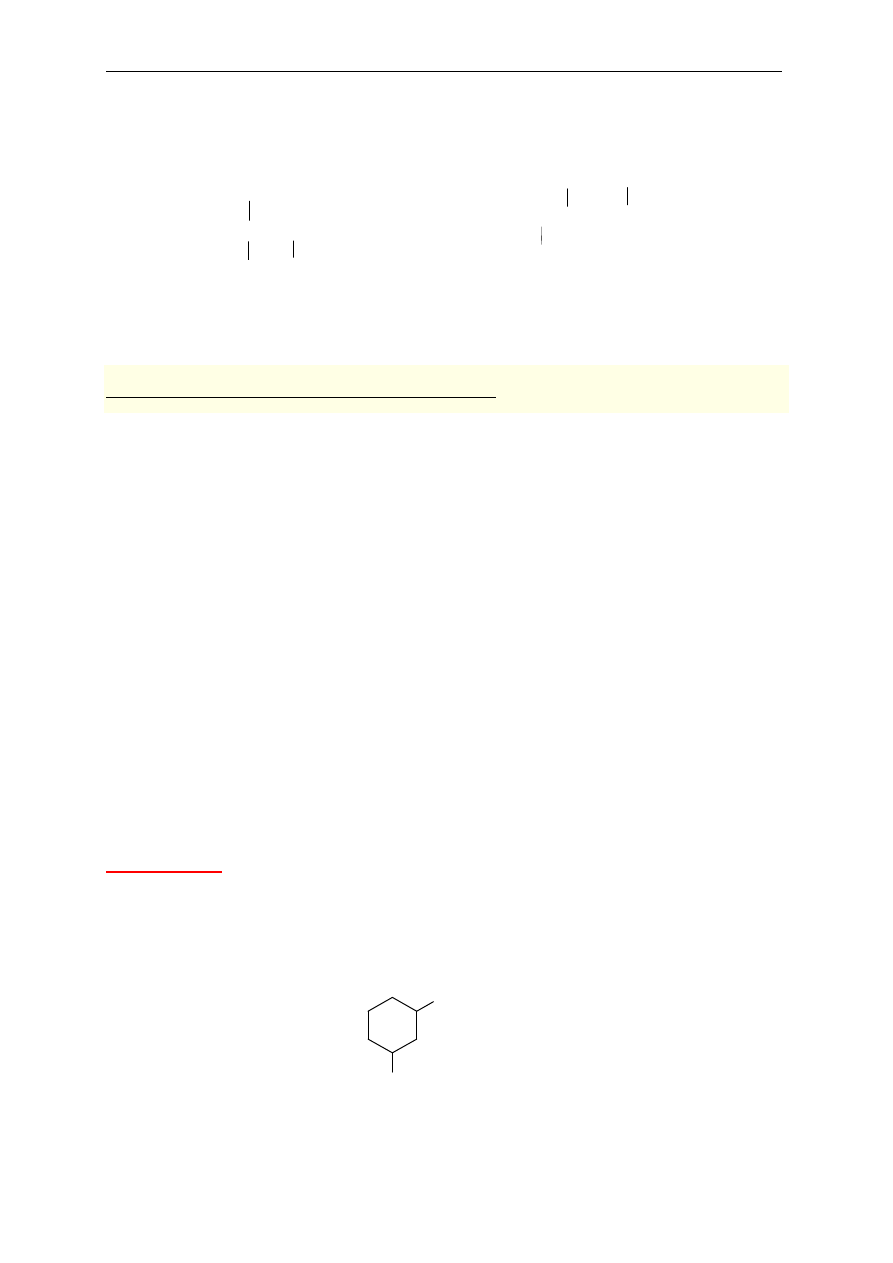
Jednopodstawione pochodne benzenu
Do podstawowej nazwy - benzen dodaje si
ę nazwę podstawnika.
CH
3
CH
CHCH
2
CHCH
2
C
CH
CH
3
4-metylookt-6-en-1-yn
CH
3
CHCH
2
CH
2
CHCH
3
CH
3
Br
2-bromo-5-metyloheksan
ClCH
2
CH
2
CHCHCH
2
CHCH
2
CH
3
CH
3
CH
2
CH
3
CH
2
CH
2
Cl
1,8-dichloro-3,6-dietylo-4-metylooktan
Zasady nazewnictwa
7
W przypadku niektórych grup jak: X = CH
3
, OH, COOH, NH
2
cz
ęsto stosuje się nazwy
zwyczajowe, odpowiednio: toluen, fenol, kwas benzoesowy, anilina.
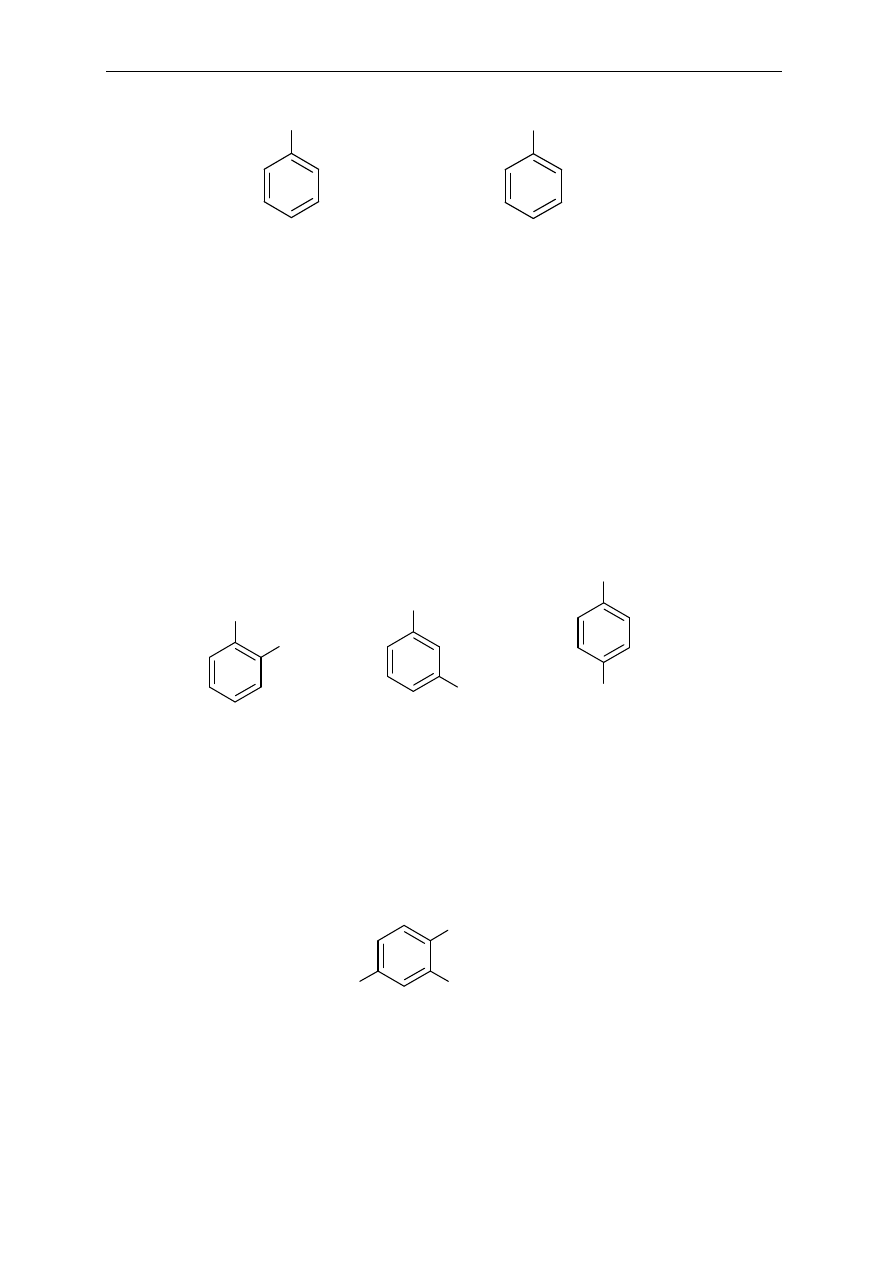
Dwupodstawione pochodne benzenu
Poło
żenia podstawników oznacza się dwojako: za pomocą liczb lub przedrostków: orto (o),
meta (
m), para (p).
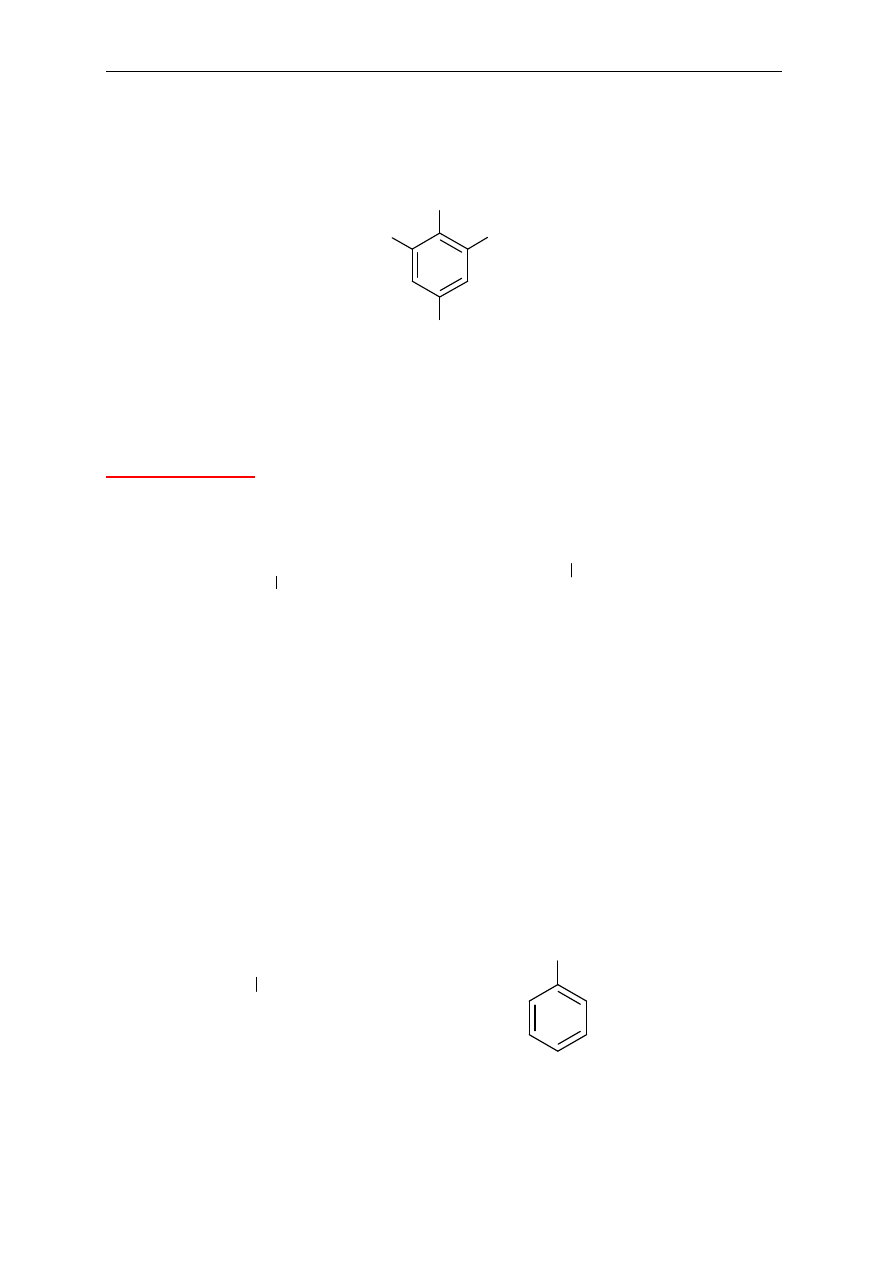
Pochodne benzenu podstawione więcej niż dwoma podstawnikami
Podstawniki wymienia si
ę w porządku alfabetycznym poprzedzając ich nazwy liczbami
wskazuj
ącymi pozycje podstawienia. Ważne jest, aby indeksy liczbowe węgli, przy których
Br
bromobenzen
Cl
Cl
Cl
CH
3
I
Br
1,2-dichlorobenzen
o-dichlorobenzen
1-bromo-4-jodobenzen
p-bromojodobenzen
3-chlorotoluen
m-chlorotoluen
Cl
NO
2
O
2
N
2-chloro-1,4-dinitrobenzen
CH
3
metylobenzen
(toluen)
Zasady nazewnictwa
8
s
ą podstawniki, były jak najniższe. W niektórych przypadkach jednopodstawiona pochodna
benzenu mo
że służyć jako nazwa podstawowa, a charakterystyczna grupa znajduje się przy
atomie w
ęgla C1.
8. Alkohole, R-OH
(charakterystyczna grupa –OH przył
ączona jest do nasyconego atomu
w
ęgla w łańcuchu alkilowym)
Tworz
ąc nazwę alkoholu za podstawową strukturę wybiera się najdłuższy łańcuch węglowy
z grup
ą hydroksylową. Do nazwy macierzystej dodaje się przyrostek –ol poprzedzony
numerem atomu w
ęgla, do którego przyłączona jest grupa –OH. Określając położenie tej
grupy istotne jest, aby indeks atomu w
ęgla był jak najniższy.
W przypadku niektórych prostych alkoholi stosuje si
ę nazwy zwyczajowe. Do słowa alkohol
dodaje si
ę nazwę grupy alkilowej lub arylowej połączonej z grupą hydroksylową, np.: alkohol
metylowy, alkohol etylowy, alkohol izopropylowy, alkohol benzylowy.
NH
2
Br
Br
Br
2,4,6-tribromoanilina
CH
3
CHCH
2
CH
3
OH
butan-2-ol
CH
3
CH
2
CHCH
2
OH
CH
3
2-metylobutan-1-ol
CH
3
CHCH
3
OH
alkohol izopropylowy
CH
2
OH
alkohol benzylowy
Zasady nazewnictwa
9
9. Fenole, ArOH
(charakterystyczna grupa –OH przył
ączona jest do pierścienia
aromatycznego)
Nazwy systematyczne fenoli tworzy si
ę dodając przedrostek hydroksy- do nazwy
w
ęglowodoru. Często używane są, w przypadku tej grupy związków, nazwy zwyczajowe.
10. Etery
(charakterystyczne wi
ązanie –C–O–C– w cząsteczce)
Etery proste, nie zawieraj
ące żadnych innych grup funkcyjnych – po słowie eter wymienia się
nazwy grup alkilowych poł
ączonych z atomem tlenu.
Etery o bardziej zło
żonej budowie – nazwę tworzy się jako pochodną macierzystego alkanu
i dodaje nazw
ę grupy alkilowej przyłączonej do atomu tlenu z końcówką –oksy.
11. Aldehydy
(charakterystyczna grupa –CHO w cz
ąsteczce)
OH
Cl
o-chlorohydroksybenzen
(o-chlorofenol)
NH
2
OH
p-aminohydroksybenzen
(p-aminofenol)
CH
3
O CH
3
CH
3
O CH
2
CH
2
Cl
eter dimetylowy
1-chloro-2-metoksyetan
CH
3
CH
2
CH
O
propanal
CH
3
CH
3
CH
2
CHCH
2
CH
O
3-metylopentanal
Zasady nazewnictwa
10
Nazw
ę aldehydu tworzy się dodając do nazwy macierzystego alkanu przyrostek –al.
Najdłu
ższy łańcuch z grupą –CHO stanowi strukturę podstawową, a atom węgla z tej grupy
oznacza si
ę jako C1.
W przypadku niektórych prostych aldehydów stosuje si
ę nazwy zwyczajowe, np.:
formaldehyd, benzaldehyd.
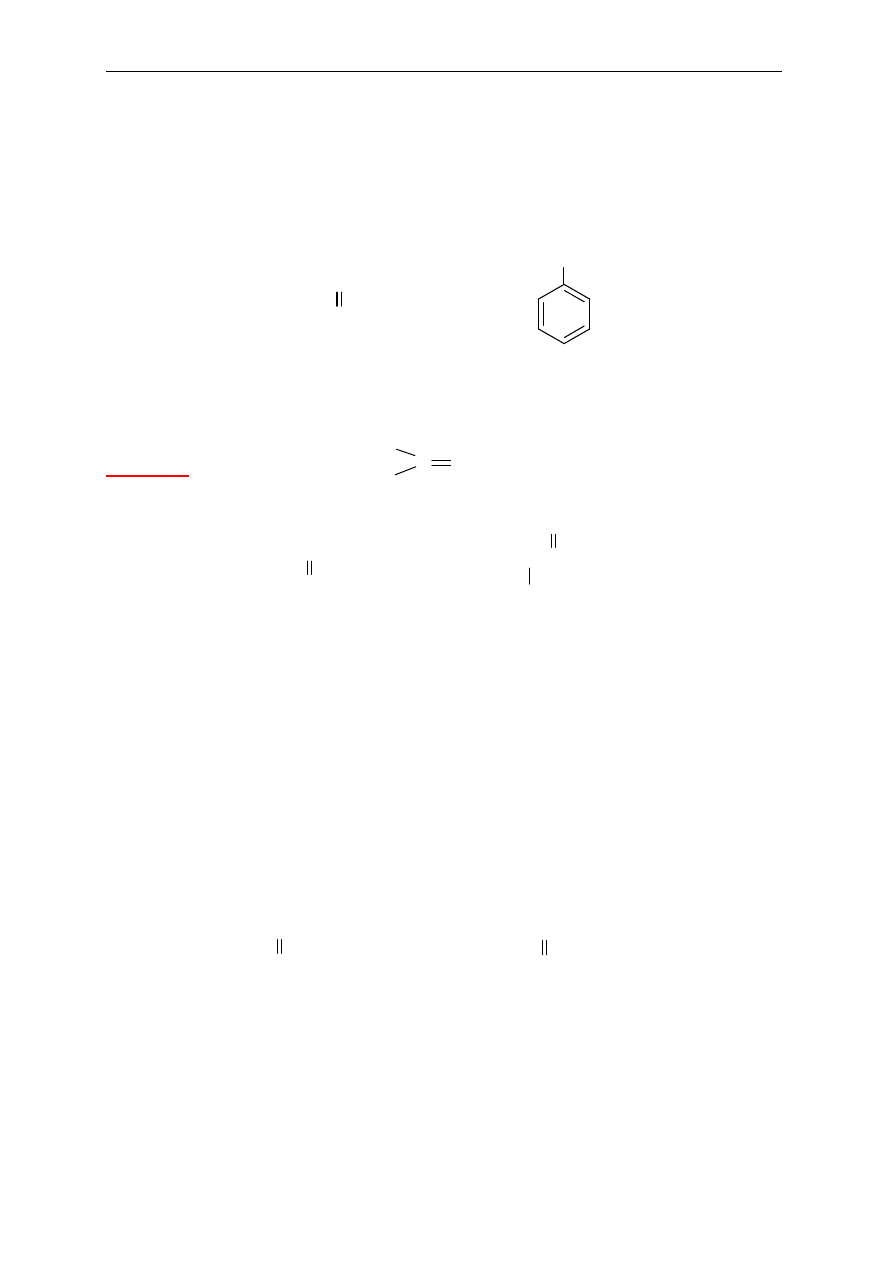
12. Ketony
(charakterystyczna grupa
w cz
ąsteczce)
Nazw
ę ketonów tworzy się od nazwy macierzystego alkanu dodając przyrostek –on
poprzedzony numerem atomu w
ęgla z grupą karbonylową. Najdłuższy łańcuch z grupą
ketonow
ą uznaje się za strukturę podstawową, a numerowanie atomów węgla rozpoczyna się
od ko
ńca bliższego karbonylowego atomu węgla.
W przypadku niektórych prostszych zwi
ązków z tej grupy nazwy tworzy się wymieniając
w kolejno
ści alfabetycznej nazwy grup połączonych z grupą karbonylową poprzedzając je
słowem „keton”.
CHO
benzaldehyd
HCH
O
formaldehyd
CH
3
CH
2
CH
2
CCH
3
O
pentan-2-on
CH
3
CH
2
CCH
3
O
butan-2-on
(keton etylowo-metylowy)
CH
3
CHCCH
3
O
CH
3
3-metylobutan-2-on
O
C
CH
3
CCH
3
O
propanon
(keton dimetylowy,
aceton)
Zasady nazewnictwa
11
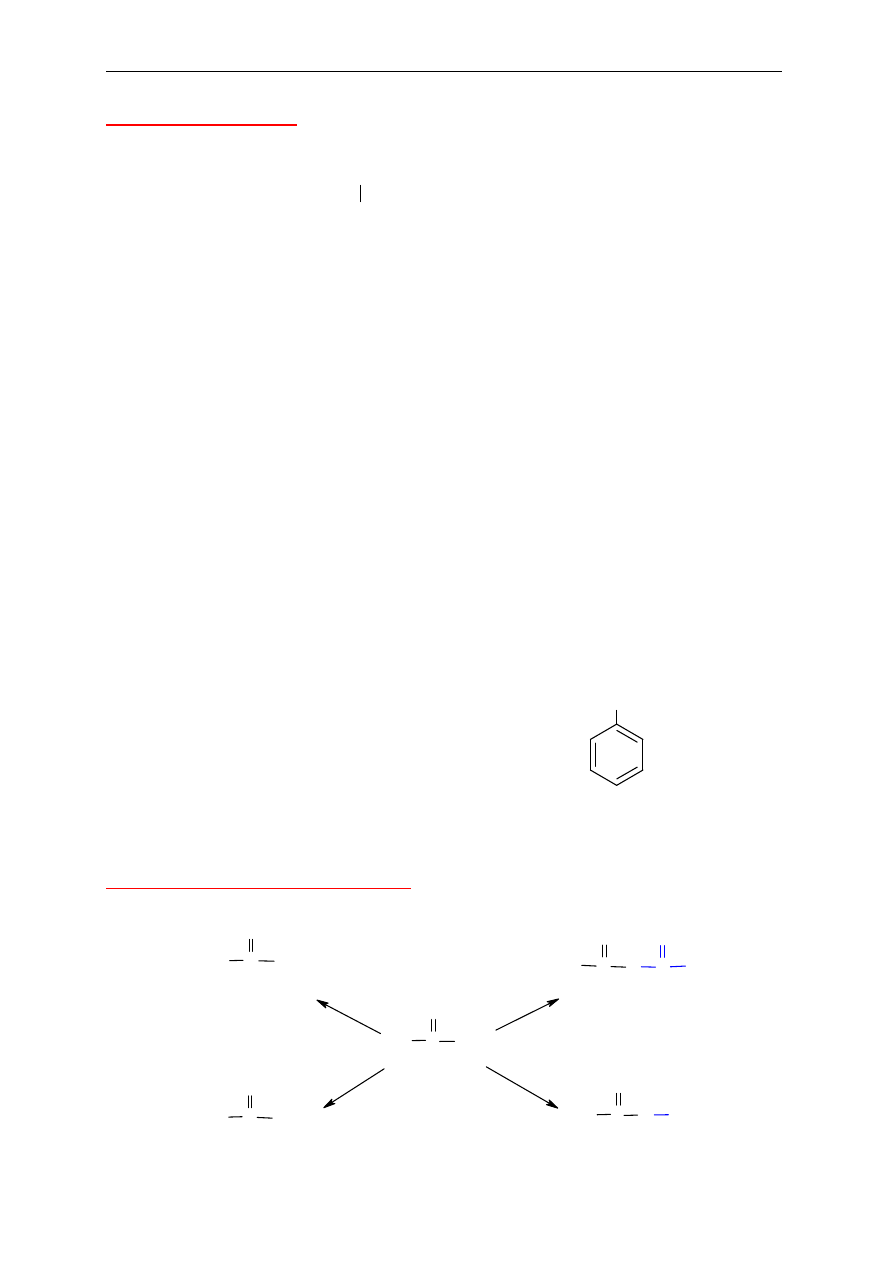
13. Kwasy karboksylowe
(charakterystyczna grupa –COOH w cz
ąsteczce)
Nazwy systematyczne kwasów karboksylowych tworzy si
ę dwojako:
1
o
sposób
Do nazwy macierzystego alkanu z ko
ńcówką –owy dodaje się słowo kwas, a atom węgla
w grupie karboksylowej jest oznaczany jako C1.
2
o
sposób
Nazwa ła
ńcucha głównego nie obejmuje grupy karboksylowej, a atom węgla, do którego
przyczepiona jest grupa karboksylowa, jest oznaczany jako C1. Do nazwy macierzystego
alkanu dodaje si
ę wówczas słowo kwas i końcówkę -karboksylowy.
W przypadku tej grupy zwi
ązków stosowane są często nazwy zwyczajowe, np.: kwas
mrówkowy, octowy, propionowy, benzoesowy.
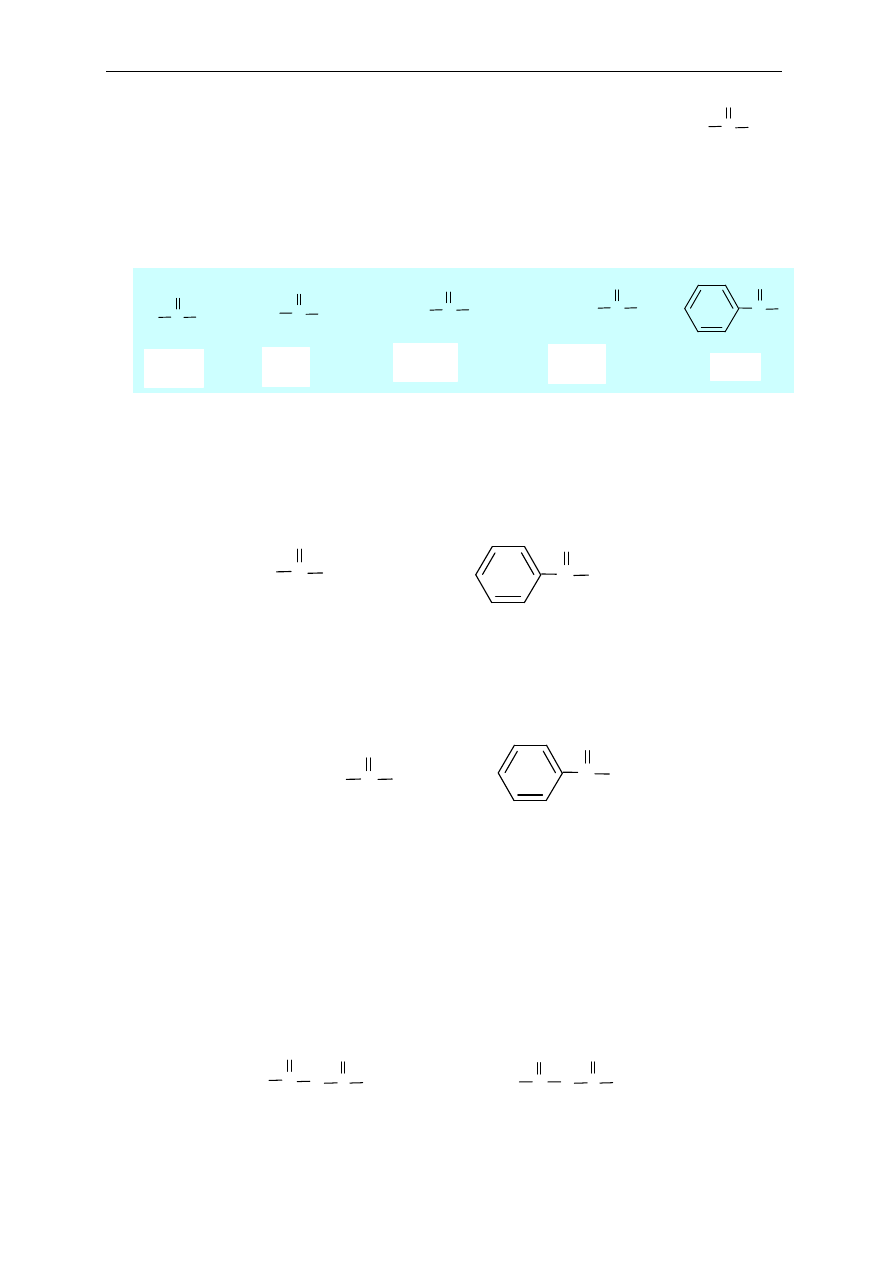
14. Pochodne kwasów karboksylowych
(halogenki kwasowe, bezwodniki kwasowe, estry,
amidy)
CH
3
CH
3
CHCH
2
COOH
kwas 3-metylobutanowy
kwas 2-metylopropanokarboksylowy
COOH
kwas benzoesowy
HCOOH
kwas mrówkowy
CH
3
COOH
kwas octowy
R C
O
OH
R C
O
X
R C
O
O
O
R
C
R C
O
O R'
R C
O
NH
2
Kwas
Halogenek
kwasowy
Bezwodnik
kwasowy
Ester
Amid
Zasady nazewnictwa
12
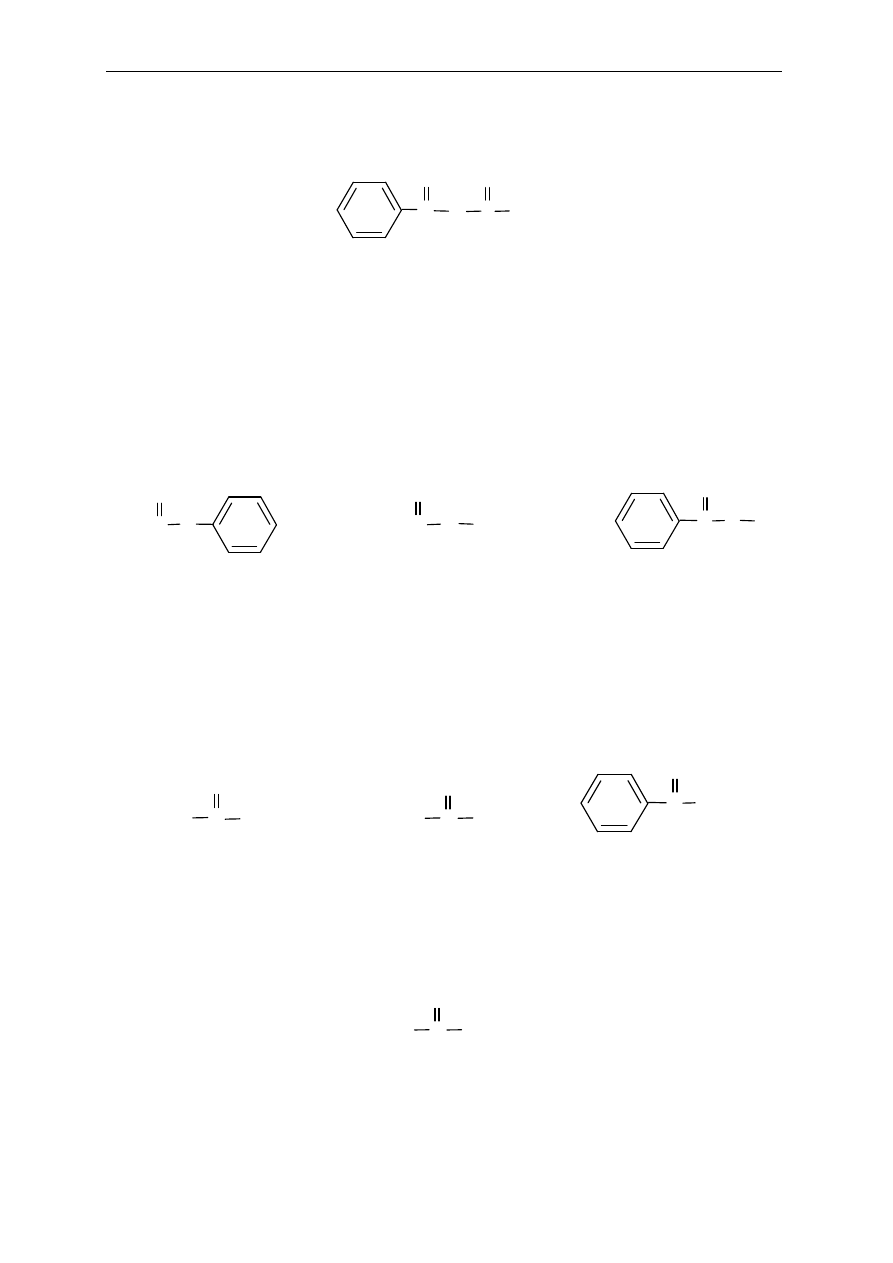
Pochodne kwasów karboksylowych zawieraj
ą charakterystyczną grupę acylową
.....
Nazw
ę tej grupy tworzy się od nazwy macierzystego alkanu dodając końcówkę –oil lub
stosuj
ąc nazwy zwyczajowe.
Przykłady grup acylowych:
Halogenki kwasowe
Nazwy halogenków kwasowych tworzy si
ę podając nazwę odpowiedniego halogenku i grupy
acylowej (systematyczn
ą lub zwyczajową).
Zwi
ązki te można również nazywać w oparciu o nazwę kwasu macierzystego poprzedzając ją
nazw
ą odpowiedniego halogenku.
Bezwodniki kwasowe
W przypadku bezwodników symetrycznych (otrzymywanych z takiego samego kwasu
karboksylowego) nazwy tworzy si
ę, zastępując słowo kwas słowem bezwodnik lub dodając
słowo bezwodnik do nazwy macierzystego kwasu.
R C
O
CH
3
C
O
O
C
Cl
Br
Chlorek etanoilu
Chlorek acetylu
Bromek benzoilu
CH
3
CH
2
C
O
Br
O
C Cl
Bromek kwasu
propanowego
Chlorek kwasu
benzoesowego
CH
3
CH
2
C
O
O C CH
2
CH
3
O
CH
3
C
O
O C CH
3
O
Bezwodnik kwasu propanowego
Bezwodnik octowy
CH
3
CH
2
C
O
CH
3
C
O
H C
O
CH
3
CH
2
CH
2
C
O
O
C
Metanoil
Formyl
Etanoil
Acetyl
Propanoil
Propionyl
Butanoil
Butyryl
Benzoil
Zasady nazewnictwa
13
Bezwodniki niesymetryczne (otrzymywane z ró
żnych kwasów karboksylowych) nazywa się
podobnie, przy czym nazwy kwasów podaje si
ę w porządku alfabetycznym.
Estry
W nazwie estru okre
śla się część kwasową i alkilową (wprowadzoną w miejsce atomu
wodoru w kwasie). Cz
ęść kwasowa ma końcówkę –an lub –ian zamiast końcówki –owy
wyst
ępującej w nazwie kwasu macierzystego, część alkilowa natomiast podawana jest
w dopełniaczu.
Amidy
Nazwy amidów tworzy si
ę, dodając do nazwy macierzystego alkanu końcówkę –oamid
lub zamieniaj
ąc końcówkę –yl (-oil) w nazwie grupy acylowej na przyrostek –amid.
Zwi
ązki te można także określać poprzedzając nazwę macierzystego kwasu karboksylowego
słowem
amid.
O
C
O C CH
3
O
Bezwodnik benzoesowo-octowy
CH
3
CH
2
C
O
O
CH
2
CH
3
O
C
CH
3
O
CH
3
C
O
O
Propanian etylu
Benzoesan metylu
Octan fenylu
CH
3
CH
2
CH
2
C
O
CH
3
C
O
NH
2
NH
2
O
C NH
2
Acetamid
Butanoamid
Benzamid
CH
3
CH
2
C
O
NH
2
Amid kwasu propanowego

Zasady nazewnictwa
14
W przypadku amidów podstawionych najpierw okre
śla się podstawniki przy atomie azotu
a nast
ępnie podaje nazwę amidu macierzystego. Nazwę podstawników poprzedza się
lokantem „N” co oznacza bezpo
średnie podstawienie przy atomie azotu.
15. Nitrozwiązki
(charakterystyczna grupa –NO
2
w cz
ąsteczce)
Do nazwy macierzystego w
ęglowodoru dodaje się przedrostek nitro-. Grupę nitrową traktuje
si
ę jako podstawnik, a jej pozycję podaje się wymieniając numer atomu węgla,
z którym jest ona zwi
ązana.
16. Aminy
Aminy alifatyczne
Aminy pierwszorzędowe (charakterystyczna grupa —NH
2
w cz
ąsteczce)
Nazwy tworzy si
ę przez dodanie przyrostka –amina do nazwy podstawnika alkilowego.
Amin
ę można potraktować również jako pochodną węglowodoru, zwłaszcza
w przypadku amin zawieraj
ących inne grupy funkcyjne. Wówczas grupę -NH
2
mo
żna
wymieni
ć jako podstawnik aminowy oraz określić jego pozycję w związku macierzystym.
CH
3
CH
2
CH
2
NO
2
1-nitropropan
CH
2
CH
2
NH
2
etyloamina
CH
3
CH
2
CHCOOH
NH
2
kwas 2-aminobutanowy
CH
3
CH
2
CH
2
CHCH
3
NH
2
2-aminopentan
CH
3
C
O
N
H
H C
O
N(CH
3
)
2
N-fenyloacetamid
N,N-dimetyloformamid (DMF)
Zasady nazewnictwa
15
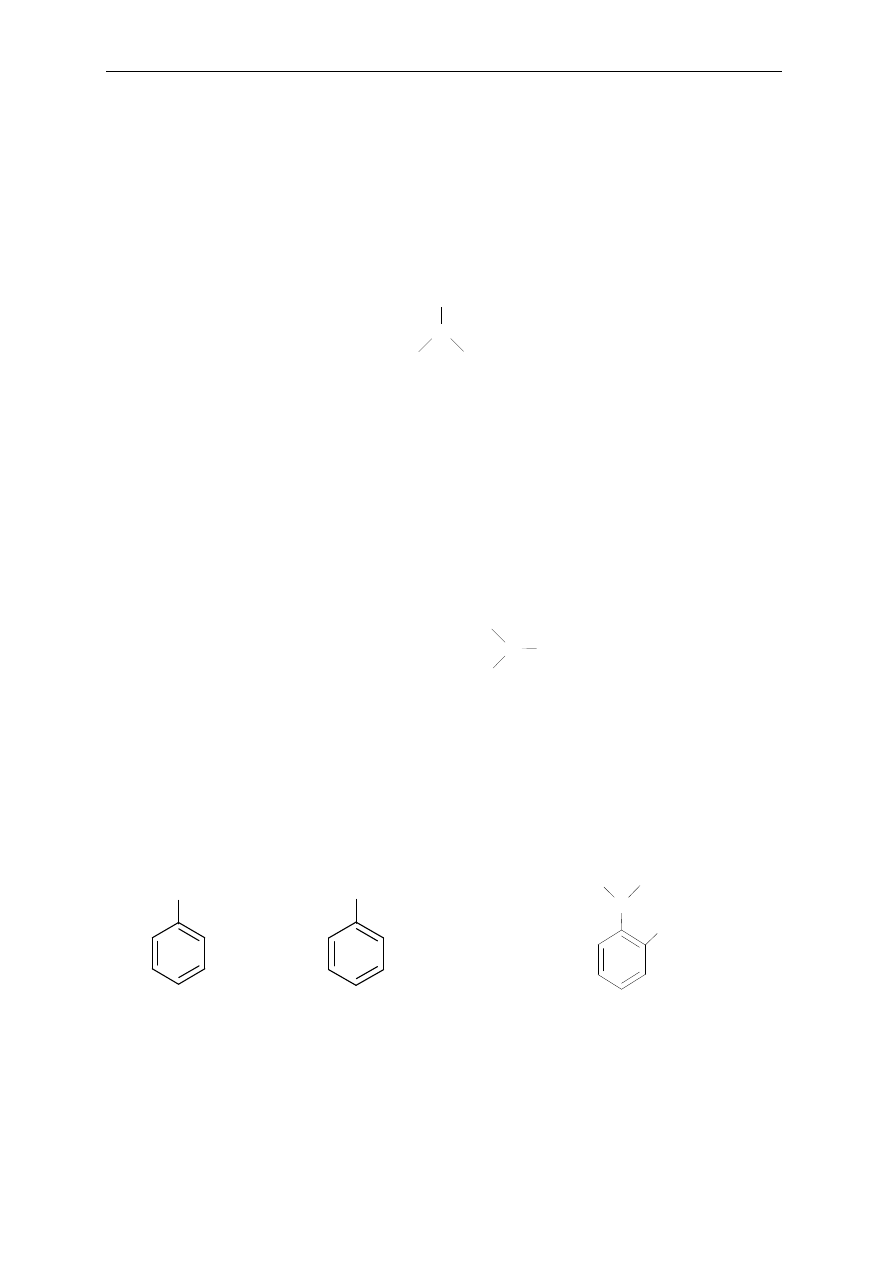
Aminy drugorzędowe i trzeciorzędowe (charakterystyczne grupy w cząsteczce,
odpowiednio: —NH— lub —N— )
│
W przypadku symetrycznych amin do nazwy dodaje si
ę przedrostek di- lub tri-, np.:
difenyloamina, trietyloamina.
Aminy niesymetryczne drugorz
ędowe i trzeciorzędowe nazywa się jako N-podstawione
aminy pierwszorz
ędowe. Nazwę największej grupy alkilowej wybiera się za nazwę
macierzyst
ą, a pozostałe grupy traktuje jako N-podstawniki (dołączone do atomu azotu).
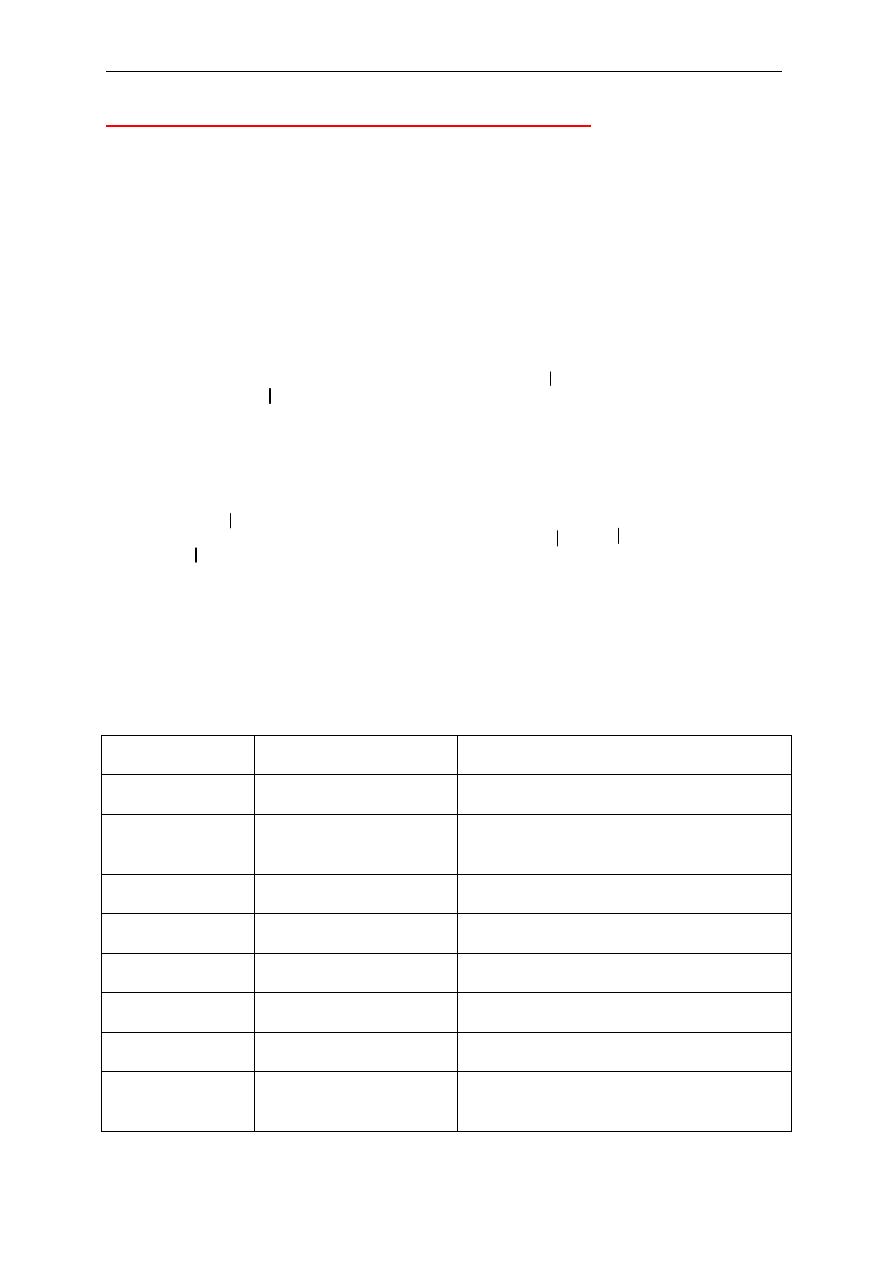
Aminy aromatyczne
Aminy aromatyczne traktuje si
ę jako pochodne aniliny (aminobenzen), a pozostałe grupy
jako N-podstawniki.
CH
2
CH
3
N
CH
2
CH
3
CH
3
CH
2
trietyloamina
CH
3
CH
2
CH
2
NHCH
3
N-metylopropyloamina
CH
3
CH
N
CHCH
2
CH
2
CH
3
CH
3
N-etylo-N-metylobutyloamina
N
Br
CH
3
CHCH
3
2-bromo-N-etylo-N-metyloanilina
NH
2
anilina
NHCH
3
N-metyloanilina
Zasady nazewnictwa
16
17. Związki zawierające w cząsteczkach różne grupy funkcyjne
Je
żeli w cząsteczce związku organicznego znajduje się kilka różnych grup funkcyjnych, to
nazw
ę systematyczną tworzy się w oparciu o zasady obowiązujące dla grupy związków
o grupie funkcyjnej maj
ącej pierwszeństwo, a inne grupy funkcyjne traktuje się jak
podstawniki.
Wybrane grupy funkcyjne, wyst
ępujące w cząsteczkach związków organicznych ułożone
według pierwsze
ństwa przedstawiono w Tabeli 1. Tabela zawiera również nazwy tych grup,
traktowanych jako podstawniki.
Przykłady:
Tabela 1. Wybrane grupy funkcyjne wyst
ępujące w związkach organicznych uszeregowane
według ich pierwsze
ństwa oraz nazwy tych grup traktowanych jako podstawniki.
Grupa funkcyjna
Klasa zwi
ązku
Nazwa podstawnika
-COOH
kwasy karboksylowe
karboksy
-COOR
estry
R-oksykarbonylo
np.
metoksykarbonylo
(R=CH
3
), etoksykarbonylo (R=C
2
H
5
) itd.
-CONH
2
amidy
karbamoilo
-CHO
aldehydy
formylo
>C=O
ketony
okso
-OH
alkohole, fenole
hydroksy
-NH
2
aminy
amino
-OR
etery
R-oksy, np. metoksy (R=CH
3
), etoksy
(R=C
2
H
5
) itd.
CH
3
CH
2
CHCOOH
NH
2
kwas 2-aminobutanowy
CH
3
CHCOOH
OH
kwas 2-hydroksypropanowy
(nazwa zwyczajowa: kwas mlekowy)
CH
2
CHCOOH
OH
NH
2
kwas 2-amino-3-hydroksypropanowy
CH
3
CHCH
2
CHCOOH
OH
OH
kwas 2,4-dihydroksypentanowy

Seminarium, część I
17
2.
Seminarium, część I:
BUDOWA I NAZEWNICTWO ZWIĄZKÓW ORGANICZNYCH
Zagadnienia
1. Klasyfikacja zwi
ązków organicznych, charakterystyczne grupy funkcyjne
2. Ogólne zasady nazewnictwa wybranych grup zwi
ązków organicznych
-
W
ęglowodory alifatyczne nasycone i nienasycone: alkany, alkeny, alkiny,
cykloalkany, cykloalkeny
-
W
ęglowodory aromatyczne (areny)
-
Halogenopochodne alkilowe i arylowe
-
Alkohole, fenole, etery
-
Aldehydy i ketony
-
Kwasy karboksylowe i ich pochodne
-
Zwi
ązki zawierające azot: związki nitrowe, aminy
3. Rz
ędowość atomów węgla, rzędowość alkoholi i amin
4. Izomeria
-
izomeria konstytucyjna (ła
ńcuchowa, położeniowa, grup funkcyjnych)
-
izomeria geometryczna (izomery
cis-trans, konfiguracja podstawników Z-E)
5. Hybrydyzacja orbitali atomowych w zwi
ązkach organicznych
6. Polaryzacja wi
ązań w związkach organicznych
Seminarium, część I
18
BUDOWA I NAZEWNICTWO ZWI ZKÓW ORGANICZNYCH
BUDOWA I NAZEWNICTWO ZWI ZKÓW ORGANICZNYCH
BUDOWA I NAZEWNICTWO ZWI ZKÓW ORGANICZNYCH
BUDOWA I NAZEWNICTWO ZWI ZKÓW ORGANICZNYCH
Zadania
1
. Klasyfikacja zwi zków organicznych
. Klasyfikacja zwi zków organicznych
. Klasyfikacja zwi zków organicznych
. Klasyfikacja zwi zków organicznych
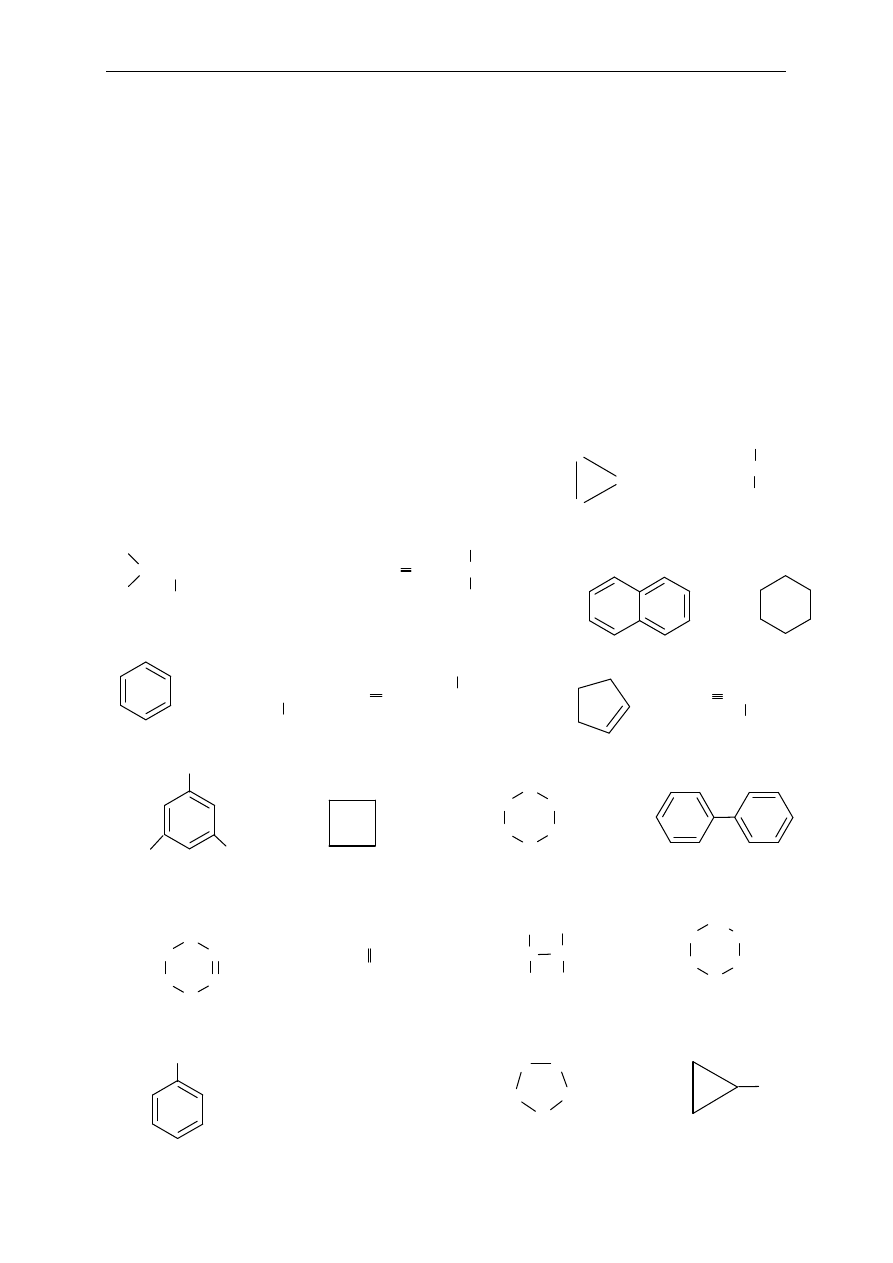
1. Przyporz
ądkuj poniższe związki do odpowiedniej grupy:
- w
ęglowodory alifatyczne lub węglowodory aromatyczne
- w
ęglowodory nasycone lub węglowodory nienasycone
- alkany, alkeny, alkiny, cykloalkany, cykloalkeny
CH
3
CH
3
CH
3
-CH=CH-CH
3
CH
3
CH
3
-C-CH
3
CH C-CH-CH
2
-CH
3
CH
3
CH
3
CH
3
-C
CH
2
=CH-CH=CH
2
CH
3
CH
3
CH
3
CH
3
C-CH
3
CH
2
CH
3
-CH
2
-C-CH
2
-CH
3
CH
3
CH-CH-CH
3
CH
3
C-CH
2
-C-CH
3
CH
3
CH
3
-CH
2
-CH
2
-C
C
H
2
C
H
2
CH
2
CH
CH
C
H
2
C
H
2
C
H
2
C
H
2
C
H
2
C
H
2
CH
2
CH
2
C
H
2
C
H
2
CH
2
C
H
2
C
H
2
C
H
2
C
H
2
CH
3
H
3
C
CH
3
CH
3
CH
3
C
H
2
C
H
2
CH
2
CH-CH
3
C
H
2
CH-CH
3
CH
3
-CH
2
-CH
2
-CH
2
-CH
2
-CH
3
CH
3
CH-CH
2
-CH-CH
3
CH
3
CH
3
-CH-CH
2
-CH
a)
b)
c)
d)
e)
f)
g)
h)
u)
v)
k)
i)
j)
l)
m)
n)
o)
p)
q)
r)
s)
t)
w)
x)
Seminarium, część I
19
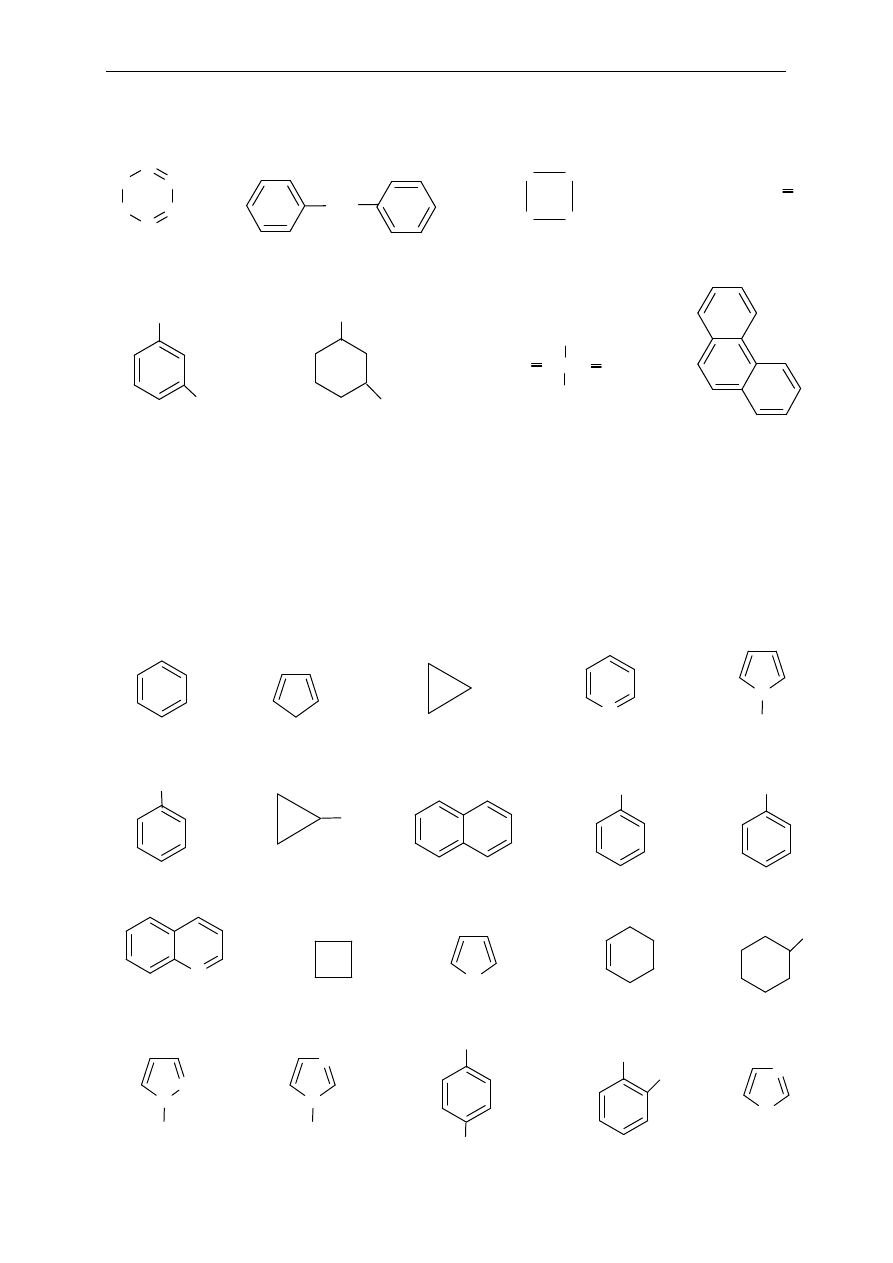
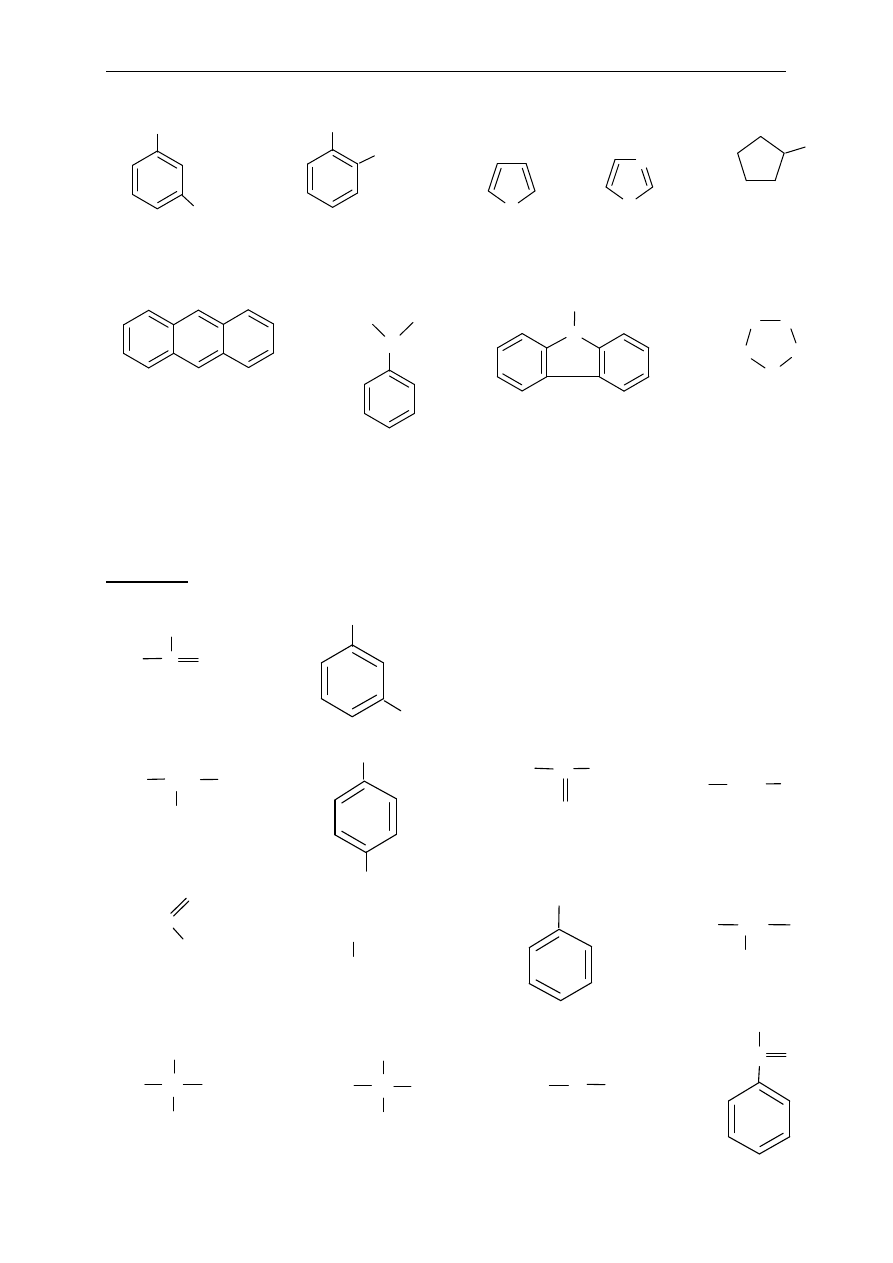
2. Które z poni
ższych związków to związki heterocykliczne, a które homocykliczne
(karbocykliczne)? W
śród homocyklicznych wskaż te, które są związkami alicyklicznymi
lub aromatycznymi.
NH
2
NO
2
NO
2
N
H
N
N
O
N
N
H
N
N
H
O
N
Cl
NH
2
Cl
CH
3
NO
2
CH
3
a)
b)
c)
d)
e)
f)
g)
h)
i)
j)
k)
l)
m)
n)
o)
p)
q)
r)
s)
t)
CH
CH
3
-CH=CH-C
CH
3
C-C-C
CH
3
CH
3
-C
CH
C
H
2
C
H
2
C
H
2
CH
2
CH
2
C
H
C
H
CH
CH
C
H
2
C
H
2
CH
3
CH
3
CH
3
CH
3
y)
z)
aa)
bb)
cc)
dd)
ee)
ff)
Seminarium, część I
20
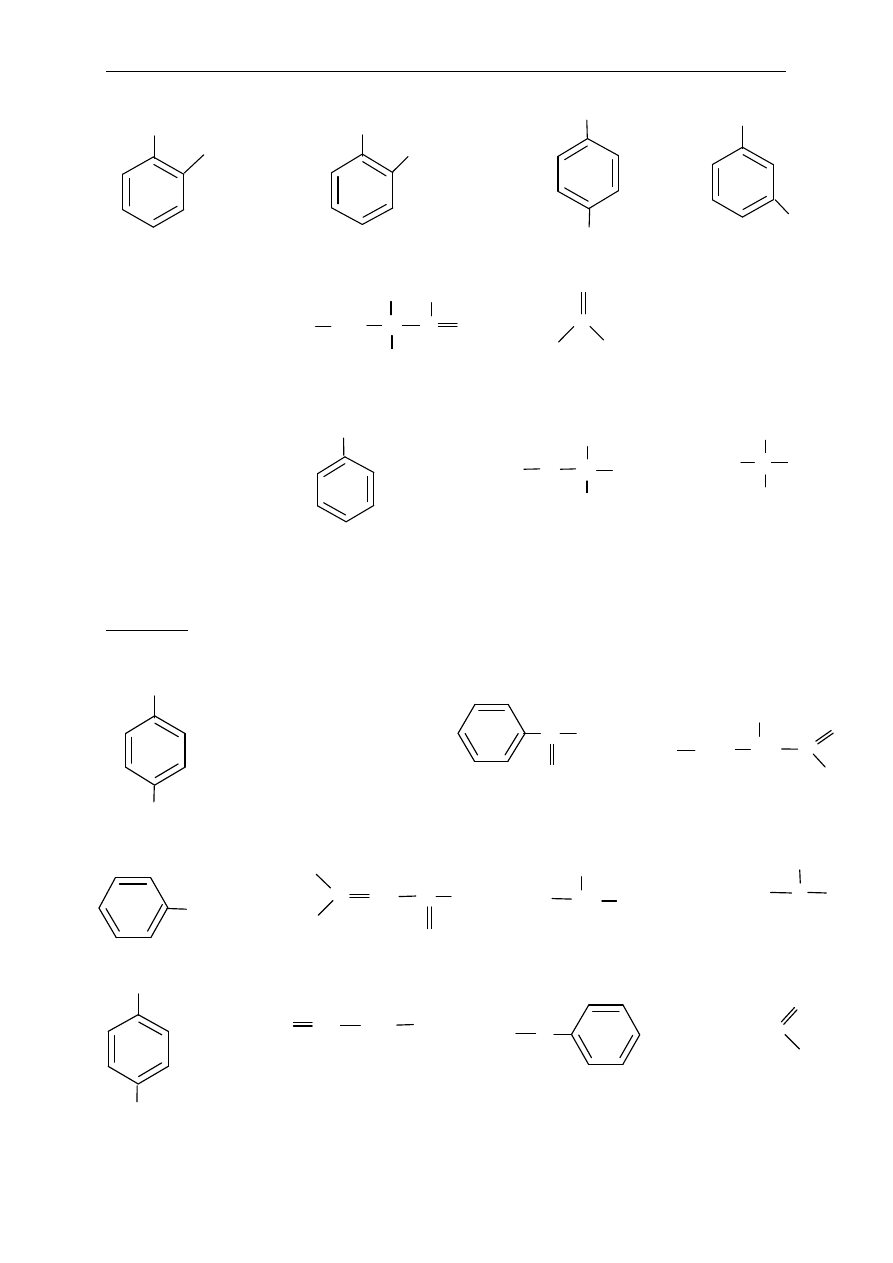
3. Na podstawie charakterystycznych grup funkcyjnych przyporz
ądkuj poniższe związki do
odpowiedniej klasy zwi
ązków organicznych:
Zestaw 3.1
CH
Br
Br
H
3
C
CH
3
S
S
N
N
H
Br
CHCl
C
H
2
C
H
2
C
H
2
C
H
2
OH
CH
3
u)
v)
w)
x)
y)
z)
aa)
bb)
cc)
NO
2
CH
3
C
O
NH
2
H
3
C
CH
3
CH
3
CH
3
-CH
2
-NO
2
NH
2
C
NH
2
Cl
H
3
C
CH
3
NH
2
CH
CH
3
CH
2
COOH
CH
3
CH
2
CH
2
OH
H
3
C
CH
3
OH
CH
CH
3
CHCH
2
OH
CH
3
CH
3
OH
H
3
C
CH
3
CH
3
OH
C
H
3
C
O
C
2
H
5
CH
3
H
C
O
CH
3
C
O
CH
3
H
C
O
a)
k)
b)
c)
d)
e)
g)
h)
j)
f)
l)
m)
n)
o)
p)
i)
Seminarium, część I
21
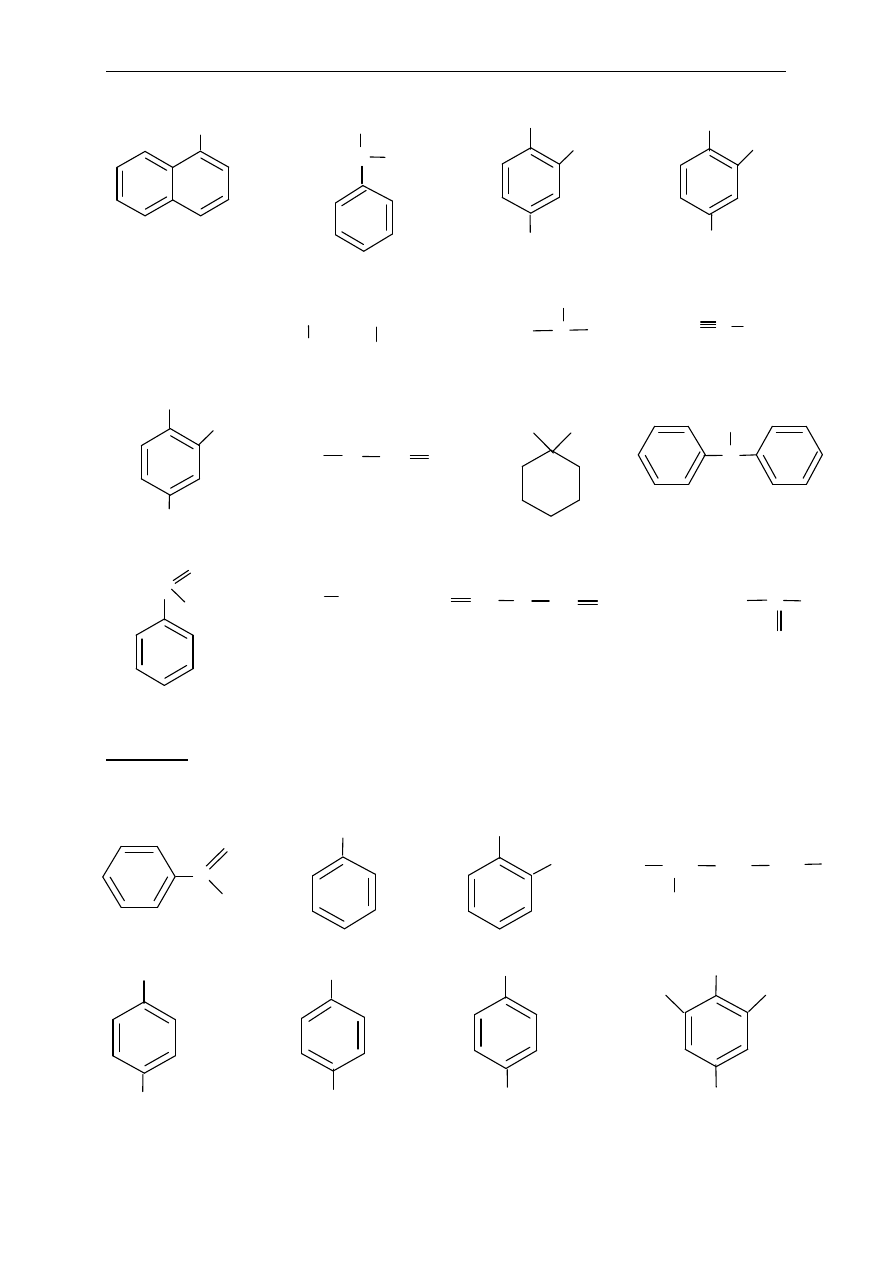
Zestaw 3.2
CH
3
NH
2
NH
2
Br
CH
3
(CH
2
)
4
NH
2
C
5
H
11
COOH
CH
3
COOH
CH
3
OH
CH
3
H
3
C
C
CH
2
H
C
O
CH
3
C
O
H
3
C
CH
2
CH
3
CH
3
CH
2
CH
2
NO
2
NHCH
3
H
3
C
CH
3
CH
3
C
COOH
CH
3
CH
3
CH
3
C
H
3
C
O
t)
q)
r)
s)
u)
v)
w)
x)
y)
z)
aa)
bb)
CH
3
(CH
2
)
4
-C
O
NH
2
N
H
CH
3
CH
3
CH
2
CH
2
NH
2
CH
3
CH
2
CH
2
COOH
CH
3
OH
O
CH
3
CH
COOH
CH
3
CH
3
CH
C
CH
2
COOH
Br
OH
OH
H
3
C
CH
2
CH
OH
H
3
C
O
CH
C
O
CH
3
C
CH
3
CH
3
C
O
CH
3
a)
b)
c)
d)
e)
f)
g)
h)
i)
j)
k)
l)
Seminarium, część I
22
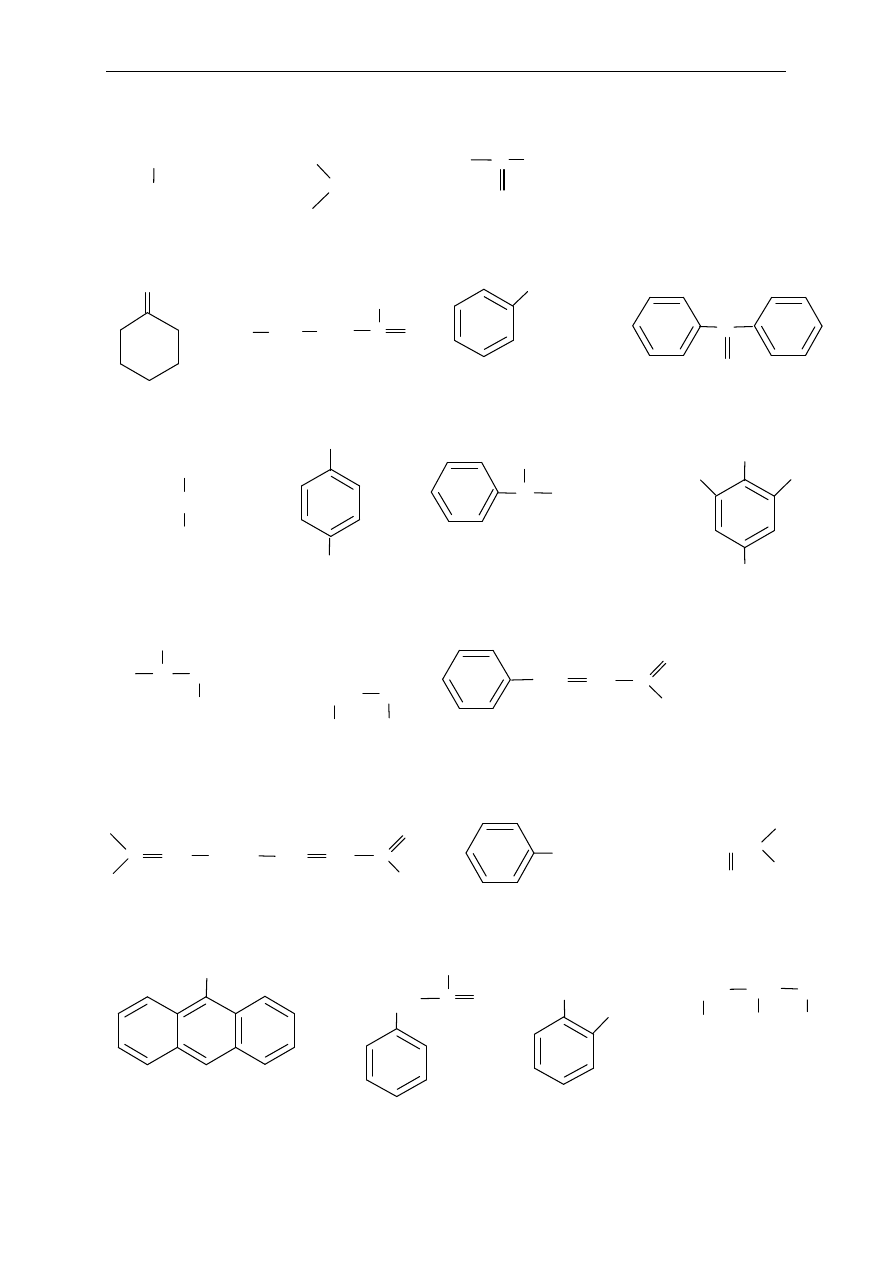
Zestaw 3.3
Cl
NO
2
NO
2
C
2
H
5
N
CH
3
COOH
NO
2
NO
2
OH
OH
O
C
Cl
CH
2
CH
2
CHCOOH
CH
3
NO
2
CH
3
N
C
3
H
7
C
2
H
5
CH
3
N
H
CH
3
(CH
2
)
3
CH
2
OH
OH
OH
OH
CH
2
OH
CH
C
CH
3
OH
CH
H
3
C
O
CH
2
CH
HC
O
CH
2
CH
2
CH
3
CH
2
CH
2
C
O
CH
3
m)
n)
o)
p)
q)
r)
u)
v)
s)
t)
w)
x)
z)
y)
aa)
bb)
COOH
NH
2
COOH
OH
COOH
Cl
CH
3
NO
2
NO
2
NO
2
C
O
NH
2
CH
3
NO
2
N(CH
3
)
2
CH
3
H
3
C
CH
2
CH
CH
2
OH
b)
a)
d)
e)
f)
g)
h)
c)
Seminarium, część I
23
OH
COOH
CH
2
CH
2
COOH
CH
3
CH=CHCOOH
CH
3
CHCOOH
COOH
CH
3
O
H-C-N
CH
3
CH
3
-CH
2
-C-CH
3
CH
3
NO
2
NH
C
2
H
5
C
2
H
5
NH
2
Br
Br
Br
N
CHCH
2
CH
3
CH
3
CH
3
CH
3
NH
2
CH
2
CH
2
NH
2
NH
2
NO
2
N
H
CH
2
CH(CH
3
)
2
OH
CH
2
CH
2
OH
CH
2
OH
CH
2
OH
CH
2
OH
CH
2
OH
CH
OH
H
3
C
CH
2
CH
2
H
C
O
CH
3
CH
2
C
O
CH
2
CH
3
H
C
O
CH
2
C
O
O
H
CH
C
O
CH
CH
C
CH
3
CH
3
(CH)
2
CH
H
CH
C
O
i)
j)
k)
l)
m)
n)
o)
p)
q)
r)
s)
t)
u)
v)
w)
x)
y)
z)
aa)
bb)
cc)
dd)
ee)

Seminarium, część I
24
2. Nazewnictwo: W glowodory
2. Nazewnictwo: W glowodory
2. Nazewnictwo: W glowodory
2. Nazewnictwo: W glowodory
4. Narysuj zwi
ązki zgodnie z nazwą:
a. 3-etylo-4,4-dimetyloheptan
b. 2,2,3,3–tetrametylopentan
c. 2,3,5-trimetylo-4-propyloheptan
d. 4–etylo–3,4,7,8–tetrametylodekan
e. 3-izopropylo-2-metylooktan
f. 1-etylo-2-metylocyklopentan
g. 2,3–dimetylobut-2-en
h. pent-2-yn
i. 2,4,4-trimetylopent-2-en
j. 3,6-dimetylookt-1-en
k. hept-3-yn
l. 5-(1,2-dimetylobutylo)-2,3,3,9-tetrametylodek-1-en
m. 3-metylocykloheksen
n. 3,4-dimetylocyklopenten
o. 1,3,5–trimetylobenzen
p. 1,3-dietylobenzen
q.
p-ksylen
5. Podaj nazwy systematyczne nast
ępujących węglowodorów:
a. (CH
3
)
2
CHCH
2
CH
2
CH(C
2
H
5
)
2
b. (C
2
H
5
)
2
C(CH
3
)CH
2
CH
3
c. CH
3
CH
2
CH(CH
3
)CH(CH
3
)CH(CH
3
)
2
d. CH
3
CH
2
CH(CH
3
)CH
2
C(CH
2
CH
2
CH
3
)(CH
2
CH
3
)
2
e. CH
3
CH
2
C(CH
3
)
2
(CH
2
)
4
CH
3
f. (CH
3
)
3
CCH
2
CH
3
g. (CH
3
CH
2
)
2
C=CH
2
h. CH
3
CH
2
CH=CHCH
2
CH
3
i. (CH
3
)
3
CCH=CH
2
j. (CH
3
)
2
CHCH=CHCH(CH
3
)
2
k. (CH
3
)
2
CHCH
2
CH=C(CH
3
)
2
l. CH
3
CH(CH
3
)C
≡
CCH(CH
3
)CH
3
m. HC
≡
CC(CH
3
)
3

Seminarium, część I
25
6. Poni
ższe nazwy nie są prawidłowe. Narysuj wzory strukturalne związków
odpowiadaj
ące każdej z tych nazw i podaj nazwy właściwe.
a. 2,2-dimetylo-6-etyloheptan
b. 3-etylo-4,4-dimetyloheksan
c. 2-izopropylo-4-metyloheptan
d. 5,5,6-trimetylooktan
e. 2-metylopent-3-en
f. 2-etyloheks-4-en
g. 3-etylo-2-metylocyklopenten
7. Nazwij nast
ępujące związki i podaj rzędowość atomów węgla:
a. C(CH
3
)
4
b. (CH
3
)
2
CHCH
2
CH
2
CH
3
c. (CH
3
)
2
CHCH(CH
2
CH
3
)
2
d. (CH
3
)
2
CHC(CH
3
)
2
CH
2
CH
3
e. (CH
3
)
3
CCH
2
CH
2
CH(CH
3
)
2
f. CH
3
CH
2
CH
2
CH(CH
3
)CH
2
C(CH
3
)
2
CH
2
CH
3
g. CH
3
CH
2
CH(CH
3
)CH
2
C(CH
3
)(CH
2
CH
3
)CH
2
CH
2
CH
3
h. CH
3
CH
2
CH
2
C(CH
3
)(CH(CH
3
)
2
)CH(CH
3
)CH
2
CH
3
8. Podaj przykład alkanu, który:
a. ma tylko pierwszorz
ędowe atomy węgla
b. ma jedynie pierwszorz
ędowe i trzeciorzędowe atomy węgla
c. ma jeden czwartorz
ędowy i jeden drugorzędowy atom węgla
d. ma dwa trzeciorz
ędowe atomy węgla, a nie ma w ogóle drugorzędowych
9. Okre
śl rzędowość atomów węgla w następujących związkach:
.
c.
a.
CH
3
H
3
C
CHCH
2
CH
3
CHCH
3
CH
2
H
2
C
H
2
C
C
b.
CH
3
C(CH
3
)
3
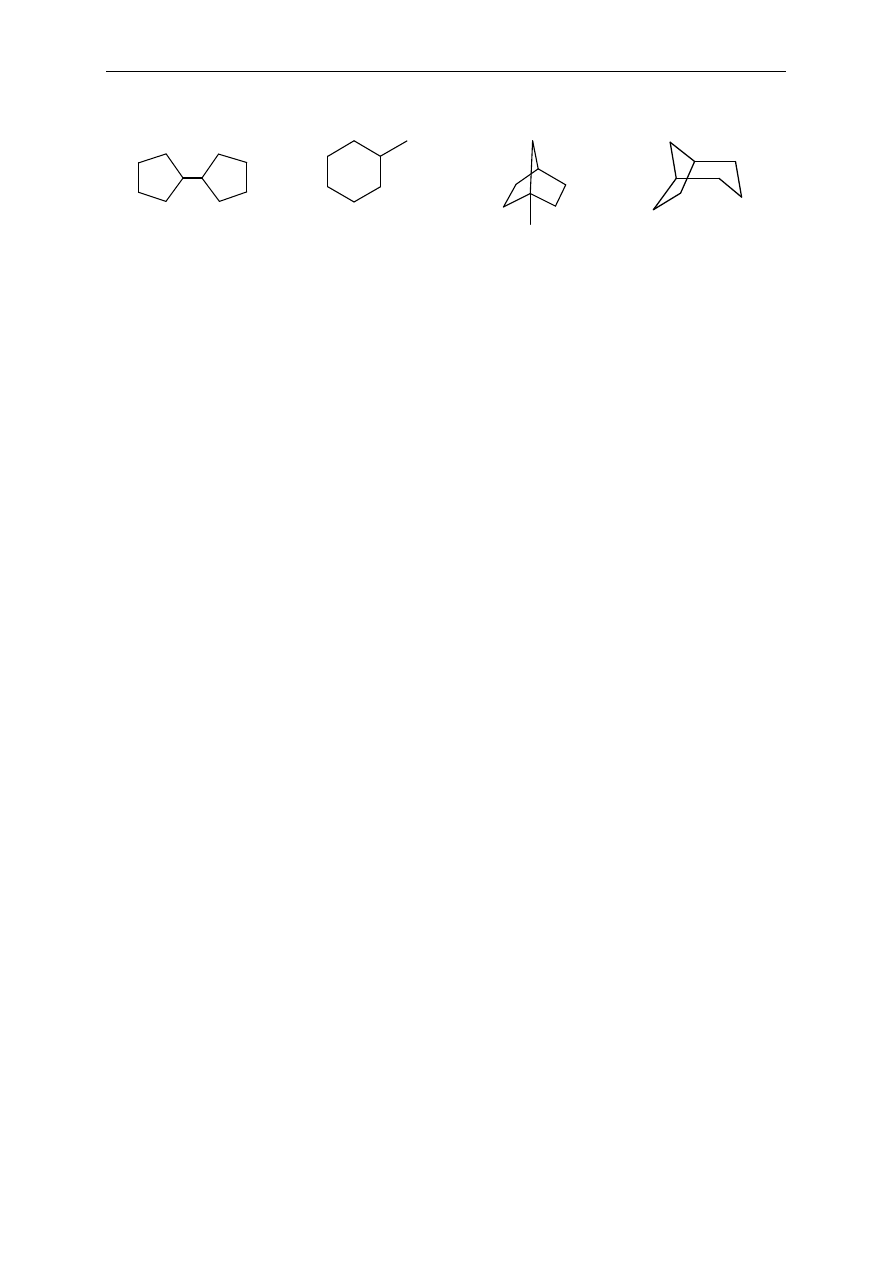
Seminarium, część I
26
10. Narysuj wzory strukturalne cykloalkanów o podanym wzorze sumarycznym spełniaj
ących
poni
ższe kryteria:
a. w
ęglowodór C
6
H
12
, który ma jeden pierwszorz
ędowy i jeden trzeciorzędowy atom
w
ęgla
b. w
ęglowodór C
6
H
12
, który ma dwa pierwszorz
ędowe i jeden czwartorzędowy atom
w
ęgla
c. w
ęglowodór C
6
H
12
, który ma dwa pierwszorz
ędowe i dwa drugorzędowe atomy
w
ęgla
3. Nazewnictwo: Halogenopochodne w glowodorów
3. Nazewnictwo: Halogenopochodne w glowodorów
3. Nazewnictwo: Halogenopochodne w glowodorów
3. Nazewnictwo: Halogenopochodne w glowodorów
11. Narysuj zwi
ązki zgodnie z nazwą:
a. chloroetan
b. 2-bromopropan
c. 2-bromo-2-metylopentan
d. 3-bromo-2,3-dimetylopentan
e. 2,3,3,4–tetrachloroheksan
f. 1–bromo–3–chloro–2,2–dimetylobutan
g. 3,3,5,5–tetrachloro-2,6–dimetyloheptan
h. 1,6–dichloro–3,4,4,5,6–pentametylooktan
i. 5-(1-chloroetylo)-5-chloro-3,4-dimetylooktan
j. 1-bromo-2-metylocyklobutan
k. 3-chloroprop-1-en
l. 3-bromobut-1-en
m. 2-chloroheks-3-yn
n. 5-chloro-4,7-dietylo-3,3,8-trimetylodek-1-en
o.
p-bromotoluen (1-bromo-4-metylobenzen)
p. chlorobenzen
q.
o-dibromobenzen
r.
m-dichlorobenzen
s. 3,5-dibromotoluen
g.
f.
e.
d.

Seminarium, część I
27
12. Podaj nazwy systematyczne poni
ższych związków:
a. (CH
3
)
2
CHCH
2
CH
2
CH(Br)CH
3
b. CH
3
CH(Br)CH
2
CH
2
CH(Cl)CH
3
c. CH
3
CH(Br)CH
2
CH
2
C(Cl)
2
CH
3
d. CH
3
CH=CHCH
2
Br
e. CH
2
(Br)CH=CHCH
2
I
f. CH(Cl)
2
C
≡
CCH
2
CH
3
g. (CH
3
)
2
C=CHCCl
3
h. CH
3
CH=C(Cl)CH(CH
2
CCl
3
)CH
2
CH
3
4. Nazewnictwo: Inne grupy zwi zków organicznych
4. Nazewnictwo: Inne grupy zwi zków organicznych
4. Nazewnictwo: Inne grupy zwi zków organicznych
4. Nazewnictwo: Inne grupy zwi zków organicznych
13. Narysuj zwi
ązki zgodnie z nazwą:
a. propan-2-ol
b. 3-metylobutan-1-ol
c. 2,2-dimetylopropan-1-ol
d.
m–jodofenol (1-hydroksy-3-jodobenzen)
e. 2,4,6–trinitrofenol (1-hydroksy-2,4,6-trinitrobenzen)
f. 3-chloropentan-2-ol
g.
p-metoksyfenol
h. eter dimetylowy (metoksymetan)
i. eter etylowo-metylowy (metoksyetan)
j. eter butylowo-propylowy (propoksybutan)
k. eter fenylowo-metylowy (metoksybenzen)
l. 2-metylobutanal
m. pentan-3-on (keton dietylowy)
n. 2,2-dimetylocyklopentanon
o. 2-hydroksybenzenokarboaldehyd (aldehyd o-hydroksybenzoesowy)
p. fenyloetanal
q. 1-fenylopropan-2-on (keton benzylowo-metylowy)
r. kwas propionowy (kwas propanowy)
s. kwas 3-chloro-2,2-dimetylopropanowy
t. chlorek butanoilu,
u. bromek formylu
v. bezwodnik propanowy
w. kwas
o-aminobenzoesowy
Seminarium, część I
28
x. kwas
o–chlorobenzoesowy
y. kwas
p–hydroksybenzoesowy
z. bezwodnik benzoesowy
aa. bezwodnik mrówkowo-pentanowy
bb. benzoesan fenylu
cc. mrówczan butylu
dd. heksanoamid
ee. kwas 2–amino–5–bromo–3–nitrobenzoesowy
ff. kwas 3,5–dinitrobenzenosulfonowy
gg. N-etylo-N-metylopropanoamid
hh. N-metylo-3-chlorobutanoamid
ii. nitrometan
jj. 2-chloro-1-nitropropan
kk. 2-(N-metylo-N-propyloamino)butan
ll. trietyloamina
mm.
difenyloamina
nn. 2-metylopropyloamina (izobutyloamina)
oo. N,N-dimetylopropyloamina
pp.
p-dinitrobenzen
qq.
m–bromonitrobenzen
rr.
m–nitrotoluen (1-metylo-3-nitrobenzen)
ss.
p–bromoanilina
14. Nazwij poni
ższe związki:
a.
CH
3
CH
2
CH
2
C
H
O
e.
O
g.
O
c.
CH
3
CH
2
C
CH
3
CH
3
O
2
N
f.
CH
3
CH
2
CH
2
CHNH
2
CH
2
CH
3
h.
O
2
N
b.
COOH
d.
CH
3
C
O
O
CH
2
CH
3
Seminarium, część I
29
15. Podaj nazwy alkoholi i okre
śl ich rzędowość:
j.
OH
COOH
n.
(CH
3
)
2
CHCH
2
CHC
6
H
5
OH
i.
Br
COOH
l.
C
H
O
Cl
v.
SO
3
H
NO
2
x.
N
CH
3
C
H
3
q.
CH
3
N
CH
3
CH
3
k.
SO
3
H
CH
3
r.
OH
NO
2
NO
2
O
2
N
o.
N
H
t
NO
2
CH
3
p.
O
C
CH
2
CH
2
CH
3
O
u.
CH
3
CH
2
C
O
Br
m.
H C
O
N
H
w.
CH
3
(CH
2
)
3
C
O
N(CH
3
)
2
s.
CH
3
CH
2
C
O
O
C CH
2
CH
2
CH
3
O

Seminarium, część I
30
a. CH
3
CH
2
CH
2
OH
b. CH
3
CH(OH)CH
2
CH
3
c. (CH
3
)
2
C(OH)CH
3
d. CH
3
CHClCH(OH)CH(CH
3
)
2
e. CH
3
CHClCH(CH3)CH(CH
3
)CH
2
OH
16. Podaj nazwy amin i okre
śl ich rzędowość:
a. C
6
H
5
NHCH
3
b. CH
3
CH
2
CH
2
N(CH
3
)
2
c. CH
3
CH
2
CH
2
CH(CH
2
CH
3
)NH
2
d. (CH
3
)
3
CNH
2
e. C
6
H
5
CH
2
NHCH
3
5. Izomeria zwi zków organicznych
5. Izomeria zwi zków organicznych
5. Izomeria zwi zków organicznych
5. Izomeria zwi zków organicznych
17. Narysuj wzory strukturalne oraz podaj nazwy pi
ęciu izomerów związku o wzorze
sumarycznym C
6
H
14
.
18. Narysuj i nazwij wszystkie monobromopochodne pentanu, C
5
H
11
Br (3).
19. Narysuj i nazwij wszystkie mo
żliwe izomery:
a. dichloro n-butanu (5)
b. dichlorocyklobutanu (3)
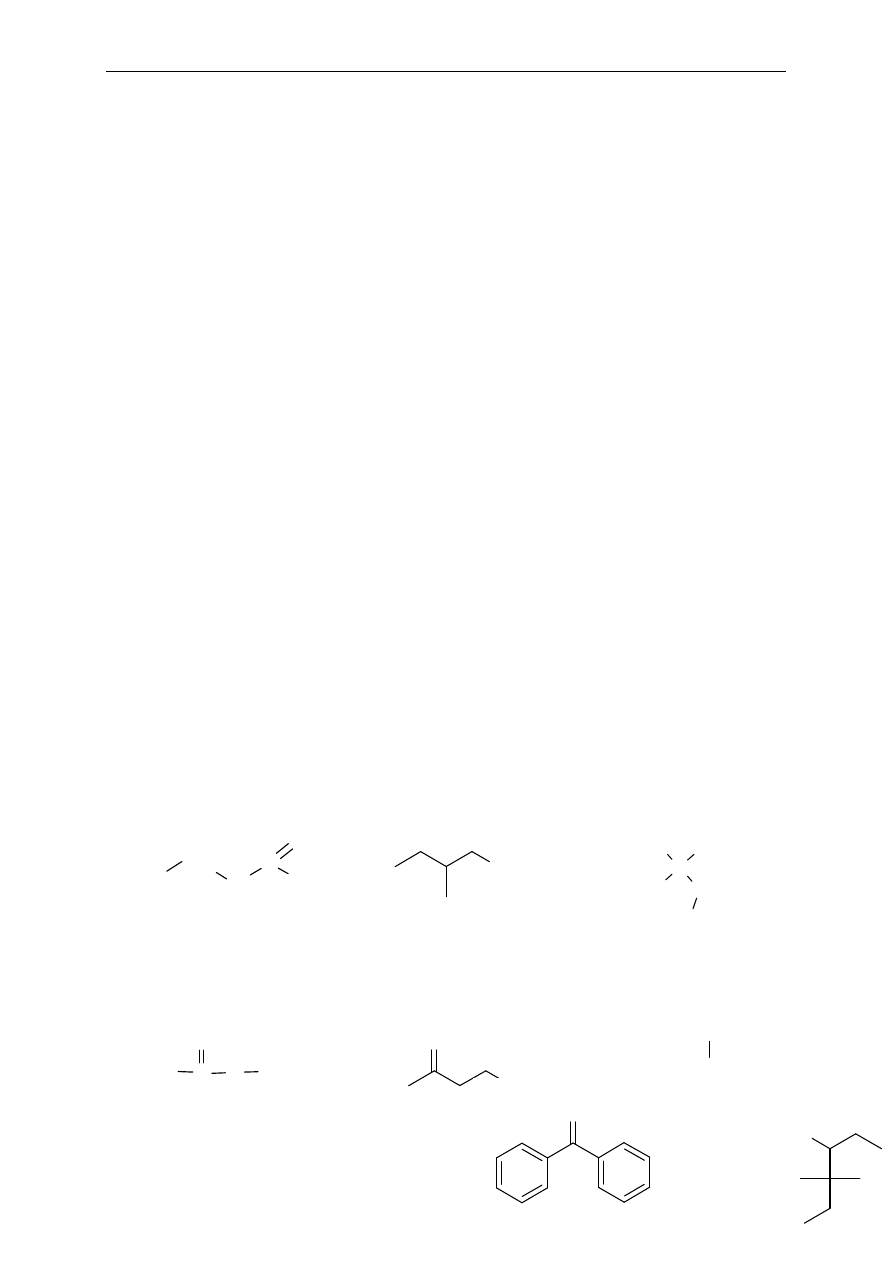
20. Które z podanych zwi
ązków mogą występować w postaci izomerów cis-trans? Narysuj
ka
żdą parę izomerów.
a. but-2-en
b. 2–metylobut-1-en
c. pent-1-en
d. 1,1-dichloroeten
e. but-1-en
f. 2–metylobut-2-en
g. pent-2-en
h. 1,2-dichloroeten

Seminarium, część I
31
21. Które z podanych zwi
ązków wykazują izomerię geometryczną (cis-trans lub Z-E)?
Narysuj wzory strukturalne izomerów i przypisz ka
żdej strukturze konfigurację Z lub E.
a. prop-1-en
b. 1-chloroprop-1-en
c. 1,2-dibromoprop-1-en
d. 1-bromo-2-chloroeten
e. 2,3-dichlorobut-2-en
f. 3–metylopent-2-en
g. 1-chloro-2-metylobut-2-en
h. 2,3-dimetylopent-2-en
i. pent-2-yn
j. 4-etylo-3-metyloheks-3-en
22. Narysuj zwi
ązki zgodnie z nazwą:
a.
trans-4-metyloheks-2-en
b.
cis–2,5–dimetyloheks-3-en
c.
trans–2–metylohept-3-en
d.
trans-3,4-dimetyloheks-3-en
e. (
Z)-3-chloro-4-metyloheks-2-en
f. (
E)-2-bromobut-2-en
g. (
E)-2,5-dibromo-3-etylopent-2-en
h. (
Z)-3-bromo-2,2- dimetyloheks-3-en
23. Przypisz konfiguracj
ę E lub Z następującym związkom:
H
C
C
H
3
C
CN
CH
2
NH
2
CH
3
H
COOH
Cl
C
C
C
C
CH
3
CH
2
Cl
CH
2
OH
H
3
C
H
3
C
Br
COOH
CH
2
Br
C
C
a.
b.
c.
d.
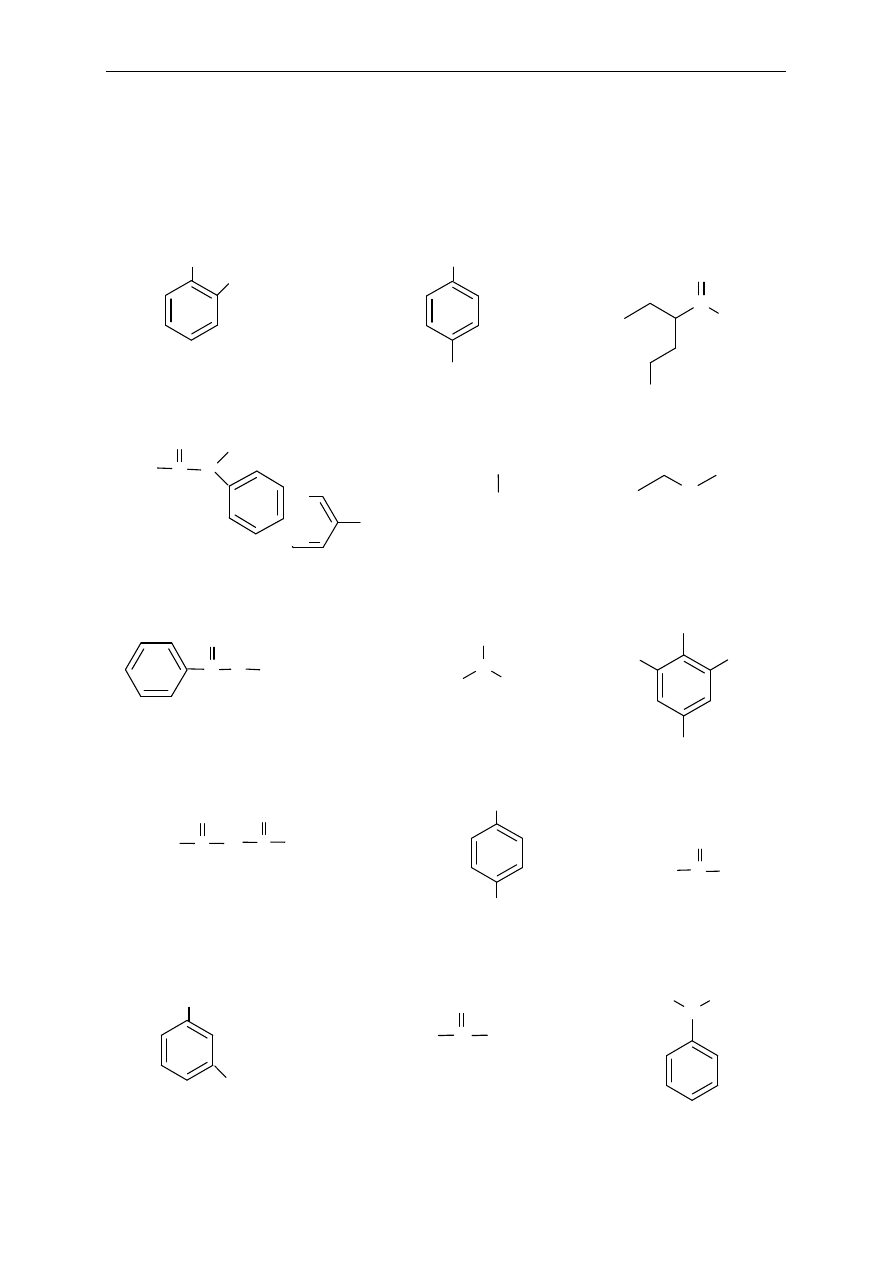
24. Narysuj wzory strukturalne i podaj nazwy wszystkich mo
żliwych izomerów:
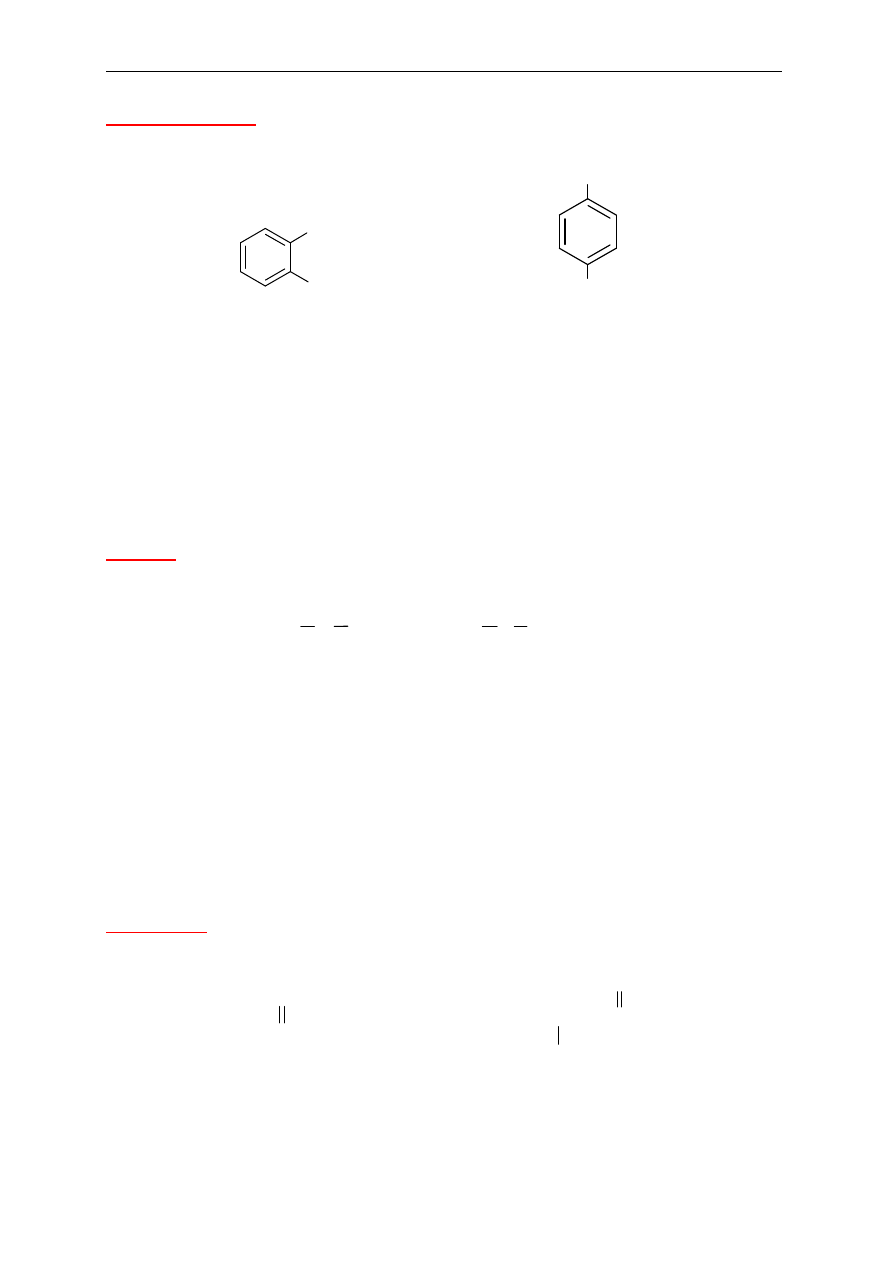
a. ksylenu (dimetylobenzenu)
b. trimetylobenzenu
Seminarium, część I
32
c. kwasu aminobenzoesowego
d. dibromonitrobenzenu
e. trinitrofenolu
25. Zaproponuj wzory strukturalne zwi
ązków spełniających następujące opisy:
a. alkohole o wzorze C
3
H
8
O
b. alkohole o wzorze C
4
H
10
O
c. ketony o wzorze C
5
H
10
O
d. aldehydy o wzorze C
5
H
10
O
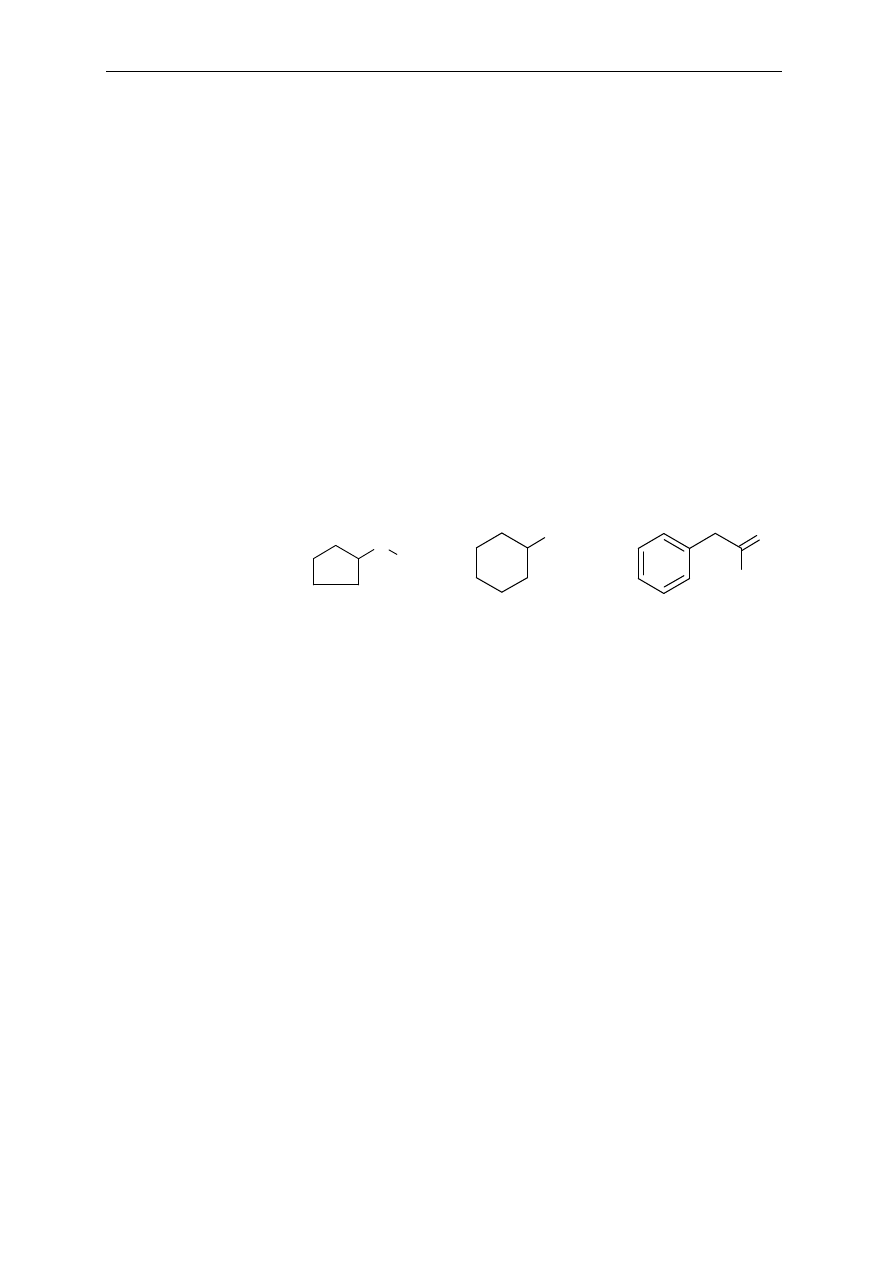
26. Dla ka
żdego z poniższych związków narysuj wzór izomeru posiadającego takie same
grupy funkcyjne:
27. Zaproponuj wzory strukturalne cz
ąsteczek o podanych wzorach sumarycznych:
a. C
3
H
8
b. C
2
H
4
O (trzy zwi
ązki)
c. C
2
H
6
O (dwa zwi
ązki)
d. CH
5
N
e. C
3
H
7
Br (dwa zwi
ązki)
f. C
3
H
9
N (cztery zwi
ązki)
6. Hybrydyzacja orbitali atomowych w zw
6. Hybrydyzacja orbitali atomowych w zw
6. Hybrydyzacja orbitali atomowych w zw
6. Hybrydyzacja orbitali atomowych w zw i zkach organicznych
i zkach organicznych
i zkach organicznych
i zkach organicznych
28. Narysuj wzory kreskowe etanu CH
3
CH
3
, propenu CH
3
CH=CH
2
, propynu CH
3
C
≡
CH
i buta-1,3-dienu CH
2
=CH-CH=CH
2
. Jaka hybrydyzacj
ę mają poszczególne atomy węgla.
Naszkicuj wzory przestrzenne tych zwi
ązków i podaj wartości wszystkich kątów między
wi
ązaniami.
c.
OH
d.
O
OH
b.
O
CH
3
a.
CH
3
CH
2
CH
2
C
≡
N
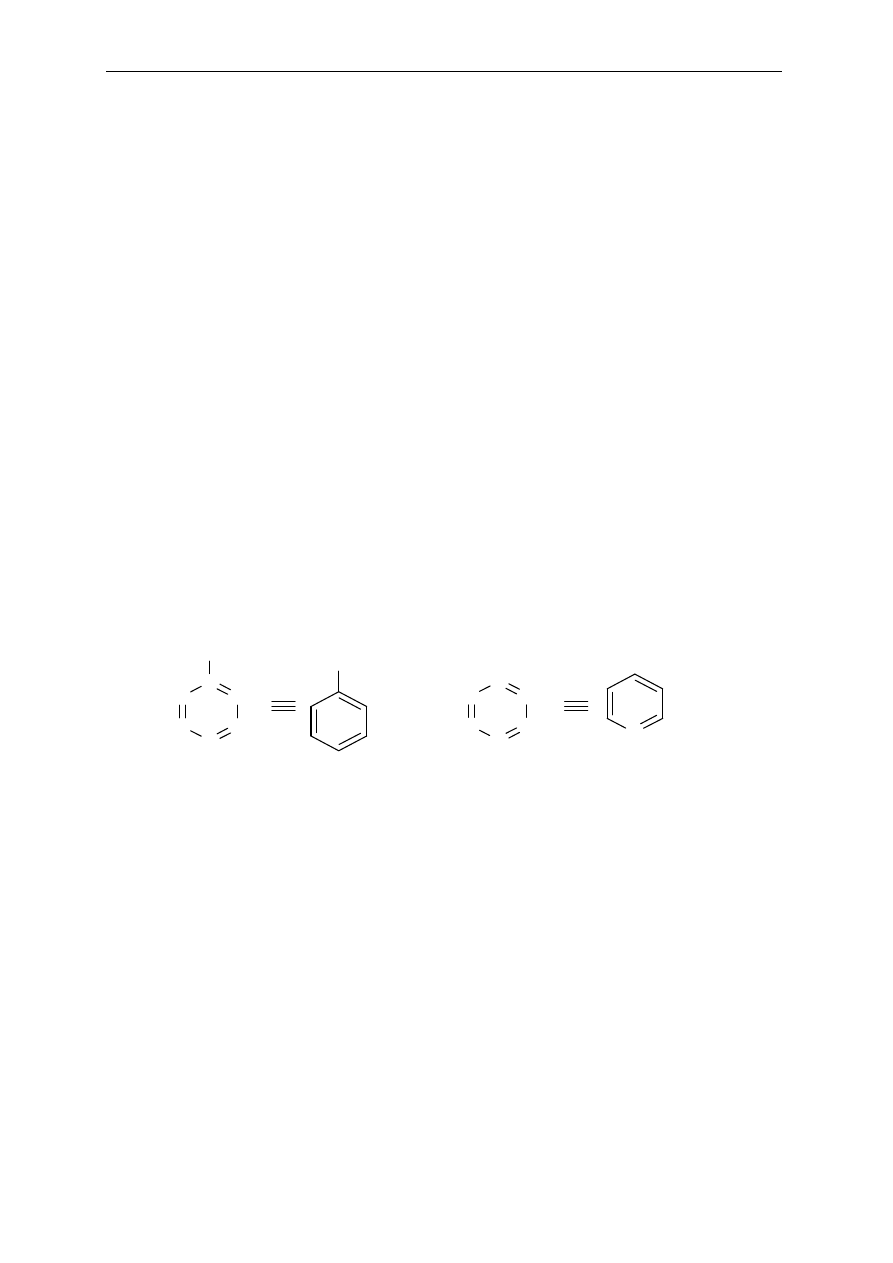
Seminarium, część I
33
29. Zaproponuj wzory strukturalne cz
ąsteczek, które zawierają:
a) dwa atomy w
ęgla o hybrydyzacji sp
2
i jeden o hybrydyzacji
sp
3
b) dwa atomy w
ęgla o hybrydyzacji sp
2
i dwa o hybrydyzacji
sp
3
c) dwa atomy w
ęgla o hybrydyzacji sp
2
i trzy o hybrydyzacji
sp
3
d) cztery atomy w
ęgla o hybrydyzacji sp
2
e) cztery atomy w
ęgla o hybrydyzacji sp
2
i dwa o hybrydyzacji
sp
3
f) dwa atomy w
ęgla o hybrydyzacji sp i dwa o hybrydyzacji sp
2
g) dwa atomy w
ęgla o hybrydyzacji sp, dwa o hybrydyzacji sp
2
i jeden o hybrydyzacji
sp
3
30. Jak
ą hybrydyzację ma atom:
a) tlenu w metoksymetanie CH
3
OCH
3
b) boru w trimetyloborze (CH
3
)
3
B
c) azotu w dimetyloaminie CH
3
NHCH
3
d) azotu w anilinie (aminobenzenie)
f) azotu w pirydynie
N
C
H
C
H
N
CH
CH
C
H
C
H
C
H
C
H
CH
CH
C
NH
2
NH
2
aminobenzen (anilina)
pirydyna
e) berylu w dimetyloberylu CH
3
BeCH
3
g) fosforu w trimetylofosfinie (CH
3
)
3
P
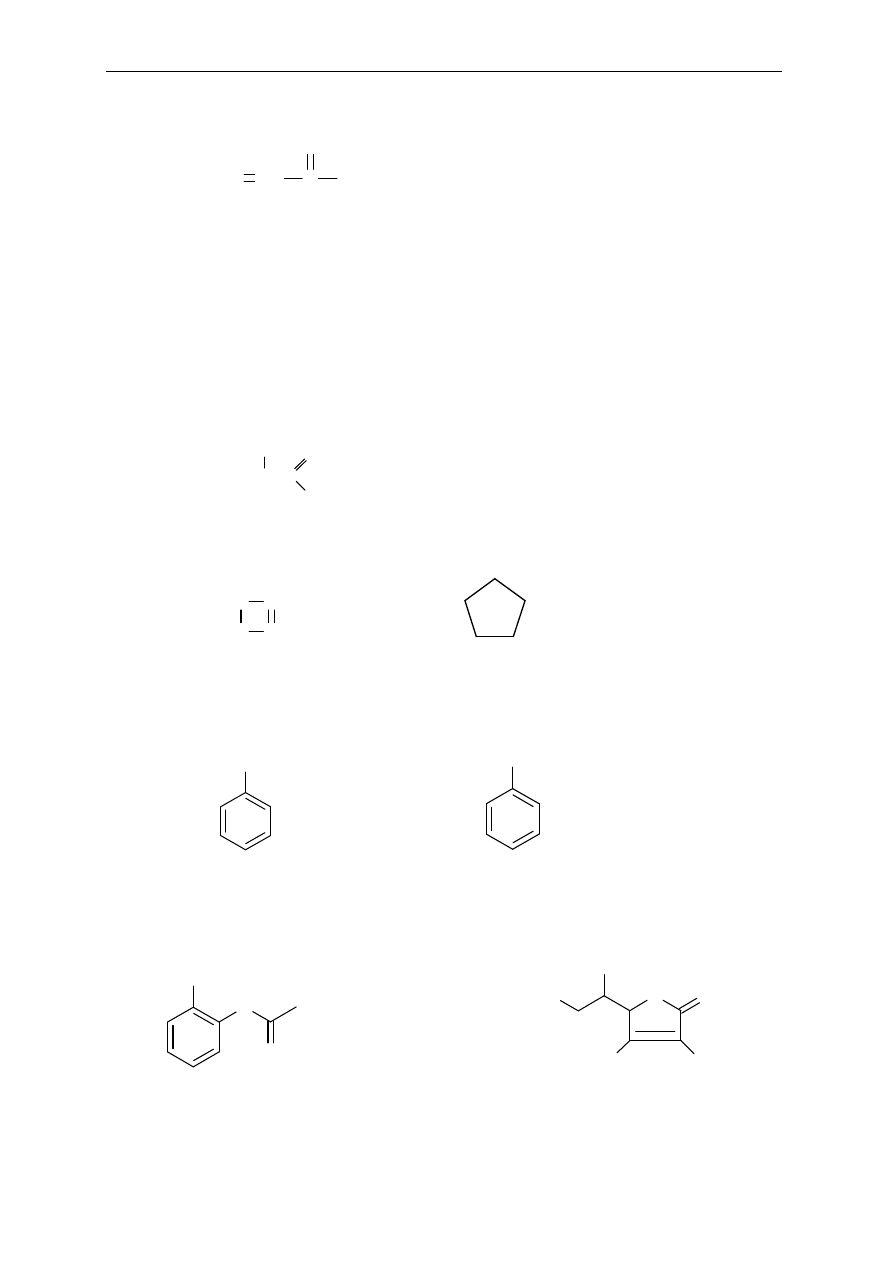
31. Okre
śl rodzaj hybrydyzacji poszczególnych atomów węgla w następujących cząsteczkach:
a) kwas etanowy (octowy) CH
3
-COOH
b) akrylonitryl CH
2
=CH-C
≡N
Seminarium, część I
34
c) but-3-en-2-on
CH
2
CH
C
CH
3
O
d) pentan CH
3
CH
2
CH
2
CH
2
CH
3
e) but-1-en-3-yn CH
2
=CHC
≡
CH
f) etoksyetan (eter dietylowy) CH
3
CH
2
OCH
2
CH
3
g) 2-metylopropen (CH
3
)
2
C=CH
2
h) 2-metylopropanal
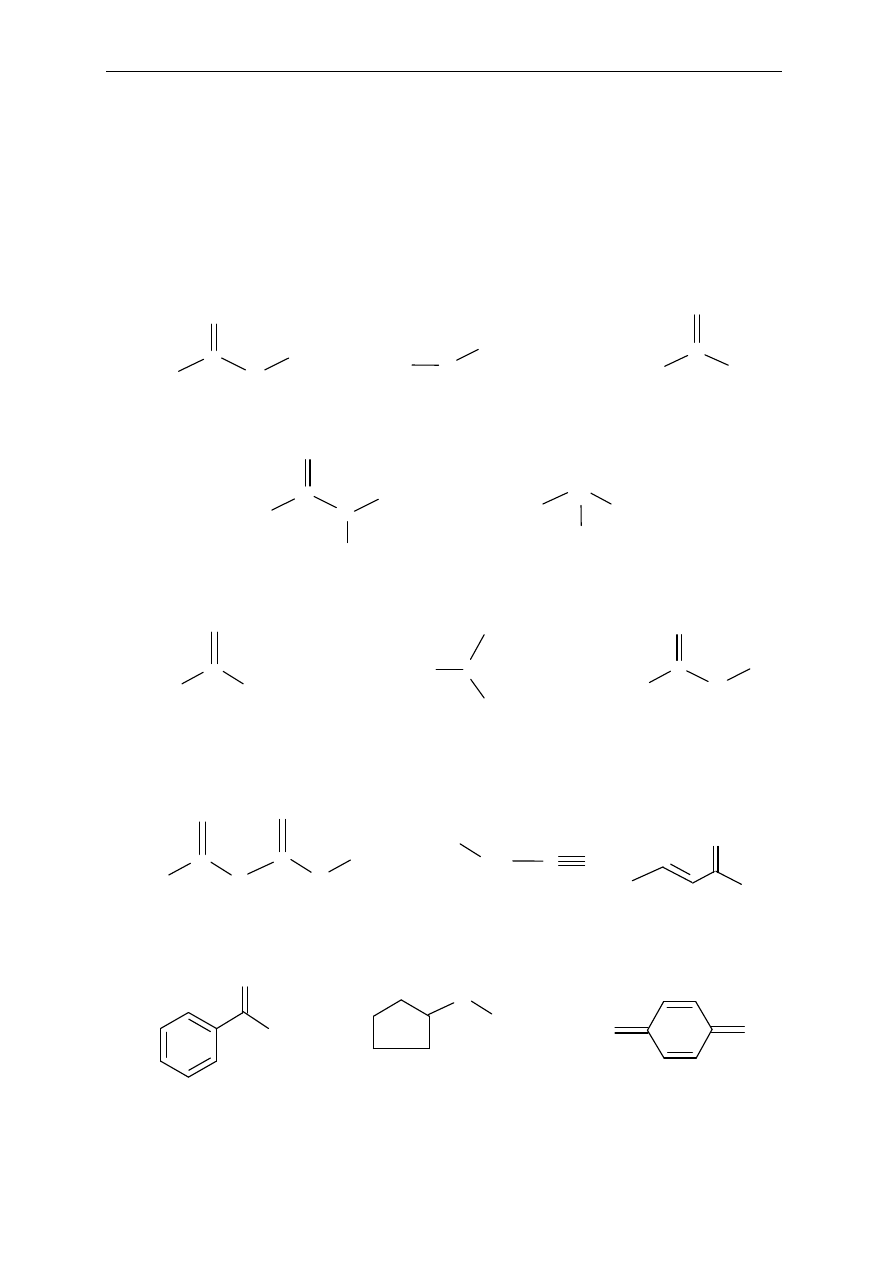
i) cyklobuten
j) cyklopentan
C
H
2
C
H
2
CH
CH
k) fenol
l) kwas benzenokarboksylowy (benzoesowy)
OH
COOH
ł) aspiryna (kwas acetylosalicylowy)
m) witamina C
COOH
O
O
O
O
OH
O
H
OH
O
H
CH
3
CHC
CH
3
O
H
Seminarium, część I
35
7. Polaryzacja wi za w zwi zkach organicznych
7. Polaryzacja wi za w zwi zkach organicznych
7. Polaryzacja wi za w zwi zkach organicznych
7. Polaryzacja wi za w zwi zkach organicznych
32. W poni
ższych związkach wskaż wiązania spolaryzowane zaznaczając atomy obdarzone
cz
ąstkowym ładunkiem ujemnym i atomy obdarzone cząstkowym ładunkiem dodatnim:
N
CH
2
CH
3
O
Cl
H
C
CH
3
CH
3
C
O
C
O
H
3
C
H
3
C
O
CH
CH
3
C
O
H
3
C
O
H
C
O
H
3
C
N
H
H
3
C
H
3
C
CH
2
CH
3
O
CH
2
CH
3
H
CH
3
CH
3
a)
b)
c)
d)
e)
f)
g)
h)
O
C
O
NH
2
O
H
3
C
H
3
C
CH
2
O
O
CH
3
O
H
O
C
O
O
CH
3
C
N
i)
j)
k)
l)
m)
n)

Seminarium, część II
36
3.
Seminarium, część II:
REAKCJE ZWIĄZKÓW ORGANICZNYCH
Zagadnienia
1. Cz
ąstki reaktywne; rodniki, czynniki elektrofilowe, czynniki nukleofilowe
2. Rodnikowe reakcje halogenowania alkanów (substytucja rodnikowa, S
R
)
3. Rozszczepianie wi
ązania podwójnego w alkenach – ozonoliza
4. Reakcje przył
ączania elektrofilowego (addycja elektrofilowa, A
E
); addycja HX oraz
halogenów
do
alkenów,
reguła
Markownikowa,
trwało
ść karbokationów,
przegrupowanie karbokationów, addycja HX oraz halogenów do alkinów
5. Reakcje przył
ączania rodnikowego w alkenach (addycja rodnikowa, A
R
)
6. Dieny; elektrofilowa addycja do alkadienów sprz
ężonych, addycja 1,4 i addycja 1,2
7. Aromatyczno
ść, reguła Hückla
8. Reakcje podstawienia elektrofilowego; substytucja elektrofilowa w zwi
ązkach
aromatycznych - S
E
Ar, struktury rezonansowe produktów po
średnich
9. Efekty kieruj
ące w reakcjach elektrofilowego podstawienia aromatycznego; wpływ
skierowuj
ący oraz aktywujący i dezaktywujący podstawników przy pierścieniu
benzenowym, efekty indukcyjne i rezonansowe
10. Izomeria optyczna (enancjomeria); chiralno
ść cząsteczek, enancjomery, mieszanina
racemiczna, czynno
ść optyczna
11. Reakcje podstawienia nukleofilowego; substytucja nukleofilowa dwuetapowa
jednocz
ąsteczkowa - S
N
1, substytucja nukleofilowa jednoetapowa dwucz
ąsteczkowa -
S
N
2, substytucja nukleofilowa w halogenkach alkilów i alkoholach
12. Reakcje eliminacji; mechanizm jednocz
ąsteczkowy, dwuetapowy – E1, mechanizm
dwucz
ąsteczkowy, jednoetapowy – E2, reguła Zajcewa
13. Efekty indukcyjne i rezonansowe a kwasowo
ść i zasadowość związków organicznych
Seminarium, część II
37
REAKCJE ZWI ZKÓW ORGANICZNYCH
REAKCJE ZWI ZKÓW ORGANICZNYCH
REAKCJE ZWI ZKÓW ORGANICZNYCH
REAKCJE ZWI ZKÓW ORGANICZNYCH
Zadania
1. Typy reakcji i reagenty
1. Typy reakcji i reagenty
1. Typy reakcji i reagenty
1. Typy reakcji i reagenty
1. Okre
śl poniższe reakcje jako reakcje addycji, eliminacji, substytucji, przegrupowania:
a) CH
3
OH + HBr
→
CH
3
Br + H
2
O
b) H
2
C=CH
2
+ H
2
→
CH
3
CH
3
c) CH
3
CH
3
+ I
2
→
CH
3
CH
2
I + HI
d) CH
3
Br + KOH
→
CH
3
OH + KBr
e) CH
3
CH
2
OH
→
H
2
C=CH
2
+ H
2
O
f) H
2
C=CH
2
+ HCl
→
CH
3
CH
2
Cl
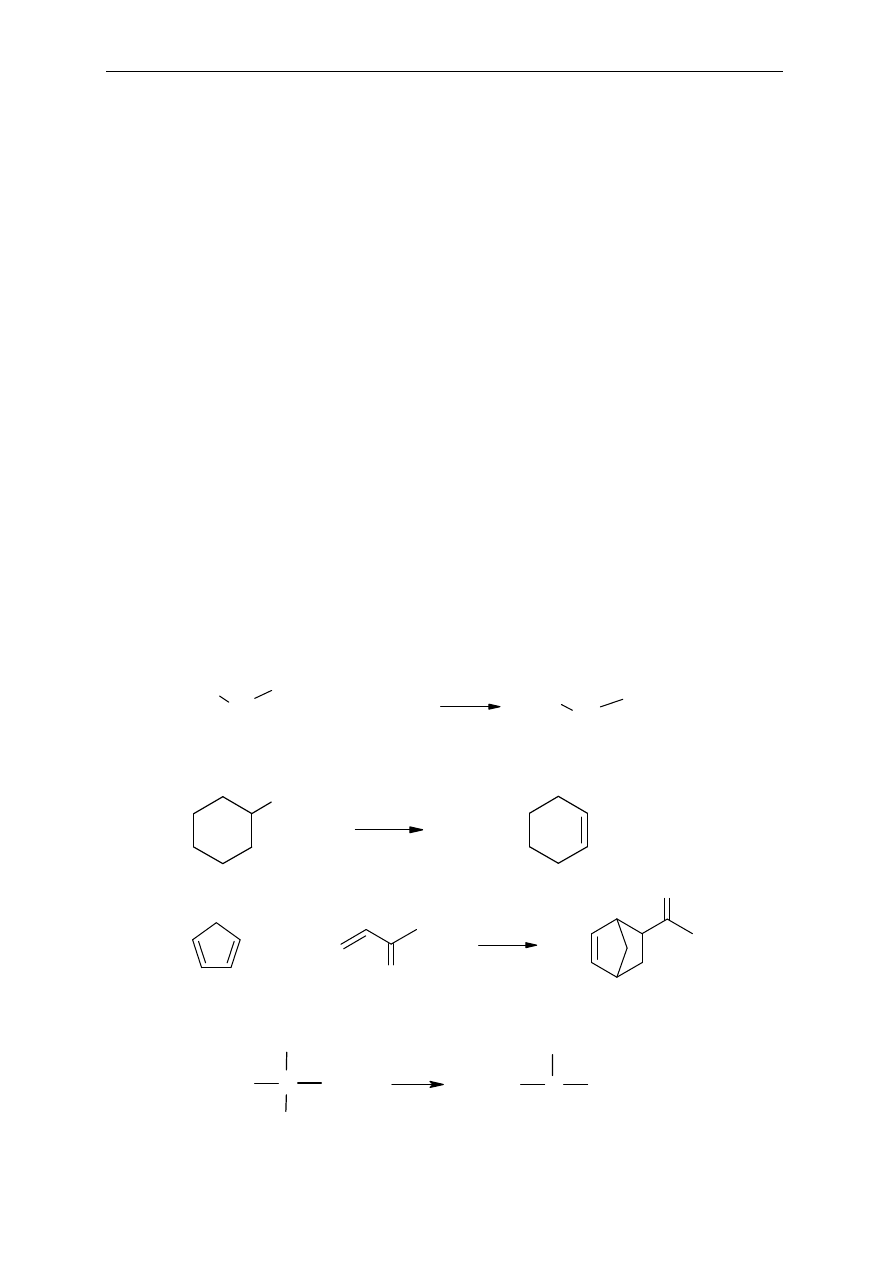
2. Zaszereguj poni
ższe reakcje do podstawowych grup: addycji, substytucji, eliminacji,
przegrupowania:
a)
b)
c)
d)
C
H
3
CH
2
Br
NaCN
C
H
3
CH
2
CN
NaBr
+
+
OH
P
2
O
5
H
2
O
+
O
O
+
temp.
CH
3
C
CH
2
H
3
C
H
CH
3
C
H
3
C
CH
3
+
+

Seminarium, część II
38
e)
3. Okre
śl, czy poniższe indywidua molekularne to nukleofil, czy elektrofil?
a) OH
¯
d) H
+
g) NO
2
+
b) Cl
¯
e) NH
3
h) CH
3
CO
+
c) Mg
2+
f) CH
3
NH
2
i) H
2
S
2. Reakcje alkanów
2. Reakcje alkanów
2. Reakcje alkanów
2. Reakcje alkanów
4. Zaproponuj wzory strukturalne wszystkich oczekiwanych produktów procesu
monochlorowania w temperaturze pokojowej nast
ępujących alkanów:
a) n-pentanu
b) 2-metylopentanu
c) n-heksanu
d) 2,2-dimetylopropanu
e) 2,2-dimetylobutanu
f) 2,2-dimetylopentanu
g) 2,2,3-trimetylopentanu
h) 2,2,4-trimetylopentanu
5. Podaj wszystkie etapy reakcji:
a) chlorowania etanu
b) bromowania 2-metylopropanu
3. Reakcje alkenów
3. Reakcje alkenów
3. Reakcje alkenów
3. Reakcje alkenów
6. Narysuj i nazwij zwi
ązki, które otrzyma się w wyniku ozonolizy podanych alkenów, po
której nast
ępuje hydroliza produktu.
CH
3
CH=CHCH
2
CH
3
O
3
Zn, H
3
O+
a)
1.
2.
N
2
O
4
NO
2
HNO
2
+
h
ν
+

Seminarium, część II
39
7. Narysuj wzór strukturalny alkenu, z którego po procesie ozonolizy, a nast
ępnie hydrolizy
wobec Zn powstaj
ą:
a) aldehyd mrówkowy i propanal
b) keton dimetylowy
c) keton dimetylowy i etanal
d) 2-metylopropanal i butan-2-on
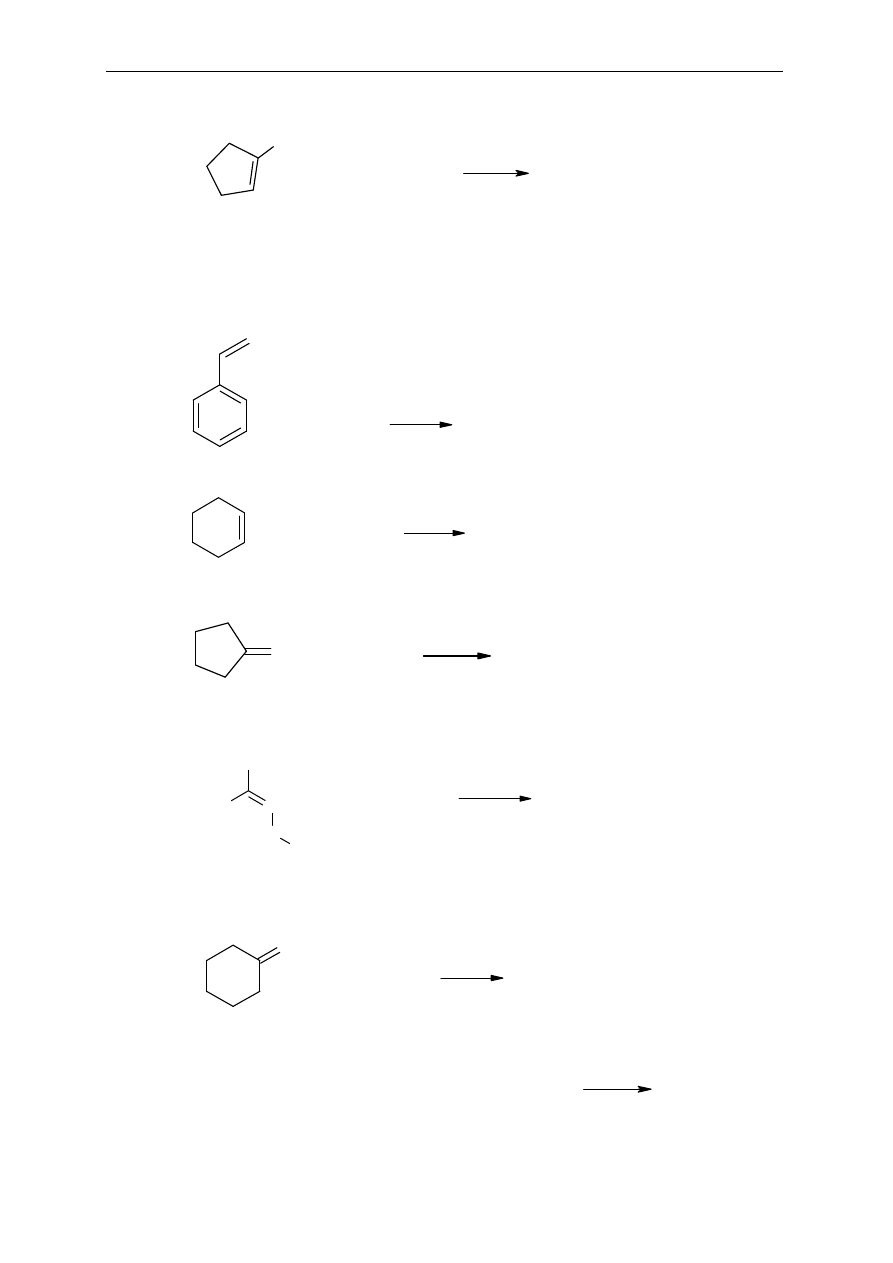
8. Podaj struktury po
średnich karbokationów oraz produkty końcowe, jakie mogą powstać
w nast
ępujących reakcjach:
a)
b)
c)
CH
3
CHCH=CH
2
CH
3
CH
3
CH=CH
2
CH
3
C=CHCH
2
CH
3
CH
3
CH
3
CH
2
C=CHCH
3
CH
3
O
3
Zn, H
3
O+
O
3
Zn, H
3
O+
O
3
Zn, H
3
O+
O
3
Zn, H
3
O+
b)
c)
d)
e)
1.
2.
1.
2.
1.
2.
1.
2.
C
H
3
CH
2
C
CH
CH
CH
3
CH
3
CH
3
+
HBr
CH
3
CH
2
C=CHC(CH
3
)
3
CH
3
+
HI
Br
H
+
Seminarium, część II
40
d)
9. Jakie s
ą spodziewane produkty następujących reakcji:
a)
b)
c)
d)
e)
f)
CH
2
CH
3
+
HBr
Br
2
+
Cl
H
+
CH
2
Cl
2
+
C
H
3
CH
CH
3
C
H
2
CH
3
Br
H
+
CH
2
Br
H
+
CH
2
=CHCH
2
CH
2
CH
2
CH=CH
2
+
2HCl

Seminarium, część II
41
g)
W przypadkach: d), e), g) podaj mechanizm reakcji.
10. Z jakich alkenów w reakcji addycji mo
żna otrzymać następujące halogenki alkilowe?
a) bromocyklopentan
b) 3-bromoheksan
c) 1-chloro-1-etylo-cykloheksan
d)
11. Addycja HCl do poni
ższych alkenów prowadzi do utworzenia mieszaniny produktów.
Podaj jakie to produkty i wyja
śnij ich powstawanie rozpisując szczegółowo mechanizm
obu reakcji.
12. Podaj produkty nast
ępujących reakcji zachodzących w środowisku nadtlenków:
CH
3
CCH=CH
2
CH
3
CH
3
CH
3
CH
2
CHCH=CH
2
CH
3
a)
b)
CH
3
CH
2
CH=CH
2
+ HBr
ROOR
a)
CH
3
CH
2
C=CHC(CH
3
)
3
CH
3
+
HBr
ROOR
b)
CH
3
CH=CHCHCH
3
CH
3
+
HBr
Cl

Seminarium, część II
42
Dla wybranych przykładów podaj mechanizm reakcji.
4. Dieny sprz
one
4. Dieny sprz
one
4. Dieny sprz
one
4. Dieny sprz
one
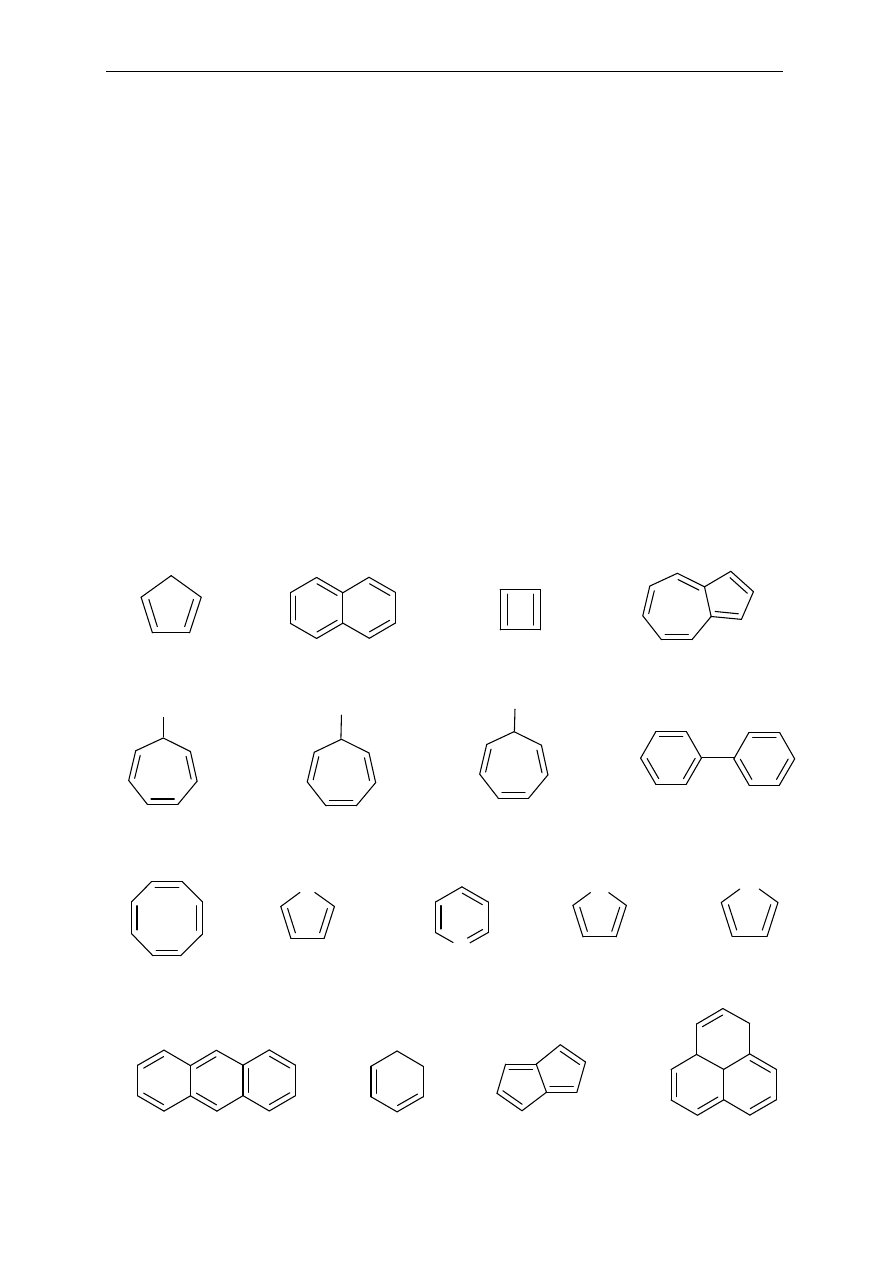
13. Które z podanych cz
ąsteczek są dienami sprzężonymi:
14. Podaj wzory oraz nazwy głównych produktów reakcji:
a) 1,3-butadienu (1mol) z Br
2
(1 mol)
b) 1,3-butadienu (1 mol) z HBr (1 mol)
c) 2,4-heksadienu (1 mol) z HCl (1 mol)
d) 2-metylo-1,3-butadienu (1 mol) z Br
2
(1 mol)
e) 2-metylo-1,3-butadienu (1 mol) z HCl (1 mol)
CH
3
-CH=CH-CH
2
-CH=CH-CH
2
-CH
3
CH
3
CH
3
C=CH-CH
2
-CH=CH-CH
3
CH
3
CH
3
-C=CH-CH=CH-CH
3
CH
3
CH
3
-CH=C=CH-CH
3
CH
3
-CH=CH-CH=CH-CH
3
CH
3
-C=CH-C=CH-CH
3
CH
3
a)
b)
c)
d)
e)
f)
CH
3
C=CHCH
2
CH
3
CH
3
+
ROOR
HBr
c)
Seminarium, część II
43
5. Reakcje alkinów
5. Reakcje alkinów
5. Reakcje alkinów
5. Reakcje alkinów
15. Podaj wzory produktów reakcji:
a) but-1-ynu z HBr (1 mol); but-1-ynu z HBr (2 mol)
b) but-2-ynu z HBr (1 mol); but-2-ynu z HBr (2 mol)
c) but-2-ynu z Br
2
(1 mol); but-2-ynu z Br
2
(2 mol)
d) pent-2-ynu z HBr (1 mol); pent-2-ynu z HBr (2 mol)
6. Aromatyczno
6. Aromatyczno
6. Aromatyczno
6. Aromatyczno
16. Który z poni
ższych związków ma charakter aromatyczny. Wyjaśnij dlaczego?
H
H
H
O
S
N
C
+
..
.
_
..
_
a)
b)
c)
e)
d)
h)
g)
f)
i)
k)
l)
m)
j)
n)
o)
p)
q)
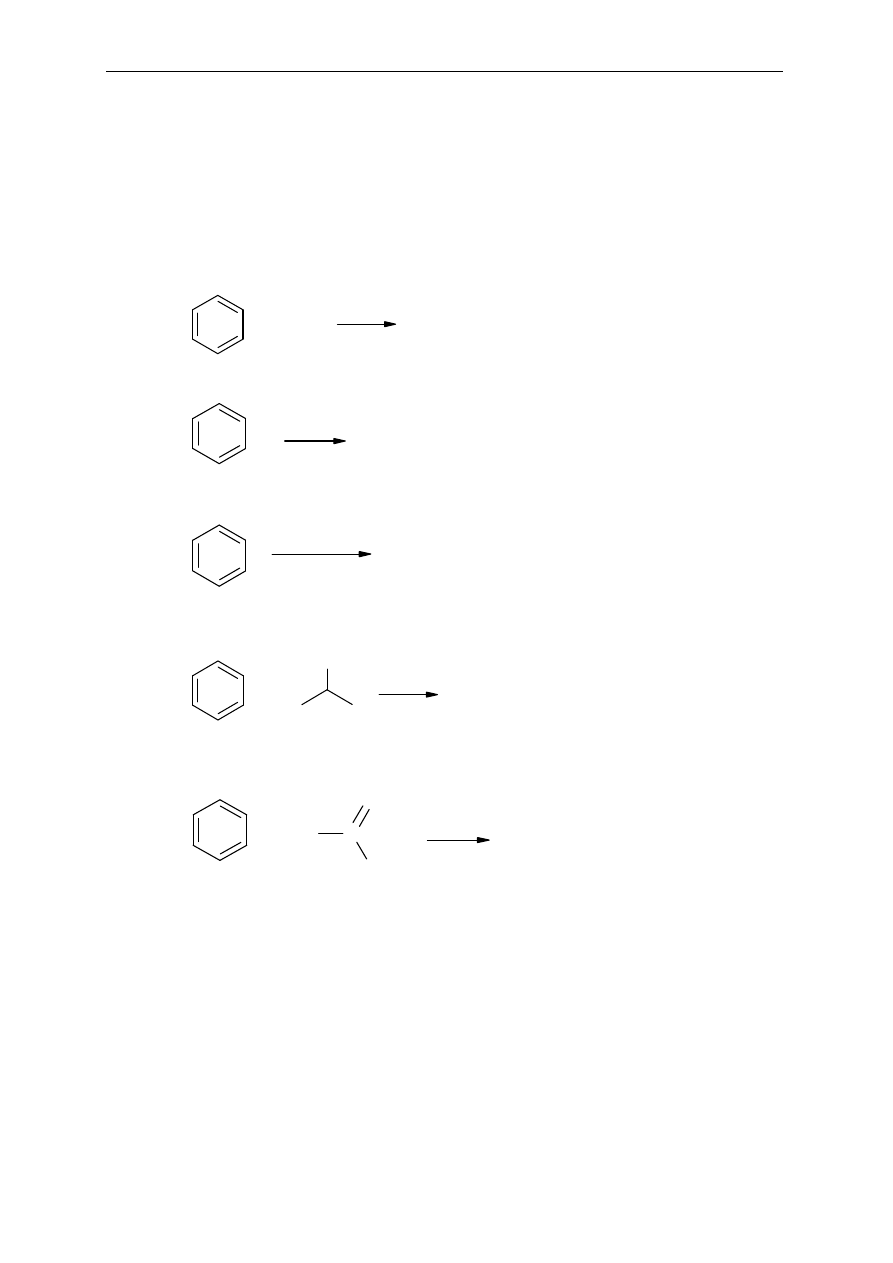
Seminarium, część II
44
7.
Reakcje
zwi zków
aromatycznych.
Efekty
indukcyjne
7.
Reakcje
zwi zków
aromatycznych.
Efekty
indukcyjne
7.
Reakcje
zwi zków
aromatycznych.
Efekty
indukcyjne
7.
Reakcje
zwi zków
aromatycznych.
Efekty
indukcyjne
i rezonansowe
i rezonansowe
i rezonansowe
i rezonansowe
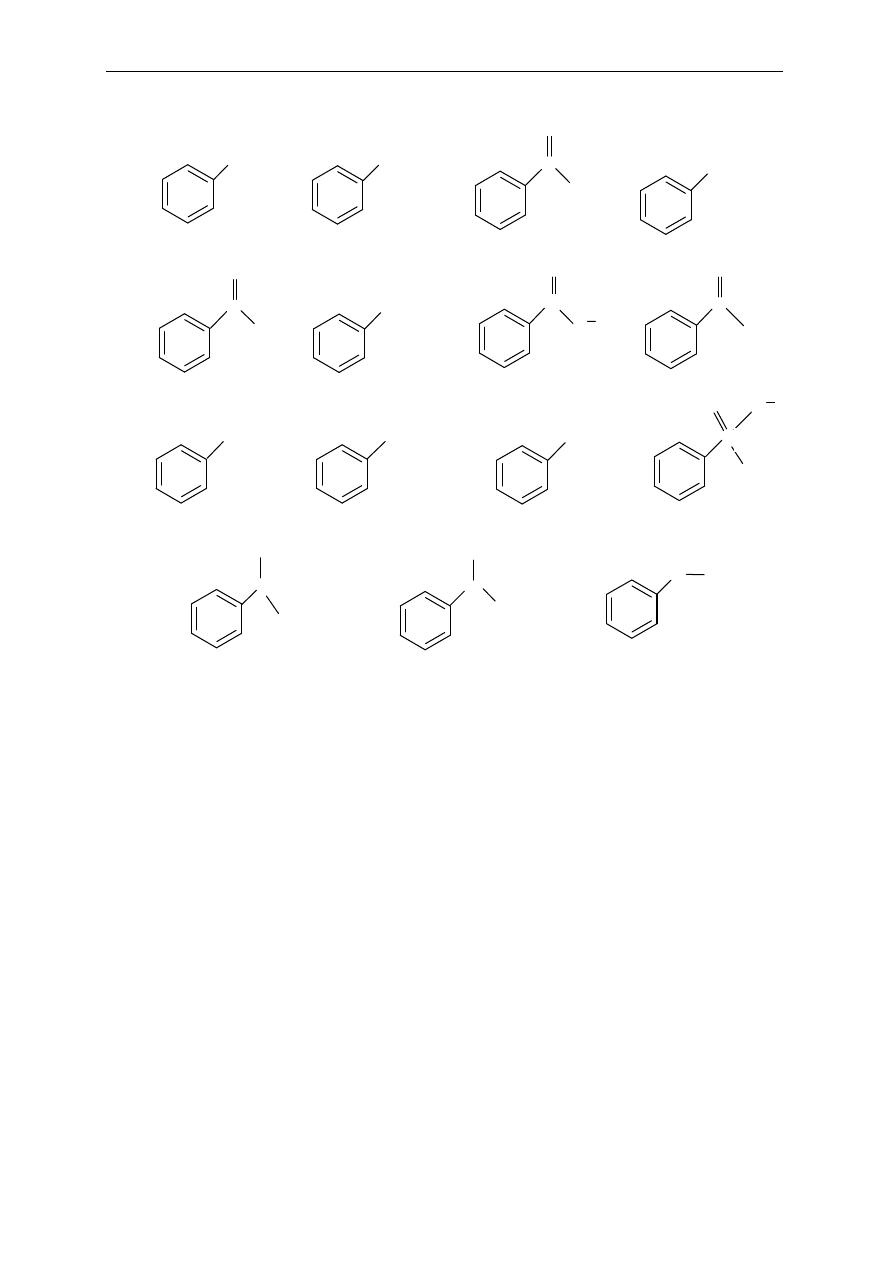
17. Narysuj wszystkie struktury rezonansowe produktów po
średnich poniższych reakcji.
Podaj produkty ko
ńcowe i nazwij je.
a)
b)
c)
d)
e)
18. Wska
ż związki, w których grupy przyłączone do pierścienia aromatycznego:
- s
ą grupami indukcyjnie wyciągającymi elektrony (wskaż kierunek polaryzacji wiązań)
- s
ą grupami indukcyjnie dostarczającymi elektronów
- dostarczaj
ą elektronów do pierścienia aromatycznego w wyniku rezonansu
- wyci
ągają elektrony z pierścienia aromatycznego na skutek rezonansu
Cl
2
FeCl
3
+
HNO
3
/H
2
SO
4
H
2
SO
4
/SO
3
Cl
AlCl
3
+
C
H
3
C
Cl
O
AlCl
3
+
Seminarium, część II
45
19. Przedstaw struktury rezonansowe aniliny ukazuj
ące efekt rezonansowy grupy aminowej,
powoduj
ący dostarczanie elektronów do pierścienia aromatycznego.
20. Przedstaw struktury rezonansowe nitrobenzenu ukazuj
ące efekt rezonansowy grupy
nitrowej, powoduj
ący wyciąganie elektronów z pierścienia aromatycznego.
21. Ni
żej wymienione podstawniki podziel na:
a) aktywuj
ące i dezaktywujące pierścień aromatyczny w reakcjach substytucji
elektrofilowej
b) kieruj
ące w pozycje orto/para i kierujące w meta
-NO
2
, -CH
3
, -CHO, -COOH, -OCH
3
, -COOCH
3
, -OCOCH
3
, -Cl, -CCl
3
, -OH,
-NHCOCH
3
, -Br, -C
≡
N, -SO
3
H, -F, -N(CH
3
)
3
+
, -NH
2
, -CH
2
CH
3
, COCH
3
, -N(CH
3
)
2
.
OH
CH
2
CH
3
NH
2
CH
3
N
S
C
O
CH
3
C
O
OH
C
O
H
Cl
CH
CH
3
CH
3
I
Br
O
CH
3
N
H
CH
3
O
O
O
OH
O
+
+
a)
b)
c)
d)
e)
f)
g)
h)
i)
j)
k)
l)
m)
n)
o)
Seminarium, część II
46
22. Zaproponuj produkty mononitrowania zwi
ązków otrzymanych w zad. 17 oraz podaj ich
nazwy.
23. Zaproponuj główne produkty monoalkilowania ni
żej podanych związków w reakcji
z chlorometanem w obeno
ści AlCl
3
:
a) bromobenzen
b) 2,4-dichlorofenol (1-hydroksy-2,4-dichlorobenzen)
c) m-bromofenol (1-bromo-3-hydroksybenzen)
d) 2,5-dibromotoluen
24. Nazwij oraz narysuj wzory głównych produktów reakcji:
- elektrofilowego chlorowania: a) m-nitrofenolu, b) kwasu p-nitrobenzoesowego
- sulfonowania: a) m-bromofenolu, b) 2,4-dibromofenolu
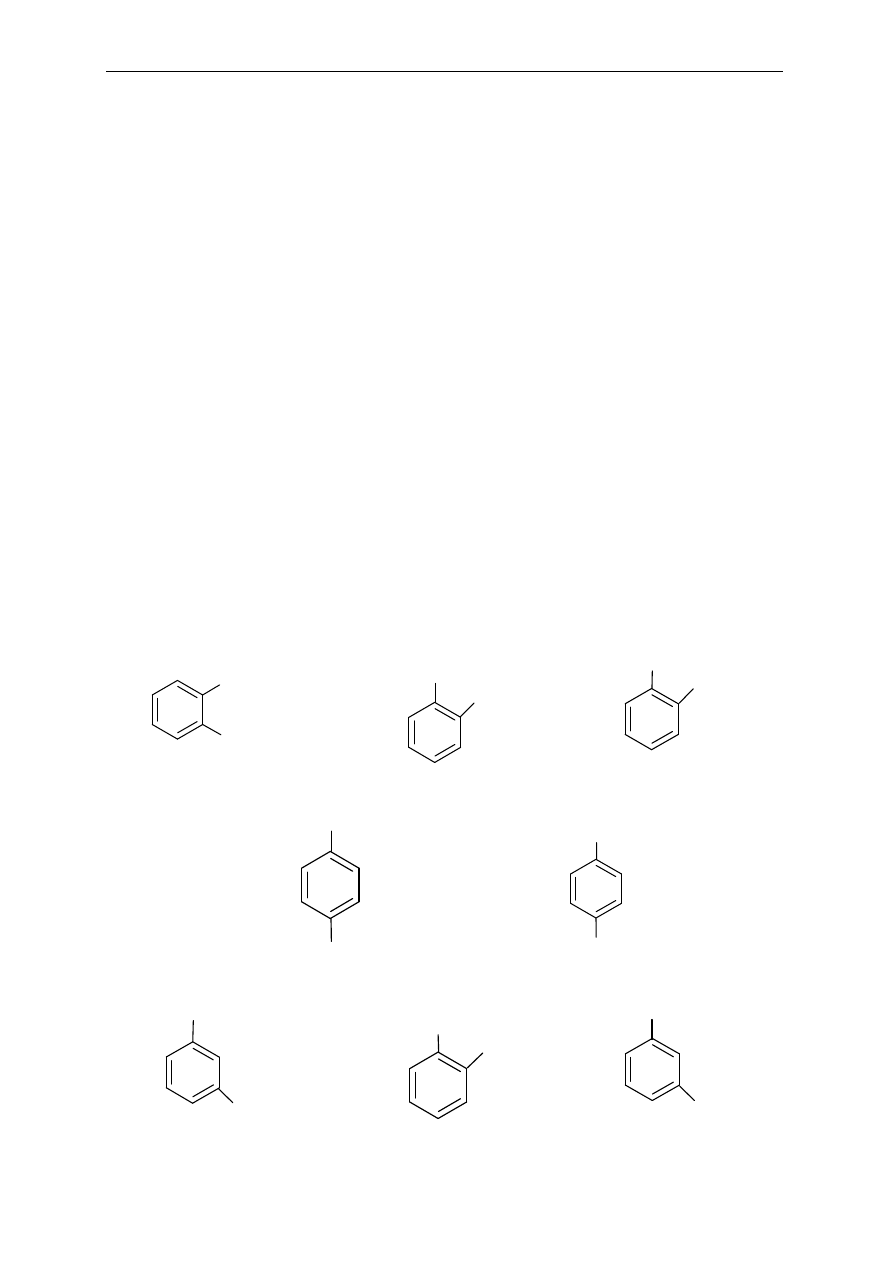
25. Zaznacz najbardziej prawdopodobn
ą pozycję w pierścieniu aromatycznym, którą zajmie
nast
ępny podstawnik, jeśli poniższe związki poddamy substytucji elektrofilowej:
a)
b)
c)
d)
e)
f)
g)
h)
COOH
COOH
Br
NO
2
NH
2
Br
COCH
3
CH
3
OCH
3
OCH
3
O
NO
2
CH
3
CH
3
CH
3
CF
3
COOH

Seminarium, część II
47
26. Uporz
ądkuj związki w każdej z grup w szeregu ich reaktywności w reakcji substytucji
elektrofilowej. Uzasadnij tak
ą kolejność.
a) benzen, nitrobenzen, fenol
b) anilina, chlorobenzen, kwas benzoesowy
c) benzaldehyd, benzen, bromobenzen
d) toluen, p-ksylen, benzen
27. Który z trzech izomerycznych trimetylobenzenów powinien najłatwiej ulega
ć reakcji
substytucji
elektrofilowej?
Uzasadnij
odpowied
ź. Podaj produkt (produkty)
mononitrowania tego trimetylobenzenu.
28. Zaproponuj schematy syntez poni
ższych związków z benzenu i odpowiednich reagentów
organicznych lub nieorganicznych:
a) p-bromonitrobenzenu
b) m-bromonitrobenzenu
c) p-etyloacetofenonu
d) kwasu m-chlorobenzenosulfonowego
8.
8.
8.
8. Izomeria optyczna i reakcje substytucji nukleofilowej
Izomeria optyczna i reakcje substytucji nukleofilowej
Izomeria optyczna i reakcje substytucji nukleofilowej
Izomeria optyczna i reakcje substytucji nukleofilowej
29. We wzorach poni
ższych związków oznacz gwiazdką * centra chiralności (asymetryczne
atomy w
ęgla):
a) CH
3
CH(NH
2
)CH
2
CH
3
b) (CH
3
)
2
CHCH(OH)CH(CH
3
)
2
c) CH
3
CH(OH)CH
2
COOH
e) HO
2
CCH(OH)CH
2
COOH
f) CH
3
CH
2
CH(OCH
3
)OH
g) ClCH
2
CH
2
OH
h) CH
3
CH(Cl)CH
2
Cl
i) CH
3
CH
2
CH(OH)CH
2
CH
3

Seminarium, część II
48
30. Które z alkoholi C
4
H
9
OH i C
5
H
11
OH wykazuj
ą izomerię optyczną? Narysuj wzory
przestrzenne enancjomerów.
31. Na przykładzie reakcji 1-chloro-3-metylobutanu z wodorosiarczkiem sodowym (NaSH)
wyja
śnij na czym polega mechanizm reakcji S
N
2. Czy chloropochodna (substrat) i tiol
(produkt) s
ą związkami optycznie czynnymi?
32. Co to jest reakcja S
N
1? Wyja
śnij mechanizm reakcji. Dlaczego produkt reakcji
chlorowcopochodnej czynnej optycznie jest optycznie nieczynny?
33. Jaki wpływ na szybko
ść przebiegającej reakcji S
N
2 pomi
ędzy 1-jodo-2-metylobutanem
a anionem cyjankowym CN
−
miałoby zmniejszenie o połow
ę stężenia anionów
cyjankowych i dwukrotne zwi
ększenie stężenia 1-jodo-2-metylobutanu? Jak wpłynęłoby
natomiast trzykrotne zwi
ększenie stężenia obu reagentów?
34. Jaki wpływ na szybko
ść przebiegającej reakcji chemicznej pomiędzy etanolem a 2-jodo-2-
metylobutanem b
ędzie miało trzykrotne zwiększenie stężenia halogenku?
35. W reakcji 1-chlorobutanu z rozcie
ńczonym roztworem NaOH otrzymano butan-1-ol.
Z bada
ń kinetycznych reakcji wynika, że dodatek zasady powoduje przyspieszenie reakcji
podstawiania. Jaki jest mechanizm tej reakcji?
36. W ka
żdej z podanych par wskaż związek, który szybciej ulega reakcji z NaI w acetonie
(reakcja S
N
2):
a) 1-chloro-2-metylopropan czy 1-chloro-2,2-dimetylopropan
b) 1-chloro-3-metylobutan czy 1-chloropropan
c) 1-bromopentan czy 3-bromopentan
d) 2-bromo-3-metyloheksan czy 2-bromo-5-metyloheksan
e) 1-jodopropan czy jodek metylu
f) 1-bromopropan czy 1-bromo-2-metylopropan
37. Jakiego produktu (produktów) mo
żna oczekiwać w reakcji 3-chloro-3-metylooktanu
z kwasem octowym? Przedstaw mechanizm reakcji oraz stereochemi
ę zarówno substratu
jak i produktu.
38. W reakcji optycznie czynnego 3-bromo-3-metyloheksanu z amoniakiem otrzymano
odpowiedni
ą aminę. Otrzymany produkt był optycznie nieczynny. Uzasadnij dlaczego.
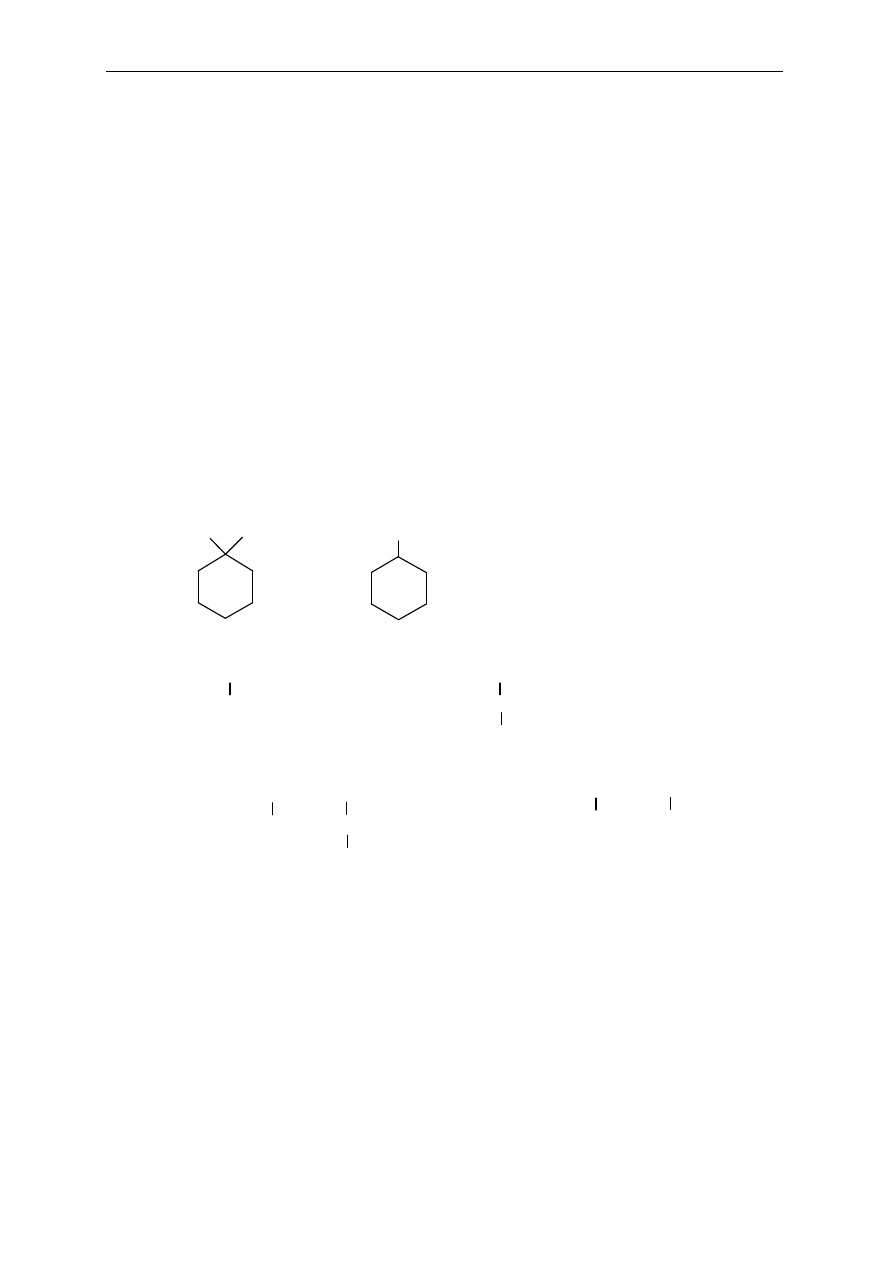
Seminarium, część II
49
39. Przedstaw mechanizm reakcji substytucji nukleofilowej:
a) 1-chloropropanu z wodorotlenkiem sodowym,
b) 1-bromobutanu z wodorotlenkiem sodowym
c) 2-bromo-2-metylopropanu z wodorosiarczkiem sodowym (NaSH)
d) 2-bromobutanu z wodorotlenkiem sodowym
e) 1-chloro-3-fenylobutanu z wodorotlenkiem sodowym
f) 2-chloro-2-fenylobutanu z wod
ą
W przypadku chiralnych substratów podaj budow
ę steryczną produktów reakcji.
40. W ka
żdej z poniższych par wskaż związek, który łatwiej ulega reakcji z HCl i uzasadnij
wybór. Narysuj i nazwij produkt(y) tej reakcji dla wszystkich podanych alkoholi.
41. Na przykładzie metanolu, który poddano działaniu HBr przedstaw mechanizm reakcji
S
N
2. Podaj równanie kinetyczne tej reakcji oraz okre
śl jaki wpływ na szybkość
przebiegaj
ącej reakcji miałoby dwukrotne zwiększenie lub dwukrotne zmniejszenie
st
ężenia anionów bromkowych?
42. Zaproponuj mechanizm reakcji 2-metylobutan-2-olu z HCl. Rozpisz poszczególne etapy
tej reakcji i wska
ż etap najwolniejszy. Czy substrat i produkt główny są optycznie
czynne?
CH
3
-C-CH
3
OH
CH
3
CH
3
OH
OH
CH
3
-CH-CH
2
-CH
3
OH
CH
3
CH
3
-CH
2
-CH-CH
2
-C-CH
3
OH
CH
3
CH
3
CH
3
-CH
2
-CH-CH
2
-CH
2
OH
czy
czy
czy
a)
b)
c)
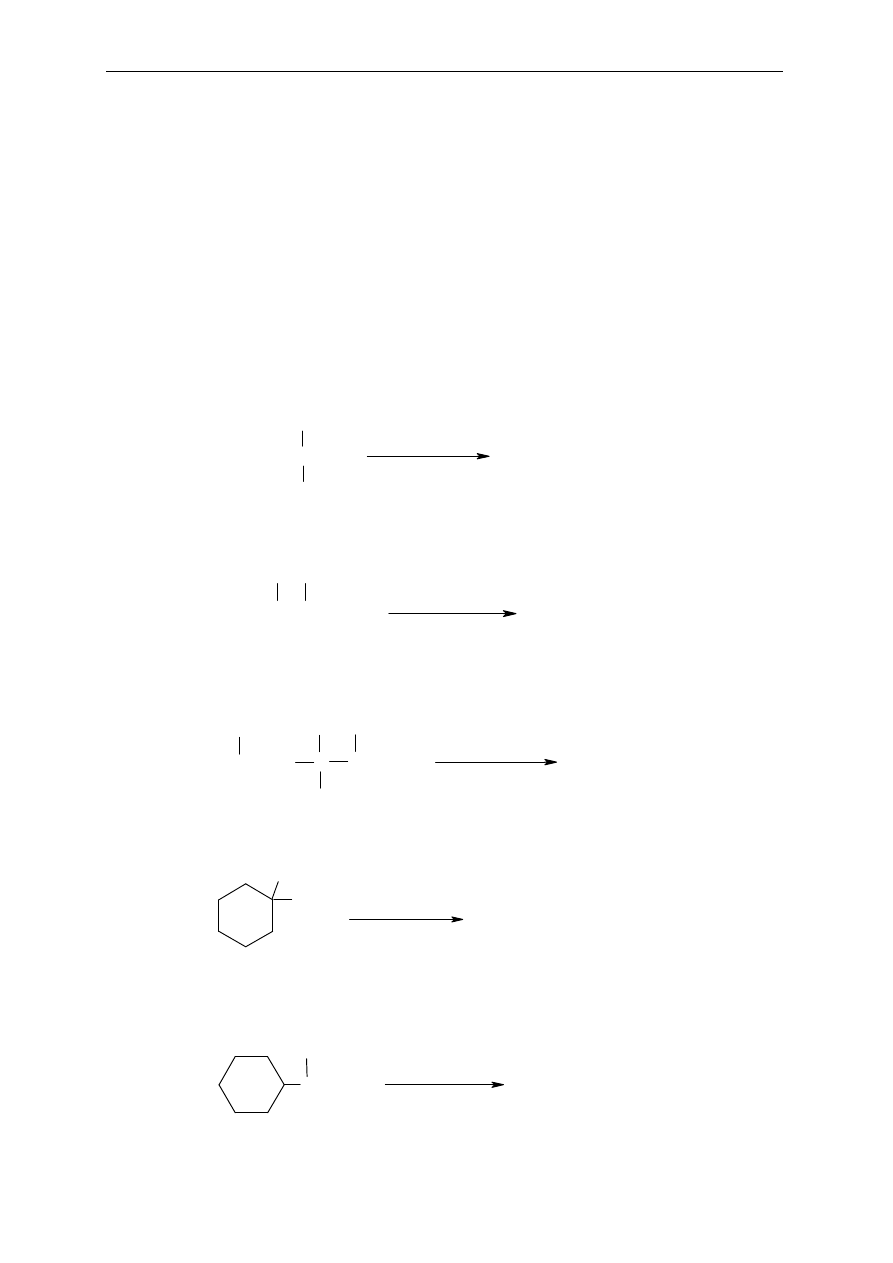
Seminarium, część II
50
43. Działaj
ąc chlorowodorem na 3-metylobutan-2-ol otrzymano mieszaninę produktów: 2-
chloro-3-metylobutan i 2-chloro-2-metylobutan. Przedstaw mechanizm reakcji oraz
wytłumacz powstawanie mieszaniny produktów wskazuj
ąc produkt główny.
9. Reakcje eliminacji
9. Reakcje eliminacji
9. Reakcje eliminacji
9. Reakcje eliminacji
44. Jakich produktów mo
żna oczekiwać po reakcjach eliminacji następujących halogenków
alkilowych? Jakie produkty b
ędą produktami głównymi?
a)
b)
c)
d)
e)
CH
3
CH
2
CCH
3
Br
CH
3
r.eliminacji
CH
3
CH
2
CHCHCH
3
Br CH
3
r.eliminacji
CH
3
CHCH
2
CHCH
3
CH
3
CH
3
CH
3
Cl
C
r.eliminacji
CH
3
Cl
r.eliminacji
CHCH
3
Br
r.eliminacji
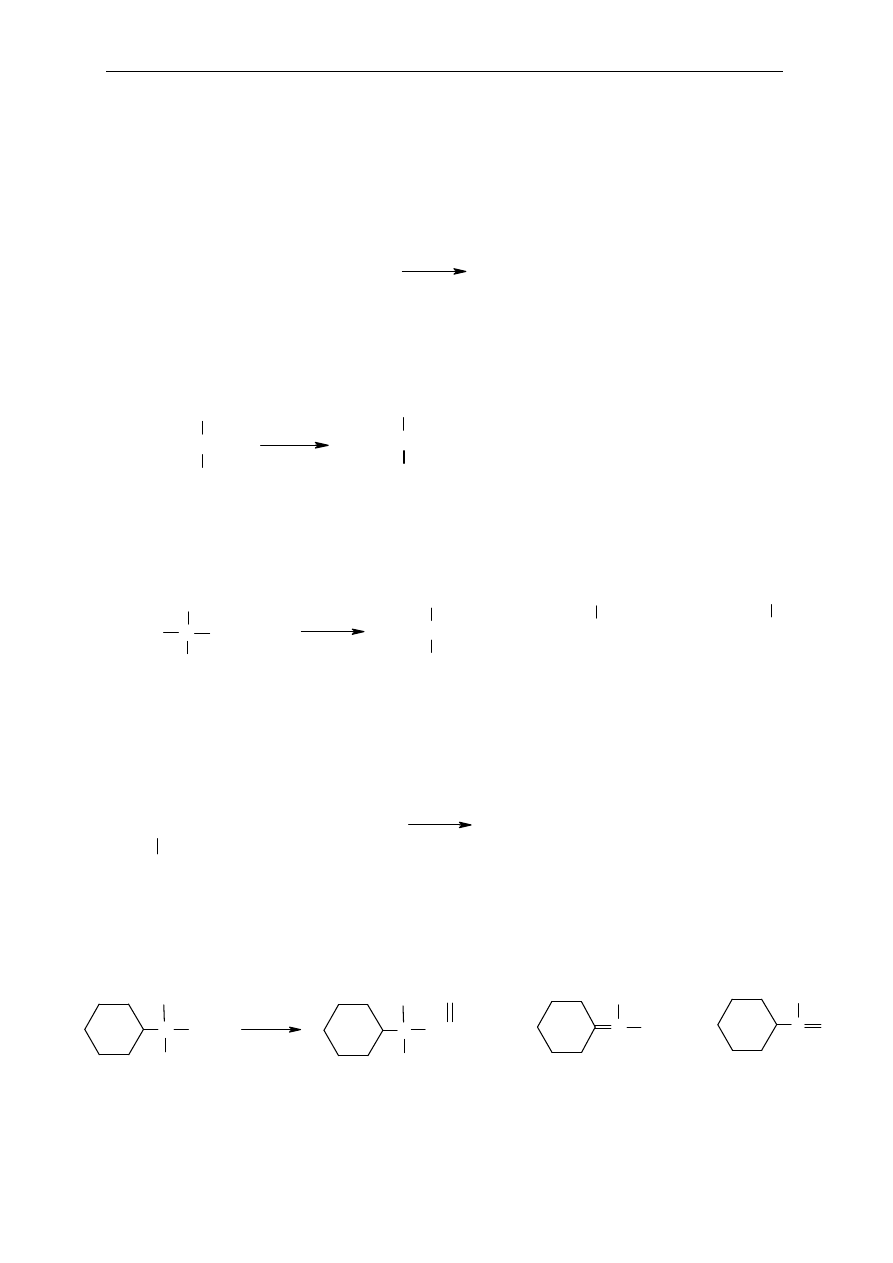
Seminarium, część II
51
45. W poni
ższych schematach reakcji wskaż produkty eliminacji oraz określ mechanizm
reakcji (E1 lub E2) prowadz
ący do utworzenia tych związków.
a)
b)
c)
d)
e)
C
Br
CH
3
CH
3
CH
3
CO
2
H
C
CH
3
CH
3
C
CH
3
CH
3
C
CH
3
CH
2
+
+
OCCH
3
O
CH
3
CHCH
2
CH
2
CH
3
Cl
C
2
H
5
ONa
+
C
2
H
5
OH
CH
3
CH=CHCH
2
CH
3
+ CH
2
=CHCH
2
CH
2
CH
3
CH
3
CH
2
CH
3
CH
3
Br
C
H O
CH
3
CCH
2
CH
3
CH
3
OH
+
CH
3
CH
3
C=CHCH
3
+
CH
3
CH
2
=CCH
2
CH
3
2
CH
3
CBr
CH
3
CH
3
CH
3
OH
CH
3
COC
2
H
5
CH
3
CH
3
+
(CH
3
)
2
C=CH
2
CH
3
CH
2
CH
2
CH
2
Cl
C
2
H
5
ONa
+
C
2
H
5
OH
CH
3
CH
2
CH
2
CH
2
OC
2
H
5
+ CH
3
CH
2
CH=CH
2

Seminarium, część II
52
46. Podaj główne produkty eliminacji oraz okre
śl mechanizm reakcji (E1 lub E2).
a)
b)
c)
d)
e)
47. Na przykładzie 2-bromobutanu, który poddano działaniu silnej zasady (OH
−
) przedstaw
mechanizm reakcji eliminacji E2. Podaj wzór i nazw
ę produktu głównego.
H
3
C
OH
ogrzew.
H
2
SO
4
THF
,
CH
3
CBr + CH
3
ONa
CH
3
CH
3
CH
3
OH
CH
3
CH
2
CH
3
CH
3
OH
C
ogrzew.
H
2
SO
4
THF
,
CH
3
CHBr + C
2
H
5
ONa
CH
3
C
2
H
5
OH
CH
3
CH
2
CH
2
Br + (CH
3
)
3
COK
(CH
3
)
3
COH
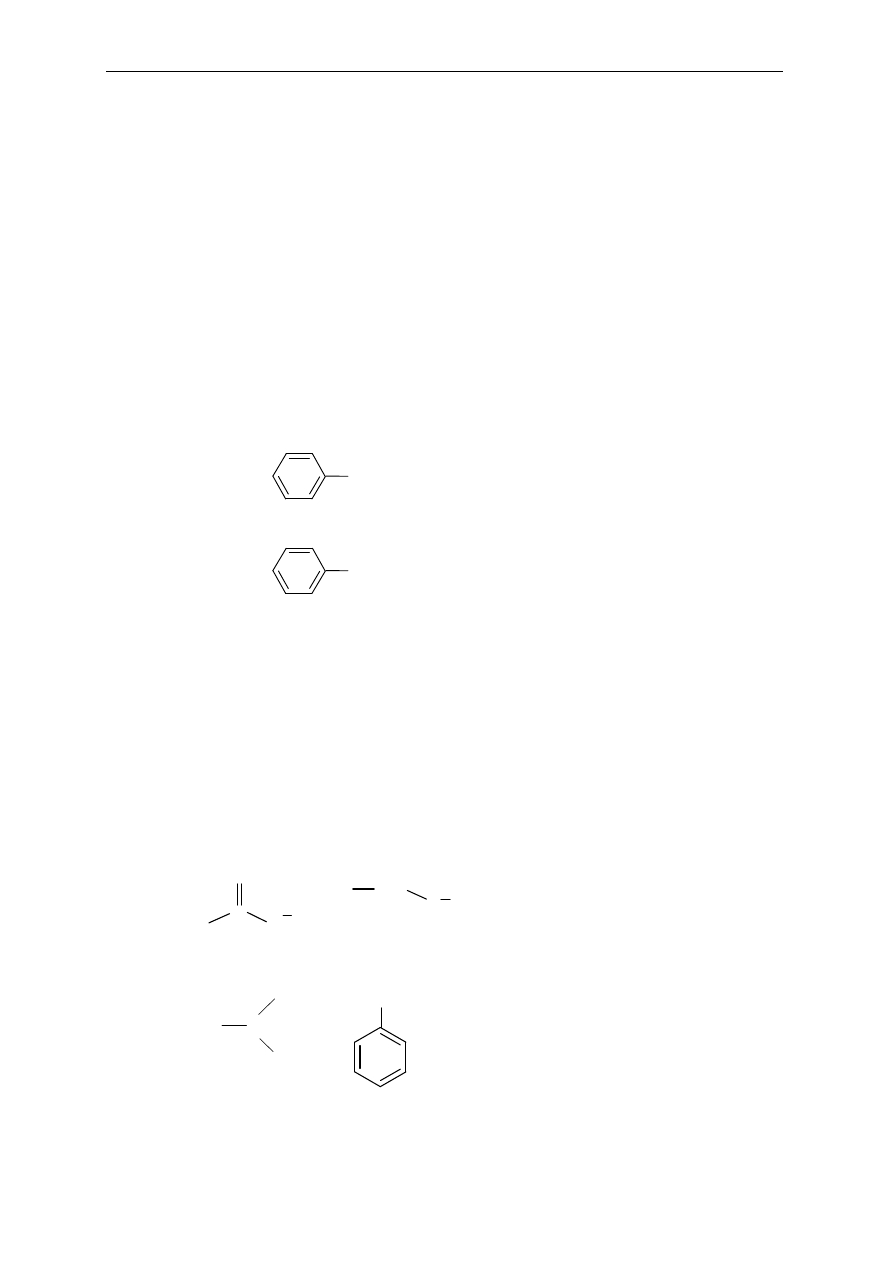
Seminarium, część II
53
10. Efekty indukcyjne i rezonansowe a kwasowo
i zasadowo
zwi zków
10. Efekty indukcyjne i rezonansowe a kwasowo
i zasadowo
zwi zków
10. Efekty indukcyjne i rezonansowe a kwasowo
i zasadowo
zwi zków
10. Efekty indukcyjne i rezonansowe a kwasowo
i zasadowo
zwi zków
organicznych
organicznych
organicznych
organicznych
48. Który ze zwi
ązków w poszczególnych parach jest mocniejszym kwasem i dlaczego?
a) CF
3
CH
2
OH, CH
3
CH
2
OH
b) FCH
2
CH
2
OH, F
2
CHCH
2
OH
c) CF
3
CH
2
CH
2
CH
2
OH, CF
3
CH
2
OH
d) CCl
3
COOH, ClCH
2
COOH
e) ClCH
2
COOH, CH
3
COOH
f) CH
3
COOH, CH
3
CH
2
OH
g) CH
3
COOH,
h) CH
3
CH
2
OH,
49. W poni
ższych parach wskaż mocniejszą zasadę. Uzasadnij wybór.
a) Cl
3
CCOO
-
, ClCH
2
COO
-
b) Cl
3
CCOO
-
, CH
3
COO
-
c) ClCH
2
COO
-
, CH
3
COO
-
d) CH
3
NH
2
, CH
3
CH
2
CH
2
NH
2
e)
f)
OH
OH
O
C
O
H
3
C
O
CH
2
H
3
C
NH
2
N
H
H
3
C
H
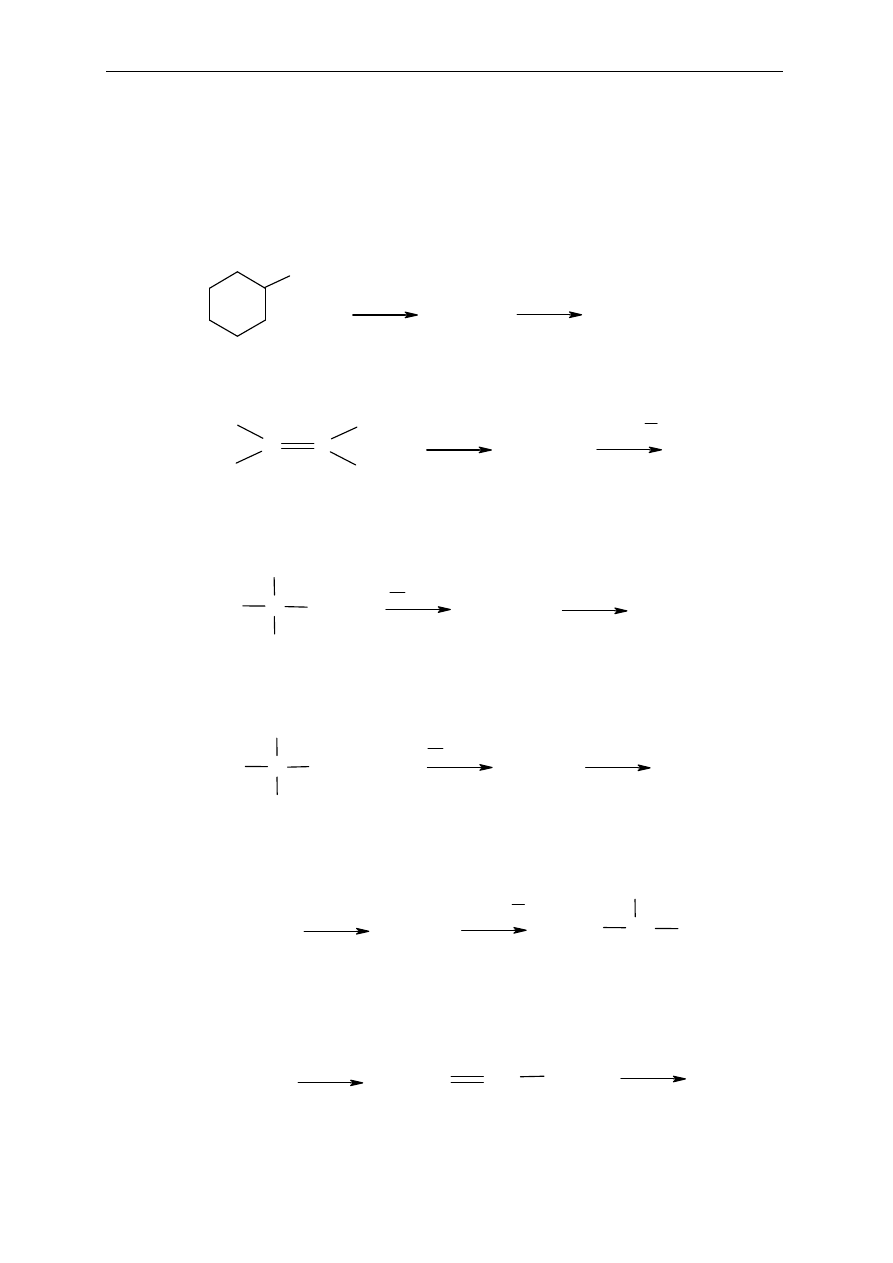
Seminarium, część II
54
11. Podsumowanie
11. Podsumowanie
11. Podsumowanie
11. Podsumowanie
50. Podaj wzory zwi
ązków od A do F na podstawie następujących schematów:
OH
H
3
PO
4
H
Cl
C
C
H
3
C
H
3
C
H
3
C
CH
3
CH
3
CH
3
H
H
I
OH
C
Cl
H
Cl
H
Br
H
3
C
CH
2
CH
3
CH
3
C
OH
H
O
H
Br
Cl
2
OH
H
3
C
CH
2
CH
3
CH
OH
CBr
CH
2
H
Br
CH
3
H
Br
A
B
a)
A
B
b)
A
B
światło
c)
A
d)
2
B
A
B
światło
e)
A
B
f)
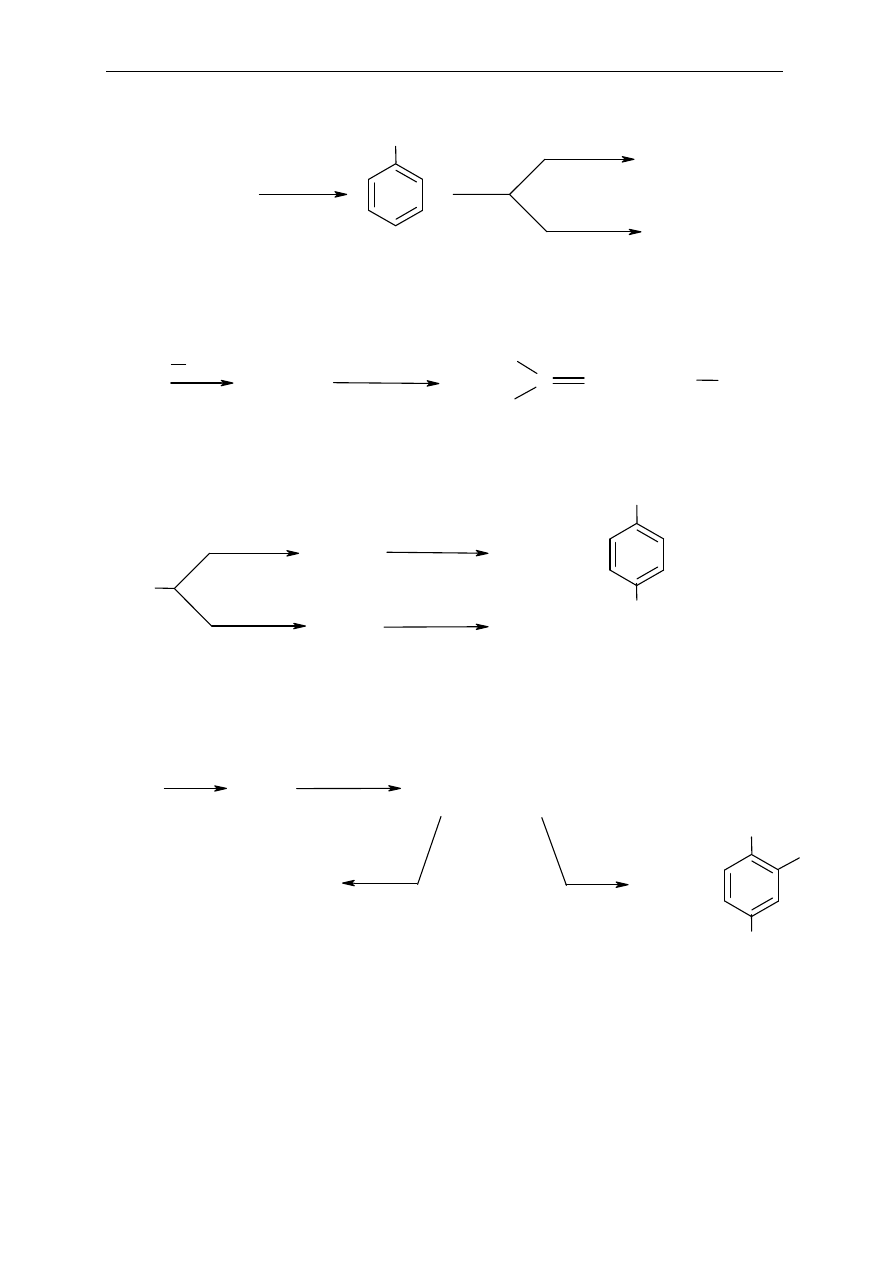
Seminarium, część II
55
CH
3
Cl
2
,
światło
Cl
2
, Fe
C
D
alkilowanie
A
B
+
g)
C
CH
3
Cl
H
3
C
CHO
H
O
O
3
Zn, H
3
O+
O
H
3
C
CH
3
chlorowanie
sulfonowanie
sulfonowanie
chlorowanie
Cl
SO
3
H
CH
3
CH
3
AlCl
3
HNO
3
H
2
SO
4
CH
3
Cl
AlCl
3
CH
3
Cl
AlCl
3
NO
2
E
F
C
A
h)
2
B
1.
2.
+
A
i)
B
+
D
E
A
j)
B
C
D
+
+
Wyszukiwarka
Podobne podstrony:
Materialy do seminarium inz mat 09 10 czesc III
4 konta ksiegowe cwiczenia, Semestr V, Finanse i Rachunkowosc, Wyklady i materialy do seminarium
DO EGZAMINU Makro 2011 12
Materialy do seminarium tech chem 13 14 id 284873
Materialy do seminarium inz mat Nieznany
Seminarium z Metrologii 2011-12 - gr 2 czw, STUDIA, Metrologia
arkusz kalkulacny technilogia V sem zadanie2, do uczenia, materialy do nauczania, rok2010-2011, 23..
Zadanie 1 baza, do uczenia, materialy do nauczania, rok2010-2011, egz I sem, I sem LP wyszukiwanie i
zestawpytan, do uczenia, materialy do nauczania, rok2010-2011, egz I sem, niedziela, V sem lp tech i
LP V sem, do uczenia, materialy do nauczania, rok2010-2011, 09.10.2010, upowszechnianie informacji
Tworzenie wykresów w arkuszu kalkulacyjnym EXCEL, do uczenia, materialy do nauczania, rok2010-2011,
Zadanie 2 baza, do uczenia, materialy do nauczania, rok2010-2011, egz I sem, I sem LP wyszukiwanie i
więcej podobnych podstron