Sprawozdanie z wykonania ćwiczenia nr 26:
„Zależność SEM ogniwa od temperatury.”
Joanna Kiszyniew
Przemysław Korożan
APARATURA: - ultratermostat
elektroda platynowa i kalomelowa
miliwoltomierz cyfrowy V-544
ODCZYNNIKI: - 0.1m roztwór I2 w 4% KI
WYKONANIE:
W ogniwie chemicznym o budowie:
![]()
zachodzą procesy:
na anodzie: 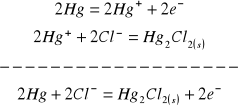
na katodzie: ![]()
co sumarycznie daje: ![]()
Na podstawie pomiaru siły elektromotorycznej ogniwa oraz jej zmiany z temperaturą można oznaczyć entalpię swobodną, entropię oraz entalpię opisanej reakcji. Podczas pracy ogniwa odwracalnego w stałej temperaturze i pod stałym ciśnieniem:
![]()
gdzie: ![]()
- entalpia swobodna
![]()
- liczba moli elektronów wymieniona w reakcji (tu: z = 2)
![]()
- siła elektromotoryczna
![]()
- stała Faradaya
Z równania Gibbsa-Helmholtza:
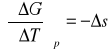
stąd:
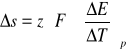
Znając ![]()
oraz ![]()
można obliczyć ![]()
na podstawie równania:
![]()
Wyszukiwarka
Podobne podstrony:
Prawo inżynierskie i ochrona własności intelektualnych. Wykład 3, Studia, Politechnika Łódzka - Pend
Testy biodegradacji, Studia, Politechnika
Chf9, Studia, Politechnika
Wyznaczanie stałej reakcji szybkości zmydlania estru, Studia, Politechnika
CH.F.L9, Studia, Politechnika
ZAKAAD CHEMI FIZYCZNEJ, Studia, Politechnika
C15, Studia, Politechnika
podstawowe informacje o ochronie prawnej wzorów przemysłowych, Studia - Politechnika Śląska, Zarządz
Sprawko spawalnictwo 1, studia, studia Politechnika Poznańska - BMiZ - Mechatronika, 2 semestr, obro
dziadek25, Studia, Politechnika
4 2 vademecum echosondy (w tym przykładzie wodnej), studia, studia Politechnika Poznańska - BMiZ - M
LABORKA7, Studia, Politechnika
Wyznaczanie stopnia asocjacji kwasu octowego w rozpuszczalni, Studia, Politechnika
deacon1, Studia, Politechnika
Destylacja wojtek, Studia Politechnika Poznańska, Semestr I, Chemia, Chemia laboratoria, Destylacja
Liczby przenoszenia jonów, Studia, Politechnika
103, Studia Politechnika Poznańska, Semestr II, I pracownia fizyczna, LABORKI WSZYSTKIE, FIZYKA 2, F
poprawione7, Studia, Politechnika
CHEMIA~7, Studia, Politechnika
więcej podobnych podstron