1
Tytuł: Czy Populacyjny Program Wczesnego Wykrywania Raka Piersi spełnia kryteria sformułowane przez
J.M.G Wilson’a według których powinny być wprowadzane badania przesiewowe?
Autor: Agnieszka Dyzmann-Sroka
Jednostka: Zakład Epidemiologii i Profilaktyki Nowotworów, Wielkopolskie Centrum Onkologii im. M.
Skłodowskiej-Curie, ul. Garbary 15, 61-866 Poznań
Tekst: Celem badań przesiewowych w onkologii jest przede wszystkim wykrycie choroby we wczesnej fazie
jej rozwoju, kiedy skuteczność leczenia jest najwyższa, gdyż w większości nowotworów obserwowana jest
silna zależność między przeżyciem a stopniem zaawansowania choroby, określonym zazwyczaj rozmiarem
guza pierwotnego lub ograniczeniem procesu nowotworowego do stanu miejscowego. Niektóre typy
nowotworów poprzedzają stany przednowotworowe, których wystąpienie zwiększa ryzyko rozwinięcia się raka
w najbliższej przyszłości. Podjęcie wczesnego leczenia przy jednoczesnej wysokiej podatności na leczenie,
zapobiega powstawaniu nowotworu.
Teoretycznie istnieje wiele różnych nowotworów, które można byłoby wykrywać w badaniu
przesiewowym. W praktyce przy podejmowaniu decyzji o wprowadzeniu badania przesiewowego należy brać
pod uwagę wiele przesłanek – już w 1968 roku sformułowano kryteria [1], według których powinny być
wprowadzane badania przesiewowe, należały do nich:
1. Ważny problem zdrowotny i społeczny.
2. Dobrze poznana i rozumiana naturalna historia choroby.
3. Możliwość wyleczenia choroby we wczesnym stadium.
4. Znacznie lepsze wyniki leczenia we wczesnym stadium.
5. Możliwość wyleczenia wykrytej choroby.
6. Istnienie odpowiednich testów pozwalających wykryć chorobę.
7. Testy te muszą być akceptowalne.
8. Należy zapewnić masowość i powtarzalność skryningu.
9. Korzyści przewyższają ryzyko.
10. Populacyjne koszty badań nie przewyższają kosztów leczenia.
Warto zbadać, czy Populacyjny Program Wczesnego Wykrywania Raka Piersi (stanowiący jedno z zadań
Narodowego programu zwalczania chorób nowotworowych [2]) w formie realizowanej obecnie w Polsce
spełnia wymogi prowadzenia badań przesiewowych zdefiniowane przez J. M. G. Wilsona?
Czy
rak
piersi
jest
ważnym
problemem
zdrowotnym
i
społecznym?
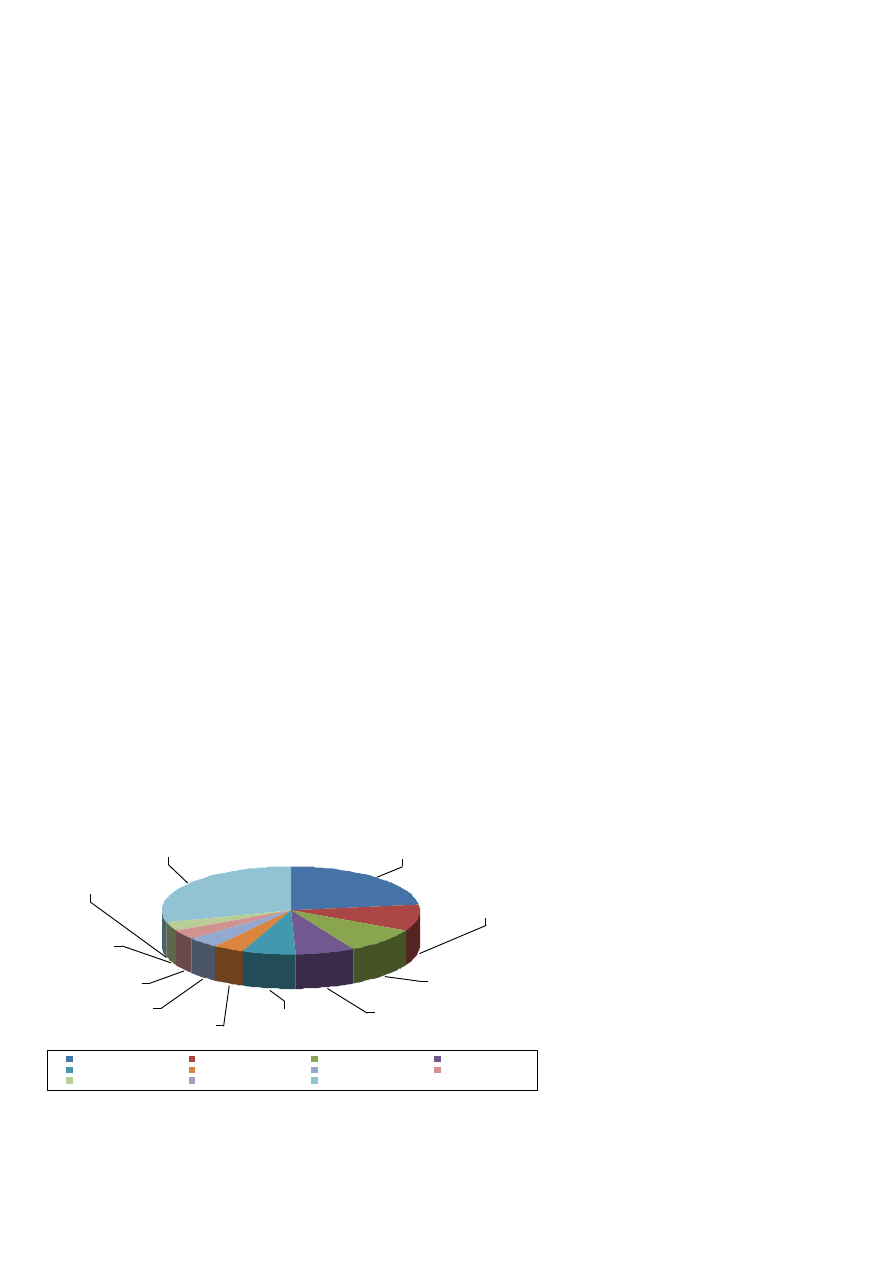
Jest to najczęściej występujący u kobiet
nowotwór złośliwy stanowiący prawie
23% wszystkich nowych przypadków
rozpoznawanych u kobiet na świecie
[3;4] – ryc. 1.
Biorąc pod uwagę ogólne starzenie się
populacji świata, oraz fakt, iż 78%
wszystkich
przypadków
tego
nowotworu rozpoznawanych jest u
kobiet w wieku powyżej 50 lat - liczba
zachorowań
będzie
wzrastać
w
kolejnych
latach.
W
2002
roku
zaobserwowano 1 151 298 nowych
zachorowań, z czego około 636 000
przypadków w krajach rozwiniętych,
514 000 w krajach rozwijających się.
Częstość występowania raka piersi
uważana jest za niską, gdy współczynnik standaryzowany zachorowalności wynosi mniej niż 20/100 000 (taki
obserwowany jest w większości krajów Afryki Subsaharyjskiej, w Chinach i innych krajach Azji Wschodniej -
Zachorowania na nowotwory złośliwe na świecie
0,00%
1 151 298;
22,75%
493 243; 9,75%
472 687; 9,34%
386 891; 7,65%
330 518; 6,53%
204 499; 4,04%
198 783; 3,93%
184 043; 3,64%
146 723,0;
2,90%
1 491 972;
29,48%
pierś
szyjka macicy
jelito grube
płuco
żołądek
jajnik
trzon macicy
wątroba
przełyk
trzustka
Inne
Ryc. 1 Rozkład zachorowalności na nowotwory złośliwe u kobiet na świecie
(źródło GLOBOCAN 2002).
2
z wyjątkiem Japonii). Najwyższe współczynniki zachorowalności (tj. od 80-90/100 000) rejestrowane są w
Ameryce Północnej, w niektórych regionach Ameryki Południowej, m.in. w Brazylii i Argentynie, w Europie
Północnej i Zachodniej oraz w Australii [3;4]. Różnica pomiędzy granicznymi wartościami wskaźników w
krajach o najniższej zachorowalności (Mozambik i Haiti 4/100 000) a krajami osiągającymi wartości
maksymalne (Belgia 92 i USA 101/100 000) różnią się aż o 97 punktów. Polska należy do krajów
charakteryzujących się średnim poziomem standaryzowanych współczynników zachorowalności na raka piersi,
niemniej w ciągu ostatnich 40-stu lat liczba zachorowań wzrosła o 373,9%; przy wzroście populacji na
poziomie 24,6%.
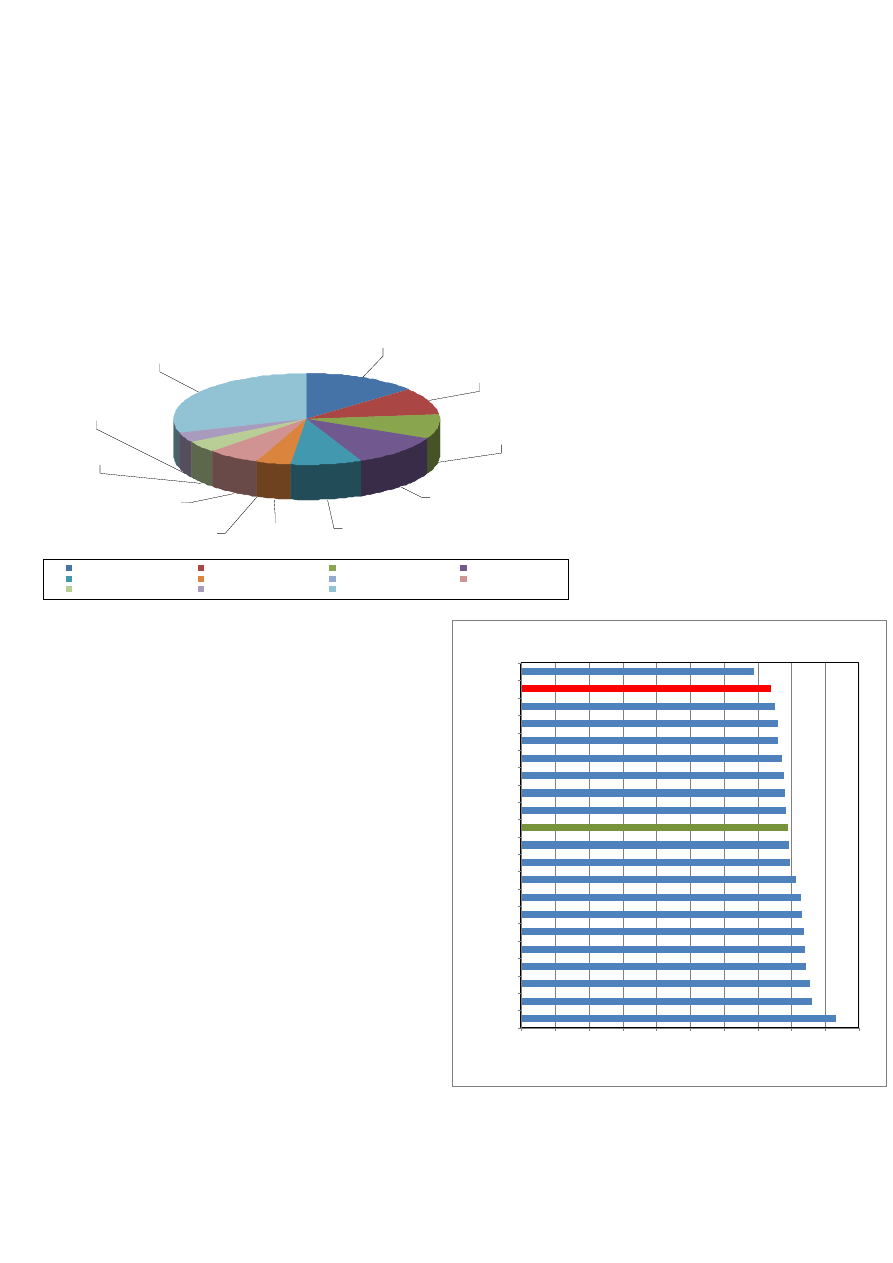
W XXI wieku rak piersi pozostaje również najczęstszą przyczyną zgonów nowotworowych u kobiet (stanowi
około 14% ogółu zgonów) – ryc. 2 [4; 5]
Szacuje się, iż w 2002 r. rak ten był
przyczyną 410 712 zgonów u kobiet
na świecie [3; 4]. Najwyższe
współczynniki
(standaryzowane)
umieralności obserwuje się na
Malcie i Cyprze (po 30/100 000),
najniższe w Mozambiku (3/100 000)
i na Haiti (2/100 000). Polska należy
do krajów o średnim wskaźniku
umieralności na raka piersi. Tym, co
wyróżnia niekorzystnie Polskę na tle
innych krajów Europy są jedne z
najniższych odsetki przeżyć 5-cio
letnich chorych na raka piersi – ryc.
3 [4].
Czy naturalna historia choroby jest dobrze
poznana i rozumiana?
Cechy naturalnego przebiegu choroby wpływają
silnie na potencjalne korzyści wynikające z
wykonania badań przesiewowych. Skuteczność badań
przesiewowych jest zależna od średniego okresu
wczesnej diagnozy (ang. mean sojourn time). W
każdym typie nowotworu długość MST jest różna i
zależy od czynników patologicznych i osobniczych.
Naturalnego przebiegu raka piersi nadal nie poznano
dogłębnie, niemniej jest to nowotwór, dla którego
udowodniono empiryczne korzyści wynikające z
wczesnego wykrycia [7]. Dlatego w programie
profilaktyki raka piersi celem badania przesiewowego
nie jest zapobieganie wystąpieniu raka, lecz wykrycie
choroby w jak najwcześniejszej fazie i zwiększenie
prawdopodobieństwa trwałego wyleczenia.
Czy w raku piersi onkolodzy mają możliwość
wyleczenia choroby we wczesnym stadium? Czy
wyniki leczenia we wczesnym stadium są istotnie
lepsze?
Czy
istnieje
możliwość
wyleczenia
wykrytej choroby?
Przeżycia 5-cio letnie C50 wg. Eurocare-4
93,4
86,3
85,7
84,5
84,1
83,7
83,1
82,8
81,4
79,7
79,5
79
78,4
78,2
77,8
77,3
76,2
76
75,3
73,9
68,9
0
10
20
30
40
50
60
70
80
90
100
Islandia
Szewcja
Finlandia
Szwajcaria
Norwegia
Włochy
Holandia
Hiszpania
Austria
Belgia
Irlandia Płn
Europa
Walia
Niemcy
Anglia
Szkocja
Irlandia
Malta
Słowenia
Polska
Czechy
Odsetek przeżyć 5-cio letnich
Zgony na nowotwory z
łośliwe na świecie
0,00%
410 712; 14,03%
273 505; 9,34%
250 532; 8,56%
330 786; 11,30%
254 297; 8,69%
124 860; 4,26%
181 439; 6,20%
124 730; 4,26%
107 479; 3,67%
869 556; 29,70%
pier
ś
szyjka macicy
jelito grube
p
łuco
żołądek
jajnik
trzon macicy
w
ątroba
prze
łyk
trzustka
Inne
Zgony na nowotwory z
łośliwe na świecie
0,00%
410 712; 14,03%
273 505; 9,34%
250 532; 8,56%
330 786; 11,30%
254 297; 8,69%
124 860; 4,26%
181 439; 6,20%
124 730; 4,26%
107 479; 3,67%
869 556; 29,70%
pier
ś
szyjka macicy
jelito grube
p
łuco
żołądek
jajnik
trzon macicy
w
ątroba
prze
łyk
trzustka
Inne
Ryc. 2 Rozkład umieralności na nowotwory złośliwe u kobiet
na świecie (źródło GLOBOCAN 2002) [3; 4; 5].
Ryc. 3 Przeżycia 5-cio letnie kobiet chorych na raka piersi (źródło
EUROCARE 4) [6]
3
Rak piersi to nowotwór, dla którego udowodniono empiryczne korzyści wynikające z wczesnego wykrycia [7].
Jak dowodzi profesor Wronkowski [8] wykrycie raka o jedno stadium wcześniej zwiększa szanse przeżycia
chorych mniej więcej o 25% - tab. 1
Czy
istnieją
odpowie
testy
pozwalające wykryć chorobę i są to
testy akceptowane przez kobiety?
Jak
wykazały
duże
badania
randomizowane
przeprowadzone
w
latach 1976-1990, badania przesiewowe
wczesnego wykrywania raka piersi
oparte
na
mammografii
mogą
zmniejszyć umieralność z powodu tego
raka średnio o 25% u kobiet w wieku
50-69
lat
[4].
Mammografia
(rentgenowskie badanie piersi) jest
obecnie
najlepszym
sposobem
wykrywania raka piersi w jego wczesnym stadium
rozwoju. Jest to ponadto badanie nieinwazyjne i
bezbolesne (chociaż należy pamiętać, że ucisk stosowany w celu uzyskania zdjęć wysokiej jakości i obniżenia
dawki promieniowania jest odczuwany przez kobiety jako dyskomfort) [9].
Czy
zapewniono
masowość
i
powtarzalność
skryningu?
Badania w ramach programu profilaktyki raka piersi
realizowane są w Polsce od 2006 roku. Do badań
kwalifikują się kobiety w wieku 50-69 lat, które nie miały
wykonanego badania mammograficznego w ciągu
ostatnich 24 miesięcy i nie były dotychczas leczone z
powodu raka piersi. Od roku 2007 kobiety z grupy ryzyka
zapraszane są poprzez imienne zaproszenia wysyłane na
adres domowy drogą pocztową (w 2009 roku wysłano
zaproszenia do prawie 130 000 Wielkopolanek). Dzięki
Systemowi Informatycznego Monitorowania Profilaktyki
(SIMP) prowadzony jest stały monitoring realizacji badań
i weryfikowane są uprawnienia do badań oraz stopień
realizacji zaleceń. Od 2007 roku Płatnik nie limituje
badań tzn. finansowane są faktyczne wykonania.
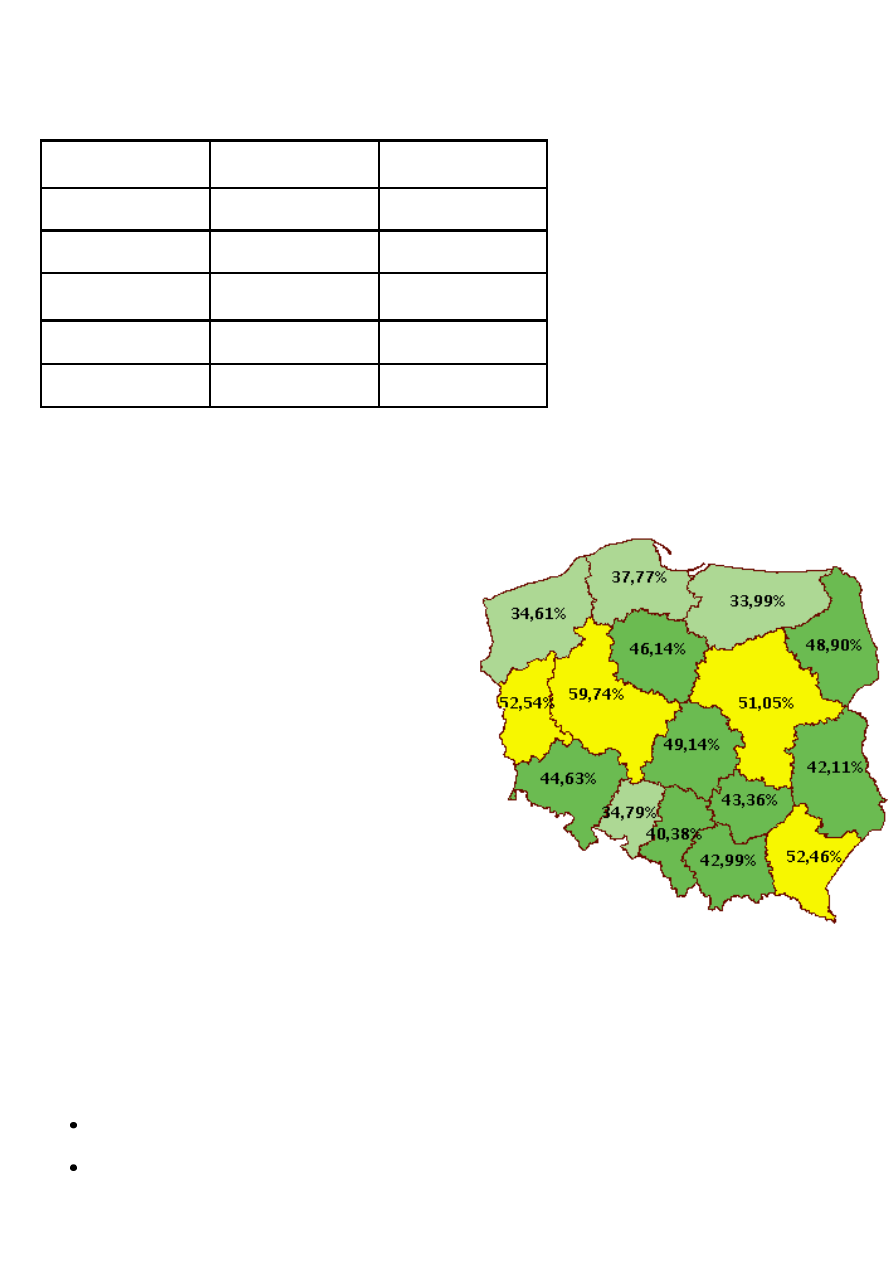
W 2009 roku objęto zaproszeniami na badania 46% Polek
(i aż 60% Wielkopolanek!) ryc. 4, co miało wpływ na
zgłaszalność kobiet na badania – w bieżącym objęciu
badaniami Wielkopolska zajmuje wysoką 3 pozycję w
Polsce.
Czy oczekiwane korzyści przewyższają ewentualne ryzyko?
Badanie mammograficzne jest badaniem rentgenowskim, dlatego też ewentualne korzyści wynikające z
wczesnego wykrycia raka piersi u kobiety potencjalnie zdrowej (tzn. zgłaszającej się do badań profilaktycznych
bez objawów raka piersi) będzie możliwe tylko przy wysokokwalifikowanej i doświadczonej kadrze pracującej
na sprzęcie wysokiej i stale monitorowanej jakości. Kryteria przyjęte w 1968 roku przez Wilson’a uznaje się
obecnie za zbyt słabe i dlatego w Polsce w 2009 roku badania realizowane były dodatkowo w oparciu o:
Zalecenie Rady Unii Europejskiej z dnia 2 grudnia 2003 r. w sprawie badań przesiewowych w kierunku
raka (2003/878/WE: Dz.U.L. 327/34-38),
European guidelines for quality assurance in breast cancer screening and diagnosis. Fourth edition [10],
stopień
zaawansowania
stadium
zaawansowania
odsetek przeżyć
5-cio letnich
0
przedinwazyjne
100
I
miejscowe
75
II
lokoregionalne
wczesne
50
III
lokoregionalne
późne
25
IV
uogólnione
5
Tabela 1 Prawdopodobieństwo przeżycia 5-ciu lat w zależności
od stadium zawansowania nowotworu [8]
Ryc. 4 Bieżące objęcie populacji zaproszeniami do programu
profilaktyki raka piersi - data generacji raportu: 2010-01-01.
Średnia wartość: 45,62 %

4
• Wymagania określone w zarządzeniu nr 81/2008/DSOZ Prezesa NFZ,
• Rozporządzenie Ministra Zdrowia z dnia 25 sierpnia 2005 r. w sprawie warunków bezpiecznego
stosowania promieniowania jonizującego dla wszystkich rodzajów ekspozycji medycznej (Dz. U. Nr
194, poz. 1625),
• Rozporządzenie Ministra Zdrowia z dnia 21 sierpnia 2006 r. w sprawie szczegółowych warunków
bezpiecznej pracy z urządzeniami radiologicznymi (Dz. U. Nr 180, poz. 1325),
• Rozporządzenie Ministra Zdrowia z dnia 30 sierpnia 2009 r. w sprawie świadczeń gwarantowanych z
zakresu programów zdrowotnych (Dz. U. Nr 140, poz. 1148).
Jakość sprzętu badana jest regularnie przez Sanepid, oddziały NFZ oraz kontrole fizyków zatrudnionych w
Wojewódzkich Ośrodkach Koordynujących. Jakość zdjęć bada zespół audytorów klinicznych zatrudnionych
przez Centralny Ośrodek Koordynujący. Wysoką jakość kadry i sprzętu potwierdzają osiągane parametry takie
jak:
czułość na poziomie 91% (wytyczne europejskie wartość akceptowana 80%, pożądana >90%) [10],
swoistość na poziomie 97% (wytyczne europejskie wartość akceptowana 60%, pożądana >90%) [10],
odsetek powtórnych wezwań na poziomie 3,6% (wytyczne europejskie – poziom akceptowany <7%)
pożądany <5%, [10],
wskaźnik wykrytych raków dla 2006 = 6,6/1000; dla 2007 = 6,5/1000; dla 2008 5,5/1000 (wytyczne
europejskie poziom akceptowany i pożądany 5/1000 badań) [10],
• średnia wieku mammografu zmniejszyła się z 9 lat w 2006 roku do 6 lat w roku 2009
• ośrodki współpracują z fizykiem medycznym,
• Świadczeniodawcy posiadają sprzęt do kontroli jakości,
wykonywane są testy kontroli jakości podstawowe i specjalistyczne
Czy populacyjne koszty badań nie przewyższają kosztów leczenia?
Analiza ekonomiczna badań przesiewowych (efekt vs. koszt) stanowi bardzo istotny aspekt oceny tych badań.
W krajach skandynawskich wykazano, że koszty prowadzenia skryningu nie są wysokie. W analizach kosztów
społecznych prowadzenia populacyjnych i aktywnych badań przesiewowych posługiwano się czysto
ekonomicznymi wskaźnikami:
koszt → efekt → dochód [7]
Jako dowód efektywności dobrze zorganizowanego programu przyjmowano jego dochód, rozumiany jako
liczba wykrytych wczesnych stadiów przednowotworowych przy równoczesnym obliczeniu różnicy kosztów
leczenia i rehabilitacji, oraz czynników społecznych w porównaniu do kosztów zaawansowanego procesu
nowotworowego.
Jak obliczył profesor Wronkowski [8] koszt badania jednej kobiety w badaniu przesiewowym raka piersi
prowadzonym w Centrum Onkologii – Instytucie wynosił około 50 zł. Przy założeniu, że wykrywa się 5
przypadków raka na 1 000 badanych kobiet w wieku powyżej 50 lat (w tym 2 przypadki wczesnego raka):
• koszt wykrycia 1 przypadku raka piersi wynosi 4 000 $,
• koszt wykrycia 1 przypadku wczesnego raka piersi wynosi 10 000 $
• koszt przedłużenia 1 roku życia kobiety, u której wykryto raka piersi w skryningu jest bardzo niski i
wynosi poniżej 1 000 $ i jest co najmniej 7-krotnie niższy od kosztu przedłużenia 1 roku życia u kobiet,
u których został on wykryty w wyniku rutynowych badań, czyli najczęściej po wystąpieniu objawów
choroby nowotworowej!
Elementem koniecznym oceny badania przesiewowego powinna być analiza epidemiologiczna zagrożenia
danej populacji nowotworami przed i po wprowadzeniu badań przesiewowych. Przed wprowadzeniem badań
przesiewowych należy określić ryzyko wystąpienia nowotworu w zależności od wieku, zachorowalność i
umieralność oraz wskaźniki przeżyć. Drugim elementem, który powinien zostać określony, jest stopień
zaawansowania choroby w momencie rozpoznania. Potencjalna liczba zgonów nowotworowych, którym można
zapobiec, oraz liczba lat życia, które uda się zyskać dzięki badaniom przesiewowym, jest proporcjonalna do
poziomu ryzyka zachorowania na dany nowotwór. Ma to decydujący wpływ na opłacalność wprowadzenia
badania przesiewowego.
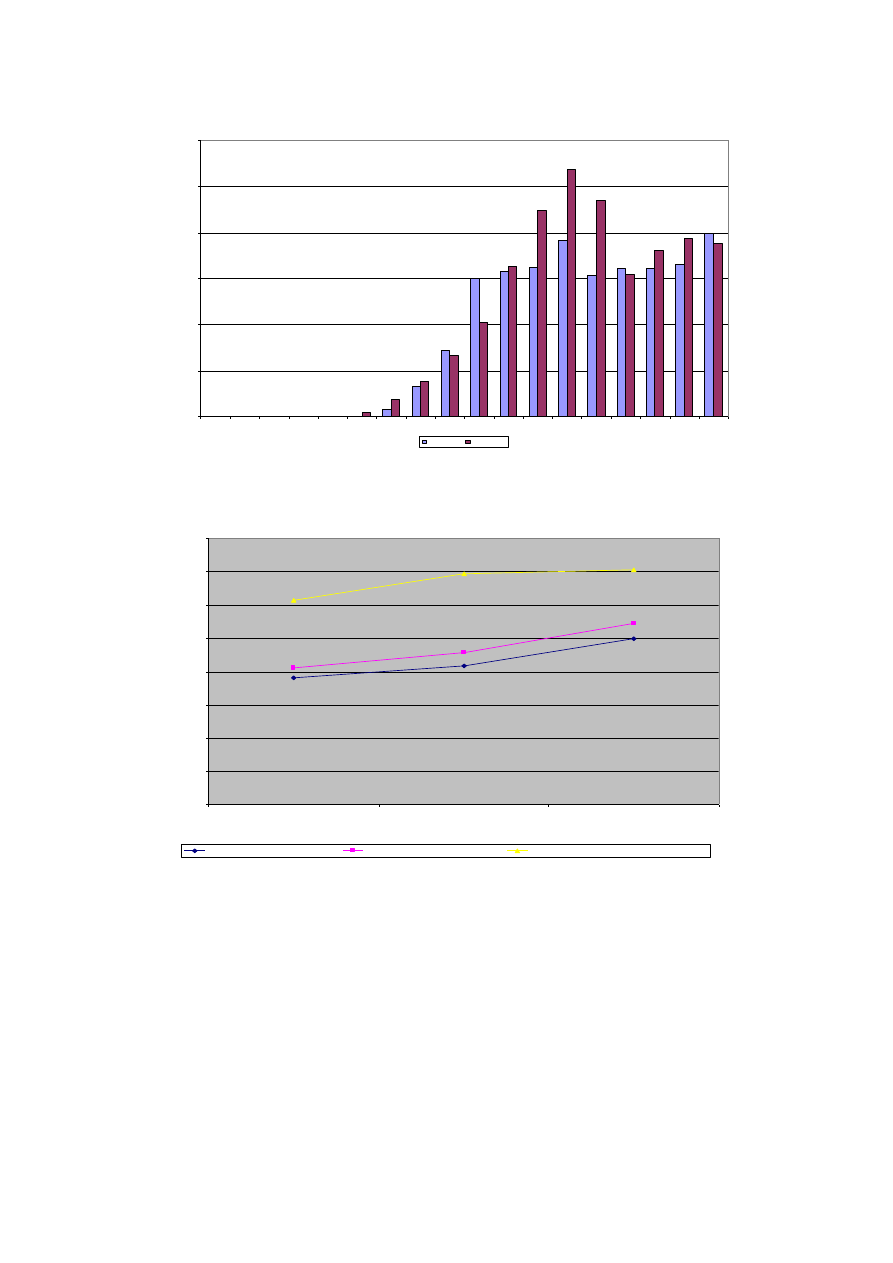
Jak pokazują dane Wielkopolskiego Rejestru Nowotworów po wprowadzeniu początkowo oportunistycznego a
od 2006/2007 roku aktywnego skryningu raka piersi zdecydowanie zwiększyła się liczba raków piersi
wykrywanych w grupie 50-69 lat (ryc. 5), co istotne stopniowo zwiększa się odsetek raków wykrywanych w
5
najniższym (tzn. miejscowym) stadium zaawansowania, przy czym najwyższy odsetek raków w stadium
miejscowym zanotowano w grupie kobiet uczestniczących w skryningu (ryc. 6).
Literatura:
1. Wilson J.M.G., Junger G. Principles and Practice of Screening for Disease. WHO 1968
2. Ustawa z dnia 1 lipca 2005 r. o ustanowieniu programu wieloletniego „Narodowy program zwalczania
chorób nowotworowych” (Dz.U.05.143.1200),
3. Globocan database, (2002); www-dep.iarc.fr/globocan/database.htm
4. Boyle P., Levin B. – red., (2008) World Cancer Report 2008, WHO - Lyon.
5. Word Heath Organization (2008). The global burden of disease: 2004 update. Switzerland; tabela strona 54-
58.
6. Annals of Oncology. Official Journal of the European Society for Medical Oncology (2003). “Survival of
Cancer Patients in Europe: the EUROCARE-3 Study” – OXFORD University Press Vol. 14; 2003 Suppl. 5
Rak piersi - Kobiety, Wielkopolska
38
42
50
41
46
54
62
70
71
0
10
20
30
40
50
60
70
80
2005 rok
2006 rok
2007 rok
rok
s
ta
d
iu
m
m
ie
js
c
o
w
e
-
%
stadium miejscow e - kobiety ogółem
stadium miejscow e - kobiety 50-69 lat
stadium miejscow e - kobiety 50-69 lat screening
Zachorowalność na raka piersi w grupach wieku w Wielkopolsce
0
0
0
0,7
0,7
0,8
8,6
32,7
71,7
149,8
157,9
162,2
191,2
154,1
160,8
160,8
165,2
199,8
0
0
0
0
0,7
4,9
18,3
38,5
66,5
103,3
163,7
224,4
269,3
235,1
154,5
181,1
194,4
188,3
0
50
100
150
200
250
300
00-04
09-maj
14-paź 15-19
20-24
25-29
30-34
35-39
40-44
45-49
50-54
55-59
60-64
65-69
70-74
75-79
80-84
85+
w
sp
ół
. s
ur
ow
y
1999 rok
2007 rok
Ryc. 5 Zmiany w strukturze nowo-rozpoznanych raków piersi w podziale na grupy wieku (źródło Wielkopolski Rejestr Nowotworów).
Ryc. 6 Odsetek nowych przypadków raka piersi zdiagnozowanych w stadium miejscowym (źródło Wielkopolski Rejestr Nowotworów)

6
and
“Survival
of
Cancer
Patients
in
Europe:
the
EUROCARE-4
Study”
–
www.eurocare.it/Scripts/Document.htm
7. Didkowska J.,Wojciechowska U. (opr.). Populacyjne programy przesiewowe w onkologii. Centrum
Onkologii – Instytut, Warszawa 2007.
8. Wronkowski Z., Zwierko M., Nowacki M.P. „Program modelowego skryningu raka piersi i raka szyjki
macicy w Polsce, 1999-2000; 2002
9. Lamch K., Dyzmann-Sroka A., Kycler W., Kubiak A., Szczepański Ł., Trojanowski M., Śmigielska M.,
ABC mammografii – mini poradnik dla kobiet. Wielkopolskie Centrum Onkologii, 2009
10.
Perry N (i współ.). European guidelines for quality assurance in breast cancer screening and diagnosis.
Fourth edition. European Communities, 2006.
O autorze: Agnieszka Dyzmann-Sroka, ukończyła w 1998 roku wydział filozofii na Uniwersytecie im. A.
Mickiewicza w Poznaniu oraz w 2008 roku Oddział Kształcenia Podyplomowego Wydziału Lekarskiego II
Uniwersytetu Medycznego im. K. Marcinkowskiego w Poznaniu. Jako kierownik Zakładu Epidemiologii i
Profilaktyki Nowotworów (w strukturach, którego znajdują się: Wielkopolski Rejestr Nowotworów, Biuro
Programu Prewencji Pierwotnej oraz Wojewódzki Ośrodek Koordynujący Populacyjny Program Wczesnego
Wykrywania Raka Piersi) w sposób szczególny angażuje się w upowszechnianie w środowisku medycznym
wiedzy o epidemiologii nowotworów złośliwych a wśród Wielkopolan zaleceń Europejskiego Kodeksu Walki z
Rakiem.
Wyszukiwarka
Podobne podstrony:
Populacyjny program wczesnego wykrywania raka piersi
Rozpoznawanie raka piersi, Dla wczesnego wykrywania raka piersi bardzo ważne znaczenie mają systemat
SPOŁECZNE ASPEKTY WCZESNEGO WYKRYWANIA RAKA PIERSI PO
Ocena skuteczności programów profilaktycznych dotyczacych raka piersi w regionie lubelskim
Czynniki ryzyka raka piersi według wytycznych — kopia
PROGRAM PROFILAKTYKI RAKA PIERSI
Profilaktyka i metody wczesnego rozpoznawania raka gruczołu piersiowego, Pomoce naukowe, studia, med
PROGRAM PROFILAKTYKI RAKA PIERSI
druk nr XIX 21 zalacznik Program profilaktyki raka piersi 2008 — kopia
Ocena toksyczności i skuteczności dwulekowego programu złożonego z docetakselu i cisplatyny w leczen
Renata Zygan Wczesne wykrywanie wad wzroku u dzieci w wieku przedszkolnym i wczesnosno szkolnym z z
Zachowania zdrowotne kobiet w zakresie zapobiegania wczesnego wykrywania stanow przedrakowych i raka
Inhibitory aromatazy w leczeniu uzupełniającym raka piersi
Leczenie chorych na raka piersi w ciąży VI LEK
więcej podobnych podstron