
Opracowanie na zaliczenie
praktyczne z mikrobów
Wg informacji przekazanych
przez dr R by efa
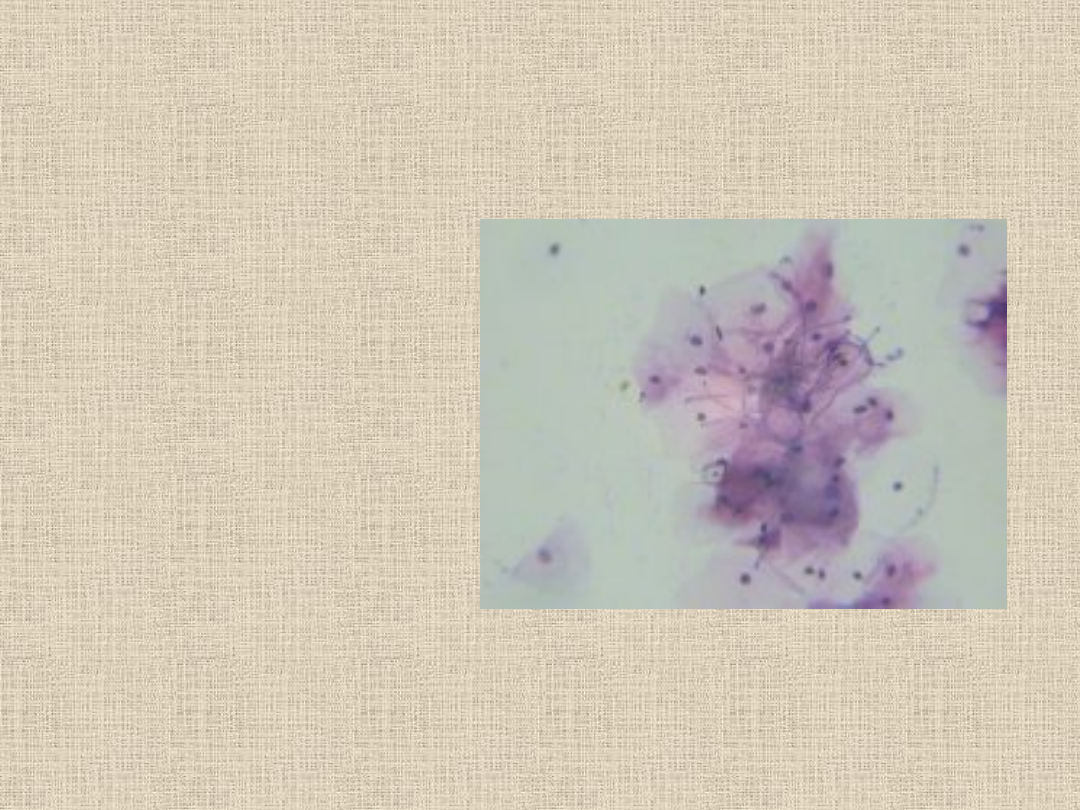
Grzyby w plwocinie
•Preparat bezpośredni
•Metoda Grama
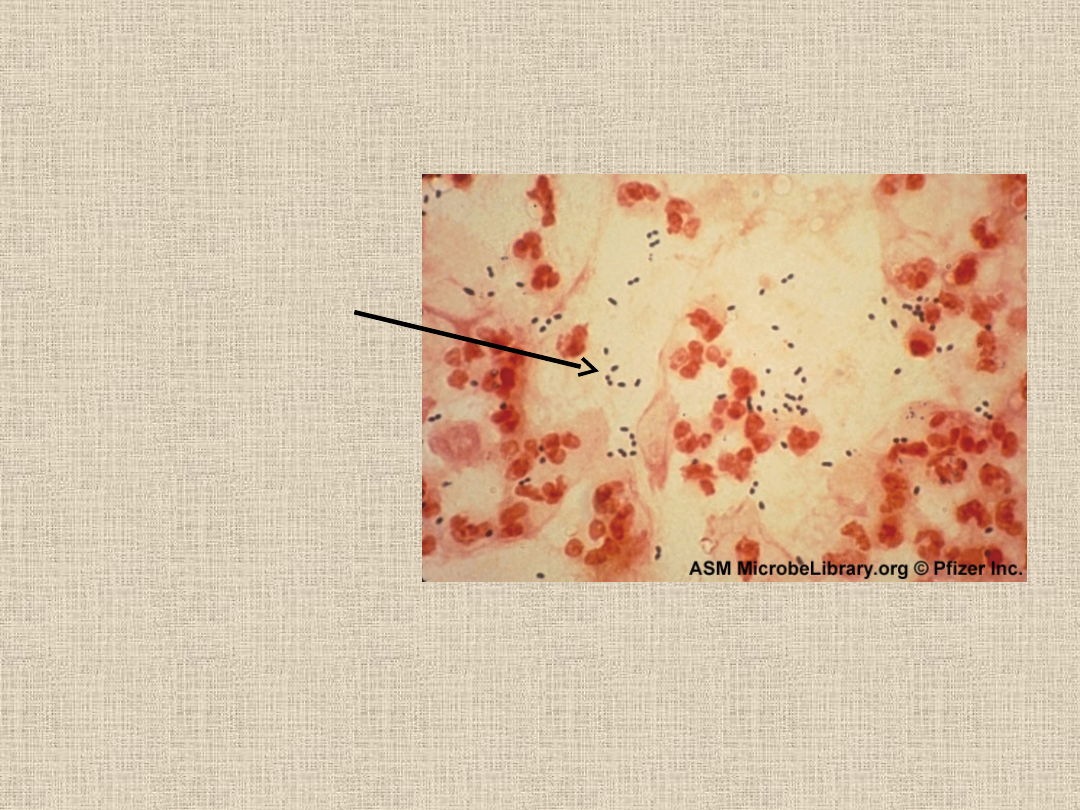
Streptococcus pneumoniae
•Preparat bezpośredni
•Barwienie metodą
Grama
•Dwoinki pomiędzy
leukocytami i
nablonkami
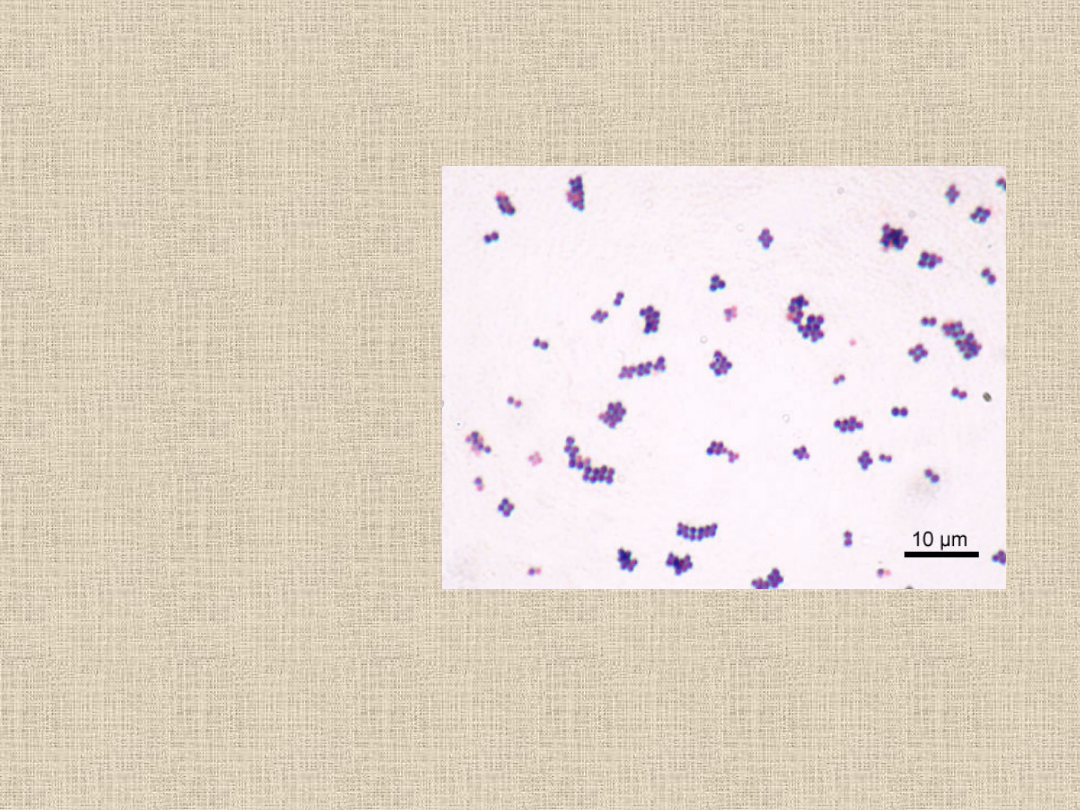
Staphylococcus aureus-
gronkowce
•Preparat pośredni
•Metoda Grama
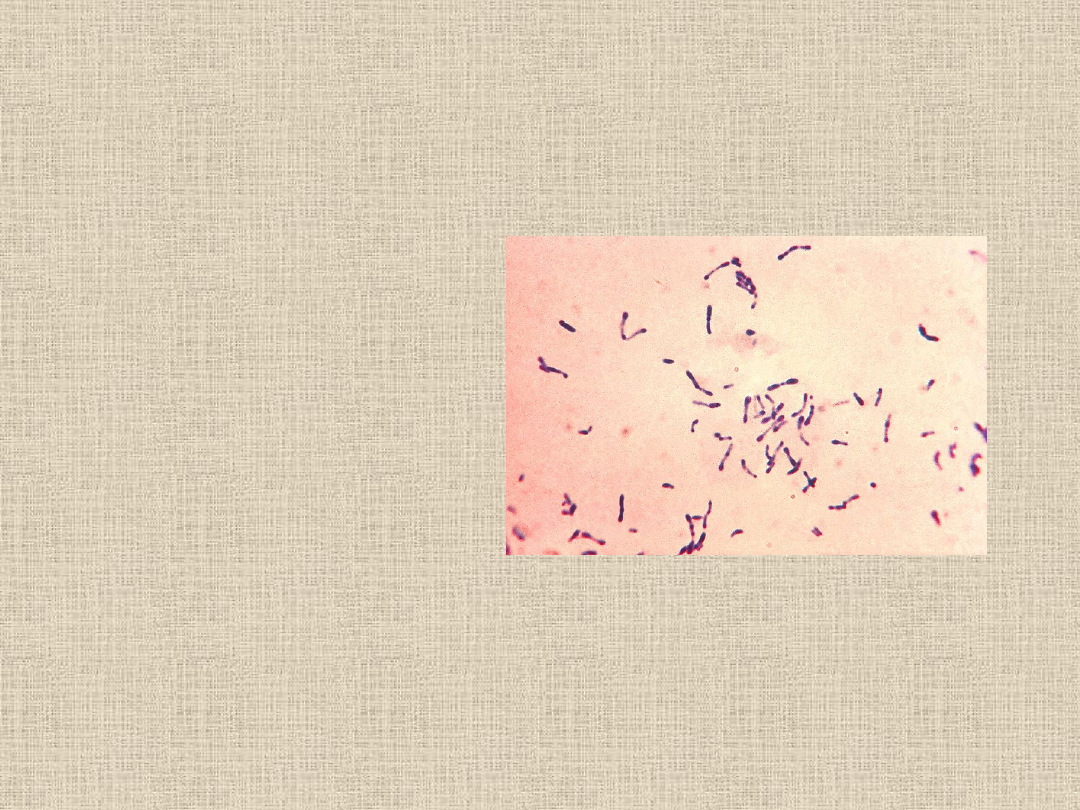
Maczugowce
•Preparat pośredni
•Metoda Grama
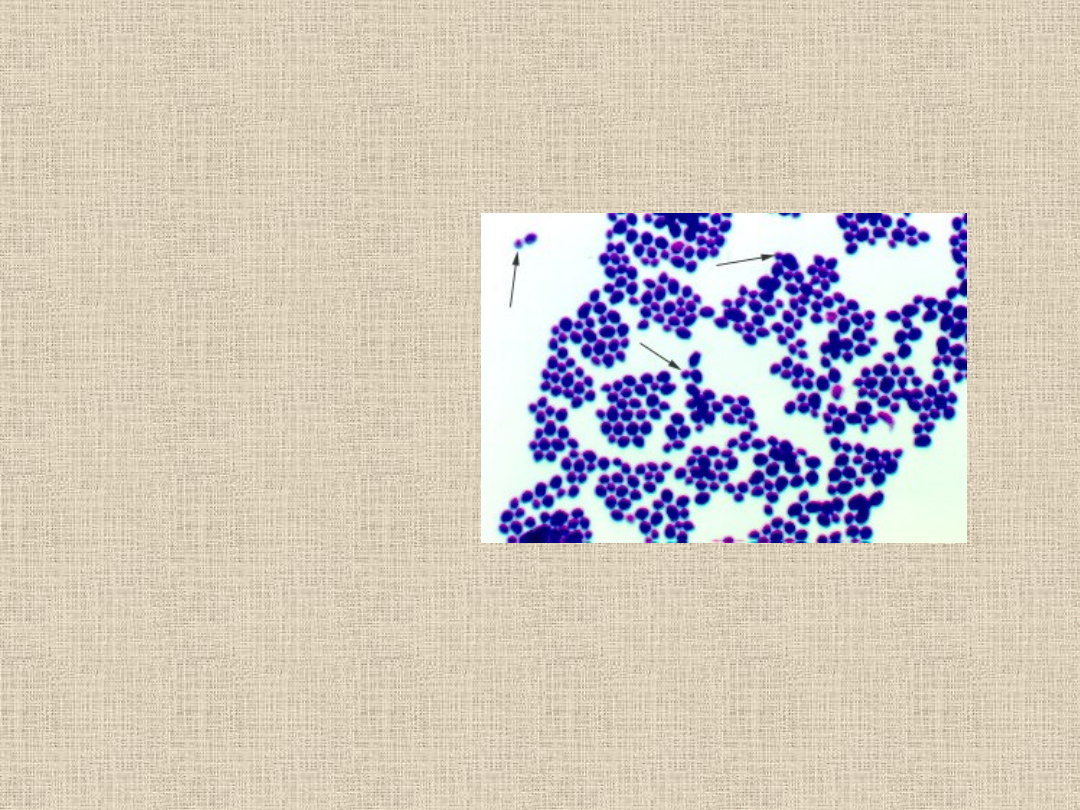
Candida albicans
•Preparat pośredni
•Metoda Grama
•Candida jest większe
od gronkowców
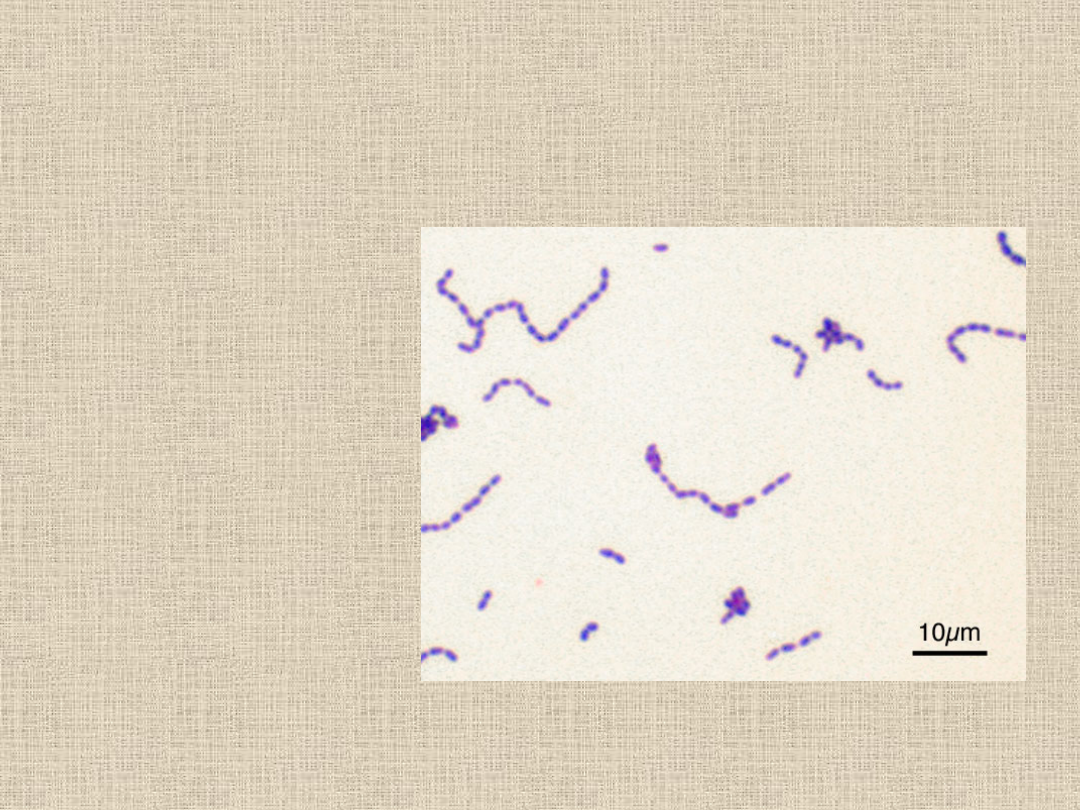
Paciorkowce
•Preparat pośredni
•Metoda Grama

Corynebacterium diptheriae
•Preparat pośredni
•Metoda Neissera
•Fioletowe- ciałka
Bebesa- Elsta
•Żółte- ciałka
wegetatywne
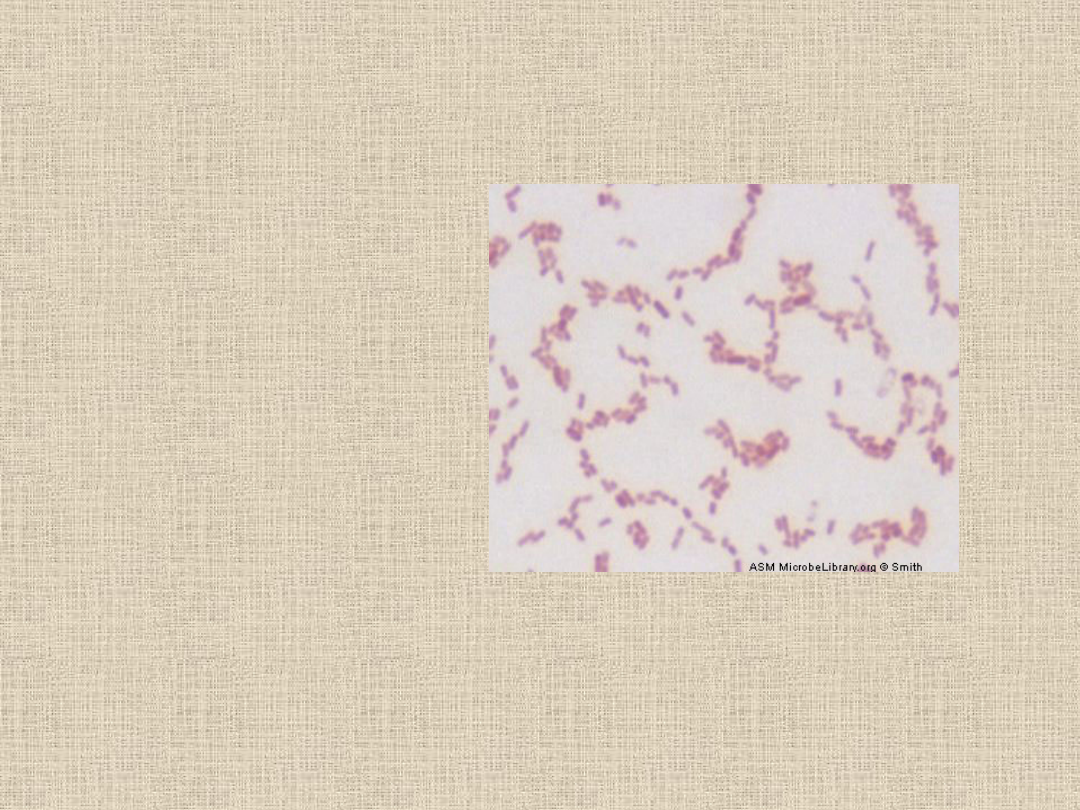
Klebsiella pneumoniae
•Metoda pośrednia
•Barwienie Grama
•Powinny być widoczne
na końcu przetrwalniki
(nie umiałam znaleźć
odpowiedniego zdjęcia)

Zgorzel gazowa
•Preparat bezpośdreni
•Metoda Grama
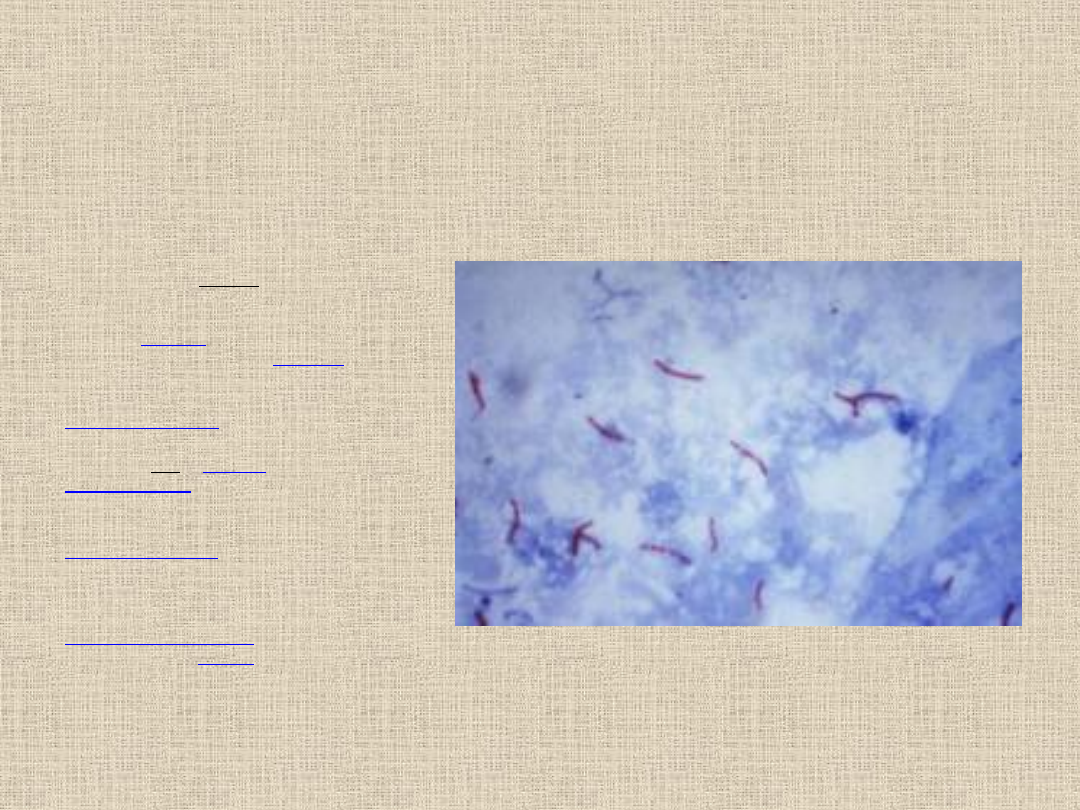
Prątki kwasooporne-
Mycobacterium tuberculosis
•Preparat bezpośredni
•Metoda Ziehl- Neelsena
Barwienie metodą Ziehla-Neelsena
1. na utrwalony rozmaz bakterii na
odtłuszczonym szkiełku podstawowym
nanosimy barwnik podstawowy
(stężona
) na 15 min. W trakcie
barwienia podgrzewamy
palnikiem (do tzw. "trzech par")
2. zlewamy barwnik. Nie spłukujemy
3. odbarwiamy preparat w 3%
roztworze HCl w
4. spłukujemy wodą destylowaną
5. nanosimy barwnik kontrastowy, np.
na 10 min.
6. spłukujemy wodą destylowaną
7. suszymy preparat na pasku bibuły i
8. przeprowadzamy obserwacje w

Micrococcus
•Metoda negatywna
•Wybarwione tło, a nie
drobnoustrój
Klebsiella/ S. performans
•Metoda pozytywno-
negatywna
•Służy do wykrywania
otoczki

Podłoże McConkeya:
- wybiórcze – uniemożliwia wzrost bakteriom
Gram(+) -> ponieważ zawiera fiolet
krystaliczny i sole źółciowe
- różnicujące -> laktoza (różnicowanie
laktozo-ujemnych i laktozo-dodatnich)
Podłoże zawiera barwnik (zwykle obojętny
barwnik czerwony) barwiący kolonie
fermentujące laktozę na różowo.
W preparacie mikroskopowym wszystkie
Gram(-) wyglądają identycznie!

Płytka z podłożem Chapmana (MSA) z wysianymi szczepami:
epidermidis i Micrococcus sp.
Pożywka Chapmana - jest to
typu wybiórczo-różnicującego
stosowana do hodowli
. Wykorzystuje się w niej fakt, że stafylokoki
(gronkowce) są w stanie rosnąć przy wysokim stężeniu
,
w przeciwieństwie do większości pozostałych bakterii. S. aureus i S. saprophyticus
fermentują mannitol, natomiast S. epidermidis nie (element różnicujący pożywki).
S. aureus można odróżnić od saprohyticus testem na
– po
wrzuceniu do krwi pierwszy ścina osocze, drugi nie.
.
w warunkach tlenowych i względnie beztlenowych
wzrasta w postaci kolonii otoczonych żółtą strefą - zmiana barwy podłoża z
różowej na żółtą jest wynikiem rozkładu mannitolu i zakwaszeniu środowiska.
Podobnie zachowują się niektóre szczepy
wykazujące te właściwości w warunkach tlenowych.
nie rozkłada mannitolu i rośnie w postaci białych kolonii nie powodując zmiany
barwy podłoża.
Poza czynnikami wzrostu (
,
(zazwyczaj w stężeniu 7,5% dla zahamowania wzrostu bakterii innych niż
gronkowce)
,
oraz czerwień fenolową.

MSBL
Identyfikacja i interpretacja kliniczna fenotypów oporności na linkosamidy,
makrolidy i streptograminy B – schemat algorytmu:
1. Szczepy wrażliwe na erytromycynę mogą być:
a) wrażliwe na linkomycynę/klindamycynę – nie stanowią one wtedy dużego problemu
klinicznego
b) oporne na linkomycynę i na klindamycynę:
- taką oporność warunkuje L-fenotyp, mechanizm związany z genem oporności lin(A)
- w zakażeniach szczepami z tego rodzaju opornością nie należy stosować linkomycyny i
klindamycyny!!
- przy wyniku wskazującym na L-fenotyp zaleca się powtórzenia badania w celu
wykluczenia błędu
2. Szczepy oporne na erytromycynę mogą być:
a) oporne na linkomycynę i klindamycynę:
- taki fenotyp oporności określamy jako MLS b konstytutywny!!
- mechanizm oporności związany jest z genem erm
- w takich przypadkach nie powinno się stosować żadnych makrolidów, linkozamidów i
streptogramin z grupy B!!
b) wrażliwe na linkomycynę i klindamycynę ze spłaszczeniem strefy zahamowania
wzrostu:
- taki fenotyp odporności określamy jako MLSb indkukcyjny!!
- mechanizm oporności również związany z genem erm
- tu również nie powinno się stosować żadnych makrolidów, linkozamidów ani
streptogramin grupy B!!
c) wrażliwe na linkomycynę i klindamycynę przy braku spłaszczenia strefy zahamowania
wzrostu:
- ten fenotyp odporności określamy jako MSb
- mechanizm związny jest z genem msr(A)
- w takich przypadkach nie powinno się stosować makrolidów 14- i 15-węglowych ani
streptogramin grupy B

metoda dwóch krążków:
- nakładamy krążki z erytromycyną i klindamycyną
w odległości 15-26 mm od krawędzi krążków

Oporność Enterokoków na wysokie stężenia aminoglikozydów
(oznaczanie HLAR):
1. oznaczanie metodą krążkowo-dyfuzyjną:
- krążki z dużym stężeniem gentamycyny (Ge-120 ug) i streptomycyną
(S-300 ug)
- oporność na takie stężenia tych dwóch antybiotyków określamy
mianem HLAR
- oporność na gentamycynę oznacza oporność na wszystkie
aminoglikozydy,
nie zawsze jednak oznacza pełną oporność na streptomycynę (inny
mechanizm)
2. szczepy oporne na gentamycynę ale wrażliwce na streptomycynę
możemy
leczyć streptomycyną w połączeniu z beta-laktamami (penicylina,
ampicylina)
oraz glikopeptydami!!
3. szczepy HLAR najczęściej są wrażliwe na inne antybiotyki:
penicylinę,
wankomycynę, teikoplaninę, ale mogą też wytwarzać beta-laktamazę
co czyni je
niewrażliwymi na beta-laktamy

1. ESBL:
- są to β-laktamazy o rozszerzonym spektrum działania (extended spectrum β-lactamases)
-warunkują oporność na penicyliny, cefalosporyny I-IV generacji (wyjątek - cefamycyny!)
-oraz na monobaktamy (aztreonam)
-są wrażliwe na inhibitory β-laktamaz, choć często efekt ten nie wystarcza, by
-szczepy były wrażliwe na połączenie beta-laktam+inhibitor
- geny tych enzymów znajdują się na plazmidach
- występują głównie u fermentujących, najczęściej u Klebsiella pneumoniae
-wywodzą się od β-laktamaz o szerokim spektrum, które dodatkowo poszerzone
-zostało o II-IV generację cefalosporyn (są wtórnymi beta-laktamazami)
-bakterie posiadające ESBL są wrażliwe na: karbapenemy, cefamycyny oraz na
-beta-laktamy w połączeniu z inhibitorami beta-laktamaz!
- należą do klasy AID
-powstały i powstają na nowo z beta-laktamaz o szerokim spektrum substratowym:
-TEM-1, TEM-2, SHV-1; w wyniku mutacji punktowych dochodzi do poszerzenia
-spektrum substratowego enzymów
-wspomniane enzymy (beta-laktamazy) o szerokim spektrum nadają oporność na
-aminopenicyliny, karboksypenicyliny, również (w dużych ilościach): ureidopenicyliny,
-cefalosporyny I generacji i cefoperazon; (w przypadku ESBL spektrum dodatkowo
-rozszerzone o II-IV generacja cefalosporyn)
-ok. 150 wariantów ESBL należących do 10 rodzin: TEM, SHV, CTX-M itd. - najczęściej
-występują u Klebsiella pneumoniae i E. coli
- poszczególne enzymy mają różną selektywność, aktywność -> preferencje substratowe
- poszczególne enzymy różnią się też aktywnością enzymatyczną i poziomem produkcji
-często szczepy produkujące ESBL pozostają wrażliwe in vivo na niektóre beta-laktamy
- należące do spektrum ESBL
-znane są gatunki Enterobacteriaceae u których gatunkowo specyficzne beta-laktamazy
-spełniają kryteria ESBL

Metycylinooporność:
-szczepy gronkowców oporne na metycylinę (MRSA, MRSNS) są oporne in vivo na wszystkie antybiotyki beta-laktamowe
-(tj. penicyliny, penicyliny skojarzone z inhibitorami beta-laktamaz, cefalosporyny, karbapenemy).
CA-MRSA:
-nowym problemem diagnostycznym i epidemiologicznym jest pojawianie się szczepów MRSA w środowisku pozaszpitalnym czyli
- CA-MRSA
-szczepy te charakteryzują się heterogennym poziomem oporności na antybiotyki beta-laktamowe, co niesie z sobą ryzyko nierozpoznania tego
-mechanizmu w rutynowej diagnostyce mikrobiologicznej a co za tym idzie – niepowodzeń terapeutycznych
-szczepy CA-MRSA poza opornością na antybiotyki beta-laktamowe związaną z metycylinoopornością, są wrażliwe na różne antybiotyki innego typu,
-podczas gdy szczepy HA-MRSA są zwykle wielolekooporne
- w przeciwieństwie do HA-MRSA, większość szczepów CA-MRSA posiada gen leukocydyny Panton-Valentine (PVL – Panton-Valentine leucocidin)
- PVL należy do cytotoksyn powodujących martwicę tkanek i lizę leukocytów
-obecność w genomie CA-MRSA genów PVL uznaje się za marker informujący nas, że mamy do czynienia ze szczepem pozaszpitalnym odmiennym
-od klonów szpitalnych!!
CA-MRSA – klinika:
- najczęściej powodują pierwotne zakażenia skóry i tkanek miękkich oraz martwicze zapalenie płuc, któremu często towarzyszy bakteriamia
- w przeciwieństwie do HA-MRSA, zakażenia CA-MRSA występują u osób młodych i bez czynników ryzyka
-75% przypadków martwiczego zapalenia płuc wywołanego przez CA-MRSA kończy się zgonem, średnia przeżywalność wynosi 4 dni, często jest
-ono wynikiem powikłań pogrypowych
Gronkowce skórne i koagulazo-ujemne szybciej nabierają oporności.
MRSA stanowi 10-25% gronkowców.
MRSA:
-dobrze zaadaptowane do przeżycia w warunkach szpitalnych, są bardzo łatwo przekazywane z pacjenta na pacjenta w obrębie oddziałów szpitalnych
-oraz pomiędzy szpitalami
- kolonizują osoby w wieku podeszłym oraz poważnie chore
- HaMRSA - Pol1 - najczęstszy
- HaMRSA - Pol2
Glikopeptydy - są skuteczne w leczeniu MRSA; zaburzają one syntezę ściany komórkowej bakterii
- wiążą się z warstwą peptydoglikanu a następnie swoiście z końcową amino-acylo-D-alanylo-D-alaniną rosnącego peptydoglikanu
Metycylinooporność:
- homogenna - wszystkie komórki są niewrażliwe
- heterogenna - 2/3 komórek jest niewrażliwych, ale reszta jest wrażliwa
VRSA:
- oporny na wankomycynę S. aureus
- mechanizm oporności polega na wytwarzaniu zmienionych prekursorów peptydoglikanu (D-Ala-...)
VISA:
- średnio wrażliwy na wankomycynę S. aureus
- polega na wiązaniu docelowego antybiotyku zanim osiągnie miejsce docelowego działania
hVISA:
- S. aureus średnio wrażliwy na wankomycynę, o heterogennej ekspresji oporności inaczej: S. aureus z obniżoną wrażliwością na wankomycynę
Zdarzają się pojedyncze przypadki VRSA u pacjentów z grup ryzyka (cukrzycą, niewydolnością nerek)

Nowe opcje terapeutyczne w leczeniu zalażeń o etiologii VRSA, VISA,
VRSA :
- streptograminy (chinupristyna B, dalfopristyna A)
- linezolid
- telitromycyna (ketolidy)
- tigecyklina (glicylcykliny – pochodne minocykliny)
- daptomycyna – nowy lek z grupy lipopeptydów, do stosowania
parenteralnego
Wskazania:
- leczenie powikłanych zakażeń skóry i tkanek miękkich, bakteriemii i
infekcyjnego zapalenia wsierdzia wywołanego przez Staphylococcus spp. i
Streptococcus spp. z wyjątkiem S. pneumoniae!
Oksazolidynony:
- chemioterapeutyki
- przedstawiciele: linezolid, eprezolid
- działają bakteriostatycznie
- ich mechanizm działania polega na hamowaniu syntezy białka na bardzo
wczesnym etapie (kompleks inicjatorowy translacji w rybosomach
bakteryjnych)
Lipopeptydy, glikopeptydy, glikolipidy:
- powodują depolaryzację błony cytoplazmatycznej i ucieczkę jonów potasu

Leczenie zakażeń szczepami produkującymi ESBL:
- nie stosować penicylin, cefalosporyn I-IV generacji (wyjątek - cefamycyny), monobaktamów
-w terapii stosujemy połączenia penicyliny z inhibitorami beta-laktamaz oraz antybiotyki innych grup
-(aminoglikozydy, fluorochinolony, karbapenemy)
Wykrywanie ESBL:
a) test dwóch krążków:
•krążki:
CAZ - ceftazidym – najlepszy wskaźnik ESBL wywodzących się z klas TEM i SHV, które są
wobec
niego bardzo aktywne
CTX - (cefotaxym – najlepszy wskaźnik ESBL wywodzących się z klasy CTX-M, które są wobec
niego
bardziej aktywne niż inne ESBL),
AMC (amoksycylina-klawulonian - w centrum)
Krążki ułożone są w odległości 2 cm (25-30 mm) od siebie.
•wynik odczytujemy jako dodatni (obecne ESBL), jeśli strefa zahamowania wzrostu wokół krążka z
•ceftazidymem (lub cefotaksymem) rozszerza się też na rejon wokół krążka z połączeniem penicyliny i i
•nhibitora (AMC – amoksycylina+klawulonian) – synergizm inhibicyjny
b) metoda :krążków kombinowanych” (combined disc method):
•porównuje się strefę zahamowania wzrostu wokół krążka z połączeniem cefalosporyny i
• inhibitora beta-laktamaz (kwas klawulanowy; jest to tzw. krążek „kombinowany”) ze strefą zahamowania
•wzrostu wokół krążka z samą cefalosporyną (bez inhibitora)

β-laktamazy AmpC:
-gatunkowo specyficzne, występują u szczepów: Enterobacter, Citrobacter,
-Serratia, Morganella, niektóre szczepy E. coli
-enzymy o bardzo szerokim spektrum: warunkują oporność na: aminopenicyliny,
-ureidopenicyliny, piperazynopenicyliny, cefalosporyny I-III generacji, monobaktamy,
-cefalosporyny o szerokim spektrum działania (cefamycyny)
- są niewrażliwe na działanie inhibitorów β-laktamaz
- geny tych enzymów znajdują się na chromosomie bakteryjnym – genoforze
-istnieją mutanty konstytutywnie wytwarzające β-laktamazy AmpC – określane są
-mianem szczepów zdereprymowanych
-leczenie: imipenem, meropenem
MBL – metalo β-laktamazy czyli karpapenemazy:
- metalozależne – kofaktorem jest przede wszystkim cynk
- są elementem naturalnej oporności na antybiotyki u Stenotrophomonas maltophila
-u Pseudomonas aeruginosa, Acinetobacter oraz Enterobacteriaceae (Serratia, Shigella,
- Klebsiella, Citrobacter itd.) są elementem oporności nabytej
- występują głównie u pałeczek niefermentujących
Wykrywanie MBL:
- CAZ, kwas 2-merkaptopropionowy
- IMP, EDTA (imipenem + EDTA)
- E-test
Kwas 2-merkaptopropionowy i EDTA są inhibitorami MBL, dlatego:
-pojawia się strefa przejaśnienia wokół krążka z ceftazidimem lub imipenemem od
-strony krążka zawierającego inhibitor

E-test:
•pełna nazwa: Epsilometer test
•służy do oznaczania wartości MIC
•na krążek z agarem, na który wysiano bakterię nakładany jest nasączony antybiotykiem pasek
•z narysowaną skalą
•antybiotyk dyfunduje tworząc gradient stężenia w agarze (najczęściej agar MH - Muellera-Hintona)
•powstaje eliptyczna strefa zahamowania wzrostu
•punkt w którym granica strefy zahamowania wzrostu przetnie się z paskiem wyznacza wartość MIC
•dla badanego szczepu
Przykład E-testu (eliptyczne przejaśnienie – strefa zahamowania wzrostu):
Document Outline
- Slide 1
- Grzyby w plwocinie
- Streptococcus pneumoniae
- Staphylococcus aureus- gronkowce
- Maczugowce
- Candida albicans
- Paciorkowce
- Corynebacterium diptheriae
- Klebsiella pneumoniae
- Zgorzel gazowa
- Prątki kwasooporne- Mycobacterium tuberculosis
- Micrococcus
- Klebsiella/ S. performans
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
Wyszukiwarka
Podobne podstrony:
Przykład opracowania na zaliczen ie
,,Polityka Oświatowa Samorządu Terytorialnego koncepcja programu ,, opracowanie na zaliczenie POL
Lista substancji na zaliczenie praktyczne, Farmacja
OPRACOWANIE NA ZALICZENIE 2011 Nieznany
Opracowanie na zaliczenie2, Politechnika Poznańska, Zasady Gospodarki Rynkowej i Organizacji
17.03.07r. ćwiczenia podstawy marketingu + opracowanie na zaliczenie, Semestr II, Podstawy marketing
Prawo spadkowe opracownanie na zaliczenie
Pytania opracowane na zaliczenie, Akademia Morska, VII semesrt
moje opracowanie na zaliczenie
Pytania opracowane na zaliczenie, Akademia Morska, Rok I, Semestr I, Zarządzanie, Zarządzanie
Pytania do opracowania na zaliczenie
ściąga na zaliczenie praktyczne, sciagi
Tematy do opracowania na zaliczenie przedmiotu, Pedagogika, Współczesne metody pedagogiczne
Procesy pielęgnowania na zaliczenie praktyk
Biochemia opracowanie na teoretyczno-praktyczny, Lekarski WLK SUM, lekarski, biochemia, egzamin, EGZ
Iwona- opracowanie na zaliczenie 20-06-09-1, Prawo konstytucyjne, Notatki+ też ściągi
Przykład opracowania na zaliczen ie
więcej podobnych podstron