
Immunologia
transplantacyjna
Seminarium 6
Przeszczepy kończyn u psów
A. Carrel
1902 - Opracowanie
techniki
zespoleń
naczyniowych i
eksperymentalnego
przeszczepiania
nerek u zwierząt
1953 – pierwszy udany
przeszczep nerki (izogeniczny)
wykonany w
Bostonie przez
zespół dr
Murray’a
biorca przeżył 9
lat
dawca przeżył 50
lat
J. E. Murray
wykonał pierwszy
udany przeszczep
nerki pomiędzy
dwoma bliźniakami
monozygotycznymi
E. Donnall Thomas
stworzył metodę
przeszczepiania
szpiku
Kolejne odkrycia
układ zgodności tkankowej
immunosupresja
Za badania nad
azatiopryną
– lekiem
immunosupresyj
nym
Za pracę
nad
antygen
ami
zgodnoś
ci
tkankow
ej
Pierwsza udana transplantacja
nerki w Polsce
Pierwsza udana
transplantacja
nerki w Polsce –
26 stycznia 1966
Biorca:
Danuta M. - 18-
letnia uczennica
szkoły
pielęgniarskiej
Co można
przeszczepić?
Rodzaje przeszczepów
W zależności od różnicy genetycznej
pomiędzy dawcą a biorcą wyróżnia się
następujące rodzaje przeszczepów:
autogeniczny (autologiczny), kiedy dawcą i
biorcą jest ten sam osobnik,
izogeniczny (syngeniczny), pomiędzy
identycznymi osobnikami tego samego gatunku
(bliźnięta monozygotyczne, szczepy wsobne u
zwierząt),
allogeniczny, pomiędzy różnymi genetycznie
osobnikami tego samego gatunku,
ksenogeniczny, pomiędzy osobnikami
odmiennych gatunków
Miejsca przeszczepiania
narządów
przeszczep
izotopowy
allotopowy
Pierwszy przeszczep twarzy
– Francja
(listopad 2005)
Pierwszy przeszczep twarzy
– Francja
(listopad 2005)

Przeszczep twarzy – Chiny
(kwiecień 2006)
25.08.1998 – pierwsza udana
transplantacja ręki

Autogeniczny
przeszczep skóry
Autogeniczny przeszczep
skóry

Odrzucanie
przeszczepu
odczyn zapalny wywołanym przez swoistą reakcję
immunologiczną, który w różnie długim czasie
prowadzi do całkowitej niewydolności
przeszczepionego narządu.
Dlaczego dochodzi do
odrzucania?
Różnice genetyczne pomiędzy
dawcą a biorcą sprawiają, że
układ odpornościowy biorcy
rozpoznaje antygeny
przeszczepu jako obce i
uruchamia reakcję (odrzucanie)
dążącą do jego zniszczenia.
Przebieg odrzucania
przeszczepu
w przebiegu odpowiedzi na antygeny
przeszczepu można wyróżnić:
fazę indukcji odpowiedzi (aferentną), w
czasie której dochodzi do prezentacji i
rozpoznania obcych antygenów,
fazę efektorową (eferentną), w której
uruchomione zostają swoiste i nieswoiste
mechanizmy odpowiedzi na przeszczep.
Leukocyty pasażerskie -
indukcja odpowiedzi na
antygeny przeszczepu
Obce antygeny
Najważniejszymi cząsteczkami rozpoznawanymi
przez komórki układu odpornościowego biorcy
są antygeny kodowane w układzie MHC.
Odpowiedź immunologiczną na obce cząsteczki MHC
wyróżnia znacznie większe nasilenie w porównaniu
do reakcji na inne antygeny.
Liczba klonów limfocytów T odpowiadających na
obce cząsteczki MHC przewyższa 100-krotnie liczbę
klonów, które zwykle rozpoznają inne antygeny
białkowe.
Zjawisko powyższe tłumaczy się w ten sposób,
że
receptor limfocytu T rozpoznaje peptyd
antygenowy łącznie z fragmentem cząsteczki
MHC
.
Prezentacja antygenów
przeszczepu

Prezentacja antygenów
przeszczepu
prezenta
cja
bezpośrednia
pośrednia
APC
dawcy (obce)
biorcy (własne)
miejsce
węzły chłonne i śledziona biorcy
czas
wczesny okres
od przeszczepu
późny okres od
przeszczpu
(odrzucanie
przewlekłe)
Komórki prezentujące antygen
wywodzą
się z komórek krwiotwórczych i
po
transplantacji ulegają w przeszczepie
wymianie na APC pochodzące od biorcy
.
Zmniejsza się wtedy bodziec indukujący
odrzucanie co tłumaczy znane z kliniki
zjawisko, że
częstość występowania i
nasilenie epizodów odrzucania
maleje w miarę upływu czasu od
zabiegu
.
Typy odrzucania
przeszczepu
odrzucanie nadostre, które rozwija się w ciągu
minut po przeszczepieniu i nieuchronnie prowadzi
do jego niewydolności,
odrzucanie ostre przyspieszone, które może
pojawić się już po 24 godzinach od zabiegu i
zazwyczaj prowadzi do niewydolności przeszczepu
w ciągu 1-6 miesięcy,
odrzucanie ostre, które może pojawić się w ciągu
kilku dni do kilku miesięcy od transplantacji,
odrzucanie przewlekłe, występujące zwykle nie
wcześniej niż po roku od zabiegu, utożsamiane
również z przewlekłą niewydolnością przeszczepu.
Morfologia odrzucania
przeszczepu (biopsja nerki)
zd
ro
w
a
n
e
rk
a
o
st
re
o
d
rz
u
ca
n
ie
n
a
cz
yn
io
w
e
o
st
re
o
d
rz
u
ca
n
ie
śr
ó
d
m
ią
żs
zo
w
e
o
d
rz
u
ca
n
ie
p
rz
e
w
le
k
łe
Nadostre odrzucanie
przeszczepu
spowodowane istnieniem w
organizmie biorcy
gotowych
przeciwciał przeciwko antygenom
dawcy
, m.in. przeciwko:
cząsteczkom MHC
antygenom grupowym układu ABO
niezbyt dokładnie poznanym
antygenom swoistym dla śródbłonka
Odrzucanie
nadostre
Kiedy pacjent może „uczulić”
się na obce MHC?
ciąża
przetaczanie krwi
przeszczep narządu
Ostre przyspieszone odrzucanie
przeszczepu
= ostre odrzucanie naczyniowe
wywołuje je obecność w osoczu
preformowanych przeciwciał przeciwko
dawcy, występujących jednak w
stężeniu, które uniemożliwia wykrycie
ich rutynowym testem cytotoksycznym
bardzo podobne do odrzucania
nadostrego

Ostre odrzucanie przeszczepu
(odrzucanie śródmiąższowe)
charakterystyczną cechą
morfologiczną są
nacieki, w których
przeważają komórki
jednojądrzaste:
limfocyty T CD8
+
(dominują)
makrofagi
limfocyty B, komórki NK,
limfocyty o fenotypie
komórek pamięci
Rola cytokin w ostrym
odrzucaniu przeszczepu
aktywują swoiste limfocyty cytotoksyczne (IL-2, IL-12, IFN-
)
bezpośrednio uszkadzają komórki przeszczepu
(limfotoksyna, TNF)
aktywują limfocyty B oraz powodują zmianę izotypu
wytwarzanych przeciwciał na uczestniczące w reakcji
cytotoksyczności zależnej od przeciwciał (ADCC) – (IL-2, -6,
IFN-)
sprzyjają powstawaniu odczynu zapalnego wpływając na
czynność śródbłonka naczyń i zwiększając ekspresję
cząsteczek ułatwiających docieranie leukocytów do miejsca
reakcji (IL-1, -2, -4, -5, -6, IFN-, TNF)
przyciągają limfocyty Tc, monocyty i komórki NK do
przeszczepu (chemokiny:CCL2, CCL3, CCL5)
hamują angiogenezę (chemokiny: CXCL9 i CXCL10)
aktywują komórki prezentujące antygen (IFN-)
Przewlekłe odrzucanie
przeszczepu
Przewlekłe odrzucanie
przeszczepu
główna przyczyna niepowodzenia
transplantacji
wynik uszkodzenia narządu przez
czynniki immunologiczne
czynniki nieimmunologiczne
jest określane jako
przewlekła
niewydolność przeszczepu
, dla
podkreślenia tylko częściowego
udziału układu odpornościowego
Przewlekłe odrzucanie
przeszczepu
rozplem
błony
wewnętrzn
ej tętnicy
włóknienie zrębu,
zanik cewej
nerkowych
zmienione
kłębuszki
nerkowe
(rozplem
mezangium,
włóknienie)
Czynniki ryzyka przewlekłego
odrzucania
przebyte epizody ostrego odrzucania,
niewielka liczba zgodnych z dawcą antygenów HLA,
niedostateczna immunosupresja
nadciśnienie tętnicze
zakażenie wirusem cytomegalii,
długi czas przechowywania narządu przed
transplantacją (zimne niedokrwienie)
palenie papierosów
hiperlipidemia
nieproporcjonalnie mała masa nerki w stosunku do
masy ciała
Mechanizmy
efektorowe w
odrzucaniu
przeszczepu

Zapobieganie
odrzucaniu
przeszczepu
1.
dobór HLA (typowanie tkankowe)
2.
immunosupresja
3.
indukcja tolerancji immunologicznej

Dobór dawcy
przeszczepu
1.
aspekty prawne
2.
aspekty immunologiczne – typowanie
tkankowe
Dobór immunologiczny dawcy
i biorcy do przeszczepu nerki
Oznaczenia materiału od biorcy
(przygotowanie do przeszczepu):
Grupa krwi (ABO i Rh)
HLA klasy I locus A i B (z limfocytów T)
HLA klasy II locus DR (z limfocytów B)
test limfocytotoksyczny z panelem
limfocytów (surowica przesyłana ze
stacji dializ co 4-12 tyg.) = PRA (panel
reactive antibody)
Typowanie tkankowe
Lepszy dobór w zakresie HLA
zmniejsza częstość epizodów
ostrego odrzucania w ciągu 1 roku
po transplantacji oraz obniża ryzyko
powstania zmian przewlekłych.

zgodność w zakresie HLA klasy I i
HLA klasy II nie jest równoważna
niezgodność w zakresie
jednego antygenu HLA
wzrost ryzyka
odrzucenia
przeszczepu
DR
5x
B
3x
A
2x
Typowanie tkankowe (HLA)
limfocyty z krwi
obwodowej lub z
węzła chłonnego
przeciwcia
ła anty-
HLA
+
dopełniacz
liza
komórek z
danym
HLA
metoda serologiczna
Dobór immunologiczny dawcy
i biorcy do przeszczepu nerki
Oznaczenia materiału od dawcy:
węzły chłonne – HLA-A, -B, -DR
badania wirusologiczne (HBV, HCV,
HIV, CMV)
Cross-match test
wykonywany w celu sprawdzenia obecności
preformowanych przeciwciał przeciwko
MHC u biorcy czekającego na przeszczep
przed przeszczep wykonywany w celu
sprawdzenia obecności u biorcy przeciwciał
przeciwko MHC dawcy (wyeliminowanie
ryzyka nadostrego odrzucania)

PRA (panel reactive
antibody)
surowica
biorcy
limfocyty 30
dawców krwi
+
PRA (panel reactive
antibody)
jeżeli limfocyty biorcy reagują z 15
surowicami z 30 – wartość
preformowanych przeciwciał wynosi 50%
(PRA=50)
biorcy z dużą ilością preformowanych
przeciwciał mają pierwszeństwo spośród
wszystkich potencjalnych biorców danego
przeszczepu
gdy PRA=50% oczekiwanie na przeszczep
wydłuża się 5-krotnie

Cross-match test
surowica
biorcy
limfocyty
dawcy
narządu
+
Dobór dawcy i biorcy nerki
przeszczep dostaje biorca który:
ma zgodne HLA z dawcą
ma takie same wirusy jak dawca (lub nie ma ich
wcale gdy dawca też ich nie ma)
ma zgodną lub identyczną grupę krwi
nie reaguje z dawcą w cross–match (próbie
krzyżowej)
nie ma w danej chwili przeciwwskazań do operacji
(np. infekcja)
gdy kilka osób spełnia w/w kryteria przeszczep
dostaje ta, która ma najwyższą wartość
preformowanych przeciwciał w badaniu z panelem
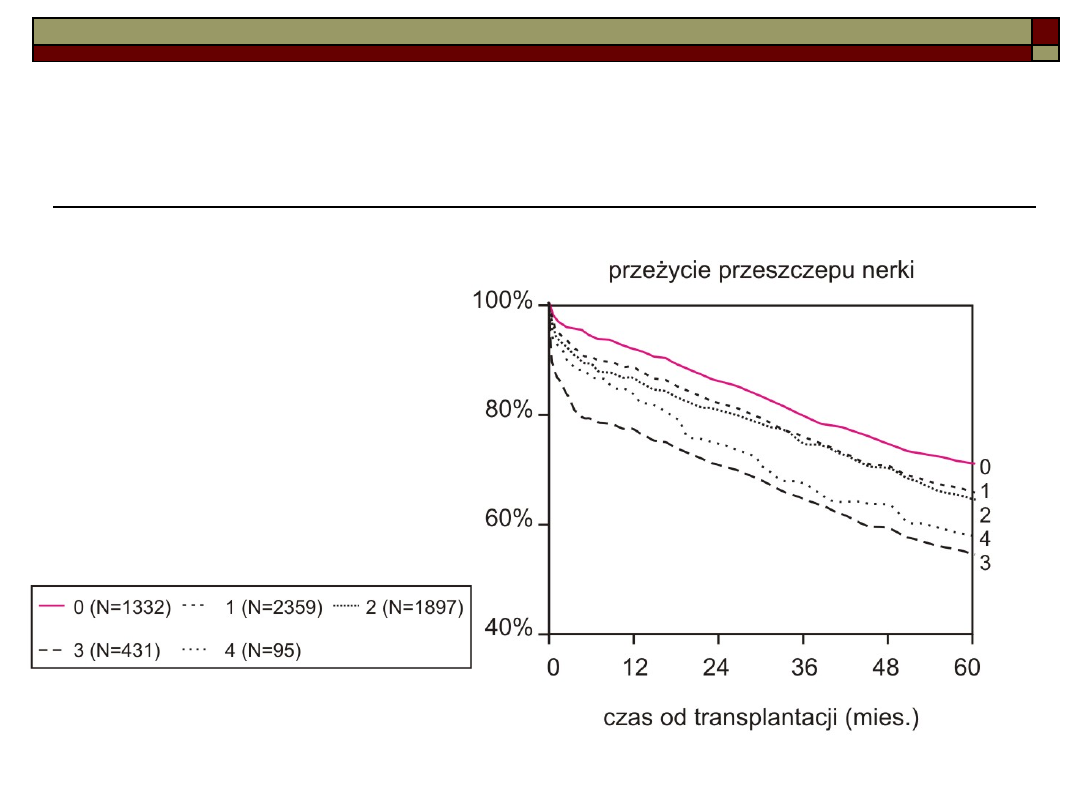
Wpływ liczby niezgodnych antygenów
HLA-B i -DR na przeżycie przeszczepu
nerki
(dane Eurotransplantu)
CREG (cross-reacting
groups)
antygeny HLA-A i HLA-B
wykazujące zbliżoną zdolność do
indukcji swoistych przeciwciał
ich posiadanie zarówno przez
dawcę, jak i biorcę zmniejsza
prawdopodobieństwo wystąpienia
swoistych przeciwciał anty-HLA

Niezgodności w zakresie
HLA
Niezgodności
zabronione (tabu)
Niezgodności
dozwolone
zwiększają ryzyko
utraty narządu
nie mają większego
znaczenia dla
dalszych losów
przeszczepu
Dobór dawcy i biorcy nerki
kto jest najlepszym dawcą rodzinnego
przeszczepu?
biorca
A 1, 9
B 8, 15
DR 3, 4 grupa krwi B, Rh +
matka
A 1, 3
B 8, 22
DR 3, 8 grupa krwi 0, Rh -
ojciec
A 2, 9
B 7, 15
DR 2, 4 grupa krwi AB, Rh+
brat
A 2, 3
B 7, 22
DR 2, 8 grupa krwi A, Rh -
siostra
A 1, 9
B 7, 8
DR 3, 4 grupa krwi B, Rh -
ciotka
A 1, 11
B 8, 15
DR 3, 5 grupa krwi A, Rh -
brat cioteczny
A 1, 16
B 8, 17
DR 3, 7 grupa krwi A, Rh -
mąż
A 4, 9
B 3, 8
DR 3, 4 grupa krwi 0, Rh +
Dobór dawcy i biorcy pozostałych
narządów - serca, wątroby i płuc
obowiązuje zgodność w zakresie
układu ABO i Rh
test cross-match wykonuje się po
wykonanym przeszczepie (zgodność
w tym zakresie nie zmienia
rokowania)

Immunosupresja
stan obniżonej lub zahamowanej
odpowiedzi immunologicznej
Immunosupresja vs
tolerancja
Leczenie
immunosupresyjne
immunosupresja farmakologiczna
pozwoliła na wydłużenie przeżycia
przeszczepów allogenicznych
często terapia rozpoczynana jest u
biorcy jeszcze przed przeszczepieniem
narządu (w przypadku przeszczepienia
komórek krwiotwórczych jest to
normą), co ma charakter profilaktyki
ostrego odrzucania
Leki o działaniu
immunosupresyjnym
glikokortykosteroidy,
inhibitory niskocząsteczkowe
inhibitory kalcyneuryny
(cyklosporyna,
takrolimus)
inhibitory kinazy mTOR
(rapamycyna,
ewerolimus)
inhibitory syntezy DNA
(azatiopryna, MMF)
inne
przeciwciała
(przeciwko CD3, CD20, CD52, CD25,
immunoglobulina antytymocytarna i antylimfocytarna)
Tolypocladium inflatum, szczep grzybów znaleziony w ziemi z
regionu Hardangger w Norwegii, który wytwarza
cyklosporynę

Mechanizmy
działania leków
immunosupresyj
nych
Działania niepożądane leków
immunosupresyjnych
związane z upośledzeniem odporności
(głównie zakażenia i niektóre
nowotwory, najczęściej raki skóry i
nowotwory układu chłonnego),
związane z działaniem toksycznym na
inne tkanki (np. nefrotoksyczność
inhibitorów kalcyneuryny)

Tolerancja na
przeszczep
Tolerancja na przeszczep
W warunkach doświadczalnych można
względnie łatwo wywołać stan tolerancji na
alloantygeny gwarantujący trwałe przyjęcie
przeszczepu allogenicznego, np. poprzez:
podawanie antygenów transplantacyjnych
przyszłego dawcy już w życiu płodowym lub
noworodkowym. Jest to tak zwana tolerancja
noworodkowa,
podawanie antygenów transplantacyjnych do
grasicy w celu wywoływania delecji określonych
klonów limfocytów T.

Miejsca uprzywilejowane
immunologicznie
mózg
przednia komora
oka
wątroba
jądro
•bariery utrudniające napływ
limfocytów
•aktywność limfocytów T
reg
•lokalne wytwarzanie IL-10 i
TGF-β
•występowanie cząsteczek FasL i
zabijanie aktywowanych
limfocytów T mających
cząsteczki Fas
Mikrochimeryzm
zjawisko obserwowane u biorców z
przeszczepem funkcjonującym przez wiele lat.
komórki dendrytyczne dawcy mogą po
zabiegu, jako tak zwane „leukocyty
pasażerskie”, migrować do obwodowych
narządów limfatycznych.
u wieloletnich biorców wykryto komórki
dawcy poza przeszczepionym narządem.
stały kontakt z komórkami dawcy w węzłach
limfatycznych jest niezbędnym warunkiem
utrzymywania tolerancji transplantacyjnej.
Przeszczep wątroby słabo
indukuje odpowiedź
immunologiczną
bogate źródło leukocytów
pasażerskich
wydzielanie rozpuszczalnych MHC
Mechanizmy tolerancji na
przeszczep
ignorancja
delecja
zahamowanie
(anergia)
supresja
adaptacja

Przeszczep komórek
hematopoetycznych
autogeniczne
allogeniczne
od dawcy spokrewnionego
od dawcy niespokrewnionego
Rodzaje przeszczepów
komórek hematopoetycznych
przeszczep
szpiku
przeszczep
komórek
macierzystych krwi
obwodowej
przeszczep
komórek
macierzystych krwi
pępowinowej
Źródła przeszczepów
autologicznych
Liczba przeszczepów komórek
hematopoetycznych 1987-2005
Allogeniczne przeszczepy
szpiku – pacjenci poniżej 20
roku życia
Allogeniczne przeszczepy
szpiku – pacjenci powyżej 20
roku życia
Wskazania do przeszczepu
komórek hematopoetycznych
Wskazania:
hematologic
zne
onkologiczn
e
Wskazania do przeszczepu
komórek hematopoetycznych
Ostre białaczki
Przewlekła białaczka szpikowa
Zespoły mielodysplastyczne
Chłoniaki nieziarnicze i ziarnica złosliwa
Anemie: Fanconiego, aplastyczna, sierpowatokrwinkowa,
talasemie
Nocna napadowa hemoglobinuria
Wrodzone niedobory odpornosci
Choroby metaboliczne (choroby spichrzeniowe)
Ciężkie schorzenia autoimmunologiczne
Guzy lite:
Drobnokomórkowy rak płuca (SCLC)
Rak jajnika
Rak jadra
Rak sutka

Przeszczepy komórek
hematopoetycznych – wg
wskazań
Dobór dawcy komórek
hematopoetycznych
optymalna całkowita zgodność
(10/10) w zakresie:
HLA-A
HLA-B
HLA-C
w
HLA-DR
HLA-DQ
HLA-DP (rzadko badane w Polsce)
Dobór dawcy i biorcy
kto jest najlepszym dawcą rodzinnego
przeszczepu?
biorca
A 1, 9
B 8, 15
DR 3, 4 grupa krwi B, Rh +
matka
A 1, 3
B 8, 22
DR 3, 8 grupa krwi 0, Rh -
ojciec
A 2, 9
B 7, 15
DR 2, 4 grupa krwi AB, Rh+
brat
A 2, 3
B 7, 22
DR 2, 8 grupa krwi A, Rh -
siostra
A 1, 9
B 7, 8
DR 3, 4 grupa krwi B, Rh -
ciotka
A 1, 11
B 8, 15
DR 3, 5 grupa krwi A, Rh -
brat cioteczny
A 1, 16
B 8, 17
DR 3, 7 grupa krwi A, Rh -
mąż
A 4, 9
B 3, 8
DR 3, 4 grupa krwi 0, Rh +
Przeszczep szpiku – pobranie
materiału
zwykle pobiera się
15-25 ml szpiku na
kg masy ciała dawcy
szpik regeneruje się
w pełni po 2-3 tyg.
optymalna dawka
komórek to 300 mln
na kg masy ciała
biorcy
Komórki macierzyste krwi
obwodowej
podawanie cytokin (G-CSF, IL-3, SCF) w
celu
mobilizacji
komórek macierzystych
ze szpiku
leukafereza
(jedna lub kilka) – izolacja
leukocytów
podanie opracowanego materiału biorcy

Przygotowanie biorcy
kondycjonowanie
ablacja szpiku przy pomocy wysokich
dawek
chemioterapii
radioterapii
Przeszczep szpiku
Przeszczep szpiku
Komórki macierzyste
szpiku wraz z krwia
dostaja sie do kosci
biorcy, aby w jamach
szpikowych odtworzyc
szpik zniszczony przez
chemo- lub
radioterapie.
Kolonizują jamy
szpikowe tą samą
drogą, którą pokonuja
w czasie rozwoju
płodowego ok. 15 tyg.
ciąży
Krew pępowinowa
Pierwsze przeszczepienie allogenicznej
jednostki krwi pępowinowej wykonano
w 1988 u dziecka z anemią Fanconiego.
Dawca jednostki była siostra chorego,
identyczna w HLA.
Przeszczepienie zakonczyło sie pełnym
sukcesem, pacjent żyje do dziś bez
nawrotu choroby.
Wyniki przeszczepiania
komórek krwiotwórczych
Przeszczep przyjmuje sie u 95% biorców
U 75% biorców wystepuje reakcja przeszczep
przeciw gospodarzowi GvHD
Szanse na pomyślny rezultat przeszczepu ma
ok. 65% dzieci i 44% dorosłych
Układ krwiotwórczy odbudowuje sie w ciagu
miesiaca, na odtworzenie układu
odpornosciowego potrzeba od 1-2 lat.
Czasami nigdy do tego w pełni nie dochodzi.
Choroba przeszczep przeciwko
gospodarzowi (GVHD)
objawy choroby wywołują limfocyty T
pochodzące z przeszczepionego szpiku,
które naciekają tkanki gospodarza i
wywierają w nich bezpośredni efekt
cytotoksyczny
równie istotne dla powstania objawów
choroby jest zwiększone wydzielanie
cytokin przez aktywowane w tkankach
limfocyty T
Podział GVHD
GVHD
ostra
przewlekła
•powstaje w ciągu 100 dni od
przeszczepienia
•pojawia się u ponad 50%
biorców
•ma często ciężki przebieg
prowadząc do zgonu chorego
•objawy choroby związane są
zajęciem
skóry, błon
śluzowych
przewodu
pokarmowego i
wątroby
•występuje u 20-30% chorych
•objawy pojawiają się zwykle w
ciągu roku od zabiegu i
przypominają dolegliwości w
chorobach
autoimmunizacyjnych
•powoduje zaburzenia odnowy
hematologicznej i wtórny
niedobór odporności.
Patogeneza GVHD

Czynniki ryzyka GVHD
Ostra GVHD
Przewlekła
GVHD
Uprzednie ciąże – u
dawcy szpiku
Duża liczba limfocytów T
w przeszczepianym
szpiku
Niezgodność HLA
Przeszczepienie od
kobiety do mężczyzny
Podeszły wiek dawcy i
biorcy
Brak stosowania
immunosupresji
Podeszły wiek dawcy i
biorcy
Przetoczenia leukocytów
dawcy
Niezgodność HLA
Przeszczepienie od
kobiety do mężczyzny
Przebyta ostra
choroba GVH po
przeszczepieniu (>2
stopnia)
Stosowanie dużych
dawek promieniowania
GVHD po przeszczepieniu
innych tkankek/narządów
GVHD może wystąpić po:
przeszczepieniu innych niż szpik narządów
zawierających potencjalnie alloreaktywne
limfocyty T, jak np.
jelito cienkie czy
wątroba
po
przetoczeniu krwi
pacjentom z
niedoborami odporności i poddawanym
głębokiej immunosupresji (np. podczas
chemioterapii nowotworów) przed
przetoczeniem należy usunąć leukocyty!!!
Usunięcie limfocytów T z zawiesiny szpiku
zmniejsza częstość występowania choroby
GVH, lecz równocześnie zwiększa ryzyko
odrzucenia przeszczepu.
W okresie odległym częściej także dochodzi
do wznowy choroby u pacjentów z białaczką.
reakcja przeszczep
przeciwko białaczce
(GVL)
reakcja przeszczep
przeciwko
nowotworowi (GVT)
GVH i GVT – podobieństwa i
różnice
Przeszczep przeciwko
gospodarzowi
Przeszczep przeciwko
białaczce
GVT/GVL
Reakcja GVT odpowiada za rzadsze
występowanie nawrotów nowotworu u
chorych, którym przeszczepiano szpik
allogeniczny, dlatego przy przeszczepieniu z
powodu choroby nowotworowej leczeniem z
wyboru jest zazwyczaj przeszczep
allogeniczny.
Prowadzone są próby potęgowania reakcji
GVT w celu eliminacji pozostałych lub
odnawiających się komórek nowotworowych.
Przy wznowie nowotworu stosuje się infuzje
limfocytów od dawcy (donor lymphocyte infusion
– DLI).
Przeszczep komórek
krwiotwórczych – powikłania
odległe
powikłania immunosupresji
z powodu
kondycjonowania
immunosupresji
potransplantacyjnej
wolnej odnowy układu
odpornościowego
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
- Slide 78
- Slide 79
- Slide 80
- Slide 81
- Slide 82
- Slide 83
- Slide 84
- Slide 85
- Slide 86
- Slide 87
- Slide 88
- Slide 89
- Slide 90
- Slide 91
- Slide 92
- Slide 93
- Slide 94
- Slide 95
- Slide 96
- Slide 97
- Slide 98
Wyszukiwarka
Podobne podstrony:
SEMINARIUM IMMUNOLOGIA Prezentacja
Cw 7 IMMUNOLOGIA TRANSPLANTACYJNA
FARMAKOLOGIA Immunologiczny, technik farmaceutyczny, farmakologia
immuno4, materiały farmacja, Materiały 3 rok, mat 3 rok, Immuno
seminarka immunologia
Seminarium 5 Odpowiedz nieswoista FARMACJA 2
26. Immunologia transplantacyjna, immunologia, immunologia, Immunologia, streszczenia
immunosupresja w transplantologii w
Seminarium 5 Odpowiedz nieswoista FARMACJA
immunologia transplantacyjna ok, Immunologia
SEMINARIUM 1 Z FARMAKOGNOZJI, materiały farmacja, Materiały 3 rok, Od Ani, Farmakognozja, Farmakogno
seminaria program, Płyta farmacja Poznań, III rok, Biologia molekularna
SEMINARIUM II, materiały farmacja, Materiały 3 rok, mat 3 rok, Biochemia
Prac IMMUNOLOGII TRANSPLANTACYJNEJ II r WL
Immunosupresja w Transplantologii 2
Leki immunomodulujące i przeciwpadaczkowe, farmacja, układ nerwowy
Wykład 5 - Immunologia transplantacyjna, Analityka Medyczna UMB, III, Immunopatologia, Wykłady
więcej podobnych podstron