
Cykl Krebsa
Łańcuch oddechowy
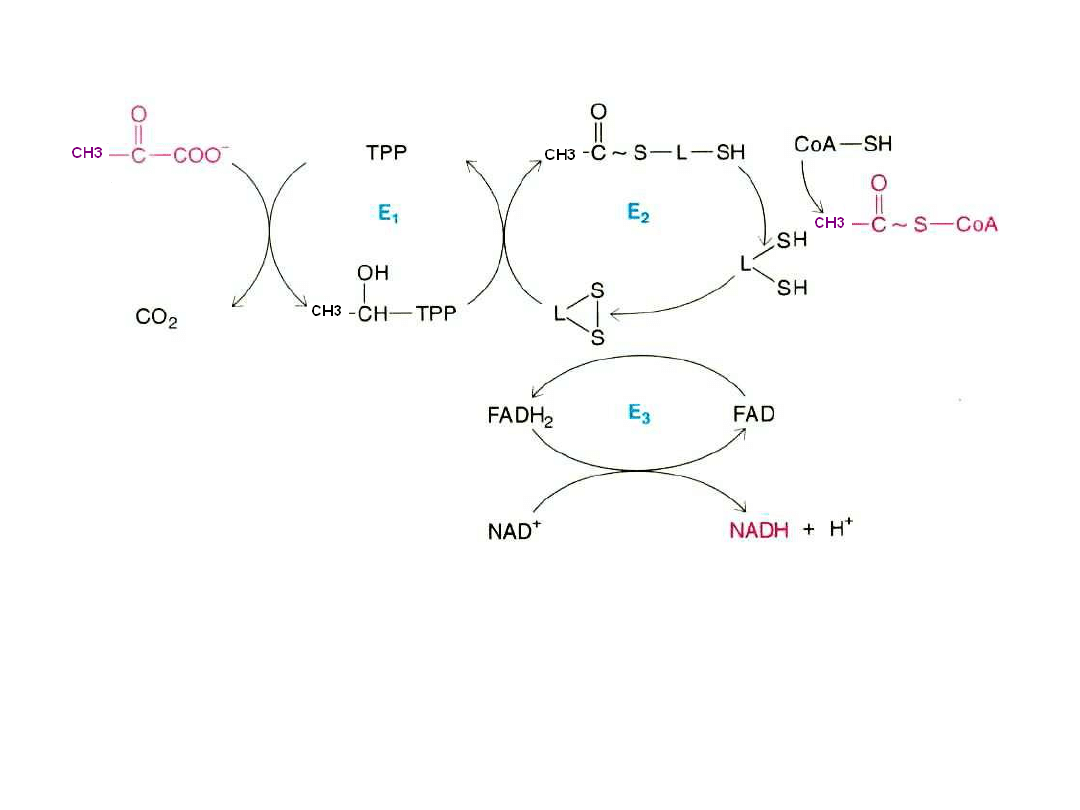
Oksydatywna dekarboksylacja
pirogronianu
Kompleks dehydrogenazy pirogronianowej:
E
1
– dehydrogenaza pirogronianowa o aktywności
dekarboksylazy
E
2
– acetylotransferaza dihydroliponianowa
E
3
– dehydrogenaza dihydroliponianowa
hydroksyet
ylo-TPP

Cykl Krebsa = Cykl kwasu
cytrynowego = Cykl kwasów
trójkarboksylowych
jest końcowym, wspólnym szlakiem utleniania substratów
energetycznych – białek (aminokwasów), kwasów tłuszczowych,
węglowodanów;
główny ośrodek metaboliczny komórki;
u eukariontów zachodzi w matrix mitochondrialnym (wewnątrz
mitochondrium);
działa wyłącznie w warunkach tlenowych, gdyż wymaga stałego
dopływu NAD
+
i FAD;
szybkość przemian cyklu zależy od zapotrzebowania komórki na
ATP;
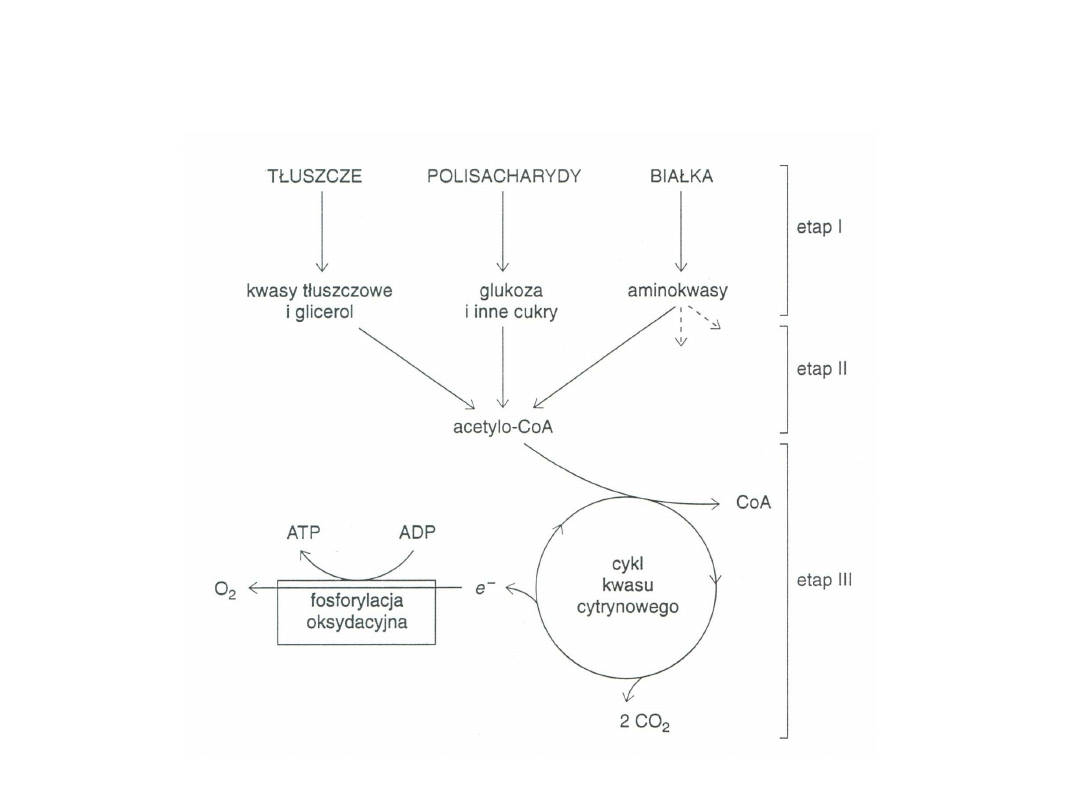
Cykl kwasu cytrynowego
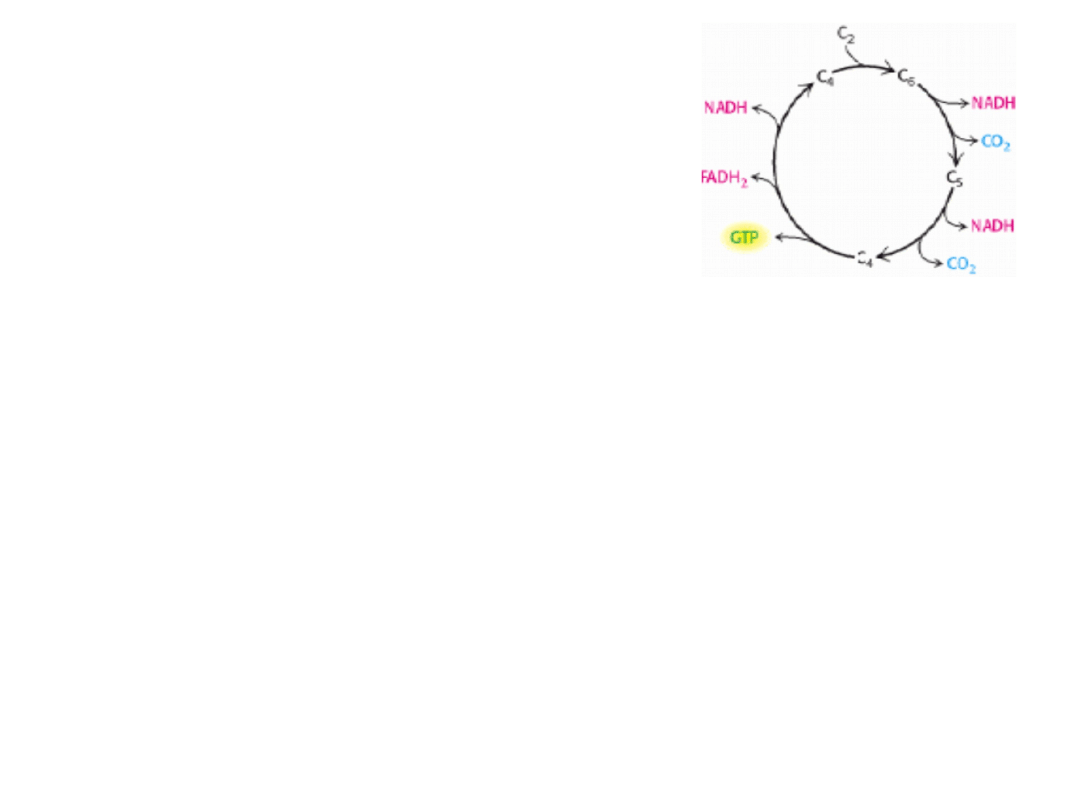
Cykl kwasu
cytrynowego
1. Związek czterowęglowy (szczawiooctan)
kondensuje z jednostką dwuwęglową
(grupą acetylową), tworząc
sześciowęglowy kwas trikarboksylowy
(cytrynian);
2. Izomer cytrynianu jest następnie oksydacyjnie dekraboksylowany –
powstaje związek pięciowęglowy (α-ketoglutaran);
3. Związek pięciowęglowy (α-ketoglutaran) ulega znów oksydacyjnej
dekarboksylacji do związku czterowęglowego (bursztynian), z którego
następnie jest regenerowany szczawiooctan;
4. Dwa atomy węgla wchodzą do cyklu w postaci grupy acetylowej i
opuszczają go w postaci dwóch cząsteczek CO
2
;
5. Trzy jony hydroniowe (6 elektronów) zostają przeniesione na 3
cząsteczki NAD
+
, natomiast jedna para atomów wodoru (a zatem dwa
elektrony) zostaje przeniesiona na FAD;
6. Funkcją cyklu kwasu cytrynowego jest odbieranie
wysokoenergetycznych elektronów z substratów energetycznych;

Funkcje cyklu kwasu cytrynowego
dostarcza wysokoenergetycznych elektronów związanych z
NADH i FADH
2
, które są zamieniane na energię
magazynowaną w ATP w łańcuchu oddechowym w procesie
fosforylacji oksydacyjnej;
dostarcza energii w postaci GTP;
dostarcza ważnych prekursorów do syntezy innych
cząsteczek (np. aminokwasów, cholesterolu i in.);
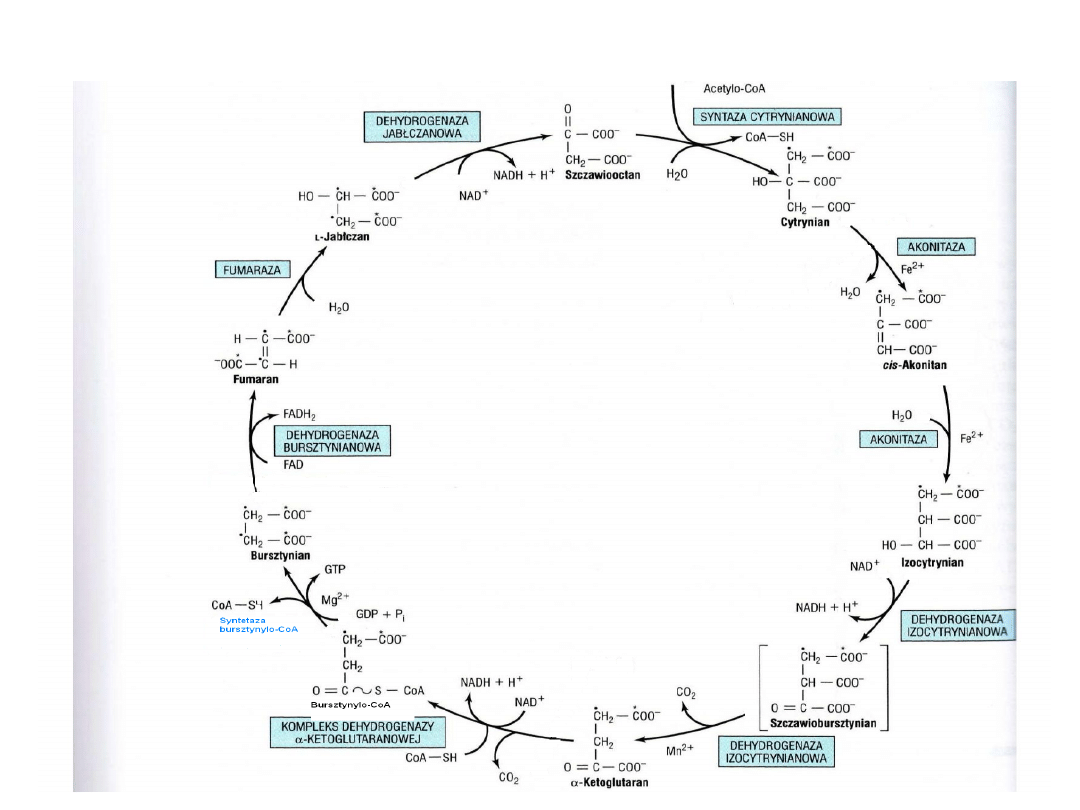
Cykl kwasu cytrynowego

Łańcuch oddechowy i fosforylacja
oksydacyjna
Łańcuch oddechowy
, ostatni etap oddychania
wewnątrzkomórkowego, przebiegający na wewnętrznych
błonach mitochondrium i polegający na przenoszeniu elektronów
i protonów na kolejne przenośniki. Kolejnym etapom tej
wędrówki elektronów towarzyszy wydzielanie się energii, która
zostaje wykorzystana do syntezy ATP z ADP. Ostatecznym
akceptorem elektronów i protonów jest tlen, a reakcja ta
prowadzi do utworzenia cząsteczki wody.
Fosforylacja oksydacyjna
– proces syntezy ATP
zachodzący w wyniku przeniesienia elektronów z NADH lub
FADH
2
na O
2
przez szereg przenośników elektronów.
Proces ten zachodzi w mitochondriach i jest głównym
źródłem ATP u organizmów tlenowych.
1. Składniki łańcucha oddechowego różnią się powinowactwem
do elektronów – wzrasta ono w miarę przebiegu łańcucha;
2. Elektrony (z NADH i FADH
2
) wchodzą w łańcuch oddechowy z
wysoką energią i w trakcie transportu energię tę powoli
tracą;
3. W miejscach, w których uwalniana jest wystarczająca ilość
energii dochodzi do pompowania protonów
Najważniejsze zasady funkcjonowania
łańcucha oddechowego
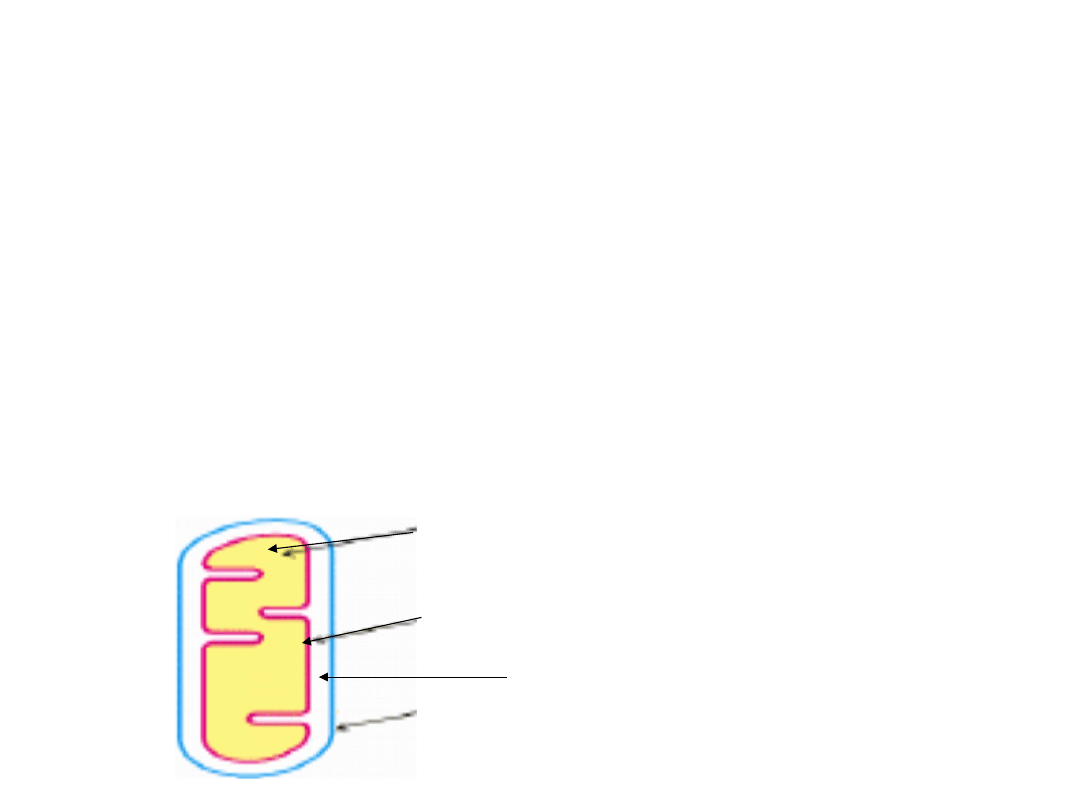
przestrzeń periplazmatyczna
matrix (wnętrze)
mitochondrium
wewnętrzna błona mitochondrium
zewnętrzna błona mitochondrium
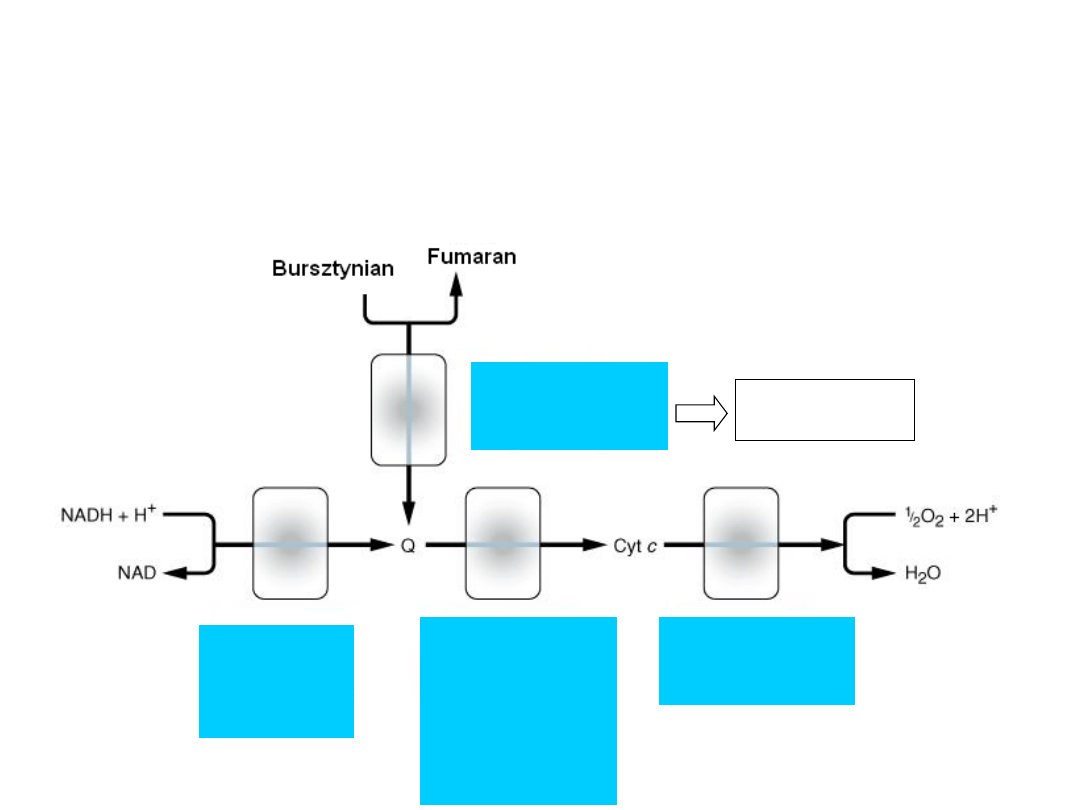
Łańcuch oddechowy
W skład łańcucha oddechowego wchodzą cztery kompleksy:
trzy pompy protonowe i kompleks związany z cyklem kwasu
cytrynowego
Kompleks II
reduktaza
bursztynian-Q
nie pompuje
protonów
Kompleks I
oksydored
uktaza
NADH-Q
Kompleks IV
oksydaza
cytochromowa
Kompleks III
oksydoredukt
aza Q-
cytochrom c =
oksydoredukt
aza
cytochromowa

Łańcuch oddechowy - ogólnie
1. Elektrony są przenoszone z NADH na O
2
poprzez trzy wielkie
kompleksy białkowe o nazwie:
• oksydoreduktaza NADH-Q
• oksydoreduktaza Q-cytochrom c
• oksydaza cytochromu c (cytochromowa)
2. Przepływ elektronów przez te kompleksy transbłonowe powoduje
transport protonów w poprzek wewnętrznej błony mitochondrialnej
3. Elektrony przenoszone są z oksydoreduktazy NADH-Q do drugiego
kompleksu łańcucha, oksydoreduktazy Q-cytochrom c przez
zredukowaną formę koenzymu Q (ubichinonu)
4. Ubichinon przenosi także do oksydoreduktazy Q-cytochrom c
elektrony z FADH
2
, który powstaje podczas utleniania bursztynianu w
cyklu kwasu cytrynowego, dostarczane przez reduktazę bursztynian-
Q
5. Cytochrom c, małe rozpuszczalne białko, przerzuca elektrony z
oksydoreduktazy Q-cytochrom c na oksydazę cytochromu c –
końcowy składnik łańcucha katalizujący redukcję O
2
.

Łańcuch oddechowy – poszczególne
kompleksy
Kompleks I – oksydoreduktaza
NADH-Q
1. Elektrony z NADH wprowadzane są do łańcucha oddechowego na
poziomie oksydoreduktazy NADH-Q. Jest to pierwsza pompa
protonowa.
2. Pierwszym etapem jest związanie NADH i przeniesienie jego dwóch
elektronów o wysokim potencjale na grupę prostetyczną kompleksu –
FMN, który przechodzi w formę zredukowaną FMNH
2
.
3. Elektrony z FMNH
2
zostają następnie przekazane na szereg centrów
żelazo-siarkowych (są to układy niehemowe), stanowiących drugi typ
grup prostetycznych oksydoreduktazy NADH-Q. Jony żelaza tych
centrów przechodzą na zmianę od stanu Fe
2+
(zredukowany) do stanu
Fe
3+
(utleniony) i odwrotnie. Tutaj nie zachodzi uwalnianie i wiązanie
protonów.
4. Elektrony centrów żelazo-siarkowych oksydoreduktazy NADH-Q są
następnie przekazywane na koenzym Q. Przejście dwóch elektronów z
NADH do koenzymu Q za pośrednictwem oksydoreduktazy NADH-Q
powoduje wypompowanie protonów z matrix mitochondrialnej.
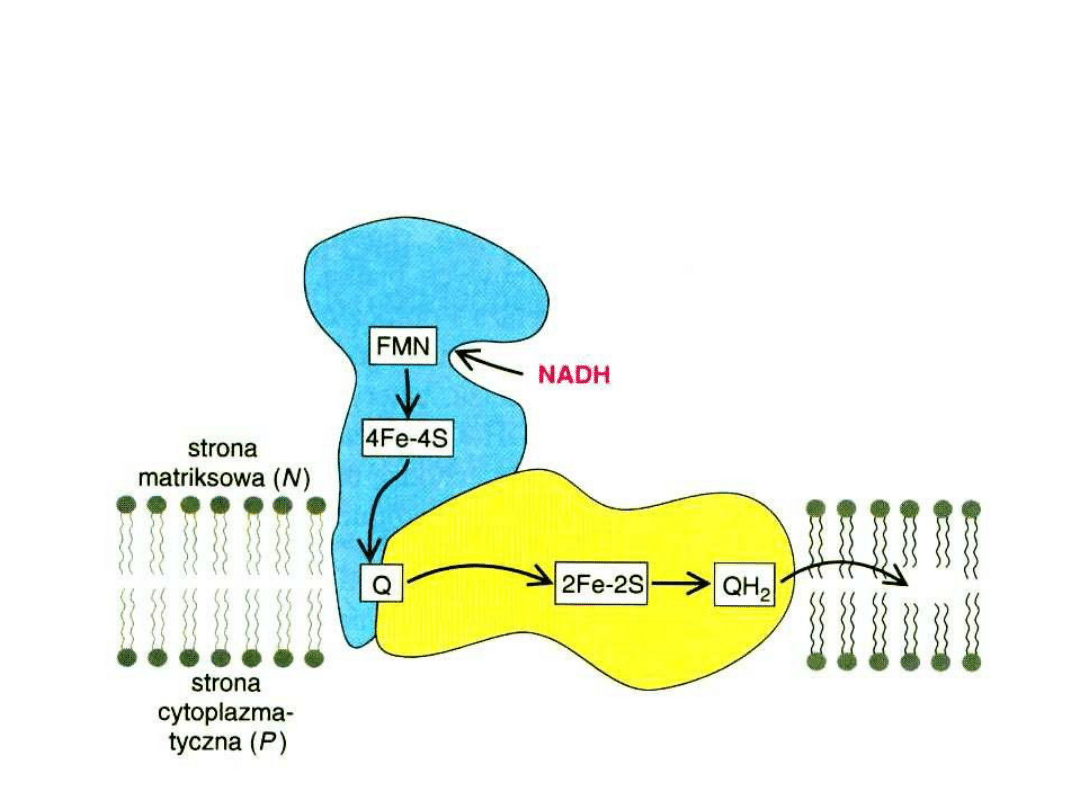
Łańcuch oddechowy – poszczególne
kompleksy
Kompleks I Oksydoreduktaza NADH-Q

Łańcuch oddechowy – poszczególne
kompleksy
Kompleks II – reduktaza bursztynian-Q
1. Dehydrogenaza bursztynianowa, enzym cyklu kwasu
cytrynowego, który tworzy FADH
2
, podczas utleniania
bursztynianu do fumaranu, stanowi część kompleksu reduktazy
bursztynian-Q.
2. Kompleks ten jest integralną częścią wewnętrznej błony
mitochondrialnej.
3. FADH
2
nie opuszcza kompleksu II. Jego elektrony są przenoszone
na centra Fe-S, a następnie na koenzym Q, który przekazuje je
dalej na łańcuch oddechowy.
4. Kompleks reduktazy brsztynian-Q nie pompuje protonów, dlatego
podczas utleniania FADH
2
tworzy się mniej cząsteczek ATP niż
podczas utleniania NADH.

Łańcuch oddechowy – poszczególne
kompleksy
Kompleks III – oksydoreduktaza Q-
cytochrom c
1. Jest to druga pompa protonowa
2. Cytochrom jest białkiem transportującym elektrony, który zawiera
hem jako grupę prostetyczną. Podczas transportu elektronów jon
żelaza cytochromu przechodzi ze stanu zredukowanego (+2) do
stanu utlenionego (+3).
3. Funkcją oksydoreduktazy Q-cytochrom c jest katalizowanie
przeniesienia elektronów z QH
2
do utlenionego cytochromu c, białka
rozpuszczalnego w wodzie, oraz równoczesne wypompowanie
protonów z matrix mitochondrialnej.

4. Oksydoreduktaza Q-cytochrom c jest dimerem.
5. Ze względu na dwa rodzaje hemów występujących w enzymie
określa się go jako cytochrom bc
1
.
6. Poza cytochromami enzym zawiera także białko żelazo-siarkowe z
centrum 2Fe-2S.
Łańcuch oddechowy – poszczególne
kompleksy
Kompleks III – oksydoreduktaza Q-
cytochrom c

Łańcuch oddechowy – poszczególne
kompleksy
Kompleks IV – oksydaza cytochromu c =
oksydaza cytochromowa
1. W ostatniej fazie łańcucha transportu elektronów zachodzi utlenianie
cytochromu c, zredukowanego na skutek działania kompleksu III,
sprzężone z redukcją O
2
do cząsteczki H
2
O.
2. Tę reakcję katalizuje oksydaza cytochromu c – kompleks IV.
3. Oksydaza cytochromu c zawiera dwa hemy A i trzy jony miedzi.
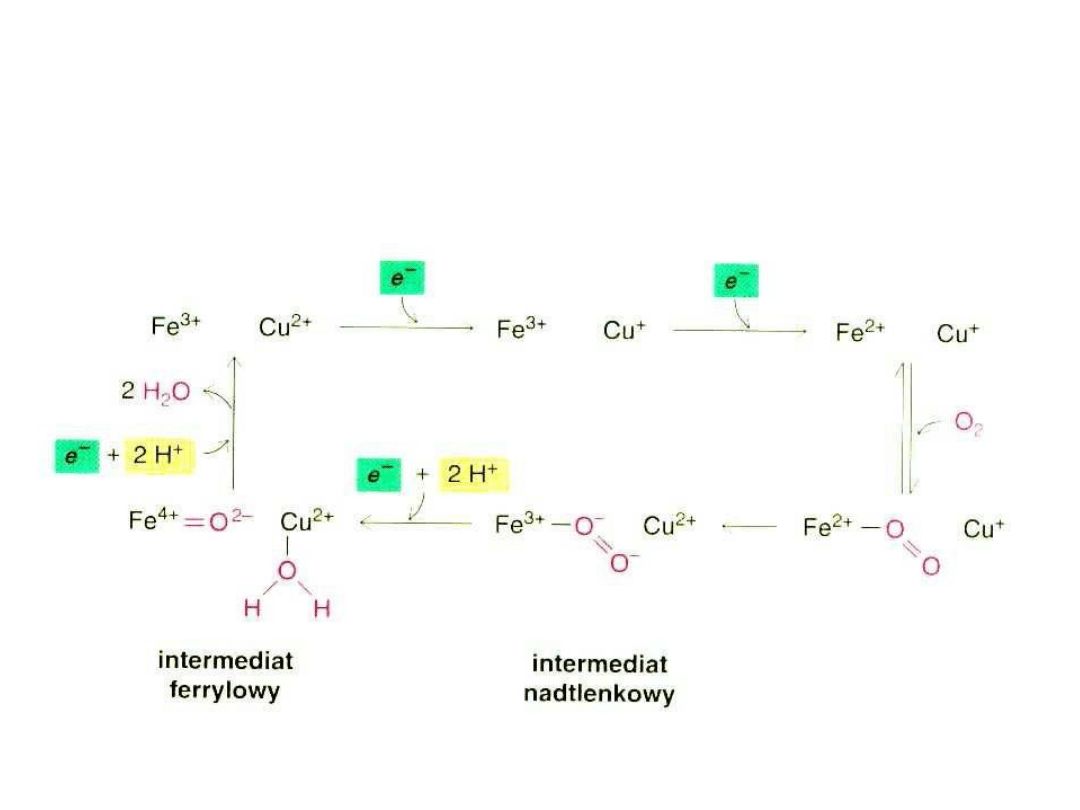
Łańcuch oddechowy – poszczególne
kompleksy
Mechanizm bezpiecznej redukcji tlenu
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
Wyszukiwarka
Podobne podstrony:
5 Wstep do metabolizmu; cykl Krebsa i lancuch oddechowy
Cykl Krebsa
cykl krebsa 3
cykl krebsa
Cykl Krebsa 2
Cykl Krebsa
Cykl Krebsa cykl kwasu cytrynowego
GLIKOLIZA + cykl Krebsa
Cykl Krebsa, cykl kwasu cytrynowego
cykl krebsa, SGGW, biochemia
cykl krebsa pdf
CYKL KREBSA (2), materiały medycyna SUM, biochemia, Kolokwium VII
węglowodany kolosy pytania, Medycyna, Biochemia ŚUM Katowice, Kolokwium węglowodany cykl Krebsa
Opracowanie pytań na kolosa Węgle i cykl Krebsa
1 cykl krebsa, Zootechnika UP Lublin, biochemia
cykl krebsa 3
17 - 21.03.2001(etanol cykl Krebsa ł oddechowy w rodniki, materiały medycyna SUM, biochemia, Kolokwi
więcej podobnych podstron