Strategia diagnostyki cytogenetycznej – konspekt do
ćwiczeń
Katedra i Zakład Genetyki Medycznej
dr Anna Skorczyk
Cytogenetyka – dział genetyki zajmujący się badaniem chromosomów
Cytogenetyka kliniczna - zajmuje się badaniem chromosomów w komórkach organizmu
ludzkiego, ich nieprawidłowości i związku z obrazem klinicznym
Cytogenetyka:
cytogenetyka klasyczna:
o
badanie kariotypu za pomocą technik prążkowania chromosomów
cytogenetyka molekularna:
o
technika FISH
o
inne techniki z wykorzystaniem sond molekularnych
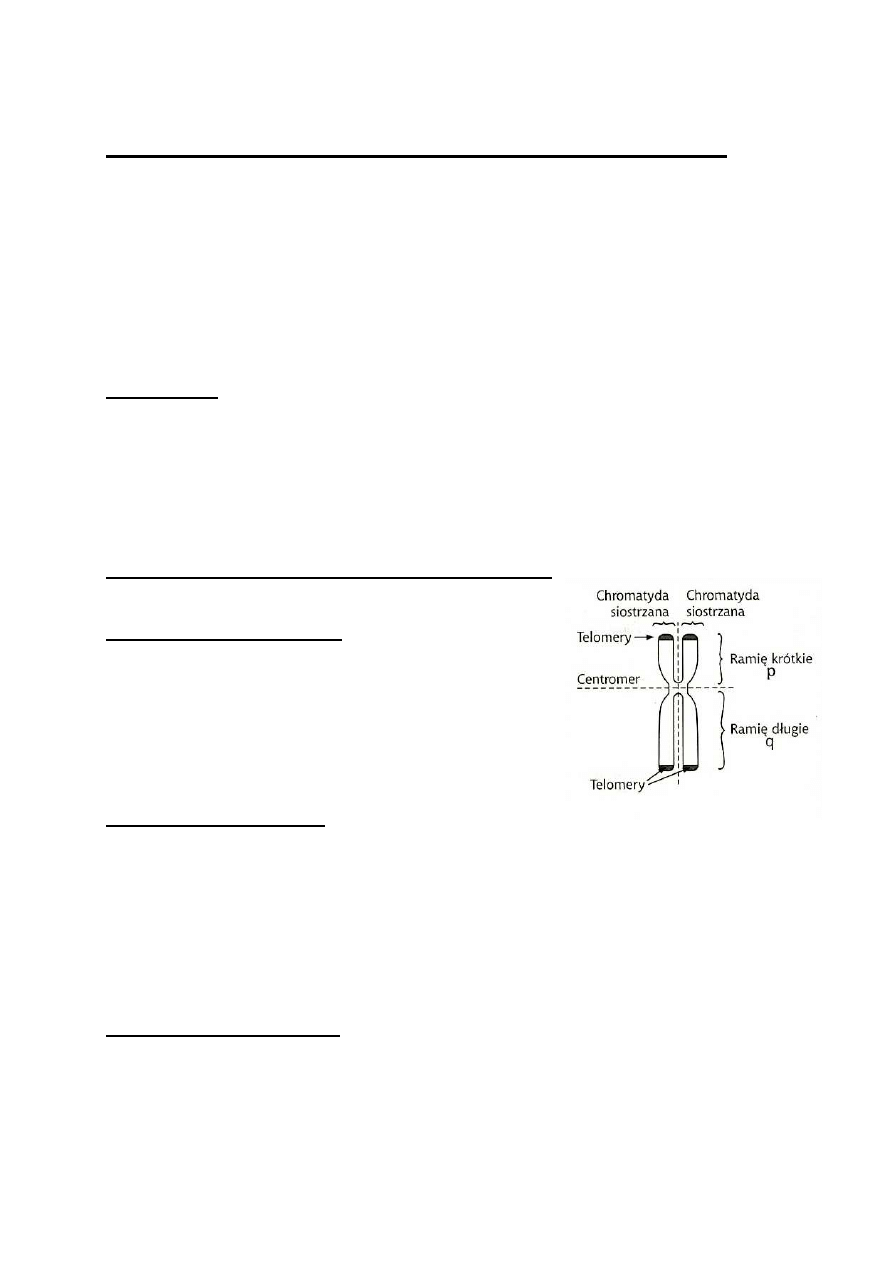
Budowa morfologiczna chromosomu w stadium metafazy:
Typy chromosomów człowieka
(na podstawie położenia centromeru):
-
Metacentryczne
-
Submetacentryczne
-
Akrocentryczne
U człowieka nie występują chromosomy telocentryczne!
Grupy chromosomów - pary
A
1-3
duże chromosomy metacentryczne
B
4-5
duże chromosomy submetacentryczne
C
6-12 i X
średnie chromosomy submetacentryczne
D
13-15
duże chromosomy akrocentryczne
E
16-18
małe chromosomy submetacentryczne
F
19-20
małe chromosomy metacentryczne
G
21-22 i Y
małe chromosomy akrocentryczne
Aberracje chromosomów:
-
aberracje liczby chromosomów
-
aberracje struktury chromosomów
Aberracje mogą dotyczyć zarówno chromosomów płci, jak i autosomów
Aberracje liczby chromosomów
- ogólna liczba chromosomów jest różna od prawidłowej liczby 46 chromosomów.
- zmiany liczbowe mogą dotyczyć zarówno całego zestawu chromosomów (poliploidie),
jak i pojedynczego chromosomu (aneuploidie).
Poliploidia
- Triploidia (69,XXX,XXY lub XYY)
-3% wszystkich poczęć,
w większości przypadków poronienia samoistne
Aneuploidia (autosomy)
- Nullisomia (utrata pary chromosomów homologicznych)
- letalne przed implantacją
- Monosomia (utrata jednego chromosomu)
- letalne w stadium embrionalnym
- Trisomia (jeden chromosom dodatkowy)
- zwykle letalne, z wyjątkiem
trisomii chromosomów 13, 18, 21
Aneuploidia (chromosomy płci)
- Dodatkowy chromosom płci
- normalna długość życia
- Utrata chromosomu płci (45,X)
- 99% przypadków-poronienia
samoistne, normalna inteligencja,
bezpłodność
Poliploidie
Triploidia - obecność dodatkowego haploidalnego zestawu chromosomów w wyniku czego
w jądrze komórkowym zamiast 46 mamy 69 chromosomów.
Triploidia powstaje w wyniku:
-
Zapłodnienia komórki jajowej przez dwa plemniki, czyli tak zwanej dispermii.
-
Połączenia się nieprawidłowej diploidalnej gamety żeńskiej z prawidłowym plemnikiem,
czyli tak zwanej dygynii.
-
Połączenia się nieprawidłowego diploidalnego plemnika z prawidłową gametą żeńską,
czyli tzw. diandrii (najrzadsze).
Triploidia – obraz kliniczny
-
Jeśli dodatkowy zestaw chromosomów pochodzi od matki charakterystyczne cechy
fenotypowe płodu to: wewnątrzmaciczne ograniczenie wzrostu, bardzo małe łożysko
(niski poziom βhCG) i hipoplazja nadnerczy.
-
Jeśli dodatkowy zestaw chromosomów pochodzi od ojca mamy do czynienia z bardzo
dużym łożyskiem i zaśniadem groniastym, przy często normalnych rozmiarach płodu.
-
Cechy fenotypowe to także: syndaktylia 3. i 4. palca, wady układu płciowego
i moczowego, wady rozwojowe mózgu, wady serca.
-
Triploidia jest aberracj
ą letalną, czyli prowadzi do obumarcia płodu (najczęściej) lub
śmierci noworodka.
Tetraploidia - obecność dwóch dodatkowych haploidalnych zestawów chromosomów
w wyniku czego w jądrze komórkowym zamiast 46 mamy 92 chromosomów.
Tetraploidia powstaje w wyniku:
-
Nieprawidłowego pierwszego podziału zygoty.
-
Tetraploidia jest aberracja letalną, prowadzącą do obumarcia zarodka/płodu.

Aneuploidie
Trisomia - występowanie dodatkowego chromosomu homologicznego danej pary.
-
Trisomia jest wynikiem zjawiska nondysjunkcji, czyli nierozdzielenia się chromosomów
homologicznych lub chromatyd w trakcie podziału mejotycznego lub mitotycznego.
-
Wynikiem nondysjunkcji jest powstanie z jednej strony gamet disomicznych (z dwoma
chromosomami) lub z drugiej strony nullisomicznych (bez chromosomu).
-
Połączenie gamety disomicznej z prawidłową prowadzi do powstania trisomii określonej
pary chromosomów.
-
Połączenie gamety nullisomicznej z gametą prawidłową prowadzi do powstania
monosomii określonej pary chromosomów.
Monosomia - brak jednego chromosomu homologicznego w danej parze.
-
Monosomia powstaje w wyniku nondysjunkcji.
-
Efektem nondysjunkcji jest powstanie gamety nullisomicznej pozbawionej chromosomu
danej pary.
-
Po połączeniu nullisomicznej gamety z gametą prawidłową powstaje monosomia
okre
ślonej pary chromosomów.
-
W przypadku zespołu Turnera (45,X) monosomia może być wynikiem opóźnionego
ruchu chromosomu Y w stadium anafazy.
Aneuploidie – skutki:
-
Wi
ększość trisomii i monosomii jest letalna – prowadzi do obumarcia zarodka/płodu
we wczesnym okresie ciąży, najczęściej w pierwszym trymestrze ciąży.
Wyjątek stanowią trisomie chromosomów pary: 13, 18 i 21 oraz monosomia
chromosomu X, które spotyka się u żywo urodzonych noworodków.
-
Także aberracje liczbowe chromosomów płci, takie jak: 47,XXY; 47,XXX; 47,XYY
zwi
ązane są z łagodniejszymi skutkami klinicznymi.
-
Monosomie są letalne w bardzo wczesnym stadium rozwojowym (embrionu), prowadząc
do bardzo wczesnej utraty ciąży, która nie jest klinicznie rozpoznawalna w tym czasie
(najczęściej kobieta jeszcze nie wie, że jest w ciąży).
-
Do nondysjunkcji najczęściej dochodzi w gamecie matczynej, podczas oogenezy (90%
przypadków), rzadko nondysjunkcja występuje w trakcie spermatogenezy.
-
Zjawisko nondysjunkcji jest zwi
ązane z wiekiem matki (efekt wieku).
-
U kobiet między 20-29 rokiem
życia ryzyko jest stałe, natomiast po ukończeniu 30
roku
życia ryzyko nondysjunkcji sukcesywnie rośnie wraz z wiekiem matki.
-
Ryzyko związane z wiekiem jest takie same dla kobiet, które wcześniej urodziły dziecko,
jak i dla kobiet, dla których jest to pierwsza ciąża.
Aberracje liczbowe:
-
powstają najczęściej de novo, a nie w wyniku odziedziczenia od rodziców.
-
Aberracje liczbowe, poza kilkoma wyjątkami prowadzą do obumarcia zarodka/płodu,
martwego porodu lub zgonu okołoporodowego
-
Aberracje liczbowe chromosomów stanowią około 50% przyczyn poronie
ń
samoistnych w pierwszym trymestrze ci
ąży.
Mozaikowo
ść - występowanie w jednym organizmie dwóch lub więcej linii komórkowych
o różnym kariotypie, pochodzących z tej samej zygoty.
Pochodzenie mozaikowości:

-
Aberracja chromosomowa powstała po zapłodnieniu, podczas pierwszych podziałów
zygoty, w wyniku nieprawidłowego podziału mitotycznego.
-
Aberracja jest wynikiem ratowania embrionu z aberracją chromosomową, kiedy z tylko
z części komórek nadmierny materiał zostaje usunięty.
Aberracje struktury chromosomów
Zrównowa
żone
•Translokacje zrównoważone
•Inwersje
Niezrównowa
żone
•Duplikacje
•Delecje
•Chromosomy pierścieniowe
•Izochromosomy
•Fragmenty centryczne
Aberracje zrównowa
żone
Translokacje
Przemieszczenie się materiału genetycznego pomiędzy chromosomami
Typy translokacji:
-
Wzajemne
-
Robertsonowskie
-
Insercyjne
Translokacja wazjemna zrownowa
żona
-
Fragmenty chromosomów oderwały się i zamieniły się miejscami.
-
Nie doszło do utraty materiału genetycznego
Translokacja robertsonowska (fuzja centryczna)
-
Dotyczy chromosomów akrocentrycznych
-
Dwa chromosomy akrocentryczne tracą ramiona krótkie i łączą się ze sobą – powstaje
jeden chromosom dwuramienny
Translokacja robertsonowska jest translokacj
ą zrównoważoną, ponieważ utrata ramion
krótkich chromosomów akrocentrycznych nie powoduje utraty genów
Inwersja
-
Chromosom ulega złamaniu w 2 miejscach, a fragment pomiędzy złamaniami ulega
odwróceniu o 180 stopni
-
Inwersja jest aberracją zrównoważoną
Inwersja paracentryczna – oba złamania są w obrębie jednego ramienia i odwrócony
fragment nie zawiera centromeru
Inwersja pericentryczna – złamania nastąpiły w obydwu ramionach chromosomu
i odwrócony fragment zawiera centromer

Aberracje niezrównowa
żone:
Delecja - utrata części chromosomu
Duplikacja - podwojenie części chromosomu
Delecje i duplikacje są aberracjami niezrównowa
żonymi – łączą się z utratą lub nadmiarem
materiału genetycznego
Chromosom pier
ścieniowy
-
Chromosom pęka w obu ramionach, dystalne części chromosomów ulegają utracie,
a pozostała część chromosomu tworzy pierścień
-
Aberracja chromosomowa niezrównowa
żona
Izochromosom
-
Nieprawidłowy chromosom, który ma delecję jednego, a duplikację drugiego ramienia
-
Może powstać wskutek poprzecznego podziału centromeru
-
Aberracja niezrównowa
żona
Chromosomy markerowe
-
Małe dodatkowe chromosomy niejasnego pochodzenia, stwierdzane w 1/2500 ciąż
-
W 90% przypadków pochodzą z krótkich ramion chromosomów akrocentrycznych
(około połowa pochodzi z chromosomu 15)
-
Chromosomy markerowe wymagają identyfikacji metodami cytogenetyki molekularnej
(FISH – malowanie chromosomów)
Kliniczne skutki aberracji chromosomowych:
Niezrównowa
żonych:
U zarodka - obumarcie
U dzieci żywo urodzonych:
- Zespoły wad wrodzonych z upośledzeniem umysłowym
- Upośledzenie umysłowe z cechami dysmorfii
- Zaburzenia cielesno-płciowe
Zrównowa
żonych
nosiciel aberracji jest zdrowy, ale mo
że mieć niepowodzenia rozrodu (brak ciąży,
poronienia samoistne, porody martwe, dzieci z zespołem wad i upośledzeniem
umysłowym)
Fenotyp osoby z niezrównowa
żoną aberracją chromosomową w zakresie autosomów
-
Często dystrofia wewnątrzmaciczna
-
Często nieprawidłowy przebieg ciąży (krwawienie z dróg rodnych, nieprawidłowa ilość
płynu owodniowego, wady płodu w badaniu USG)
-
Wady wrodzone, w tym wady narządów wewnętrznych, często wada serca
-
Dysmorfia twarzy, dysplastyczne małżowiny uszne
-
Upo
śledzenie umysłowe – zawsze, nawet przy słabo wyrażonych pozostałych w/w
objawach
Zespoły mikrodelecji
-
Delecje chromosomów są bardzo małe, na granicy rozdzielczości metod klasycznej
cytogenetyki, a nawet submikroskopowe
-
Diagnostyka: analiza chromosomów prometafazowych (HRBT) i FISH
-
Fenotyp: dysmorfia, wady rozwojowe i upośledzenie umysłowe

Przykłady zespołów mikrodelecji:
Z. Pradera-Williego 15q11-12
Z. Angelmana 15q11-12
Z. Wolf-Hirschhorna 4p16.3
Z. Miller-Dieker 17q13
Wskazania do okre
ślenia kariotypu:
-
Zespół wad wrodzonych współistniejący z opóźnieniem rozwoju/upośledzeniem
umysłowym
-
Upośledzenie umysłowe
-
Podejrzenie zespolu mikrodelecji
-
Zaburzenia różnicowania płci
-
Niepowodzenia rozrodu (brak ciąży, poronienia samoistne, obumarcie ciąży, zgon
dziecka w okresie perinatalnym)
Badanie kariotypu:
-
można użyć każdej rosnącej tkanki, najczęściej wykorzystuje się limfocyty krwi
obwodowej, czasem także na komórki szpiku kostnego lub fibroblasty skóry
-
w diagnostyce prenatalnej - komórki płynu owodniowego lub kosmówki
Badanie kariotypu z limfocytów krwi obwodowej:
-
pobrać jałowo do probówki z heparyną ok. 2-5 ml krwi
żylnej (od noworodka 1 ml)
i dostarczyć do laboratorium cytogenetycznego
-
jeśli transport krwi jest następnego dnia, probówkę z krwią przechowywać w lodówce
(+4ºC). Można też probówkę z krwią przesyłać szybką pocztą
-
nie wolno mrozić probówki z krwią przeznaczoną do badania kariotypu
Uwaga: u noworodka z wadami wrodzonymi, który zmarł zanim zdążono pobrać krew na
badanie kariotypu, można jeszcze jak najwcześniej (ew. nawet do 1 godz. po zgonie) pobrać
krew bezpośrednio z serca
Hodowla limfocytów krwi obwodowej
•przygotowanie pożywki do hodowli i dodanie do niej krwi
•hodowla w cieplarce przez 72 h
•zatrzymanie podziałów komórkowych – kolcemid
•rozproszenie chromosomów - roztwór hipotoniczny
•utrwalanie zawiesiny – metanol+kwas octowy
•nałożenie na szkiełka mikroskopowe
Podstawow
ą metodą badania cytogenetycznego jest standardowa ocena kariotypu
(najczęściej metoda prążkowa GTG).
Jednak w przypadku bardziej złożonych problemów diagnostycznych lub małych zmian
w obrębie struktury chromosomów niezbędna jest analiza z zastosowaniem innych technik np.
cytogenetyki molekularnej.
Techniki pr
ążkowe:
- prążki G (barwienie GTG)
- prążki Q (barwienie
OFQ)
- prążki C (barwienie
CTG)
- barwienie AgNOR (barwienie srebrowe)
- prążki R (barwienie
RBA) (prążkowania odwrotnego, ang. reverse)
Kiedy wykonuje się standardową analizę kariotypu?
•Aberracje liczby: poliploidie, aneuploidie (trisomia, monosomia)
•Aberracje
struktury:
delecje,
insercje,
translokacje,
chromosomy
pierścieniowe,
izochromosomy
Postępowanie w przypadku trudności w wykazaniu aberracji chromosomowej przy
zastosowaniu standardowego badania kariotypu
•Analiza
większej
liczby
płytek
metafazowych
(poszukiwanie
mozaikowości)
•Analiza chromosomów prometafazowych (HRBT – high resolution banding technique)
•Badanie kariotypu na podstawie fibroblastów skóry
•Metody cytogenetyki molekularnej (FISH)
Wskazania do badania kariotypu na podstawie fibroblastów skóry:
• Kariotyp mozaikowy w badaniu limfocytów
•Brak aberracji chromosomowej w badaniu standardowym (limfocyty) przy fenotypie
wskazującym na aberrację
• Fenotyp zespołu Pallister-Killian
Zasady zapisu kariotypu:
1) Liczba określająca całkowitą ilość chromosomów w komórce
2 )Po przecinku wymienione chromosomy płciowe
3) Po przecinku ewentualny opis aberracji
np. 46,XY
47,XX,+21
45,X
47,XXY
46,XX,t(2;6)(p12;q21)
FISH – fluorescencyjna hybrydyzacja in situ
Sondy stosowane w FISH:
malujące (wcp. – ang. whole chromosome paint)- pokrywające cały chromosom lub
poszczególne ramiona
alfa-satelitarne (centromerowe, telomerowe)
specyficzne (unikalne) dla poszczególnych sekwencji lub określonego locus
Materiał do badania FISH:
•fibroblasty
•limfocyty
•komórki szpiku kostnego
•komórki płynu owodniowego
•komórki trofoblastu
•komórki nabłonka jamy ustnej
•skrawki parafinowe
mozaikowata tetrasomia 12p (dwie normalne 12tki plus izochromosom 12p)
których tkanek
Genetyka kliniczna FISH
•diagnostyka submikroskopowych aberracji chromosomowych
•identyfikacja złożonych aberracji struktury chromosomów
•identyfikacja dodatkowego materiału chromosomowego
•identyfikacja chromosomów markerowych
•szybka diagnostyka aneuploidii chromosomowych
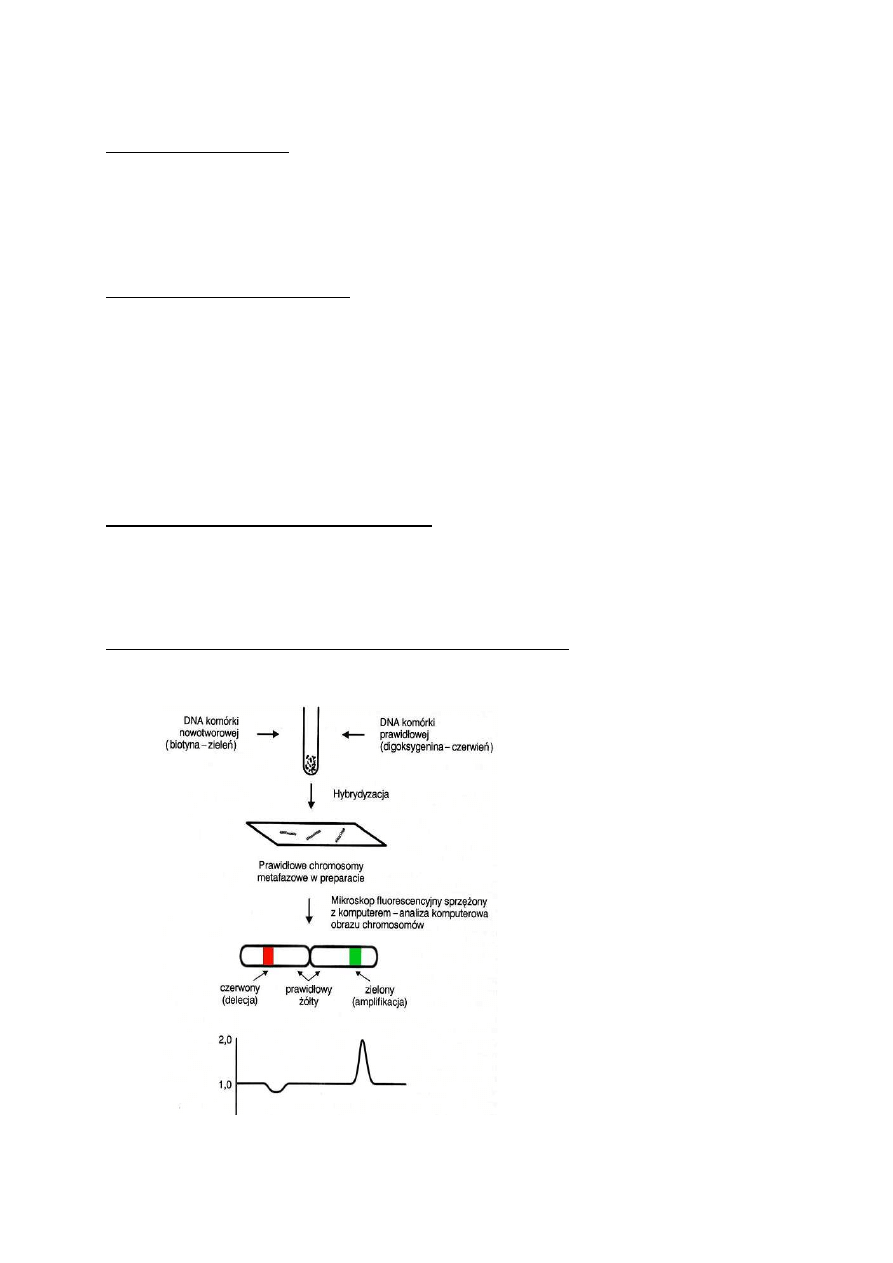
FISH w diagnostyce nowotworów
•detekcja amplifikacji genu
•badanie materiału genetycznego w jądrach interfazowych
•identyfikacja komórek szpiku kostnego dawcy po przeszczepie
•detekcja wczesnego nawrotu choroby
•monitorowanie efektu terapii
Cytogenetyka molekularna – inne techniki
•M-FISH (ang. multicolour FISH)
•SKY (SKY-FISH) (ang. spectral karyotyping)
•CGH (ang. comparative genomic hybridization) - porównawcza hybrydyzacja genomowa
CGH - Porównawcza hybrydyzacja genomowa – zasada metody
arrayCGH
Porównawcza hybrydyzacja ge
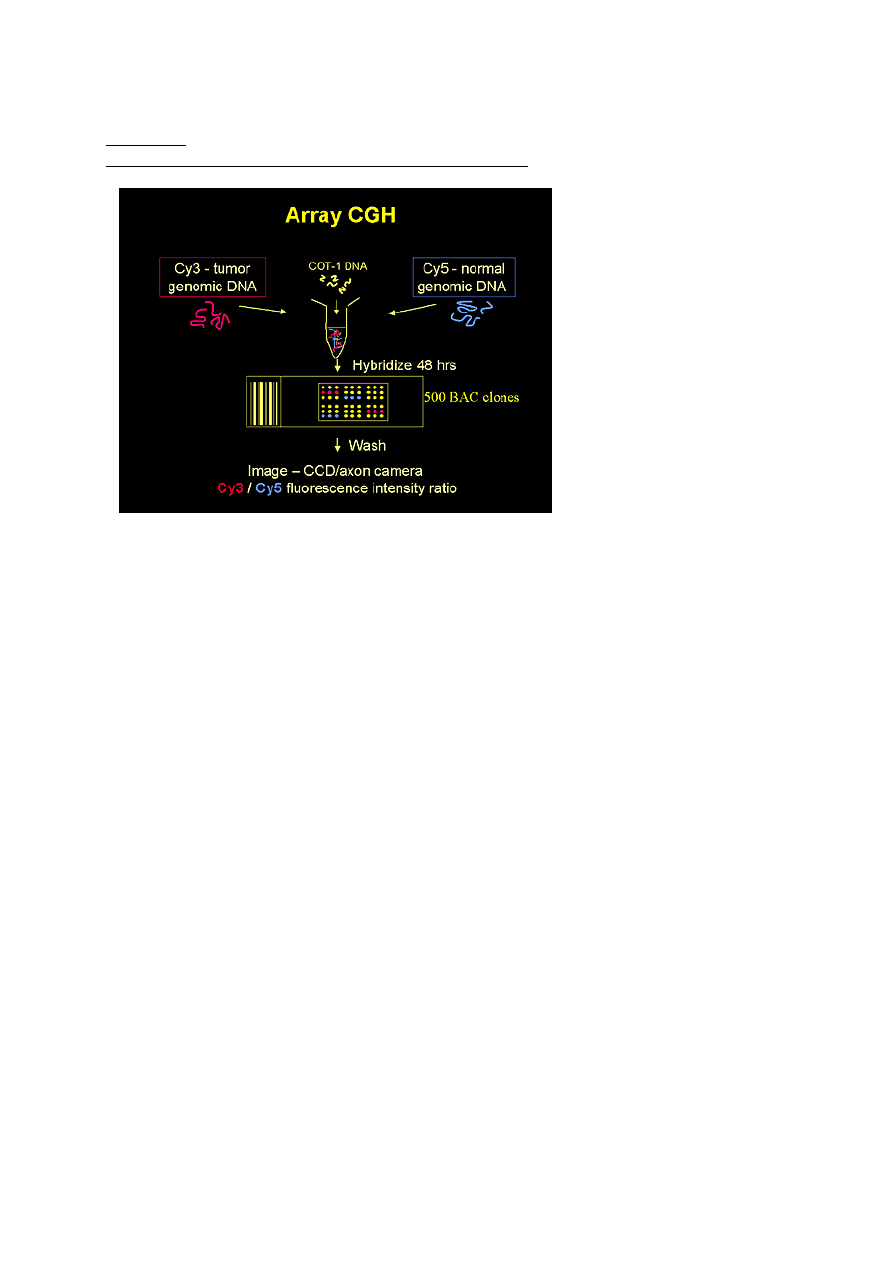
ArrayCGH
Porównawcza hybrydyzacja genomowa do mikromacierzy
Wyszukiwarka
Podobne podstrony:
konspekty do ćwiczeń, ratownictwo, patofizjologia
Konspekt do ćwiczeń gimnastycznych dla dzieci 3 (2), Konspekt do ćwiczeń gimnastycznych dla dzieci 3
14.04, Konspekt do cwiczenia 4-wyniki, Politechnika Łódzka
Metrologia - ola i bartek, Konspekt do cwiczenia 1B.O., Politechnika Łódzka
Konspekt do cwiczenia 2, Elektronika i Telekomunikacja, z PENDRIVE, Politechnika - EiT, 2011 2012 -
Opioidy konspekt do ćwiczen, farma;)
2010 10 01 Konspekt do cwiczenid 27147
konspekty do ćwiczeń
konspekt do ćwiczeń nr 2 z geologii
Konspekt do cwiczenia 1, Elektronika i Telekomunikacja, z PENDRIVE, Politechnika - EiT, 2011 2012 -
Konspekt do cwiczenia 5, Elektronika i Telekomunikacja, z PENDRIVE, Politechnika - EiT, 2011 2012 -
konspekty do ćwiczeń, ratownictwo, patofizjologia
ćwiczenia, Konspekt do zajęć gimnastyki korekcyjno, Konspekt do zajęć gimnastyki korekcyjno - kompen
więcej podobnych podstron