
Farmakoterapia cukrzycy

Cukrzyca jest zbiorem chorób metabolicznych,
charakteryzujących się hiperglikemią wywołaną
zaburzeniami:
• wydzielania insuliny,
• działania insuliny
• lub obydwu tych nieprawidłowości.
Przyczyny hiperglikemii istotnie się różnią w
zależności od typu cukrzycy.

Cukrzyca nie jest jedną chorobą
(klasyfikacja cukrzycy):
Typ 1
(ze zniszczeniem komórek beta wysp
Langerhansa)
Autoimmunologiczna ( cukrzyca typu
LADA),
idiopatyczna.
Typ 2
od form z przeważającą insulinoopornością
z względnym niedoborem insuliny, po formy
z bezwzględnym niedoborem insuliny, z lub
bez
insulinooporności.

Nazewnictwo stanów hiperglikemicznych
prawidłowa glikemia na czczo
: 70–99 mg/dl (3,4––5,5 mmol/l);
nieprawidłowa glikemia na czczo (IFG, impaired fasting glucose):
100–125 mg/dl (5,6–6,9 mmol/l);
nieprawidłowa tolerancja glukozy
(IGT, impaired glucose tolerance):
w 120. minucie OGTT według Światowej Organizacji Zdrowia (WHO,
World Health Organization) glikemia 140–199 mg/dl (7,8––11 mmol/l);
stan przedcukrzycowy
— IFG i/lub IGT;
cukrzyca
— jedno z następujących kryteriów:
1. objawy hiperglikemii i glikemia przygodna ≥ 200 mg/dl (≥ 11,1
mmol/l),
2. 2-krotnie glikemia na czczo ≥ 126 mg/dl (≥ 7,0 mmol/l),
3. glikemia w 120. minucie OGTT według WHO ≥ 200 mg/dl (≥ 11,1
mmol/l).
Zalecenia kliniczne dotyczące postępowania u chorych na cukrzycę, 2012
Interpretacja wyników badań stężenia
glukozy?
1. < 100 mg/dl ( 5,6 mmol/l) norma
2. 100- 125 mg/dl ( 5,6- 6,9 mmol/l)
nieprawidłowa tolerancja glukozy
na czczo
3. ≥126 mg/d ( 7,9mmol/l) CUKRZYCA
( obowiązują 2 nieprawidłowe
wyniki, lub objawy kliniczne)

Glikemia w 120 min oznaczona we krwi
żylnej - interpretacja
1. < 140 mg/dl ( 7,8 mmol/l) norma
2. od 140
– 199 mg/dl ( 7,8- 11,0 mmol/l)
nieprawidłowa tolerancja glukozy.
3. ≥ 200 mg/dl ( 11,1mmol/l) CUKRZYCA
Do rozpoznania cukrzycy konieczne jest
stwierdzenie dwóch nieprawidłowych wyników
badań.

Glikemia
przygodna ≥ 200 mg/dl
( 11,1mmol/l) oznaczona w próbce krwi pobranej w
dowolnej porze dnia niezależnie od spożytego posiłku
(przy obecnych objawach klinicznych) upoważnia do
rozpoznania CUKRZYCY.
W sytuacji braku objawów klinicznych konieczne jest
oznaczenia ponowne glikemii oraz wykonanie innych
badań np: profilu glikemii, HbA1c
( UWAGA !!!! W takiej sytuacji NIE WYKONUJE SIĘ
KRZYWEJ PO PODANIU GLUKOZY)

CUKRZYCA TYPU 1

Cukrzyca typu 1 charakteryzuje się bezwzględnym
niedoborem insuliny
Jawne objawy choroby występują wówczas, kiedy
zniszczeniu ulegnie około 80 -90 % komórek ß.
Najczęściej początek jest nagły, i często ma związek z
przebytą chorobą infekcyjną.

OBJAWY
W moczu pojawia się glukoza (
glukozuria
) i ciała
ketonowe
Senność i zmęczenie
Rozmyte widzenie
Silne pragnienie (
polidypsja
), silny głód
Częste oddawanie moczu (
poliuria
, inaczej częstomocz)
Utrata wagi
Nudności
Oddech może nabrać zapachu
acetonu

PRZYCZYNY
W 90% przypadków - reakcja autoimmunologiczna skierowana
przeciwko komórkom ß wysp trzustki.
Ryzyko zachorowania na cukrzycę związane jest z predyspozycją
genetyczną.

Epidemiologia
cukrzyca typu 1 pojawia się najczęściej we wczesnym
dzieciństwie lub w okresie pokwitania,
może ujawnić się także w wieku produkcyjnym oraz podeszłym, w
którym częściej występuje jako utajona cukrzyca
autoimmunologiczna dorosłych (latent autoimmune diabetes of
the adult
– LADA).
Ocenia się, że u około 40% wszystkich pacjentów chorych na
cukrzycę typu 1 chorobę zdiagnozowano po 20 roku życia.

Cele leczenia cukrzycy
•
Zapobieganie ostrym powikłaniom –
brak hipoglikemii
•
Profilaktyka rozwoju przewlekłych powikłań cukrzycy
–
okołonormoglikemia, mała zmienność glikemii
•
Zapewnienie pacjentom jakości życia jak najbardziej zbliżonej
do sposobu życia osób zdrowych –
insulinoterapia dostosowana
do trybu życia

Leczenie cukrzycy opiera się na:
1
. Indywidualnie dostosowanej dla każdego
pacjenta insulinoterapii.
2. Prawidłowo zaplanowanych pod względem
jakości oraz ilości posiłkach z uwzględnieniem
wszystkich składowych
(białek, tłuszczów,węglowodanów, błonnika, soli
mineralnyvh, mikroelementów i witamin).
3. Kontrolowanym wysiłku fizycznym.

Leczenie chorych na cukrzycę typu 1 polega na
uzupełnieniu lub zastąpieniu insuliny i
uzyskaniu prawidłowego metabolizmu węglowodanów, białek oraz
tłuszczów oraz zapobieganiu powikłaniom ostrym – hipoglikemii,
hiperglikemii oraz późnym – mikro- i makroangiopatii.
powinno być tak prowadzone, aby choroba w jak najmniejszym
stopniu pogarszała jakość życia osoby z cukrzycą.
według aktualnych wytycznych wartość HbA1C powinna być ≤
6,5,0%. U niektórych pacjentów (osoby w podeszłym wieku)
dopuszcza się wartość HbA1C ≤ 7,0%.
glikemia na czczo i przed posiłkami (dotyczy również samokontroli)
powinna mieścić się w przedziale 70–110 mg/dl (3,9–6,1 mmol/l) a
2 godziny po posiłku — podczas samokontroli: < 140 mg/dl (7,8
mmol/l);

Rodzaje insulin
insulina zwierzęca pochodzi od zwierząt,
natomiast insulina ludzka jest uzyskiwana laboratoryjnie
analogi insuliny
to zmodyfikowane metodą inżynierii genetycznej
preparaty insuliny ludzkiej o działaniu wolnym lub szybkim:
Każdy z tych rodzajów insuliny można również podzielić na szybkość
działania:
insulina o szybkim działaniu
insulina o krótkim działaniu
insulina o średnim działaniu
insulina o długim działaniu

Insulina ludzka
Obecnie insulinę produkuje się głównie metodą rekombinacji
DNA o budowie identycznej z białkiem ludzkim.
Na rynku polskim dostępne są zarówno krótkodziałające
(Gensulin R, Actrapid, Humulin R, Polhumin R), o pośrednim
czasie działania (Gensulin N, Insulatard, Humulin N,
Polhumin N) jak i gotowe mieszanki insulin ludzkich.

Analogi insuliny
Jest to zmodyfikowana metodami inżynierii
genetycznej insulina (najczęściej o nieznacznie
zmienionym składzie aminokwasowym).
Posiadają one w porównaniu do insuliny ludzkiej
zmieniony profil wchłaniania i czas działania
.

Analogi insuliny
Analogi szybkodziałające (Humalog,
NovoRapid, Apidra)
różnią się od ludzkich insulin
krótkodziałających szybszym początkiem działania
i wcześniejszym uzyskaniem maksymalnej
aktywności, za to mają krótszy okres działania.
Działanie to zmniejsza ryzyko wystąpienia
hipoglikemii
poposiłkowej, wymaga jednak
podawania insuliny do każdego posiłku (również
przekąsek).

Analogi insuliny
Analogi długodziałające (Levemir, Lantus)
Są preparatami, które charakteryzują się stabilnym,
dłuższym i bezszczytowym profilem działania w
porównaniu do ludzkich insulin o przedłużonym
działaniu. Ten efekt potencjalnie zmniejsza ryzyko
niedocukrzenia szczególnie w godzinach nocnych i
poprawia komfort życia.

Mieszanki insulinowe.
Są to gotowe fabrycznie przygotowane mieszanki insulin o
krótkim i pośrednim czasie działania (mieszanki ludzkie) lub
analogu szybkodziałającego (mieszanki analogowe).
Leczenie mieszankami insulinowymi zarezerwowane jest
praktycznie dla osób z cukrzycą typu 2, które wymagają
leczenia insuliną.
Nie powinny być stosowane poza nielicznymi wyjątkami w
cukrzycy typu 1, dla których najbardziej odpowiednim
modelem jest intensywna insulinoterapia za pomocą insuliny
długo i krótkodziałającej.

Mieszanki insulinowe.
Nazwa mieszanek insulinowych jest często
skonstruowana tak, że liczba np: 30-40-50 lub M3-M5
mówi o procencie któtkodziałającej fazy insuliny w
mieszance.
Przykład: Mixtard 30, Gensulin M30, Polhumin Mix 30,
Humulin M3 świadczy o 30 % zawartości insuliny o
szybkim (okołoposiłkowym) profilu działania natomiast
70% insuliny o pośrednim czasie działania

Stosując kryterium podziału - czas działania danego
preparatu insuliny stosowane w Polsce można
podzielić na:
insuliny
krótkodziałające
analogi szybkodziałające
insuliny o pośrednim czasie działania
insuliny
długodziałające
analogi bezszczytowe
Wyodrębniono również grupę mieszanek insulinowych i
analogowych cechujących się dwoma szczytami działania
związanymi z udziałem insuliny szybko lub krótkodziałającej
oraz składowej o działaniu przedłużonym.

Preparaty insulin dostępne w Polsce
oraz ich uproszczony profil działania
Insuliny krótkodziałające
Początek działania: 30 min
Maksymalne działanie: 1-3 godz
Czas działania: 6-8 godz
Preparaty: Actrapid, Humulin R, Gensulin R,
Polhumin R

Preparaty insulin dostępne w Polsce
oraz ich uproszczony profil działania
Szybkodziałające analogi
Początek działania: 5-15 min
Maksymalne działanie: 30-90 min
Czas działania: 4-6 godz
Preparaty: NovoRapid, Humalog, Apidra

Preparaty insulin dostępne w Polsce
oraz ich uproszczony profil działania
Insuliny o pośrednim czasie działania
Początek działania: 1,5 godz
Maksymalne działanie: 3-10 godz
Czas działania: 10-16 godz
Preparaty: Insulatard, Humulin N, Gensulin N,
Polhumin N, Monotard HM, Insuman Basal

Preparaty insulin dostępne w Polsce
oraz ich uproszczony profil działania
Insuliny długodziałające
Początek działania: 4 -5 godz.
Maksymalne działanie: 10 - 12 godz.
Czas działania: 16 - 24 godz.
Preparaty: Humulin, Ultratard HM

Preparaty insulin dostępne w Polsce
oraz ich uproszczony profil działania
Analogi długodziałające, bezszczytowe
Początek działania: 2 godz. do pełnego działania
Maksymalne działanie: 8 godz
Czas działania: 16-20-24 godz
Preparaty: Levemir, Lantus

Preparaty insulin dostępne w Polsce
oraz ich uproszczony profil działania
Mieszanki insuliny
krótkodziałającej i o
przedłużonym działaniu 30/70
Początek działania: 30-45 min
Maksymalne działanie: 2-3/4-8 godz., I- szczyt dla
fazy
któtkodziałającej, II- dla długodziałającej
Czas działania: 10-16 godz
Preparaty: Mixtard 30, Gensulin M30, Humulin
M3, Polhumin Mix3

Preparaty insulin dostępne w Polsce
oraz ich uproszczony profil działania
Mieszanki analogowe
Początek działania: 15 min
Maksymalne działanie: 1-2/4-8 godz., I- szczyt dla
fazy
któtkodziałającej, II- dla długodziałającej
Czas działania: 10-16 godz
Preparaty: NovoMix 30 (30/70), NovoMix50
(50/50), Humalog Mix 25 (25/75), Humalog Mix 50
(50/50)

Insulina bazalna
Insulina bazalna
powinna być podawana codziennie o tej samej porze.
Zbyt wczesna pora iniekcji może spowodować, że zacznie się zmniejszać
aktywność insuliny w godzinach porannych.
Optymalne pory podawania insulin:
– insuliny o pośrednim czasie działania i Levemir: godz. 22.00–23.00
(preferowana pora bliżej godz. 23.00) , Lantus: godz. 19.00–20.00
Insuliny bazalne
należy wstrzykiwać w tkankę podskórną ud
(przednia
i
boczna powierzchnia, nie wewnętrzna)
lub
pośladków
(górny zewnętrzny
kwadrant). Z
tych okolic insulina wchłania się wolno (najwolniej z tkanki
podskórnej ud), co zapewnia jej optymalne działanie w nocy i rano. Podanie
insuliny bazalnej w
tkankę podskórną brzucha lub przedramion skraca czas jej
działania.

Insulina przedposiłkowa
Insulinę przedposiłkową należy wstrzykiwać
w
tkankę podskórną
brzucha lub ud
. Z
tych miejsc jej wchłanianie jest najszybsze.
Insuliny ludzkie należy podawać
30 min przed głównymi posiłkami
,
analogi szybko działające tuż przed posiłkiem.
Jeżeli stosuje się insuliny krótko działające, należy spożywać 3
główne posiłki i 3 przekąski, w przypadku analogów szybko
działających – wykonuje się iniekcje przed każdym posiłkiem, również
niedużym.
Insulinę należy wstrzykiwać do tkanki podskórnej. Insulina jest
produkowana w
formie wkładów do penów insulinowych

Insulina a liczba posiłków
Iniekcje mieszanek insulinowych ludzkich należy
wykonywać
pół godziny przed śniadaniem lub
kolacją
, a
analogowych tuż przed śniadaniem lub
kolacją.
Jeżeli stosuje się mieszanki insulin ludzkich, należy
spożywać 3 główne posiłki i 3 przekąski,
w
przypadku mieszanek analogowych należy
spożywać 3 posiłki.

SPOSOBY LECZENIA
Leczenie substytucyjne
insuliną,
podawaną do organizmu z
zewnątrz.
Insulinę podaje się podskórnie, za pomocą:
strzykawek,
penów
(piór) insulinowych
lub
pompy insulinowej
.
Przy
pompie insulinowej
stosuje się jedynie insulinę
krótkodziałającą.
Większość preparatów insuliny wytwarza się w
organizmach
modyfikowanych genetycznie
–
drożdżach
i bakteriach
Escherichia coli
.

Przyczyną wysokiego poziomu glukozy po posiłku
mogą być:
1.
Krótka przerwa pomiędzy podaniem insuliny a posiłkiem (po
podaniu insuliny Regular lub Actrapid odstęp pomiędzy
podaniem insuliny a posiłkiem powinien wynosić około 30-45
min)
2.
Nieprawidłowo wyliczona dawka insuliny na ilość
węglowodanów w posiłku (ocena na OKO)
3.
Zaczynająca się choroba ( kwasica, infekcja, odwodnienie)
4.
Podanie insuliny przemrożonej ( insuliny zamarzniętej nie
należy używać)
5.
Obecność w posiłku dużej ilości tłuszczu ( tłuszcz opóźnia
działanie insuliny i opróżnianie żołądka)
6.
Duża ilość węglowodanów o wysokim indeksie glikemicznym

Skutki uboczne, interakcje i przeciwwskazania
działania insulin
Najważniejszym i najczęstszym skutkiem ubocznym działania
insuliny jest hipoglikemia. Sporadycznie mogą wystąpić reakcje
alergiczne w
miejscach nakłuć lub – przy niewystarczającej rotacji
miejsca iniekcji
– lipodystrofia (zanik tkanki tłuszczowej)
Nie wolno stosować insuliny w przypadku alergii na insulinę lub przy
istniejącej hipoglikemii
.

Cukrzyca typu 2

Epidemiologia i etiologia
Cukrzyca typu 2 dotyczy około 90% wszystkich osób z cukrzycą.
Przyczyna: zaburzony metabolizm węglowodanów oraz oporność na
insulinę a także zaburzone jej wydzielanie z trzustki.
We wczesnej fazie produkcja insuliny zazwyczaj jest prawidłowa,
natomiast w
późniejszych stadiach trzustka wydziela
niewystarczającą jej ilość, a po kilku lub kilkunastu latach trwania
choroby, produkcja i wydzielanie insuliny z
trzustki całkowicie ustaje.
Rozwój cukrzycy typu 2 jest, z jednej strony, uwarunkowany
genetycznie, z
drugiej strony, dużą rolę w jej ujawnieniu odgrywają
czynniki środowiskowe oraz inne czynniki ryzyka.
Czynniki te często występują w postaci zespołu
metabolicznego.

Czynniki zwiększonego ryzyka rozwoju cukrzycy
Nadwaga lub otyłość (BMI ≥25 kg/m
2
).
Cukrzyca w rodzinie.
Mała aktywność fizyczna.
Etniczna lub środowiskowa grupa narażenia.
Przebyta cukrzyca ciążowa lub urodzenie dziecka o
masie >4 kg.
Uprzednio stwierdzone IFG lub IGT.
Nadciśnienie.
Hiperlipidemia (TG, HDL).
Choroba układu sercowo-naczyniowego.
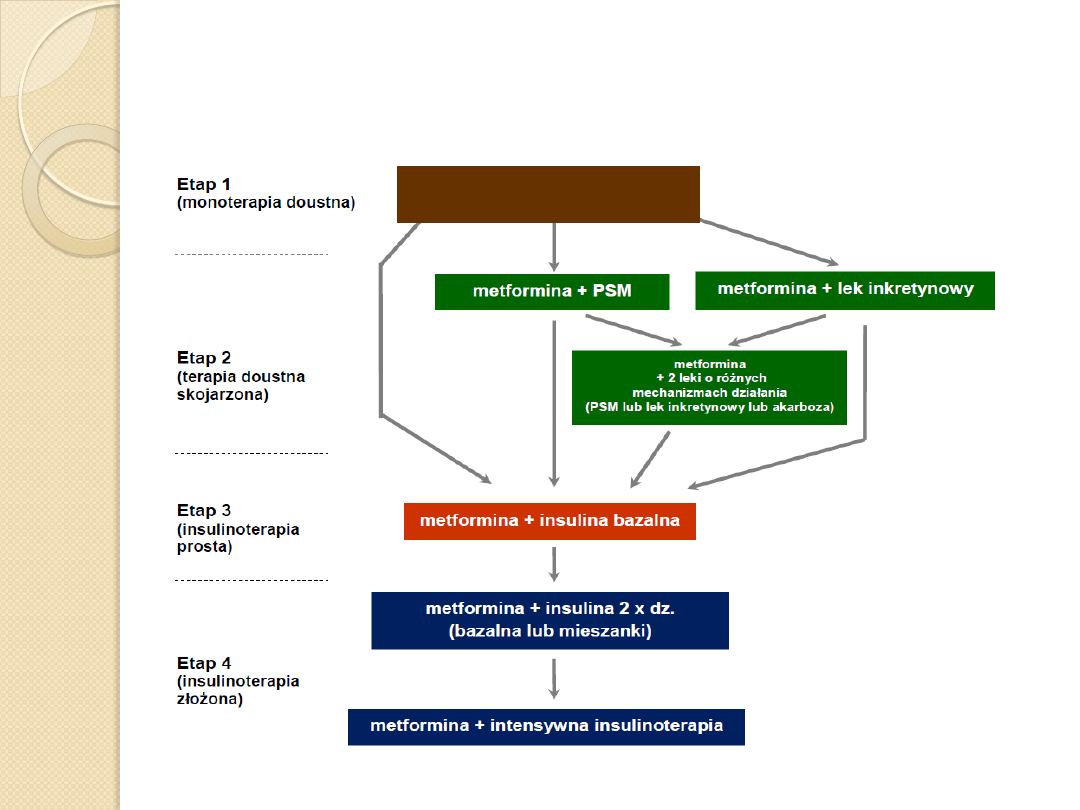
metformina (PSM,
gliptyna)
Algorytm postępowania w cukrzycy typu 2
– zalecenia PTD 2013
Zalecenia kliniczne dotyczące postępowania u chorych na cukrzycę 2013

Klasyczne objawy cukrzycy t2
występują rzadko.
Zwiększone wartości glukozy we krwi często są wykrywane
przypadkowo, np. podczas
badań kontrolnych, akcji medialnych
(diabetobusy),
badań zdrowotnych lub też przy pojawieniu się
powikłań naczyniowych (zawał, wylew).
Jeśli okazjonalnie wartości glukozy we krwi przekraczają 200 mg/dl
(ponad 11,1 mmol/l), i dodatkowo
występują objawy cukrzycy
wówczas rozpoznanie jest jednoznaczne.
U
osób z cukrzycą typu 2 często zwiększone wartości glukozy we krwi
obserwowane
są na czczo lub po dużym posiłku.
Stwierdzenie na czczo
wartości glukozy w przedziale 100–125
mg/dl jest wskazaniem do przeprowadzenia doustnego testu
tolerancji glukozy (OGTT).

Leczenie cukrzycy typu 2
Leczenie hiperglikemii powinno
uwzględniać dwa podstawowe
patomechanizmy stanowiące podłoże
cukrzycy typu 2:
insulinooporność
Zaburzenia wydzielania insuliny.

Leczenie cukrzycy typu 2
Monoterapia -leki doustne
Terapia wielolekowa
Terapia skojarzona
Insulinoterapia

Podsumowanie
Cukrzycę można rozpoznać łatwo i bez wielkiego
nakładu pracy i pieniędzy
Leczenie cukrzycy musi być leczeniem
wieloczynnikowym, należy dążyć do wyrównania
glikemii, ale także dyslipidemii i ciśnienia tętniczego
Dobre leczenie cukrzycy teraz przyniesie choremu
korzyść w przyszłości

Leczenie cukrzycy - „stare leki”
Inhibitory α-glukozydazy
Metformina
Pochodne sulfonylomocznika
Glinidy

Inhibitory glukozydazy - Akarboza-Glucobay®
Akarboza hamuje enzym α-glukozydazę w błonie jelita cienkiego.
opóźnia się wchłanianie węglowodanów, dzięki czemu można
zredukować wzrost poziomu glukozy poposiłkowej we krwi.
Efekt terapeutyczny leków jest widoczny najczęściej po kilku tygodniach
leczenia, kiedy to stężenie glukozy we krwi może się nieznacznie
obniżyć.
Skuteczność inhibitorów α-glukozydazy w porównaniu do metforminy,
czy insulinotropowych leków przeciwcukrzycowych jest niewielka.
Leki te nie wpływają na wydzielanie insuliny z trzustki, a tym samym nie
prowadzą do hipoglikemii.
Nie mają one wpływu na zwiększenie masy ciała.
Akarbozę można łączyć z innymi lekami przeciwcukrzycowymi.

Inhibitory α-glukozydazy
Terapię z zastosowaniem inhibitorów α-glukozydazy
należy rozpoczynać stopniowo, dzięki czemu można
uniknąć nieprzyjemnych skutków ubocznych.
Inhibitory α-glukozydazy przyjmuje się wraz
z
pierwszym kęsem posiłku.

Pochodne biguanidów - metformina
Metformina
to jeden z najczęściej stosowanych doustnych leków
hipoglikemizujących.
Zmniejsza produkcję glukozy w wątrobie (proces glukoneogenezy),
zwiększa jej obwodowe zużycie przez komórki tłuszczowe,
mięśniowe i komórki tkanki łącznej oraz zmniejsza wchłanianie
glukozy z przewodu pokarmowego.
Poza tym poprawia wykorzystanie glukozy w tkankach obwodowych.
zmniejszenie wchłaniania jelitowego glukozy, zmniejszenie uczucia
głodu, spadek wagi ciała, korzystnie wpływa na lipidy poprzez
nasilenie lipolizy i hamowanie lipogenezy, co powoduje obniżenie
stężenia TG, VLDL, LDL-cholesterolu i wzrost HDL-cholesterolu,
wykazuje korzystny efekt przeciwkrzepliwy
.

Metformina
jest lekiem pierwszego rzutu
w leczeniu cukrzycy t.2.
Metforminę można łączyć z innymi lekami przeciwcukrzycowymi oraz
z
insuliną.
Obniża podstawowe stężenie glukozy we krwi oraz glikemię po
posiłkową. Metformina obniża również wartość HbA1C o ok. 1–2%.
Terapia Metforminą obniża ryzyko makroangiopatii i mikroangiopatii,
a
także korzystnie wpływa na inne parametry zespołu metabolicznego.
Lek przynosi także dobre efekty w terapii zespołu policystycznych jajników
(insulinooporność).
Przeciwwskazaniem do stosowania metforminy jest niewydolność nerek.
Terapia Metforminą nie ma wpływu na wystąpienie hipoglikemii.
Metformina dopuszczona jest także do stosowania u dzieci i młodzieży
od 10 roku życia
.

Dawkowanie metforminy
Metforminę przyjmuje się podczas
posiłków lub po posiłkach

Działania niepożądane i interakcje
Stopniowe zwiększanie dawki znacznie zredukowało ryzyko kwasicy
mleczajowej, oraz objawów ze strony przewodu pokarmowego jak:
utrata apetytu, smaku, nudności, wymioty, biegunka, ponieważ objawy
ze strony przewodu pokarmowego u osób stosujących małe dawki są
mniej nasilone i zwykle przejściowe.
Istotne interakcje Metforminy występują z alkoholem i środkami
kontrastowymi zawierającymi jod. Leki kontrastowe stosowane
w
radiologii po podaniu dożylnym mogą spowodować niewydolność
nerek. Również stosowanie blokeru H2 cymetydyny u osób
stosujących pochodne biguanidu zwiększa ryzyko wystąpienia kwasicy
mleczajowej
.

Działania niepożądane i interakcje
Ryzyko kwasicy mleczanowej może zwiększyć się podczas operacji,
dlatego przed planowanymi zabiegami operacyjnymi. Zaleca się
odstawienie Metforminy na 48 godz. przed zabiegiem i 48 godzin po
zabiegu, w sytuacjach wyjątkowych minimum 24 godz. Fakt leczenia
Metforminą należy zgłosić lekarzowi.
Przyjmowanie Metforminy w połączeniu z większą ilością alkoholu (
powyżej kieliszka wina, małego piwa, małego drinka) zwiększa ryzyko
wystąpienia kwasicy mleczanowej oraz hipoglikemii.
Zaleca się aby pacjenci leczeni Metforminą w miarę możliwości
unikali spożywania alkoholu. Dotyczy to także leków zawierających
alkohol, które są przyjmowane w większych ilościach.

Pochodne sulfonylomocznika (PSM)
Mechanizm działania polega na pobudzeniu produkcji i wydzielania insuliny
przez komórki β trzustki poprzez wpływ na receptor błonowy, obniżeniu
stężenia glukagonu we krwi.
Leki tej grupy zwiększają wrażliwość komórki β na bodziec glikemiczny,
dodatkowy mechanizm to nasilenie insulinowrażliwości przez zwiększenie
liczby receptorów insulinowych w tkankach obwodowych i wątrobie.
Poza tym pochodne sulfonylomocznika wykazują działanie pozatrzustkowe:
nasilają transport węglowodanów do tkanki tłuszczowej i mięśni.
Są skuteczne tylko wówczas, kiedy trzustka jest jeszcze w stanie
przynajmniej częściowo wytwarzać insulinę
.
Pochodne sulfonylomocznika mogą indukować hipoglikemię, pobudzać apetyt,
a w
ten sposób prowadzić do zwiększenia masy ciała.

Wskazania
◦
Leków tych nie zaleca się jako leków pierwszego rzutu, za
wyjątkiem osób u których przeciwwskazane jest
przyjmowanie metforminy
◦
Cukrzyca typu 2 w monoterapii szczególnie u osób z
prawidłową masą ciała i niewielką nadwagą, gdy leczenie
niefarmakologiczne jest nieskuteczne
◦
cukrzyca typu 2 w terapii skojarzonej z pochodnymi
biguanidów, insuliną, GLP i DPP4.

Terapia pochodnymi sulfonylomocznika
Terapia pochodnymi PSM powinna być tak prowadzona aby
ryzyko wystąpienia hipoglikemii było jak najmniejsze.
Rozpoczyna się od najmniejszej skutecznej dawki, którą
stopniowo kontrolując poziomy glukozy we krwi można
zwiększać.
Dawka podtrzymująca ustalana jest indywidualnie w oparciu o
pomiary glukozy we krwi.
Pochodne sulfonylomocznika przyjmuje się zazwyczaj 1- 2 x
dziennie
bezpośrednio przed śniadaniem (ewentualnie do
śniadania) oraz przed kolacją.
W
przypadku wyższych dawek można stosować podział na dawkę
poranną i wieczorną.

Działania niepożądane
Najczęstszym działaniem ubocznym jest
hipoglikemia,
którą
można zredukować, stosując stopniowe dawkowanie.
Wydzielanie insuliny może prowadzić do wzrostu apetytu,
a
tym samym do zwiększenia masy ciała.
Sporadycznie może wystąpić nadwrażliwość skóry i odczyny
alergiczne (wysypki, świąd skóry, rumień guzowaty,
fotodermatoza).
Dolegliwości żołądkowo-jelitowe, występują przede
wszystkim na początku terapii i zazwyczaj mają charakter
przejściowy.
Po wielu latach występuje wtórna niewrażliwość na lek.

Interakcje i przeciwwskazania
Pochodne SM wykazują interakcję z wieloma lekami, które nasilają lub
osłabiają ich działanie między innymi alkohol etylowy nasila działanie PSM i
może wywołać hipoglikemię. Wywołują zaburzenia hematologiczne,
wątrobowe, zapalenie naczyń (rzadko występują).
Pochodnych sulfonylomocznika
nie wolno
stosować u osób u których
produkcja insuliny w
trzustce wygasła (np. cukrzyca typu 1) w śpiączce
ketonowej, oraz stanie
przedśpiączkowym, a także u osób z ciężkimi
zaburzeniami funkcji nerek i wątroby, w ciąży i okresie karmienia,
nadwrażliwości na lek, w okresie ciężkich stresów, ostrych chorób
towarzyszących, w okresie przed i po operacji w zatruciach.
We wczesnej niewydolności nerek można stosować glikwidon eliminowany
głównie przez przewód pokarmowy
Leki te nie są dopuszczone do stosowania u dzieci

Glinidy-nateglinid i repaglinid
Zwiększają poposiłkowe wydzielanie insuliny
(podanie leku wyzwala wyrzut insuliny).
Obniżają glikemię poposiłkową, mogą być
stosowane w cukrzycy typu 2 we wczesnym
etapie leczenia oraz w terapii skojarzonej,
szczególnie gdy dominuje hiperglikemia
poposiłkowa.
Są szybko wchłaniane i eliminowane z przewodu
pokarmowego.

Glinidy -nateglinid i repaglinid
Glinidy
przyjmuje się do głównych posiłków
.
Lek może być aplikowany
od 30 minut przed
posiłkiem do czasu bezpośrednio przed posiłkiem.
Jeśli pacjent opuści posiłek, powinien także
zrezygnować z przyjęcia glinidu.
Glinidy nie są dopuszczone do stosowania u dzieci.

Działania niepożądane, interakcje i przeciwwskazania
Przeciwwskazania takie jak dla pochodnych sulfonylomocznika
Działania niepożądane: nietolerancja ze strony przewodu pokarmowego -
bóle brzucha, biegunki, zaparcia, wzrost transaminaz wątrobowych,
hipoglikemie ( ze względu na krótszy okres półtrwania rzadziej niż przy
stosowaniu PSM) , przyrost masy ciała.
Przeciwwskazane przyjmowanie repaglinidu w
połączeniu z gemfibrozylem,
może nasilić działanie obniżające glukozę we krwi.
Interakcja zachodzi przypuszczalnie przez hamowanie CYP2C8. Ponieważ
nateglinid metabolizowany jest przez inny izoenzym, ta interakcja jego nie
dotyczy.
Przy leczeniu repaglinidem
należy unikać stosowania fibratów (betafibratu lub
fenofibratu
)

Leczenie cukrzycy typu 2,
Terapia wielolekowa
W razie braku dobrego wyrównania glikemii
za pomocą metforminy lub pochodnej
sulfonylomocznika można dołączyć drugi lek
z innej grupy:
MTF + SM
MTF + inhibitor
α-glukozydazy
SM + MTF
SM + inhibitor
α-glukozydazy
MTF + SM + inhibitor
α-glukozydazy


Efekt inkretynowy
Jest to większa sekrecja insuliny po
doustnym podaniu glukozy w
porównaniu z wydzielaniem insuliny
po podaniu glukozy dożylnym
.

Hormony inkretynowe
Glukagonopodobny peptyd 1
–GLP –1
Zależny od glukozy polipeptyd
insulinotropowy -GIP

GLP-1, inkretyna, hormon peptydowy
wydzielany przez komórki przewodu
pokarmowego
efekty działania:
• zwiększenie wydzielania insuliny zależne od glikemii-
poprawa pierwszej fazy wydzielania
• zahamowanie wydzielania glukagonu
• zmniejszenie łaknienia
• stymulacja wzrostu i neogenezy komórek β
• zmniejszenie apoptozy komórek
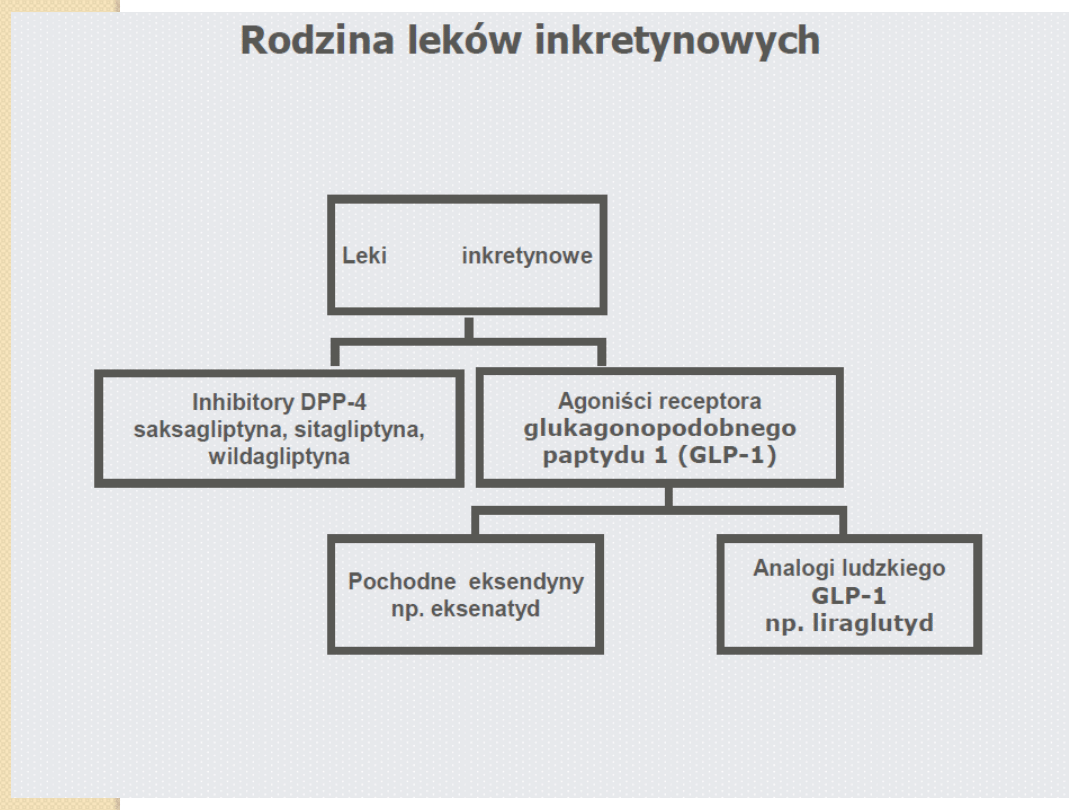

Inkretynomimetyki
Leki będące
substytutami GLP-1
,
analogi GLP-1
Leki
zwiększające działanie
naturalnego GLP-1
, inhibitory DPP-IV

Leki stosowane w terapii cukrzycy
Gliptyny
i preparaty złożone zawierające gliptyny
czyli
inhibitory dipeptydylo-peptydazy ( DPP-4)
Leki doustne, których działanie polega na hamowaniu aktywności
enzymu rozkładającego GLP-1, jednego z podstawowych
hormonów inkretynowych.
Efektem ich działania jest zwiększenie stężenia GLP-1 oraz
wydłużenia czasu jego działania.
Zaletą jest małe ryzyko hipoglikemii oraz neutralny wpływ na
masę ciała.

Preparaty na rynku
(dostępne w Polsce).
•
Sitagliptyna (Januwia),
•
Wildagliptyna (Galvus)
•
Saksagliptyna (Onglyza)
•
Linagliptyna ( Trajenta)
•
Alogliptyna ( Nesina)
•
Badania kliniczne nad:
Dutogliptyną i Gemigliptyną
•
Leki te należy przyjmować z meforminą, lub
pochodnymi sulfonylomocznika

11-11-18
Zwiększają one zależne od glukozy
wydzielanie insuliny a hamują wydzielanie
glukogonu.
Zaletą ich jest możliwość stosowania
doustnego a wadą w Polsce cena.

Działania niepożądane
Częstymi skutkami ubocznymi są dolegliwości żołądkowo-jelitowe, które
często ustępują po kilku dniach. Przy utrzymujących się ciężkich
dolegliwościach pacjenci powinni natychmiast skontaktować się z lekarzem
ponieważ istnieje podejrzenie
zapalenia trzustki
.
Mimetyków inkretynowych nie wolno stosować u pacjentów z cukrzycą
typu 1 oraz w każdej innej postaci w której nie stwierdza się wydzielania
insuliny przez trzustkę
Ograniczenia stosowania GLP-
1 dotyczą pacjentów z zaawansowaną
niewydolnością nerek i wątroby oraz u pacjentów z przewlekłymi
chorobami jelit oraz u osób z potwierdzoną gastroparezą.
Eksenatydu i liraglutydu
nie należy stosować przy jednoczesnej terapii
insulinowej oraz u dzieci i
młodzieży poniżej 18 roku życia
.

Podsumowanie
Analogi GLP-1 i inhibitory DPP-IV
:
normalizują lub zmniejszają uszkodzenie efektu
inkretynowego stwierdzanego w cukrzycy typu 2
spowalniają naturalną historię cukrzycy typu 2
są skutecznymi lekami p/ cukrzycowymi
są bezpieczne -minimalne ryzyko hipoglikemii
nie powodują przyrosty masy ciała
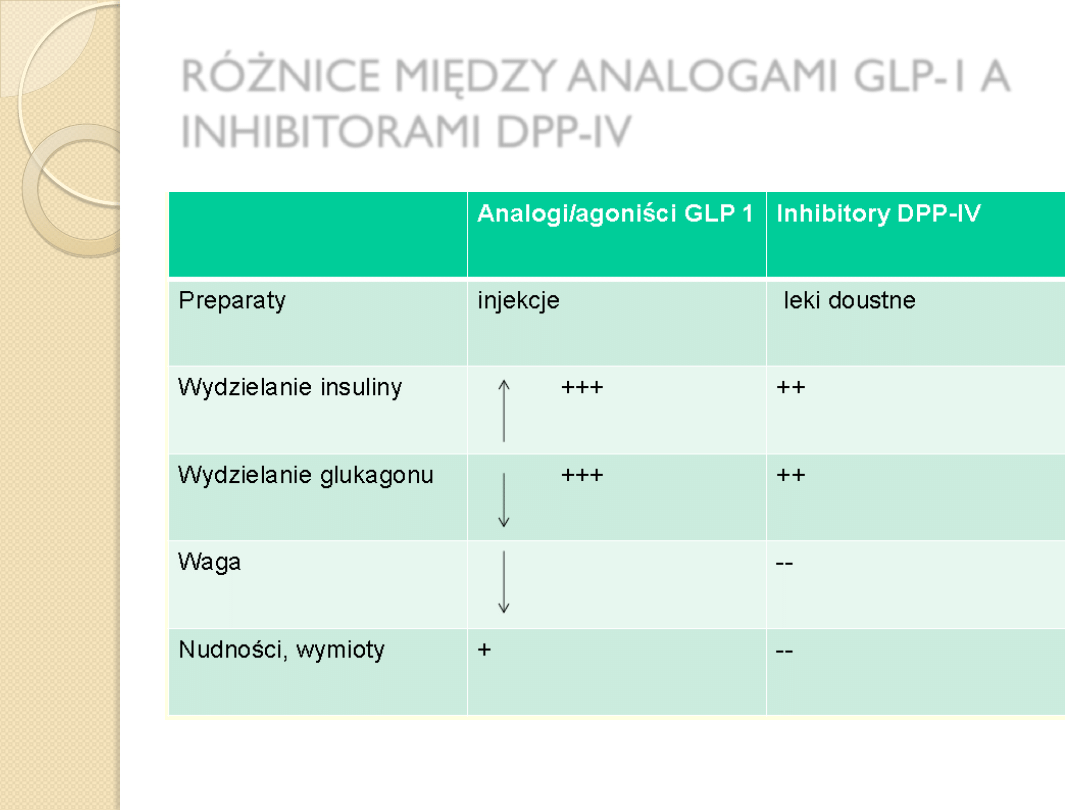
RÓŻNICE MIĘDZY ANALOGAMI GLP-1 A
INHIBITORAMI DPP-IV

Zaletą terapii mimetykami inkretynowymymi w przeciwieństwie do
insuliny jest ich stałe dawkowanie, co znacznie ułatwia
leczenie.
Mimetyki inkretynowe obniżają wartość HbA1c o ok. 0,5–1%, przy
czym liraglutyd, według pierwszych wyników badań, wydaje się
być nieco efektywniejszy niż eksenatyd.
Znaczenie mimetyków inkretynowych w leczeniu cukrzycy będzie
można ocenić dopiero wtedy, kiedy dostępne będą wyniki badań
długoterminowych.

Ze względu na fakt opóźniania opróżniania żołądka, możliwe są
interakcje ze wszystkimi lekami wykazującymi niewielkie spektrum
terapeutyczne lub w
przypadku których konieczny jest ścisły nadzór
kliniczny.
Klinicznie opisano interakcję z kumarynami (doustnymi
antykoagulantami), dlatego u tych pacjentów na początku terapii
GLP-
1 oraz po zmianie dawki należy monitorować czas
protrombinowy.
Dawki antykoagulantów należy dopasowywać do wyników badań.
Odporne na działanie soku żołądkowego preparaty substancji
niestabilnych w
środowisku kwaśnym, jak np. inhibitory pompy
protonowej, należy przyjmować przynajmniej godzinę przed, lub
cztery godziny po podaniu eksenatydu

Leki zwiększające wydalanie glukozy
przez nerki
Gliflozyny
(selektywny bloker
aktywności enzymu kotransportera
sodowo-glukozowego).
- dapagliflozyna- ( Forxiga)
-
kanagliflozyna
- empagliflozyna

Leki zwiększające wydalanie glukozy
przez nerki
hamują kotransporter 2 glukozy zależny od jonów Na
SGLT-2 w cewkach nerkowych.
Transporter ten jest odpowiedzialny za około 90%
reabsorbcji glukozy z nerek do krwioobiegu. Leki te
zmniejszają stężenie glukozy we krwi niezależnie od
poziomu insuliny oraz nie powodują przyrostu masy ciała.
Obserwowane jest hamuje zwiększone ryzyko zakażeń
układu moczowego.

Rola witaminy D w profilaktyce cukrzycy
receptory dla Vit
D zostały zidentyfikowane w kom. ß oraz
komórkach immunologicznych .
Niedobór Vit D upośledza syntezę i sekrecję insuliny
predysponując do rozwoju cukrzycy t2.
Niedobór Vit D we wczesnym okresie życia predysponuje
do rozwoju cukrzycy t 1 i 2 przyspieszając zachorowanie na
te choroby.
Stwierdzono ,że zachorowanie na cukrzycę miało związek z
polimorfizmem genu dla receptora Vit D.
Badania na zwierzętach wykazały ( nieotyłych myszach), że
podanie myszą alfa 25-dihydroxy Vit D lub strukturalnego
analogu, opóźniało zachorowanie na cukrzycę poprzez
modulowanie reakcji immunologicznej.
Sugeruje się, że terapia Vit D powinna być jedną z wielu
metod profilaktyki cukrzycy t 1 i 2.

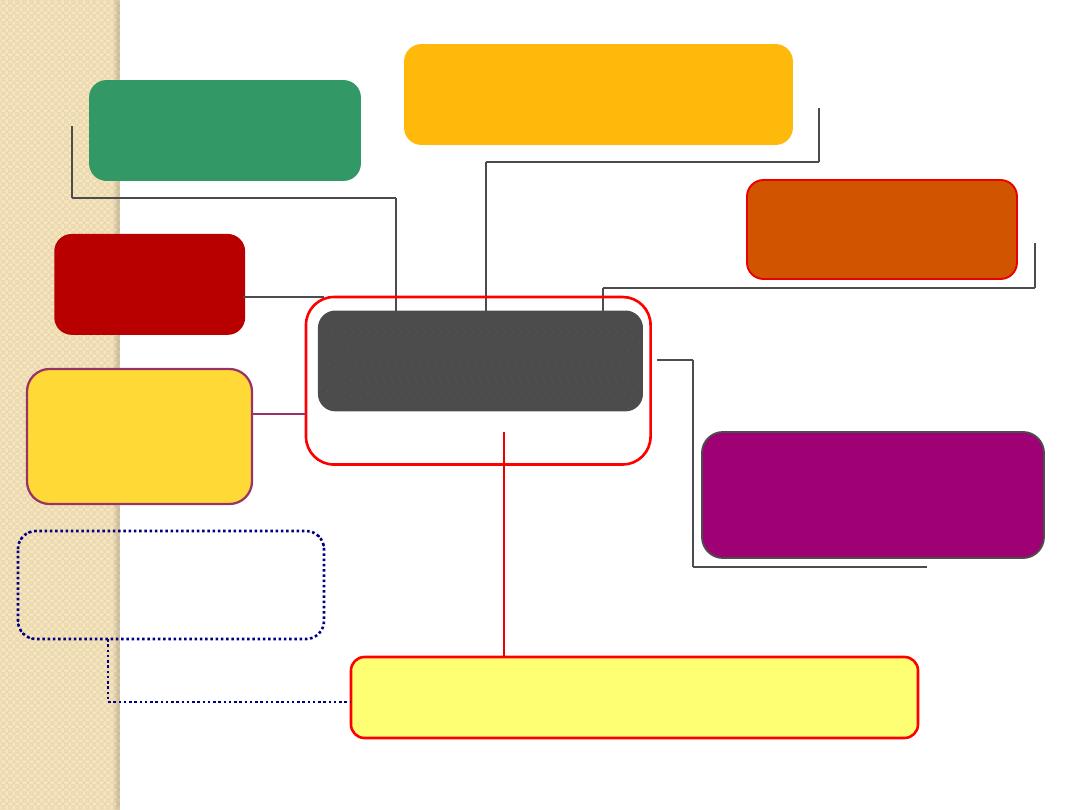
ZESPÓŁ
METABOLICZNY
OTYŁOŚĆ
ZABURZENIA
METABOLIZMU GLUKOZY
NADCIŚNIENIE
DYSLIPIDEMIA
ZABURZENIA
UKŁADU KRZEPNIĘCIA
I FIBRYNOLIZY
INSULINOOPORNOŚĆ
ZESPÓŁ
POLICYSTYCZNYCH
JAJNIKÓW
Zaburzenia
endokrynologiczne
Wyszukiwarka
Podobne podstrony:
Program zajęć ED, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, materialy Kamil, Szkoła, L
EDi4 2-lista 2004, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, materialy Kamil, Szkoła,
Wskaznik do rutki, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, materialy Kamil, płytkas
Zestawy Miernictwo2, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, materialy Kamil, płytka
2 regulacja napiecia modelu transformator zaczepy, aaa, studia 22.10.2014, Materiały od Piotra cukro
instalacja qqqqqqqqqq, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, materialy Kamil, pły
13 sieci zabespieczenia cyfrowe protokuł, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, m
projekt wieś, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, materialy Kamil, Szkoła, Uczel
wyklad12tt20, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, materialy Kamil, Szkoła, Elekt
cw 8 moje, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, materialy Kamil, płytkas V, Szkoł
wyklad07tt08, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, materialy Kamil, Szkoła, Elekt
zadania sieci elektroenergetycznych, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, materia
LABEN4, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, materialy Kamil, Szkoła, Energoelekt
Wyklad11tt16 19, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, materialy Kamil, Szkoła, El
2. Matlab, aaa, studia 22.10.2014, Materiały od Piotra cukrownika, metody numeryczne w technice, lab
więcej podobnych podstron