1. Wstęp
Celem ćwiczenia jest zapoznanie się z przemianami gazów i równaniem gazu doskonałego,
opanowanie umiejętności zastosowania pierwszej zasady termodynamiki do przemian gazowych oraz
poznanie metody wyznaczania wartości κ=c
p
/c
v
.
Ilość ciepła potrzebna do ogrzania ciała jest proporcjonalna do jego masy, przyrostu temperatury i
zależy od własności ciała, określonych jego ciepłem właściwym. Ciepło właściwe jest liczbowo równe ilości
ciepła potrzebnej do ogrzania jednostki masy ciała o jeden stopień. Dla gazów ciepło właściwe wyznaczone
przy zachowaniu stałego ciśnienia c
p
jest znacznie większe od ciepła właściwego wyznaczonego przy stałej
objętości c
v
. Stosunek κ=c
p
/c
v
jest wykładnikiem we wzorze Poissona pV
κ
=const opisującym przemianę
adiabatyczną i może on być wyznaczony poprzez wykorzystanie zmiany parametrów gazu zamkniętego w
naczyniu o ściankach źle przewodzącym ciepło i poddawanego określonym przemianom gazowym.
Jeżeli powietrze w naczyniu o temperaturze otoczenia T
1
i ciśnieniu p
1
nieznacznie większym
od atmosferycznego rozprężymy adiabatycznie do ciśnienia atmosferycznego b, jego temperatura
obniży się do wartości T
2
< T
1
. Po zamknięciu zbiornika temperatura gazu po kilku minutach powraca
do wartości T1 i jednocześnie ciśnienie gazu wzrasta do wartości p
2
< p
1
. Różnice ciśnień p
1
- b = p'
oraz p
2
- b = p'' określamy mierząc różnice wysokości słupów cieczy w otwartym manometrze
cieczowym (U-rurce). Są one odpowiednio równe h
1
i h
2
. Oznacza to że p' = ρgh
1
a p'' = ρgh
2
,
gdzie ρ - gęstość cieczy w U-rurce a g - przyśpieszenie ziemskie. Korzystając z praw opisujących
przemiany gazu otrzymujemy wzór:
κ=
p '
p '−p ' '
(1)
Zastępując p' oraz p" przez wyrażenia zawierające h
1
i h
2
nadajemy mu postać:
κ=
h
1
h
1
−
h
2
(2)
dzięki czemu aby obliczyć κ wystarczy wyznaczyć h
1
i h
2
.
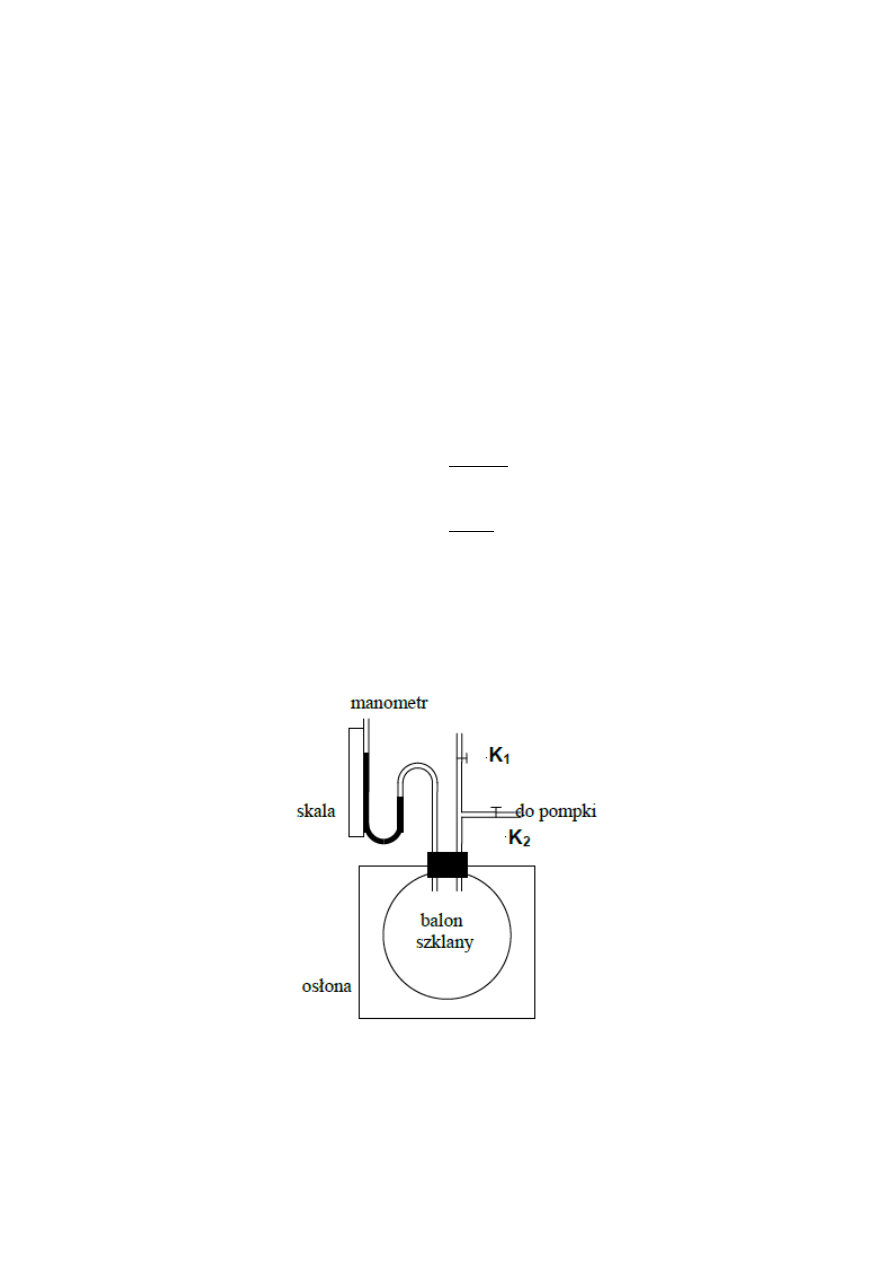
Zestaw pomiarowy składa się z obudowanego balonu szklanego zamkniętego korkiem
posiadającym dwa otwory (wyloty). Przez jeden z nich wyprowadzono rurkę z kranami K
1
i K
2
umożliwiającymi zwiększenie ciśnienia powietrza w balonie przy pomocy pompki przyłączonej do
wylotu kranu K
2
, a następnie jego rozprężenie adiabatyczne przez otwarcie kranu K
1
. Przez drugi
wylot balon połączony jest z manometrem cieczowym (rys. 1).
Rys. 1. Schemat układu do wyznaczania wartości κ
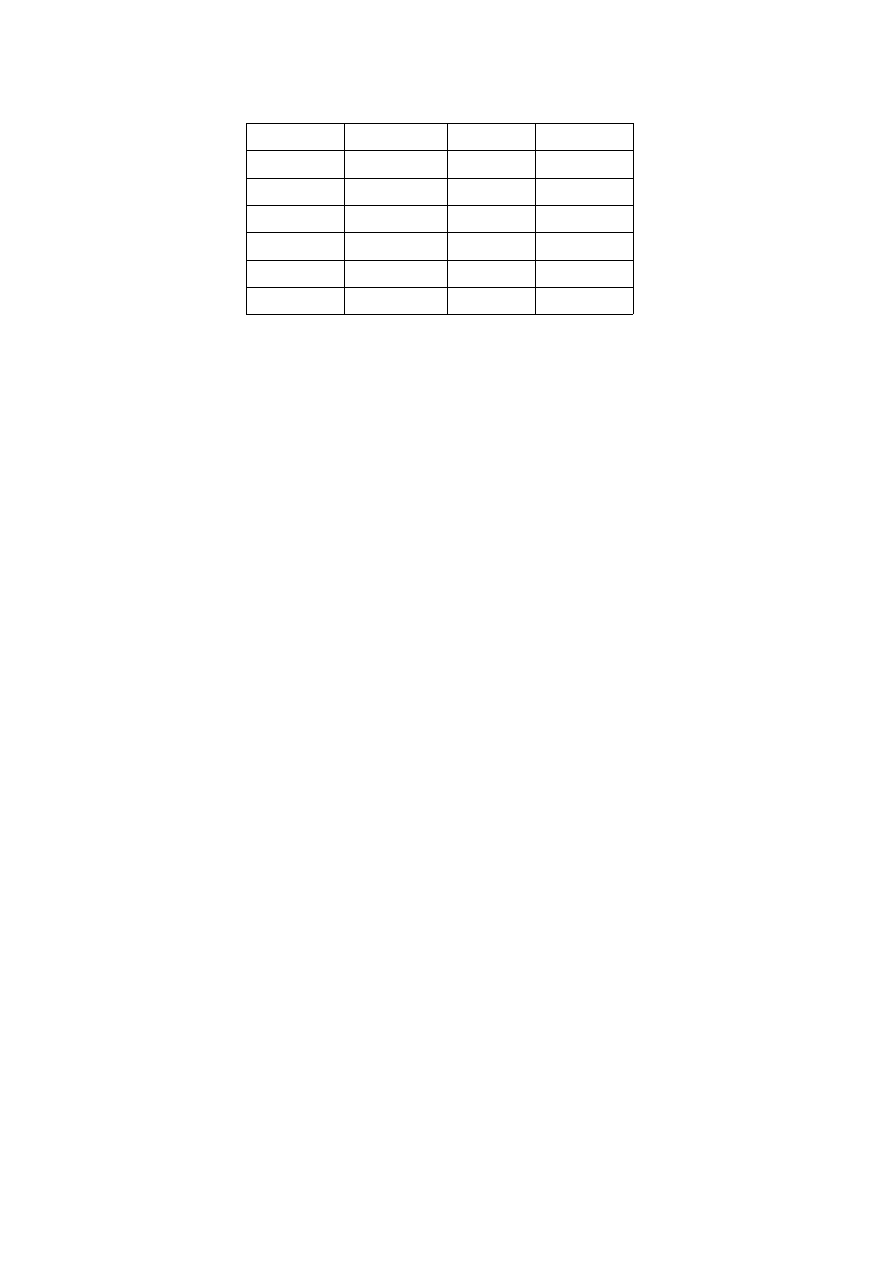
2. Wyniki pomiarów i obliczenia
Lp.
h
1
[cm]
h
2
[cm]
κ
1
2,1
0,7
1,5
2
5,0
0,6
1,14
3
3,3
1,2
1,57
4
4,5
1,5
1,5
5
4,7
1,6
1,52
6
5,3
1,5
1,39
Tabela 1. Wyniki pomiarów. κ została obliczona ze wzoru (2).
Z powyższej tabeli możemy obliczyć średnią:
¯
κ=
1,44
Zgodnie z rozkładem studenta dla α=0,95:
t
p
=2,57
Δκ
α
=0,15
Więc ostatecznie:
κ=1,44±0,15
3. Wnioski
Oczekiwana wartość κ=c
p
/c
v
1,4 mieści się w zakresie błędu otrzymanej wartości, co świadczy o
poprawności wykonania pomiarów.
4. Bibliografia
Praca zbiorowa pod red. Grzegorza Derfla, Instrukcje do ćwiczeń I Pracowni Fizycznej,
Instytut Fizyki PŁ, Łódź 1998
Wyszukiwarka
Podobne podstrony:
więcej podobnych podstron