Spis treści
I. Ilościowe określenia składu roztworów strona
Ułamek wagowy (masowy) 2
Procent wagowy (masowy) 2
Procent objętościowy 2
Ułamek molowy 3
Procent molowy 3
Stężenie molowe 3
Stężenie procentowe 3
Stężenie normalne 4
Stężenie molarne (molalność) 4
Przeliczanie wzajemne stężeń 5
Roztwory rozcieńczone 6
II. Obliczenia podczas sporządzania roztworów
Przygotowanie roztworów z czystych składników 7
Rozcieńczanie roztworów 7
Zwiększanie stężenia roztworu przez odparowanie
rozpuszczalnika 8
Zwiększanie stężenia roztworu przez dodanie składnika
stanowiącego substancję rozpuszczoną 9
Mieszanie roztworów o różnych stężeniach 9
Reakcje w roztworach 10
Rozpuszczanie hydratów 11
Wzory do ilościowego określenia składu roztworów i do obliczeń podczas sporządzania roztworów
I. Ilościowego określenia składu roztworów
Ułamek wagowy (masowy) wi składnika i jest to stosunek masy mi tego składnika do masy m całego roztworu. Określa on liczbę gramów składnika w jednym gramie roztworu.
![]()
gdzie:
wi - ułamek wagowy
mi - masa i-tego składnika
m - masa roztworu
mi - suma mas wszystkich i-tych składników roztworu:
![]()
Suma ułamków wagowych wszystkich składników roztworu równa się jedności:
![]()
Procent wagowy (masowy) - jest to ułamek wagowy pomnożony przez sto. Wyraża stężenie tego składnika w 100g roztworu.
![]()
[% wag.]
Procent objętościowy - jest to stosunek objętości vi tego składnika do objętości v całego roztworu, pomnożony przez sto
![]()
[% obj.]
Objętość całkowita v równa się ściśle sumie objętości poszczególnych składników tylko w przypadku roztworu doskonałego, przy czym v i vi należy wyznaczyć w tych samych warunkach ciśnienia i temperatury. Procenty objętościowe stosowane są przeważnie do wyrażania składu roztworów gazowych.
Ułamek molowy xi składnika i nazywamy stosunek liczby moli n-tego składnika do sumy liczby moli ni = n1+n2+...+nn wszystkich składników roztworu
![]()
Podobnie jak suma ułamków wagowych, tak i suma ułamków molowych wszystkich składników roztworu równa się jedności.
![]()
Procent molowy - jest to ułamek molowy pomnożony przez sto.
![]()
Stężenie molowe c(X) składnika X w danym roztworze jest to stosunek liczby moli tego składnika n(X) do objętości roztworu v.
![]()
czyli wyraża ono liczbę moli składnika X w 1dm3 lub liczbę milimoli w 1 cm3 albo liczbę kilomoli w 1m3.
Wzór można przedstawić w inny sposób. Jeżeli przez mx oznaczymy masę składnika X w gramach, M(X) - jego masę molową, w g/mol, m - całkowitą masę roztworu w gramach, d gęstość roztworu w g/cm3, przy czym:
![]()
oraz ![]()
to otrzymamy
![]()
W przypadku gdy gęstość roztworu d' wyrażona jest w g/dm3, wzór przyjmuje prostszą postać
![]()
Stężenie procentowe - jest to wyrażony w procentach stosunek masy substancji rozpuszczonej ms do masy roztworu mr (czyli sumy masy substancji rozpuszczonej ms i masy rozpuszczalnika ma)
![]()
czyli
![]()
Można również interpretować stężenie procentowe jako procent wagowy substancji rozpuszczonej w stosunku do masy roztworu przyjętej za 100%.
W trzecim sposobie interpretacji zakłada się, że jest ono równe liczbie gramów substancji rozpuszczonej w 100g roztworu.
Stężenie normalne, nazywane także stężeniem równoważnikowym, jest to stosunek liczby równoważników n(1/zX) składnika X w roztworze do objętości roztworu
![]()
Podobnie jak stężenie molowe można wyrazić stężenie normalne
![]()
![]()
Związek pomiędzy stężeniem normalnym i stężeniem molowym jest taki, jak pomiędzy liczbą równoważników i liczbą moli
![]()
Stężenie normalne może być wyrażone tak, jak stężenie molowe w mol/dm3, mmol/dm3 lub mol/m3
Stężenie molarne (molalność) cm(X) jest to stosunek liczby moli n(X) składnika X do masy rozpuszczalnika mr(kg) w kilogramach. Wyraża ono liczbę moli składnika X w jednym kilogramie rozpuszczalnika
![]()
gdzie:
mr - masa rozpuszczalnika w gramach
mx - masa składnika X (substancji rozpuszczonej) w gramach
M(X) - masa molowa tego składnika (g/mol)
Przeliczanie wzajemne stężeń
W celu przeliczenia danego stężenia na inne stężenie można stosować podane niżej zależności, które wynikają ze wzorów określających te stężenia.
1) Ułamek wagowy - ułamek molowy
(procent wagowy - procent molowy)
![]()
![]()
Wzór ogólny dla danego składnika i ma postać
![]()
gdzie:
Mśr - oznacza średnią masę roztworu, którą można obliczyć przy pomocy ułamków molowych lub wagowych oraz wartość mas molowych poszczególnych składników;
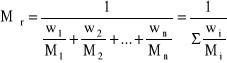
Zależność pomiędzy procentem wagowym i procentem molowym jest taka sama, jak pomiędzy ułamkiem wagowym i ułamkiem molowym
![]()
oraz ![]()
więc:
![]()
2) Ułamek wagowy (lub procent wagowy) - stężenie molowe. Związek pomiędzy ułamkiem wagowym i stężeniem molowym wynika ze wzoru
![]()
zatem
![]()
3) Stężenie molowe - stężenie molarne. Zależność między tymi sposobami wyrażania stężeń można przedstawić następująco
![]()
4) Stężenie molowe - stężenie procentowe
![]()
Roztwory rozcieńczone
W przypadku roztworów o dużym rozcieńczeniu, tzn. gdy masa mx substancji rozpuszczonej jest bardzo mała w porównaniu z masą mr rozpuszczalnika (mx<<mr), wtedy wzory określające poszczególne rodzaje stężeń oraz wzory przeliczeniowe przyjmują w pewnych przypadkach prostsza postać, na przykład:
![]()
![]()
![]()
Z równań tych oraz ze wzoru określającego stężenie molarne Cm(X), wynikają następujące przybliżone zależności:
![]()
![]()
oraz
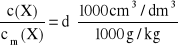
gdzie: Mr - masa molowa rozpuszczalnika.
II. Obliczenia podczas sporządzania roztworów
Do obliczeń przeprowadzanych podczas sporządzania roztworów można zastosować tzw. regułę krzyżową mieszania, opartą na zapisie, w którym po lewej stronie umieszcza się stężenia roztworów początkowych ![]()
i ![]()
, w środku stężenie roztworu końcowego ![]()
, a po prawej stronie różnicę stężeń roztworów początkowego i końcowego.
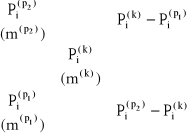
przy czym
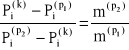
oraz
![]()
gdzie: ![]()
,![]()
i ![]()
- masy odpowiednio roztworów początkowych i końcowych.
Na ogół przyjmuje się ![]()
1) przygotowanie roztworów z czystych składników
W celu zastosowania krzyżowej reguły mieszania postępuje się w ten sposób, że czysty rozpuszczalnik (wodę traktuje się jako roztwór o stężeniu 0,0%, a czystą substancję rozpuszczoną - jako roztwór o stężeniu 100%.
2) rozcieńczanie roztworów
Podczas rozcieńczania roztworu masa mi rozpuszczonej w nim substancji pozostaje nie zmieniona.
Ponieważ
![]()
oraz ![]()
zatem
![]()
stąd
![]()
przy czym
![]()
wobec czego zależność![]()
można wyrazić w następującej postaci
![]()
gdzie:
m(p) - masa roztworu początkowego
m(k) - masa roztworu końcowego (po rozcieńczeniu)
![]()
- zawartość w % wag. Substancji rozpuszczonej i w roztworze początkowym
![]()
- zawartość w % wag. Substancji rozpuszczonej i w roztworze końcowym
mr - masa dodanego rozpuszczalnika.
3) zwiększanie stężenia roztworu przez odparowanie rozpuszczalnika
Podobnie jak przy rozcieńczaniu roztworu, zwiększanie stężenia przez odparowanie rozpuszczalnika nie powoduje zmiany masy substancji rozpuszczonej. Słuszny jest więc wzór
![]()
ale
![]()
zatem
![]()
gdzie:
mr - masa odparowanego rozpuszczalnika.
4) zwiększanie stężenia roztworu przez dodanie składnika stanowiącego substancję rozpuszczoną
W tym przypadku nie ulega zmianie masa rozpuszczalnika mr (w roztw. początkowym p) = mr ( w roztw. końcowym k), wobec czego słuszna jest następująca zależność:
![]()
przy czym
![]()
zatem
![]()
gdzie:
![]()
i ![]()
- zawartość rozpuszczalnika w roztworze początkowym i końcowym (w % wag.)
mi - masa dodanego składnika i
Równanie![]()
można wyrazić w inny sposób, wprowadzając zamiast ![]()
i ![]()
zawartość składnika rozpuszczonego
![]()
i ![]()
![]()
stąd
![]()
lub
![]()
5) mieszanie roztworów o różnych stężeniach
Po zmieszaniu dwóch roztworów tej samej substancji otrzymuje się roztwór, w którym zawartość substancji rozpuszczonej równa się sumie jej zawartości w roztworach początkowych
![]()
zatem
![]()
przy czym
![]()
więc
![]()
gdzie:
![]()
i ![]()
- zawartość (w % wag.) substancji rozpuszczonej w roztworach początkowych
![]()
i ![]()
- masy tych roztworów
6) reakcje w roztworach
Polega na wykorzystaniu zależności
![]()
stanowiącej przekształcenie definicji stężenia molowego. Dla każdej reakcji wymiany podwójnej:
![]()
gdzie:
w - współczynniki stechiometryczne
X - wzory substancji,
Stosunek molowy substratów S1 i S2, wyrażony stosunkiem odpowiednich iloczynów typu ![]()
, jest równy stosunkowi współczynników stechiometrycznych równania chemicznego
![]()
7) rozpuszczanie hydratów
Stężenie roztworu soli tworzącej hydrat oblicza się jako stężenie soli nie uwodnionej. Obliczając masą substancji rozpuszczonej należy pominąć masę wody hydratacyjnej. Masa roztworu jest sumą masy rozpuszczalnika i masy substancji rozpuszczonej wraz z wodą hydratacyjną.
Wyszukiwarka