G1: Dziedziczenie niemendelowskie - opisać.
dziedziczenie cytoplazmatyczne, dziedziczenie pozachromosomowe, dziedziczenie niemendlowskie związane z materiałem genetycznym zlokalizowanym poza chromosomami, w mitochondriach, plastydach i plazmidach występujących w cytoplazmie komórki; główne cechy d. c. to brak segregacji lub segregacja niemendlowska genów pozachromosomowych i dziedziczenie uniparentalne (po matce lub po ojcu); w czasie zapłodnienia udział gamet męskiej i żeńskiej w przekazywaniu cytoplazmy u wielu gatunków nie jest jednakowy, często cała cytoplazma pochodzi z komórki jajowej, w takiej sytuacji mitochondria i plastydy przekazywane są potomstwu przez matki; u drzew szpilkowych jednak cytoplazmę przekazuje także pyłek
G2: Proces powstawania przeciwciał.
Zasadniczą cechą limfocytów B jest możliwość produkcji przeciwciał. Podczas odpowiedzi odpornościowej limfocyty B wiążą antygeny za pomocą BCR, czyli receptora, w którego skład wchodzi swoiste, charakterystyczne dla danej komórki przeciwciało. Po związaniu antygenu najbardziej typową sytuacją jest jego przetworzenie i wystawienie na powierzchni komórki w postaci kompleksu z białkami MHC. Kompleks ten jest rozpoznawany przez swoisty względem danego antygenu limfocyt T pomocniczy. Dopiero po takim rozpoznaniu dochodzi do transformacji blastycznej i powstaniu komórki plazmatycznej produkującej przeciwciała. Antygeny, które powodują taki typ reakcji nazywamy antygenami grasiczozależnymi. W odróżnieniu od nich, antygeny grasiczoniezależne nie wymagają obecności limfocytów T pomocniczych i mogą bezpośrednio aktywować limfocyty B.
Przedstawiony powyżej schemat odpowiedzi z udziałem limfocytów B (odpowiedzi humoralnej) jest charakterystyczny dla komórek dziewiczych, tj. takich, które nie miały wcześniej do czynienia z danym antygenem. Powtórne pobudzenie (podczas odpowiedzi wtórnej) danego limfocytu, funkcjonującego teraz jako limfocyt pamięci nie wymaga już obecności limfocytów pomocniczych. Nie oznacza to jednak, że antygen jest już grasiczoniezależny. Związane jest to z faktem, że antygeny grasiczozależne indukują proces przełączania klas, co doprowadza do tego, że komórka wydziela przeciwciała klas innych niż IgM i IgD. Antygeny grasiczoniezależne nie powodują przełączania klas i w związku z tym nie dają w rezultacie komórek B pamięci. Ponadto w limfocytach stymulowanych antygenami grasiczoniezależnymi nie dochodzi do dojrzewania powinowactwa.Anatomicznie miejscem syntezy przeciwciał jest śledziona i szpik kostny, w których komórki plazmatyczne lokują się po pobudzeniu.Limfocyty B są stymulowane za pomocą licznych cytokin, przy czym największą rolę odgrywają cytokiny pochodzące od limfocytów Th2. Mimo istotnej roli w odpowiedzi odpornościowej przeciwko mikroorganizmom żyjącym pozakomórkowo, limfocyty B mogą też być przyczyną chorób autoimmunizacyjnych i innych stanów patologicznych (np. związanego z zapleniem wątroby kłębuszkowego zapalenia nerek).
G3: Jaki związek ma zróżnicowanie w trakcie embiogenezy z tubulinami.
Embriogeneza inaczej rozwój zarodkowy to rozwój zarodka, który rozpoczyna się w chwili zapłodnienia, aż do monentu wydostania się (wyklucia) zarodka z osłon jajowych (u jajorodnych i jajożyworodnych) lub do opuszczenia układu rozrodczego samicy (urodzenia, u żyworodnych).
Zapłodnienie - połączenie się jąder komórek rozrodczych (męskiej i żeńskiej) w wyniku czego powstaje nowa komórka nazywana zygotą.
Bruzdkowanie (ang. cleavage), segmentacja, pierwszy etap rozwoju zarodkowego zwierząt tkankowych; seria mitotycznych podziałów zapłodnionej (lub rozwijającej się partenogenetycznie) komórki jajowej na coraz mniejsze komórki — blastomery; w wyniku bruzdkowania powstaje morula, a następnie blastula. W czasie bruzdkowania ani masa, ani objętość, ani zasadniczy kształt zarodka nie ulegają zmianie.
Gastrulacja (ang. gastrulation) - proces w rozwoju zarodka zwierząt, następujący po bruzdkowaniu. W wyniku gastrulacji powstaje gastrula. W procesie gastrulacji dochodzi do zgrupowania komórek pełniących podobne funkcje w organizmie.
Organogeneza - tworzenie się i rozwój narządów w trakcie rozwoju zarodkowego i larwalnego
Tubulina - Białko globularne tworzące protofilament mikrotubul. Białka te w mikrotubulach występują w postaci heterodimerów składających się z tubuliny alfa i tubuliny beta, z kolei każda z podjednostek składa się z trzech domen. Podjednostka alfa ma masę cząsteczkową 55-57 kDa, a beta ok. 53kDa. Heterodimer tubuliny ma wymiary 3,5x4 nm. Istnieje też tubulina gama zlokalizowana w centrosomach, stanowiąca miejsce nukleacji (podstawę do dobudowywania kolejnych cząsteczek) mikrotubul. W centrosomach odkryto również tubuliny delta i epsilon mogące odgrywać rolę w formowaniu mitotycznego wrzeciona podziałowego.
* Wrzeciono podziałowe - właściwie: wrzeciono kariokinetyczne - to wrzecionowata struktura zbudowana z włókien białka (tzw. mikrotubul). Włókna te są kurczliwe i zawierają niewielkie ilości RNA. Wrzeciono kariokinetyczne odgrywa ważną rolę w procesie "wędrówki" chromosomów do przeciwległych biegunów komórki.
G4: Proszę opisać budowę immunoglobulin i budowę genów kodujących immunoglobuliny.
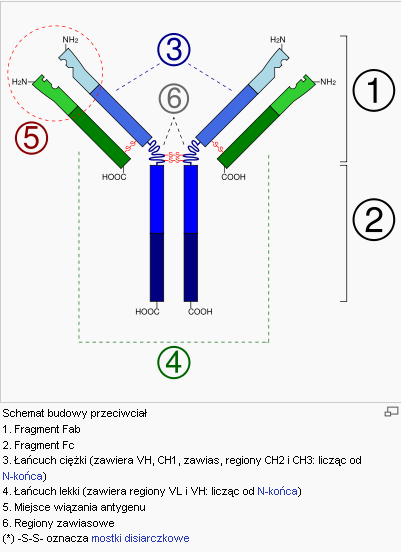
a) Wszystkie przeciwciała mają podobną budowę. Są to białkowe cząsteczki o kształcie litery "Y" o masach cząsteczkowych od 150 do 970 kDa, złożone (w formie monomerycznej) z czterech glikozylowanych łańcuchów peptydowych. Dwa z tych łańcuchów, określane mianem łańcuchów ciężkich (IgH - na rysunku kolor niebieski) są dłuższe i związane ze sobą wiązaniami dwusiarczkowymi. Pozostałe dwa łańcuchy, nazywane lekkimi (IgL - kolor zielony) są związane z łańcuchami ciężkimi również za pomocą mostków dwusiarczkowych. Obydwa łańcuchy ciężkie w danej cząsteczce są identyczne, podobnie jest z łańcuchami lekkimi. Region, w którym występują wiązania dwusiarczkowe pomiędzy IgH (miejsce zgięcie łańcuchów) nazywamy regionem zawiasowym, gdyż warunkuje on tzw. zmienność segmentalną, czyli możliwość rozchylania się ramion przeciwciała.
Zastosowanie papainy umożliwia rozcięcie przeciwciała i uzyskanie z pojedynczej cząsteczki dwóch fragmentów Fab (ang. Antigen Binding - wiążących antygen) oraz jednego fragmentu Fc (ang. Crystalization - krystalizującego). Miejsce cięcia enzymu wypada nieco powyżej regionu zawiasowego. Na podstawie takiego trawienia enzymatycznego udało się potwierdzić istnienie dwóch funkcjonalnych części:
fragmentów Fab, odpowiadających ramionom przeciwciała i wiążących się z antygenem
fragmentu Fc, pełniącego funkcję efektorową, czyli odpowiadającego za różne zjawiska, które zapoczątkowuje związanie antygenu, np. immunofagocytozę. Fragment Fc jest związany z cytofilnością przeciwciał.
Badania nad budową przeciwciał pozwoliły wniknąć głębiej w budowę ich łańcuchów peptydowych. Okazało się, że każdy łańcuch posiada część stałą (ciemniejszy kolor na schemacie), która jest taka sama u wszystkich przeciwciał danej klasy (klasy są opisane dalej), oraz część zmienną (jaśniejszy kolor na schemacie), różniącą się wśród przeciwciał o różnej swoistości. Część zmienna łańcucha ciężkiego nosi nazwę VH, zaś łańcucha lekkiego - VL. Części stałe są oznaczone symbolami CH (łańcuch ciężki) i CL (łańcuch lekki), przy czym każda domena części stałej łańcucha ciężkiego jest oznaczona cyfrą. Jak widać, w skład fragmentu Fc wchodzi wyłącznie część stała IgH, zaś w skład Fragmentu Fab - fragment części stałej łańcucha ciężkiego oraz kompletne łańcuchy lekkie. Każde z ramion przeciwciała (Fab) zawiera więc część wiążącą antygen, zwaną paratopem (na rysunku otoczona czerwonym, przerywanym okręgiem), który złożony jest zarówno z fragmentów IgH, jak i IgL, funkcje efektorowe natomiast zależą jedynie od IgH.
b) Każdy łańcuch (L i H) składa się z części zmiennej V (odpowiednio VH i VL) i stałej C
(CH i CL). Cześć stała jest wspólna dla wielu immunoglobulin, natomiast przeciwciała wiążące różne antygeny maja różne części zmienne. Cześć zmienna łańcucha L jest kodowana przez dwie grupy genów V i J, a cześć stała przez gen C. Na chromosomie 2 są geny kodujące łańcuchy lekkie k, na chromosomie 22 geny kodujące łańcuch lekki l, a na chromosomie 14 znajdują się geny kodujące łańcuch cieżki immunoglobulin. Dotychczas zidentyfikowano około 300 genów V i 5 genów J kodujących VL oraz 200 genów V, 12 genów D i 4 geny J kodujące VH. Podczas produkcji immunoglobuliny, w DNA limfocytu B, następuje zbliżenie przypadkowo wybranego genu V do jednego z genów J na drodze rekombinacji (rearanżacji). W ten sposób powstaje pojedynczy duży gen, który koduje VL i który podlega transkrypcji wraz z genem kodującym C. Informacyjny RNA (mRNA) nie może być wykorzystany bezpośrednio do syntezy białka, ponieważ przepisaniu uległ również zbędny odcinek DNA leżący pomiędzy genem VJ i genem C. Dopiero po jego wycięciu powstaje dojrzały mRNA, na matrycy, którego syntetyzowany jest lekki łańcuch immunoglobuliny.
Łancuch cieżki immunoglobuliny powstaje na podobnej zasadzie jak łańcuch lekki. Jednak główna różnica jest obecność dodatkowej grupy genów D, zlokalizowanej pomiędzy
genami V i J. W ten sposób powstaje zrekombinowany gen VDJ kodujący VH.
G5: Cechy charakterystyczne (charakteryzujące) transpozony.
Transpozon to sekwencja DNA, która może przemieszczać się na inną pozycje w genomie tej samej komórki w wyniku procesu zwanego transpozycją. Transpozycja powoduje mutacje i może zmieniać ilość DNA w genomie.
Rozróżniamy dwie klasy transpozonów:
transpozony klasy I: retrotranspozony (ang. retrotransposons). Wymagają przepisania z DNA na RNA, a następnie przy użyciu odwrotnej transkryptazy (ang. reverse transcriptase) zostają skopiowane na DNA, wreszcie wklejone do genomu, niekiedy w wielu kopiach.
transpozony klasy II. Przemieszczają się w genomie poprzez wycinanie z pierwotnego położenia, następnie "wklejanie się" w nowe miejsce przy użyciu enzymu transpozazy.
*retranspozony ->
Istnieją dwa typy retrotranspozonów. Jeden zawiera na obu końcach długie powtórzone sekwencje nukleotydów (LTR), natomiast drugi ich nie posiada. Ponadto retrotranspozony zawierają geny kodujace enzymy niezbędne do przemieszczania się w procesie transpozycji. Po wniknięciu retrotranspozonu (transpozonu RNA) do komórki gospodarza (lub po transkrypcji retrotranspozonu zintegrowanego z genomem gospodarza na transpozonowej matrycy RNA) następuje synteza pierwszej nici DNA przez enzym zwany odwrotną transkryptazą. W ten sposób powstaje pozachromosomowa, dwuniciowa cząsteczka zbudowana z jednej nici RNA i jednej nici DNA. Następnie matrycowa nić RNA jest wytrawiana (przez enzym RNA-zę), a na jej miejsce syntetyzowana jest druga (komplementarna do pierwszej) nić DNA. Taki dwuniciowy DNA zostaje za pomocą enzymu integrazy wstawiony do genomu gospodarza.
Retrotranspozony niezawierające LTR stanowią około 20% ludzkiego genomu.
* Transpozaza -> enzym (EC 2.7.7) przeprowadzający reakcję transpozycji czyli przemieszczania się po genomie ruchomych elementów zwanych transpozonami. Transpozaza wiąże się z DNA i przecina je, uwalniając transpozon, a następnie przecina docelową cząsteczkę DNA i przyłącza do niej transpozon.
Przykład:
Z przemieszczaniem się transpozonów mogą być związane bardzo poważne zmiany w DNA: delecje, inwersje i duplikacje obejmujące bardzo nieraz obszerne rejony i powodujące nieraz utratę funkcji niektórych genów, a wzmożoną ekspresję innych. Co jednak u możliwia transpozycję, czyli wędrówkę transpozonów przez geny?
transpozon z grupy IS - najprostszych transpozonów bakteryjnych. Transpozon IS1 występuje u E. coli i ma długość zaledwie 768 par zasad. Koduje on specyficzną nukleazę, zwaną transpozazą. Na obu końcach tego transpozonu z najdują się krótkie, niemal identyczne, lecz przeciwnie skierowane 23- nukleotydowe sekwencje ITR.
Transpozaza rozpoznaje obie sekwencje terminalne, a także krótką (dla IS1 9 par zasad) sekwencję akceptorową (docelową) w genomie gospodarza. Transpozaza nacina obie nici na końcach transpozonu i w obrębie sekwencji docelowej, tworząc lepkie końce. Podczas następującego później wbudowywania transpozonu następuje podwojenie sekwencji akceptorowej tak, że w efekcie IS1 w nowym położeniu jest oflankowany przez dwie sekwencje docelowe.
W procesie transpozycji niezbędne są też enzymy gospodarza: polimeraza I DNA i ligaza
G6: Opisać totipotencjalne, jak powstawają, techniki...
Komórki macierzyste, inaczej komórki pnia (ang. stem cells) - komórki, które posiadają obydwie wymienione poniżej cechy:
są zdolne do potencjalnie nieograniczonej liczby podziałów. Inaczej mówiąc są nieśmiertelne i samoodnawialne.
mają zdolność do różnicowania się do innych typów komórek.
Totipotencja jest zdolnością pojedynczej komórki do zróżnicowania się w każdy typ komórkowy organizmu. Z definicji komórką totipotencjalną jest zygota. U ssaków totipotipotencją charakteryzują się komórki macierzyste i komórki zarodkowe węzła zarodkowego blastocysty. W czasie pierwszych godzin po zapłodnieniu, komórka dzieli się na identyczne, totipotencjalne komórki. Około cztery dni po zapłodnieniu, po wielu cyklach podziału, komórki te zaczynają się specjalizować. Komórki totipotencjalne przekształcają się w komórki pluripotencjalne, które mogą się przekształcić w wiele typów komórek organizmu, lecz nie wszystkie. Komórki pluripotencjalne różnicują się dalej w komórki multipotencjalne, z których wykształcają się komórki o specyficznej funkcji. Na przykład, multipotencjalne komórki krwi mogą wytworzyć erytrocyty, leukocyty oraz megakariocyty, z których powstają płytki krwi.
komórki totipotencjalne (totipotentne) - mogą różnicować się do każdego typu komórek danego organizmu, jest to komórka powstała w wyniku zapłodnienia - zygota, lub komórki blastuli do stadium kilku blastomerów, komórki totipotencjalne są zdolne do wykształcenia całego organizmu, są najbardziej pierwotnymi komórkami,
Ze względu na pochodzenie komórki macierzyste podzielono na komórki zarodkowe, płodowe i dorosłe. Komórki macierzyste można otrzymywać zarówno z zarodków ludzkich uzyskanych metodą zapłodnienia pozaustrojowego, z zarodków uzyskanych poprzez klonowanie tkanki płodu po poronieniu czy aborcji, z krwi pępowinowej uzyskanej podczas porodu, jak i z organizmu ludzkiego, w którym występują komórki macierzyste dorosłe.Pojawiają się także doniesienia o możliwości pobierania komórek macierzystych ze zwłok.
G7: Proszę opisać proces determinacji płci. Dlaczego mogą istnieć ... Z genotypu XY i fenotypu żeńskim. (dziwnie sformułowane pytanie :/ )
Determinacja płci, procesy różnicujące rozwój organizmów w kierunku organizmów żeńskich i męskich. Istnieje fenotypowa determinacja płci (czynniki środowiskowe warunkują wykształcenie się danej płci) i genetyczna determinacja płci (związana z genami znajdującymi się na chromosomach płci).
Chromosomy płci, heterosomy, allosomy - determinujące płeć chromosomy u rozdzielnopłciowych organizmów eukariotycznych. Płeć osobnika determinuje ich obecność lub ich liczba w stosunku do liczby autosomów.
U człowieka występują 22 pary chromosomów autosomalnych i jedna para chromosomów płci, która odpowiada za determinację płci. Łącznie kariotyp człowieka tworzą 23 pary chromosomów. Osobnik posiadający chromosomy XX jest płci żeńskiej, natomiast osobnik z jednym chromosomem X i jednym chromosomem Y - będzie płci męskiej. X jest większy od Y, i zawiera więcej genów. Y zawiera gen SRY determinujący płeć męską. Płeć determinowana jest zatem przez chromosom otrzymany od ojca.
System XY występuje też u innych ssaków. U ptaków system determinacji płci jest odwrotny. Samice mają dwa różne chromosomy płci (ZW), a samce dwa jednakowe (ZZ). Płeć determinowana jest zatem przez chromosom otrzymany od matki.
U muszki owocowej Drosophila melanogaster samice mają dwa chromosomy X, a samce chromosom X i chromosom Y, ale płeć osobnika zależy od stosunku liczby chromosomów X do autosomów.
G8: Opisać proces powstawania przeciwciał i wyjaśnić, dlaczego organizm może wytwarzać miliardy białek rozpadających różne antygeny.
tak jak G2....
G9: Proszę wyjaśnić czym różni się klonowanie genów od klonowania organizmów i opisać w skrócie wybrane w obu przypadkach metody.
Klonowanie organizmów oznacza procedurę otrzymywania organizmów o takiej samej informacji genetycznej, z reguły poprzez procedurę transferu jądra z komórki somatycznej do komórki jajowej pozbawionej uprzednio jądra. W przypadku klonowania roślin stosuje się procedurę odróżnicowania komórek dawcy do komórek merystematycznych.
Proces w przypadku owcy Dolly. Składał się z siedmiu etapów. Najpierw pobrano komórki somatyczne od jednego osobnika i hodowano je in vitro (tak żeby pozostawały w spoczynku). Następnie, pobraną od innego osobnika komórkę jajową, pozbawiono jądra komórkowego. Obie komórki połączone zostały impulsem elektrycznym (elektrofuzja). Wtedy nowe jądro przejęło funkcje tego usuniętego wcześniej. Na skutek podziałów mitotycznych tej komórki, powstał zarodek, który potem został wprowadzony do macicy innej samicy. W rezultacie, powstała owca będąca kopia genetyczną osobnika, z którego pobrano komórkę somatyczną.
Klonowanie genów - w genetyce i biologii molekularnej proces wyosobniania genu. Polega na łączeniu fragmentów materiału genetycznego z wektorem molekularnym i ich namnażaniu w innym organizmie. Otrzymuje się w ten sposób wiele kopii tego samego genu. Termin klonowanie genów odnosi się też do identyfikacji genów poprzez wykorzystanie procedury klonowania genów. Jeśli pojedynczy fragment genomu jest przenoszony z jednego wektora do drugiego, taki proces określa się mianem subklonowania.
.
G10: Gene targeting - opisać, zastosowanie, czemu nie można używać mikroiniekcji.
Gene targeting, czyli „homologiczna wymiana genów”
Gene targeting jest to technika w genetyce wykorzystująca rekombinacje homologiczną, aby zmienić endogenne geny. Metoda może być wykorzystana do usunięcia genu, wycięcia eksonów oraz wprowadzenia miejscowych mutacji. Gene targeting może być stałe lub okresowy. Warunki przeprowadzenia procesu są specyficzne podczas wzrostu / życia organizmu oraz limitowane przez specyficzne tkanki. Np. Gene targeting wymaga stworzenia specyficznego wektora dla każdego interesującego nas genu.
Metoda mikroiniekcji polega na bezpośrednim wstrzykiwaniu roztworu DNA do obserwowanej pod mikroskopem komórki (ang. injection = zastrzyk). Umożliwia ona dokładnie kontrolowane wprowadzanie dowolnego rodzaju substancji do pojedynczej komórki. W ten sposób przenoszono nie tylko DNA, ale także RNA, białka, a nawet mitochondria. Oczywiście, warunkiem zastosowania tej metody jest posiadanie bardzo kosztownej aparatury, a także opanowanie jej obsługi, wymagającej dużej zręczności. W metodzie tej komórki transformowane są pojedynczo, więc jej wydajność mierzona bezwzględną liczbą uzyskanych transformantów jest znikoma (choć jeśli odnieść ją do liczby poddanych manipulacji komórek to zbliża się do 100%). Metoda jest więc uważana za klasyczną (wspominają ją wszystkie podręczniki), ale w praktyce stosowana jest zupełnie sporadycznie.
G11: Metody klonowania zwierząt i możliwe wykorzystanie tych zwierząt w biotechnologii i medycynie.
Klonowanie jest to proces oparty na przenoszeniu (transferze) jąder komórkowych - tej samej technice, którą od wielu lat stosują naukowcy do kopiowania zwierząt z komórek zarodkowych. W tym celu potrzebne są dwie komórki. Pierwsza z nich - biorca - jest na ogół nie zapłodnionym oocytem pobranym od zwierzęcia tuż po owulacji. Takie komórki jajowe powinny rozwijać się po odpowiedniej stymulacji. Drugą z nich jest dawca jądra. To ona ma zostać skopiowana. Badacz, patrząc w silnie powiększający mikroskop, przytrzymuje oocyt dzięki przyssaniu go do końca małej pipety i za pomocą niezwykle cienkiej mikropipety usuwa z niego chromosomy, twory zawierające DNA komórki (w tym stadium nie znajdują się one w wyodrębnionym jądrze). Następnie komórka-dawca wraz ze swoim jądrem jest łączona z oocytem. Niektóre ze zrekonstruowanych w ten sposób oocytów zaczynają się rozwijać tak jak normalne zarodki i jeśli przeszczepi się je do macicy matki zastępczej, mogą urodzić się młode.
Choć klonowanie metodą przenoszenia jąder komórkowych jest powtarzalne, ma także pewne ograniczenia. Niektóre otrzymane w ten sposób cielęta i jagnięta są niezwykle duże, ale zjawisko to występuje także, gdy zarodki hoduje się in vitro przed ciążą. Co ważniejsze, transfer jąder nie jest techniką wydajną. We wszystkich dotychczas opisanych badaniach nad klonowaniem notuje się konsekwentnie bardzo duży odsetek zgonów w czasie rozwoju zarówno zarodkowego, jak i płodowego. Dane pochodzące z różnych laboratoriów wskazują, że zaledwie 1-2% osobników przeżywa do porodu. Niestety, nawet te zwierzęta, które przetrwały do swoich narodzin, giną wkrótce po nich.
Zastosowanie w medycynie:
Klonowanie daje wiele nowych możliwości. Jedną z nich jest tworzenie genetycznie zmodyfikowanych narządów zwierzęcych nadających się na przeszczepy dla ludzi. Obecnie umierają rokrocznie tysiące pacjentów, którzy oczekują na transplantację serca, wątroby czy nerki. Narząd pochodzący od świni przeszczepiony człowiekowi zostanie szybko zniszczony przez „supersilną” reakcję immunologiczną. Jest ona wywoływana przez białka znajdujące się na powierzchni komórek świni po uprzednim zmodyfikowaniu ich przez enzym zwany transferazą a-galaktozylu. To pozwala sądzić, że przeszczep narządu genetycznie zmienionej świni pozbawionej tego enzymu byłby tolerowany, jeśli lekarze dodatkowo podawaliby pacjentom leki działające hamująco na inne, mniej nasilone reakcje immunologiczne.
Zastosowanie biotechnologiczne (przykład)
Chodzi o połączenie komórki jajowej krowy, z której usunięto jądro, z komórką somatyczną człowieka. Tego typu twory nie dają się w laboratorium hodować zbyt długo i bardzo dobrze, bo chroni to przed nadużyciami ale ten czas wystarczy, żeby pobrać pierwotne komórki zarodkowe. Wiele przesłanek wskazuje na to, że można będzie z nich otrzymać różne tkanki, oczywiście identyczne pod względem genetycznym z tkankami człowieka, którego komórki wprowadzono do krowiego jajeczka.
G12: Organizmy transgeniczne i wykorzystanie
Są to organizmy niosące sztucznie wprowadzone geny, które mogą być przekazywane następnym pokoleniom. Wprowadzony gen określa się mianem transgenu.
Modyfikacje zwierząt mają na celu głównie uzyskanie zwierząt o pożądanych cechach w hodowli - szybciej rosnące świnie, ryby, zastosowaniu ich w produkcji białek, enzymów, innych substancji wykorzystanych w przemyśle farmaceutycznym (jako bioreaktory), uodpornieniu na choroby.
Modyfikacje zwierząt nie są tak popularne jak roślin, głównie ze względu na trudności w samym procesie modyfikacji, proces jest bardzo skomplikowany i trwa długo, koszty są bardzo duże. Zwierzęta modyfikowane genetycznie często chorują, czy są bezpłodne.
Modyfikacje mające na celu wytwarzanie w organizmie zwierząt genetycznie zmienionych białek wykorzystywanych jako leki - czyli wykorzystywanie ich jako bioreaktorów.
Uzyskanie szybszego wzrostu zwierząt hodowlanych.
Odporność na choroby.
Modyfikowane świnie jako dawcy narządów.
G13: Imprinting genetyczny - co to jest, opisac zjawisko
Imprinting genomowy, rodzicielskie piętno genomowe, naznaczenie genetyczne - polega na różnym stopniu metylacji genów w komórkach jajowych i komórkach plemnikowych. Gen jest metylowany na allelu pochodzącym od jednego z rodziców. Nakładanie imprintingu zachodzi w czasie gametogenezy. Wtedy jest znoszony wzór metylacji odziedziczony po rodzicach i nakładany nowy, zależny od płci. Do zmetylowango nukleotydu nie mogą się przyczepić czynniki transkrypcyjne, co powoduje wyciszenie genu.
Zjawisko to pozwala zapobiegać partenogenezie, która jest możliwa u niewielkiej liczby gatunków (np. u pszczół) i powoduje zmniejszenie zmienności organizmów. Imprinting jest wynikiem konkurencji materiału genetycznego żeńskiego (przekazywanie genów, wychowanie potomstwa) i męskiego (odżywianie i rozwój zarodka).
Gdy z zygoty u myszy, przed zlaniem sie jąder komórkowych plemnika i komórki jajowej usuwamy przedjądrze męskie i wprowadzamy żeńskie, to zarodek zamiera na skutek niedorozwoju zarodka, a gdy usuwamy przedjądrze żeńskie i wprowadzamy męskie - zarodek zamiera na skutek niedorozwoju trofoblastu.
Przykładowo imprintingowi ulegają geny Igf2 - gen na insulinopodobny czynnik wzrostu; pracuje głównie w macicy, ale niezmetylowany jest allel ojcowski oraz H19 - gen, który wycisza ekspresję Igf2 i ustala się równowaga w rozwoju zarodka między genomem męskim i żeńskim.
Konsekwencje zaburzeń imprintingu:
zaśniad groniasty (nowotwór embrionalny; 2n pochodzi tylko od ojca, powstaje np. w wyniku polispermii, a materiał genetyczny od matki jest eliminowany);
potworniak jajnika;
zespół Pradera-Williego i zespół Angelmana. Oba powstają w wyniku zaburzeń imprintingu fragmentu chromosomu 15 (15q11) - brak imprintingu ojcowskiego powoduje zespół Pradera-Williego, a brak imprintingu matczynego zespół Angelmana.
Zespół Pradera-Williego (zespół Pradera-Labharta-Williego, ang. Prader-Willi syndrome, Prader-Labhart-Willi syndrome, PWS) - anomalia chromosomalna, najczęściej spowodowana częściową delecją długiego ramienia chromosomu 15 pochodzenia ojcowskiego. Zespół objawów jako pierwsi opisali szwajcarscy lekarze Andrea Prader, Heinrich Willi, Alexis Labhart i Guido Fanconi w 1956 roku [1]. Charakterystyczne cechy tego zespołu to niski wzrost, opóźnienie umysłowe oraz otyłość spodowana mniejszym niż u zdrowych ludzi zapotrzebowaniem energetycznym przy jednoczesnym ciągłym niepohamowanym uczuciu głodu. Uważa się, że zespół Pradera-Williego jest najczęstszą genetycznie uwarunkowaną przyczyną otyłości.
Zespół Angelmana (ang. Angelman syndrome, AS) - rzadki, genetycznie uwarunkowany zespół spowodowany najczęściej delecją fragmentu chromosomu 15 w regionie 15q11-q13. Zespół Angelmana charakteryzują głównie objawy neurologiczne: upośledzenie umysłowe, ataksja, padaczka, charakterystyczne ruchy przypominające marionetkę i napady śmiechu bez powodu (stąd dawna, zarzucona nazwa zespołu, happy puppet syndrome). Mniej wyrażone są cechy dysmorficzne twarzy, takie jak duże usta (makrostomia), wystający język (glossoptosis), szeroko rozstawione zęby. Tęczówki prawie zawsze są niebieskie. Niezwykłą cechą dzieci z zespołem Angelmana jest ich fascynacja wodą.
Wyszukiwarka
Podobne podstrony:
pytania z egzaminu, Aparatura Procesowa, Biologia komórki i Genetyka, sem IV egz
Genetyka EGZAMIN TEORIA, Aparatura Procesowa, Biologia komórki i Genetyka, sem IV egz
0 Wiadomosci wymagane na kolokwiach, Aparatura Procesowa, Biologia komórki i Genetyka
POPGatlik Idzik Aut2 11 (2), Aparatura Procesowa, Biologia komórki i Genetyka
rozwiązanie egzaminu z biolkom, WETERYNARIA, biologia komórki
Egzamin5, UG, SEM2, BIOLOGIA KOMÓRKI, EGZAMINY
biologia- na egzamin!!!, medycyna, I rok, biologia, giełdy, egzamin praktyczny
Egzamin4, UG, SEM2, BIOLOGIA KOMÓRKI, EGZAMINY
zag na egzamin (opracowac)
Egzamin6, UG, SEM2, BIOLOGIA KOMÓRKI, EGZAMINY
Pytania na Egzamin Botanika, Studia, BIOLOGIA UMCS, 1 rok, Botanika
Egzamin7, UG, SEM2, BIOLOGIA KOMÓRKI, EGZAMINY
Egzamin2, UG, SEM2, BIOLOGIA KOMÓRKI, EGZAMINY
Biologia kom -rki - egzamin, UG, SEM2, BIOLOGIA KOMÓRKI
Pytania na egzamin, Zarządzanie procesami
Egzamin 3 luty 2009, Biologia Komórki, Zagadnienia do egzaminu
więcej podobnych podstron