1. Przedstawiać budowę atomu.- Joanna Mandziuk
Atom jest skupieniem drobnych cząstek materii, zwanych elementarnymi tj: elektrony, protony, neutrony. Protony i neutrony to inaczej nukleony i tworzą one jądro atomu a wokół niego krążą elektrony.
Każdy atom składa się z części wewnętrznej tzw. Jądra i części zewnętrznej- powłok elektronowych. Średnice wszystkich atomów są bardzo małe i zawierają się w granicach od 0,106 nm(nanometr tj 10-9) dla azotu do 0,58 nm dla fransu. Znacznie mniejsze rozmiary mają jądra atomów zbudowane z protonów i elektronów. Podstawową jednostką atomu jest jego masa atomowa (ciężar atomowy) wyrażona jednostką względną w stosunku do 1/16 masy atomu tlenu. Praktycznie za masę atomu przyjęto masę jego jądra (tj. protonów i neutronów) gdyż masa elektronów jest bardzo mała.
Elektrony krążą dookoła jądra z bardzo dużą prędkością po ściśle określonych eliptycznych orbitach (torach) i zawierają w sobie jeden elementarny ładunek elektryczności ujemnej, równoważąc w ten sposób dodatnio naładowane jądro o ładunku równym sumie ładunków wszystkich elektronów, tak że atom jako całość jest elektrycznie obojętny.
Od struktury elektronowej a zwłaszcza od konfiguracji elektronów powłoki zewnętrznej zależą właściwości chemiczne pierwiastków. Atomy z powłoką zewnętrzną całkowicie wypełnioną elektronami mają kulistą chmurę elektronów, są chemicznie obojętne i w przyrodzie występują jako jednoatomowe. Atomy z powłoką zewnętrzną niecałkowicie wypełnioną mają mniej symetryczną powłokę elektronową, są skłonne do łączenia się w cząsteczki (np. wodór)
Elektrony krążące po zewnętrznej powłoce nazywa się elektronami walencyjnymi lub wartościowości. Od nich zależą wiązania atomowe. Atom z niecałkowicie wypełnioną zewnętrzną powłoką, dążąc do uzyskania struktury elektronowej zbliżonej do struktury gazu szlachetnego, oddaje swoje lub przyłącza elektrony walencyjne innego atomu. Pierwiastki oddające swe elektrony walencyjne nazywa się elektrododatnimi, przyłączające elektrony-elektroujemnymi.
Struktura elektronowa atomu gęstość chmury elektronowej na jednostkę objętości można przedstawić jako iloczyn funkcji z których każda jest uzależniona odpowiednio od odległości promieniowej od jądra (r) lub kątów określających położenie punktu względem jądra we współrzędnych biegunowych. Strukturę elektronową należy sobie wyobrazić jako chmurę elektronową wokół jądra. Duże prawdopodobieństwo znalezienia elektronów w danym miejscu odpowiada dużej gęstości chmury elektronowej. Elektron może zajmować ściśle określone stany magnetyczne związane z gęstościami chmur elektronowych. Charakteryzowane przez 4 liczby kwantowe: główną, poboczną, magnetyczną, spinową.
*Główna- określa liczbę powłok węzłowych kulistych ze środkiem w jądrze lub płaszczyzn przechodzących przez jądro na których gęstość chmury elektronowej jest równa.
*Poboczna-określa liczbę płaszczyzn węzłowych przechodzących przez jądro charakteryzuje moment pędu.
*Magnetyczna-moment pędu elektronów określa składową tego momentu w kierunku przyłożonego pola magnetycznego.
*Spinowa-wpływ pola magnetycznego wytworzony przez elektron walencyjny wirujący wokół własnej osi.
Proton składa się z dwóch kwarków u i jednego kwarku d jego ładunek wynosi +1
Neutron składa się z dwóch kwarków d i jednego kwarku u i jest elektrycznie obojętny (ład.0)
Nukleony mają po dwa kwarki: górny +2/3 i dolny -1/3.
Kwarki- cząstki niestabilne, występują po 2 lub po 3. Są utrzymywane w tych grupach za pomocą glonów (kwanty energii spajające kwarki). Jest 8 rodzajów glonów a różnią się one kolorem i podobnie jak kwarki wpływają na oddziaływanie elektromagnetyczne. Kwarki wchodzące w skład pojedynczego protonu lub elektronu musza cechowac się różnymi „kolorami”: czerwony, niebieski, zielony.
Mezony-cząstki złożone z dwóch kwarków, niestabilne
Bariony- cząstki złożone z trzech kwarków
2. Na czym polega związek między położeniem pierwiastka w układzie okresowym i jego własnościami metalicznymi?- Sylwia Onacik
ęłęóMetaliczność, rozumiana zarówno jako właściwość chemiczna (tworzenie wodorotlenków) jak i fizyczna (połysk, kowalność, przewodnictwo elektryczne i cieplne itp.) maleje ze wzrostem numeru grupy a rośnie wraz z numerem okresu. Generalnie więc zmienia się rosnąco "po przekątnej" od fluoru do fransu. Odwrotnie zmienia się elektroujemność, co jest zrozumiałe, bowiem obie te cechy wywodzą się z tych samych źródeł - wielkości promienia jonowego i łatwości osiągnięcia oktetu elektronowego na zewnętrznej powłoce.
Jeśli przez metaliczność pierwiastka rozumiemy jego zasadowość (tworzenie wodorotlenków), to kwasowość będzie rosła generalnie tak jak elektroujemność, choć tu zależności nie są tak proste i jednoznaczne
Ze względu na własności i miejsce w układzie okresowym tradycyjnie rozróżnia się:
metale alkaliczne
metale ziem alkalicznych
metale przejściowe
metale ziem rzadkich.
3. Wymień i krótko omów typy wiązań występujących w materiałach.- Natalia Bartos
Wymień i krótko omów typy wiązań występujących w materiałach?
Rozróżnia się cztery typy wiązań międzyatomowych: jonowe, atomowe (kowalencyjne), międzycząsteczkowe (van der Waalsa) i metaliczne.
Wiązanie jonowe
Wiązanie jonowe jest wynikiem dążenia różnych atomów do tworzenia trwałych 8-elektronowych konfiguracji gazów szlachetnych poprzez uwspólnienie elektronów.
Kryształy, zwane jonowymi, cechują się dużą wytrzymałością i twardością oraz wysoką temperaturą topnienia. Mają także skłonność do łupliwości wzdłuż płaszczyzn. Wiązanie jonowe występuje głównie w kryształach halogenków pierwiastków alkalicznych i ziem alkalicznych.
Wiązanie atomowe
Wiązanie atomowe powstaje w wyniku powstawania par elektronów (o różnych spinach) wiążących atomy , co wynika z dążenia do tworzenia 2- lub 8- elektronowych konfiguracji gazów szlachetnych. Uwspólnione elektrony przechodzą kolejno od jednego atomu do drugiego, zamieniając je w jony dodatnie, które są przyciągane przez elektrony znajdujące się między nimi. Wiązanie atomowe jest bardzo silne i prowadzi do dużej wytrzymałości mechanicznej i wysokiej temperatury topnienia. Występują one w dwuatomowych cząsteczkach gazów (H2,N2,O2), a także w materiałach półprzewodnikowych (Si, Ge).
Wiązanie van der Waalsa
Wiązanie to jest wynikiem powstawania chwilowych dipoli na skutek nierównomiernego rozkładu ładunków w chmurach elektronowych atomów. Te z kolei indukują dipole w sąsiednich atomach, co umożliwia ich wiązanie. Wiązanie to jest jednakże bardzo słabe (ok. 103 - 104 razy słabsze niż atomowe).
Wiązanie metaliczne
Powstanie wiązania metalicznego polega na przekształceniu atomów tego samego metalu lub atomów różnych metali w zbiór kationów i swobodnie poruszających się między nimi elektronów.
Wiązanie metaliczne może istnieć w stanie stałym lub ciekłym. Występuje w metalach i związkach międzymetalicznych, które wykazują własności metaliczne.
4. Co to jest podstawowy period identyczności, komórka elementarna, komórka sieciowa?- Ola Kubala
Najbliższa odległość atomów na prostej sieciowej to podstawowy period identyczności lub parametr sieci. Przesunięcie (translacja prostej sieciowej) o period identyczności w kierunku różnym od kierunku prostej powoduje znalezienie płaszczyzny sieciowej. Trzy rodziny równoległych płaszczyzn sieciowych dzielą sieć przestrzenną na identyczne równoległościany o parametrach a, b, c stanowiące podstawowe periody identyczności. Równoległościany te to elementarne komórki sieciowe, w pełni charakteryzujące kryształ o sieci prymitywnej. Komórka sieciowa może być opisana za pomocą
a). periodów identyczności - parametry sieci a, b, c
b). kątów między nimi zawartych α, β, γ
Komorka elementarna najmniejsza, powtarzalna część struktury kryształu, zawierająca wszystkie rodzaje cząsteczek, jonów i atomów, które tworzą określoną sieć krystaliczną. Komórka elementarna powtarza się we wszystkich trzech kierunkach, tworząc zamkniętą sieć przestrzenną, której główną cechą jest symetria. Komórka elementarna ma zawsze kształt równoległościanu. Najprostszym typem komórki elementarnej jest komórka regularna prosta (sześcienna) której wielkość określa się długością boku sześcianu, zwaną parametrem sieci i oznaczaną literą a. Sieć regularna nie jest jednak w wystarczająco zwarty sposób obsadzona atomami, toteż w praktyce spotykane są sieci regularne zawierające atomy rozmieszczone dodatkowo bądź we wnętrzu komórki elementarnej (sieć regularna przestrzennie centryczna), bądź na jej ściankach (sieć regularna płasko centryczna) Pierwszy typ sieci oznaczany jest symbolem A2 a drugi symbolem A1. Sieć regularna płaska występuje w większości metali np. : aluminium, niklu, miedzi srebrze, złocie platynie, palladzie, ołowiu. Metale te wykazują szczególnie dobrą plastyczność na gorąco, a niektóre także na zimno i są bardzo dobrymi przewodnikami ciepła i prądu elektrycznego.
Sieć regularna przestrzennie centryczna występuje takich metalach jak : żelazo α chrom, wolfram, molibden, wanad, tantal, niob, sód, potas. Metale tej grupy są mniej ciągliwe niż metale grupy pierwszej i nadają się przeważnie tylko do obróbki plastycznej na gorąco.
Oprócz omówionych sieci spotyka się jeszcze sieć heksagonalna przestrzennie centryczną i tetragonalną. Pierwsza występuje w magnezie, cynku, kadmie i rtęci, druga w białej cynie, galu i indzie. Metale o sieci heksagonalnej mają znacznie gorsze własności plastyczne niż metale o sieci regularnej tylko niektóre z nich mogą być obrabiane na gorąco i na zimno. Metale o sieci tetragonalnej cechuje niska twardość i niska temperatura topnienia. Sieć heksagonalna przestrzennie centryczna oznaczana jest symbolem A3.
5. Co to jest układ krystalograficzny? - Dariusz Górka
Układ krystalograficzny - system klasyfikacji kryształów ze względu na wewnętrzny układ cząsteczek w sieci krystalicznej.
System wyróżnia siedem układów:
Trójskośny
Jednoskośny
Rombowy
Romboedryczny (trygonalny)
Heksagonalny
Tetragonalny
Regularny
6- wyjaśnij pojęcie anizotropii kryształów. - Małgorzata Kudlak
Anizotropia kryształów- zależność własności fizycznych (rozszerzalność termiczna, przewodnictwo elektryczne, współczynnik załamania światła) i chemicznych (szybkość wzrostu i rozpuszczania) kryształu od kierunku przestrzennego. Anizotropia kryształów jest konsekwencją uporządkowanej struktury krystalicznej.
7. Co to są defekty punktowe, liniowe, dyslokacje krawędziowe, śrubowe, wektor Burgersa?- Tośka Zarakowska
Co to są defekty punktowe?
Defektami punktowymi nazywa się zakłócenia periodycznej budowy sieci krystalicznej, spowodowane brakiem atomu lub jonu w określonym węźle sieci albo obecnością dodatkowego atomu w pozycji międzywęzłowej. Stężenie takich defektów zależy od temperatury oraz od rodzaju i ciśnienia otoczenia kryształu. Defektem punktowym jest także atom obcej domieszki oraz, w przypadku związków chemicznych, atom w położeniu węzłowym, jednakże w miejscu drugiego składnika (tzw. anti-site ).
Do punktowych zaliczamy wakancje, atomy międzywęzłowe, atomy domieszek (substytucyjne i międzywęzłowe) i defekty złożone np. podwójna wakancja (diwakancja) lub atom domieszki połączony z wakancją. Wspólną cechą tych defektów jest to, że ich pole naprężeń ma symetrię kulistą, której centrum znajduje się w środku defektu
Wakancja jest defektem powstałym w wyniku nieobsadzenia węzła sieci przez atom. Wskutek tego sąsiednie atomy przesuwają się w kierunku pustego miejsca, co wywołuje zniekształcenie sieci i wytwarza pole naprężeń rozciągające. Wakancje zalicza się do defektów termodynamicznie trwałych, co oznacza, że przy każdej temperaturze ustala się ich równowagowa koncentracja Nv, zgodna z prawem Boltzmanna: nv -w/kT Nv = ÄÄ ÷ A e na gdzie Nv - liczba wakancji, na - liczba atomów, A - stała, w - energia niezbędna do utworzenia jednej wakancji (wynosi ok.0,8 eV), k - stała Boltzmanna.
Z wzoru wynika, że jest to zależność wykładnicza, tzn. że równowagowa koncentracja wakancji rośnie gwałtownie z temperaturą i w pobliżu temperatury topnienia ich koncentracja Nv = ok. 5*10-4, podczas gdy przy temperaturze pokojowej Nv = ok.10-15, czyli że zmiana wynosi 11 rzędów wielkości (1011 razy). W kryształach jonowych taki defekt nazywa się defektem Shottky'ego.
Co to są defekty liniowe?
Defekty liniowe, zwane dyslokacjami, mają jeden wymiar znacznie większy w porównaniu z dwoma pozostałymi (poprzecznymi). Wokół nich następuje zniekształcenie sieci. Początkowo zostały one wprowadzone na bazie rozważań teoretycznych w celu wytłumaczenia rozbieżności między teoretyczną i rzeczywistą granicą plastyczności kryształów. Podczas gdy teoretyczne naprężenie poślizgu (dla idealnych kryształów) wynosi G/30 (G - moduł ścinania), to rzeczywiste jest ok. 1000 razy mniejsze i wynosi poniżej 1 MPa. Póżniej wykryto występowanie dyslokacji w kryształach i stwierdzono, że odgrywają one zasadniczą rolę w procesie odkształcenia plastycznego metali, a także przy ich umocnieniu. Dyslokacje różnią się orientacją, sposobem ich powstawania i własnościami. Mogą być krawędziowe, śrubowe lub mieszane, jednostkowe lub cząstkowe, poślizgowe lub osiadłe. Dyslokacje wprowadzają zaburzenie układu atomów ułatwiające ich przesuwanie się względem siebie pod wpływem naprężeń, a więc odkształcenie plastyczne. Poza tym są one ośrodkami nagromadzenia energii odkształcenia, odgrywają rolę w dyfuzji, przemianach fazowych, korozji i innych procesach.
Co to jest dyslokacja krawędziowa?
Najprostszym modelem dyslokacji krawędziowej jest kryształ, z którego usunięto lub do którego wstawiono fragment płaszczyzny atomowej tzw.ekstrapłaszczyzny. W miejscu ekstrapłaszczyzny powstają naprężenia ściskające, a pod nią rozciągające. Krawędź ekstrapłaszczyzny jest dyslokacją krawędziową. Płaszczyzna prostopadła do ekstrapłaszczyzny i przechodząca przez jej krawędź a-c stanowi płaszczyznę poślizgu tej dyslokacji i działają w niej naprężenia styczne. Wzdłuż płaszczyzny poślizgu występuje niezgodność w układzie atomów, gdyż ekstrapłaszczyzna wprowadza dodatkowy atom, który nie ma dopowiednika poniżej niej. To znacznie ułatwia ścinanie kryształu wzdłuż płaszczyzny poślizgu czyli poślizg.
W zależności od usytuowania ekstrapłaszczyzny można umownie rozróżniać dyslokacje dodatnie (z ekstrapłaszczyzną skierowaną nad płaszczyznę poślizgu) oznaczane symbolem Á lub ujemne ( z ekstrapłaszczyzną skierowaną pod płaszczyznę poślizgu) oznaczane symbolem Â. O dyslokacjach takich mówi się, że mają przeciwne znaki (ich pola naprężeń są obrócone o 180°). Jeśli takie dyslokacje znajdują się na jednej płaszczyźnie poślizgu, wówczas się przyciągają, a po spotkaniu następuje ich anihilacja. Dyslokacje krawędziowe jednakowego znaku odpychają się.
Co to jest dyslokacja śrubowa?
Modelem dyslokacji śrubowej jest kryształ, w którym nastąpiło ścięcie o jedną odległość międzyatomową wzdłuż określonej płaszczyzny pod warunkiem, że wszystkie atomy na części płaszczyzny poślizgu zostaną przesunięte w tym samym kierunku, równolegle do granicy tego przesunięcia , to ona stanowi dyslokację śrubową. Efektem dyslokacji śrubowej jest charakterystyczne zniekształcenie sieci kryształu polegające na tym, że płaszczyzny atomowe prostopadłe do linii dyslokacji tworzą powierzchnię śrubową, przy czym dyslokacja jest jej osią. W zależności od kierunku skręcenia płaszczyzn atomowych dyslokacje mogą być prawo lub lewoskrętne. Mówi się, że są to dyslokacje przeciwnych znaków, gdyż jeśli są równoległe przyciągają się, a po spotkaniu ulegają anihilacji. Dyslokacje tego samego znaku odpychają się. Dyslokacje śrubowe mogą przemieszczać się przez poślizg po każdej płaszczyźnie, na której znajduje się dyslokacja, ale nie mogą się wspinać.
**Na czym polega różnica między dyslokacją krawędziową i śrubową?
Jeśli jako podstawę definicji dyslokacji przyjmiemy orientację tzw.wektora Burgersa b (co do wielkości równego najbliższej odległości międzyatomowej w kierunku poślizgu) względem kierunku dyslokacji, to okazuje się, że różnica między dyslokacjami jest głównie ilościowa. W przypadku dyslokacji krawędziowej kąt między linią dyslokacji i b jest równy 90°, a dla dyslokacji śrubowej jest równy zeru. Różnice w orientacji b mają jednak swe konsekwencje w zróżnicowaniu własności dyslokacji, głównie w charakterze pól naprężeń, możliwości ruchu, oddziaływania z defektami punktowymi i inn. Jeśli kąt ten jest zawarty między 0 i 90° mamy do czynienia z dyslokacją mieszaną. Dyslokacja taka może być jednakże rozłożona na składowe krawędziowe i śrubowe.
Co to jest wektor Burgersa dyslokacji i jak się go wyznacza?
Wektor Burgersa wskazuje kierunek i wielkość przesunięcia atomów przy powstawaniu lub ruchu dyslokacji. Wektor Burgersa jednoznacznie charakteryzuje dyslokację. Dla tej samej dyslokacji, b ma wartość stałą. Kierunek, zwrot i wielkość wektora Burgersa można wyznaczyć za pomocą tzw. obwodu Burgersa. Najpierw w pobliżu dyslokacji wybieramy jeden atom jako punkt początkowy obwodu (np.atom A). Następnie przesuwamy się od tego atomu w kierunku zgodnym z ruchem wskazówek zegara od atomu do atomu o taką samą liczbę odległości międzyatomowych, parami we wzajemnie równoległych, ale przeciwnych kierunkach, zakreślając zamknięty obwód. W przypadku gdy wewnątrz zakreślonego obwodu znajduje się dyslokacja, to obwód nie zamyka się i odcinek domykający BA stanowi wektor Burgersa tej dyskolacji. Zwrot wektora Burgersa jest zgodny z kierunkiem wykreślania obwodu.. Wektor Burgersa i linia dyslokacji wyznaczają płaszczyznę poślizgu dyslokacji. Dla dyslokacji krawędziowej jest to jedna płaszczyzna, dla śrubowej wiele płaszczyzn równoległych do linii dyslokacji.
8. Na czym polega zjawisko dyfuzji?- Monika Romankiewicz
Dyfuzja - jest to samorzutne przenikanie cząsteczek jednej fazy układu w głąb fazy drugiej, spowodowane bezładnym ruchem cieplnym, a także większych cząstek zawieszonych w płynach. Dyfuzja zachodzi w każdej temperaturze. Obserwujemy ją pomiędzy gazami, cieczami i ciałami stałymi. Szybkość dyfuzji wzrasta przy podwyższaniu temperatury.
Przenikanie cząsteczek lub cząstek może być:
jednokierunkowe (dyfuzja jednokierunkowa),
dwukierunkowe (dyfuzja dwukierunkowa).
Zjawisko to uwarunkowane jest stężeniem na granicy zetknięcia dwóch faz i prowadzi do wyrównania stężeń w układzie oraz do utworzenia - jeśli jest to możliwe - jednorodnych mieszanin (roztworów) stałych, ciekłych i gazowych.
Dyfuzja jednokierunkowa - zachodzi w procesach obróbki cieplnej jak nawęglanie i azotowanie stali, przy tworzeniu się roztworów stałych metali, przy przenikaniu gazów przez metale, przy pochłanianiu gazu w cieczy oraz zjawiskach osmozy.
Przykładami dyfuzji dwukierunkowej są: nieograniczone mieszanie się gazów, tworzenie się roztworów ciekłych w granicach rozpuszczalności lub wzajemnej mieszalności składników.
Dyfuzję można zaobserwować na różnych przykładach np. jeśli położymy na sobie płytkę złota i srebra to po upływie kilkunastu miesięcy można zauważyć w złocie cząsteczki srebra i na odwrót.
9. Co to są defekty powierzchniowe, granice międzyfazowe? - Sandra Jastrzębska
Defekty sieci krystalicznej - niedoskonałości kryształów polegające na punktowym lub warstwowym zerwaniu regularności ich sieci. Defekty występują praktycznie we wszystkich rzeczywistych kryształach. Wynikają one z natury procesu krystalizacji.
1. Punktowe:
- wakansy - wolne miejsca w sieci krystalicznej,
- wyjście atomu na powierzchnie kryształu,
- atomy międzywęzłowe - opuszczające węzły na wskutek drgań cieplnych,
2. Liniowe - inaczej dyslokacje:
- krawędziowe - poprzez wprowadzenie ekstrapłaszczyzny między nieco rozsunięte płaszczyzny sieciowe, miarą dyslokacji jest wektor Burgersa, wyznaczony poprzez kontur Burgersa i prostopadły do linii dyslokacji krawędziowej,
- śrubowe - powstają w wyniku przesunięcia płaszczyzn atomowych, wektor Burgersa równoległy do linii dyslokacji śrubowej,
- mieszane - liniowa i krawędziowa występujące w strukturach rzeczywistych,
3. Defekty powierzchniowe
Wyróżniamy tutaj:
Błędy ułożenia,
Powierzchnie wewnętrzne kryształów (np. granice ziaren, granice bliźniaków i granice międzyfazowe),
Powierzchnie zewnętrzne kryształów.
Błędy ułożenia:
Jeśli rozważymy problem gęstego upakowania kul, to okazuje się, że istnieją tylko dwie możliwości.
Poniżej przedstawiono je schematycznie:
Możliwe sposoby gęstego upakowania kul. Kule pierwszej warstwy znajdują się w położeniach A, środki kul drugiej warstwy umieszczamy w położeniach oznaczonych jako B.
Trzecią warstwę kul możemy umieścić:
- w położeniach C (następnie powtarzając procedurę od początku, uzyskujemy ułożenie ABC ABC .....),
- w położeniach B (następnie powtarzając procedurę od początku, uzyskujemy ułożenie AB AB ....)
Te sposoby upakowania atomów, traktowanych jako sztywne kule, realizowane są w przyrodzie w dwóch strukturach krystalograficznych:
- w regularnej płasko centrowanej (RPC), gdzie występuje sekwencja warstw atomowych ABC ABC ABC .....,
- w heksagonalnej zwartej (HZ), gdzie występuje sekwencja warstw atomowych AB AB AB ....
Na poniższych rysunkach przedstawiono ułożenie atomów w obu tych strukturach.
Ułożenie atomów w krysztale RPC jest sekwencją ułożenia płaszczyzn gęstego upakowania {111}.
Rozważmy teraz ścinający ruch jednej warstwy atomowej względem drugiej, który występuje w zjawisku poślizgu kryształu. Przemieszczenie to możemy opisać jako ruch dyslokacji “doskonałej”, która w sieci RPC opisana jest wektorem Burgersa: b=
.Pokazano to na górnej części poniższego rysunku (atomy warstwy górnej zaznaczono linia przerywaną). Jednak od razu można zauważyć, że będzie istniała tendencja do łatwiejszego ruchu atomów, pokazanego na rysunku dolnym.
12. Co to są dendryty, wiskery i szkło metaliczne?-Marta Czopek
SZKLO METALICZNE: CIAłO AMORFICZNE (struktura posrednie między stanem krystalicznym a stanem ciekłym). Podczas gdy atomy w metalu są uporządkowane w określone grupy, atomy w szkle metalicznym są rozmieszczone przypadkowo, podobnie jak te w cieczach. Pierwszym twórcą metody produkcji stopów metali o strukturze podobnej do struktury szkła był Pol Duwez z California Institute of Technology w Pasadenie, który stworzył ten materiał w 1960 roku . Szkła te przez analogię nazwano później szkłami metalicznymi. Powstają w stopach metali z udziałem niemetali, utworzonych z atomów o zróżnicowanych wielkościach. Aby wytworzyć taki materiał niezbędne jest niezwykle szybkie schłodzenie ciekłego stopu. Otrzymuje się je w postaci taśm o szerokości do 12 mm, drutów lub proszków. Ta nowa grupa materiałów ma bardzo interesujące właściwości magnetyczne i mechaniczne, lepsze niż materiały polikrystaliczne, tradycyjnie stosowane w technice. Poza tym są to materiały odporne na działanie środowiska. Szkła metaliczne stosowane są w elektronice, energetyce i przemyśle lotniczym zastępując dominujące dotychczas materiały krystaliczne. Szkło metaliczne z pewnością jest o wiele bardziej wytrzymałe od innych metali. Topi się w bardzo niskich temperaturach i może być formowany przez nas prawie jak plastik.
DENDRYTY:Wydzielanie się utajonego ciepła krzepnięcia na granicy międzyfazowej kryształu i znacznie przechłodzonej cieczy jest wzrost jej temp. gradient temp. w cieczy jest wtedy ujemny. Jeżeli na granicy międzyfazowej powstanie jakakolwiek wypukłość wzrasta ona w kierunku zwiększającego się przechłodzenia cieczy. Warunki takie sprzyjają wzrostowi dendrytycznemu w kształcie "choinek". Ponieważ na powierzchniach dendrytów temp. jest wyższa niż między nimi, płaskie powierzchnie graniczne są niestabilne, co decyduje o tworzeniu się bocznych gałęzi. Każde rozgałęzienie rośnie do chwili utraty stabilności jego granicy, co staje się początkiem wzrostu kolejnych rozgałęzień. Kierunek wzrostu dendrytów i ich rozgałęzień jest zgodny z kierunkiem osi piramidy utworzonej przez płaszczyzny najczęściej osadzone atomami tworzących się kryształów. W sieciach regularnych i tetragonalnych osie dendrytów są wzajemnie prostopadłe, natomiast w sieciach heksagonalnych nachylone pod kątem 60 stopni. W tablicy 4-1 podano uprzywilejowane kierunki wzrostu dendrytów w zależności od typu sieci przestrzennej tworzących się kryształów. Krystalizacja dendrytów w cieczy metalicznej kończy się gdy wydzielające się ciepło krzepnięcia spowoduje wzrost temp. cieczy i kryształu do temp. równowagi. Powstały ciekły metal krystalizuje już wyłącznie w wyniku doprowadzania utajonego ciepła krzepnięcia przez utworzoną fazę stałą. Wówczas wypełnieniu ulega przestrzeń międzydendrytyczna, a proces krystalizacji w tych obszarach przebiega znacznie wolniej niż wzrost dendrytów.
WISKERY - cienkie włókna ceramiczne albo monokryształy Zastosowanie:
- składnik kompozytowy do wzmacniania tworzyw;
- odpowiedzialne elementy samolotów i rakiet.
- elementy spowalniające - np. związki berylu
Służą do spowalniania szybkich neutronów do prędkości, przy których występuje szczególnie wielkie prawdopodobieństwo rozszczepienia jądra atomowego.
- elementy absorpcyjne - np. węglik boru
Służą one zarówno do regulacji lub wyłączania reaktora, jak też do ekranowania.
13. Co to jest plastyczność metali omówić mechanizmy i metody odkształcenia plastycznego- Jarek Gawroński
Plastyczność metali (kowalność) jest to zdolność metali do odksztłcenia się podczas obróbki polegającej na wywieraniu narzędziem na obrabiany materiał nacisku przekraczającego granicę jego plastyczności, mającego na celu trwałą zmianę kształtu i wymiarów obrabianego przedmiotu .Kowalność określa się na podstawie prób technologicznych np rozpłaszczania do określonych wymiarów. Powstanie pęknięć świadczy o złej kowalności i dyskwalifikuje materiał.
Metody:
Odkształcenie plastyczne następuje przez poślizg lub bliźniakowanie.
Poślizg jest to przesunięcie się jednej części kryształu względem drugiej. Poślizg w metalach zachodzi w określonych płaszczyznach oraz kierunkach.. Płaszczyzna poślizgu przy odkształcaniu na zimno jest zwykle płaszczyzną kryształu najgęściej obsadzona atomami, a kierunkiem poślizgu - kierunek o największej gęstości atomów. Metale i stopy o podobnej strukturze krystalicznej posiadają takie samy systemy poślizgów;
Poślizg następuje na skutek działania siły stycznej, równoległej do płaszczyzny poślizgu.
Bliźniakowanie polega na obrocie i przesunięciu części kryształu wzdłuż określonego kierunku w taki sposób, aby ułożenie atomów w części przesuniętej było lustrzanym odbiciem ułożenia atomów w części nie przesuniętej.
Bliźniakowanie powoduje zmianę orientacji pasma bliźniaczego w stosunku do pozostałej części kryształu.
14. Na czym polega zjawisko bliźniakowania w obróbce plastycznej? - Piotrek Szymański
Bliźniakowanie - polega na jednorodnym ścinaniu o wektor bliźniakowania kolejnych warstw atomów w płaszczyznach bliźniakowania. Podczas bliźniakowania, pod działaniem naprężenia stycznego, następuje przesunięcie względem siebie kolejnych warstw atomowych wskutek ruchu poślizgowego części dyslokacji. Zbliźniakowane części kryształu względem płaszczyzny bliźniakowania są identyczne. Zbliźniakowana część kryształu ulega skręceniu względem części nieodkształconej w taki sposób że ich struktury krystaliczne są symetryczne osiowo względem płaszczyzny bliźniakowania.
15. Co to jest nadplastyczność, zgniot?- Marta Juda
Nadplastyczność - zdolność metali i ich stopów do dużych odkształceń plastycznych.
Zgniotem określa się zmiany, jakie zachodzą w strukturze i właściwościach metali pod wpływem odkształcenia plastycznego na zimno. Zgniot zachodzi poniżej temperatury rekrystalizacji, gdyż szybkość procesów dyfuzyjnych jest mała.
16. Na czym polega zjawisko rekrystalizacji, zdrowienia, poligonizacji?- Sylwia Parol
Rekrystalizacja proces zachodzący w metalach podczas wyżarzania rekrystalizującego, którego efektem jest odbudowa struktury krystalicznej metalu po zgniocie i przywrócenie mu pierwotnych właściwości fizycznych i mechanicznych.
Zdrowienie w czasie wygrzewania odkształconego plastycznie metalu można zaobserwować że w pewnej temp następuje usunięcie zniekształceń sieci krystalicznej zjawisko to nosiu nazwę zdrowienia.
Poligonizacja występuje w wyższych temp niż zdrowienie; Dyslokacje które w zgniecionym metalu rozmieszczone są w sposób nieuporządkowany przemieszczają sie wzdłuż płaszczyzny łatwego poślizgu grupując sie w rzędach. Proces ten prowadzi do powstawania granic subziarn tj obszarów o nieznacznie różniącej się orientacji krystalograficznej. W ten sposób ziarna zgniecionego metalu rozpadają się na szereg subziarn skręconych względem siebie o niewielkie kąty paru minut.
18. Co to są stopy, roztwory stałe, graniczne, ciągłe, domeny antyfazowe? -Aga Stępień
Stopy-substancje dwu-lub wieloskładnikowe, makroskopowe wykazujące własności metaliczne. Co najmniej jeden z głównych składników stopu jest metalem. Składnikami stopów są substancje proste(pierwiastki) lub złożone - np.. związki nie ulegające przemianom.
Stopy metali charakteryzują się wiązaniem metalicznym.
Skład chemiczny stopów jest wyrażany przez:
-stężenie masowe składników
-stężenie atomowe składników
Stopy mogą mieć strukturę jedno-lub wielofazową. Liczba rodzaj i własności faz są uzależnione od składu chemicznego stopu.
Roztwory stałe-stanowią jednorodną fazę o wiązaniu metalicznym i strukturze krystalicznej o własnościach typowo metalicznych. Mogą być:
-podstawowe(rozpuszczalnikiem jest pierwiastek będący składnikiem stopu)
-wtórne(rozpuszczalnikiem jest faza między metaliczna).
W zależności od zakresu stężenia składnika rozpuszczonego roztwory stałe dzielimy na:
-graniczne
-ciągłe
Dodatkowo ze względu na rozmieszczenie atomów składnika rozpuszczonego, dzielimy na:
-międzywęzłowe(atomy pierwiastka rozpuszczonego są usytuowane w sposób nieuporządkowany w przestrzeniach międzywęzłowych sieci metalu rozpuszczalnika)
-różnowęzłowe(atomy metalu rozpuszczonego zajmują przypadkowo dowolne węzły w sieci krystalicznej metalu rozpuszczalnika)
Roztwór stały graniczny-występuje wtedy, gdy stężenie składnika rozpuszczonego jest ograniczone w pewnym zakresie.
Roztwór stały ciągły-występuje w przypadku nieograniczonej rozpuszczalności obydwu składników w stanie stałym w całym zakresie stężeń tj. od 0 do 100%
19. W jakich stopach występują nadstruktury?- Roksana Glinka
Nadstruktury to dwuskładnikowe roztwory stałe, w kórych wyniku powolnego, chłodzenia lub wyżarzania nastąpiło uporządkowanie przedtem chaotycznie rozmieszczonych atomów. Występują w stopach miedzi ze złotem, miedzi z platyną, miedzi z niklem i żelazem, kobaltu z wanadem i żelazem.
20. co to jest regula faz (liczba stopni swobody)? -Bartek Rogalski
Reguła Faz Gibbsa - reguła określająca liczbę faz f mogących współistnieć w stanie równowagi fazowej układu o n składnikach i s stopniach swobody. Matematycznie wyrażona jest wzorem: f = n - s + 2. Stopniami swobody nazywa się liczbę parametrów stanu (zmiennych niezależnych), które mogą zmieniać się niezależnie od siebie, bez naruszenia stanu równowagi układu. Dla układu o n składnikach, znajdującego się w stanie równowagi, największa liczba faz może występować, gdy s przyjmuje wartość najmniejszą, czyli 0 (zero). Np. dla układu jednoskładnikowego, tj. czystej substancji (np.wody), f = 1 + 2 = 3 przy s = 0 w równowadze termodynamicznej mogą występować jednocześnie trzy fazy - zakładając, że do opisu układu wystarczą dwa parametry np. ciśnienie i temperatura - tylko w ściśle określonej temperaturze i przy ściśle określonym ciśnieniu (dla wody temp. T =273,16 K, ciśnienie p = 610,7 Pa). Zmiana któregoś z tych parametrów spowoduje przejście jednej z faz w inną z dwóch pozostałych, gdyż przy s=1 mogą występować w równowadze tylko dwie fazy. W przypadku
substancji dwuskładnikowych (np. roztwory) w równowadze termodynamicznej mogą występować jednocześnie najwyżej 4 fazy (f = 2 + 2 = 4). Reguła Faz Gibbsa została opracowana 1874 przez fizyka amer.
J.W. Gibbsa. Stosuje się ją w formie uogólnionej także do skomplikowanych układów, w których zachodzą reakcje chemiczne w postaci f = n - s + 2 - r, gdzie r - ilość reakcji chemicznych
zachodzących w układzie.
21. Co to jest i do czego słuzy reguła dźwigni??- Kasia Kowalska
Reguła dźwigni (reguła odcinków) - służy do określania procentowego lub wagowego udziału faz w stopie przy danej temperaturze w stanie równowagi.
W procesie krystalizacji zarówno pierwotnej jak i wtórnej( w stanie stałym)zmienia się nie tylko skład poszczególnych faz , ale i ilość każdej fazy. W dowolnym punkcie wykresu równowagi można w obszarze jednoczesnego występowania dwóch faz określić ich ilość oraz ich skład chemiczny za pomocą reguły dźwigni.
Ilościowy stosunek poszczególnych faz określa się za pomocą wzorów(stosunek odpowiednich odcinków), które obrazują zawartość poszczególnych faz.
W tym celu zakładamy że odległość mierzona według prostej poziomej między poszczególnymi fazami wynosi wagowo 1 (100%). Wówczas poszczególne odcinki poziome mierzone w tej samej skali mają się do siebie w stosunku odwrotnym do zawartości procentowej poszczególnych faz lub składników
22. Co to są stopy podeutektyczne i nadeutektyczne? - Joanna Kalinowska
Stopy podeutektyczne i nadeutektyczne są to stopy odlewnicze aluminium z krzemem( nazywane siluminami) Stopy te wyróżniamy na podstawie zawartości krzemu w danym stopie.
Stopy podeutektyczne zawierają od 4 do 10 % krzemu
Stopy nadeutektoidalne zawierają od 13 do 30% krzemu
24. Jaka jest różnica pomiędzy przemianą eutektyczną i perytektyczną?-Mateusz Borowski
W dwuskładnikowym układzie równowagi fazowej w przypadku przemiany eutektycznej mamy do czynienia z wtórną krystalizacją tzn. powstają kryształy (α, β) które są czystymi kryształami składników; w przypadku przemiany perytektycznej dochodzi do reakcji cieczy z wcześniej wydzielonymi kryształami- powstają inne kryształy (ciecz + α → β)
23. Jakie własności mają stopy eutektyczne? - Karolina Gałaj
Eutektyk, mieszanina eutektyczna - mieszanina dwóch lub więcej składników strukturalnych stopu (faz kryształów) o określonym składzie chemicznym, która wydziela się z roztworów ciekłych lub stopów w określonej temperaturze zwanej temperaturą eutektyczną. Temperatura eutektyczna jest na ogół znacznie niższa od temperatury krzepnięcia czystych składników. Kryształy mieszaniny eutektycznej są bądź czystymi kryształami składników, bądź też roztworami stałymi o różnych składach. W tym ostatnim przypadku mówi się o eutektykach roztworów stałych. W zależności od ilości składników rozróżnia się eutektykę podwójną, potrójną itd.
Stopy eutektyczne mają następujące właściwości:
1. Stała temperatura krzepnięcia (najmniejsza w układzie)
2. Stały skład chemiczny
3. Drobnoziarnistość (dobre właściwości mechaniczne)
25. Co to jest trójkąt Gibasa? - Magdalena Sobczyk
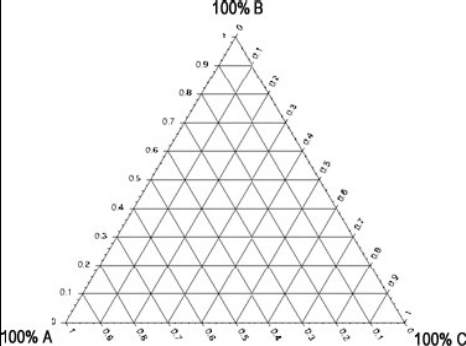
Trójkąt Gibbsa. Nazywany inaczej trójkątem składu - przedstawia początkowy skład danego stopu. Jest to trójkąt równoboczny. Każdy wierzchołek odpowiada zawartości 100% czystego pojedynczego składnika A,B i C ,boki trójkąta opisują skład procentowy lub częściej ułamki molowe zawartości par składników(stopom podwójnym), odpowiednio: AB, AC i BC, punkty wewnątrz trójkąta odpowiadają stopom potrójnym Trójkąt Gibbsa pozwala na przedstawienie dowolnego stopu zawierającego do 3 składników. Współrzędne każdego punktu wyznaczają bezpośrednio skład stopu .Miejsce przecięcia się trzech prostych prostopadłych do boków trójkąta z tymi bokami, gdy są one poprowadzone taki sposób aby wszystkie trzy przecinały się w jednym punkcie wewnątrz trójkąta, wyznacza rzeczywiste stężenie składników dla tego punktu.
Na wykresie zaznacza się tzw. binody czyli krzywe graniczne rozpuszczalności odpowiednich par składników, dzięki czemu można w prosty sposób odczytać z trójkąta, czy przy określonym stężeniu składników A, B, C układ będzie jedno, dwu czy trójfazowy.
Trójkąty Gibbsa są zawsze rysowane dla określonej temperatury i ciśnienia. Trójkąt Gibbsa dla tego samego układu w innej temperaturze albo ciśnieniu może mieć zupełnie inny przebieg.
26. Co to są stale węglowe? Kasia Adamczyk
Stal węglowa - stop węgla z żelazem (najczęściej do ok. 1,5% C), stal, w której pierwiastkiem kształtującym jej charakterystyki jest węgiel.
Stal węglowa stosowana jest powszechnie przy wytwarzaniu konstrukcji oraz części urządzeń mechanicznych, wszędzie tam, gdzie jej charakterystyki są wystarczające.
Stale węglowe dzieli się na:
stale węglowe zwykłej jakości ? stosowane bez dodatkowej obróbki
stale węglowe podwyższonej jakości ? często poddawane dodatkowej obróbce cieplnej lub chemicznej.
W zależności od zawartości węgla dzielimy je na:
stale niskowęglowe - o zawartości węgla do około 0,3%
stale średniowęglowe - o zawartości od 0,3 do 0,6%
stale wysokowęglowe - o zawartości powyżej 0,6%
W zależności od zawartości zanieczyszczeń P i S dzielimy je na:
stale zwykłej jakości - P + S = 0,10%
stale wyższej jakości - P + S = 0,07%
stale najwyższej jakości - P + S = 0,03%
W zależności od stopnia odtlenienia stale dzielimy na:
stale uspokojone - najczęściej wyższej i najwyższej jakości
stale półuspokojone
stale nieuspokojone
stale niestarzejące się - uspokojone
W zależności od zastosowania stale dzielimy na:
stale konstrukcyjne
stale narzędziowe
stale o szczególnych właściwościach fizycznych i chemicznych
27. Jakie dodatki zawierają stale węglowe? - Justyna Ryczkowska
Pierwiastki wpływające korzystnie na właściwości stali:
1.Mangan- odtlenienie stali, związanie siarki, zwiększenie hartowności, umocnienie stali
2.Krzem- odtlenienie stali, umocnienie ferrytu, zwiększenie oporu elektrycznego oraz zmniejszenie stratności stali magnetycznie miękkich. Poprawia żaroodporność stali i powoduje korzystne obniżenie stężenia gazów stali lanej oraz przeciwdziała segregacji fosforu i siaki.
3.Nikiel- umocnienie stali poprzez roztwór, zwiększenie hartowności, obniżenie temperatury przejścia stali w stan kruchy i stabilizacja austenitu w stalach nierdzewnych i żaroodpornych.
4.Chrom- zwiększenie hartowności, odporność na ścieranie, korozję i utlenianie
5.Molibden- zwiększenie hartowności, wywołanie twardości wtórnej, odporność na ścieranie
6.Miedź- poprawia odporność na korozję
7.Bor-poprawia hartowność
Pierwiastki wpływające niekorzystnie na właściwości stali:
1.Fosfor-podwyższenie temperatury przejścia w stan kruchości, gruboziarnistość i segregacja
2.Siarka- kruchość stali na gorąco, pogarsza spawalność i wytrzymałość stali na zmęczenie
3.Wodór- powstawanie płatków śnieżnych, odwęglanie, segregacja fosforu
4.Azot- zmniejszenie plastyczności i kruchości, zwiększenie skłonności stal do starzenia
5.Tlen- zmniejszenie własności wytrzymałościowych oraz plastycznych
29. Co to jest ferryt, austenit, perlit, ladebutyt, cementyt? - Piotrek Szymański
Ferryt - roztwór stały węgla w żelazie α zawierający niewielkie ilości, mniejsze niż 0,025%, węgla oraz niekiedy inne dodatki stopowe. Wypolerowany przekrój ferrytu oglądany pod mikroskopem w powiększeniu x250 pokazuje strukturę ziarnistą, posiadającą jasnoszary kolor. Jako że cała zawartość węgla rozpuszczona jest w sieci krystalicznej żelaza, nie jest widoczny jako oddzielna faza. Ferryt, jest to jedna z możliwych odmian alotropowych stali, stabilna do temperatury przemiany eutektoidalnej (układ żelazo-węgiel) - do temp. 770 °C, jest materiałem miękkim i ciągliwym, mniej wytrzymały, twardy i plastyczny niż austenit. Ferromagnetyk o temperaturze Curie wynoszącej 770 °C, zaś powyżej jej jest paramagnetykiem. Wytrzymałość RM - 300MPa, twardość - 80HB, plastyczność A10 - 40%, udarność KC -180J/ cm2 .
Austenit - międzywęzłowy roztwór stały węgla oraz niekiedy innych dodatków stopowych w żelazie γ (gamma). Rozpuszczalność węgla w austenicie bez dodatków stopowych nie przekracza 2,11% (w temperaturze ok. 1150°C). Austenit nie zawierający poza węglem innych dodatków stopowych jest stabilny tylko w temperaturach powyżej 723°C (tzw. punkt eutektoidalny). Austenit schłodzony poniżej tej temperatury rozpada się na mieszaninę ferrytu i perlitu, jeśli zawiera do 0,77% węgla, lub perlitu i cementytu, jeśli zawiera więcej niż 0,77% węgla. W przypadku zawartości 0,77% węgla przemienia się w perlit. Bardzo szybko schładzany austenit, przy zachowaniu pewnych warunków, może nie ulec rozpadowi na opisane wyżej mieszaniny, tylko przemienić się w martenzyt. Duże ilości dodatków stopowych, takich jak nikiel, obniżają temperaturę przemiany austenitycznej tak, że austenit pozostaje stabilny w normalnych temperaturach. Austenit jest bardziej wytrzymały i bardziej plastyczny niż ferryt. Jest paramagnetykiem.
Perlit - mieszanina eutektoidalna ferrytu z cementytem zawierająca 0,77% węgla. Powstaje podczas przemiany eutektoidalnej w temperaturze 727°C. Nazwę swą zawdzięcza perlistemu odcieniowi, jaki posiada wypolerowany przekrój tego stopu. Perlit ma budowę ziarnistą. Pojedyncze ziarno perlitu zbudowane jest z płytek (w przekroju widocznych jako linie) ferrytu i cementytu ułożonych na przemian. Przy odpowiednim powiększeniu mikroskopowym (zwykle x250 do x500) widoczna jest wewnętrzna struktura perlitu, przy czym jasnoszare linie reprezentują ferryt, podczas gdy ciemnoszare cementyt. Wytrzymałość RM - 700-800MPa, twardość 180-220 HB, plastyczność A10 - 8%, udarność 40J/cm2
Ledeburyt - mieszanina eutektyczna austenitu z cementytem (lub ferrytu z cementytem - ledeburyt przemieniony) , zawierająca 4,3% węgla. Ledeburyt powstaje w krzepnącym ciekłym roztworze żelaza z węglem, gdy zawartość węgla jest w granicach 2,06% - 6,67%, w temperaturze 1147°C. Dla zawartości węgla mniejszej niż 4,3% stop zawiera austenit i ledeburyt, przy równej - tylko ledeburyt i jest eutektykiem, a powyżej ledeburyt i cementyt. Ledeburyt jest stabilny do temperatury 727°C, poniżej której rozpada się austenit. Ledeburyt przechodzi wtedy w tzw. ledeburyt przemieniony. Staje się wtedy podwójną eutektyką. Pierwotnie występujący w niej cementyt, zachowuje swą formę, a austenit rozpada się na mieszaninę perlitu i cementytu. Strukturę tę można ujednolicić przez wyżarzanie.
Cementyt - (węglik żelaza, Fe3C) - jedna z podstawowych faz międzymetalicznych z grupy węglików, występującą w stopach żelaza z węglem i innymi pierwiastkami. Cementyt jest jednym ze składników stali; jest materiałem twardym i kruchym, posiada strukturę krystaliczną rombową, jego twardość to około 65 HRC (800 HB), jest fazą metastabilną o zawartości węgla do 6,67%. Posiada liczne wiązania metaliczne, co sprawia, że posiada własności metaliczne. W temp 210 jest ferromagnetykiem, zaś powyżej 210 jest paramagnetykiem. W zależności od zawartości węgla w stopie można rozróżnić:
cementyt pierwotny, wydzielający się przy krzepnięciu stopów o zawartości 4,3-6,67% węgla z roztworu ciekłego ubożejącego w węgiel, w postaci grubych igieł
cementyt trzeciorzędowy, wydzielający się z ferrytu na skutek obniżania się w nim rozpuszczalności węgla wraz ze spadkiem temperatury.
Cementyt jest odporny na działanie czynników chemicznych, trudno trawi się nitalem (Mi1Fe). Dla ujawnienia cementytu w stopach żelaza stosuje się trawienie na gorąco pikrynianem sodu (Mi6Fe), który barwi cementyt na brunatno lub czarno. Cementyt może tworzyć roztwory stałe różnowęzłowe i na miejscu atomów węgla mogą wchodzić atomy azotu, zaś na miejsce atomów żelaza atomy manganu, chromu, wolframu.
30.Jaki jest wpływ węgla i innych dodatków na własności stali? Izabela Łapińska
Stale nie są czystymi stopami żelaza z węglem, lecz zawierają pewne ilaści dodatków, uwarunkowanych względami technologicznymi (np. mangan, krzem, aluminium), które są wprowadzane w celu lepszego odtlenienia lub odsiarczenia stali. Inne pierwiastki jak S, P, O, H, N pozostają w stali w nieznacznych ilościach, gdyż ich całkowite usunięcie byłoby bardzo kosztowne i nieopłacalne. Pomimo, że występują w małych ilościach, wywierają one jednak istotny wpływ na własności stali. Niektóre pierwiastki dostają się do stali przypadkowo, najczęściej ze złomu. Są to np. Ni, Cu, Cr, których ilość w stalach węglowych jest również ograniczona.
Węgiel - (stale węglowe dzieli się na 3 grupy: niskowęglowe (poniżej 0,25°/o C), średniowęglowe (0,25-0,6% C) i wysokowęglowe (powyżej 0,6% C).
Wzrost zawartości węgla w stali powoduje zmniejszenie zawartości miękkiego składnika strukturalnego (ferrytu), a zwiększenie - twardego cementytu. Zawartość %C rośnie to maleje: udarność (U) i własności spawalnicze aż do całkowitej niespawalności
W związku z tym własności wytrzymałościowe stali węglowych zwiększają się ze wzrostem zawartości węgla, podczas gdy własności plastyczne maleją.
Węgiel obniża temperaturę topnienia. Podwyższa wytrzymałość doraźną i granicę plastyczności, obniża wydłużenie i przewężenie podczas rozciągania.
Węgiel umożliwia hartowanie stali, zmniejsza przewodność cieplną i gęstość, pogarsza spawalność stali, powodując pęknięcia hartownicze.
Siarka przedostaje się do stali z rud lub paliwa. Normalna zawartość siarki wynosi poniżej 0,05%, a w stalach o wysokiej jakości w granicach 0,02-0,03%. Z układu równowagi Fe-S wynika, że nie rozpuszcza się ona w żelazie, natomiast tworzy siarczek żelazawy FeS, który wchodzi w skład eutektyki o temperaturze topnienia znacznie niższej niż żelaza (988°C). Ponieważ eutektyka(mieszanina dwóch lub więcej faz krystalicznych o określonym składzie) ta wydziela się głównie na granicach ziaren austenitu, powoduje ona osłabienie stali w temperaturze czerwonego żaru (powyżej 800°C) i uniemożliwia jej obróbkę plastyczną na gorąco. Powyżej 12000C stal jest również łamliwa, gdyż wtedy FeS topi się - zjawisko to nazywa się kruchością na gorąco. Siarka zmniejsza spawalność i pracę uderzenia i jeszcze bardziej niż fosfor powoduje skłonność do segregacji. Siarka może powodować wystąpienie struktury pasmowej .
Krzem przechodzi do stali z kwaśnego obmurza pieca lub żużla, względnie jest do stali dodawany przy odtlenieniu. Występuje ze względów technologicznych. Nie wpływa widocznie na własności stali ( poza stalami specjalnymi na rdzenie transformatorów). Powstający przy tym SiO2 wiąże się zazwyczaj z innymi tlenkami na twarde i kruche krzemiany. Przy rozwalcowywaniu stali krzemiany są rozdrabniane i układają się w pasma (struktura włóknista).
Krzem w stali podwyższa wytrzymałość i twardość, zmniejsza jednak znacznie wydłużenie względne przy rozciąganiu, a zatem plastyczność podczas obróbki plastycznej na zimno. Z tego powodu głęboko ciągnione blachy nie powinny zawierać powyżej 0,2 % Si. Krzem występujący w niewielkich ilościach utrudnia spawanie, szczególnie spawanie gazowe.
Mangan służy do odtleniania i uspokajania stali, Stosowany jako odtleniacz. Zmniejsza skłonność do kruchości w podwyższonych temperaturach. Podwyższa twardość i wytrzymałość. Tworzy również wiązania siarki w trudno topliwy siarczek manganu- MnS. Mn i MnO występujące w większych ilościach, powodują powstawanie struktury włóknistej, a tym samym znaczny spadek pracy uderzenia w próbie udarności w kierunku poprzecznym do walcowania.
Fosfor dostaje się do stali, podobnie jak siarka, z rudy. Zwykle zawartość fosforu w stalach wynosi ok. 0,05%, a w stalach o wysokiej jakości 0,02- 0,03%. Fosfor nie tworzy w stali żadnej nowej fazy. Fosfor podwyższa nieznacznie odporność na korozję i odporność na ścieranie, powoduje jednak skłonność do pęknięć w strefach przejściowych spoin. Ponadto fosfor podwyższa wytrzymałość przy niewielkim spadku wydłużenie względnego przy rozciąganiu, obniża jednak silnie pracę uderzenia. Niekiedy celowo wprowadza się większe ilości fosforu w celu zwiększenia kruchości wióra w stalach automatowych i polepszenia skrawalności
Molibden
Podstawowy składnik stali perlitycznych, przeznaczonych do pracy w podwyższonych temperaturach. Powoduje wzrost odporności stali na pełzanie i relaksację. Podnosi wytrzymałość i osłabia procesy dyfuzyjne w stali. Powyżej 450oC układ stali molibdenowych przestaje być stabilny -(skłonność stali molibdenowych do grafityzacji).
Tytan (T)
Głownie Jako dodatek stabilizujący strukturę stali w stalach austenitycznych.
Wanad
Wpływa dodatnio, podwyższając odporność na pełzanie w stalach chromowo- molibdenowych:
Chrom
Dodawany do stali pracujących w podwyższonych temperaturach
-do 2.5% wzrost odporności na pełzanie i relaksację
> 2.5% spadek w/w parametrów
- jako dodatek do stali molibdenowych powoduje znaczny wzrost wytrzymałości i odporności na pełzanie w podwyższonych temperaturach.
>1.5% - dla poprawy własności antykorozyjnych
w stalach molibdenowych - dla stabilizacji struktury i obniżenia skłonności do grafityzacji.
Nikiel (N)
Podnosi odporność chemiczną (antykorozyjną ).
Tlen i tlenki to składniki bardzo szkodliwe, gdyż ich obecność w ilości ponad 0,003% silnie zmniejsza plastyczność. Rozpuszczalność tlenu w stanie stałym jest bardzo mała (poniżej 0,01%) i dlatego występuje on głównie w postaci tlenków. Obecność tlenków żelaza jest niepożądana, gdyż pogarszają one znacznie plastyczność stali. Stal odtlenia się wprowadzając pierwiastki o większym powinowactwie do tlenu, takie jak Si, Mn, Al. Stąd obecność w stalach oprócz manganu do 0,3% Si i 0,1% Al. Tlenki krzemu (i krzemiany mogą działać szkodliwie na skutek tworzenia struktury pasmowej i włóknistej ) manganu i tlenki aluminium mogą być przyczyną powstawania wtrąceń gniazdowych i powłokowych, które sprzyjają tworzeniu się struktury pasmowej lub bliźniaków a także (wypływają częściowo do żużla) te które pozostają w stali są kruche (np. Al2O2) i w wyniku obróbki plastycznej wyciągają się w łańcuszkowate pasma złożone z drobnych cząstek. Obniżają one własności mechaniczne stali, a zwłaszcza bardzo ujemnie wpływają na wytrzymałość zmęczeniową.
Azot zawartość azotu w kilku setnych procenta powoduje kruchość stali. Azot jest rozpuszczany w stali podczas wytopu z powietrza. Występowanie azotu w stali powoduje pojawienie się niebezpiecznego utwardzenia po zgniocie, które występuje po szybkim chłodzeniu, jak również po wolnym chłodzeniu, jeżeli stal była tylko poddana obróbce plastycznej na zimno. Występujące w roztworze atomy azotu układają się na powstałych przy odkształceniach dyslokacjach i blokują przez to płaszczyzny poślizgu. Powoduje to podwyższenie granicy plastyczności i wytrzymałości doraźnej oraz zmniejszenie wydłużenia względnego podczas rozciągania, a zwłaszcza znaczny spadek pracy uderzenia w próbie udarności i wzrost temperatury kruchości na zimno.
Wodór rozpuszczalność wodoru w żelazie jest duża i wzrasta ze wzrostem temperatury. Wodór podwyższa nieco wytrzymałość doraźna i granice plastyczności, jednak znacznie obniża wydłużenie względne i przewężenie przy rozciąganiu, powoduje kruchość. Przy chłodzeniu podczas wytwarzania stali wodór powoduje nieuspokojenie stali, które przyczynia się do powstania pęcherzy gazowych. Jeżeli chłodzenie jest dostatecznie szybkie, wodór pozostaje w roztworze, stwarzając niebezpieczeństwo wystąpienia po pewnym czasie znacznie. Wodór ma bardzo małą średnicę atomu i przedostaje się łatwo do obszarów między węzłowych sieci żelaza, tworząc roztwór stały międzywęzłowy. Ponadto atomy wodoru występują w miejscach defektów struktur w postaci molekuł H2.
31. Podział stali ze względu na stopień odtlenienia. - Ewelina Nikodemska
a) uspokojone - zawierają pierwiastki (Al., Si, Mn) o dużym powinowactwie do tlenu w takich ilościach, aby nastąpiło dalsze odtlenianie ciekłej stali, a nie zachodziła reakcja odtleniania drogą utleniania węgla we wlewnicy
b) półuspokojone - wstępne odtlenianie przeprowadza się mniejsza ilością odtleniaczy, w wyniku czego we wlewnicy występuje częściowe odtlenianie węglem rozpuszczonym w kąpieli. Wydzielający się tlenek węgla tworzy pęcherze gazowe, które kompensują częściowo skurcz przy krzepnięciu.
c) nieuspokojone - minimalna ilość pierwiastków odtleniających powoduje intensywne odtlenianie we wlewnicy drogą reakcji węgla z tlenem rozpuszczonym w żelazie. Powstaje duża ilość pęcherzy gazowych.
33. Co to są stale nietypowe,automatowe, żeliwa, staliwo? - Anna Gętka
ŻELIWO- stop odlewniczy żelaza z węglem, krzemem, manganem, fosforem, siarką i innymi składnikami zawierającymi od 2% do 3,6% węgla w postaci cementytu lub grafitu. Występowanie konkretnej fazy węgla zależy od szybkości chłodzenia. Żeliwo otrzymuje się przez przetapianie surówki z dodatkami złomu stalowego lub żeliwnego w piecach zwanych żeliwniakami. Tak powstały materiał stosuje się do wykonywania odlewów. Żeliwo charakteryzuje się niewielkim - 1,0% do 2,0% skurczem odlewniczym, łatwością wypełniania form, a po zastygnięciu obrabialnością. Wyroby odlewnicze po zastygnięciu, by usunąć ewentualne ostre krawędzie i pozostałości formy odlewniczej, poddaje się szlifowaniu. Odlew poddaje się także procesowi sezonowania, którego celem jest zmniejszenie wewnętrznych naprężeń, które mogą doprowadzić do odkształceń lub uszkodzeń wyrobu. Żeliwo dzięki wysokiej zawartości węgla posiada wysoką odporność na korozję.
Przykłady zastosowania żeliwa:
obudowa skrzyni biegów,
piece żeliwne.
STALIWO- to stop żelaza z węglem w postaci lanej (czyli odlana w formy odlewnicze), nie poddana obróbce plastycznej. W odmianach użytkowych zawartość węgla nie przekracza 1,5%, suma typowych domieszek również nie przekracza 1%. Właściwości mechaniczne staliwa są nieco niższe niż własności stali o takim samym składzie po obróbce plastycznej. Wynika to z charakterystycznych dla odlewów: gruboziarnistości i pustek międzykrystalicznych. Staliwo ma natomiast znacznie lepsze właściwości mechaniczne od żeliwa, w szczególności - jest plastycznie obrabialne, a odmiany o zawartości węgla poniżej 0,25% są również dobrze spawalne. Ze względu na skład chemiczny rozróżnia się staliwa:
węglowe - zawierające tylko składniki zwykłe i zanieczyszczenia z przerobu hutniczego
stopowe - zawierające dodatkowo wprowadzone celowo domieszki stopowe
STAL AUTOMATOWA- stal wykorzystywana do produkcji drobnych części np.: śrub, nakrętek, podkładek itp. Używana na części nie podlegające silnym obciążeniom.
Stal taka, dostarczana w postaci prętów, jest używana w automatach, które pracując przy minimalnym nadzorze ludzkim, wymagają stali tworzącej krótkie i łamliwe wióry. Zapewnia się to przez zwiększony dodatek siarki do 0,35% i fosforu do 0,15%. Siarka, tworząca z metalami kruche siarczki, najbardziej wpływa na łamliwość wiórów.
STAL NIESTOPOWA(węglowa)- stop węgla z żelazem (najczęściej do ok. 1,5% C). Stal węglowa stosowana jest powszechnie przy wytwarzaniu konstrukcji oraz części urządzeń mechanicznych, wszędzie tam, gdzie jej charakterystyki są wystarczające.
34. Co to są żeliwa sferoidalne i jak się je wytwarza? -Michał Kowalski
Żeliwo sferoidalne - żeliwo szare, w którym grafit występuje w postaci kulkowej, pod postacią sferoidalnych skupień. Uzyskuje się je w wyniku modyfikowania żeliwa o tendencji krzepnięcia jako szare, lecz o bardzo małym stężeniu siarki i fosforu. Jako modyfikatorów używa się ceru lub magnezu. W wyniku tego zabiegu grafit występuje w tych żeliwach w postaci kulistej. Skupienia te mogą występować w osnowie perlitu lub ferrytu. Żeliwo sferoidalne posiada dobre własności wytrzymałościowe. Może ulegać odkształceniu bez uszkodzeń, odporne na ściskanie i zginanie. Odporne na wysokie ciśnienia. Dzięki cieńszym ściankom rury z tego materiału są lżejsze. Dzięki swoim własnościom znalazło zastosowanie do wyrobu wałów korbowych silników spalinowych.
Skład chemiczny żeliwa sferoidalnego
posiada wyższą zawartość węgla i krzemu,
posiada ograniczoną do 0.02% zawartość siarki,
zawartość fosforu i manganu zależy od rodzaju osnowy metalowej ( dla struktury ferrytycznej-jest najmniejsza )
35. Na czym polega hartowanie stali? Wymienić rodzaje i cel stosowania.- Marta Dawidowicz
Hartowanie - uzyskanie twardszej struktury odpornej na scieranie - poprzez powstanie austenitu - pol. na podgrzaniu do temperatury przy ktorej powstaje austenit.
* Hartowanie powierzchniowe - gdy wymaga sie duzej twardosci w warstwie
wierzchniej oraz wystarczajaco wytrzymalego i plastycznego rdzenia.
cel stosowania:
-Stale konstrukcyjne, do ulepszania cieplnego o malej hartownosci i stezeniu
C > 0,4%.
W przypadku hartowania pow. podwyzszona twardosc warstwy wierzchniej zalezy
glownie od stezenia wegla w stali.
Po hartowaniu prawie wszystkie stale maja bardzo niskie wlasciwosci
plastyczne.
36. Co to jest odpuszczanie stali?- Piotr Badyra
Proces odwrotny do hartowania.
Odpuszczanie - jest zabiegiem cieplnym, któremu poddawana jest stal wcześniej zahartowana. Celem odpuszczania jest usunięcie naprężeń hartowniczych oraz zmiana własności fizycznych zahartowanej stali, a przede wszystkim zmniejszenie twardości, a podniesienie udarności zahartowanej stali.
Twardość - podatność lub odporność ciał stałych na odkształcenia powierzchni, zgniecenie jej lub zarysowanie, pod wpływem zewnętrznego nacisku.
Udarność - odporność materiału na złamanie przy uderzeniu
37. Co to jest banit i martenzyt?-Daria Minkina
Martenzyt to metastabilna faza stopu żelaza i węgla powstala podczas szybkiego schlodzenia z większą prędkością od prędkości krytycznej z temperatury , w której występuje austenit.Przemiana ta polega na przebudowie sieci RSC na sieć TPC.Martenzyt ma strukturę drobnoziarnistą,posiada strukturę listwową lub płytkową.Jest fazą bardzo twardą i kruchą,powstaje w czasie hartowania stali.
Bainit to mieszanina przesyconego ferrytu i węglikow.Powstaje w wyniku przemiany bainitycznej,która czesciowo ma charakter dyfuzyjny.Jego twardość jest mniejsza od twardości martenzytu.jest składnikiem stopów żelaza.Wyróżnia się 2 rodzaje:
Bainit górny(powstaje w wyniku przemiany zachodzącej powyżej 300stopni C)
Bainit dolny(powstaje w wyniku przemiany zachodzącej poniżej 300stopni C)
38. Co to jest hartownosc stali?- Ewa Koczyk
Hartowność stali - jest podatnością stali na hartowanie, czyli tworzenie struktury twardszej, odpornej na scieranie (struktury martenzytycznej). Na hartownośc wpływa głównie skład chemiczny stali.
Przez hartowność rozumie się głębokość na jaką stal da się zahartować. Miarą hartowności jest więc grubość strefy zahartowanej. Przy hartowaniu przedmiotów stalowych nie następuje zwykle zahartowanie na wskroś, gdyż szybkość chłodzenia jest większa na powierzchni, a mniejsza w rdzeniu.
39. Na czym polega i w jakim celu jest stosowana obróbka powierzchniowa? - Maciej Gunia
Obróbka powierzchniowa jest końcową fazą całkowitego procesu obróbki i ma na celu osiągnięcie - przy możliwie najmniejszych kosztach wytwarzania - odpowiednio dużej jakości obrobionego przedmiotu, zgodnej z wymaganymi warunkami technicznymi dotyczącymi dokładności wymiarów, dokładności kształtu i gładkości powierzchni.
Istnieją trzy podstawowe rodzaje obróbki powierzchniowej:
Obróbka bardzo dokładna występuje w tych przypadkach, gdy główny nacisk kładzie się na uzyskanie odpowiednio małych błędów wymiarowych (np, wewnętrzne powierzchnie pasowanych wciskowo tulei łożyskowych lub wewnętrzne powierzchnie gniazd łożyskowych).
Obróbka ostateczna występuje wtedy, gdy przede wszystkim chodzi o uzyskanie odpowiednio małych błędów kształtu (np.: obróbka powierzchni stołów przedmiotowych obrabiarek, skrobanych płyt traserskich i kontrolnych liniałów powierzchniowych).
Obróbka gładkościowa ma na celu głównie osiągnięcie odpowiednio dużej gładkości powierzchni (np.: polerowane powierzchnie zwierciadeł metalowych, ozdobnych elementów nadwozi samochodowych).
Wpływ obróbki powierzchniowej na właściwości użytkowe warstwy wierzchniej:
Elementy mechanizmów maszyn, szczególnie silnie obciążone i narażone na zużycie, powinny być po obróbce dokładnej poddawane obróbce powierzchniowej. Stosując różne sposoby obróbki powierzchniowej, można uodpornić elementy maszyn na: zużycie ścierne przy poślizgu, zużycie wskutek tarcia tocznego (łuszczenie, pitting), obciążenia udarowe, obciążenia cieplne, korozję atmosferyczną, korozję w wysokiej temperaturze, korozję chemiczną, erozję. Można również stworzyć lepsze warunki dla przepływu płynów.
Konstrukcja elementu i technologia jego warstwy wierzchniej mają również wpływ na inne własności użytkowe, jak: trwałość pasowania, wytrzymałość połączeń spawanych, zdolność do tłumienia drgań, szczelność, opory przepływu itp. Ustalając wymagania konstrukcyjno-eksploatacyjne należy uwzględnić w doborze własności użytkowych, że każdy ze sposobów obróbki powierzchniowej może wpłynąć na zmianę kilku cech użytkowych elementu.
40. Co to jest stal stopowa, stal sprężynowa, narzędziowa, nierdzewna i kwasoodporna? -Ola Czerska
Stal stopowa - stal, w której oprócz węgla występują inne dodatki stopowe o zawartości od kilku do nawet kilkudziesięciu procent, zmieniające w znaczny sposób charakterystyki stali. Dodatki stopowe dodaje się by:
podnieść hartowność stali
uzyskać większą wytrzymałość stali
zmienić pewne właściwości fizyczne i chemiczne stali
Stale stopowe, zwykle bardzo drogie, używane są w zastosowaniach specjalnych, tam gdzie jest to uzasadnione ekonomicznie.
Stal sprężynowa - stal używana do produkcji resorów, sprężyn i drążków skrętnych. Stale sprężynowe są stalami węglowymi zawierającymi 0.6% - 0.85% węgla stalami niskostopowymi zawierającymi dodatki krzemu, manganu, chromu i wanadu. Większość stali sprężynowych charakteryzuje się podwyższoną zawartością krzemu, która normalnie jest niepożądanym zanieczyszczeniem. W tych jednak aplikacjach jest wymaganym dodatkiem obniżającym plastyczność stali.
Stal narzędziowa - stal do produkcji narzędzi, elementów przyrządów pomiarowych oraz odpowiedzialnych uchwytów. Stale narzędziowe charakteryzują się wysoką twardością, odpornością na ścieranie, niewielką odkształcalnością i niewrażliwością na przegrzanie. Cechy te osiąga się przez wysoką zawartość węgla i odpowiednią obróbkę cieplną przy narzędziach mało odpowiedzialnych oraz użycie odpowiednich dodatków stopowych połączone z odpowiednią obróbką cieplną w przypadku odpowiedzialnych narzędzi.
Stale narzędziowe dzieli się na:
stale narzędziowe węglowe
stale narzędziowe stopowe
stale do pracy na zimno
stale do pracy na gorąco
stale szybkotnące.
Stal nierdzewna - stal odporna na działanie czynników atmosferycznych, rozcieńczonych kwasów, roztworów alkalicznych i podobnych. Nierdzewność stali uzyskuje się poprzez zwiększoną zawartość chromu. Zwiększona zawartość węgla także wpływa na wzrost nierdzewności stali, lecz zbyt duża jego zawartość powoduje kruchość stali. Stale nierdzewne podlegają obróbce cieplnej, hartowaniu i odpuszczaniu.
Stal kwasoodporna (kwasówka) - stal odporna na działanie kwasów o mniejszej mocy od kwasu siarkowego. Kwasoodporność uzyskuje się dzięki stabilizacji austenitu w normalnych warunkach, co można uzyskać dzięki wysokim zawartościom chromu (17-20%) i niklu (8-14%), oraz innych dodatków stopowych, takich jak mangan, tytan, molibden i miedź. Stale kwasoodporne stosowane są po polerowaniu. Jako że w wysokich temperaturach dodatki stopowe mają tendencję do łączenia się z węglem tworząc twarde węgliki, po spawaniu elementów wykonanych ze stali kwasoodpornych wymagana jest ich obróbka cieplna.
Stale kwasoodporne wykorzystuje się do budowy zbiorników kwasów oraz instalacji przemysłowych, do ich produkcji i dystrybucji, oraz innych instalacji zawierających kwasy, np. w przemyśle farbiarskim, przy produkcji nawozów sztucznych itp.
41. Co to są stopy metali nieżelaznych?Podaj przykłady - Monika Pyszniak
Stopy metali nieżelaznych, stopy, w których żelazo nie stanowi głównego
składnika i może być najwyżej składnikiem stopowym. Najliczniejszą
grupę wśród stopów metali nieżelaznych stanowią:
- stopy miedzi (m.in. brązy, mosiądze, miedzionikiel, melchior, nowe
srebro, tombak),
- stopy niklu (m.in. monel, chromel, permaloj, alumel, inconel, nichrom,
nimonic),
- stopy cynku (np. znal),
- stopy cyny (np. lutowia),
- stopy aluminium (np. duraluminium),
- stopy magnezu (np. elektron).
42. Opisać zjawisko zjawisko zużycia trybologicznego.- Michał Baran
Zużywanie tribologiczne
Zużywanie tribologiczne wywołane jest tarciem, ma charakter mechaniczno - fizyczno - chemiczny. Towarzyszy zawsze tarciu suchemu i mieszanemu:
mechaniczne procesy zużywania: polegają na oddzielaniu cząstek ze współpracujących powierzchni przez mikroskrawanie występami mikronierówności lub luźnymi cząstkami ściernymi
fizyczne procesy zużywania: związane jest z adhezją trących się ciał, (sczepianie, zrastanie, dyfuzja) wywołują zużycie przez oddzielenie cząstek z jednego ciała i nanoszenie ich na ciało współpracujące, lub przez mikroskrawanie przeciwpowierzchni utworzonymi narostami
chemiczne procesy zużywania: zachodzą pomiędzy trącymi się materiałami i ośrodkiem, w którym przebiega proces tribologiczny
Podstawowe rodzaje tarcia tribologicznego:
Zużywanie utleniające
Zużywanie wodorowe
Zużywanie ścierne
Zużywanie zmęczeniowe
Zużywanie odkształceniowe
Zużywanie adhezyjne
Zużywanie cieplne
Fetting
43. Definicja i klasyfikacja tworzyw sztucznych oraz zastosowanie, utylizacja.- Mikołaj Wiaderny
Tworzywa sztuczne - materiały oparte na polimerach syntetycznych lub zmodyfikowanych naturalnych, zastępujące tradycyjne tworzywa takie jak drewno, ceramika, metal, kauczuk naturalny, gutaperka i inne. Ponadto, wiele tworzyw sztucznych posiada własności niemożliwe do uzyskania z zastosowaniem surowców naturalnych.
W skład tworzyw sztucznych oprócz polimerów wchodzą różnego rodzaju dodatki nadające im określone właściwości fizyczne. Mogą to być:
napełniacze
plastyfikatory
stabilizatory
- antyozonanty
- dodatki zmniejszające palność
antystatyki
barwniki
dodatki przeciwścierne
Współcześnie paleta dostępnych tworzyw sztucznych umożliwia w praktyce zastąpienie nimi niemal każde tworzywo naturalne. Tworzywa sztuczne nie mają jednak zwykle własności identycznych z tworzywami naturalnymi. Zwykle tworzywa sztuczne mają takie same a nawet lepsze te własności, które są najbardziej istotne dla danego zastosowania, może mieć jednak gorsze mniej istotne własności.
Tworzywa sztuczne mogą być klasyfikowane na wiele sposobów:
Ze względu na zastosowanie
konstrukcyjne,
powłokowe,
adhezyjne,
włóknotwórcze,
specjalne (wymieniacze jonowe, polimery biomedyczne itp).
Ze względu na właściwości fizykochemiczne
Duromery - twarde, trudnotopliwe o wysokiej odporności mechanicznej służące jako materiały konstrukcyjne - inaczej nazywane sztucznymi metalami. Niektóre duromery zastępują też materiały ceramiczne.
Plastomery - popularnie zwane termoplastami mniej sztywne od duromerów ale łatwotopliwe i zwykle rozpuszczalne - dzięki ich topliwości można je przetwarzać poprzez topienie i wtryskiwanie do form lub wytłaczanie, dzięki czemu można z nich uzyskać bardzo skomplikowane kształty. Stosowane są zamiast drewna i niekiedy zamiast metalu, np. jako obudowy do maszyn i urządzeń, elementy wyposażenia domowego.
Elastomery - tworzywa, które można rozciągać i ściskać; w wyniku rozciągania lub ściskania elastomery zmieniają znacznie swój kształt ale po odjęciu siły wracają do poprzednich wymiarów. Elastomery zastąpiły prawie całkowicie kauczuk naturalny, ale znalazły też szereg nowych zastosowań niedostępnych dla zwykłego kauczuku.
Ze względów ekologicznych trwają prace nad biologicznie rozkładającymi się tworzywami sztucznymi, produkowanymi na bazie roślinnej czy zwierzęcej.
Zastosowanie:
- butelki, wypełniacze do poduszek
- folia do miękkich opakowań spożywczych, torby na zakupy, worki na odpady
- pojemniki na filmy do aparatów fotograficznych, opakowania do jogurtu, nakrętki do butelek
- rury wodociągowe, wykładzina, okna, parapety, ceraty
- torebki na chipsy, pojemniki na śmieci
- tacki do pakowania mięsa, kubki do gorących napojów, opakowania
- płyty CD
- klocki lego
- lalki barbie
- zapewne sedes w kiblu też...
Dla bardziej wnikliwych :
Tradycyjne materiały opakowaniowe (drewno, szkło i metale) wypierane są przez tworzywa sztuczne, z których wytwarza się 20 - 25% opakowań. Są to różne folie, np. worki samonośne, różne torby i torebki, folia do pakowania mleka, butelki Szerokie zastosowanie maja opakowania sztywne ze styropianu.
Tworzywa sztuczne nie są dotychczas podstawowym materiałem konstrukcyjnym. Domeną tworzyw sztucznych w budownictwie jest wyposażenie wnętrz (wykładziny podłogowe, ramy okienne i drzwiowe) oraz pokrycia dachowe (płyty z laminatów poliestrowych, płyty PCW i PMM jako świetliki). Z PCW metodą wytłaczania wytwarza się poręcze i listwy podłogowe. Nowością są tapety samoprzylepne z warstwą pianki (izolator cieplny i akustyczny). Nowością w budownictwie są profilowane blachy z warstwą ochronno - ozdobną tworzywa; służą one jako wykładzina zewnętrzna budynków i w budowie statków. Przyszłościowym materiałem budowlanym są polimerobetony, złożone z wypełniacza mineralnego i żywicy syntetycznej, np. epoksydowej. Gwarantuje to uzyskanie dużej wytrzymałości polimerobetonów (ich wysoka ocena na razie uniemożliwia szersze stosowanie). Zastępowanie tradycyjnej armatury i rurociągów wyrobami z tworzyw sztucznych jest ograniczone małą odpornością na gorącą wodę, szczególnie pod ciśnieniem panującym w wysokich budynkach.
Tworzywa sztuczne służące w gospodarstwie Podlegają podobnie jak w medycynie ścisłej kontroli władz sanitarnych. Dotyczy to nie tylko sprzętu kuchennego, ale i wyrobów toaletowych oraz materiałów będących jedynie wyposażeniem mieszkaniowym. Muszą być jednak wykonane z odpowiednich tworzyw sztucznych. Pierwotnie stosowane były tworzywa termoreaktywne (bakelit czy aminoplasty);obecnie stosuje się termoplasty, jak polistyren (gatunki uszlachetnione), polietylen, zwłaszcza odporny na wrzącą wodę polipropylen. Najbardziej użyteczne do wyrobu robotów kuchennych, a nawet maszynek do parzenia kawy są poliwęglany.
Dzięki fizjologicznej objętości prawie wszystkich polimerów i możliwości ich stosowania w styczności z organizmem żywym, i to nie tylko w krótkotrwałych kontaktach, ale i na stałe (wszczepy - endoprotezy) zastosowanie tworzyw sztucznych w medycynie jest szerokie. Specjalną pozycję zajmują włókna sztuczne z medycynie. Na razie nie ma przeciwwskazań stosowania tworzyw sztucznych w medycynie w przypadkach dających konkretne korzyści. Pozaustrojowe stosowanie tworzyw sztucznych w medycynie nie budzi zastrzeżeń. Najszersze zastosowanie osiągnęły strzykawki jednorazowego użytku wytwarzane np. z polipropylenu. Cewniki, dreny, a z najbardziej skomplikowanych wyrobów - sztuczna nerka wyrabiane są z polietylenu (rurki, cewniki), polichlorku winylu (rurki, naczynia), celofanu (folie półprzepuszczalne do dializy pozaustrojowej). W stomatologii stosuje się polimetakrylan metylu, w okulistyce - sztywne i elastyczne szkła kontaktowe, w chirurgii - nici (włókna w medycynie). W farmacji tworzywa sztuczne stosuje się głównie jako materiał opakowaniowy; fiolki, tuby, a zwłaszcza popularne listki z pastylkami lub drażetkami umieszczonymi w gniazdkach uformowanych w folii PCW metodą termoformowania i zespolonej z folią aluminiową. Z tworzyw sztucznych wykonane są pojemniki ułatwiające dozowanie leku, np. kroplomierze. Z innych zastosowań tworzyw sztucznych w medycynie wymienić należy ortopedię, protetykę, chirurgię plastyczną, transport ciężko chorych (do tego celu służy płaski materac z folii PCW zawierający wewnątrz kluseczki styropianowe, nałożony na część ciała jako materac po usunięciu powietrza za pomocą pompki ssącej usztywnia się, formułując funkcjonalne nosze dopasowane do pacjenta).
Tworzywa sztuczne w rolnictwie spełniają różnorodne funkcje np. folia z polietylenu (PE) wydatnie zwiększyła możliwości upraw cieplarnianych, zarówno przez budowę pneumatycznych obiektów, jak i pokrywanie konstrukcji nośnej. Dobra izolację termiczną spełnia również cienka folia (np. 0,03 mm) rozpięta nad tradycyjną szklarnią. Do wykładania silosów z kiszonkami, zabezpieczania przed wilgocią stoków i kopców z produktami rolnymi stosuje się folię z polichlorku winylu (PCW). Rury, zwłaszcza z PE, służą do doprowadzania wody, a cienkościenne ? do bezpośredniego nawadniania poprzez mikrozaworki. Jest to tzw. kropelkowe nawadnianie pozwalające na racjonalne doprowadzenie wody do układu korzeniowego upraw zielonych (drzew, krzewów, pomidorów, truskawek). W melioracji stosowane są coraz częściej perforowane rury z PCW. Z folii PCW metodą termoformowania otrzymuje się doniczki i cienkościenne kaptury służące jako indywidualna osłona roślin przed przymrozkami. Pewne znaczenie praktyczne mają pianki spulchniające glebę gliniastą, a w piaszczystej magazynujące wilgoć . Naczynia z tworzyw sztucznych oraz wyposażenie stanowisk hodowlanych zwierząt (koryta, kanały ściekowe, ażurowe podłogi) ułatwiają obsługę i umożliwiają utrzymanie czystości oraz dezynfekcję pomieszczeń.
Utylizacja:
Tworzywa Sztuczne albo zostają wyrzucone na wysypiska śmieci tudzież spalone z kiepskim wpływem na środowisko, albo zostają poddane recyklingowi (ewent. reCYClingowi).
Tworzywa Sztuczne ulegają powolnemu procesowi naturalnego rozkładu zanieczyszczeń w wyniku którego powstają substancje przyjazne dla środowiska ale ta biodegradacja trwa bardzo długo. Tworzywa sztuczne podczas spalania wytwarzają trujące substancje. W krajach wysoko rozwiniętych odchodzi się od stosowania opakowań z tworzyw sztucznych zastępując je szkłem lub tekturą, są to materiały które mogą zostać ponownie użyte. Plastik ulega rozkładowi nawet do 500 lat i podczas rozpadu wydziela związki metali ciężkich, które były używane do produkcji danego tworzywa.
Obecny stan rozwoju procesów recyklingu odpadów z tworzyw sztucznych powoduje, że tylko niewielka ich część jest poddawana recyklingowi produktu i recyklingowi materiałowemu. Większość tworzyw sztucznych poddawana jest recyklingowi termicznemu lub zgazowaniu. Główną tego przyczyną jest różnorodność tworzyw sztucznych, dodatki, a także przeszkody ekonomiczne.
Kody recyklingu tworzyw sztucznych:
W celu uproszczenia recyklingu tworzyw sztucznych został wprowadzony przez Society of the Plastics Industry Inc (USA)' w 1988 specjalny kod oznaczania tych tworzyw. Pierwotnie został on zaprojektowany dla tworzyw stosowanych w naczyniach i opakowaniach stosowanych w gospodarstwach domowych. Później jednak został rozszerzony na inne tworzywa, a także na metale. Symbole te ułatwiają ich sortowanie w sortowniach odpadków. Dodatkowo informują też konsumentów z jakim tworzywem mają do czynienia.
Kody zawierają trzy strzałki, tworzące trójkąt, z grotami skierowanymi zgodnie z ruchem wskazówek zegara. Wewnątrz trójkąta znajduje się liczba oznaczająca kod tworzywa, a pod trójkątem umieszczany jest skrót literowy, pochodzący z angielskiej nazwy głównego polimeru wchodzącego w skład oznakowanego tworzywa. Kod ten bywa też stosowany do metali kolorowych i aluminium.
45. Co to są termoplasty, kopolimery, styropian, poliamidy, pleksiglas, teflon, elastomery?-Karol Kapuściński
Termoplasty, tworzywa termoplastyczne, tworzywa polimeryczne zbudowane z makrocząsteczek, głównie liniowych, rzadziej rozgałęzionych. Nieograniczenie długo plastyczne w podwyższonej temperaturze, a twarde w temperaturze otoczenia (proces ten w przypadku termoplastów jest odwracalny). Na ogół rozpuszczają się w rozpuszczalnikach organicznych na zimno lub na gorąco (np. polietylen), jedynym nie rozpuszczającym się termoplastem jest politetrafluoroetylen.
Do najważniejszych termoplastów zalicza się: polistyren, polietylen, poli(chlorek winylu), poli(metakrylan metylu), politetrafluoroetylen i poliamidy.
Kopolimery - rodzaj polimerów, których łańcuchy zawierają dwa lub więcej rodzajów merów. W odróżnieniu od kopolimerów, polimery zawierające tylko jeden rodzaj merów nazywa się często homopolimerami. Głównym powodem otrzymywania kopolimerów są ich szczególne własności fizyczne, których nie mogą posiadać homopolimery i ich proste mieszaniny zawierające te same mery.
Styropian- to porowate tworzywo sztuczne otrzymane poprzez spienienie granulek polistyrenu zawierających porofor. Spienienie uzyskuje się przez podgrzanie granulek zazwyczaj parą wodną. Składa się z zamkniętych komórek o obłych kształtach, wewnątrz których znajduje się pianka polistyrenowa. Komórki są ze sobą połączone i występują między nimi niewielkie pustki powietrzne, co uwidacznia się na przełomie styropianu. Jest to materiał nieodporny na działanie rozpuszczalników aromatycznych, olejów, smarów.
Styropian stosowany jest często w budownictwie (można stosować tylko odmianę FS), jako lekki (od ok. 10 - do ponad 40 kg/m3), materiał termoizolacyjny do temperatury + 80°C oraz jako rdzeń izolacyjno-konstrukcyjny przy produkcji budowlanych płyt warstwowych. Bywa stosowany jako materiał do wykonywania izolacji akustycznej, chociaż jego skuteczność jest niska.
Poliamidy to polimery, które posiadają wiązania amidowe -C(O)-NH- w swoich głównych łańcuchach.
Poliamidy mają bardzo silną tendencję do krystalizacji dodatkowo wzmacnianą tworzeniem się wiązań wodorowych między atomem tlenu i azotu z dwóch różnych grup amidowych. Dzięki temu poliamidy są bardziej twarde i trudniej topliwe niż poliestry nie mówiąc już o polimerach winylowych. Z poliamidów produkuje się przede wszystkim włókna zwane nylonami i aramidami oraz tworzywa sztuczne o podwyższonej odporności mechanicznej nadające się np. do produkcji kół zębatych.
Pleksiglas syntetyczna żywica akrylowa, bardzo twarda odmiana polimetakrylanu , z którego wytwarza się powszechnie używane (w samochodach, samolotach, optyce, chemii itd.) szkło organiczne o małej łamliwości.
Teflon - nazwa handlowa polimeru o nazwie systematycznej: politetrafluoroetylen -[-CF2-CF2-]n- (PTFE). Czysty politetrafluoroetylen jest całkowicie nietopliwy i zaczyna rozkładać się w temperaturze 327°C. W temperaturze ok. 260°C przechodzi z fazy krystalicznej do fazy condis, w której staje się przezroczysty i dość miękki - ale nie płynny.
Jedną z najważniejszych cech PTFE jest jego wyjątkowo mała energia powierzchniowa, dzięki czemu ma on dobre własności smarujące, oraz nie przywierają do niego żadne zanieczyszczenia. Inną ważną własnością PTFE jest jego wysoka odporność chemiczna. Praktycznie nie reaguje on ani nie rozpuszcza się w niczym oprócz stężonego kwasu fluorowodorowego.
Ze względu na nietopliwość PTFE nie można go obrabiać w typowy dla tworzyw sztucznych sposób (np: przez wytłaczanie lub wtrysk) lecz trzeba stosować techniki spiekania proszku - podobne do stosowanych w materiałach ceramicznych.
Elastomery - to polimerowe tworzywa sztuczne lub naturalne, które cechuje zdolność do odwracalnej deformacji pod wpływem działania sił mechanicznych, z zachowaniem ciągłości jego struktury. Elastomery to szersza grupa materiałów niż gumy, które stanowią tylko jedną z klas elastomerów.
Elastomer posiada zdolność zmiany w szerokim zakresie swoich wymiarów w momencie gdy jest poddawany naprężeniom rozciągającym, ścinającym lub ściskającym oraz następnie powrót do poprzednich wymiarów. Zdolność elastomerów do zmiany wymiarów wynika z ich specyficznej budowy chemicznej.
47. Jakie są metody przetwórstwa tworzyw sztucznych?-Maciej Jeż
Przetwórstwo tworzyw sztucznych jest to formowanie z tych tworzyw
końcowych produktów.
Podstawowe techniki przetwórstwa:
1. wtłaczanie
2. wtrysk
3. prasowanie:
- tłoczenie
- przetłaczanie
- formowanie płyt
4. walcowanie i kalandrowanie
5. odlewanie
48. Co to są materiały ceramiczne? Wymień ich rodzaje.-Madzia Cieślińska
Ceramikę stanowią materiały nieorganiczne o jonowych i kowalencyjnych wiązaniach międzyatomowych, wytwarzane zwykle w wysokotemperaturowych procesach związanych z przebiegiem nieodwracalnych reakcji, chociaż do tej grupy materiałów zaliczane są również szkła oraz beton i cement, pomimo że przy ich wytwarzaniu zachodzą wszystkie z tych procesów.
Tworzywa ceramiczne odznaczają się przede wszystkim odpornością na działanie wysokiej temperatury i czynników chemicznych, dobrymi właściwościami mechanicznymi i dielektrycznymi, oraz twardością. Wadą ich jest kruchość, która uniemożliwia obróbkę mechaniczną i utrudnia łączenie wyrobów ceramicznych ze sobą lub innymi materiałami.
Klasyfikacja materiałów ceramicznych:
-ceramika inżynierska (specjalna, drobnoziarnista) wytwarzana w wyniku spiekania w wysokiej temperaturze, bez udziału fazy ciekłej, bardzo czystych związków takich jak tlenki, węgliki, azotki ale także diament i wykazują w stanie stałym postać krystaliczną bez udziały fazy szklistej
-cermetale - złożone z drobnych cząstek krystalicznych np. węglików lub azotków równomiernie rozłożonych w osnowie metali lub ich stopów stanowiących lepiszcze.
Materiały te bywają zaliczane do ceramiki inżynierskiej lub materiałów kompozytowych. Cermetale są wytwarzane metodami metalurgii proszków ze spiekaniem w wysokiej temperaturze
- ceramika porowata (tradycyjna) obejmuje masowo produkowane materiały, ogniotrwałe lub stosowane w technice sanitarnej. Charakteryzuje się udziałem fazy szklistej otaczającej składniki krystaliczne, utworzone głównie z Al2O3, SiO2 i H2O.
W skład ceramiki porowatej zaliczany jest również cement oraz beton.
- szkła- podlegają odszkleniu (denitryfikacji), stając się materiałami krystalicznymi lecz okres ten trwa kilkaset lat. Podstawowymi składnikami szkłotwórczymi są: SiO2, B2O3 i P2O5, tlenki arsenu i germanu, a także siarka, selen i fluorek ołowiu. W skład szkła mogą wchodzić również tlenki zasadowe metali alkalicznych i ziem alkalicznych, a także tlenki pośrednie takich metali jak aluminium i berylu.
Szkło jest przezroczyste dla światła widzialnego, jest izolatorem elektrycznym a także cechuje się bardzo małą przewodnością cieplna.
-ceramika szklana, zwana dewitryfikatorem lub pyroceramiką powstaje przez krystalizację masy szklanej w ściśle określony sposób umożliwiający utworzenie struktury bardzo drobnoziarnistej, bez porowatości. Otrzymuje się ją w wyniku krystalizacji szkła na zarodkach tworzonych przez niewielkie dodatki Cu, Ag lub Au pod wpływem promieniowania ultrafioletowego.
49. Wymienić i scharakteryzować rodzaje porcelany. - Paulina Sławińska
Porcelana - rodzaj białej, przeświecającej ceramiki wysokiej jakości, wynaleziony w Chinach w VII w. Porcelana jest wytwarzana z mieszanki glinki kaolinowej ze skaleniem i kwarcem poprzez wypalanie uformowanych wyrobów w temperaturze od 920-980°C (wyroby nieszkliwione, tzw. biskwit) aż do 1280-1460°C (wyroby szkliwione). Charakteryzuje się niską nasiąkliwością, bardzo dobrymi właściwościami dielektrycznymi, dużą wytrzymałością mechaniczną, wysoką odpornością na działanie czynników chemicznych i nieprzepuszczalnością dla cieczy i gazów.
W technice używana jako materiał na nisko- i wysokonapięciowe izolatory i sprzęt laboratoryjny, oraz jako wyroby gospodarstwa domowego.
Rozróżnia się ceramikę twardą (o składzie: 40-60% kaolinu, 20-30% skalenia, 20-30% kwarcu) i miękką (25-40% kaolinu, 25-40% skalenia, 30-45% kwarcu).
Fajans - rodzaj ceramiki podobny nieco do porcelany wytwarzanej z zanieczyszczonego kaolinu.
Po wypaleniu (w temperaturach przekraczających 1000°C) wyroby fajansowe mają kolor od białego do jasnokremowego. Wytwarza się je najczęściej w wersji powleczonej nieprzezroczystym szkliwem.
Porcelit - rodzaj białej do kremowej, szkliwionej, nieprześwitującej ceramiki wytwarzany podobnie jak porcelana, lecz z surowców (kaolin, skaleń, kwarc) o najczęściej gorszej jakości. Uformowane wyroby poddaje się wypalaniu w temp. ~1325°C w celu osiągnięcia zamierzonej nieprzesiąkliwości, wytrzymałości i twardości.
W technice używany jako materiał do produkcji m.in. sanitariatów.
51. Co to są spieki i kompozyty, wymienić i omówić rodzaje i zastosowanie.- Kasia Łozińska
ęłęóKompozyty są to tworzywa składające się z dwóch lub więcej faz o właściwościach nieosiągalnych w żadnym innym materiale. Do najbardziej znanych kompozytówmnależą: żelazo-beton, eternit, szkło zbrojone siatką metalową, węgliki spiekane cermetale i in.
Kompozyty dzielimy na umacniane cząstkami (dyspersyjnie) i włóknami (włókniste). Te z kolei dzielimy na umacniane włóknami ciętymi i ciągłymi.
ęłęóKompozyt składa się z osnowy i umieszczonego w niej drugiego składnika (zbrojenia) o znacznie lepszych właściwościach mechanicznych.
Zbrojenie może mieć postać proszku lub włókien. Dodawane jest do kompozytu w dużej ilości. Oddziałuje ono zazwyczaj tylko fizycznie na osnowę.
ęłęóPodział kompozytów ze względu na osnowę:
1)kompozyty metalowe
●kompozyty o osnowie ze stopu metali lekkich ( Mg, Al, Ti)
●kompozyty o osnowie ze stopu srebra i miedzi
●kompozyty o osnowie ze stopu niklu
●kompozyty o osnowie ze stopu ołowiu i cynku
2) kompozyty polimerowe (żywice termoutwardzalne jak fenoplasty i aminoplasty; duroplasty chemoutwardzalne, silikony, tworzywa termoplastyczne)
3) kompozyty ceramiczne (materiały budowlane jak cement i gips; materiały hutnicze
- głównie ogniotrwałe; materiały stosowane w elektronice)
zastosowanie:
ęłęóKompozyty pozwalają na otrzymywanie lekkich, mocnych i elastycznych konstrukcji. Są nimi także materiały żarowytrzymałe (np. łopatki turbin gazowych) i narzędzia (np. węgliki spiekane).
Spieki - są to półwyroby lub wyroby gotowe otrzymane metodami metalurgii proszków tzn. przez prasowanie i spiekanie. Główną zaletą metalurgii proszków jest to, że można wytwarzać spieki niemożliwe do otrzymania innymi metodami.
Zależnie od doboru składników rozróżnia się:
• spieki proste - jednoskładnikowe,
• spieki złożone - wielofazowe.
Do najważniejszych spieków złożonych zalicza się:
• pseudostopy,
• spieki ceramiczno-metalowc (cermety),
• spieki grafitowo-metalowe, łączące własności grafitu z własnościami metalu, którym bywa najczęściej miedź, żelazo lub brąz,
• spieki diamentowo-metalowe,
• materiały porowate (np. łożyska ślizgowe, filtry) i in..
Spieki znalazly zastosowanie w przemyśle motoryzacyjnym i maszynowym. Wykonuje się z nich np. częsci maszyn (m.in. koła zębate)
ęłęó
Cermet - jest to spiek ceramiczno-metalowy uzyskiwany na drodze spiekania proszków ceramicznych i metalowych. Stanowi on tworzywo o większej wytrzymałości mechanicznej niż materiały ceramiczne i o większej odporności na działanie wysokich temperatur niż metale. Stosowany jest do wyrobu elementów wytrzymałych na ścieranie w wysokiej temperaturze, np. wyrobu ostrzy skrawających (węgliki spiekane), łopatek, turbin, poszycia kadłubów samolotów odrzutowych, elementów aparatury elektrotechnicznej i jądrowej |
52. Co to są farby i rozpuszczalniki? - Paweł Dmochowski
Farba to substancja powłokotwórcza służąca do ochronnego lub dekoracyjnego pokrywania
powierzchni dowolnych przedmiotów. Może zalegać na ich powierzchni, lub nieznacznie
wnikać w głąb. Składa się z substancji barwiących - najczęściej w postaci pigmentów
oraz substancji dodatkowych: spoiw, wypełniaczy, rozcieńczalników, rozpuszczalników,
a także substancji błonotwórczych, dyspergujących, konserwujących, opóźniających wysychanie,
reagujących z podłożem itp.
Rozpuszczalnik to ciecz zdolna do tworzenia roztworu po zmieszaniu z ciałem stałym,
inną cieczą lub gazem. Najbardziej znanym rozpuszczalnikiem jest woda.
Większość rozpuszczalników to związki chemiczne o małej lepkości i stosunkowo niskiej
temperaturze wrzenia. Mała lepkość powoduje, że mogą one dość łatwo penetrować rozpuszczaną
substancję, zaś niska temperatura wrzenia umożliwia ich oddestylowywanie i parowanie.
Gat. Rm[MPa] Re[MPa] A5[%] HB Struktura
37017 370 230 17 <179 F
40012 400 250 12 <201 F
50007 500 320 7 170-241 F+P
55002 550 360 2 181-210 P+F
60003 600 370 3 192-269 P+F
65003 650 400 2 221-280 P
70002 700 420 2 228-302 P
80002 800 480 2 248-302 #
90002 900 530 2 241-302 #
Wyszukiwarka
Podobne podstrony:
Prawo administracyjne materialne pytania i odpowiedzi na egzamin (1)
Odpowiedzi na egzamin z Podstaw Zarządzania (dr M. Pawłowski WSM Warszawa Kawęczyńska), Pliki, Mater
odpowiedzi na egzamin hodowla owiec
Odpowiedzi na egzamin cz 2
kartografia odpowiedzi na egzamin
ODPOWIEDZI NA EGZAMIN Z PRAWA 1
Odpowiedzi na egzamin
Pytania i odpowiedzi na egzamin, Budownictwo - studia, I stopień, I rok, Chemia
Test wiedzy na egzamin końcowy 2005, materiały dla policjantów
pytania i odpowiedzi na egzamin, SGGW Technika Rolnicza i Leśna, NOM
odpowiedzi na egzamin wiedzy ogólnej z policji, Pomoce dydaktyczne
Towaroznawstwo żywności - zagadnienia na egzamin, Nauka, Towaroznawstwo żywności, Zagadnienia
EIE- pytania i odpowiedzi na egzamin
odpowiedz NA EGZAMIN, PYTANIA NA EGZAMIN
Pedagogika społeczna, Egzamin - zagadnienia, Pedagogika społeczna-pytania i odpowiedzi na egzamin
odpowiedzi na egzamin twf
odpowiedzi na egzamin
więcej podobnych podstron