Zagadnienia treningowe na egzamin z Chemii żywności:
1. Struktura wody w stanie stałym, ciekłym i gazowym.
STRUKTURA WODY LÓD
Dipolowa budowa wody i zdolność do tworzenia wiązań wodorowych sprzyja ich wzajemnemu łączeniu się w uporządkowane układy zarówno w stanie stałym, jak i w stanie ciekłym. Struktura tych układów wynika z wewnętrznej geometrii cząsteczki.
W stanie stałym woda tworzy sieć krystaliczną. Kryształy najpopularniejszej postaci
lodu - lodu zwykłego- mają strukturę heksagonalną. Oprócz struktury lodu zwykłego, lód może występować w dziewięciu innych strukturach polimorficznych, a także w postaci amorficznej. W stanie stałym każda cząsteczka wody jest trwale powiązana z czterema innymi cząsteczkami; każdy atom tlenu tworzy wiązania kowalencyjne z dwoma atomami wodoru i dwa wiązania wodorowe z atomami wodoru sąsiednich cząsteczek.
W większości żywności mrożonej lód ma postać heksagonalną zwykłego lodu, jeżeli proces krystalizacji zachodził z umiarkowaną szybkością i w środowisku nie zawierającym substancji mających wpływ na tworzenie się wiązań wodorowych. Aktywne właściwości lodu mogą mieć istotne znaczenie dla trwałości żywności i innych materiałów biologicznych przechowywanych w stanie zamrożonym.
STRUKTURA WODY - TOPNIENIE
W czasie ogrzewania lodu do temperatury bliskiej temperaturze topnienia wzmagające się drgania cieplne cząsteczek powodują coraz częstsze zrywanie wiązań wodorowych. W temperaturze 0°C liczba zerwanych wiązań jest tak znaczna, że lód przemienia się w ciecz. Po zniszczeniu luźnej, lecz sztywnej struktury lodu w chwili topnienia cząsteczki wody zbliżają się ku sobie, w skutek czego ciekła woda zajmuje mniejszą objętość i wykazuje większą gęstość od lodu. Wynika to z tego, że wiązania wodorowe łączące cząsteczki wody w siatce krystalicznej lodu są dłuższe niż w ciekłej wodzie.
W temperaturze 0°C nie następuje jednak zerwanie wszystkich wiązań wodorowych. W wodzie ciekłej pozostają jeszcze ugrupowania cząsteczek o podobnym ułożeniu jak w stanie stałym. Ze wzrostem temperatury liczba czynnych wiązań wodorowych zmniejsza się , co powoduje że objętość wody mimo ogrzania ulega dalszemu zmniejszeniu. Gęstość jej jeszcze wzrasta i w temp. 4°C osiąga maksimum. Podczas dalszego ogrzewania efekty spowodowane pękaniem wiązań wodorowych odgrywają coraz mniejszą rolę. Wzrost energii i ich ruchliwość pociąga za sobą natomiast wzrost objętości - podobnie jak dla wszystkich cieczy.
STRUKTURA WODY CIEKŁEJ, PAROWANIE
Typową formę lodu cechuje struktura luźnej sieci krystalicznej o gęstości 0,922 g/cm3. Zniszczenie tej sieci po ogrzaniu lodu do temperatury powyżej 0°C prowadzi do rozerwania zaledwie 15% wiązań wodorowych, przy wzroście gęstości układu do 0,9995 g/cm3 (w temp. 4°C) i zmniejszeniu objętości.
Dzięki wiązaniom wodorowym ciekła woda zachowuje częściowo strukturę krystaliczną lodu. Jednakże struktura wody ciekłej jest tak dynamiczna, że nie istnieją w niej trwałe kryształy. Cząsteczki nieustannie łączą się ze sobą dzięki przyciąganiu dipoli (asocjacja) w pseudokryształy, które równie szybko (10-10 - 10-11s) powstają i ulegają rozpadowi.
W miarę wzrostu temperatury energia kinetyczna cząsteczek wody staje się większa niż energia łączących je wiązań wodorowych i woda przechodzi w stan gazowy.
2. Pojęcie anomalnej rozszerzalności temperaturowej wody.
Wszystkie substancje wraz ze wzrostem temperatury zwiększają swą objętość, a wraz ze obniżeniem temperatury zmniejszają ją. Z wodą jest nieco inaczej. Zmniejsza swą objętość wraz z obniżeniem temperatury, ale tylko do 4°C. Poniżej tej temperatury woda z powrotem zwiększa swoją objętość.
Podczas zamarzania woda zwiększa zatem swoją objętość i dlatego lód (mający mniejszą gęstość) pływa po wodzie. Ta anomalna rozszerzalność wody i fakt, że w temperaturze 40C ma ona największą gęstość, powodują, że zimą, gdy temperatury powietrza są niskie, na dnie zbiorników wodnych utrzymuje się woda o temperaturach wyższych od 00C. Natomiast latem, gdy temperatura powietrza jest wysoka, przy dnie zbiorników wodnych zbiera się woda chłodniejsza, ponieważ ma większą gęstość niż woda cieplejsza utrzymująca się na powierzchni. Takie właściwości wody pozwalają utrzymać na dnie zbiorników wodnych niewielkie wahania temperatur w ciągu roku i gwarantują stałość warunków życia w wodach.
3. Rola wody w żywności.
· Główny czynnik wpływający na intensywność procesów biochemicznych, chemicznych i fizycznych oraz tych, które decydują o rozwoju drobnoustrojów.
· Właściwa ilość wody , charakterystyczna dla danego produktu, decyduje o konsystencji, wygładzie i smaku żywności oraz jej podatności na zepsucie.
· Większość procesów konserwowania żywności opiera się na eliminacji możliwie dużych ilości wody z produktu.
· Całkowita zawartość wody w danym materiale żywnościowym wyznacza się termograwimetrycznyie, czyli wykorzystując utratę masy pod wpływem ogrzewania. Ogrzewanie przeprowadza się w piecu używając mikrofali lub promieni podczerwonych. Ilość wody wyznacza się z różnicy masy próbki danego produktu przed i po wysuszeniu go do stałej masy w temperaturze 105°C. Zawartość wody jest wyrażana w procentach w przeliczeniu na suchą masę lub masę materiału wilgotnego. Jeśli żywność zawiera duże ilości soli albo tłuszczów należy zaznaczyć czy zawartość tych składników w oznaczeniu została uwzględniona.
4. Rodzaje wody w żywności.
Woda strukturalna (krystaliczna, związana chemicznie) <0,03% jest integralną częścią składników niewodnych, ulokowana w wolnych przestrzeniach makrocząsteczek lub związana w postaci wodzianów.
Woda związana w postaci monowarstwy (0,1-0,9%) silnie oddziałuje z grupami polarnymi i zjonizowanymi składników niewodnych.
Woda związana w dalszych kilku warstwach (1-5%) o strukturze uporządkowanej wokół hydrofilowych grup składników niewodnych, stabilizowana wiązaniami wodorowymi, utworzonymi miedzy tymi grupami a wodą oraz miedzy cząsteczkami samej wody.
Woda wolna (nie związana): ok. 5-96% rozpuszczalnik substancji organicznych i związków mineralnych. Łatwo wydziela się z produktu, pod wpływem czynników zewnętrznych, o właściwościach zbliżonych do właściwości wody w rozcieńczonych roztworach soli, powiązana siecią wzajemnych wiązań wodorowych.
Woda uwięziona (5-96%) o właściwościach wody wolnej, ale uwięziona w niewypełnionych przestrzeniach składników strukturalnych lub w żelach, przez co jej przepływ jest utrudniony.
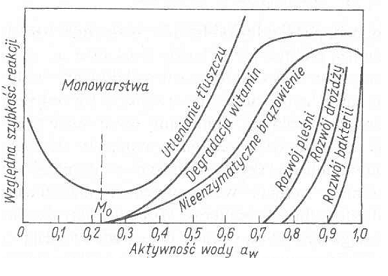
5. Pojęcie aktywności wody. Szybkość reakcji w zależności od aktywności wody.
Aktywność wody (aw) w żywności jest definiowana jako stosunek ciśnienia pary wodnej nad żywnością do ciśnienia pary wodnej nad czystą wodą w tej samej temperaturze.
aw = p/p0
Czysta chemicznie woda ma aktywność aw=1. Ze wzrostem stężenia związków rozpuszczalnych aktywność wody spada poniżej wartości 1. Aktywność wody oznacza się przez umieszczenie małej próbki substancji badanej w zamkniętej komorze na czas wystarczający do osiągnięcia równowagi, a następnie mierzy się ciśnienie lub wilgotność względną w komorze. Aktywność wody jest miara zawartości wody wolnej w danym materiale. Woda związana jest mniej dostępna.
AKTYWNOŚĆ WODY A REAKCJE ENZYMATYCZNE
Zawartość wody ma wpływ na konformację białek enzymatycznych, które decydują o aktywności i zdolności katalitycznej enzymów.
Brak fazy wodnej uniemożliwia transport substratów i produktów reakcji. Większość reakcji enzymatycznych rozpoczyna się wraz z pojawieniem się wody luźnie związanej, to jest powyżej aktywności odpowiadającej warstwie monomolekularnej.
Gdy aw<0,3 szybkość reakcji hydrolizy enzymatycznej staje się nieistotna. Działanie innych grup enzymów (amylazy, peroksydazy) jest hamowane, gdy aw < 0,8.
AKTYWNOŚĆ WODY A REAKCJE NIEENZYMATYCZNE
Niektóre reakcje nieenzymatyczne zachodzą z maksymalna szybkością przy średnich wartościach aktywności wody. Powodem spadku szybkości reakcji przy większych wartościach aw może być efekt rozcieńczania lub hamowanie przez produkt, gdy woda jest jednym z produktów reakcji. Taki przebieg ma reakcja Maillarda, prowadząca m.in. do utraty lizyny i odpowiedzialna za brązowienie oraz degradacje witaminy B1.
AKTYWNOŚĆ WODY A REAKCJE UTLENIANIA
Duży wpływ na trwałość i jakość żywności mają reakcje utleniania. W reakcjach autooksydacji, związanych z wolnymi rodnikami woda może przyspieszać lub hamować utlenianie.
W środowisku charakteryzującym się małą wartością aw reakcja utleniania zachodzi, ale wzrost zawartości wody może zmniejszyć szybkość reakcji.
zPrzeciwutleniające działanie wody może być spowodowane m.in. utrudnieniem dyfuzji tlenu do miejsc reakcji, zmniejszeniem stężenia jonów metali, wiązaniem produktów pośrednich autooksydacji lipidów, przyspieszeniem tych reakcji, których produkty mają właściwości przeciwutleniające.
zPrzy zawartości wody związanej w warstwie monomolekularnej szybkość reakcji utleniania zachodzących zarówno w fazie wodnej, jak i w fazie lipidowej są bardzo małe.
zDalsze zwiększanie aw do zakresu średniej wilgotności zwiększa szybkość reakcji autooksydacji. Woda może sprzyjać procesom utleniania przez zwiększenie ruchliwości i rozpuszczalności jonów metali uczestniczących w tych reakcjach, jak też przez pęcznienie białek (eksponowanie nowych powierzchni reakcji), które ułatwiają działanie rodników powstających w procesie utleniania lipidów.
6. Wymienić mikro- i makroelementy. Omówić właściwości mikro- i makroelementów, źródła występowania, skutki niedoboru i nadmiaru.
7. Podać wzory strukturalne 5 kwasów organicznych występujących w żywności.
W jakich produktach występują te kwasy.
8. Wymienić produkty zakwaszające i alkalizujące.
Produkty zakwaszające:
a) silnie: mięso, wędliny, cukier i prod.zawierające cukier, sztuczne słodziki, mąka pszenna, biały ryż, sery żółte, czarna herbata, kakao, czekolada, alkohole wysokoprocentowe
b)średnio zakwaszające: ryby, jaja, chleb żytni, płatki zbożowe, makaron pełnoziarnisty, ryż brązowy, orzeszki ziemne
c) słabo: twaróg, orzechy, kasza gryczana, otręby, fruktoza, makaron sojowy
Prodykty alkalizujące:
a)silnie: bakłażan, dynia, cukinia, ogórki, sałaty, soki warzywno-owocowe, kiwi, arbuz, ananas
b)średnio: buraki, brokuły, kapusta, marchw, seler, pomidor, cytryna, winogrona, banany, fasolka szparagowa
c)słabo: kalafior, cebula, kiełki, czereśnie, dojrzałe jabłka.
9. Wyjaśnić zasadę działania buforu octanowego i amonowego.
Roztworami buforowymi nazywamy roztwory zachowujące stałą wartość pH i nieczułe na niewielkie dodatki kwasów i zasad. Są to przeważnie roztwory słabych kwasów i ich soli lub słabych zasad i ich soli.
a) Bufor octanowy:
Protonodawca: CH3COOH
Protonobiorca: CH3COONa
w roztworze zachodzą reakcje: CH3COOH ◄═►CH3COO- + H+
CH3COONa ―►CH3COO- + Na+
podczas dodawania mocnego kwasu: H+ + CH3COO-―► CH3COOH
podczas dodawania mocnej zasady: OH- + CH3COOH ―►H2O + CH3COO-
b) Bufor amonowy
Protonobiorca: NH3
Protonodawca: NH4+
w roztworze zachodzą reakcje: NH3 + H2O ◄═► NH4+ + OH-
NH4Cl ―► NH4+ + Cl-
podczas dodawania mocnego kwasu: H+ + NH3 ―► NH4+
podczas dodawania mocnej zasady: OH- + NH4+ ―► NH3 + H2O
10. Co to są polichlorowane bifenyle, dioksyny, dibenzofurany, pestycydy, akrylamid.
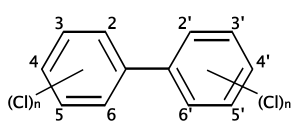
POLICHLOROWANE BIFENYLE (PCB) - ogólna nazwa organicznych związków chemicznych, pochodnych bifenylu, w którym część atomówwodoru zastąpiono atomami chloru.
Właściwości fizyczne i chemiczne
Są związkami lipofilowymi (lipofilowość rośnie wraz z ilością atomów chloru). Dobrze rozpuszczają się w tłuszczach i niepolarnych rozpuszczalnikach organicznych, źle w wodzie. Do wody przechodzą przede wszystkim kongenery (pochodne różniące się liczbą i/lub miejscem podstawienia atomów chloru) o niskim stopniu schlorowania.
Są praktycznie substancjami niepalnymi
Posiadają bardzo niską prężność par (są praktycznie nielotne)
Są odporne na rozkład pod wpływem czynników fizycznych i chemicznych
Powyższe właściwości sprawiają, że PCB są trwałe i łatwo rozprzestrzeniają się w środowisku. Nagromadzają się w kolejnych etapach łańcucha pokarmowego.
Najbardziej skażone są surowce i produkty pochodzenia morskiego oraz ryby słodkowodne. W żywności pochodzenia zwierzęcego najwięcej PCB znajduje się w produktach bogatych w tłuszcz (tłuste ryby, wątroby, tkanka tłuszczowa).
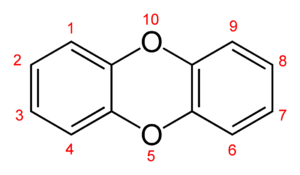
DIOKSYNY
Dioksyny - potoczna nazwa grupy organicznych związków chemicznych będących pochodnymi oksantrenu. Składają się one z dwóch pierścieni benzenowych połączonych przez dwa atomy tlenu oraz od jednego do ośmiu atomów chloru przyłączonych do pierścieni benzenowych. Podobnymi związkami są dibenzofurany, które niekiedy zalicza się do dioksyn.
Dioksyny są jednymi z najbardziej toksycznych związków, jakie otrzymano w wyniku syntezy. Istnieją jednak na Ziemi w śladowych ilościach jako produkt spalania drewna.
Potoczna nazwa "dioksyny" odnosi się do wszystkich możliwych chloropochodnych oksantrenu (dibenzo-1,4-dioksyny). Każda z tych pochodnych nazywana jest kongenerem. Dla dibenzodioksyny istnieje 75 możliwych kongenerów. Z 75 dioksyn 7 jest bardzotoksycznych. Najbardziej niebezpiecznym kongenerem jest 2,3,7,8-tetrachlorodibenzodioksyna, w skrócie 2,3,7,8-TCDD, a często oznaczana jako TCDD.
Na drugim miejscu znajduje się 1,2,3,7,8-PCDD, dwukrotnie mniej toksyczna niż TCDD. Pozostałe dioksyny są znacznie mniej toksyczne od wyżej wymienionych. Całkowitą toksyczność próbki można określić, sumując zawartości poszczególnych składników pomnożone przez współczynnik toksyczności. Dla TCDD ma on wartość 1, dla innych proporcjonalnie mniej - 0,5, 0,01 czy 0,001. Określa się w ten sposób tak zwany równoważnik toksyczny, czyli TEQ.
DIBENZOFURAN- organiczny związek chemiczny o szkielecie fluorenu. Polichlorowane pochodne dibenzofuranu (PCDF) są związkami o strukturze i właściwościach podobnych do dioksyn.
PESTYCYDY (łac. pestis - zaraza, pomór, caedo - zabijam) - substancje syntetyczne lub naturalne, stosowane do zwalczania organizmów szkodliwych lub niepożądanych, używane głównie doochrony roślin uprawnych, lasów, zbiorników wodnych, ale również zwierząt, ludzi, produktów żywnościowych, a także do niszczenia żywych organizmów, uznanych za szkodliwe, w budynkach inwentarskich, mieszkalnych, szpitalnych i magazynach.
Klasyfikacja pestycydów:
· Ze względu na kierunek zastosowania i sposób dzialania
ü Zoocydy - do zwalczania szkodników zwierzęcych
ü Bakteriocydy - do zwalczania szkodnikow bakterii
ü Herbicydy - do zwalczania szkodników chwastów.
ü Fungicydy- do zwalczania szkodnikow grzybów
· Właściwości chemiczne - grupa około 100 związków
· Właściwości toksykologiczne - 5 klas ( 1 klasa- trucizny, 5 klasa- związki praktycznie nieszkodliwe )
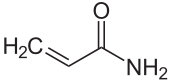
AKRYLAMID (akryloamid, 2-propenoamid), C3H5NO - organiczny związek chemiczny należący do amidów (amid kwasu akrylowego), stosowany głównie jako monomer przy produkcji poliakrylamidu.
Akrylamid tworzy się w reakcji pomiędzy asparaginą i cukrami redukującymi w wyniku tzw. reakcji Maillarda. Może powstawać już w temperaturze 120 °C, optimum to 140-180 °C. Akrylamid przyczynia się do występowania m.in. nowotworów przewodu pokarmowego[5] oraz uszkadza układ nerwowy (jest neurotoksyną).
Duże ilości akrylamidu powstają podczas obróbki termicznej (smażenia w głębokim tłuszczu, pieczenia) produktów spożywczych zawierającychskrobię (węglowodany). Komitet ekspertów ds. Dodatków do Żywności (JECFA - organ doradczy WHO i FAO) podaje, że największy udział w ogólnym spożyciu akrylamidu mają frytki (16-30%), chipsy ziemniaczane (6-46%), kawa (13-39%), ciasta, ciastka i herbatniki (10-20%) oraz chleb i inne gatunki pieczywa (10-30%).
11. Wymienić podstawowe alergeny pokarmowe. Charakterystyka alergenów pokarmowych.
Pokarmy wywołujące ok. 90% wszystkich IgE-zależnych alergii pokarmowych:
· Orzechy arachidowe
· Orzechy rosnące na drzewach
· Mleko
· Jaja
· Soja
· Ryby
· Skorupiaki
· Pszenica
ALERGENY MLEKA
· Mleko krowie - ok. 30 różnych białek o potencjalnym charakterze alergennym, stanowiących ok. 30-35 g masy w litrze.
· W wyniku koagulacji uzyskuje się dwie frakcje - kazeinę i białka serwatkowe, stanowiące odpowiednio ok. 80 i 20%.
· Kazeina:
- białko najbardziej przydatne jako materiał budulcowy do syntezy hemoglobiny i białek osocza krwi,
- posiada wysoką wartość biologiczną, dorównującą białku mięsa i znacznie przewyższającą wartość białek zbóż i roślin strączkowych,
- wysoka zawartość takich aminokwasów jak: walina, leucyna, prolina, lizyna, kwas glutaminowy i kwas asparaginowy.
- w porównaniu z białkiem jaja kurzego wykazuje niedobór cystyny i cysteiny, natomiast może być cennym lizynowym uzupełnieniem produktów zbożowych.
-W skład kazeiny wchodzą cztery różne frakcje: a S1, a S2, b i k, tworzące micele. 55% kazeiny stanowi frakcja αs, 25% frakcja β, 5% frakcja γ, a dalsze 15% frakcja к.
-Budowa miceli nie jest jednorodna. Poszczególne frakcje kazeiny mają zróżnicowaną budowę I-rzędową oraz charakteryzują się różnymi właściwościami funkcjonalnymi.
-αS1, a S2, b-kazeina są podatne na działanie jonów wapnia, zaś k-kazeina nie. Cząsteczka kazeiny jest odporna na działanie wysokich temperatur, ale wrażliwa na obecność proteinaz i egzopeptydaz; łatwo ulega hydrolizie proteolitycznej podczas procesów trawiennych.
-Homologi kazeiny mleka krowiego występujące w mleku innych zwierząt, np. kozy czy kobyły, są w 80-90% identyczne pod względem budowy chemicznej, co wskazuje na bezzasadność wprowadzania tych rodzajów mleka do diety alergików.
-Pacjenci uczuleni na kazeinę są z reguły alergikami wrażliwymi na wszystkie cztery frakcje tego białka.
-Immunologiczna obrona organizmu wyrażająca się powstawaniem przeciwciał antykazeinowych klasy IgE wiąże się ze zjawiskiem reakcji krzyżowych pomiędzy epitopami poszczególnych frakcji kazeinowych.
· BIAŁKA SERWATKOWE:
-Wśród białek serwatkowych najsilniejszymi alergenami są: β-laktoglobulina (β-lg) i a-laktoalbumina (α-la).
-Specyficzna struktura β-laktoglobuliny pozwala na interakcje z kazeiną podczas stosowania procesów termicznych. β-lg jest relatywnie odporna na hydrolizę kwasową i działanie proteaz, dlatego też w dużym stopniu pozostaje niestrawiona podczas obecności w układzie pokarmowym, głównie w śluzówce jelita.
-Bardzo korzystnym zjawiskiem jest możliwość wzbudzenia tolerancji organizmu poprzez podawanie niewielkich dawek antygenu w postaci np. wybranych zhydrolizowanych frakcji β-lg.
-β-lg nie występuje w natywnym mleku kobiecym, ale może być wykryta jako zanieczyszczenie obecne w wyniku diety, w składzie której znajduje się mleko krowie.
-α-la stanowi składnik systemu enzymatycznego transferazy galaktozydowej odpowiedzialnej za proces syntezy laktozy.
-α-la pochodząca z mleka krowiego wykazuje duże podobieństwo w budowie do α-la pochodzenia ludzkiego.
ALERGENY JAJA:
¢Jaja są często spożywane przez ludzi i stanowią drugi w kolejności po mleku krowim, pokarm obcogatunkowy wprowadzany do diety dziecka.
¢Najwięcej uczuleń na jajko spotyka się w 4÷5 roku życia, raczej nie później niż w pierwszej dekadzie.
¢Jajo składa się w 56-61% z białka i w 27-32% z żółtka, resztę stanowi skorupka (ok. 8-12%).
¢Białko jaja to głównie woda (ok. 88%) i część białkowa (~ 10%), która stanowi najważniejsze źródło alergenów.
¢Żółtko składa się z wody (50%), lipidów (34%) i białka (16%).
¢Najczęściej uczulającym białkiem jest:
- owotransferyna (53%),
- owomukoid (38%),
- owoalbumina (32%)
- lizozym (15%).
¢Z reguły 100% badanych pacjentów-alergików uczulonych na jajo kurze wykazuje pozytywną reakcję na obecność owoalbuminy.
¢Wśród białek obecnych w żółtku jaja zwraca uwagę a-liwityna, która może uczulać poprzez drogi oddechowe.
¢Apowitelina jest kolejnym alergenem wyizolowanym z frakcji lipoproteinowej żółtka jaja kurzego. Stwierdzono, że apowitelina I i VI są głównymi alergenami jaja . Do alergenów o mniejszym znaczeniu immunologicznym zalicza się lizozym, owomucynę i foswitynę.
¢Najwięcej uczuleń na jajo dotyczy dzieci w 4 -5 roku życia
¢Alergia na jaja może być również chorobą zawodową pracowników zatrudnionych w przetwórstwie jaj. Pomiary stężenia alergenu w pomieszczeniach zakładu pracy wskazywały na ich obecność zarówno w miejscu bezpośredniego kontaktu w obrębie linii technologicznych, jak i w przyległych pomieszczeniach biurowych. Dlatego też zalecany jest środowiskowy monitoring stężenia alergenu jaja w przetwórniach .
ALERGENY RYB
¢Historyczna rola alergii spowodowanej spożywaniem ryb (tzw. opaczne reakcje organizmu).
¢Białko wyizolowane z tkanki mięsnej ryb posłużyło Prausnitzowi i Kustnerowi do udowodnienia istnienia w surowicy krwi czynnika, który wiele lat później zdefiniowano jako immunoglobulinę klasy IgE.
¢Białko to było pierwszym alergenem, którego sekwencja aminokwasowa została opisana, a alergen nazwano Cod M, zapoczątkowując tym samym stosowanie nowej nomenklatury dla alergenów. W późniejszej systematyce nazwę zmieniono na Gad c1.
¢Alergia na ryby zdarza się częściej w krajach, gdzie spożycie ryb jest wyższe (Norwegia, Japonia) niż obserwowane przeciętnie w pozostałych państwach.
¢Gad c 1 jest głównym alergenem, który został wyizolowany z tkanki mięsnej dorsza i sklasyfikowany jako parwalbumina. Białka należące do tej grupy kontrolują ruch jonów wapnia z i do komórki. Stwierdzono ich obecność w mięśniach ryb (0,05-0,1%) i gadów. Obecność białka zbliżonego w swojej strukturze do Gad c 1 została potwierdzona w tkance mięsnej innych gatunków ryb, np. karpia czy szczupaka.
ALERGENY SKORUPIAKÓW
¢Spożywanie skorupiaków w Polsce ogranicza się do szczególnych okazji i nie jest powszechne. Na świecie jednak stanowi na tyle istotny problem, że skorupiaki trafiły na listę "wielkiej ósemki" jako rodzaj pożywienia o wysokim potencjale alergennym.
¢W Stanach Zjednoczonych rozróżnia się ok. 30 jadalnych gatunków skorupiaków, m. in. krewetki, kraby, langusty i raki.
¢Alergeny krewetki należą do najlepiej scharakteryzowanych. Oszacowano, że spożycie 1÷2 krewetek średniej wielkości jest w stanie pobudzić reakcję anafilaktyczną u uczulonych osób.
¢Uczulenia na alergeny krabów zauważono głównie w środowiskach zawodowo związanych z przetwarzaniem mięsa krabów. Reakcje IgE-zależne dotyczą głównie ekstraktów uzyskanych podczas gotowania krabów, nie zaś podczas kontaktu z surowcem w stanie nieprzetworzonym.
¢Tropomiozyna została również określona jako alergen langusty, Pan s 1 (Panulirus stimpsoni) i Hom a 1, homara amerykańskiego (Homarus americanus). Obydwa te białka zostały sklonowane, przebadano ich sekwencje i stwierdzono, że są homologiczne do alergenu krewetki Pen a 1.
ALERGENY ORZECHÓW ARACHIDOWYCH
¢Orzechy arachidowe (Arachis hypogeae) należą do rodziny roślin strączkowych. Stanowią wartościowy składnik żywności, ale jednocześnie są popularnym źródłem wielu silnych alergenów.
¢Około 7-10% białka ogółem zawiera substancje białkowe o stwierdzonym charakterze alergennym. Dwoma najbardziej znanymi, wyizolowanymi i scharakteryzowanymi alergenami orzechów arachidowych są białka Ara h 1 i Ara h 2.
¢Ostatnio wyizolowane alergeny występujące w składzie orzeszków arachidowych oznaczono kolejno Ara h 4 (36 kDa), Ara h 5 (14 kDa), Ara h 6 (16kDa), Ara h 7 (14,5 kDa). Wyizolowano również ostatnio nowy alergen orzeszków ziemnych należący do oleozyn, rodziny niskocząsteczkowych białek biorących udział w formowaniu ciał tłuszczowych arachidów.
¢Reakcje IgE-zależne były silniejsze dla ekstraktów uzyskanych dla orzeszków prażonych, niż dla natywnych.
¢Częstotliwość występowania alergii na orzeszki arachidowe wynosi ok. 0,5 ÷ 0,7% populacji ogółem. Ten rodzaj alergii pokarmowej jest najpowszechniejszy w Stanach Zjednoczonych (ok. 2 mln pacjentów), a w Europie w takich krajach jak Wielka Brytania, Holandia, Francja. Problem alergii na orzeszki ziemne praktycznie nie występuje w Niemczech, chociaż badania wykonywane w tym kierunku wskazują pojawienie się symptomów chorobowych wśród pacjentów, zbliżonych do zanotowanych wcześniej w Ameryce czy Wielkiej Brytanii.
¢W krajach o odmiennych preferencjach pokarmowych problem ten przedstawia się jeszcze inaczej, i tak np. w Arabii Saudyjskiej ok. 20% pacjentów-alergików cierpi na ten rodzaj alergii. Uczulenia na arachidy są tam najczęściej występującą formą choroby, powodującą częste przypadki anafilaksji.
¢Nie została określona w sposób jednoznaczny ilość progowa dawki białka arachidowego, która może pobudzić organizm do walki z alergenem.
ALERGENY SOI
¢Soja- popularne źródło białka wprowadzanym do diety dziecka już w okresie niemowlęcym w postaci specjalnych odżywek, szczególnie dla tych, które wykazują alergie na mleko krowie.
¢W 50% dzieci reagujących alergicznie na mleko jest również uczulone na soję.
¢Głównym scharakteryzowanym alergenem soi jest Gly m 1. Sekwencja aminokwasowa cząsteczki Gly m1jestzbliżona do budowy papainy oraz proteinazy tiolowej. Alergen Gly m1 w 30% posiada identyczną budowę jak Der p1, główny alergen kurzu, który także jest proteazą tiolową.
¢Inne alergeny w soji: Gly m2, Gly m3, Gly m Bd30k.
¢Zidentyfikowano również alergeny występujące w lecytynie sojowej, która jest stosowana powszechnie jako emulgator w procesach technologicznych przemysłu spożywczego, farmacji i produkcji kosmetyków. Lecytyna składa się głównie z fosfolipidów, aczkolwiek potwierdzono także obecność białek powodujących reakcje IgE-zależne. Lecytyna soi może być również źródłem tzw. ukrytych alergenów .
ALERGENY PSZENICY
¢Uczulenia dotyczą głównie osób zawodowo narażonych na ekspozycje alergenami zbóż np. pracownicy przetwórni zbóż i piekarze.
¢Głównym alergenem mogącym przyczynić się do anafilaksji jest Tri a 19 (omega - 5 gliadyna) - białko odpowiadające za natychmiastową reakcję alergiczną u dzieci.
¢Uczulenia na pszenicę nie należy mylić z celiakią, czyli chorobą trzewną, która jest enteropatią glutenową. Gluten występujący najobficiej w pszenicy, ale też i w życie, jęczmieniu oraz owsie, jest główną przyczyną zmian w obrębie jelita czczego. Jedynie dieta bezglutenowa pozwala na pozbycie się symptomów celiakii. Za bezglutenowe uważa się prolaminy ryżu, kukurydzy, prosa i sorga, a także grykę .
12. Pojęcie nietolerancji pokarmowej oraz reakcji alergicznej na pokarm. Formy reakcji alergicznych.
Nietolerancja pokarmowa - szereg odtwarzalnych, niepożądanych reakcji na pokarm, w tym :
-reakcji alergicznych, które z definicji związane są z systemem odpornościowym (np. alergia na orzechy arachidowe lub celiakia),
-niepożądanych reakcji będących wynikiem niedoboru pewnych enzymów (np. nietolerancja laktozy lub dziedziczna nietolerancja fruktozy),
-reakcji farmakologicznych (np. nadwrażliwość na kofeinę) i innych, niezdefiniowanych reakcji.
Do nietolerancji pokarmowej nie zalicza się zatrucia pokarmowego, wywołanego przez bakterie i wirusy, pleśnie, związki chemiczne, toksyny i substancje drażniące obecne w produktach żywnościowych; termin ten nie obejmuje także awersji pokarmowej (niechęć do pewnych produktów i w konsekwencji, unikanie ich).
Reakcje nietolerancji pokarmowej to zwykle odtwarzalne, niepożądane reakcje na określony pokarm lub jego składnik, powstające bez względu na to, czy dana osoba świadoma jest jego spożycia czy też nie.
Alergiczną reakcję na pokarm - niewłaściwa reakcję systemu odpornościowego na spożycie produktu, który u większości osób nie powoduje niepożądanych skutków. Alergiczne reakcje na produkty spożywcze różnią się gwałtownością przebiegu, mogą mieć nawet skutek śmiertelny.
W przypadku alergii pokarmowej, wchodzące w skład pokarmu białko, na które dana osoba jest nadwrażliwa (np. niektóre białka zawarte w orzechach arachidowych), uznawane jest przez system odpornościowy jako niebezpieczne. Składnik taki nosi miano alergenu.
FORMY REAKCJI ALERGICZYCH:
oW których system odpornościowy reaguje na alergen produkcją przeciwciał, zwanych immunoglobulinami E (IgE), które pobudzają inne komórki (np. komórki tuczne) do uwalniania substancji wywołujących stan zapalny.
oReakcje w których istotną rolę odgrywają limfocyty T (np. w celiakii).
Do reakcji IgE-niezależnych zalicza się także późną nadwrażliwość na mleko krowie, chociaż mechanizm powstawania tej alergii nie został do końca zdefiniowany.
Alergia pokarmowa występuje stosunkowo rzadko, choć u osób które na nią cierpią, czyli 1-2% dzieci i mniej niż 1% dorosłych, może mieć przebieg gwałtowny. Termin ten jest często nadużywany dla określenia niepożądanych reakcji na pokarm.
REAKCJA ALERGICZNA
¢Reakcje alergiczne zlokalizowane są zwykle w określonej części ciała, a do objawów zalicza się m.in. egzemę, zaczerwienienie, obrzęk tkanek (np. warg), trudności w oddychaniu.
¢Gwałtowna reakcja może skutkować anafilaksją (np. alergia na orzechy arachidowe z gwałtownym przebiegiem), kiedy to następuje reakcja raczej układowa, objawiająca się nagłym spadkiem ciśnienia krwi i silnym wstrząsem.
Anafilaksja - Jakie są objawy?
Reakcja alergiczna o groźnym przebiegu, charakteryzująca się wystąpieniem niektórych lub wszystkich niżej podanych objawów:
¢Obrzęk tkanek w obrębie jamy ustnej i gardła.
¢Trudności w mówieniu lub przełykaniu.
¢Trudności w oddychaniu.
¢Pokrzywka (swędzące czerwone lub białe wykwity na skórze).
¢Bóle brzucha, nudności, wymioty.
¢Spadek ciśnienia krwi.
¢Zapaść i utrata przytomności.
13. Co to są NNKT, podać znaczenie NNKT dla organizmu człowieka. Wymienić i podać wzory strukturalne kwasów należących do NNKT.
Niezbędne nasycone kwasy tłuszczowe (NNKT):
· Zapobieganiu i leczeniu miażdżycy oraz innych stanów chorobowych prowadzących do zaburzeń gospodarki ustroju lipidami,
· Obniżenie poziomu cholesterolu i triacyloglicerydów w surowicy krwi,
· Zapobiegają powstawaniu zakrzepów naczyniowych, poprawiają pracę serca i przepływ krwi przez naczynia wieńcowe,
· Niektóre z kwasów polienowych są prekursorami prostagladyn, hormonów tkankowych.
14. Rodzaje pożądanych przemian zachodzących w tłuszczach: przeestryfikowanie (rodzaje enzymów, zastosowanie, znaczenie żywieniowe i technologiczne), uwodornienie (rodzaje enzymów, zastosowanie, rodzaje izomerów powstających w trakcie uwodornienia), hydroliza alkaliczna.
1. Interestryfikacja - reakcja wymiany acyli miedzy estrami, głównie między triacyloglicerolami.
Za pomocą tej reakcji można dokonać zmiany sposobu rozkładu kwasów tłuszczowych w triacyloglicerolach jednego lub kilku składników tłuszczowych, uzyskując tłuszcze zmodyfikowane o pożądanym zakresie temperatury topnienia i właściwościach krystalizacyjnych, plastyczności i konsystencji.
Proces ten zmienia strukturę i skład triacylogliceroli, natomiast nie zmienia naturalnej budowy występujących w nich kwasów tłuszczowych. W procesie tym nie powstają nienasycone kwasy tłuszczowe o konfiguracji trans.
Wymiana grup acylowych pomiędzy estrami może zachodzić:
-wewnątrz cząsteczek acylogliceroli tzw. przeestryfikowanie intramolekularne, wewnątrzcząsteczkowe
-pomiędzy cząsteczkami acylogliceroli tzw. przeestryfikowanie intermolekularne, międzycząsteczkowe
Proces przeestryfikowania to reakcja katalityczna.
Jako katalizatory stosowane są m.in.:
katalizatory chemiczne:
• metale alkaliczne (sód, potas, ciekły stop sodu i potasu);
• wodorotlenek sodu;
• alkoholany (CH3ONa, C2H5ONa i glicerynian sodu);
katalizatory biologiczne
Biokatalizatory reakcji enzymatycznego przeestryfikowania, zwane lipazami - hydrolazy estrów glicerolowych.
Zastosowanie procesu przeestryfikowania:
• otrzymywanie margaryny bez izomerów trans (tzw. „zero trans”);
• otrzymywanie tanich substytutów tłuszczów cukierniczych, piekarniczych i kuchennych np.: produkcja ekwiwalentów masła kakaowego;
• otrzymywanie produktów tłuszczowych o lepszych właściwościach żywieniowych i dietetycznych np.: odżywki dla niemowląt, sportowców, preparaty dla osób mających zaburzenia w wydzielaniu żółci i w pracy trzustki
• otrzymywania koncentratów kwasów tłuszczowych szeregu n-3 \
• otrzymywania emulgatorów żywnościowych
2. Uwodornienie polega na wysycaniu wodorem podwójnych wiązań występujących w cząsteczkach kwasów tłuszczowych surowca. Uwodornienie jest reakcją katalityczną, którą można przyspieszać przez niektóre heterogeniczne lub homogeniczne katalizatory, zawierające takie metale, jak Pt, Pd, Ni, Cu i Co. Z tych metali tylko nikiel ma znaczenie przemysłowe. W przypadku katalizatora niklowego stężenie metalu w oleju (zawiesina) wynosi ok. 0,05%. Ponieważ ten proces opiera się na mechanizmie reakcji odwracalnej (uwodornienie-odwodornienie), czynnikiem determinującym jego przebieg jest stężenie wodoru na powierzchni katalizatora.
W celach spożywczych prowadzi się tylko częściowe uwodornienie olejów. Dlatego ważnymi cechami tak prowadzonego procesu są selektywność i izomeryzacja.
Selektywność jest związana z różnymi szybkościami reakcji uwodornienia nienasyconych kwasów tłuszczowych o różnym stopniu nienasycenia (np. trienów, dienów, monoenów).
Izomeryzacja wynika z tego, że podwójne wiązania pozostawione w częściowo uwodornionym tłuszczu mogą mieć zmienioną pozycję lub konfigurację (cis-trans).
Proces uwodornienia tłuszczów jest często stosowany w przemyśle tłuszczowym, do zmiany ich charakteru fizycznego i chemicznego oraz składu występujących w nich kwasów tłuszczowych.
Uwodornienie tłuszczów prowadzi się w dwóch ważnych celach - zwiększenie ich stabilności oksydatywnej oraz przekształcenia olejów w produkty plastyczne, które są bardziej przydatne do wyrobu margaryn i innych tłuszczów jadalnych.
Powstające podczas uwodornienia izomery geometryczne oraz izomery położenia są niekorzystne z punktu widzenia żywieniowego. Badania wykazują, że izomery trans podnoszą poziom frakcji LDL cholesterolu we krwi, zaburzają funkcje komórek limfatycznych, a także mają związek z chorobami nowotworowymi.
3. Hydroliza alkaliczna prowadzi do powstania soli odpowiedniego kwasu oraz alkoholu. Produktami zmydlania tłuszczów są mydła i gliceryna. Mydła to sole sodowe lub potasowe wyższych kwasów tłuszczowych głównie kwasów palmitynowego, stearynowego i oleinowego.
15. Przemiany niepożądane w tłuszczach: autooksydacja (etapy procesu), fotosensybilizowane utlenianie (charakterystyka).
AUTOOKSYDACJA
Autooksydacja jest rodnikową reakcja łańcuchową, w której można wyróżnić trzy podstawowe etapy.
INICJACJA (zapoczątkowanie reakcji) - hemolityczne oderwanie wodoru i utworzenie węglowego rodnika alkilowego w obecności inicjatora.
PROPAGACJA (rozwijanie reakcji) - reakcja rodnika z O2 i utworzenie rodnika nadtlenowego, który następnie reaguje z nienasyconym lipidem (alken-RH) i tworzy się wodoronadtlenek oraz nowy rodnik lipidowy. Nowo powstały rodnik reaguje z O2 tworząc rodnik nadtlenkowy itd. W ten sposób autooksydacja staje się rodnikowym procesem łańcuchowym.
TERMINACJA (zakończenie reakcji). Reakcja łańcuchowa może być zakończona (co oznacza przerwanie łańcucha) na skutek rekombinacji rodników i tworzenia się nierodnikowych produktów, które nie są ani inicjatorami, ani propagatorami reakcji
FOTOUTLENIANIE obejmuje reakcję alkenu z tlenem w obecności światła i odpowiedniego sensybilizatora (uczulacza).
Takie sensybilizatory, jak chlorofil czy erytrozyna, przekształcają tlen w jego bardziej reaktywny stan singletowy. W tym stanie tlen reaguje z alkenem bez wytwarzania rodnika (reakcja enowa), przyłączając się do jednego z węgli podwójnego wiązania.
Ta reakcja jest połączona z migracją podwójnego wiązania i zmianą jego konfiguracji z cis w trans.
Jest inhibowana przez „wygaszacze” tlenu singletowego, jak np. b-karoten czy tokoferole.
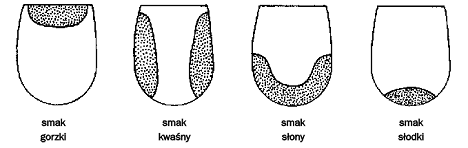
16. Przedstawić rozmieszczenie kubków smakowych na języku. Scharakteryzować smak słodki, słony, gorzki, kwaśny, umami.
[UZUPEŁNIĆ]
17. Witaminy rozpuszczalne w tłuszczach i w wodzie (charakterystyka, źródła występowania, rola w organizmie, skutki niedoboru i nadmiaru).
[CAŁY WYKŁAD]
18. Charakterystyka etapów reakcji Maillarda. Pozytywne i negatywne skutki reakcji Maillarda.
Trzy etapy.
I ETAP
Cukier redukujący reaguje ze związkiem zawierającym wolną grupę aminową (aminokwasy, peptydy lub białka). Produktem tej reakcji są skondensowane N-podstawione glikozyloaminy - aldozoamina lub ketozoamina, które ulegają
przegrupowaniu Amadori tworząc produkty przegrupowania Amadori (1-amino-1-deoksyketoza) bądź
przegrupowaniu Heynsa tworząc produkty przegrupowania Heynsa (2-amino-2-deoksyaldoza).
II ETAP
Produkty przegrupowania Amadori są prekursorami wielu związków odpowiedzialnych za kształtowanie cech sensorycznych produktów żywnościowych.
Procesy cieplnego przetwarzania żywności prowadzą do obniżenia wartości żywieniowej białek, głównie poprzez blokowanie cennego egzogennego aminokwasu, jakim jest lizyna, co prowadzi bezpośrednio do zmniejszenia ilości dostępnej lizyny.
Przykładem wpływu procesów termicznych na jakość białek występujących w danym produkcie jest zmniejszenie dostępnej lizyny w produktach zbożowych, takich jak: makaron, chleb, płatki śniadaniowe czy wyroby ciastkarskie.
Dalsze przemiany produktów zaawansowanej fazy reakcji Maillarda są zależne od pH środowiska.
>Przy pH = 7 oraz w środowisku kwaśnym w reakcji 1,2-enolizacji tworzą się głównie furfurale (F) - gdy w próbce występują pentozy, lub hydroksyfurfurale (HMF) - gdy w próbce występują heksozy (Związki te są niepożądane w produktach spożywczych - toksyczność, mutagenność? )
>Przy pH > 7 przemiany produktów przegrupowania Amadori obejmują głównie 2,3-enolizację, podczas której powstają reduktony tj. 4-hydroksy-5-metylo-2,3-dihydrofuran-3-on i tworzą się różne produkty rozszczepienia, włączając acetal, diacetyl i aldehyd pirogronowy.
Wszystkie te związki są wysoce reaktywne i uczestniczą w dalszych reakcjach.
Jednym z najlepiej scharakteryzowanych związków z grupy produktów zaawansowanej fazy reakcji Maillarda jest N-α-karboksymetylolizyna (CML)
III ETAP
Obejmuje wiele zachodzących po sobie reakcji tj. cyklizację, dehydratację i kondensację, prowadzących do powstania barwnych związków wielkocząsteczkowych.
Dzieli się je (w zależności od masy molekularnej) na dwie klasy: związki niskocząsteczkowe oraz melanoidyny - wielkocząsteczkowe polimery.
Melanoidyny są szeroko rozpowszechnione w produktach żywnościowych - nadają brązowy kolor i wpływają na ich jakość. W znacznych ilościach występują w kawie, kakao, chlebie i miodzie.
POZYTYWNE I NEGATYWNE EFEKTY REAKCJI MAILLARDA:
W wyniku reakcji Maillarda tworzą się zaawansowane końcowe produkty odpowiedzialne za niszczenie struktur podstawowych aminokwasów, obniżenie strawności białek, inaktywację enzymów oraz obniżenie podatności białek na proteolizę. Produktami reakcji są zatem zarówno substancje uznawane za kancerogenne i mutagenne, jak i substancje wykazujące właściwości przeciwutleniające i przeciwbakteryjne, wywierające pozytywny wpływ na organizm człowieka.
Reakcje Maillarda są powszechnym problemem w przechowywanym odtłuszczonym sproszkowanym mleku, z uwagi na wysoką koncentrację laktozy i reaktywne białko.
19. Charakterystyka procesu karmelizacji. Rodzaje związków zapachowych powstających podczas karmelizacji. Melanoidyny i ich właściwości.
PROCESY KARMELIZACJA - ogrzewanie roztworów wodnych sacharydów w obecności kwasowych lub zasadowych katalizatorów powodujące szereg następujących po sobie reakcji chemicznych z udziałem cukrów.
W procesie karmelizacji wytwarza się kilka związków zapachowych oraz polimerowych form karmelu.
W zależności od sposobu prowadzenia karmelizacji (temperatura, katalizator) otrzymuje się karmel albo do aromatyzowania środków albo jako barwnik spożywczy.
W reakcji karmelizacji powstają także związki zapachowe. Ważnym związkiem zapachowym, wytwarzanym w pierwszych fazach karmelizacji jest DIACETYL.
Diacetyl odpowiada za zapach maślany lub mlecznych cukierków.
Poza diacetylem, powstają inne związki zapachowe, na przykład FURANY jak hydroksymetylofurfural (HMF) i hydroksyacetylofurfuran (HAF),
FURANONY jak hydroksydimetylofuranon (HDF), dihydroksydimetylofuranon (DDF) oraz maltol z dwucukrów i hydroksymaltol z cukrów prostych.
REAKCJE MAILLARDA zachodzą w żywności pod wpływem podwyższonej temperatury, a także długiego przechowywania.
Hodge opisał schemat reakcji, składający się z 3 etapów: wczesnego, zaawansowanego i końcowego, prowadzący do powstania końcowych produktów reakcji zwanych melanoidynami.
Melanoidyny w żywności:
właściwości przeciwutleniające, które mogą wpływać na długość okresu przechowywania produktów żywnościowych;
działanie przeciwutleniające, antymutagenne, obniżające poziom cholesterolu oraz stymulujące wzrost bakterii jelitowych.
20. Krótka charakterystyka procesu brązowienia enzymatycznego. Enzymy odpowiedzialne za inicjację reakcji brązowienia.
Brązowa barwa, która pojawia się po nacięciu lub zeskrobaniu powierzchni owoców (jabłka, banany), warzyw (surowe ziemniaki), wystawionej na działanie powietrza, jest wynikiem działania enzymów, a samo zjawisko nazywa się BRĄZOWIENIEM ENZYMATYCZNYM.
Enzymy odpowiedzialne za inicjację reakcji brązowienia to: FENOLAZA, FENOLOKSYDAZA, TYROZYNAZA, POLIFENOLOOKSYDAZA I KATECHOLAZA.
W roślinach enzym najczęściej nazywa się polifenolooksydazą (PPO) - jego głównym substratem są polifenole. Jest on odpowiedzialny za istotne zmiany koloru (pożądane jak i niepożądane) w żywności. W nienaruszonej tkance rośliny enzym i jego substraty są oddzielone przez strukturę komórki i brązowienie nie zachodzi. Cięcie lub inne uszkodzenie integralności tkanki pozwala enzymom i substratom na wejście w kontakt. Wystawienie tych powierzchni na działanie tlenu powoduje gwałtowną reakcję brązowienia.
Polifenoloksydaza (PPO) katalizuje dwa typy reakcji: hydroksylację i oksydację. Typowymi substratami dla PPO w tkankach roślin są : aminokwas tyrozyna, polifenole jak katechina, kwas kawowy i kwas chlorogenowy.
Istnieją trzy składniki niezbędne dla przebiegu brązowienia enzymatycznego: aktywna polifenolooksydaza, tlen i odpowiedni substrat. Eliminacja jednego z nich może zapobiec reakcji brązowienia. Dodatkowo, obecność czynnika redukującego zdolnego do zamiany oquinonów z powrotem do związków fenolowych może efektywnie hamować brązowienie.
Wyszukiwarka