Sprawozdanie z ćwiczenia nr 25: Energia aktywacji przepływu lepkiego.
Wstęp teoretyczny:
Wyobraźmy sobie strumień cieczy przepływającej w dodatnim kierunku osi x z prędkością v. Prędkość strumienia cieczy, podobnie jak gazu, nie jest jednolita. W strumieniu panuje gradient prędkości w kierunku osi z. Siłę tarcia wewnętrznego, odpowiedzialną za powstanie tego gradientu, opisuje dla większości cieczy prawo Newtona: chcąc utrzymać przepływ cieczy i tym samym związany z nim gradient prędkości makroskopowej dv/dz należy działać siłą:
![]()
gdzie: S - pole przesuwanej warstwy cieczy; - współczynnik lepkości dynamicznej.
Wartości liczbowe są dla cieczy znacznie większe niż dla gazów.
W niektórych zagadnieniach przepływu lepkiego wygodniej jest posługiwać się tzw. współczynnikiem lepkości kinematycznej v, który zdefiniowany jest wzorem:
![]()
gdzie: ρ - gęstość.
Jednostka lepkości kinematycznej w układzie cgs nazywa się stokes. Czasami wprowadza się też wielkość zwaną płynnością, będącą odwrotnością współczynnika lepkości dynamicznej.
Współczynnik lepkości cieczy jest, przeciwnie niż gazów, malejącą funkcją temperatury, dającą się zazwyczaj przedstawić równaniem Arrheniusa - Guzmana:
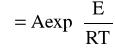
W tym równaniu A i E są wielkościami stałymi, charakterystycznymi dla danej cieczy. Wielkość E nazywana jest energią aktywacji lepkości. Równanie to dobrze opisuje zachowanie się cieczy niepolarynych; dla cieczy polarynych stwierdza się dość znaczne odstępstwa.
Opracowanie wyników:
Lepkość kinematyczną obliczam ze wzoru:
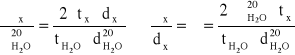
gdzie: x - lepkość gliceryny w odpowiedniej temperaturze [g/(s*cm)] lub [cP]; H2O - lepkość wody w temperaturze 20oC wynosi 1 [g/(s*cm)] lub [cP]; tx - czas przepływu 100 cm3 gliceryny w odpowiedniej temperaturze [s]; tH2O - czas przepływu 100 cm3 wody [s]; dx - gęstość gliceryny w odpowiedniej temperaturze [g/cm3]; dH2O - gęstość wody [g/cm3]; - lepkość kinematyczna [cm2/s] lub [cSt].
Lepkość dynamiczną h obliczam ze wzoru:
![]()
[g/(s*cm)] lub [cP]
Lp. |
Czas wypływu 100 ml cieczy [s] |
Temperatura [K] |
1/T |
Gęstość [g/cm3] |
Lepkość kinematyczna [cst] |
Lepkość dynamiczna |
ln |
1 |
155 |
308,15 |
0,003245 |
1,251 |
6,3 |
7,9 |
2,07 |
2 |
135 |
313,15 |
0,003193 |
1,248 |
5,5 |
6,9 |
1,93 |
3 |
90 |
323,15 |
0,003095 |
1,2415 |
3,7 |
4,6 |
1,52 |
4 |
50 |
333,15 |
0,003002 |
1,235 |
2,0 |
2,5 |
0,93 |
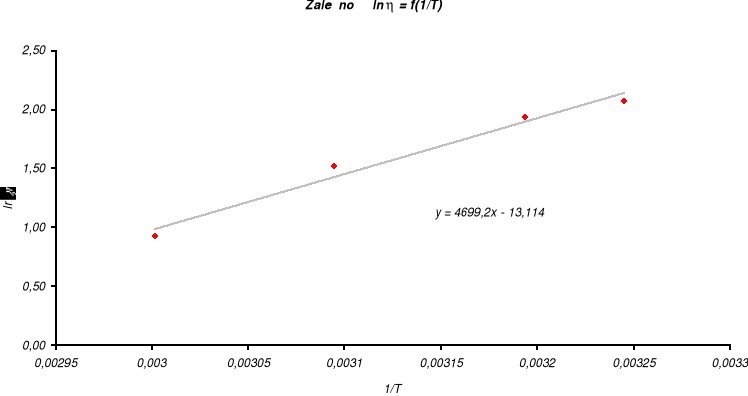
Z danych zawartych w tabeli sporządzam wykres zależności ln = f(1/T) oraz obliczam regresję liniową i błędy regresji:
1/T = x |
ln = y |
x2 |
x*y |
0,003245 |
2,07 |
1,05E-05 |
6,72E-03 |
0,003193 |
1,93 |
1,02E-05 |
6,16E-03 |
0,003095 |
1,52 |
9,58E-06 |
4,70E-03 |
0,003002 |
0,93 |
9,01E-06 |
2,78E-03 |
Współczynniki prostej liniowej:
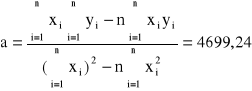
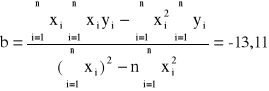
Błędy regresji:
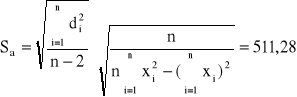
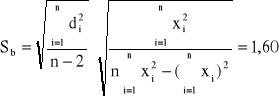
Korzystając z równania Arrheniusa - Guzmana oraz z równania prostej na wykresie wyznaczam stałe:
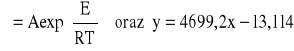
Wpierw logarytmuje równanie A. - G., w wyniku czego otrzymuje:
![]()
W równaniu tym ln = y (z równania liniowego: y = ax + b), lnA = b, E/R = a oraz 1/T = x. Z powyższych założeń można wyznaczyć stałe dla równania:
![]()
które wynoszą odpowiednio: A'= E/R = 4699,2 oraz B = lnA = -13,114.
Korzystając z założeń i stałych równania wyznaczam energię aktywacji przepływu lepkiego:
![]()
Błąd energii aktywacji obliczam ze wzoru (gdzie A' = Sa):
![]()
Energia aktywacji przepływu lepkiego wynosi: 39,07![]()
4,25 [kJ/mol].
Błędy dla lepkości dynamicznej obliczam ze wzoru:
![]()
gdzie: dT = 1 [K]; T - temperatura [K]; A = 4699,2; B = -13,114; dA = Sa; dB = Sb.
![]()
![]()
![]()
![]()
![]()
Wnioski.
Z doświadczenia i obliczeń wynika, że lepkość zależna jest od temperatury oraz ze wzrostem temperatury lepkość cieczy maleje. Z wykresu wynika, że ln jest liniową funkcją odwrotności temperatury. Energia aktywacji przepływu lepkiego wynosi 39,07![]()
4,25 [kJ/mol]. Błędy powstałe w eksperymencie wynikać mogą z źle odmierzonego czasu wypływu oraz złego odczytu temperatury.
3
Wyszukiwarka
Podobne podstrony:
Iloczyn rozpuszczalności soli trodno rozpuszczalnych, studia, chemia, chemia fizyczna, sprawozdania,
HCOOH, studia, chemia, chemia fizyczna, sprawozdania, sprawka
Diagram fazowy Gibbsa, studia, chemia, chemia fizyczna, sprawozdania, sprawka
Entropia mieszania, studia, chemia, chemia fizyczna, sprawozdania, sprawka
Energia aktywacji przepływu lepkiego
Badanie lepkości cieczy metodą Hopplera, studia, chemia, chemia fizyczna, sprawozdania, sprawka
izoterma adsorbcji, studia, chemia, chemia fizyczna, sprawozdania, sprawka
Stała szybkości reakcji jodowania acetonu, studia, chemia, chemia fizyczna, sprawozdania, sprawka
Ciepło rozpuszczania soli jonowej, studia, chemia, chemia fizyczna, sprawozdania, sprawka
Kinetyka reakcji elektroutlenienia 1-propanolu, studia, chemia, chemia fizyczna, sprawozdania, spraw
Elektronowe widma absorpcyjne, studia, chemia, chemia fizyczna, sprawozdania, sprawka
Dyspersja współczynnika załamania światła, studia, chemia, chemia fizyczna, sprawozdania, sprawka
HCl i HJ, studia, chemia, chemia fizyczna, sprawozdania, sprawka
Jonity1, studia, chemia, chemia fizyczna, sprawozdania, sprawka
Izoterma adsorpcji 1, studia, chemia, chemia fizyczna, sprawozdania, sprawka
HCl, studia, chemia, chemia fizyczna, sprawozdania, sprawka
HJ, studia, chemia, chemia fizyczna, sprawozdania, sprawka
Grupy symetrii, studia, chemia, chemia fizyczna, sprawozdania, sprawka
Entalpia parowania, studia, chemia, chemia fizyczna, sprawozdania, sprawka
więcej podobnych podstron