Numer i tytuł ćwiczenia: 7-2. Wyznaczanie klasycznej stałej dysocjacji z pomiarów przewodnictwa. |
|||||
Imię i nazwisko osoby prowadzącej zajęcia: Dr Ewa Więckowska-Bryłka |
|||||
Data wykonania ćwiczenia: |
Godzina: |
Numer grupy studenckiej |
Zespół |
Nazwiska osób wykonywujących ćwiczenie: |
Punkty za spr. |
21.04.15 |
8.15-11.00 |
8 |
K |
Agnieszka Ordyniak Karolina Podbielska Milena Podlińska |
|
Uwagi prowadzącego: |
|
||||
Sprawozdanie z ćwiczeń chemii fizycznej
Cel ćwiczenia:
Opanowanie pomiaru przewodnictwa właściwego, poznanie metody wyznaczania stałej konduktometrycznej maczynka, zapoznanie z takimi wielkościami fizykochemiczne jak: przewodnictwo właściwe, równoważnikowe, stopień dysocjacji i stała dysocjacji.
Wstęp teoretyczny:
Stopień dysocjacji słabych elektrolitów inaczej niż elektrolity mocne, które ulegają w roztworach wodnych całkowitej dysocjacji, zależy w wyraźny sposób od stężenia. Charakter tej zależności można określić za pomocą termodynamiki. Między cząsteczkami niezdysocjowanymi i powstałymi w wyniku dysocjacji jonami ustala się stan równowagi termodynamicznej z charakterystyczną dla danego elektrolitu stałą dysocjacji(K), która nie zależy od stężenia i jest tylko funkcją temperatury i ciśnienia.
Duże znaczenie praktyczne ma prawo rozcieńczeń Ostwalda
![]()
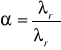
gdzie Kc jest stałą dysocjacji, która można wyznaczyć eksperymentalnie. (Wystarczy w tym celu określić np. na podstawie pomiarów przewodnictwa elektrycznego roztworów, stopień dysocjacji danego elektrolitu).W miarę rozcieńczania roztworu wzajemne oddziaływania między składnikami elektrolitu maleją i współczynniki aktywności przybierają wartości coraz bardziej zbliżone do jedności.
Pomiar przewodnictwa właściwego - pomiar oporu/przewodnictwa przewodnika w omomierzach/konduktomierzach. Składa się to z 2 etapów:
1. wyznaczenie stałej naczynka ( pojemność oporowa) , np. ze wzoru (za pomocą wyznaczenia przewodnictwa właściwego i przewodnictwa cieczy wzorcowej)
![]()
2. Wyznaczenie oporu/przewodnictwa roztworu z powyższego wzoru (przewodnictwo w znacznym stopniu zależy od temperatury - zmiana temp o 1K powoduje wzrost przewodnictwa średnio o 2-2.5%).
Przewodnictwo równoważnikowe roztworu elektorlitu mocnego zmienia się w niewileku stopniu wraz ze zmianą steżenia, dla słabych elektrolitów zmiany są bardzo duże. Można je wyliczyć ze wzoru:
![]()
Wykonanie ćwiczenia:
W pierwszej części ćwiczenia obliczaliśmy stałą naczynka konduktometrycznego.
Zadanie polegało na trzykrotnym zmierzeniu przewodnictwa roztworu KCl o stężeniach 0,020, 0,010, 0,005 mol/dm3 oraz znanym przewodnictwie właściwym. Z otrzymanych wyników wyliczyliśmy stałą naczynka, a następnie wartość średnią k (za pomoca wyżej wskazanego wzoru), jako średnią arytmetyczną poszczególnych wyników.
Numer roztworu: |
C [mol/dm3] |
ϰwz [S/m] |
λwz [S] |
k= ϰwz/ λwz [m-1] |
Wartość średnia k [m-1] |
1 |
0,020 |
0,27335 |
0,005203 |
52,5370 |
53,4645 |
2 |
0,010 |
0,14180 |
0,002607 |
54,3920 |
|
3 |
0,005 |
0,07525 |
0,001245 |
60,4418 |
|
λwz=(0,00520+0,00521+0,00520)/3=0,005203[S]
λwz=(0,00262+0,00259+0,00261)/3=0,002607[S]
λwz=(0,001243+0,001241+0,001252)/3=0,001245 [S]
k=0,27335/0,005203=52,5370 [1/m]
k=0,14180/0,002607=54,3920 [1/m]
k=0,07525/0,001245=60,4418 [1/m]
średnia wartość k: k=(52,5370 +54,3920)/2=53,4645 [1/m]
Druga część zadania polegała na wyznaczeniu stałej dysocjacji słabego elektrolitu.
Otrzymany roztwór CH3COOH rozcięczyliśmy do objętości 100 cm3, (wodą destylowaną) i dla tego roztworu wykonaliśmy pomiar przewodnictwa (również 3 razy). Następnie odmierzyłyśmy za pomocą pipety 50 cm 3 roztworu do oddzielnej zlewki i dodaliśmy 50 cm3 wody destylowanej (roztwór rozcieńczony dwukrotnie), zmierzyłyśmy przewodnictwo (w taki sam sposób wykonaliśmy jeszcze 4 pomiary). Otrzymane wartości zapisałyśmy w dołączonej tabeli. Obliczyłyśmy przewodnictwo właściwe, przewodnictwo równoważnikowe, stopień dysocjacji, stałą dysocjacji K i średnią jej wartość.
Obliczenia:
Przewodnictwo
Nr r-ru |
c stężenie molowe r-ru [mol·m-3] |
przewodnictwo λ [S] |
przewodnictwo właściwe χ=kλ [S·m-1] |
przewodnictwo równoważnikowe λr=χ/c [S·m2·mol-1] |
stopień dysocjacji α=λr/λr |
stała dysocjacji
|
Średnia stała dysocjacji |
1 |
16,7 |
0,000387 |
0,0207 |
0,001240 |
0,03174 |
0,01738 |
0,01652 |
2 |
8,35 |
0,000269 |
0,01438 |
0,001722 |
0,04402 |
0,01693 |
|
3 |
4,175 |
0,0001875 |
0,01002 |
0,0024 |
0,06143 |
0,01679 |
|
4 |
2,0875 |
0,000128 |
0,006843 |
0,00328 |
0,08395 |
0,01607 |
|
5 |
1,0434 |
0,00008733 |
0,0004669 |
0,00447 |
0,1144 |
0,01542 |
|
λ=(0,000389+0,000386+0,000386)/3=0,000387 [S]
λ=(0,000269+0,000269+0,000269)/3=0,000269 [S]
λ=(0,0001877+0,0001874+0,0001874)/3=0,0001875 [S]
λ=(0,0001288+0,0001291+0,0001285)/3=0,000128 [S]
λ=(0,0000867+0,0000875+0,0000878)/3=0,00008733 [S]
Przewodnictwo właściwe(χ=kλ) :
χ=53,4645*0,000387=0,02070 [S/m]
χ=53,4645*0,000269=0,01438 [S/m]
χ=53,4645*0,0001875=0,01002 [S/m]
χ=53,46450,000128=0,006843 [S/m]
χ=53,4645*0,00008733=0,0004669 [S/m]
Przewodnictwo równoważnikowe (λr=χ/c) :
λr=0,0207/16,7=0,001240 [S*m2/mol]
λr=0,01438/8,35=0,001722 [S*m2/mol]
λr=0,01002/4,175=0,0024 S*m2/mol]
λr=0,006843/2,0875=0,00328 [S*m2/mol ]
λr=0,0004669/1,0434=0,00447 [S*m2/mol]
Stopień dysocjacji (α=λr/λr):
α=0,001240/0,3907=0,031740,031
α=0,001722/0,3907=0,04402
α=0,0024/0,3907=0,06143
α=0,00328/0,3907=0,08395
α=0,00447/0,3907=0,1144
Stała dysocjacji:
K=(0,03174*0,03174*16,7)/1-0,03174=0,01738
K=(0,04402*0,04402*8,35)/1-0,04402=0,01693
K=(0,06143*0,06143*4,175)/1-0,06143=0,01679
K=(0,08395*0,08395*2,0875)/1-0,08395=0,01607
K=(0,1144*0,1144*1,0434)/1-0,1144=0,01542
Średnia stała dysocjacji:
Kśr=(0,01738+0,01693+0,01679+0,01607+0,01542)/5=0,01652
Wnioski i obserwacje:
Kwas octowy jest słabym elektrolitem, ponieważ:
Wraz ze wzrostem stężenia roztworu rośnie wartość przewodnictwa właściwego. Można jednak zauważyć na wykresie, że elektrolit nie osiągną jeszcze maksymalnej wartości przewodnictwa, gdyż nie nastąpił nie nastąpił spadek przewodnictwa.
Wraz ze wzrostem stężenia roztworu, maleje wartość przewodnictwa równoważnikowego.
Stała dysocjacji kwasu octowego jest niemalże jednakowa, niezależnie od stężenia roztworu.
Błędy w pomiarach mogą wynikać z:
Niedokładnego odmierzenia objętości roztworów,
Nieprecyzyjnego ogrzania roztworów,
Niedostatecznego zanurzenia elektrod naczynka konduktometrycznego w roztworach.
Wyszukiwarka
Podobne podstrony:
7[1].1(2), Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, chemia fizyczna, s
SPRAWOZDANIE-4-1-1, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, chemia fi
10-1-gr-11-A, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, chemia fizyczna
127d879b364443a7c898e032e415ed88, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia organ
2015 pyt tren do wykł VII, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, ch
ch fizyczna 13, POLITECHNIKA ŁÓDZKA, Technologia Żywności i Żywienia Człowieka, semestr 4, Chemia fi
pytania treningowe wykład II 2015, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizy
chemia zywnos, POLITECHNIKA ŁÓDZKA, Technologia Żywności i Żywienia Człowieka, semestr 4, Chemia Żyw
Zagadnienia teoretyczne 41, POLITECHNIKA ŁÓDZKA, Technologia Żywności i Żywienia Człowieka, semestr
2015 pytania tren do wykł VI, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna,
pyt tren wykł III 2015, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, chem
6-1, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, chemia fizyczna, sprawoz
Część teoretyczna do kolokwium C, POLITECHNIKA ŁÓDZKA, Technologia Żywności i Żywienia Człowieka, se
8-1, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, chemia fizyczna, sprawoz
Fizyczna 43, POLITECHNIKA ŁÓDZKA, Technologia Żywności i Żywienia Człowieka, semestr 4, Chemia fizyc
wykresy15, POLITECHNIKA ŁÓDZKA, Technologia Żywności i Żywienia Człowieka, semestr 4, Chemia fizyczn
(10-1), Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, chemia fizyczna, spra
więcej podobnych podstron