
HIPERLIPIDEMIA I JEJ TERAPIA.
LEKI HIPOLIPEMICZNE

Statyny
Historię wprowadzenia do lecznictwa statyn
zapoczątkowały badania Japończyka Akiro Endo,
który zainspirowany pracami Fleminga - odkrywcy
peniciliny, poszukiwał pośród produktów
wytwarzanych przez saprofityczne grzyby, substancji
obniżających poziom cholesterolu. W tym celu
przebadał ponad 6000 szczepów pleśni i w 1973 roku
udało mu się wyodrębnić z Penicillum citrinum
związek nazwany później - mewastatyną. Była ona
pierwszym lekiem z grupy statyn zaliczanym do
inhibitorów reduktazy 3-hydroksy-3-metylo-glutarylo-
koenzymu A (HMG-CoA). Nie znalazła ona jednak
wtedy szerszego zastosowania w leczeniu
hiperlipidemii. Odkrycie to ukierunkowało jednak
badania firmy Merck, która w oparciu o strukturę
nowego specyfiku wyprodukowała i wprowadziła do
lecznictwa pierwszy, uznany preparat hipolipemiczny
- lowastatynę.

Pojawiła się ona na rynku amerykańskim w
1987 roku, zapoczątkowując całą serię po
dobnie działających specyfików. Były to:
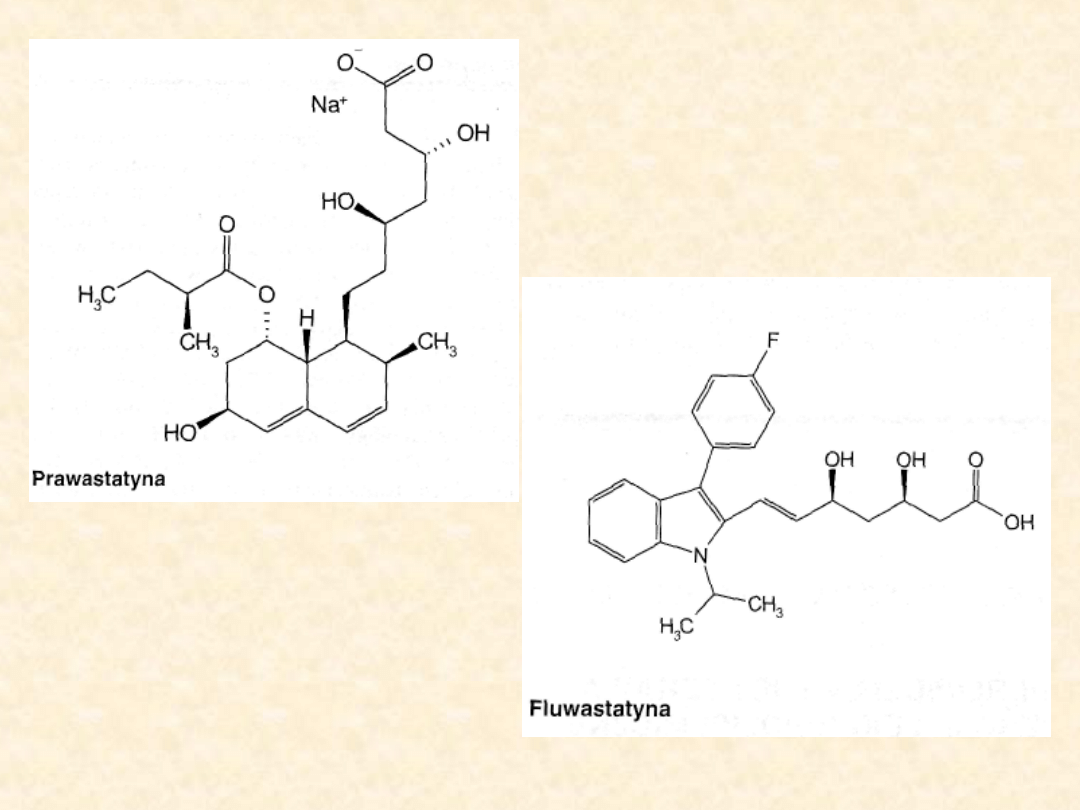
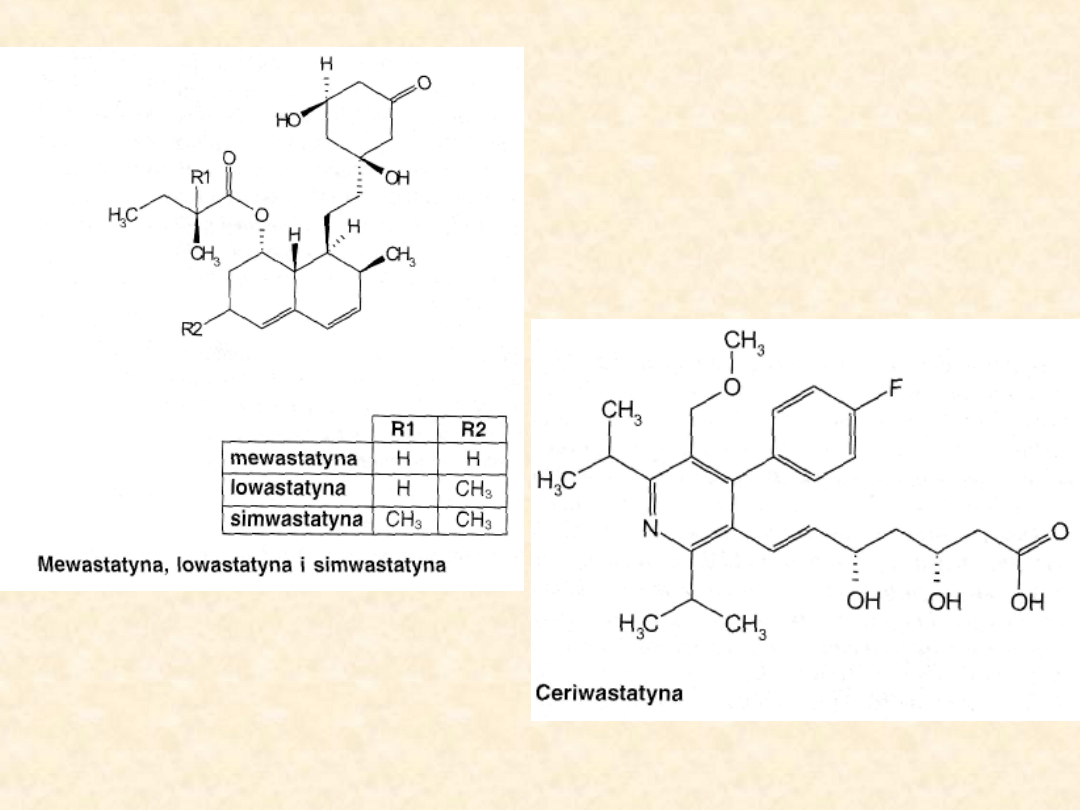
simwastatyna, prawastatyna,
fluwastatyna, ceriwastatyna,
atorwastatyna.
Statyny różnią się pod względem struktury
chemicznej i właściwości
farmakokinetycznych. Wszystkie są jednak
specyficznymi, kompetycyjnymi inhibitorami
reduktazy HMG-CoA, enzymu katalizującego
wczesny etap biosyntezy cholesterolu.
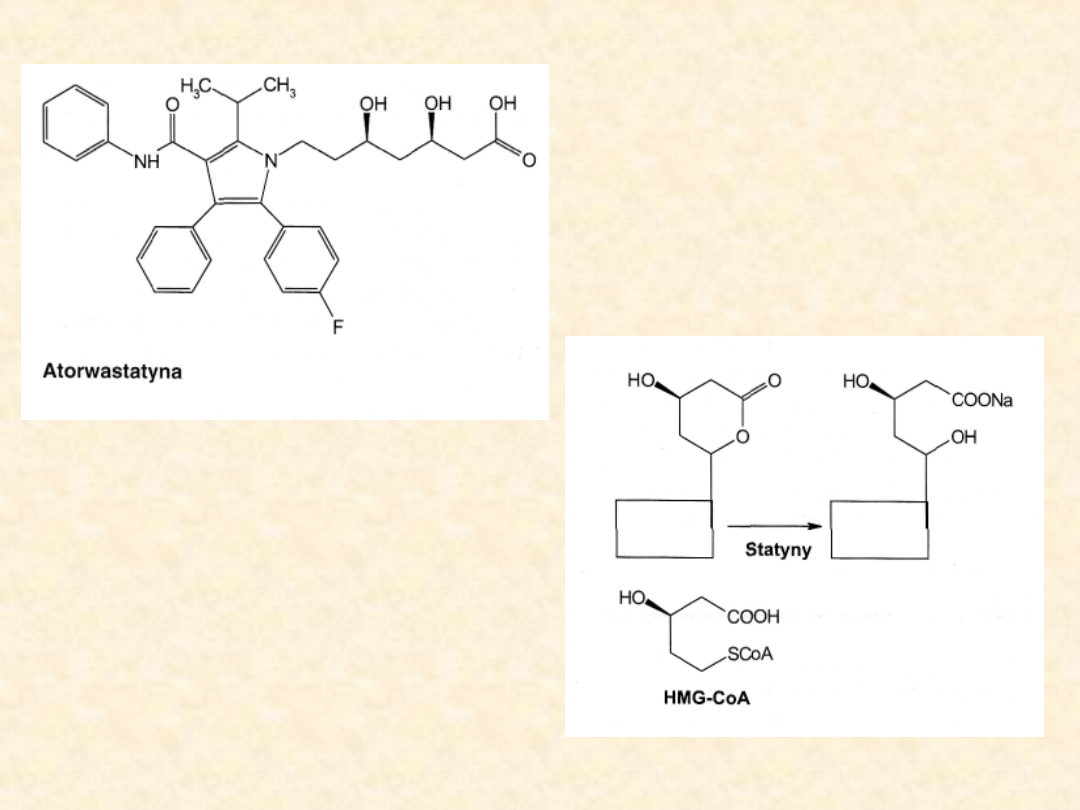
Wykazując podobieństwo strukturalne
fragmentu laktonowego cząsteczki do 3-hyd-
roksy-3-metyloglutarylo-CoA (HMG-CoA),

mogą one reagować z tym samym centrum
aktywnym substratu (HMG-CoA), nie tworząc jednak
dalszych produktów reakcji.
Wśród wymienionych związków trzy o budowie
laktonowej: lowastatyna, simwastatyna i
mewastatyna są prolekami ulegającymi aktywacji
dopiero po enzymatycznej hydrolizie do
odpowiedniego hydroksykwasu.
Hamując produkcję endogennego cholesterolu,
statyny powodują zmniejszenie jego puli w
komórkach wątrobowych, a w efekcie stymulacji
procesu tworzenia receptorów LDL - wzmagając
usuwanie cząsteczek cholesterolu LDL z krążącej
krwi. Stanowi to ich główny mechanizm działania.
Obniżenie poziomu frakcji cholesterolu LDL jest
uzyskiwane także na innej drodze, a mianowicie
poprzez spadek syntezy głównego prekursora LDL w
wątrobie, lipoprotein VLDL.

Wpływ statyn na zmniejszone powstawanie frakcji
VLDL, a także jej remnantów oraz wzrost liczby
receptorów LDL sprzyja nie tylko obniżeniu poziomu
całkowitego cholesterolu w surowicy, ale również
spadkowi stężenia triglicerydów. Siła działania
poszczególnych statyn jest zróżnicowana i zależy
głównie od dawki poszczególnych leków oraz
rodzaju zaburzeń hiperlipemicznych. Efektem
klinicznym jest zazwyczaj obniżenie poziomu
całkowitego cholesterolu w osoczu o 15-30%, frakcji
LDL o 20-40%, poziomu triglicerydów o 10-20% i
wzrost stężenia cholesterolu-HDL o 5-15%.
Należy jednak pamiętać, że leki te nie są efektywne
w hipercholesterolemii rodzinnej (FH),
związanej z defektem genu kodującego receptor
LDL.

Statyny odgrywają istotną rolę w zapobiega niu i
leczeniu miażdżycy. Działanie ich wyraża się
bowiem nie tylko ilościowymi zmianami składu
lipoprotein, ale również bezpośrednim lub
pośrednim wpływem na sam rozwój procesu
miażdżycowego. Rezultatem takiego współdziałania
jest uzyskanie o wiele lepszych efektów
terapeutycznych, niż wynikałoby to jedynie z
samego obniżenia poziomu lipoprotein. Działanie
tego typu nazywane jest działaniem plejotropowym,
czyli niezależnym od głównego wskazania. Statyny
bowiem, z wyjątkiem prawastatyny, hamują
proliferację komórek mięśni gładkich i obniżają
kumulację estrów cholesterolu w makrofagach,
stabilizując w ten sposób zmiany miażdżycowe.
Zapobiegając chemicznej modyfikacji lipoprotein
LDL i ich utlenieniu do związków toksycznych oraz
wolnych rodników, wykazują także właściwości
antyoksydacyjne.

Hamują również agregację płytek oraz obniżają
tkankowy ak tywator plazminogenu (tPA), inhibitor
aktywatora plazminogenu (PAI-1) i poziom
fibrynogenu, wpływając korzystnie na upośledzony
układ krzepnięcia, fibrynolizy i w konsekwencji
obniżając ryzyko zakrzepu. Statyny są na ogół dobrze
tolerowane. W praktyce medycznej należy jednak
pamiętać, że wchodzą w liczne interakcje z innymi
specyfikami. Swoistym przykładem i ostrzeżeniem
świadczącym o konieczności nie lekceważenia tego
problemu może być opisywany w literaturze fachowej
przypadek związany z ceriwastatyną (Lipobay,
Baycol), po podaniu której u niektórych pacjentów
dochodziło do ciężkich, a nawet śmiertelnych
powikłań wywołanych niewydolnością nerek,
spowodowanych mioglobinurią.

Szczegółowo przeprowadzona analizalizą tych
przypadków wykazała, że ich bezpośrednią
przyczyną była rabdomioliza (proces
polegający na uwalnianiu białka z
uszkodzonych mięśni), do której dochodziło w
wyniku interakcji dużych dawek ceriwastatyny
z innym preparatem hipolipemicznym -
gemfibrozilem (fibraty). Doniesienia o
potencjalnie śmiertelnych działaniach
niepożądanych Lipobayu (34 przypadki)
spowodowały wycofanie tego preparatu z
lecznictwa na całym świecie poza Japonią,
gdzie nie stwierdzano takich powikłań,
ponieważ nie stosowano fibratów w leczeniu
hiperlipidemii

Najpoważniejszym powikłaniem obserwowanym
podczas leczenia statynami jest miopatia . Zespół ten
objawia się bólami mięśniowymi, bądź osłabieniem
mięśni i/lub wzrostem stężenia fosfokinazy kreatyny
(CPK). Występuje u 0,1-0,2% pacjentów, choć w
przypadku fluwastatyny i ceriwastatyny odsetek
ten jest znacznie mniejszy i porównywalny do grupy
osób otrzymujących placebo. Prawdopodobieństwo
wystąpienia miopatii i rabdomiolizy prowadzącej, do
niewydolności nerek wzrasta u osób leczonych
statynami, stosowanymi łącznie z innymi lekami, na
przykład cyklosporyną, erytromycyną,
klaritromycyną, kwasem nikotynowym, fibratami,
lekami przeciwgrzybiczymi z grupy azoli,
cymetydyną, metotrek-satem oraz z niektórymi
antagonistami wapnia, na przykład mibefradilem.

Mogą powodować także wzrost aktywności enzymów
wątrobowych w surowicy, głównie aminotransferazy
alaninowej i asparaginowej. Dotyczy to od 0,8%
(fluwastatyna) do 1,9% (lowastatyna) leczonych
osób. Jednak najczęstszymi działaniami
niepożądanymi są zaburzenia żołądkowo-jelitowe (6-
10% leczonych) oraz bóle głowy (4%). Zwykle mają
one charakter przemijający i nie wymagają
przerwania terapii.
Leczenie statynami rozpoczynamy od minimalnych
dawek, stopniowo je zwiększając, aż do uzyskania
oczekiwanych efektów leczenia. Podczas terapii
niezbędne jest prowadzenie badań kontrolnych:

-
transaminazy - przed rozpoczęciem oraz podczas
terapii wskazane są kontrolne badania co 6 - 8
tygodni.
Po ustabilizowaniu dawki leku transaminazy badamy
co 3 miesiące w pierwszym roku leczenia, a
następnie co 6 miesięcy. Trzykrotny wzrost
aktywności transaminaz, powyżej górnej granicy
normy jest wskazaniem do przerwania terapii
-
fosfokinazy kreatyny (CPK) - u osób skarżących
się na bóle mięśniowe i osłabienie mięśni oraz w
przypadkach stosowania terapii skojarzonej.
-
wskaźnika protrombinowego - u osób
przyjmujących antykoagulanty. Dotyczy to te
rapii simwastatyną i lowastatyna.

Statyny podawane są w dawce
jednorazowej, najczęściej wieczorem, z
wyjątkiem atorwas-tatyny i
ceriwastatyny, które można podawać o
różnych porach dnia.
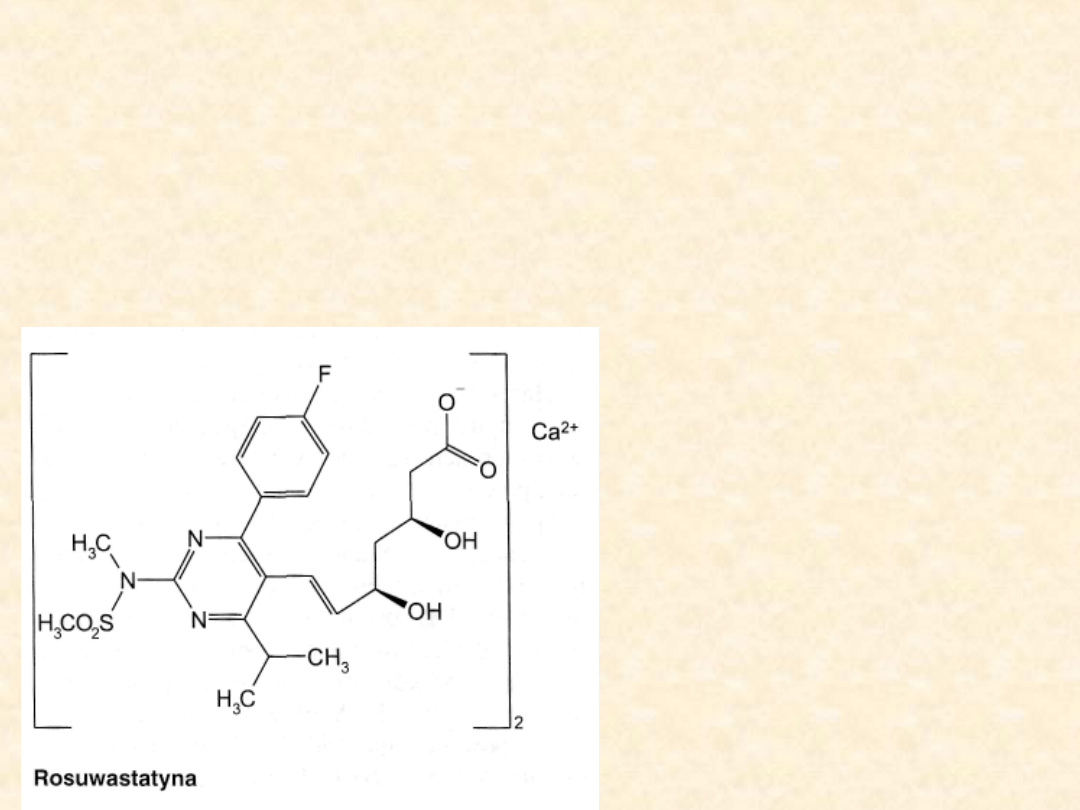
W ostatnim okresie na rynek zastał
wprowadzony nowy preparat z tej grupy, o
nazwie rosuwastatyna (Crestor).
Według zapewnień producenta, opartych na
testach klinicznych, jest ona lekiem
skuteczniejszym od atorwastatyny,
simwastatyny i prawastatyny, gdyż już w
najniższej dawce, to jest 10 mg, wywołuje
znacznie większe obniżenie frakcji
cholesterolu LDL. Ponadto jest specyfikiem
bezpieczniejszym, rzadziej wywołującym
typowe dla statyn działania niepożądane.

Fibraty
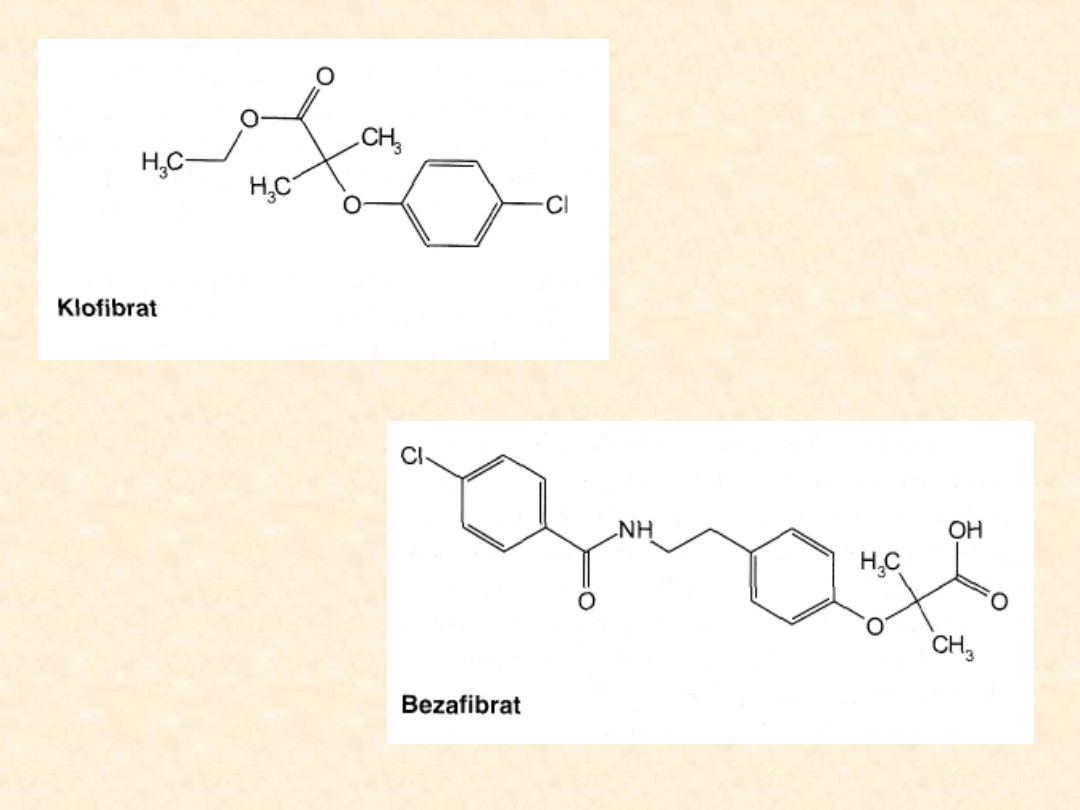
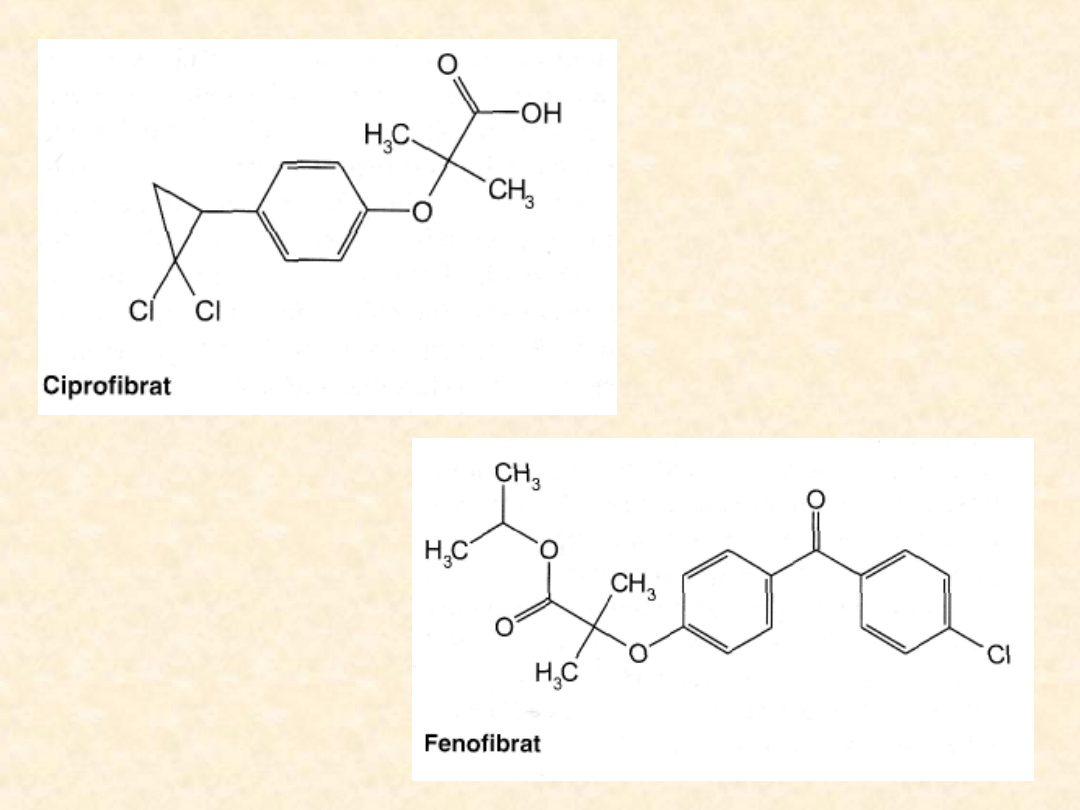
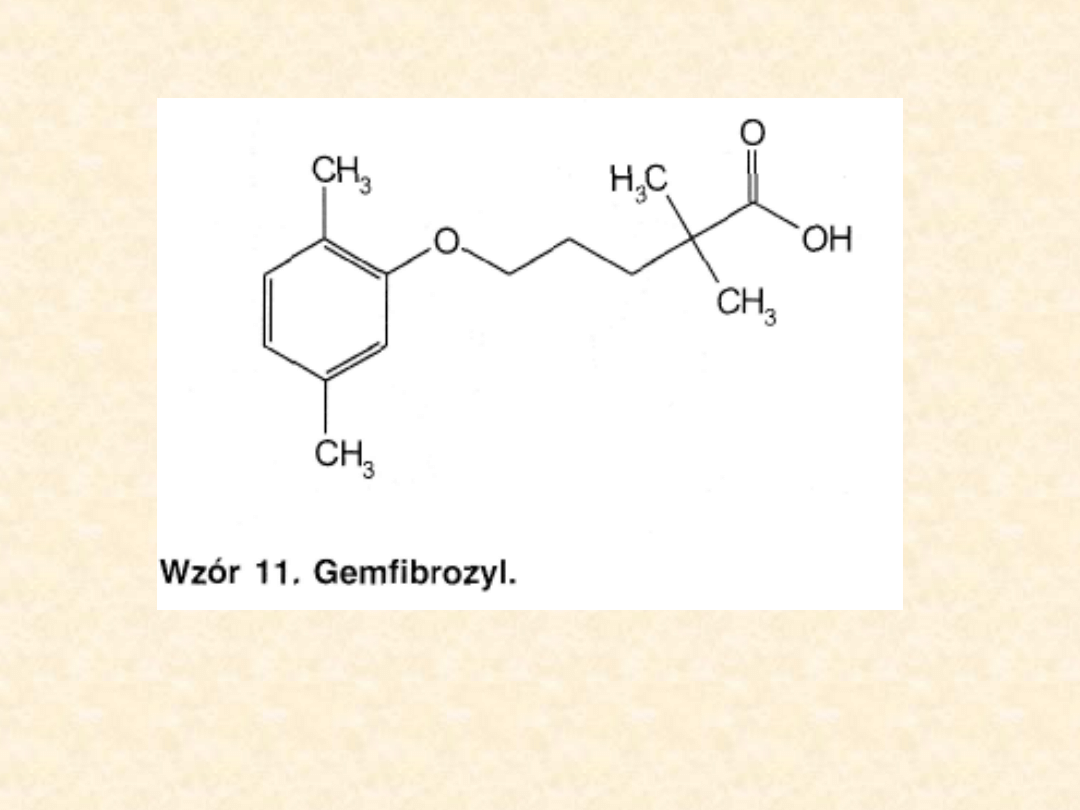
Fibraty są grupą leków hipolipemicznych, stosowaną
od ponad 30 lat. Najstarszym z nich, obecnie bardzo
rzadko wykorzystywanym, głównie w hiperlipidemii
typu III (tzw. choroba remnantów) jest klofibrat. W
praktyce terapeutycznej zastosowanie mają leki
nowszej generacji: bezafibrat, ciprofibrat,
fenofibrat i gemfibrozil.
Fibraty hamują syntezę lipoprotein VLDL w wątrobie
oraz przyspieszają ich katabolizm przez zwiększenie
aktywności lipazy lipoproteinowej (LL) i obniżenie
poziomu apolipoproteiny CIII (inaktywatora lipazy
lipoproteinowej). Zwiększają także usuwanie
cząsteczek lipoprotein LDL oraz zmieniają ich
strukturę w wyniku zwiększenia rozmiarów oraz
zmniejszenia gęstości.
Proces ten prowadzi to do redukcji liczby wysoce arterogennych
małych, gęstych LDL, w kierunku większych lipopro tein, które
mają większe powinowactwo do receptora LDL i łatwiej są
usuwane z surowicy krwi. Ponad to fibraty zwiększają produkcję
frakcji HDL, a przez to transport zwrotny cholesterolu.

Badania ostatnich lat dostarczyły także dowodów na
swoisty mechanizm działania tych leków za
pośrednictwem receptorów jądrowych PPAR
(peroxisome proliferator activated receptor). Są one
kluczowymi przekaźnikami bodźców do genów
kontrolujących metabolizm lipidów. Badane fibraty.
poprzez PPAR-s, wzmagały ekspresję genu dla lipazy
lipoproteinowej, natomiast hamowały dla
apolipoproteiny CIII, czego efektem był spadek
stężenia triglicerydów. Oprócz korzystnego wpływu
na poziom lipidów i lipoprotein, fibraty z wyjątkiem
gemfibrozilu wykazują także inne mechanizmy
działania, sprzyjające zapobieganiu miażdżycy,
działając na upośledzony proces krzepnięcia i
fibrynolizy, spowodowany zbyt wysokim stężeniem
fibrynogenu i PAI-1. Natomiast gemfibrozil i
bezafibrat obniżają poziom PAI-1.
Doniesienia ostatnich lat mówią także o anty
oksydacyjny m działaniu gemfibrozilu, co z
pewnością może mieć istotne znaczenie
farmakologiczne.

W świetle przedstawionych powyżej mechanizmów
działania, wskazaniem do podawania fibratów są więc
zaburzenia wyrażające się wzrostem stężenia
triglicerydów oraz towarzyszące im zmiany w profilu
innych lipoprotein.
Fibraty należą do leków dobrze tolerowanych. Kliniczne
objawy niepożądane występują u 5-15% leczonych, ale
zwykle nie wymagają zaprzestania kuracji. Do
najczęściej obserwowanych działań niepożądanych (5-
10% chorych) należą dolegliwości ze strony przewodu
pokarmowego (zaparcia, biegunki, wzdęcia, suchość w
ustach, brak łaknienia, bóle brzucha), dolegliwości ze
strony innych narządów (zapalenie i bóle mięśni,
alergiczne odczyny skórne, padanie włosów, bole
głowy, zaburzenia potencji, uczucie zmęczenia).
Wyjątkowo rzadko podczas ich stosowania dochodzi do
rabdomiolizy z mioglobinurią i ostrej niewydolności
nerek. Częstość występowania tego powikłania wzrasta
u chorych z istniejącą niewydolnością nerek lub przy
terapii skojarzonej ze statynami.
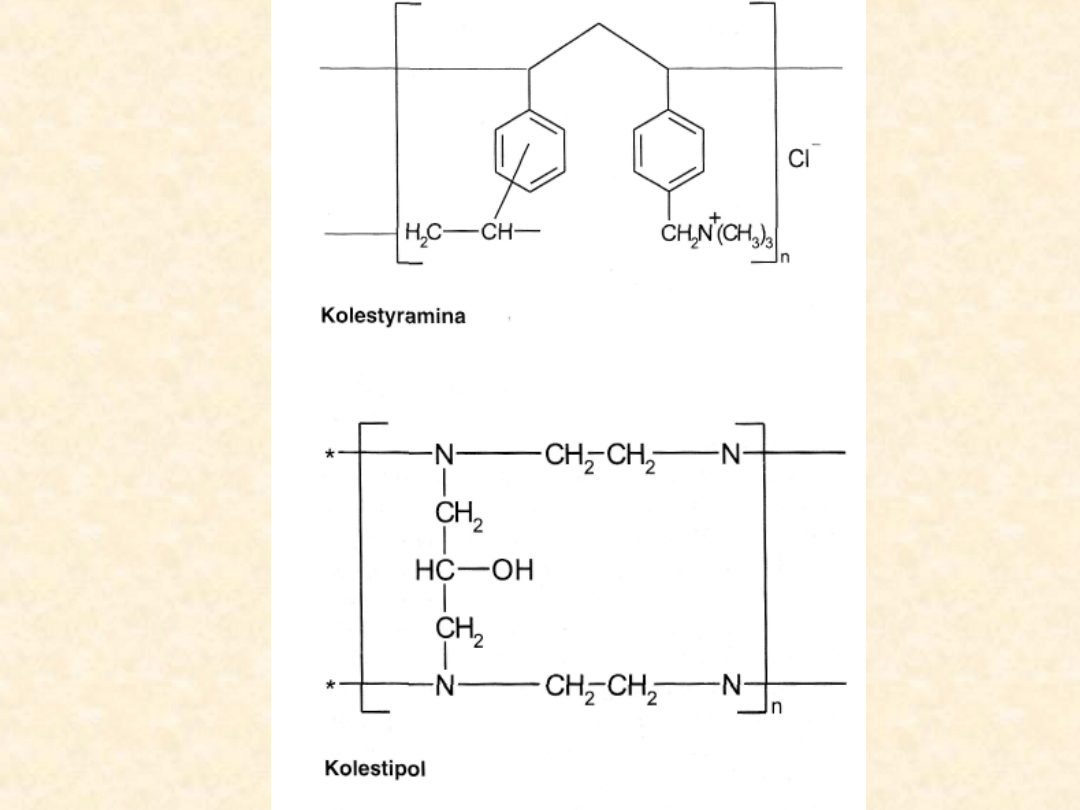

Żywice jonowymienne
W 1970 r. zostały wprowadzone do lecznictwa pierwsze
żywice jonowymienne (kolestyramina, kolestipol),
zastosowane jako leki obniżające poziom cholesterolu
w przypadkach hipercholesterolemii. Żywice te są
nierozpuszczalne w wodzie, odporne na działanie
enzymów trawiennych i nie ulegają absorpcji z
przewodu pokarmowego.
W pH żołądka, tworzą czwartorzędowe sole amoniowe,
które wymieniają aniony z kwasami żółciowymi, wiążąc
je nieodwracalnie w jelicie i hamując ich zwrotne
wchłanianie. Obniżenie poziomu kwasów żółciowych w
wątrobie sprzyja dalszej konwersji kolejnych porcji
cholesterolu do kwasów żółciowych i zatem jego
eliminacji z ustroju. Redukcja zawartości cholesterolu w
wątrobie pobudza także aktywność receptorów LDL na
hepatocytach, co prowadzi do wzmożonego wiązania
lipoprotein LDL i spadku ich stężenia we surowicy krwi.

Żywice należą do leków obniżających poziom
cholesterolu w surowicy i we frakcji LDL średnio o 15-
30%. Nieznacznie podnoszą także cholesterol-HDL (3-
5%). Nie wpływają na poziom triglicerydów, bądź mogą
go nieznacznie podwyższać. Są lekami pierwszego
rzutu w terapii hipercholesterolemii, szczególnie
zalecanymi u mężczyzn poniżej 45 roku życia i kobiet
poniżej 55 roku życia. U osób z ciężką postacią tego
schorzenia można je kojarzyć ze statynami. Żywice
należą do leków dość bezpiecznych, zatem można je
stosować u kobiet ciężarnych i karmiących oraz u
dzieci. Wskazana jest wtedy suplementacja kwasem
foliowym w dawce 5 mg/24 h. Natomiast są
bezwzględnie przeciwwskazane u osób z wysoką
hipertriglicerydernią (> 500 mg/dL), z rodzinną
dysbetalipoproteinemią oraz ze skłonnościami do
ciężkich zaparć, żylaków odbytu i wrzodów
trawiennych. Należy je także ostrożnie stosować u
chorych z podwyższonym poziomem triglicerydów
(powyżej 200 mg/dL).

Działania niepożądane tych preparatów związane są
głównie z dolegliwościami żołądkowo-jelitowymi,
takimi jak: zaparcia, wzdęcia, uczucie pełności w
nadbrzuszu, nudności. Należy także pamiętać, że
mogą one zmniejszać wchłanianie innych leków i z
tego też powodu inne specyfiki powinny być
przyjmowane przynajmniej l godzinę przed lub 4
godziny po podaniu żywic. I chociaż żywice mogą
zmniejszać także wchłanianie witamin rozpuszczalnych
w tłuszczach i kwasu foliowego, jednak rutynowe ich
podawanie nie jest zalecane. Obserwowany niekiedy
po ich stosowaniu wzrost stężenia triglicerydów ma
zwykle charakter przejściowy, podobnie jak wzrost
poziomu transaminaz i fosfatazy alkalicznej. Żywice
można kojarzyć ze wszystkimi lekami
hipolipemicznymi, a dzięki terapii skojarzonej uzyskać
korzystniejsze efekty przy mniejszych dawkach
poszczególnych leków oraz zmniejszyć występowanie
działań niepożądanych.

W Polsce z grupy żywic jonowymiennych
zarejestrowane są następujące leki: kolestyramina
(Questran, Vasosan P- z dodatkiem pektyny, Vasosan S
– z dodatkiem sacharozy) oraz Kolestipol (Colestid).
Kwas nikotynowy i jego pochodne
Kwas nikotynowy wpływa na poziom lipo-protein
poprzez hamowanie syntezy VLDL w wątrobie. Jest to
efektem obniżenia dopływu wolnych kwasów
tłuszczowych oraz wzrostem katabolizmu VLDL, w
wyniku aktywacji lipazy lipoproteinowej (LL). Obniżenie
poziomu VLDL prowadzi w konsekwencji do
ograniczenia konwersji cząsteczek VLDL do LDL i
spadku ich stężenia w surowicy krwi. Kwas nikotynowy
należy do najskuteczniejszych leków hipolipemicznych.
Jest efektywny we wszystkich rodzajach dyslipidemii.
Obniża poziom cholesterolu LDL w surowicy o 10-25%
oraz poziom triglicerydów o 20-50%.

Ponadto korzystnie wpływa na poziom frakcji
choresterolu HDL (wzrost o 15-35%) i na procesy
krzepnięcia krwi,
obniżając stężenie fibrynogenu w surowicy i pobudzając
fibrynolizę. Wykazano także
korzystne działanie kwasu nikotynowego w profilaktyce
ChNS. Pomimo tak korzystnego działania na profil
lipidów i niskich kosztów terapii, kwas nikotynowy jest
lekiem rzadko stosowanym ze względu na złą tolerancję
oraz liczne przeciwwskazania. Wywołuje bowiem
przykre uderzenia gorąca i zaczerwienienia skóry, daje
liczne objawy ze strony przewodu pokarmowego,
zaostrza chorobę wrzodową, pogarsza tolerancję
glukozy, wywołuje podwyższenie poziomu kwasu
moczowego, upośledza czynność wątroby oraz
prowadzi do wzrostu stężenia homocysteiny. Może
wywoływać także zaburzenia miarowości pracy serca,
obniżenie ciśnienia krwi, zmiany skórne (przebarwienia,
rogowacenia), bądź nasilać działanie leków
hipotensyjnych.
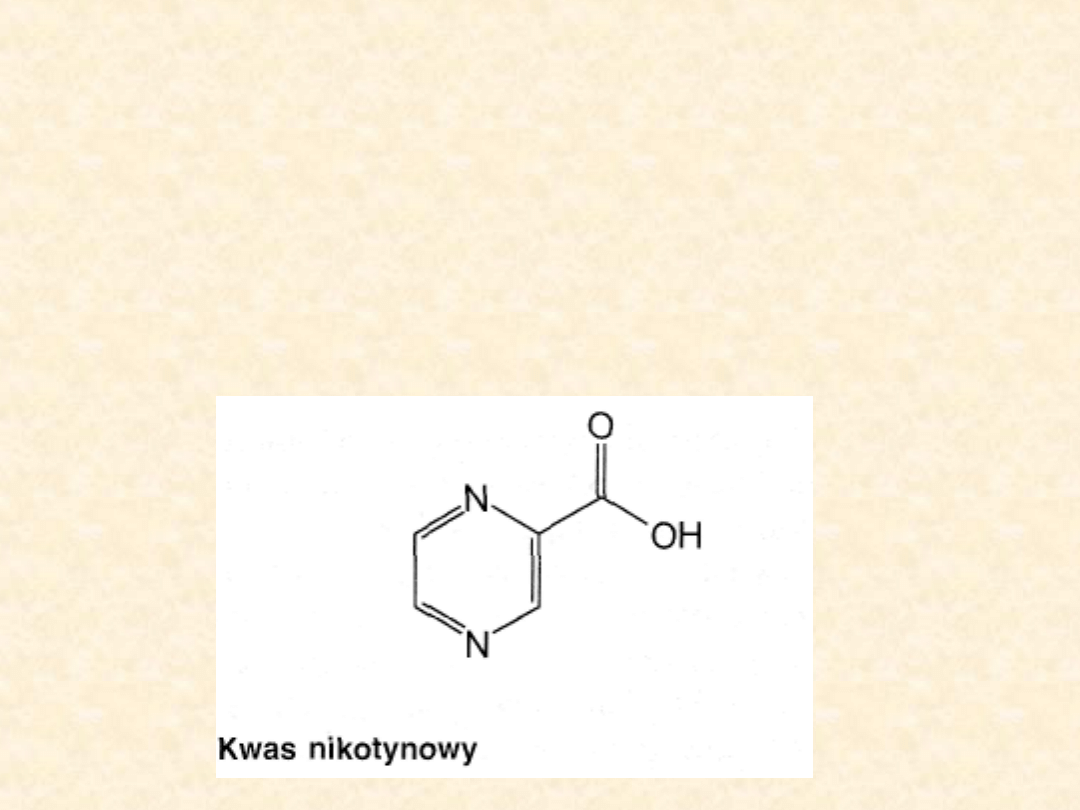
Kwas nikotynowy nie powinien być podawany
kobietom ciężarnym, osobom ze świeżym zawałem
serca, dna, upośledzoną czynnością wątroby, chorobą
wrzodową i nadwrażliwością na lek. Ogólnie uważa się
iż nie powinien być podawany także chorym na
cukrzycę. Nieco łagodniejsze stanowisko panuje w
stosunku do jego pochodnych. Podczas terapii należy
co 12 tygodni monitorować aktywność
aminotransferaz, poziom glukozy i kwasu moczowego.

W lecznictwie znajduje zastosowanie krystaliczny kwas
nikotynowy bądź jego pochodne (preparaty wolno
uwalniające kwas nikotynowy). Leczenie
rozpoczynamy od małych dawek (100 mg/24 h),
stopniowo je zwiększając aż do uzyskania
zamierzonego efektu terapeutycznego. Dawka
maksymalna kwasu nikotynowego wynosi około 6 g/24
h, a jego pochodnych 2 g/24 h. W hiperlipidemii
złożonej można go kojarzyć ze statynami. Lekiem o
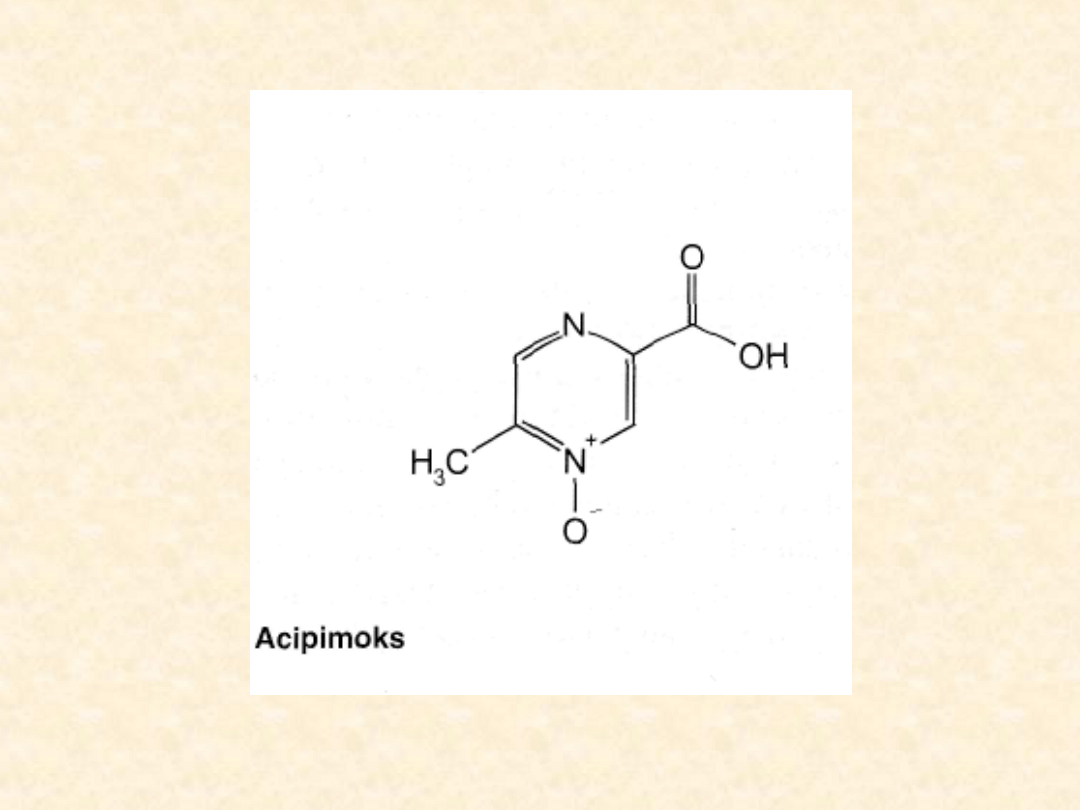
dużym podobieństwie strukturalnym do kwasu
nikotynowego jest acipimoks.
Zmniejsza on uwalnianie kwasów tłuszczowych,
hamując lipolizę tkanki tłuszczowej. Następstwem tego
procesu jest ograniczenie tworzenia frakcji VLDL i LDL
oraz zmniejszenie stężenia triglicerydów i cholesterolu
we krwi.

Sitosterole
. Fitosterole i fitostanole są to związki o budo
wie steroidowej, występujące w komórkach
roślinnych. Tak jak cholesterol, pełnią niezwykle
istotną rolę w stabilizacji roślinnych błon
komórkowych. Dotychczas zidentyfikowano w
roślinach ponad 40 związków sterolowych, z
których najważniejsze to: (Beta-sitosterol,
tigmasterol i kampestrol. Fitostanole są
natomiast mniej znaną klasą związków
roślinnych, stanowiącą uwodornioną formą
fitosteroli.
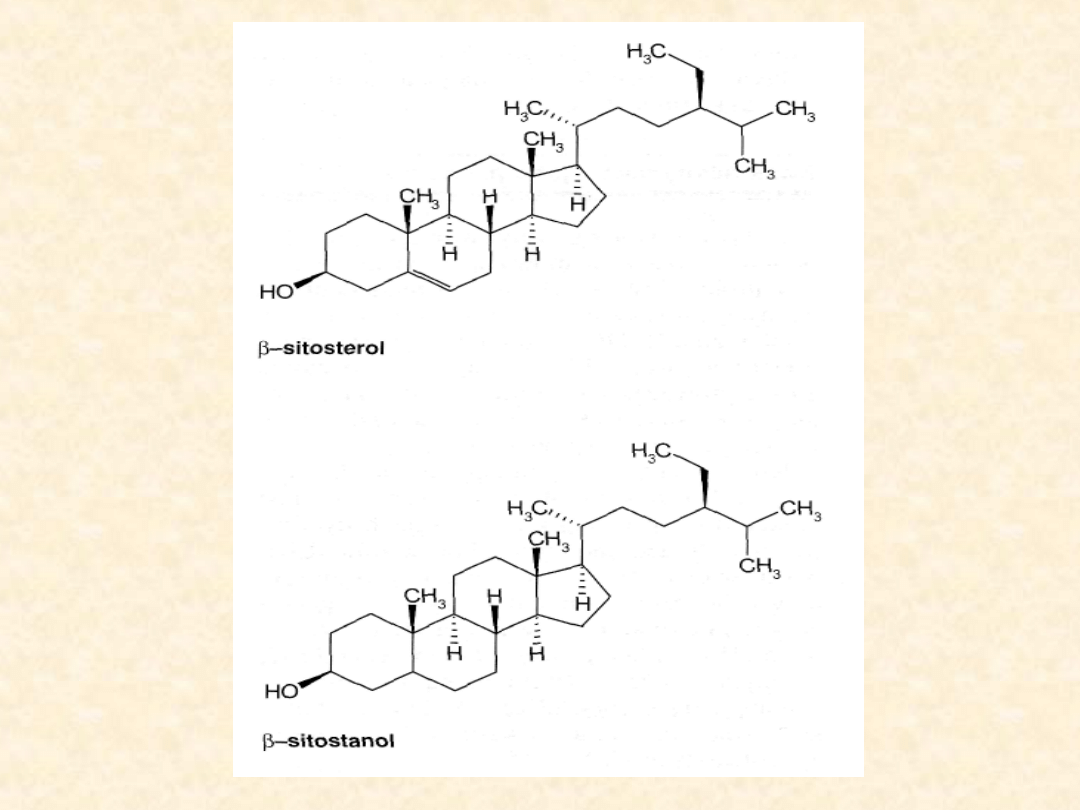

Przy porównaniu budowy cholesterolu i fitosteroli, już
na pierwszy rzut oka widać ich znaczne podobieństwo.
Stanole, sterole oraz ich estry hamują wchłanianie
endogennego cholesterolu z jelit, powodując obniżenie
jego poziomu o około 10%. Propozycja zredukowania
podwyższonego poziomu cholesterolu przez
wprowadzenie w codziennej diecie żywności
zawierającej dodatek naturalnych fitosteroli jest
bardziej atrakcyjna niż terapia oparta na restrykcyjnej
diecie lub/i stosowaniu leków. Sam pomysł nie jest
jednak nowy, gdyż Beta-sitosterol był już w tym celu
używany (od 1950 r.) zarówno jako supplement do
żywności jak i lek (Cytellin, Merck). Znaczenie tej
grupy leków znacznie jednak zmalało po
wprowadzeniu na rynek statyn. Czynnikiem
ograniczającym stosowanie jest także ich słaba
rozpuszczalność, zmuszająca pacjentów do zażywania
olbrzymich dawek dobowych (25 g/24 h).

Przełomem w leczeniu sitosterolami stało się
więc, wprowadzenie do lecznictwa lepiej
rozpuszczalnych estrów stanoli i steroli,
zaakceptowane przez FDA w 2000 roku.
Sitosterole występują na rynku głównie jako
żywność funkcjonalna lub dodatek do żywności.
Należą do nich takie produkty jak dostępny
również u nas Benecol (Uniłever), czy
występujący w USA Take Control™, Phytrol™
(Novartis).

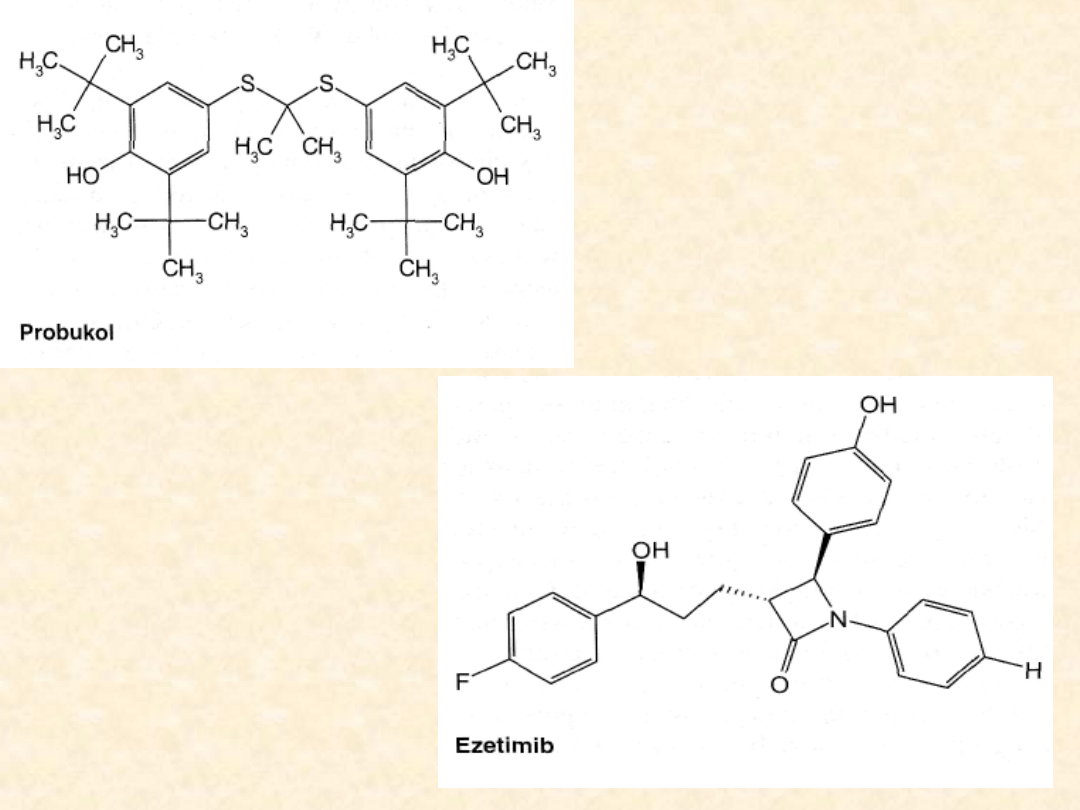
Leki o różnej strukturze
Probukol zmniejsza stężenie cholesterolu frakcji LDL
poprzez oddziaływanie z receptorami LDL. Ponadto jest
silnym przeciwutleniaczem, hamującym utlenianie
lipidów.
Stosuje się go w terapii skojarzonej z inhibitorami
reduktazy HMG-CoA i żywicami jonowymiennymi.
Najnowszym lekiem obniżającym poziom lipidów
jest ezetimib (Zetia).
Mechanizm działania tego leku jest inny od dotychczas
omawianych. Zetia nie hamuje syntezy cholesterolu w
wątrobie i nie wzmaga wydzielania kwasów
żółciowych, natomiast hamuje wchłanianie
cholesterolu w jelicie cienkim, obniżając na tej drodze
jego dostarczanie z jelita do wątroby. Nie blokuje także
wchłanianią trigłicerydów, kwasów tłuszczowych,
kwasów żółciowych i witamin rozpuszczalnych w
tłuszczach.

W badaniach klinicznych u pacjentów z
hipercholesterolemią Zetia redukowała wchłanianie
cholesterolu o 54%, całkowity poziom cholesterolu i
frakcji LDL, podnosząc jednocześnie poziom
cholesterolu-HDL.
Najnowsze spostrzeżenia kliniczne wykazały, że
jednoczesne stosowanie ezetimibu z
atorwastatyną skuteczniej obniża poziom
cholesterolu niż stosowanie każdego z nich osobno. W
badaniach na grupie kontrolnej 628 pacjentów
zaobserwowano, że łączne podawanie tych leków
powoduje obniżenie cholesterolu-LDL o 55%
(atorwastyna obniża o 42% a ezetimib o 18%). Tak
korzystny efekt działania wynika z różnych
mechanizmów działania tych leków. Atorwastatyna
hamuje bowiem syntezę cholesterolu, natomiast
ezetimib absorpcję cholesterolu przez ścianę jelita.
Synergizm działania leków pozwala zatem na
obniżenie dawki atorwastatyny i uzyskanie lepszych
efektów terapeutycznych.

Colesewelam HC1 (WelChol) jest polimerem
wykazującym silne powinowactwo do kwasów
żółciowych. W przeciwieństwie do większości
stosowanych leków obniżających poziom
cholesterolu, nie jest absorbowany do krwi.
Wiąże kwasy żółciowych w jelicie cienkim,
powodując uruchomienie enzymów
wątrobowych przekształcających istniejące
zasoby cholesterolu w kwasy żółciowe i
obniżając w ten sposób całkowite jego zasoby.
WelChol jest stosowany w tabletkach 625 mg
sam lub razem z inhibitorami reduktazy HMG-
CoA, z którymi wykazuje efekt addytywny,
zwiększając zarazem skuteczność statyn od
8% do 16%.

Perspektywy
Pomimo potężnego arsenału leków, jakimi
dysponuje medycyna w walce z hiperlipidemią,
trwają nieustanne poszukiwania nowych, skutecz
niejszych specyfików. Badania te, prowadzo ne
wielokierunkowo są zarówno kontynuacją prac w
obrębie znanych już grup terapeutycz nych, z
uwzględnieniem poznanych mechanizmów
działania, jak i poszukiwaniem nowych punktów
uchwytu. Jedną z możliwych dróg realizacji
koncepcji mających na celu obniżenie poziomu
cholesterolu jest intensyfikacja jego transportu
zwrotnego z tkanek do wątroby Zachodzi ona z
udziałem lipoprotein HDL, które wykorzystując
techniki ultrawirowania można podzielić na dwie
podfrakcje: HDL2 i HDL3.

Różnią się one składem apolipoprotein, i tak podfrakcja
HDL3 zawiera zarówno apoA-I jak i apoA-II. natomiast
HDL2 jedynie apoA-I. Z przeprowadzonych badań
wynika, że właśnie apoA-I wykazują większą aktywność
w usuwaniu nadmiaru cholesterolu, a zatem w
podwyższeniu poziomu apoA-I (frakcji HDL2) można
poszukiwać nowych metod walki z hiperlipidemią. Efekt
ten można uzyskać na różnych drogach, a jedną z
najprostszych jest podawanie apoA-I w kompleksach z
fosfatydocholiną (re-kombinowana apoA-I). Metoda ta
stosowna z powodzeniem na zwierzętach i ludziach
wydaje się być terapią bezpieczną. Istotnym
ograniczeniem w jej stosowaniu jest jednak konieczność
podawania apolipoproteiny dożylnie, w postaci
długotrwałego wlewu.

Endogenna apoA-I jest syntetyzowana w wątrobie oraz
w ścianie jelita cienkiego i krąży w organizmie na
przemian w stanie wolnym lub jako element lipoprotein
HLD i jest uwalniana do osocza podczas przekazywania
estrów cholesterolu z cząsteczek HDL na VLDL i LDL.
Proces ten podlega regulacji za pośrednictwem białka
transportującego CETP, które jest odpowiedzialne za
przenoszenie nowo zestryfikowanego cholesterolu na
cząsteczki lipoprotein, zawierające apoB (VLDL, IDL,
LDL) oraz dostarczanie go do tkanek. Brak CETP
wywołuje zatem permanentne podwyższenie poziomu
frakcji cholesterolu-HDL i może stanowić jedną z metod
walki z hipercholesterolemią. Blokowanie białka CETP
przeprowadza na różnych drogach. I tak firma Avant
Immuno-therapeutics kieruje od lat badaniami nad
zastosowaniem u ludzi przeciwciał CETP.

Natomiast firmy Merck, Aventis i CV
Therapeutics prowadzą prace nad lekami
wpływającymi na gen odpowiedzialny za
syntezę białka ABC l (ATP-binding cassette
transporter-1), pobudzającego powstawanie
cząsteczek CEPR, przenoszących cholesterol z
komórki do błony komórkowej i
umożliwiających jego wychwyt przez HDL. Jak
dowodzą przeprowadzone badania, ekspresja
genu ABC l i synteza CERP wzrasta w wyniku
obładowaniu komórek cholesterolem i maleje
po jego usunięciu przez apolipoproteiny. Zatem
opracowanie leków pobudzających gen ABC l
wywoływałoby więc podwyższenie stężenia
frakcji HDL i skuteczniejsze usuwanie
cholesterolu z komórek.
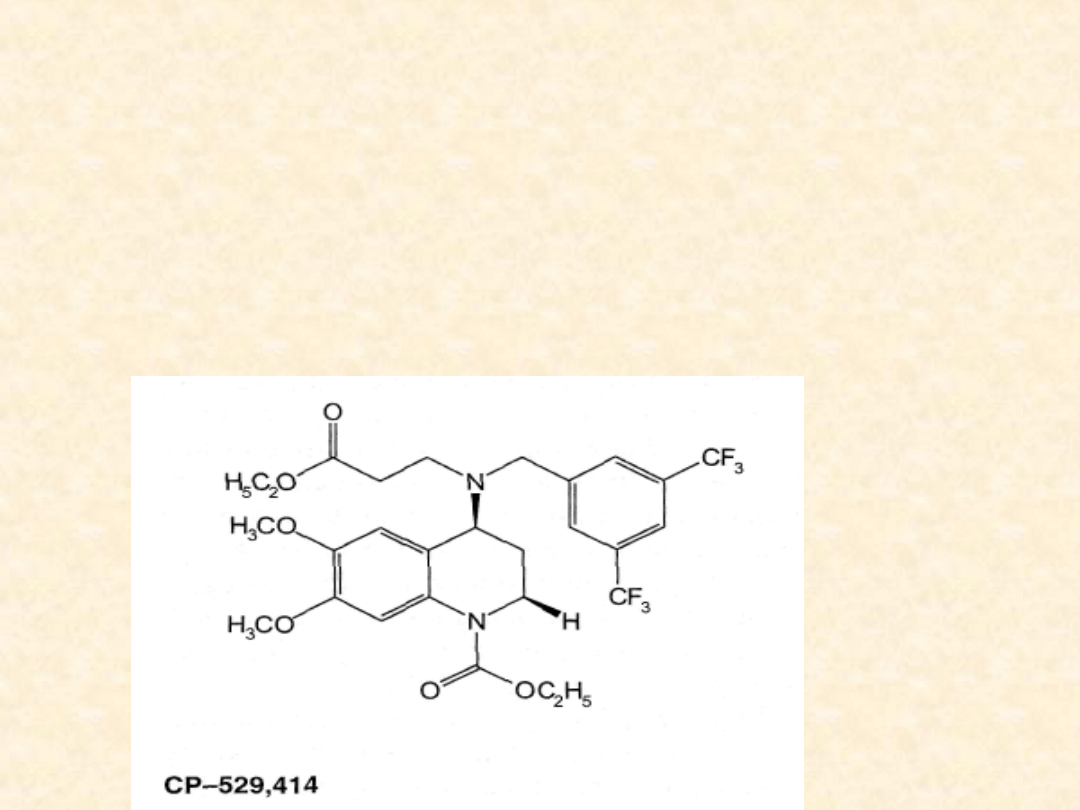
Trwają także prace nad poszukiwaniem leków
blokujących selektywnie CETP. W 1998 r.
naukowcy z firmy Pfizer wprowadzili do II etapu
badań nowy lek o symbolu CP-529,414,
uzyskując wzrost stężenia frakcji cholesterolu-
HDL o około 70% i nie obserwując istotnych
działań niepożądanych.

I choć od tego czasu pojawiło się wiele sprzecznych
informacji na temat samego działania, jak i działań
niepożądanych stosowania nowego preparatu, w firmie
Pfizer trwają już prace nad możliwością jego połączenia
z atorwastatyną.
Akceptorami lipidów, w tym cholesterolu krążącego we
krwi, mogą być także liposomy (pęcherzyki
fosfolipidowe, PLV). Budowa ich i duże rozmiary
warunkują jednokierunkowe działanie, to znaczy
wychwyt cholesterolu, przy jednoczesnym braku
możliwości wnikania do przestrzeni
międzykomórkowych i łączenia się z błoną komórkową.
Podane dożylnie krążą zatem we krwi i transportują
cholesterol z tkanek obwodowych do wątroby. Terapię
liposomami ogranicza jednak duża szybkość ich
eliminacji z krążenia.

Badania nad nowymi lekami hipolipemicznymi
prowadzą zarówno wielkie koncerny farmaceutyczne,
jak i małe firmy. Jednym z takich ośrodków jest
prywatna firma biofarmaceutyczna QuatRx
Pharmaceutical Company. Opracowany w niej związek
o symbolu QRX-401, będący w fazie badań klinicznych,
jest doustnym lekiem nowej klasy, o podwójnym
mechanizmie działania. Obniża on bowiem zarówno
poziom cholesterolu LDL, jak i lipoproteiny. QuatRx
Pharmaceutical Company prowadzi także badania nad
nową grupą leków podwyższających poziom frakcji
cholesterolu-HDL, pozytywnego czynnika w
zapobieganiu miażdżycy.

Obniżanie poziomu cholesterolu wywołują także sole
potasowe i wapniowe kwasu glukarowego. Kwas D-
glukarowy i jego sole są związkami wydalanymi przez
człowieka z moczem. Redukują one specyficznie
całkowity cholesterol we krwi szczurów, będących
zarówno na nisko- jak i wysokotłusz-czowej diecie o
około 12-15%. Obniżają także poziom cholesterolu-LDL
o 30-35% a triglicerydów do 40%. Sugeruje to, że
związki te mogą być naturalnymi regulatorami
cholesterogenezy. Przypuszcza się także, że D-
glukarany mogą wpływać na syntezę cholesterolu,
jego metabolizm i wydzielanie w formie kwasów
żółciowych. We wstępnych badaniach,
przeprowadzonych na ludziach, D-glukarany
redukowały całkowity cholesterol do 12%, cholesterol-
LDL do 28% i triglicerydy do 43%.

Kolejna grupę potencjalnych leków hipolipemicznych
stanowią cyklodekstryny. Są one oli-gosacharydami,
powstającymi przez enzymaty czną modyfikację skrobi.
Wśród nich duże znaczenie terapeutyczne ma (3-
cyklodekstryna, wykazująca zdolność do łączenia się z
cząsteczkami kwasów żółciowych i steroli i
zwiększająca ich wydalanie z kałem. Działanie to
prowadzi do zmniejszenia puli cholesterolu LDL oraz
obniżenia stężenia triglicerydów w osoczu. Mała
średnica cząsteczek cyklodekstryn umożliwia także ich
wnikanie do przestrzeni międzykomórkowej, gdzie
łącząc się z błoną komórkową wiążą cholesterol,
usuwając go na przykład z blaszki miażdżycowej. Mogą
być także wykorzystane jako nośniki w terapii genowej,
dostarczając do tkanek potrzebne geny, na przykład
gen apoA-I. Obecnie prowadzone badania mają na celu
zmniejszenie toksyczności cyklodekstryn poprzez
modyfikację chemiczną ich cząsteczek.

Innym punktem uchwytu dla nowo powstającej grupy
leków może być farnezoid X receptor (FXR). Jest on
czujnikiem transkry plujący m kwasy żółciowe.
Otrzymano już kilka klas związków będących
aktywatorami tego receptora, które w przyszłości
mogą być wykorzystane do wyjaśnienia fizjologicznej
roli receptora FRX oraz poszukiwaniu nowych leków
wpływających na metabolizm cholesterolu i kwasów
żółciowych. Nową, bardzo obiecującą grupę leków
obniżających poziom cholesterolu są inhibitory enzymu
acylotransferazy acylo-CoA : cholesterol (ACAT).
Enzym ten aktywowany przez poziom wolnego
cholesterolu, jest odpowiedzialny za jego
wewnątrzkomórkową estryfikację w makrofagach,
wątrobie i jelicie. Utworzone na tej drodze estry
cholesterolu stają się częścią naturalnego rdzenia
lipoprotein, stanowiąc rezerwuar wolnego cholesterolu,
będącego prekursorem dla biosyntezy między innymi
hormonów steroidowych.

Współcześnie prowadzone badania sugerują
obecność dwóch różnych odmian ACAT, kodowanych
przez dwa różne geny. ACAT1 jest obecny we
wszystkich komórkach. Natomiast jedynie ludzka
wątroba zawiera zarówno ACAT l, jak i ACAT2, z
przewagą ACAT1. Występuje on jednak głównie w
makrofagach, gdzie bierze udział w estryfikacji
cholesterolu oraz tworzeniu komórek piankowych,
będących elementami strukturalnymi blaszki
miażdżycowej. Natomiast ACAT2, występujący w
wyściółce jelita, aktywuje transport zwrotny
cholesterolu z jelita do wątroby. Blokowanie
aktywności enzymów ACAT ma znaczącą rolę nie
tylko w zapobieganiu rozwojowi miażdżycy, ale
także w obniżaniu absorpcji egzogennego
cholesterolu i jego kumulacji w komórkach ścian
naczyń krwionośnych, a także sekrecji cząsteczek
VLDL przez hepatocyty, wpływającej pośrednio na
poziom trigłicerydów surowicy.
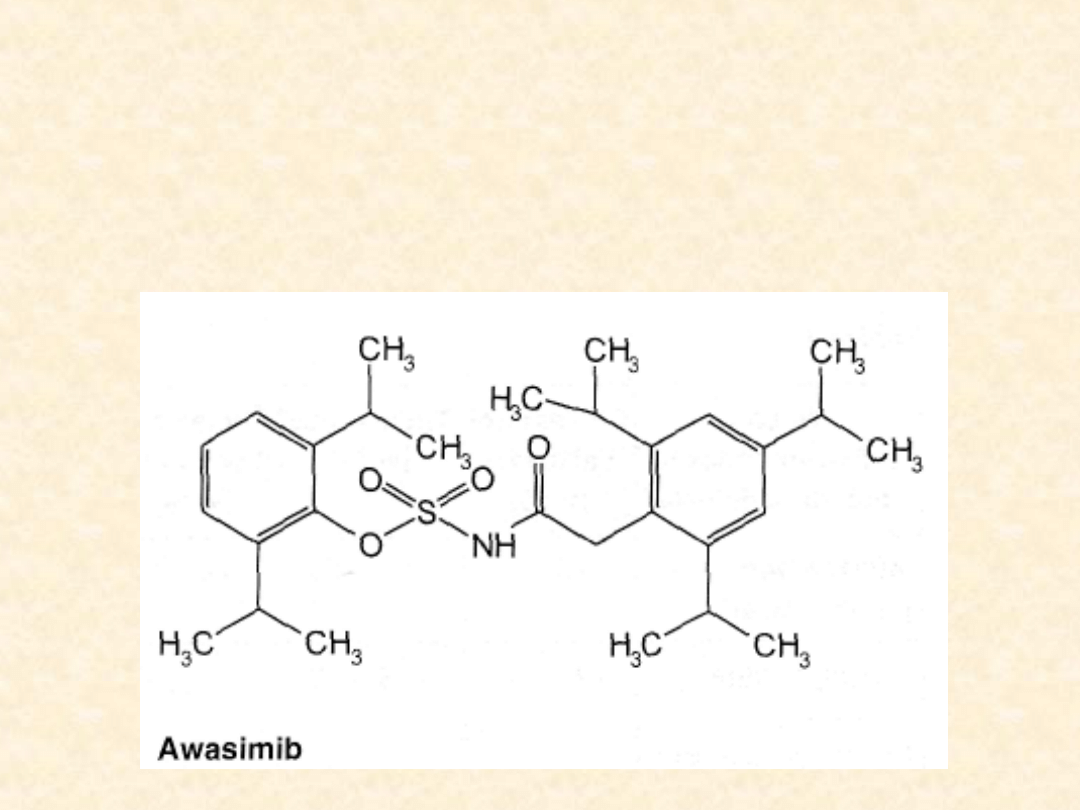
Inhibitory ACAT są ciągle na etapie badań
klinicznych. Wiele z nich przechodzi modyfikacje
chemiczne ze względu na zbyt małą efektywność i
zbyt wysoką toksyczność. Wśród nich najbardziej
obiecującym preparatem jest awasimib.

Awasimib redukuje poziom całkowitego cholesterolu
i cholesterolu LDL, nie wykazując znaczących
działań niepożądanych. W badaniach in vitro na
ludzkich makrofagach redukuje tworzenie komórek
piankowych przez zwiększanie uwalniania wolnego
cholesterolu i hamowanie wychwytu
zmodyfikowanej frakcji LDL. Stosowanie awasimibu
sprzyja także stabilności blaszki miażdżycowej i
redukuje odkładanie lipidów w ścianach naczyń.
Ponadto lek ten wykazuje synergizm ze statynami, a
łączona terapia nie tylko wpływa na zahamowanie
procesu uszkadzania naczyń krwionośnych, ale
również na cofanie się zmian. Inhibitory ACAT,
wykazują także inne ciekawe zastosowanie.
Ostatnio w piśmiennictwie można spotkać coraz
więcej doniesień na temat ich wykorzystania w
leczeniu choroby Alzheimera. Badaniami tymi objęty
jest także awasimib.

Nutraceutyki
Zgodnie ze stanowiskiem Międzynarodowego
Towarzystwa Miażdżycowego, zalecającego w
pierwszym etapie terapii hiperlipidemii leczenie
dietetyczne, kończąc artykuł należałoby wspomnieć
choć w kilku słowach „leki" pochodzące z naszej
codziennej diety, czyli nutraceutyki.
Ich ciekawym przykładem jest polikosanol. Jest to
naturalna mieszaniną pierwszorzędowych alkoholi
otrzymywanych z wosku trzciny cukrowej. Jej
głównym składnikiem jest oktakosanol, 28-węglowy
łańcuchowy alkohol, występujący także w skórkach i
powierzchniowej warstwie wielu owoców. Z
przeprowadzonych badań wynika, że oktakosanol
wpływa na metabolizm tłuszczów, ułatwiając ich
zamianę w energię. Szczególnie interesujące jest
jednak jego działanie hipolipemiczne.

W dawce 10-20 mg obniża skutecznie stężenie
cholesterolu całkowitego o 17-21%, frakcji cholesterolu
LDL o 21-29% oraz podwyższa stężenie frakcji
cholesterolu HDL 8-15%.
Nie wpływa jednak na poziom triglicerydów.
Mechanizm jego działania nie jest dokładnie poznany.
Przypuszcza się, że hamuje syntezę cholesterolu w
wątrobie oraz wpływa na katabolizm cząsteczek LDL,
zwiększając ich wychwyt przez hepatocyty.
Równocześnie wykazuje działanie ochronne w stanach
przedzawałowych, zapobiegając rozwojowi zmian
miażdżycowych. Hamuje bowiem agregację płytek
krwi, powstawanie komórek piankowych i zapobiega
proliferacji komórek śródbłonka
naczyniowego.Polikosanol jest specyfikiem dobrze
tolerowanym, nie wykazującym działań niepożądanych
nawet podczas długotrwałej terapii dawkami powyżej
20 mg/24 h. Jest więc preparatem bardzo obiecującym,
stosowanym z powodzeniem w hipercholes-terolemii w
krajach Ameryki Południowej i Środkowej już od 1991 r.

Prowadzone obecnie badania nad zdrowotnymi
walorami produktów sojowych wskazują, że soja może
być jednym z wielu czynników zmniejszających ryzyko
zachorowania na choroby nowotworowe i miażdżycę.
Zaobserwowano, że długotrwałe spożywanie przez
osoby z podwyższonym poziomem cholesterolu około
85 g suchego ziarna soi dziennie, może obniżać
cholesterol całkowity we krwi o około 20%. Korzystny
wpływ przypisuje się tu fitoestrogenom
izoflawonowym, genisteinie i daidzeinie. Stwierdzono,
że obniżają one między innymi poziom cholesterolu
całkowitego zarówno u ludzi, jak i zwierząt
doświadczalnych, frakcji cholesterolu LDL i VLDL, przy
jednoczesnym zachowaniu poziomu frakcji
cholesterolu HLD. Mechanizm ich działania
hipolipemicznego nie jest jeszcze do końca
poznany.

W profilaktyce zmian miażdżycowych istotną rolę
odgrywa na pewno antyoksydacyjne działanie
flawonoidów, które eliminując chemiczną modyfikację
lipoprotein LDL i ich utlenienie do związków
toksycznych oraz wolnych rodników, czynią je ważnym
czynnikiem w procesie hamowania rozwoju zmian
miażdżycowych.

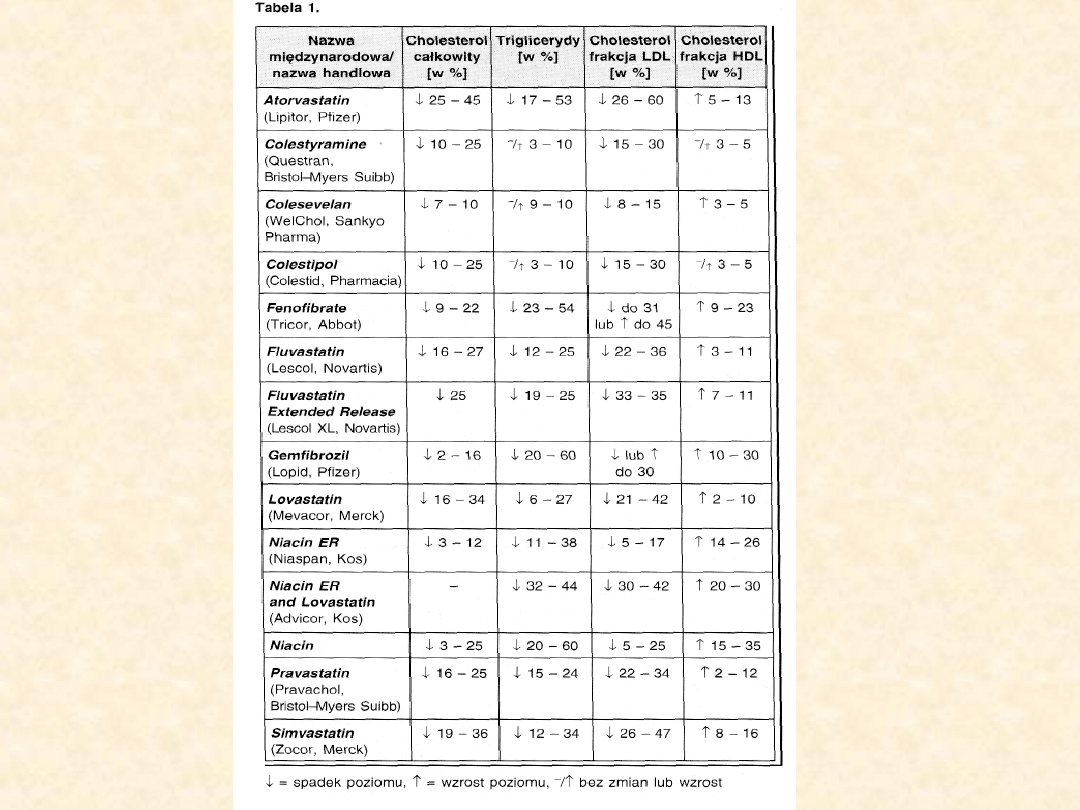
• Podsumowanie
• Ze względu na duże znaczenie
terapeutyczne leków hipolipemicznych i
wielokierunkowość prowadzonych
badań, prezentowany artykuł nie
wyczerpuje w pełni tematu.
Zaprezentowane grupy preparatów
ukazują jednak ogromne możliwości
regulacji gospodarki lipidowej a główne
efekty stosowania podstawowych leków
wpływających na poziom lipidów
(cholesterolu całkowitego, triglicerydów,
cholesterolu LDL, cholesterolu HDL)
prezentuje tabela l.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
Wyszukiwarka
Podobne podstrony:
PROBLEMY FARMAKOTERAPII WIEKU PODESZŁEGO
PROBLEMY ZDROWOTNE WIEKU PODESZŁEGO 1
Problemy psychiatryczne osób w wieku podeszłym
Problemy psychiatryczne osób w wieku podeszłym
urazy w wieku podeszłym
Urazy wieku podeszłego
Aktywizacja osób w wieku podeszłym
Zespoły pozapiramidowe u osób w wieku podeszłym
pacjent z nadcisnieniem tetniczym w wieku podeszlym
depresja w wieku podeszłym, STUDIA, Pielęgniarstwo, Materiały z pielęgniarstwa
Zaburzenia psychiczne wieku podeszłego, Pielęgniarstwo licencjat cm umk, III rok, Geriatria i pielęg
Postawy osob w wieku podeszlym wobec wlasnej starosci
choroba alzheimera i inne zespoły otępienne wieku podeszłego
zywienie osob w wieku podeszlym
Patofizjologia wieku podeszłego
więcej podobnych podstron