Konkursy w województwie podkarpackim w roku szkolnym 2006/2007
Kod ucznia
Kod szkoły
–
–
Dzień Miesiąc
Rok
D A T A U R O D Z E N I A U C Z N I A
.........................................
pieczątka WKK
KONKURS PRZEDMIOTOWY CHEMICZNY
DLA UCZNIÓW GIMNAZJUM
ETAP WOJEWÓDZKI
Drogi Uczniu,
witaj na II etapie konkursu chemicznego. Przeczytaj uważnie instrukcję i postaraj
się prawidłowo odpowiedzieć na wszystkie pytania.
• Arkusz liczy 13 strony i zawiera 36 zadań.
• Przed rozpoczęciem pracy sprawdź, czy Twój test jest kompletny.
Jeżeli zauważysz usterki, zgłoś je Komisji Konkursowej.
• Zadania czytaj uważnie i ze zrozumieniem.
• Do każdego zadania (od 1. do 36.) są podane cztery odpowiedzi:
A, B, C, D.
Odpowiada im następujący układ na karcie odpowiedzi:
A
B
C
D
•
Wybierz tylko jedną odpowiedź i zamaluj kratkę
z odpowiadającą jej literą – np. gdy wybrałeś odpowiedź „A”:
A
B
C
D
•
Staraj się nie popełnić błędów przy zaznaczaniu odpowiedzi, ale
jeśli się pomylisz,
błędne zaznaczenie otocz kółkiem i zaznacz inną odpowiedź
A
B
C
D
•
Odpowiedzi zaznacz czarnym długopisem bądź piórem. Nie
używaj korektora i kalkulatora
•
Możesz korzystać z tablic dołączonych do zestawu zadań
•
Brudnopis nie podlega ocenie
Pracuj samodzielnie
.
Powodzenia!
Czas pracy:
90 minut
Liczba punktów
możliwych
do uzyskania:
50
Strona 1 z 13

Konkursy w województwie podkarpackim w roku szkolnym 2006/2007
Skorupa ziemska zawiera około 0,14% węgla w postaci: związków, węgli kopalnych
oraz w stanie wolnym. Węgiel nie rozpuszcza się w wodzie ani w rozpuszczalnikach
organicznych. Jest podstawowym pierwiastkiem w związkach organicznych.
Zadanie 1. (0-1 pkt)
Liczba atomowa węgla wynosi:
A. 12
B. 12u
C. 6
D. 6u
Zadanie 2. (0-1 pkt)
Masa atomowa węgla wynosi:
A. 12
B. 12u
C. 6
D. 6u
Zadanie 3. (0-1pkt)
Liczba elektronów w izotopie C–13 wynosi:
A. 13
B. 6
C. 7
D. 4
Zadanie 4. (0-1 pkt)
Alotropowymi odmianami węgla są:
A. diament
B. grafit
C. fullereny
D. wszystkie wymienione odmiany
Zadanie 5. (0-1 pkt)
Jeden ze związków węgla jest składnikiem powietrza (ok. 0,03%). Jest nim:
A. tlenek węgla (II)
B. tlenek węgla (IV)
C. kwas węglowy D.
węglan wapnia
Strona 2 z 13

Konkursy w województwie podkarpackim w roku szkolnym 2006/2007
Zadanie 6. (0-1 pkt)
Tlenek węgla (IV) znajduje się w:
A. gaśnicy śniegowej
B. wodzie sodowej
C. szampanie
D. we wszystkich wymienionych
Zadanie 7. ( 0-2 pkt.)
1u = 0,166 •10
-23
g
Ile kilogramów waży atom węgla?
A. 1,992•10
-23
Brudnopis
B. 1,992•10
-27
C. 1,992•10
-26
D. 0,1992•10
-23
Zadanie 8. (0-2 pkt.)
W jakim stosunku masowym połączony jest węgiel z tlenem w tlenku węgla (II)?
Brudnopis
A. 1:1
B. 3:4
C. 3:8
D. 4:3
Zadanie 9. (0-2 pkt.)
Zawartość procentowa węgla w węglanie wapnia wynosi:
A. 20%
Brudnopis
B. 40%
C. 48%
D. 12%
Zadanie 10. (0-1 pkt)
Tlenek węgla (IV) jest pochłaniany przez:
A. CaCO
3
B. NaOH
C. KOH
D. odpowiedzi B i C są prawidłowe
Strona 3 z 13

Konkursy w województwie podkarpackim w roku szkolnym 2006/2007
Zadanie 11. (0-1 pkt)
Węgiel (IV) jest składnikiem:
A. octanu metylu
B. marmuru
C. celulozy
D. wszystkich wymienionych w pkt A,B,C
Zadanie 12. (0-1 pkt)
Tlenek węgla (II) słabo rozpuszcza się w H
2
O, a roztwór jest:
A. lekko zasadowy
B. obojętny, gdyż tlenek węgla ( II ) nie reaguje z wodą
C. lekko kwaśny, gdyż powstały kwas słabo
dysocjuje
D. kwaśny, gdyż zachodzą inne reakcje
Zadanie 13. (0-1 pkt)
pH roztworu, o którym mowa w zadaniu 12, wynosi:
A. 7
B. mniej niż 7
C. więcej niż 7
D. nie można określić
Zadanie 14. (0-2 pkt.)
W jakim stosunku masowym połączony jest węgiel z wodorem w oktanie?
Brudnopis
A. 8:18
B. 16:3
C. 3:16
D. 18:8
Zadanie 15. (0-2 pkt.)
Ile moli CO
2
przereagowało całkowicie z CaO jeżeli powstało 25g węglanu wapnia?
A. 1 mol
Brudnopis
B. 0,5 mola
C. 0,2 mola
D. 0,25 mola
Strona 4 z 13
Konkursy w województwie podkarpackim w roku szkolnym 2006/2007
Zadanie 16. (0-2 pkt.)
Jaka jest masa cząsteczkowa kwasu, który w reakcji z KOH daje sól o masie
cząsteczkowej 212u, a w reakcji z CaO sól o masie 310u ?
Brudnopis
A. 62u
B. 63u
C. 98u
D. 82u
Zadanie 17. (0-1 pkt)
Jony OH
-
powstaną w reakcji H
2
O z tlenkami podanymi w zestawie:
A. K
2
O i CO
2
B. CaO i SO
2
C. K
2
O i Na
2
O
D. SO
2
i CO
2
Zadanie 18. (0-2 pkt.)
9,6g jonów siarczanowych (VI) stanowi:
Brudnopis
A. 1 mol jonów
B. 10 moli jonów
C. 0,1 mola jonów
D. żadna z odpowiedzi A,B,C nie jest poprawna
Zadanie 19. (0-2 pkt.)
W procesie dysocjacji elektrolitycznej 0,5 mola cząsteczek Ba(OH)
2
(zakładając
całkowitą dysocjację) powstaje:
Brudnopis
A. 6,02 •10
23
jonów OH
-
B. 12,04 •10
23
jonów OH
-
C. 1 mol jonów OH
-
D. odpowiedzi A i C są prawidłowe
Strona 5 z 13

Konkursy w województwie podkarpackim w roku szkolnym 2006/2007
Zadanie 20. (0-1 pkt)
Próbkę skały wapiennej zalano roztworem kwasu solnego. Gaz wydzielający
się w wyniku reakcji zidentyfikujesz:
A. na podstawie charakterystycznego zapachu
B. sprawdzając jego palność
C. przepuszczając go przez roztwór wodorotlenku wapnia
D. nie ma możliwości zidentyfikowania metodami wymienionymi w pkt A,B,C
Zadanie 21. (0-1 pkt)
Jest kwaśną cieczą, w cząsteczce są dwa atomy węgla, można go otrzymać
z wina. Jaki to związek?
A.
etanol
B. kwas węglowy
C. kwas etanowy
D. żadna substancja wymieniona w pkt A,B,C
Zadanie 22. (0-1 pkt)
Jest solą, cząsteczka zawiera 2 metale i tlen. Tworzy fioletowo-czerwone
kryształy, można ją kupić w aptece. Co to za substancja?
A. jodyna
B. lapis
C. gips
D. manganian (VII) potasu
Zadanie 23. (0-1 pkt)
Występuje m. in. we krwi, zawiera 24 atomy w cząsteczce, jest reduktorem:
A. hemoglobina
B. białko
C. glukoza
D. sacharoza
Strona 6 z 13

Konkursy w województwie podkarpackim w roku szkolnym 2006/2007
Zadanie 24. (0-1 pkt)
Aby dokonać przemian
C
2
H
6
eten
C
2
H
4
Br
2
tlenek węgla (IV)
niezbędne są:
A. wodór i brom
B. wodór i tlen
C. brom i tlen
D. brom wodór i tlen
Zadanie 25. (0-2 pkt.)
W równaniu reakcji
x C
2
H
6
+ y O
2
= z CO
2
+ 6 H
2
O
współczynniki x,y,z przyjmują kolejno wartości:
A. 2,3,4
B. 2,7,4
C. 1,2,3
D. 7,2,4
Brudnopis
Zadanie 26. (0-1 pkt )
Wodorotlenek miedzi (II) nie jest substratem reakcji:
A. fermentacji octowej
B. wykrywania białka
C. badania właściwości redukcyjnych glukozy
D. otrzymywania tlenku miedzi (II)
Strona 7 z 13

Konkursy w województwie podkarpackim w roku szkolnym 2006/2007
Zadanie 27. (0-2 pkt.)
Rozpuszczono 5 g NaOH w wodzie. Ile cm
3
kwasu azotowego (V) o stężeniu
Cm = 2 mol•dm
-3
potrzeba do zobojętnienia tego roztworu?
Brudnopis
A. 0,0625
B. 62,5
C. 625
D. 6,25
Zadanie 28. (0-2 pkt.)
Jaką objętość zajmie CO
2
powstały z rozkładu 50g CaCO
3
?
Brudnopis
A. 22,4 dm
3
B. 224 cm
3
C. 11,2 dm
3
D. 1120 cm
3
Zadanie 29. (0-2 pkt.)
I - próba Tollensa i Trommera
II - próba biuretowa i ksantoproteinowa
III- próba akroleinowa
metody badań mające na celu
identyfikację rodzaju substancji
A. I-białek
II-cukrów
prostych
III-tłuszczów
B. I-tłuszczów
II-białek III-cukrów
prostych
C. I-cukrów prostych
II-białek III-tłuszczów
D. I-cukrów prostych
II-tłuszczów
III-białek
Strona 8 z 13
Konkursy w województwie podkarpackim w roku szkolnym 2006/2007
Zadanie 30. (0-2 pkt.)
„Złoto” 18 karatowe zawiera 75% Au, 14 karatowe 58,3% Au.
Ile stopu 18 karatowego należy użyć do przyrządzenia 7,5g stopu 14
karatowego?
A. 4,3725g
B. 5,38g
C. 5,83g
D. 5,83 mg
Zadanie 31. (0-1 pkt)
Do 4 probówek z roztworem azotanu (V) baru wkroplono roztwory:
do I - H
2
SO
4
, do II - Na
2
SO
4
, do III - NaCl, do IV - HCl
Osad wytrącił się w probówkach:
Brudnopis
Brudnopis
A. I i III
B. II i III
C. III i IV
D. I i II
Zadanie 32. (0-1 pkt)
Stal jest stopem:
A. Fe i Zn
B. Fe i C
C. Fe i Al
D. Fe i Cu
Zadanie 33. (0-2 pkt.)
Stalowy przedmiot waży 500 kg. Ile zostałoby z niego po 3 latach (gdyby nie był
zabezpieczony przed korozją) jeżeli rocznie 20% stali ulega zniszczeniu?
Brudnopis
A. 100 kg
B. 300 kg
C. 200 kg
D. 256 kg
Strona 9 z 13

Konkursy w województwie podkarpackim w roku szkolnym 2006/2007
Zadanie 34. (0-1 pkt)
Do roztworu HCl zanurzono blaszki: cynkową, miedzianą, srebrną, żelazną
(każda w oddzielnej probówce z kwasem). Wydzielenie wodoru zauważono na
blaszkach:
A. Zn i Cu
B. Zn i Fe
C. Fe i Cu
D. Zn i Ag
Zadanie 35. (0-1 pkt)
W reakcji hydrolizy tłuszczu w roztworze NaOH powstaje:
A. glicerol i woda
B. glicerol i kwas
C. mydło i woda
D. glicerol i mydło
Zadanie 36. (0-1 pkt)
Stosowanie ciekłego wodoru jako paliwa przyszłości jest zasadne ponieważ:
A. wodór jest trudno rozpuszczalny w H
2
O i nie będzie zanieczyszczał zbiorników
wodnych
B. spala się wybuchowo
C. jedynym produktem spalania jest woda
D. jest najlżejszym gazem
Strona 10 z 13

Konkursy w województwie podkarpackim w roku szkolnym 2006/2007
BRUDNOPIS
(nie podlega ocenie)
Strona 11 z 13
Konkursy w województwie podkarpackim w roku szkolnym 2005/2006
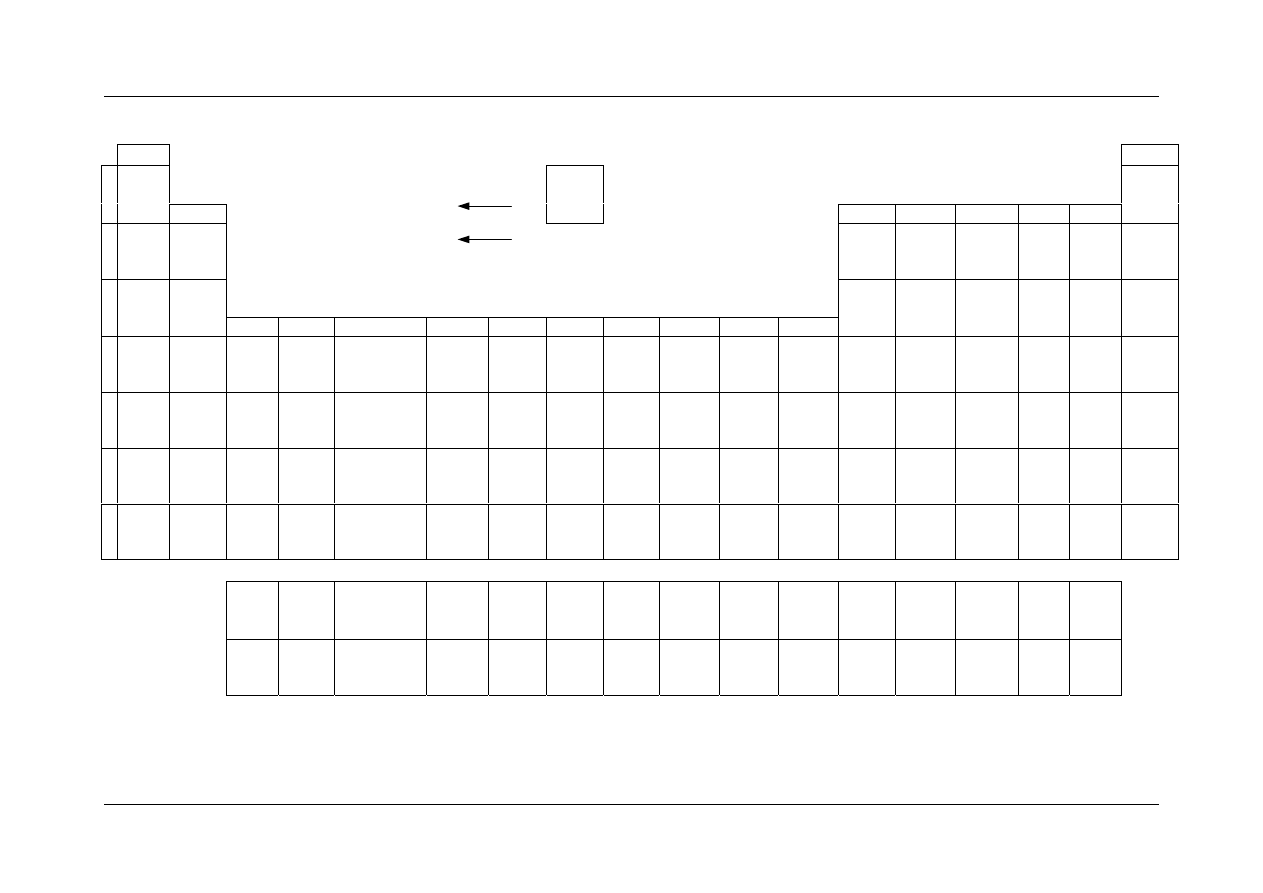
U
K Ł A D O K R E S O W Y P I E R W I A S T K Ó W C H E M I C Z N Y C H
1
18
1
1
H
wodór
1,01
2
12
Mg
magnez
24,31
13 14 15 16 17
2
He
hel
4,0
2
3
Li
lit
6,94
4
Be
beryl
9,01
5
B
bor
10,81
6
C
węgiel
12,01
7
N
azot
14,01
8
O
tlen
16,0
9
F
fluor
19,0
10
Ne
neon
20,18
3
11
Na
sód
22,99
12
Mg
magnez
24,31
3 4
5
6 7 8 9 10 11 12
13
Al
glin
26,98
14
Si
krzem
28,09
15
P
fosfor
30,97
16
S
siarka
32,06
17
Cl
chlor
35,45
18
Ar
argon
39,95
4
19
K
potas
39,10
20
Ca
wapń
40,08
21
Sc
skand
44,96
22
Ti
tytan
47,88
23
V
wanad
50,94
24
Cr
chrom
51,99
25
Mn
mangan
54,94
26
Fe
żelazo
55,85
27
Co
kobalt
58,93
28
Ni
nikiel
58,69
29
Cu
miedź
63,55
30
Zn
cynk
65,38
31
Ga
gal
69,72
32
Ge
german
72,59
33
As
arsen
74,92
34
Se
selen
78,96
35
Br
brom
79,9
36
Kr
krypton
83,8
5
37
Rb
rubid
85,47
38
Sr
stront
87,62
39
Y
itr
88,91
40
Zr
cyrkon
91,22
41
Nb
niob
92,91
42
Mo
molibden
95,94
43
Tc
technet
96,90
44
Ru
ruten
101,07
45
Rh
rod
102,91
46
Pd
pallad
106,42
47
Ag
srebro
107,87
48
Cd
kadm
112,41
49
In
ind
114,82
50
Sn
cyna
118,69
51
Sb
antymon
121,75
52
Te
tellur
127,60
53
I
jod
126,91
54
Xe
ksenon
131,29
6
55
Cs
cez
132,91
56
Ba
bar
137,33
La-Lu
57-71
72
Hf
hafn
178,49
73
Ta
tantal
180,95
74
W
wolfram
183,85
75
Re
ren
186,21
76
Os
osm
190,2
77
Ir
iryd
192,2
78
Pt
platyna
195,08
79
Au
złoto
196,97
80
Hg
rtęć
200,59
81
Tl
tal
204,38
82
Pb
ołów
207,2
83
Bi
bizmut
208,98
84
Po
polon
208,98
85
At
astat
209,99
86
Rn
radon
222,02
7
87
Fr
frans
223,02
88
Ra
rad
226,03
Ac-Lr
89-103
104
Rf
rutherford
261,1
105
Db
dubn
262,11
106
Sg
seaborg
263,12
107
Bh
bohr
262,12
108
Hs
has
265,1
109
Mt
meitner
266,1
110
Uun
111
Uuu
112
Uub
114
Uuq
57
La
lantan
138,91
58
Ce
cer
140,12
59
Pr
prazeodym
140,91
60
Nd
neodym
144,24
61
Pm
promet
144,91
62
Sm
samar
150,36
63
Eu
europ
151,96
64
Gd
gadolin
157,25
65
Tb
terb
158,93
66
Dy
dysproz
162,5
67
Ho
holm
164,93
68
Er
erb
167,26
69
Tm
tul
168,93
70
Yb
iterb
173,04
71
Lu
lutet
174,97
89
Ac
aktyn
227,03
90
Th
tor
232,04
91
Pa
protaktyn
231,04
92
U
uran
238,03
93
Np
neptun
237,05
94
Pu
pluton
244,06
95
Am
ameryk
243,06
96
Cm
kiur
247,07
97
Bk
berkel
247,07
98
Cf
kaliforn
251,08
99
Es
einstein
252,08
100
Fm
ferm
257,09
101
Md
mendelew
258,1
102
No
nobel
259,1
103
Lr
lorens
260,1
liczba atomowa
masa atomowa [u]
Konkursy w województwie podkarpackim w roku szkolnym 2006/2007
T
A B E L A R O Z P U S Z C Z A L N O Ś C I N I E K T Ó R Y C H S O L I
I W O D O R O T L E N K Ó W W W O D Z I E
OH
-
Cl
-
NO
3
-
S
2-
SO
3
2-
SO
4
2-
CO
3
2-
PO
4
3-
CH
3
COO
-
Li
+
R R R R R R R N R
Na
+
R R R R R R R R R
K
+
R R R R R R R R R
NH
4
+
R R R R R R R R R
Ag
+
N N R N N T N N R
Mg
2+
N R R
−
N R N N R
Ca
2+
T R R R N T N N R
Cu
2+
N R R N
−
R N N R
Ba
2+
R R R R N N N N R
Zn
2+
N R R N N R N N R
Pb
2+
N T R N N N N N R
Fe
2+
N R R N N R N N R
Fe
3+
N R R N
−
R
−
N
−
Al
3+
N R R
−
−
R
N R
−
Szereg aktywności metali
K Na Li Ca Mg Al Mn Zn Fe Sn Pb H
2
Cu
R – substancja rozpuszczalna; T – substancja trudno rozpuszczalna; N – substancja
praktycznie nierozpuszczalna;
− oznacza, że substancja nie została otrzymana lub
rozkłada się w wodzie
Hg Ag Au Pt
R
O Z P U S Z C Z A L N O Ś Ć N I E K T Ó R Y C H S U B S T A N C J I
W Z A L E Ż N O Ś C I O D T E M P E R A T U R Y
Rozpuszczalność [ g / 100 g H
2
O ]
Substancja
0
o
C 20
o
C 40
o
C 60
o
C 80
o
C 100
o
C
KNO
3
13,6 31,9 62,9 109,0 170,9 242,4
K
2
CO
3
158,5 167,3 181,4 202,7 230,9 268,6
K
2
SO
4
8,53 11,0 14,8 18,4 21,5 24,0
CuSO
4
24,0 35,5 53,2 81,8 131,2 139,5
NaCl
35,6 35,9 36,4 37,1 38,0 39,0
NH
4
Cl
29,4 37,1 45,8 55,3 65,7 77,0
CH
3
COONa
79 111 192 139 153 170
C
12
H
22
O
11
179 204 238 288 363 488
Strona 13 z 13
Document Outline
Wyszukiwarka
Podobne podstrony:
2006 07 Kolorowy gadzet RGBid 2 Nieznany
1 zaburzenia krążenia 1 2006 07 III
Egzamin zawodowy 2006 07
HYDROLOGIA 07 id 207788 Nieznany
Materiał wyłożony zima 2006 07, materiały
2003 07 Szkola konstruktorowid Nieznany
hih kolo kolo2 07 id 709394 Nieznany
2006 07 lodz IIetapid 25539
I CSK 304 07 1 id 208210 Nieznany
Fizjologia Cwiczenia 07 id 1743 Nieznany
algebra 2006 wyklad id 57189 Nieznany (2)
Kwaśniewski J , 2006 07 26 dr kwasniewski pl, Jak długo O zaleceniach dietetycznych
więcej podobnych podstron