
ĆW. 1
WPŁYW STĘŻENIA I TEMPERATURY
NA LEPKOŚĆ ROZTWORÓW
CEL ĆWICZENIA
Wyznaczenie lepkości względnej roztworu gliceryny
względem lepkości wody – cieczy o znanych
parametrach.
Zbadanie wpływu temperatury na lepkośd.
Określenie wielkości energii aktywacji przepływu.
1

Wykonanie dwiczenia
• Określenie masy piknometru wypełnionego
wodą
oraz
piknometru
wypełnionego
roztworem gliceryny.
• Pomiar czasu przepływu wody i roztworu
gliceryny pomiędzy dwoma poziomami w
wiskozymetrze Ubbelohde’a
(czyt. ubeloda)
dla różnych temperatur.
2
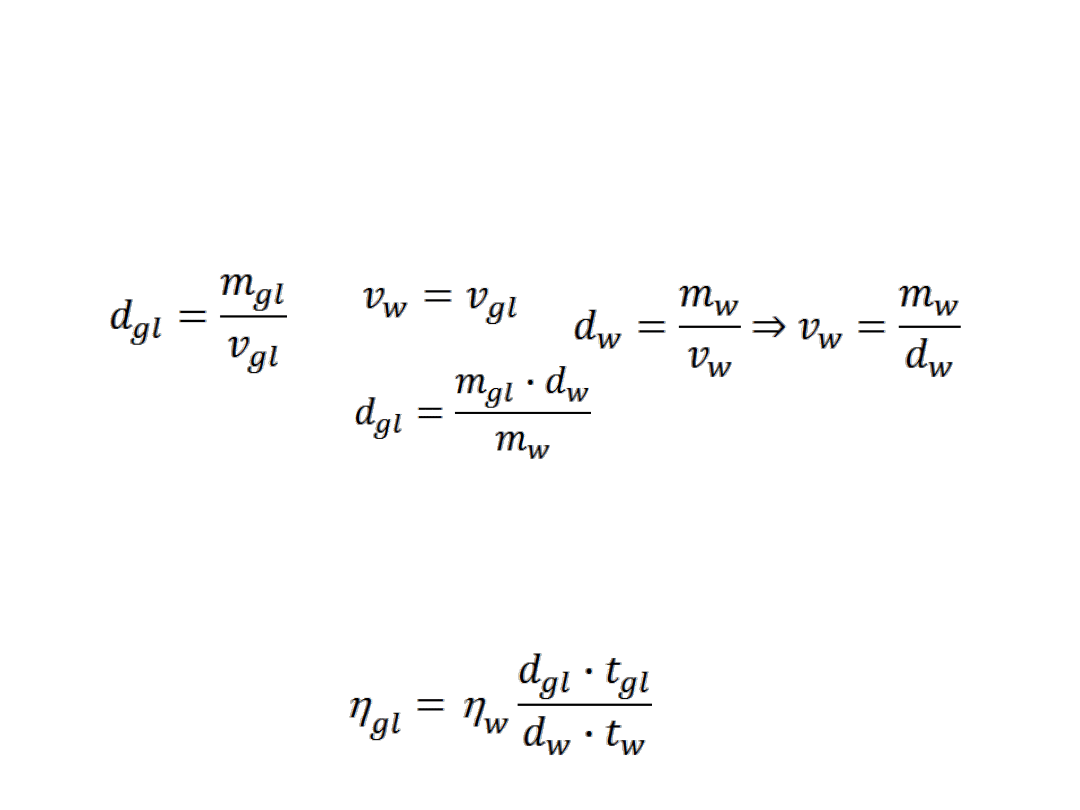
Opracowanie wyników
• Określenie gęstości roztworu gliceryny:
• Określenie stężenia roztworu gliceryny na podstawie jego
gęstości,
• Obliczenie lepkości roztworu gliceryny dla poszczególnych
temperatur z zależności:
3

Opracowanie wyników
• Sporządzenie wykresu log
= f(1/T), (osie muszą
byd opisane!)
• Jeśli wykres ma charakter liniowy – wyliczenie
energii aktywacji przepływu oraz stałej A z
równania
prostej
y
=
ax
+
b,
gdzie
a = E
A
/R , b = log A (na wykresie podajemy
wartośd współczynnika korelacji R
2
, jeżeli jego
wartośd jest zbyt niska – należy to skomentowad),
• Jeśli wyniki wymagają komentarza – należy go
umieścid na sprawozdaniu.
4

Najważniejsze zagadnienia
• Lepkośd – definicje i jednostki.
• Warunki przepływu laminarnego i
turbulentnego.
• Metody pomiaru lepkości – zasady pomiaru.
• Zależnośd lepkości od temperatury. Równanie
Arrheniusa-Guzmana.
• Znaczenie lepkości w praktyce.
5

ĆW. 2
WYZNACZENIE STAŁEJ DYSOCJACJI
SŁABEGO KWASU ORAZ ROZPUSZCZALNOŚCI
SOLI TRUDNOROZPUSZCZALNYCH
METODĄ POMIARÓW PRZEWODNICTWA
Cel dwiczenia
Obliczenie stałej dysocjacji kwasu chlorooctowego,
Obliczenie rozpuszczalności oraz iloczynów
rozpuszczalności trudnorozpuszczalnych soli PbSO
4
,
PbI
2
, CaSO
4
, SrCO
3
.
6

Wykonanie dwiczenia
• Pomiar przewodnictwa właściwego i temperatury
wody destylowanej przy pomocy konduktometru,
• Pomiar przewodnictwa właściwego i temperatury
roztworów CH
2
ClCOOH,
• Przygotowanie roztworu kwasu o wybranym
stężeniu, pomiar przewodnictwa i temperatury
otrzymanego roztworu,
• Pomiar przewodnictwa właściwego i temperatury
soli.
7
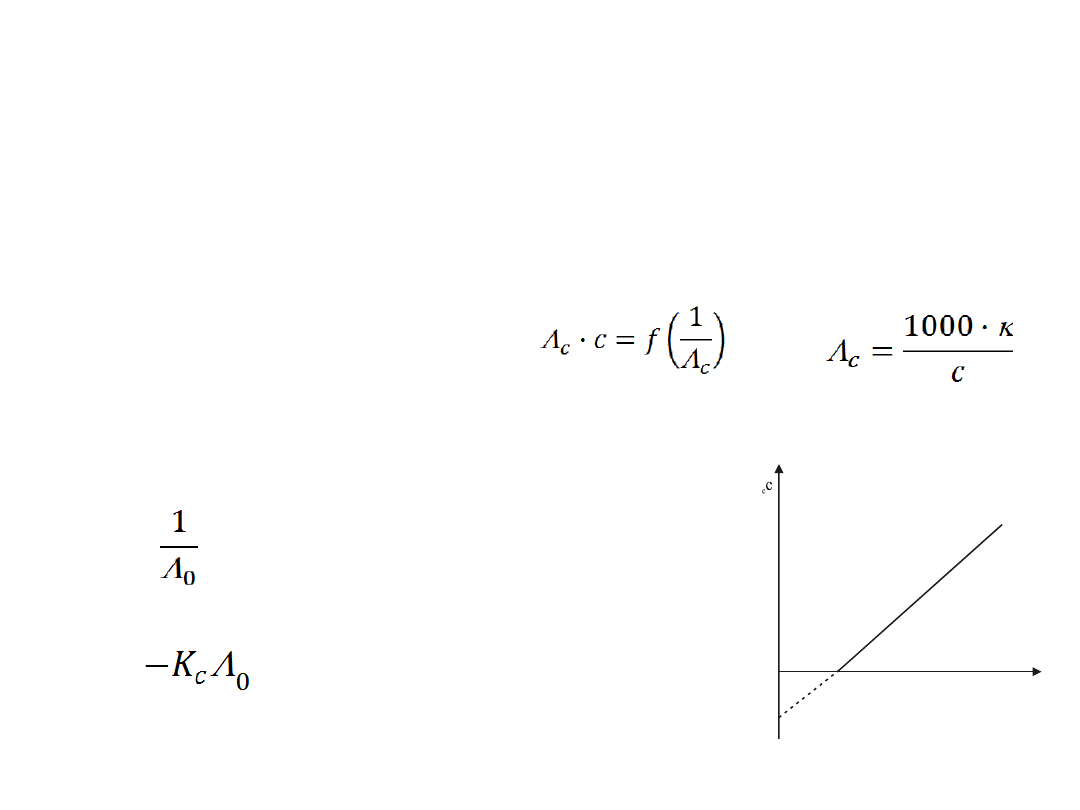
Opracowanie wyników
• Określenie skorygowanych wartości przewodnictwa
właściwego roztworów kwasu oraz soli,
• Obliczenie
przewodnictwa
równoważnikowego
z
zależności
• sporządzenie wykresu
• Wyznaczenie stałej dysocjacji kwasu z wykresu:
Punkt przecięcia prostej z osią OX (y = 0)
x =
Punkt przecięcia prostej z osią OY (x=0)
y=
Y
X
0
C
8
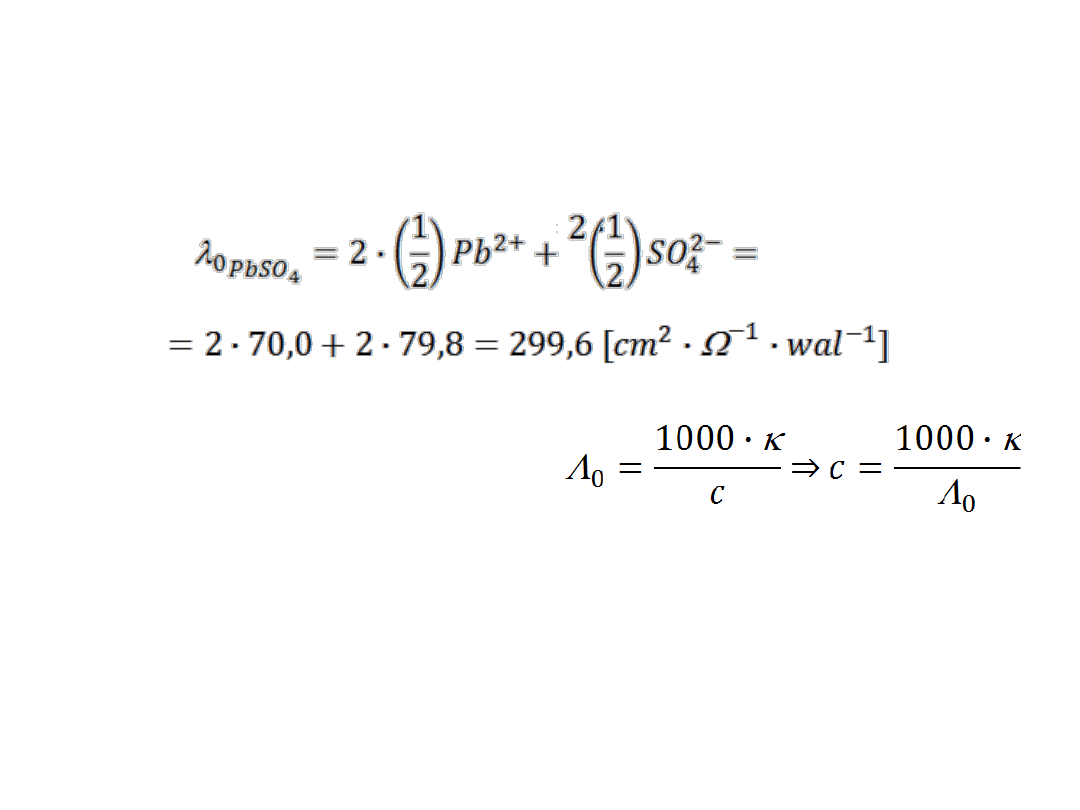
Opracowanie wyników
• Obliczenie granicznych przewodnict badanych soli,
np.:
• Obliczenie wartości rozpuszczalności z zależności:
gdzie c = s (rozpuszczalnośd)
• Obliczenie iloczynów rozpuszczalności soli,
• Komentarz do wyników.
9

Najważniejsze zagadnienia
• Przewodnictwo, przewodnictwo właściwe,
przewodnictwo równoważnikowe, przewodnictwo
graniczne, definicje, jednostki, metoda pomiaru.
• Teorie kwasów i zasad,
• Sens fizyczny stałej i stopnia dysocjacji, od czego zależą
te wielkości, związek między tymi wielkościami.
• Prawo niezależnej wędrówki jonów.
• Rozpuszczalnośd, iloczyn rozpuszczalności, związek
między nimi.
• Stężenia i przeliczanie stężeo.
10

ĆW. 4
Korozja i pasywacja stali
Cel dwiczenia
Porównanie
szybkości
korozji
stali
węglowej
i
kwasoodpornej (1H18N9) w kwasie siarkowym (VI)
przez wyznaczenie wskaźników szybkości korozji,
Wyznaczenie potencjałów korozji stali węglowej i
kwasoodpornej
w roztworze H
2
SO
4
,
Porównanie podatności do pasywacji stali węglowej i
kwasoodpornej na podstawie przebiegu polaryzacji
anodowej oraz porównanie zdolności utleniających
H
2
SO
4
w zależności od stężenia kwasu.
11

Wykonanie dwiczenia
• Wyznaczenie ubytku masy próbek ze stali
węglowej i kwasoodpornej po umieszczeniu ich
na czas 0,5-1h w roztworze kwasu siarkowego
(VI),
• Pomiar potencjału odwracalnego próbek ze stali
węglowej
i kwasoodpornej względem elektrody odniesienia
(NEK
lub
Ag/AgCl)
w czasie 30 min,
• Wyznaczenie krzywej polaryzacji stali węglowej i
kwasoodpornej w dwóch roztworach H
2
SO
4
o
różnym stężeniu (0,1M i 1M).
12
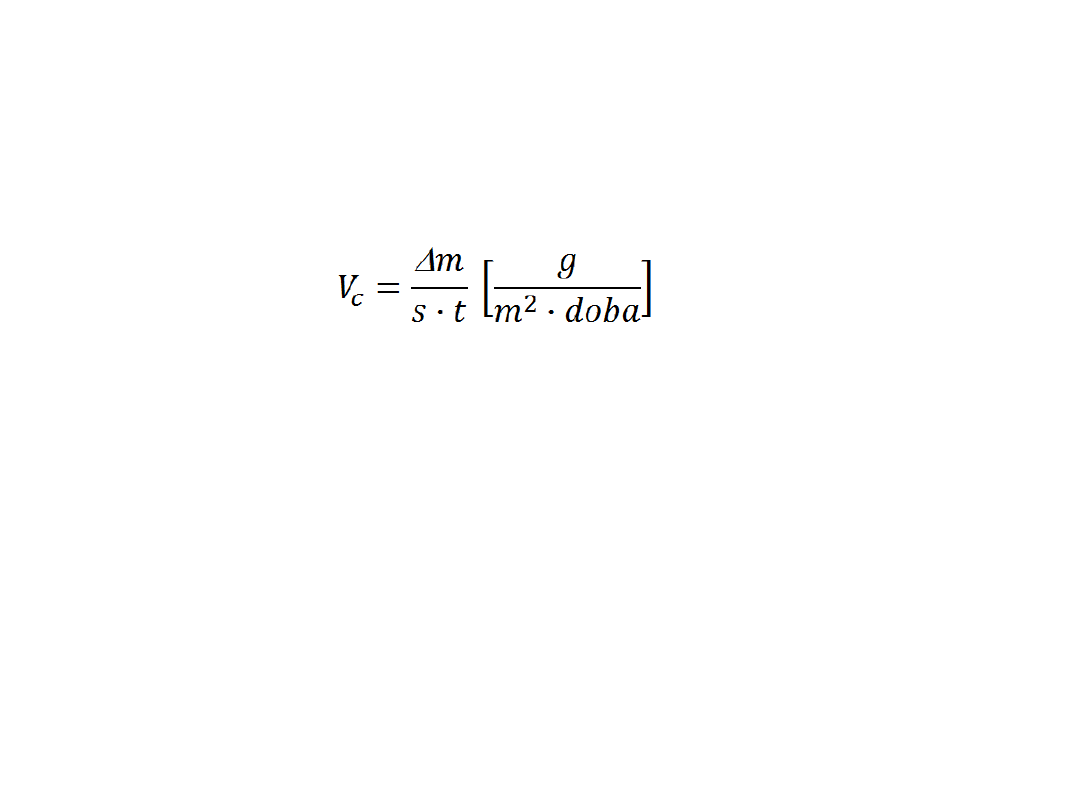
Opracowanie wyników
• Obliczenie szybkości korozji próbek stali węglowej i
kwasoodpornej na podstawie ubytku masy z zależności:
• Wyznaczenie graficznego przebiegu i omówienie
zależności potencjału korozyjnego od czasu dla stali
węglowej i kwasoodpornej,
• Omówienie przebiegu krzywych polaryzacji stali
węglowej
i kwasoodpornej w kwasie siarkowym (VI), porównanie
podatności stali na pasywację w zależności od rodzaju
stali i stężenia kwasu.
13

Najważniejsze zagadnienia
• Praca ogniw korozyjnych, procesy anodowe i
katodowe.
• Anodowa i katodowa kontrola procesów
korozyjnych.
• Korozja żelaza z depolaryzacją wodorową i
tlenową.
• Stan pasywny metali. Pasywacja anodowa.
• Metody ochrony metali przed korozją.
14

ĆW. 7
RÓWNOWAGA W UKŁADZIE DWUSKŁADNI-
KOWYM
CIAŁO STAŁE – CIECZ
Cel dwiczenia
Wyznaczenie diagramu równowagi fazowej stopu
dwuskładnikowego
Sn-Pb,
na
podstawie
analizy
termicznej.
Wykonanie dwiczenia
Pomiar zmian temperatury podczas stygnięcia cyny i
ołowiu oraz ich stopów za pomocą termoelementu.
15

Opracowanie wyników
• Wyznaczenie
graficznego
przebiegu
i
omówienie krzywych stygnięcia Sn, Pb oraz ich
stopów,
• Wyznaczenie na podstawie krzywych stygnięcia
diagramu fazowego ciecz-ciało stałe dla układu
dwuskładnikowego cyna-ołów.
16

Najważniejsze zagadnienia
• Podstawowe definicje: układu, parametrów stanu, fazy,
przemiany fazowej, składników niezależnych, stopni
swobody,
• Charakterystyka stanów skupienia materii,
• Warunek równowagi fazowej, reguła faz Gibbsa,
• Diagram równowagi fazowej, ogólne właściwości,
eutektyka,
• Analiza termiczna układu jako sposób wyznaczania
diagramów,
• Przykłady
diagramów
fazowych,
dla
układu
dwuskładnikowego,
w układzie ciało stałe- ciecz.
17
Wyszukiwarka
Podobne podstrony:
chemia fizyczna egzamin id 1122 Nieznany
Chemia fizyczna notatki id 1122 Nieznany
chemia fizyczna egzamin id 1122 Nieznany
PO lab 5 id 364195 Nieznany
lab [5] id 258102 Nieznany
Chemia fizyczna sprawozdanie (6 1) id 112219
lab [1] id 258099 Nieznany
Chemia kliniczna kontrola id 11 Nieznany
chemia okiem niechemika id 1126 Nieznany
chemia maj 2005 id 112453 Nieznany
Lab 4 id 257946 Nieznany
chemia przykladowe zad id 11281 Nieznany
Lab 1 id 257555 Nieznany
Chemia Organiczna Cz1 id 112665 Nieznany
fcs lab 5 id 169065 Nieznany
chemia tematy 1kolos id 112928 Nieznany
Chemia fizyczna sciaga id 112218
więcej podobnych podstron