
6.1. Nakładanie powłok malarskich metod
elektroforetyczn
6.1.1. Wprowadzenie
Malowanie elektroforetyczne nale y do jednej z bardziej nowoczesnych metod nanoszenia powłok
malarskich. Pierwsza przemysłowa linia do malowa nia elektroforetycznego została uruchomiona w
zakładach Forda w roku 1960. Obecnie proces ten jest stosowany prawie we wszystkich zakładach
samochodowych, równie w Polsce, do nanoszenia powłok podkładowych na karoserie pojazdów
samochodowych.
Do malowania elektroforetycznego stosuje si specjalne farby, tzw. wodorozcie czalne. Ich cech
charakterystyczn jest to, e jako rozpuszczalnik stosowana jest woda. Ma to ogromne znaczenie
ekologiczne, gdy eliminuje silnie toksyczne rozpuszczalniki organiczne. Farba jest roztworem
koloidalnym polimerów, czyli zwi zków wielkocz steczkowych oraz pigmentów, wypełniaczy i innych
dodatków w wodzie. Malowanie zachodzi w wyniku przepływu pr du elektrycznego. W polu
elektrycznym koloidalne cz stki farby, które s obdarzone ładunkiem elektrycznym, w druj do
odpowiednich elektrod. Proces ruchu cz stek koloidalnych w polu elektrycznym nosi nazw
elektroforezy, przy czym w drówka cz stek koloidalnych o ładunku dodatnim do katody nazywana jest
katoforez , a cz stek o ładunku ujemnym do anody — anoforez .
6.1.2. Rodzaje i budowa układów koloidalnych
Układy koloidalne s układami wieloskładnikowymi o wygl dzie układu jednolitego, zło onymi z fazy
zwanej o rodkiem rozpraszaj cym i składnika rozpraszanego. Wymiary cz stek rozpraszanych
(koloidalnych) wahaj si w granicach 10
-6
—10
-9
m. Wymiary cz stek w koloidach s mniejsze ni
w zawiesinie, ale wi ksze ni w roztworach rzeczywistych.
Z tego wzgl du koloidy wykazuj wła ciwo ci po rednie mi dzy roztworem rzeczywistym a
zawiesin , chocia nie ma ostrej granicy mi dzy tymi trzema rodzajami mieszanin.
Koloidy nie s typowymi układami dwufazowymi jak zawiesiny, gdy cz stki koloidalne nie
spełniaj wszystkich kryteriów fazy, zwłaszcza kryterium równowagi termodynamicznej faz. W
zawiesinach ka da z faz zachowuje swoje wła ciwo ci fizykochemiczne, a rozdzielenie składników jest
mo liwe w wyniku procesów fizycznych, jak: s czenie, odwirowanie, sedymentacja. Koloidy nie s
równie układami jednofazowymi jak roztwory rzeczywiste. W odró nieniu od roztworów
rzeczywistych nie ulegaj dializie, czyli nie przechodz przez błony półprzepuszczalne. Cz stki
koloidalne maj zdolno rozpraszania wiatła; jest to tzw. efekt Tyndalla, który w roztworach
rzeczywistych nie wyst puje. Koloidy nazywa si jednorodnymi układami z powierzchni rozdziału.
Wszystkie układy koloidalne s termodynamicznie w stanie równowagi nietrwałej, co wyra a si stałym
wzrostem wymiarów cz stek prowadz cym do zmniejszenia powierzchni rozgraniczaj cej fazy; w miar
upływu czasu mo e wyst pi rozdział faz (segregacja) na substancje, z których układ koloidalny powstał.
W zale no ci od stanu skupienia fazy rozpraszaj cej i rozpraszanej wyró nia si 8 rodzajów
układów koloidalnych. Rodzaje te podano w tablicy 6.1.
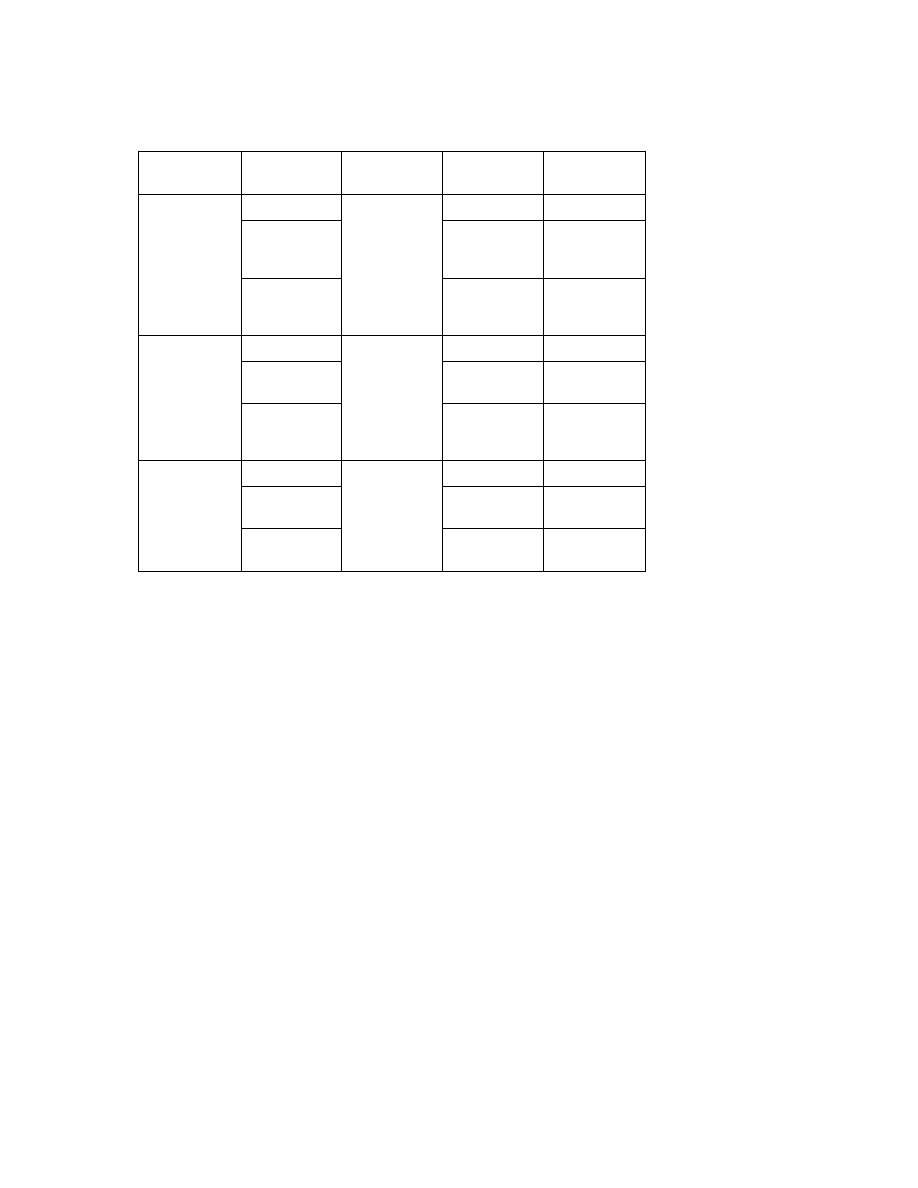
T a b l i c a 6.1
Podział układów koloidalnych ze wzgl du na stan skupienia
O rodek
rozpraszaj cy
Substancja
rozproszona
Rozdaj koloidu
Nazwa układu
koloidalnego
Przykłady
gaz
nie istnieje
-
ciecz
aerozole ciekłe
(mgły koloidalne)
mgły, chmury
Gaz
ciało stałe
aerozole
(gazozole)
aerozole stałe
(dymy koloidalne)
dym, kurz
gaz
piany
piana mydlana
ciecz
liozole, emulsje
(emulsoidy)
mleko, białko
Ciecz
ciało stałe
zole, roztwory
koloidalne
zawiesiny
koloidalne
(suspensoidy)
zole tlenków
metali,
wodorotlenków
gaz
piany stałe
pumeks
ciecz
piany stałe
(emulsje stałe)
kwarc mleczny
Ciało stałe
ciało stałe
pirozole
zole stałe
szkło rubinowe,
perły fosforowe
Układy koloidalne, w których faz rozpraszaj c jest gaz, nosz ogóln nazw aerozoli. S one
zwykle mniej trwałe ni układy z faz rozpraszaj c ciekł lub stał .
Spo ród wszystkich układów koloidalnych najwi ksze znaczenie w przemy le maj te, w których
o rodek rozpraszaj cy jest w fazie ciekłej, a zwłaszcza układy cieczy w cieczy, czyli emulsje, i układy
ciało stałe w cieczy, czyli zole (suspensje). Te ostatnie zwane s równie roztworami koloidalnymi.
Istniej dwa typy zoli:
1.
liofobowe — zole liofobowe s wła ciwymi roztworami koloidalnymi; powstaj w wyniku
rozpraszania stałej substancji nierozpuszczalnej w fazie rozpraszanej;
liofilowe — zolami liofilowymi nazywane s roztwory zwi zków wielko cz steczkowych, w
których zwi zek wielkocz steczkowy jest rozpuszczalny w fazie ciekłej. Liofilowe roztwory
koloidalne polimerów s to wła ciwie roztwory rzeczywiste, gdy faza rozpraszana (zwi zek
wielkocz steczkowy) ma wielko pojedynczych makrocz steczek. Z tego wzgl du s one ter-
modynamicznie trwałe, podobnie jak roztwory rzeczywiste. Z uwagi na wielko cz steczek
fazy rozpraszanej maj one jednak e wła ciwo ci molekularno-kinetyczne takie jak układy
koloidalne, np. nie ulegaj dializie.
Nale y zaznaczy , e zwi zki wielkocz steczkowe oprócz liofilowych roztworów koloidalnych,
mog równie tworzy termodynamicznie nietrwałe liofobowe roztwory koloidalne (zole). Powstaj one,
jak wszystkie zole, wówczas, gdy zwi zek wielkocz steczkowy nie rozpuszcza si w o rodku rozpra-
szaj cym (np. wodorozcie czalne farby stosowane do malowania elektroforetycznego, lateksy).
Ka d substancj stał , ciekł czy gazow mo na w odpowiednich warunkach przeprowadzi w stan
koloidalny. Osi ga si to w wyniku zdyspersowa-nia (rozproszenia) cz stek zawiesiny lub te w
wyniku kondensacji cz stek roztworu rzeczywistego. Ze wzgl du na małe wymiary cz stek koloidalnych
powierzchnia rozdziału faz jest bardzo rozwini ta. Koloidy mo na charakteryzowa powierzchni
wła ciw . Jest to stosunek całkowitej powierzchni cz stki zdyspergowanej do jej masy lub obj to ci:
m
2
/g lub m
2
/m
3
. Znaczne rozwini cie powierzchni w roztworach koloidalnych powoduje, e zjawiska
elek-trokinetyczne zachodz ce na granicy faz odgrywaj wyj tkowo du rol . Na ka dej granicy faz, a
wi c i na powierzchni cz stek koloidalnych wyst puje podwójna warstwa elektryczna. Wewn trzna
warstwa, zwana a d s o r p c y j - n , powstaje w wyniku selektywnej adsorpcji jonów lub cz steczek
dipolowych na powierzchni fazy stałej. Zaadsorbowane jony lub cz steczki s ci le zwi zane z
powierzchni cz stki koloidalnej i nie ulegaj oderwaniu nawet w przypadku mieszania.
Zjawisko adsorpcji jonów na granicy faz powoduje, e cz stki koloidalne s obdarzone ładunkiem
elektrycznym. O jego znaku decyduje ładunek warstwy wewn trznej — adsorpcyjnej. Warstwa
zewn trzna dyfuzyjna o przeciwnym znaku nie jest zwi zana z cz stk koloidaln . Jest ona ruchoma.
Cz stka koloidalna wraz z otaczaj c j warstw dyfuzyjn nosi nazw miceli koloidalnej. Cz stki
koloidalne mog adsorbowa zarówno ładunki dodatnie, jak i ujemne. Zale y to od budowy chemicznej
fazy rozpraszanej i o rodka rozpraszaj cego, a niekiedy od st enia i rodzaju jonów w roztworze, np. ko-
loidalny roztwór jodku srebra AgJ w roztworze zawieraj cym nadmiar jodku potasu KJ adsorbuje jony J
-
i cz stki maj ładunek ujemny. Natomiast w roztworze zawieraj cym nadmiar azotanu srebra AgNO
3
cz stki koloidalne adsor-buj jony Ag
+
i maj ładunek dodatni.
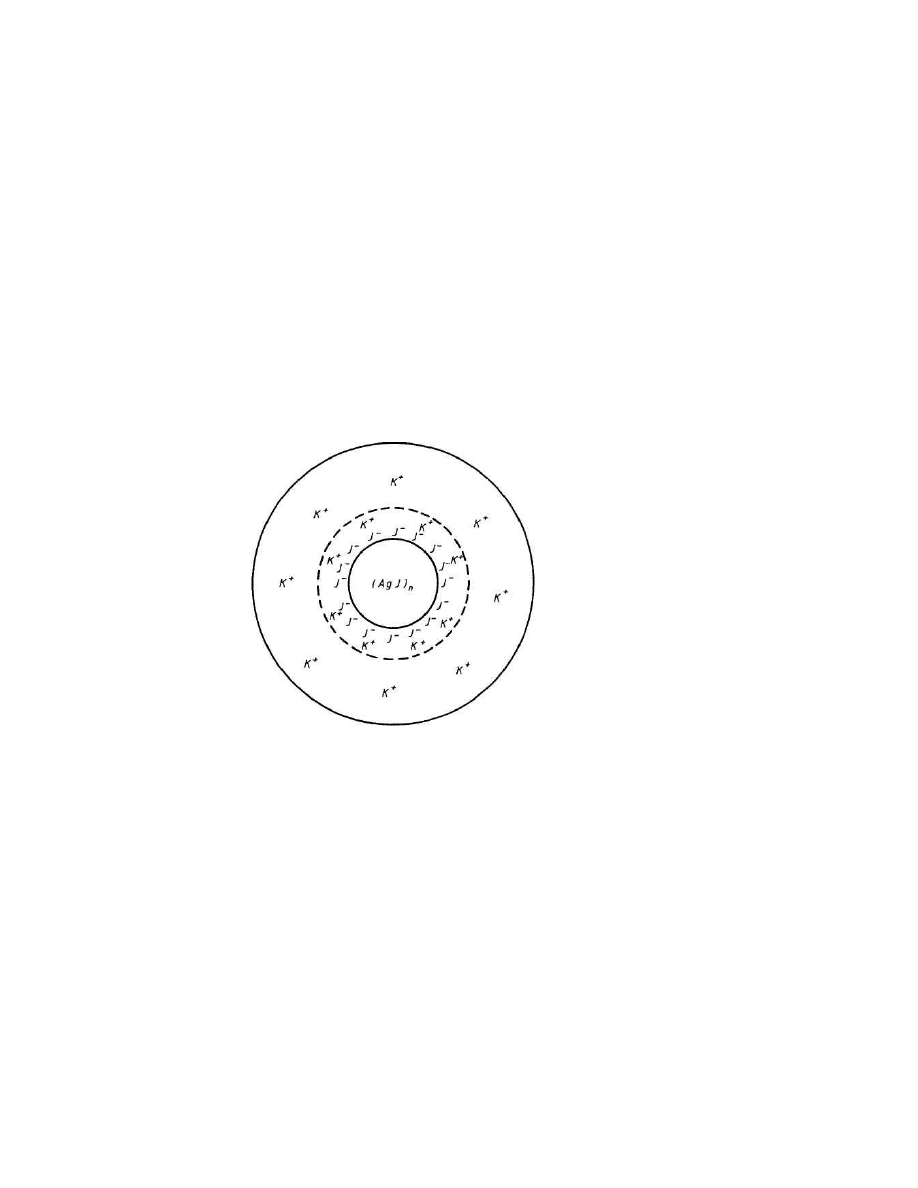
Na rys. 6.1 przedstawiono budow tzw. miceli jodku srebra w roztworze wobec nadmiaru jodku
potasu. W skład miceli koloidalnej wchodzi j dro zbudowane z wielu cz steczek substancji
rozpuszczonej (w tym przypadku cz steczek AgJ). Wokół j dra zaadsorbowane s jony jednego znaku
(jony jodko-we J
-
). Oprócz tych jonów trwale zaadsorbowanych w warstwie wewn trznej znajduj si w
mniejszej ilo ci przeciwnie naładowane jony potasowe K
+
, tzw. przeciwjony. Obecno ładunku
elektrycznego na cz stkach koloidalnych jest wynikiem przewagi w warstwie wewn trznej adsorpcyjnej
jonów jednego znaku (przewaga jonów J
-
nad jonami K
+
). J dro z warstw wewn trzn adsorpcyjn
stanowi cz stk koloidaln . Na rys. 6.1 oznaczono j lini przerywan . Pozostałe jony potasowe K
+
znajduj si w o rodku otaczaj cym cz stk i tworz dookoła niej tzw. zewn trzn warstw dyfuzyjn .
Rys. 6.1. Budowa miceli koloidalnej jodku srebra w roztworze jodku potasu
6.1.3. Zasada procesu malowania elektroforetycznego
Malowanie elektroforetyczne jest to proces technologiczny wykorzystywany do pokrywania metali
lub powierzchni metalizowanych powłokami antykorozyjnymi, dekoracyjnymi lub elektroizolacyjnymi.
Technologia procesu malowania elektroforetycznego podobna jest do nakładania powłok
elektrolitycznych. Przedmiot przeznaczony do malowania musi by odpowiednio przygotowany, tzn.
musz by usuni te wszelkie zanieczyszczenia i lady rdzy. Zwykle tego typu obróbk wykonuje si
mechanicznie. W warunkach laboratoryjnych mo e to by cieranie papierem ciernym o
odpowiedniej granulacji. Przedmiot nale y równie odtłu ci . Mo na stosowa odtłuszczaj ce k piele
alakaliczne. Przy niezbyt zabrudzonych próbkach wystarczy przemy w rozpuszczalnikach organicznych.
Przygotowanie powierzchni metalu przez obróbk wst pn jest wa nym elementem procesu. Wpływa na
zmian przewodnictwa powierzchni, a ponadto zapewnia odpowiedni adhezj cz stek materiału
malarskiego do powierzchni. Ma wi c ono decyduj cy wpływ na wynik malowania.
Przedmiot przeznaczony do malowania jest nast pnie przenoszony do k pieli zawieraj cej
koloidalny roztwór farby i stanowi odpowiedni elektrod . Proces malowania prowadzi si przy stałym
napi ciu, stosuj c pr d stały. Warto napi cia zale y od stosowanej metody. Dla procesu katoforezy
konieczne jest wy sze napi cie ni dla anoforezy. Proces malowania trwa krótko, ok. 120 sekund.
Przedmiot przeznaczony do malowania mo e by anod lub katod . Zale y to od składu k pieli do
malowania elektroforetycznego. Je eli cz stki koloidalne uzyskaj ładunek ujemny, osadzaj si na
anodzie. Proces nosi wtedy nazw malowania anoforetycznego. Istniej równie farby, w których

cz stki koloidalne uzyskuj ładunek dodatni. Farby takie osadzaj si na katodzie. Proces malowania
nazywa si wówczas malowaniem katoforetycznym.
Do malowania anoforetycznego stosuje si farby, w których materiałem po-włokotwórczym s
polimery akrylowe, alkidowe, fenolowe. Polimery te zawieraj grupy funkcyjne zdolne do dysocjacji,
np. grupy karboksylowe -COOH w polimerach akrylowych, grupy -OH w polimerach fenolowych.
Takie polimery nazywane s polielekrolitami. Mog one uzyskiwa ładunek nie tylko w wyniku
adsorpcji jonów na powierzchni cz stek koloidalnych (ładunek ujemny), ale równie wskutek dysocjacji
grup funkcyjnych. Powstaj wówczas makrojony oraz proste jony małocz steczkowe. We wszystkich
wymienionych polimerach stosowanych w procesie anoforezy makrojony maj ładunek ujemny.
Cz ciowo zoboj tnion cz steczk ywicy akrylowej [ - CH
2
- CH - ]
n
mo na schematycznie
przedstawi wzorem COO
H
gdzie:
R — ła cuch makrocz steczki,
B — jon jednowarto ciowej zasady neutralizuj cej, np. NH4, Na
+
.
Warto z zale y od stopnia dysocjacji ywicy akrylowej, a wi c od warunków zewn trznych,
takich jak: temperatura, st enie, pH. Warto y zale y od stopnia zoboj tnienia ywicy. Zoboj tnienie
polikwasu zasad NaOH lub NH
4
OH prowadzi si w celu zwi kszenia rozpuszczalno ci ywicy. Wzrost
warto ci x, czyli zwi kszenie liczby grup karboksylowych, zmniejsza rozpuszczalno ywicy w wodzie.
Pod wpływem przyło onego napi cia ujemnie naładowane cz stki farby b d w drowa do
elektrody dodatniej (anody), któr stanowi przedmiot przeznaczony do malowania. W obszarze
anodowym zachodzi reakcja makrojonów ywicy z jonami wodorowymi, powstałymi w wyniku procesu
elektrolizy wody. Reakcje zachodz ce na anodzie mo na opisa równaniami
Przedstawiony proces powoduje wzrost warto ci x we wzorze makrocz steczki ywicy. Sprawia to,
e materiał malarski osadza si na anodzie w postaci nierozpuszczalnej warstwy.
Na anodzie nie b d cej metalem szlachetnym, np. na stali, zachodz
dodatkowo reakcje jonów ywicy z jonami metalu. Reakcje
przebiegaj według równa
Powstaj wówczas nierozpuszczalne w wodzie sole polikwasów.
Do malowania katoforetycznego stosuje si farby, w których materiałem powłokotwórczym s
ywice epoksydowo-aminowe, epoksydowo-fenolowe lub poliuretanowe. Ogólny wzór ywicy tego
typu mo na przedstawi nast puj co:
R
3
N lub RNH
2
. Przy neutralizacji kwasem cz steczka ywicy
staje si polikationem
R
3
NH
+
lub RNH3. Jako kation osadza si na katodzie. Korzystn konsekwencj
malowania na katodzie jest brak reakcji rozpuszczania metalu podło a. Poprawia to efekty dekoracyjne
powłok. Nie wyst puje równie szkodliwy wpływ zanieczyszczenia farby anionami z procesu
przygotowania powierzchni (anionami CrO
4
2-
, PO
4
3-
). Pozwala to na stosowanie procesu fosforowania
przed malowaniem.
Malowanie katoforetyczne wymaga stosowania wy szych napi podczas nakładania oraz
rozbudowanej strefy płukania. Ogólnie koszt urz dze do malowania katoforetycznego oraz cena farb
katoforetycznych s wy sze ni w procesie anoforezy. Jednak koszt ten jest równowa ony przez znacznie
lepsze wła ciwo ci antykorozyjne powłok katoforetycznych w porównaniu z anoforetycznymi.
W polu elektrycznym wyst puje równie zjawisko elektroosmozy. Jest ono jakby odwrotno ci
elektroforezy. Cz stki zdyspergowane pozostaj nieruchome, natomiast porusza si faza rozpraszaj ca,
przewa nie woda. Zjawisko to wyst puje w cienkich kapilarach, kanalikach materiałów porowatych lub
błon półprzepuszczalnych, utworzonych z osadzonego na elektrodzie materiału koloidalnego. W tych
warunkach obj to warstwy dyfuzyjnej utworzonej na granicy faz jest na tyle du a, e cała masa wody
znajduje si w tej warstwie. Warstw dyfuzyjn stanowi roztwór jonów, które nie zostały zaadsorbowane
na powierzchni. Jony s hydratowane dipolami wody. Przedstawiony na rys. 6.2 model odpowiada
malowaniu anoforetycznemu. Cz stki koloidalne stanowi ce ciank naczynia s naładowane ujemnie
(adsorbuj jony ujemne). W tym przypadku w warstwie dyfuzyjnej przewa aj jony dodatnie.
Rys. 6.2. Schemat elektroosmozy w rurce kapilarnej: 1 — ujemnie naładowana cianka kapilary, 2 — warstwa dyfuzyjna wody
zawieraj ca nadmiar jonów dodatnich, poruszaj ca si w kierunku
elektrody ujemnej
W czasie procesu malowania katoforetycznego cianki maj ładunek dodatni, a warstwa dyfuzyjna
jest naładowana ujemnie.
W obydwu procesach anoforezy lub katoforezy, pod wpływem przyło onego napi cia jony
znajduj ce si w warstwie dyfuzyjnej wraz z otoczk dipoli wody hydratowanej na tych jonach b d
przesuwa si do odpowiednich elektrod. W procesie malowania anoforetycznego, gdy materiał malarski
o ładunku ujemnym osadza si na anodzie, hydratowane jony dodatnie d
do katody. W procesie
malowania katoforetycznego, gdy dodatnio naładowane cz stki farby osadzaj si na katodzie,
warstwa dyfuzyjna naładowana ujemnie d y do anody.
W wyniku elektroosmozy zawarto wody w powłoce ulega zmniejszeniu poni ej 10%.
6.1.4. Zalety malowania elektroforetycznego
Powłoki otrzymywane tym sposobem maj wiele zalet, odró niaj cych je od powłok nakładanych
innymi metodami. Powłok nało on elektroforetycz-nie cechuje równomierne osadzenie materiału
malarskiego oraz dobre pokrycie wszelkich zagł bie , wkl ni itp. Wynika to z mechanizmu
procesu. Materiał malarski osadza si pocz tkowo na cz ci poło onej najbli ej elektrody przeciwległej.
Poniewa osadzana powłoka jest warstw nie przewodz c , stanowi zatem du y opór dla
przepływaj cego pr du i utrudnia elektroosadzanie. Wskutek tego nast pne partie materiału malarskiego
osadzaj si na cz ciach bardziej oddalonych. Dzi ki tej wła ciwo ci otrzymuje si powłoki o znacznej
równomierno ci, odtwarzaj ce wiernie kształt powierzchni pokrywanej. Ta cecha powłok malarskich
nakładanych metod elektroforetyczn wpływa na polepszenie ich wła ciwo ci ochronnych.
Z innych zalet malowania elektroforetycznego nale ałoby wymieni mo liwo kontrolowania
grubo ci powłoki, krótki czas pokrywania i mo liwo prowadzenia procesu systemem ci głym. Poza
tym, istotn spraw jest stosowanie farb wodorozcie czalnych, co eliminuje konieczno u ycia
deficytowych rozpuszczalników organicznych, niebezpiecze stwo po aru oraz mo liwo rozmi kczenia
powłoki w zamkni tych pomieszczeniach wskutek parowania rozpuszczalnika.
Wydajno pr dowa procesu elektroforetycznego jest znacznie wi ksza ni procesu elektrolitycznego
nakładania metali.
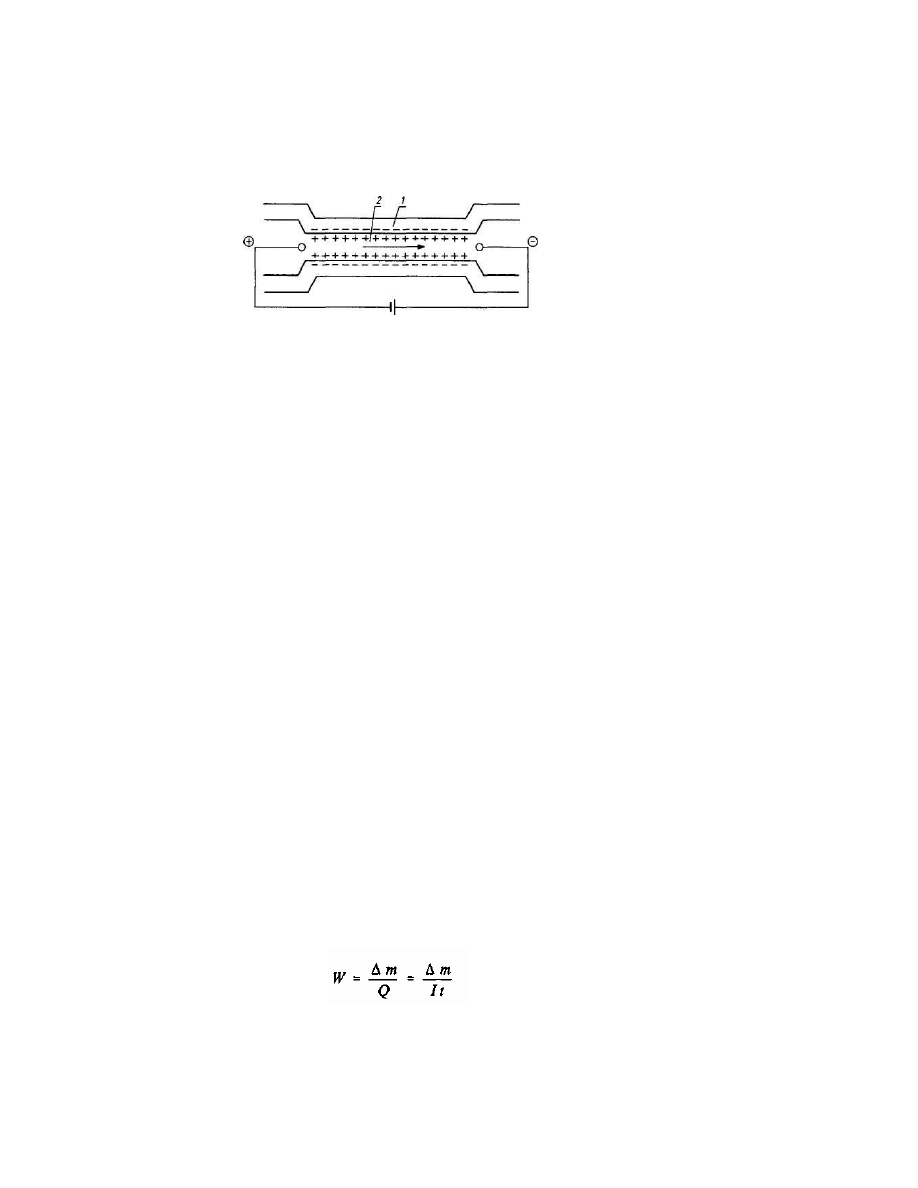
W procesie malowania elektroforetycznego jako wydajno pr dow przyjmuje si ilo osadzonego
materiału malarskiego, przypadaj c na jednostk przepływaj cego ładunku. Zale no t mo na
wyrazi nast puj cym wzorem
gdzie:
m — masa osadzonego materiału malarskiego [g],
Q— przepływaj cy ładunek,
/ - nat enie pr du [mA]),
t — czas [s].
Mas osadzonego materiału okre la si metod wagow , porównuj c mas przedmiotu po i przed

malowaniem. Ilo przepływaj cego ładunku mo na okre li za pomoc miernika przepływaj cego
ładunku. W procesie malowania elektroforetycznego zu ywa si mniej energii elektrycznej na
przeniesienie jednostki masy ni przy elektrolitycznym nakładaniu metali, z uwagi na znacznie wi ksz
mas cz stek koloidalnych w stosunku do masy pojedynczych jonów metali.
Wyszukiwarka
Podobne podstrony:
18, Wyznaczanie ciepła właściwego cieczy w stałym ciśnieniu metodą elektryczną, Artur Grudziński
Elektrochemiczne nakładanie powłok metalowych, Energetyka, I rok, chemia
18, Cw 18 - Pomiar ciepla wlasciwego cieczy w stalym cisnieniu metoda elektryczna, Jacek Konikowski
8 Spawalnicze metody nakładania powłok
18 Ochrona przeciwprzepięciowa w linii i stacji elektroenergetycznej
Wyznaczanie współczynnika rozszerzalności liniowej metodą elektryczną 1 (2)
Laboratorium Podstaw Fizyki spr) Pomiar współczynnika rozszerzalności liniowej metali metodą elektry
Wytrzymałość materiałów, Pomiar odkształceń - metoda elektrycznych tensometrów, Badanie odkształceń
Metoda elektrooporowa
OI13 Wyznaczanie wspolczynnika rozszerzalnosci liniowej cial stalych metoda elektryczna
Otrzymywanie metali metodami elektrochemicznymi
Otrzymywanie proszków metali metodami elektrochemicznymi
Metoda elektrooporowa, archeologia(2)
Pomiar temperatury metodami elektrycznymi
Metoda elektrooporowa3
Wyznaczanie współczynnika rozszerzalności liniowej metodą elektryczną2, Wyznaczenie współczynnika ro
Wyznaczanie współczynnika rozszerzalności, Wyznaczenie współczynnika rozszerzalności liniowej metodą
Wyznaczanie współczynnika rozszerzalności liniowej metodą elektryczną 1 (3), Wyznaczenie współczynni
więcej podobnych podstron