
ATH - Inżynieria Środowiska – semestr 2 – Chemia Organiczna
1
by michal_czdz
Kolokwium – CHEMIA ORGANICZNA
(laboratorium) 28.04.2009r.
ZAGADNIENIA DO KOLOKWIUM
KRYSTALIZACJA
1) Cechy dobrego rozpuszczalnika
2) Dlaczego oznaczamy temperaturę topnienia po skooczeniu
krystalizacji?
3) Rodzaje sączenia
4) Rodzaje lejków
DESTYLACJA
1) Definicja destylacji
2) Elementy zestawu do destylacji
3) Rodzaje destylacji

ATH - Inżynieria Środowiska – semestr 2 – Chemia Organiczna
2
by michal_czdz
ODPOWIEDZI DO ZAGADNIEŃ
KRYSTALIZACJA
1) Cechy dobrego rozpuszczalnika
Rozpuszczalnik używany do krystalizacji powinien posiadad następujące cechy:
1. dużą zdolnośd rozpuszczania krystalizowanej substancji na gorąco i stosunkowo
niewielką w temperaturze pokojowej lub poniżej tej temperatury
2. powinien albo rozpuszczad zanieczyszczenia bardzo dobrze albo też rozpuszczad
je tylko w niewielki stopniu
3. sprzyjad wytwarzaniu dobrze wykształconych kryształów oczyszczonego związku
4. powinien byd łatwy do usunięcia z powierzchni kryształów (mied stosunkowo
niską temperaturę wrzenia)
5. rozpuszczalnik nie może reagowad chemicznie z substancją oczyszczaną
2) Dlaczego
oznaczamy
temperaturę
topnienia
po
skooczeniu
krystalizacji?
Oznaczamy temperaturę topnienia w celu sprawdzenia dokładności procesu
krystalizacji (czystości otrzymanego związku). W razie potrzeby produkt krystalizacji
poddaje się ponownej krystalizacji ze świeżego rozpuszczalnika. Krystalizację
powtarza się aż do chwili otrzymania czystego związku który charakteryzuje się stałą,
charakterystyczną dla siebie temperaturą topnienia.
3) Rodzaje sączenia
a) Grawitacyjne
b) Pod zmniejszonym ciśnieniem
Do sączenia pod zmniejszonym ciśnieniem stosuje się lejki sitowe (Buchnera).
c) Pod zwiększonym ciśnieniem
4) Rodzaje lejków
a) Szklane (zwykłe)
b) Lejki sitowe (do zmniejszonego ciśnienia)
c) Szklany (perforowany)
d) Szklany ze spiekiem (spiek jest sączkiem)

ATH - Inżynieria Środowiska – semestr 2 – Chemia Organiczna
3
by michal_czdz
DESTYLACJA
1) Definicja destylacji
Destylacja jest metodą rozdzielania substancji wykorzystując występowanie różnicy
między składem cieczy będącej mieszaniną dwu lub większej ilości składników, a
składem pary wytworzonej z tejże cieczy. Metoda ta służy do rozdzielania substancji
różniących się temperaturą wrzenia (lotnością).
2) Elementy zestawu do destylacji
1. Kolba destylacyjna lub zwykła kolba okrągło denna
Objętośd kolby powinna byd tak dobrana aby stanowiła
lub
jej
pojemności. Kolbę ogrzewa się za pomocą palnika gazowego, elektrycznej czaszy
grzejnej, łaźni wodnej, olejowej lub piaskowej.
2. Chłodnica Liebiga lub powietrzna
Gdy temperatura destylujących par nie przekracza temperatury
do
ich skraplania używa się chłodnic wodnych Liebiga. Wyższa temperatura (w
przypadku chłodnic Liebiga) grozi pęknięciem chłodnicy.
Natomiast do temperatur powyżej
stosuje się chłodnice chłodzone
powietrzem.
Chłodnicę Liebiga podłącza się w taki sposób, aby kierunek przepływu wody był
przeciwny do kierunku przepływu destylatu (wlot wody od dołu).
3. Termometr do pomiaru temperatury par
Termometr do pomiaru temperatury umocowuje się w szyjce kolby za pomocą
złącza szlifowego lub korka gumowego z wywierconym odpowiednim otworem
zwracając szczególną uwagę, by zbiorniczek rtęci termometru znajdował się
możliwie dokładnie na poziomie wylotu par do chłodnicy. Jedynie przy takim
położeniu termometr wskazuje rzeczywistą temperaturę par uchodzących do
chłodnicy.
4. Odbieralnik destylatu
Najczęściej jako odbieralniki destylatu służą kolby stożkowe, ssawkowe,
gruszkowe lub okrągło denne.
W przypadku destylacji substancji niepalnych, nieszkodliwych dla zdrowia można
odbieralnik postawid pod koocówkę chłodnicy tak, aby destylat swobodnie
spływał do odbieralnika. Najczęściej jednak koocówkę chłodnicy łączy się szczelnie
z odbieralnikiem za pośrednictwem szklanego przedłużacza.
3) Rodzaje destylacji
a) destylacja prosta
Polega ona na stopniowym przeprowadzaniu destylowanej cieczy w stan pary i
skraplaniu wytworzonych par. Służy ona do rozdzielania substancji różniących się
temperatura wrzenia o co najmniej
.
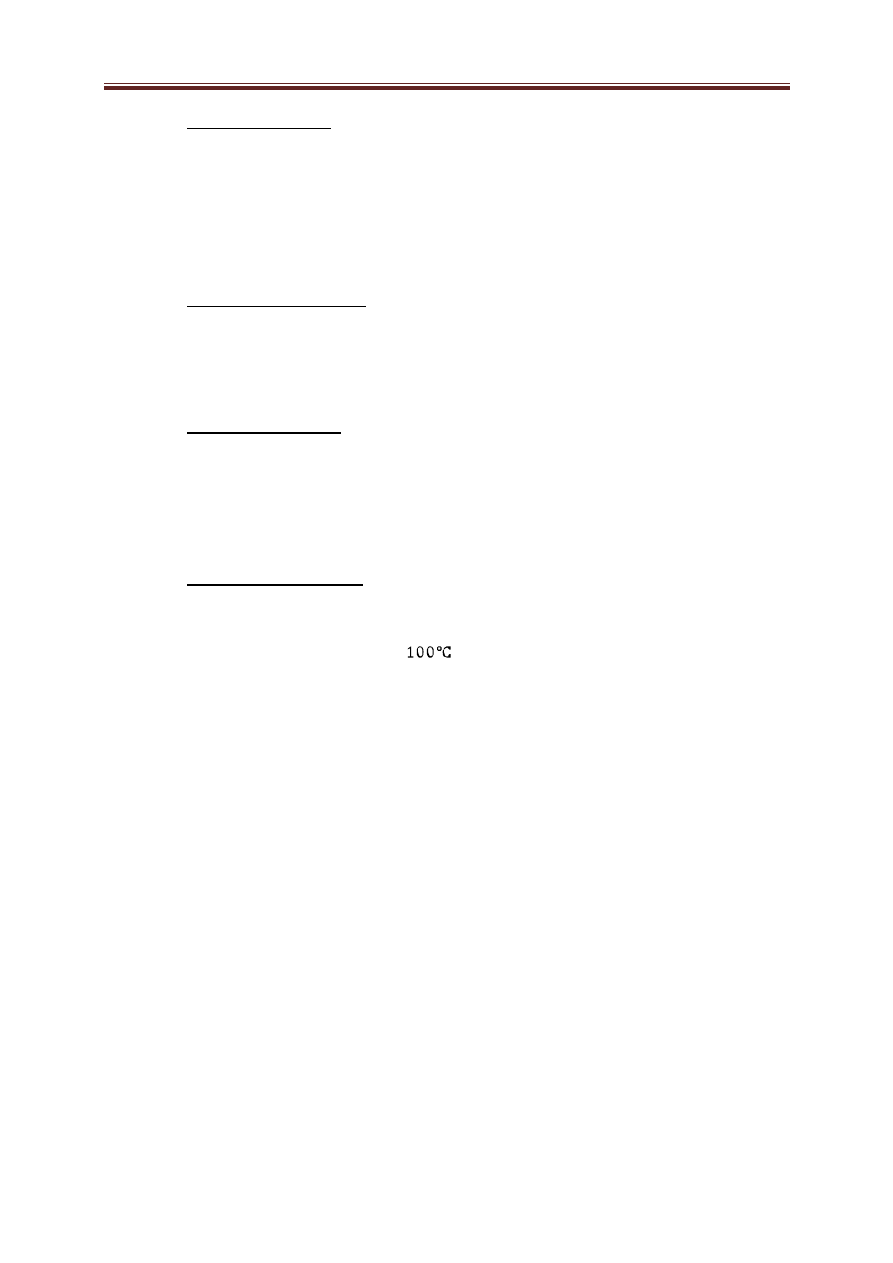
ATH - Inżynieria Środowiska – semestr 2 – Chemia Organiczna
4
by michal_czdz
b) destylacja frakcyjna
Polega ona na stopniowym przeprowadzaniu destylowanej cieczy w stan pary i
skraplaniu wytworzonych par. Jest stosowana dla substancji, które różnią się
nawet nieznacznie temperatura wrzenia. W tym rodzaju destylacji destylat dzieli
się na porcje (frakcje) o możliwie wąskim zakresie temperatur wrzenia.
Poszczególne frakcje można poddad ponownie destylacji frakcyjnej. Po każdej
kolejnej destylacji uzyskuje się frakcje o większej czystości.
c) destylacja rektyfikacyjna
Rektyfikacja – może służyd jako zastąpienie wielokrotnych procesów destylacji.
Rektyfikację prowadzi się przy użyciu kolumny rektyfikacyjnej, w której
wielokrotnie zachodzi proces odparowywania cieczy i skraplania par, co prowadzi
do spotęgowania różnicy w składzie cieczy i pary z niej uzyskanej.
d) destylacja próżniowa
Destylacja próżniowa polega na przedestylowaniu cieczy pod zmniejszonym
ciśnieniem w niższej temperaturze. Ten sposób destylacji dotyczy cieczy, które
podczas destylacji pod ciśnieniem atmosferycznym rozłożyły się.
Destylacja próżniowa wykorzystuje fakt, że temperatura wrzenia cieczy maleje
wraz ze zmniejszaniem się ciśnienia, pod którym prowadzi się destylację.
e) destylacja z parą wodną
Destylacja z parą wodną przebiega zawsze w temperaturze niższej od
temperatury wrzenia składnika bardziej lotnego, którym zwykle jest woda, a więc
w temperaturze nie wyżej niż
.
Destylacji z parą wodną poddaje się substancje nierozpuszczalne lub słabo
rozpuszczalne w wodzie.
Wyszukiwarka
Podobne podstrony:
2009 04 06 mat finid 26662 Nieznany
28 04 2013 cw id 31908 Nieznany
2014 04 28 23 31 22id 28401 Nieznany
TRENING Z CHEMII NA 2 KOLOKWIUM TrenZAO 2, I rok, chemia org
ETI MYSLENICE 08 2009 wyniki kolokwiow chemia
28 04 2014 Jaskowska id 31909 Nieznany (2)
bik 02 2009 04 id 85660 Nieznany
kolokwium chem.org, Studia PŁ, Ochrona Środowiska, Chemia, organiczna
chemia org rcje id 112618 Nieznany
28 04 2013 cw id 31908 Nieznany
2014 04 28 23 31 22id 28401 Nieznany
2009 04 08 POZ 06id 26791 ppt
matura 2009 dwu a1 DWU m2009 id Nieznany
2009 EGZ WSTEPNY NA AM ODP(2) Nieznany
28 rozdzial 27 vmxgkzibmm3xcof4 Nieznany (2)
CHORZOW1 TRAGEDIA 28 01 2006 id Nieznany
więcej podobnych podstron